Académique Documents
Professionnel Documents
Culture Documents
Ci3 23 24 fm1
Ci3 23 24 fm1
Transféré par
luc couraudTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Ci3 23 24 fm1
Ci3 23 24 fm1
Transféré par
luc couraudDroits d'auteur :
Formats disponibles
MPSI 23/24 C-I-3-FM1
DESCRIPTION ET TRANSFORMATIONS DU SYSTEME CHIMIQUE
Comment obtenir une solution aqueuse ?
La solution obtenue est toujours limpide. Elle peut être ou non colorée, selon la nature des espèces dissoutes.
On choisit comme solvant de l’eau distillée
… composé ionique (un « sel »)
… moléculaire
Ex : NaCl(s) (le « sel de cuisine » )
… gaz
Ex : sucre
On dissout une petite quantité de …
très soluble … solide … liquide
La quantité dissoute est peu soluble
assez faible pour que le Pour obtenir une seule phase,
la solution obtenue soit La quantité dissoute est trop importante : une
partie du solide ne se dissout pas. Pour le liquide doit être miscible
limpide : les ions se avec le solvant
dispersent dans l’eau récupérer la solution limpide, il suffit de filtrer.
Comment faire l’inventaire des espèces chimiques initialement présentes dans une solution ?
Exemple de la solution obtenue par dissolution d’un composé ionique solide
Exemple de la solution obtenue par mélange de deux solutions
On suppose qu’aucune réaction chimique ne se produit au moment même du mélange (cas étudié ultérieurement).
Comment exprimer une constante d’équilibre ?
Pour écrire l’expression littérale de la constante K d’un équilibre, on utilise les valeurs des concentrations,
pressions partielles à l’équilibre … Attention, on donne généralement les valeurs initiales (au moment du mélange
des réactifs), a priori différentes de celles à l’équilibre. Etablir un bilan de matière est alors indispensable.
Quelques exemples :
2
PNO 2
2
aNO2 ( g )
2
P 2 o PNO
P K=
o2
- en phase gazeuse : N2O4(g) = 2 NO2(g) ,d’où K = = P = o 22 .
NO 2
soit o
aN2O4 ( g ) PN2O4 P PN2O4 P N 2O4 P
Po
- en milieu hétérogène : Fe(s) + Cu2+=Fe2++ Cu(s) (action en solution aqueuse du cuivre(II) sur le fer)
Fe 2+
aFe2+ .aCu( s ) o
.1 Fe 2+
K= ( aq )
= c soit K=
aFe( s ) 2 .aCu 2+ Cu 2+ Cu 2+
( aq )
1.
co
- en milieu homogène (solution aqueuse) : on suppose que toutes les espèces sont des solutés.
2A B + C no +
aB .aC B .C ( no + )
t=0 no no 0 .
K = = = V V soit K =
no−2 no+ no − 2 ( no − 2 )
t
A
2 2
aA
2
V
- en milieu homogène (phase gazeuse) : décomposition de N2O4(g) en utilisant le taux d’avancement :
N2O4(g) = 2 NO2(g) total gaz
EI n 0 n
EF n(1-) 2n n(1+)
PN2O4V = n (1 − ) RT (1) PNO2V = n (1 + ) RT (2) PV = n (1 + ) RT (3)
PN2O4V n (1 − ) RT
On divise membre à membre (1) par (3) : =
PV n (1 + ) RT
PNO2V 2n RT 1− 2
et (2) par (3) : = soit PN2O4 = P et PNO2 = P
PV n (1 + ) RT 1+ 1+
2
2
P
4 2
1 + 2 1 + P
2 2
PNO P
K= 2
= = . soit K= . o
PN2O4 .P o 1 − P.P o 1 + 1 − P o (1 + )(1 − ) P
1+
Organigramme récapitulatif
On se place dans les cas usuels (quantités manipulées, hors solvant, environ du même ordre de grandeur) :
On écrit l’équation-bilan équilibrée de la réaction.
Si celle-ci est fournie, ne pas multiplier les coefficients par une constante.
On déduit le bilan de matière avec un tableau d’avancement.
K > 104
OUI NON
La transformation est quasi-totale, on La transformation est un équilibre, on
identifie le réactif limitant. applique la loi d’action des masses.
On détermine l’avancement final.
On déduit la composition finale du système.
Vous aimerez peut-être aussi
- Réhabilitation Des Structures en Béton ArméDocument110 pagesRéhabilitation Des Structures en Béton ArméNoel Faure100% (1)
- Chapitre 3 - Les Principaux Défauts de SoudageDocument58 pagesChapitre 3 - Les Principaux Défauts de SoudageSourour Trabelsi100% (1)
- TS - Chim 2 - TP Ch1 CorrigéDocument2 pagesTS - Chim 2 - TP Ch1 CorrigéZakaria AIT EL CAIDPas encore d'évaluation
- TP00 H2O2corr PDFDocument2 pagesTP00 H2O2corr PDFEl Ouahabi SoufyanePas encore d'évaluation
- TD3 Chimie Generale +CORRIGE 2016-2017Document6 pagesTD3 Chimie Generale +CORRIGE 2016-2017Awatif BePas encore d'évaluation
- FZ1 - 2008 - Manuel D'atelier 06122015Document566 pagesFZ1 - 2008 - Manuel D'atelier 06122015Bernard FLEURY67% (3)
- (Pouliethérapie Cours) CouleurDocument57 pages(Pouliethérapie Cours) CouleurYasmina Ais78% (18)
- Cours Electrostatique ElectrocinétiqueDocument70 pagesCours Electrostatique ElectrocinétiqueabdoutadibPas encore d'évaluation
- Sujet Corrige Exam 2017Document6 pagesSujet Corrige Exam 2017huihu100% (1)
- TP N° 5 - Oxydo-Réduction - PDFDocument7 pagesTP N° 5 - Oxydo-Réduction - PDFleilalargate_37809290% (1)
- 4578Document9 pages4578Rhaim AyaPas encore d'évaluation
- Recueil Chimie 3Document8 pagesRecueil Chimie 3Safae RezzoukPas encore d'évaluation
- 5-Calcul Des Arbres100 PDFDocument15 pages5-Calcul Des Arbres100 PDFhamzaPas encore d'évaluation
- Td3 Transformation Chimique CorrDocument2 pagesTd3 Transformation Chimique CorrAdri LebPas encore d'évaluation
- But de La Manipulation 2Document4 pagesBut de La Manipulation 2Ducker MambikiPas encore d'évaluation
- TD 4 SPRM Partie 2 Thermodynamique électrochimique GC GPI 2021 Aide Résolution PDFDocument9 pagesTD 4 SPRM Partie 2 Thermodynamique électrochimique GC GPI 2021 Aide Résolution PDFYang WuPas encore d'évaluation
- 42 Exo TitrageDocument9 pages42 Exo TitrageMohamed Ibn alfaridhPas encore d'évaluation
- Cours 3 Chimie Des SolutionsDocument10 pagesCours 3 Chimie Des SolutionsLoubna El JehouariPas encore d'évaluation
- NH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationDocument3 pagesNH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationRitaj-Rayane Karim100% (1)
- CHIM105BS1DS20405Document2 pagesCHIM105BS1DS20405tv tvPas encore d'évaluation
- Physique CDocument5 pagesPhysique CDado khadidja SoumaréPas encore d'évaluation
- Acide / Base:: Ah + B A + BHDocument2 pagesAcide / Base:: Ah + B A + BHCAKPOPas encore d'évaluation
- CHIM105BS1DS20708Document4 pagesCHIM105BS1DS20708tv tv100% (2)
- Chap 3 Diagrammes EpHDocument4 pagesChap 3 Diagrammes EpHcours importantPas encore d'évaluation
- Cours PCTDocument54 pagesCours PCTJoy TowendoPas encore d'évaluation
- Physique CDocument4 pagesPhysique CBachire MbenguePas encore d'évaluation
- HhjkoDocument4 pagesHhjkoiyadhPas encore d'évaluation
- D Equilibres Oxyred PowerDocument45 pagesD Equilibres Oxyred Powermenin noorPas encore d'évaluation
- Chap6 TD Diagrammes EpHDocument5 pagesChap6 TD Diagrammes EpHlahcen elamraouiPas encore d'évaluation
- 5-Les Équilibres ChimiquesDocument43 pages5-Les Équilibres ChimiqueslilybarachantPas encore d'évaluation
- Correction Contrôle ChimieSol (2018 2019)Document8 pagesCorrection Contrôle ChimieSol (2018 2019)Mohamed ChadghanPas encore d'évaluation
- Sans TitreDocument3 pagesSans TitreouidadPas encore d'évaluation
- C1Chim Transformations Lentes RapidesDocument3 pagesC1Chim Transformations Lentes RapidesMohamed El Ouahdani75% (4)
- Ds Diagramme e PH Nickel Avril 19Document2 pagesDs Diagramme e PH Nickel Avril 19amel amoul100% (1)
- C1Chim Transformations Lentes Rapides PDFDocument3 pagesC1Chim Transformations Lentes Rapides PDFAzizElheniPas encore d'évaluation
- TD5 Transformation Chimique-CorrDocument3 pagesTD5 Transformation Chimique-CorrOut Of (Order)Pas encore d'évaluation
- CC2 CorrectionDocument4 pagesCC2 Correctionbessama84Pas encore d'évaluation
- Résumé Cours Chimie 02 S2 Partie 01 21-22Document17 pagesRésumé Cours Chimie 02 S2 Partie 01 21-22Mohamed AminePas encore d'évaluation
- Chapitre 4 Influence Des Réactions Chimiques Sur Les Réaction D'oxydoréduction S3 2020 - 21Document16 pagesChapitre 4 Influence Des Réactions Chimiques Sur Les Réaction D'oxydoréduction S3 2020 - 21MOHAMED MAZOUARIPas encore d'évaluation
- Chapitre Solubilité 2018Document22 pagesChapitre Solubilité 2018Younes AsfalouPas encore d'évaluation
- Cours SolubilitéDocument20 pagesCours Solubilitéyasser ouramdanePas encore d'évaluation
- Chimie Corrigé1Document11 pagesChimie Corrigé1Raphaël AubertPas encore d'évaluation
- Thermochimie Chap2 2018-19 PDFDocument37 pagesThermochimie Chap2 2018-19 PDFYassine AttachPas encore d'évaluation
- Chap3 T5 Eleve 2223 PDFDocument40 pagesChap3 T5 Eleve 2223 PDFCHELLALI Rabah Kheir EddinePas encore d'évaluation
- Correction TD Série 4-20-21Document13 pagesCorrection TD Série 4-20-21ZouikrPas encore d'évaluation
- Cours PCT A TIRERDocument60 pagesCours PCT A TIRERJoy TowendoPas encore d'évaluation
- Fich PC SP 3mDocument2 pagesFich PC SP 3mNemir MimirPas encore d'évaluation
- Diagrammes Potentiel-Ph Diagrammes Potentiel-Ph: ExercicesDocument12 pagesDiagrammes Potentiel-Ph Diagrammes Potentiel-Ph: Exercicescours importantPas encore d'évaluation
- TD N°9 RMGX Corrigé 2021Document4 pagesTD N°9 RMGX Corrigé 2021RobertoPas encore d'évaluation
- Chapitre I Les SolutionsDocument5 pagesChapitre I Les Solutionskalidou BaPas encore d'évaluation
- C PB03 Saq CaDocument3 pagesC PB03 Saq CaZineb ZahimPas encore d'évaluation
- SolubiDocument5 pagesSolubiAdil ELPas encore d'évaluation
- DS 6 PC - Correction Ge NeDocument3 pagesDS 6 PC - Correction Ge NeSANDROPas encore d'évaluation
- Chap 3 Diagrammes EpHDocument7 pagesChap 3 Diagrammes EpHayoub echraaPas encore d'évaluation
- Exercice Eau Oxygenee + Corrige PDFDocument3 pagesExercice Eau Oxygenee + Corrige PDFCamusPas encore d'évaluation
- Ensb Lessons-Chimie-Reactions PrecepitationDocument24 pagesEnsb Lessons-Chimie-Reactions PrecepitationsalahPas encore d'évaluation
- CCP PC2014c1c 1Document5 pagesCCP PC2014c1c 1Yahya ElmokhtariPas encore d'évaluation
- Chap 3 Oxido ReductionDocument29 pagesChap 3 Oxido ReductionAmine Barca100% (1)
- DS 7 E PH + Electrolyse + OrgaDocument10 pagesDS 7 E PH + Electrolyse + Orgavitalfire58Pas encore d'évaluation
- DERNIERE PARTIE ''Equilibres Acido-Basiques en Solution Aqueuse'' 2023Document28 pagesDERNIERE PARTIE ''Equilibres Acido-Basiques en Solution Aqueuse'' 2023Malak elPas encore d'évaluation
- TD EQ3 BisDocument6 pagesTD EQ3 BisJassir AmgroudPas encore d'évaluation
- Cours Trans Rapides Et LentesDocument5 pagesCours Trans Rapides Et Lentesboustakatb100% (1)
- Corrige de L'Epreuve de Sciences PhysiquesDocument6 pagesCorrige de L'Epreuve de Sciences PhysiquesKéitaPas encore d'évaluation
- BATAN - Série 3 Chimie Minérale Descriptive - C245 - BCG - S4 - 2019 - 2020Document8 pagesBATAN - Série 3 Chimie Minérale Descriptive - C245 - BCG - S4 - 2019 - 2020Yassine MOUHIBPas encore d'évaluation
- PSP On 2 1 23 24 Eq AlgebriquesDocument2 pagesPSP On 2 1 23 24 Eq Algebriquesluc couraudPas encore d'évaluation
- Osp c3 23 24 DimensionDocument1 pageOsp c3 23 24 Dimensionluc couraudPas encore d'évaluation
- PSP On 1 23 24 Outils GraphiquesDocument2 pagesPSP On 1 23 24 Outils Graphiquesluc couraudPas encore d'évaluation
- PSP On 3 1 23 24 Integ DerivationDocument1 pagePSP On 3 1 23 24 Integ Derivationluc couraudPas encore d'évaluation
- Evolution Temporelle D'Un Systeme Chimique: MPSI 23/24 C-I-4-EDocument5 pagesEvolution Temporelle D'Un Systeme Chimique: MPSI 23/24 C-I-4-Eluc couraudPas encore d'évaluation
- Pi1!23!24 FM Et MementoDocument7 pagesPi1!23!24 FM Et Mementoluc couraudPas encore d'évaluation
- CL 1 23 24 IntroductionDocument2 pagesCL 1 23 24 Introductionluc couraudPas encore d'évaluation
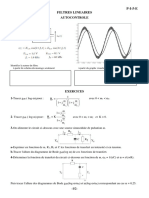
- MPSI 23/24 P-I-5-E Filtres Lineaires: AutocontroleDocument11 pagesMPSI 23/24 P-I-5-E Filtres Lineaires: Autocontroleluc couraudPas encore d'évaluation
- Pi8 23 24 Papl1 DiffractionDocument2 pagesPi8 23 24 Papl1 Diffractionluc couraudPas encore d'évaluation
- Cii2 23 24 fm4 Regle Du GammaDocument2 pagesCii2 23 24 fm4 Regle Du Gammaluc couraudPas encore d'évaluation
- Classeur 1Document2 pagesClasseur 1luc couraudPas encore d'évaluation
- Pi5 23 24 MementoDocument2 pagesPi5 23 24 Mementoluc couraudPas encore d'évaluation
- Les Impacts de La Crise de 1929 AuDocument4 pagesLes Impacts de La Crise de 1929 Auluc couraudPas encore d'évaluation
- 5 - Gdyel - Bilan PuissanceDocument1 page5 - Gdyel - Bilan PuissanceZoubir CherfiniPas encore d'évaluation
- Champ-Metre 433mhzDocument5 pagesChamp-Metre 433mhzcris eloPas encore d'évaluation
- Un Corrigé Du Concours Mines-Ponts Maths-1-Filière MP: B B B B B B B B BDocument4 pagesUn Corrigé Du Concours Mines-Ponts Maths-1-Filière MP: B B B B B B B B BOmar BesbesPas encore d'évaluation
- Cours ProbabilitéDocument11 pagesCours Probabilitéyassine HaddoualiPas encore d'évaluation
- TP 1. Observation Des Régimes D'Écoulement Du Fluide-ConvertiDocument3 pagesTP 1. Observation Des Régimes D'Écoulement Du Fluide-Convertiriad boutouatouPas encore d'évaluation
- Détermination Des Propriétés Dynamométriques Des Fils TextilesDocument4 pagesDétermination Des Propriétés Dynamométriques Des Fils Textilesdifferent music100% (1)
- f1 Courbes Surfaces-3d 16-17Document48 pagesf1 Courbes Surfaces-3d 16-17Dramane CoulibalyPas encore d'évaluation
- Série 1 - Erreurs de MesureDocument2 pagesSérie 1 - Erreurs de MesureSelma Seniorita100% (1)
- Leroy Somer COMPABLOC 3000Document18 pagesLeroy Somer COMPABLOC 3000Lalah Salim RambinintsoaPas encore d'évaluation
- Poly TD Electronique PDFDocument20 pagesPoly TD Electronique PDFEdmond Ouattara100% (1)
- Serie 220162017Document4 pagesSerie 220162017Youssra DjePas encore d'évaluation
- Transformation Chimiquebilan de MatièreDocument3 pagesTransformation Chimiquebilan de MatièreKamal LaourdaniPas encore d'évaluation
- Coiled Tubing Partie 1Document23 pagesCoiled Tubing Partie 1Salah Mohamed AmeurPas encore d'évaluation
- Chapitre 6 CEM en Électronique de PuissanceDocument6 pagesChapitre 6 CEM en Électronique de Puissanceسمير المتوليPas encore d'évaluation
- Ed 84Document4 pagesEd 84tafouzeltPas encore d'évaluation
- Exo 4Document4 pagesExo 4Beny AbdouPas encore d'évaluation
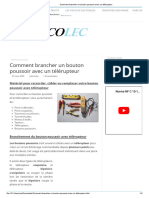
- Comment Brancher Un Bouton Poussoir Avec Un TélérupteurDocument5 pagesComment Brancher Un Bouton Poussoir Avec Un Télérupteurdgmemmanuel90Pas encore d'évaluation
- Exercices Fluo XDocument6 pagesExercices Fluo XLucas Petiot100% (3)
- Mémoire Finale (Chapitre2)Document28 pagesMémoire Finale (Chapitre2)Âÿâčhê ÎsmâïlPas encore d'évaluation
- Appareil Respiratoire IsolantDocument49 pagesAppareil Respiratoire IsolantEdja Edjam100% (1)
- 123 PDFDocument4 pages123 PDFOussama Abdaoui Jr.Pas encore d'évaluation
- Baccalaureat Blanc A n2 - Mai 2015Document2 pagesBaccalaureat Blanc A n2 - Mai 2015Soukoura AliPas encore d'évaluation
- Devoir de Synthèse N°3 - Physique - 3ème Technique (2011-2012) MR Fezai Mourad PDFDocument3 pagesDevoir de Synthèse N°3 - Physique - 3ème Technique (2011-2012) MR Fezai Mourad PDFLotfi BoucharebPas encore d'évaluation