Académique Documents
Professionnel Documents
Culture Documents
Chimie 3
Transféré par
LAILA ASLOUZICopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Chimie 3
Transféré par
LAILA ASLOUZIDroits d'auteur :
Formats disponibles
Transformations 2ème partie : Transformations non totales
Chapitre 3
d’un système chimique
chimiques s’effectuant Safi
dans les deux sens Niveau : 2BACSPF
❶ Réactions acido – basiques (Rappel)
❶❶ Définitions
Selon Bronsted, un acide est toute espèce chimique capable de céder un proton 𝐻 + au cours d’une
transformation chimique.
Selon Bronsted, une base est toute espèce chimique capable de capter un proton 𝐻 + au cours d’une
transformation chimique.
❶❷ Couple acide / base
Deux espèces chimiques forment un couple acide / base si l’on peut passer de l’une à l’autre par gain ou perte
d’un proton 𝐻 + .
Le passage d’un acide 𝑨𝑯 à sa base conjugué 𝑨− (au l’inverse) est exprimé par une écriture appelée demi –
équation acido-basique (protonique) :
𝑨𝑯 ⇄ 𝑨− + 𝑯+
Remarque :
− Si l’acide est le réactif, la demi – équation protonique s’écrit sous la forme : 𝑨𝑯 ⇄ 𝑨− + 𝑯+
− Si la base est le réactif, la demi – équation protonique s’écrit sous la forme : 𝑨− + 𝑯+ ⇄ 𝑨𝑯
❶❸ Equation d’une réaction d’acido – basique
Une réaction d’acido – basique met en jeu un transfert d’un proton 𝐻 + de l’acide 𝑯𝑨𝟏 d’un couple 𝑯𝑨𝟏 ⁄𝑨− 𝟏
vers la base 𝑨𝟐− d’un autre couple 𝑯𝑨𝟐 ⁄𝑨− 𝟐 .
En effet, On écrit les demi – équations protoniques correspondantes à chaque couple, puis o fait la somme :
𝐻𝐴1 ⇄ 𝐴1− + 𝐻 +
𝐴− +
2 + 𝐻 ⇄ 𝐻𝐴2
𝐻𝐴1 + 𝐴− −
2 → 𝐴1 + 𝐻𝐴2
Exercices d’application :
Déterminer les couples mise en jeu dans la réaction, puis écrire l’équation bilan de la réaction dans les cas
suivantes :
❶ Réaction d’un acide 𝐴𝐻 avec l’eau 𝐻2 𝑂.
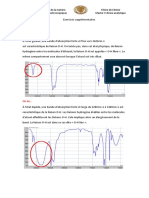
❷ Réaction de l’acide benzoïque 𝐶6 𝐻5 𝐶𝑂𝑂𝐻 avec l’eau 𝐻2 𝑂.
❸ Réaction de l’ammoniaque 𝑁𝐻3 avec l’eau 𝐻2 𝑂.
❹ Réaction de l’ammoniaque 𝑁𝐻3 avec les ions oxonium 𝐻3 𝑂+ .
❷ Le pH d’une solution aqueuse
❷❶ Définition du pH d’une solution aqueuse
Les propriétés acides ou basiques des solutions aqueuses dépendent de leur concentration en ions oxonium
𝐻3 𝑂+ . Pour déterminer ces propriétés, on mesure le pH de ces solutions.
Pour des solutions aqueuses diluées, le 𝑝𝐻 est défini par la relation suivante :
𝒑𝑯 = −𝒍𝒐𝒈[𝑯𝟑 𝑶+ ]
[𝑯𝟑 𝑶+ ] : Représente la concentration des ions oxonium en (𝒎𝒐𝒍. 𝑳−𝟏 ).
Prof : CHOUIKHI OTMANE Page 1 sur 5
Chapitre 3 : 2BACSPF
Remarques :
✓ 𝑝𝐻 est une grandeur sans unité.
✓ A partir de la mesure de 𝑝𝐻, on peut déterminer la concentration des ions oxonium en utilisant la relation :
[𝑯𝟑 𝑶+ ] = 𝟏𝟎−𝒑𝑯
✓ 𝒑𝑯 et [𝑯𝟑 𝑶+ ] sont inversement proportionnelles :
❷❷ Mesure du pH
On peut simplement avoir une indication sur la valeur du 𝑝𝐻 en utilisant :
✓ Des indicateurs colorés : ce sont des solutions aqueuses qui changent sa couleur selon la valeur du pH.
✓ Le papier pH : qui prend une couleur spécifique selon l’acidité de la solution.
Pour être plus précis, on utilise un appareil de mesure appelé pH-mètre.
❸ Les transformations totales et les transformations limitées (non totales)
❸❶ Les transformations totales
Activité 1 :
On dissout une quantité 𝒏 = 𝟑, 𝟖. 𝟏𝟎−𝟑 𝒎𝒐𝒍 de chlorure d’hydrogène 𝑯𝑪𝒍(𝒈), dans un volume 𝑽 = 𝟏𝟎𝟎 𝒎𝑳
d’eau distillée, on obtient une solution aqueuse d’acide chlorhydrique de concentration 𝑪 = 𝟑, 𝟖. 𝟏𝟎−𝟐 𝒎𝒐𝒍. 𝑳−𝟏
. A l’aide d’un pH-mètre, on mesure le 𝑝𝐻 de cette solution et on trouve que 𝒑𝑯 = 𝟏, 𝟒𝟐.
− +
Les couples acido-basiques misent en jeu sont : 𝐻𝐶𝑙(𝑔) ⁄𝐶𝑙(𝑎𝑞) et 𝐻3 𝑂(𝑎𝑞) ⁄𝐻2 𝑂(𝑙) .
❶ Ecrire l’équation bilan de la réaction.
− +
𝐻𝐶𝑙(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝑙(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞)
❷ Complétez le tableau d’avancement suivant en utilisant 𝐶, 𝑉, et les avancements 𝑥, 𝑥𝑓 , et 𝑥𝑚𝑎𝑥 .
− +
L’équation de la réaction 𝐻𝐶𝑙(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝑙(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞)
L’état L’avancement Les quantités de matière en (mol)
Initiale 0 𝐶. 𝑉 0 0
Intermédiaire 𝑥 𝐶. 𝑉 − 𝑥 𝑥 𝑥
En excès
Etat finale
𝑥𝑓 𝐶. 𝑉 − 𝑥𝑓 𝑥𝑓 𝑥𝑓
expérimentale
Cas de disparition
𝑥𝑚𝑎𝑥 𝐶. 𝑉 − 𝑥𝑚𝑎𝑥 𝑥𝑚𝑎𝑥 𝑥𝑚𝑎𝑥
totale de l’acide
❸ Déterminer l’avancement maximal 𝒙𝒎𝒂𝒙 .
On suppose qu’il y a disparition totale de l’acide :
Puisque l’eau est en excès, alors 𝐻𝐶𝑙 est le réactif limitant, c-à-d : 𝐶. 𝑉 − 𝑥𝑚𝑎𝑥 = 0
D’où : 𝑥𝑚𝑎𝑥 = 𝐶. 𝑉 A.N : 𝑥𝑚𝑎𝑥 = 3,8. 10−3 𝑚𝑜𝑙
❹ Déterminer la concentration finale en ions oxonium [𝐻3 𝑂+ ]𝑓 et déduire la valeur de l’avancement final 𝑥𝑓 .
On a : [𝐻3 𝑂+ ]𝑓 = 10−𝑝𝐻 A.N : [𝐻3 𝑂+ ]𝑓 = 10−1,42 = 3,8. 10−2 𝑚𝑜𝑙. 𝐿−1
𝑛𝑓 (𝐻3 𝑂 + ) 𝑥𝑓
D’après le T.A : [𝐻3 𝑂+ ]𝑓 = =
𝑉 𝑉
+]
Donc : 𝑥𝑓 = [𝐻3 𝑂 𝑓. 𝑉 A.N : 𝑥𝑓 = [𝐻3 𝑂+ ]𝑓 . 𝑉 = 3,8. 10−3 𝑚𝑜𝑙
Prof : CHOUIKHI OTMANE Page 2 sur 5
Chapitre 3 : 2BACSPF
❺ Comparer les avancements maximal et final, Que peut-on conclure?
On constate que 𝑥𝑓 = 𝑥𝑚𝑎𝑥 .Donc la réaction est totale.
Conclusion :
Une transformation totale est une transformation dans laquelle l’un des réactifs disparait complètement. Dans ce
cas : 𝒙𝒇 = 𝒙𝒎𝒂𝒙
❸❷ Les transformations limitées
Activité 2 :
Dans une fiole jaugée, on introduit un peu de l’eau distillée et on ajoute un volume 𝑽𝟏 = 𝟐 𝒎𝑳 d’acide
éthanoïque 𝑪𝑯𝟑 𝑪𝑶𝑶𝑯(𝒍) . Puis on remplit la fiole jaugée avec de l’eau jusqu’à le trait de jauge pour obtenir une
solution S de concentration 𝑪𝟐 et de volume 𝑽𝟐 = 𝟏, 𝟎 𝑳 . On immerge l'électrode de pH-mètre dans cette
solution et on trouve que 𝒑𝑯 = 𝟑, 𝟏𝟎.
On donne :
− La masse volumique de l’acide éthanoïque : 𝝆 = 𝟏, 𝟎𝟓 𝒈. 𝒄𝒎−𝟑
− La masse molaire de l’acide éthanoïque : 𝑴 = 𝟔𝟎 𝒈. 𝒎𝒐𝒍−𝟏
− Les couples acido-basiques misent en jeu : 𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑙) ⁄𝐶𝐻3 𝐶𝑂𝑂(𝑎𝑞)
− +
et 𝐻3 𝑂(𝑎𝑞) ⁄𝐻2 𝑂(𝑙)
❶ Écrire l'équation de réaction acido-basique entre l’acide éthanoïque et l’eau.
− +
𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝐻3 𝐶𝑂𝑂(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞)
❷ Calculer la quantité de matière initiale d’acide éthanoïque et déduire sa concentration dans la solution S.
La quantité de matière initiale :
𝑚 𝜌. 𝑉1 1,05 × 2
𝑛𝑖 (𝐶𝐻3 𝐶𝑂𝑂𝐻) = = A. N: 𝑛𝑖 (𝐶𝐻3 𝐶𝑂𝑂𝐻) = = 3,5. 10−2 𝑚𝑜𝑙
𝑀 𝑀 60
La concentration de la solution S :
𝑛𝑖 3,5. 10−2
𝐶2 = A. N: 𝐶2 = = 3,5. 10−2 𝑚𝑜𝑙. 𝐿−1
𝑉2 1
❸ Complétez le tableau d’avancement suivant.
− +
L’équation de la réaction 𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝐻3 𝐶𝑂𝑂(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞)
L’état L’avancement Les quantités de matière en (𝑚𝑜𝑙)
Initiale 0 𝐶2 . 𝑉2 0 0
Intermédiaire 𝑥 𝐶2 . 𝑉2 − 𝑥 𝑥 𝑥
En excès
Etat finale
𝑥𝑓 𝐶2 . 𝑉2 − 𝑥𝑓 𝑥𝑓 𝑥𝑓
expérimentale
Cas de disparition
𝑥𝑚𝑎𝑥 𝐶2 . 𝑉2 − 𝑥𝑚𝑎𝑥 𝑥𝑚𝑎𝑥 𝑥𝑚𝑎𝑥
totale de l’acide
❹ Déterminer l’avancement maximal 𝑥𝑚𝑎𝑥 .
On suppose qu’il y a disparition totale de l’acide :
Puisque l’eau est en excès, alors 𝐶𝐻3 𝐶𝑂𝑂𝐻 est le réactif limitant, c-à-d : 𝐶2 . 𝑉2 − 𝑥𝑚𝑎𝑥 = 0
D’où : 𝑥𝑚𝑎𝑥 = 𝐶2 . 𝑉2 A.N : 𝑥𝑚𝑎𝑥 = 3,5. 10−2 𝑚𝑜𝑙
❺ Déterminer la concentration finale en ions oxonium [𝐻3 𝑂+ ]𝑓 et déduire la valeur de l’avancement final 𝑥𝑓 .
On a : [𝐻3 𝑂+ ]𝑓 = 10−𝑝𝐻 A.N : [𝐻3 𝑂+ ]𝑓 = 10−1,42 = 7,9. 10−4 𝑚𝑜𝑙. 𝐿−1
𝑛𝑓 (𝐻3 𝑂 + ) 𝑥𝑓
D’après le T.A : [𝐻3 𝑂+ ]𝑓 = =
𝑉 𝑉
+]
Donc : 𝑥𝑓 = [𝐻3 𝑂 𝑓 . 𝑉2 A.N : 𝑥𝑓 = [𝐻3 𝑂+ ]𝑓 . 𝑉2 = 7,9. 10−4 𝑚𝑜𝑙
Prof : CHOUIKHI OTMANE Page 3 sur 5
Chapitre 3 : 2BACSPF
❻ Comparer les avancements maximal et final, Que peut-on conclure?
On constate que 𝑥𝑓 < 𝑥𝑚𝑎𝑥 . Donc la réaction n’est pas totale.
Conclusion :
Une transformation chimique n’est pas totale (limitée) lorsque l’avancement final 𝑥𝑓 est inférieur à l’avancement
maximal 𝑥𝑚𝑎𝑥 : 𝒙𝒇 < 𝒙𝒎𝒂𝒙
❸❸ Le taux d’avancement final d’une réaction chimique
Le taux d’avancement final 𝝉 d’une réaction chimique est égal au quotient de l'avancement final 𝑥𝑓 par
l'avancement maximal 𝑥𝑚𝑎𝑥 de cette réaction :
𝒙𝒇
𝝉=
𝒙𝒎𝒂𝒙
Si 𝝉 = 𝟏 ( 𝑥𝑓 = 𝑥𝑚𝑎𝑥 ), alors la transformation est totale.
Si 𝝉 < 𝟏 ( 𝑥𝑓 < 𝑥𝑚𝑎𝑥 ), la transformation est limitée.
𝜏 : est une grandeur sans unité, on peut l’exprimer en pourcentage.
❹ Etat d’équilibre d’un système chimique
❹❶ Sens d’évolution d’un système chimique
Activité 3 :
Question : Un système chimique évolue-t-il toujours dans le même sens ?
Om prépare une solution aqueuse (S) d’acide éthanoïque 𝑪𝑯𝟑 𝑪𝑶𝑶𝑯 de concentration 𝑪 = 𝟏𝟎−𝟐 𝒎𝒐𝒍. 𝑳−𝟏 par
dissolution d’acide éthanoïque dans l’eau pure, puis on verse dans deux béchers A et B, un même volume
𝑽 = 𝟐𝟎 𝒎𝑳 de la solution (S), et à l’aide d’un pH-mètre on mesure son 𝑝𝐻. Doc (𝒂)
• On ajoute avec précaution deux gouttes d’acide éthanoïque pur dans le bécher (1). Après agitation, on mesure
le 𝒑𝑯𝟏 de la solution obtenue. Doc (𝒃)
• On ajoute environ 𝟎, 𝟓𝒈 d’éthanoate de sodium solide 𝑪𝑯𝟑 𝑪𝑶𝑶𝑵𝒂 dans le bécher (2). Apres agitation, on
mesure le 𝒑𝑯𝟐 de la solution obtenue. Doc (𝒄)
❶ Ecrire l’équation acido-basique qui a eu lieu lors de la préparation de la solution S.
− +
𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝐻3 𝐶𝑂𝑂(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞)
❷ Dans quel sens le système chimique contenu dans le bécher (1) a-t-il évolué?
En ajoutant les deux gouttes d’acide éthanoïque, on constate une diminution du 𝑝𝐻, qui résulte donc d’une
augmentation de la concentration en ions oxonium 𝐻3 𝑂+ , ça signifie que le système a donc évolué dans le sens
de la formation d’ions 𝐻3 𝑂+ , c’est-à-dire dans le sens direct de l’équation de la réaction mise en jeu :
𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙) → 𝐶𝐻3 𝐶𝑂𝑂 − (𝑎𝑞) + 𝐻3 𝑂+ (𝑎𝑞)
❸ Dans quel sens le système chimique contenu dans le bécher (2) a-t-il évolué?
En ajoutant 0,5 g d’éthanoate de sodium, on observe une augmentation du pH et donc une diminution de la
concentration en ions 𝐻3 𝑂+ , ça signifie que le système a donc évolué dans le sens de la disparation d’ions 𝐻3 𝑂+ ,
c’est-à-dire dans le sens inverse de la réaction :
Prof : CHOUIKHI OTMANE Page 4 sur 5
Chapitre 3 : 2BACSPF
− +
𝐶𝐻3 𝐶𝑂𝑂(𝑎𝑞) + 𝐻3 𝑂(𝑎𝑞) → 𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙)
❹ Comparer les deux sens d’évolution.
La réaction mise en jeu peut donc s’effectuer dans les deux sens. Donc l’écriture de la réaction est modifiée en
remplaçant la flèche → par ⇄ . On écrit alors :
𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝐻2 𝑂(𝑙) ⇄ 𝐶𝐻3 𝐶𝑂𝑂 − (𝑎𝑞) + 𝐻3 𝑂+ (𝑎𝑞)
Conclusion :
Au cours de chaque transformation chimique limitée (non totale), une réaction se produite dans les deux sens,
direct et inverse, qu’on l'exprime par l'équation suivante :
𝐴 + 𝐵 ⇄ 𝐶 + 𝐷
Quand la transformation chimique est limitée, l’état final du système chimique est appelé état d’équilibre.
❹❶ Interprétation microscopique de l’état d’équilibre
On considère le système chimique suivant :
𝐴 + 𝐵 ⇄ 𝐶 + 𝐷
• A l'état initial, le système contient les espèces chimiques 𝐴 et 𝐵, la réaction se produit alors dans le sens
direct avec la vitesse 𝒗𝟏 .
• A l’état intermédiaire, 𝐴 et 𝐵 se réagissent, ç-à-d que ses quantités de matière ainsi que les chocs entre elles
diminuent, donc la vitesse 𝒗𝟏 diminue alors que les espèces chimiques 𝐶 et 𝐷 apparaissent et la réaction
alors commence se produire dans le sens inverse avec la vitesse 𝒗𝟐 , leurs quantités de matière, ainsi que les
chocs entre elles augmentent, donc la vitesse 𝒗𝟐 augmente.
• Lorsque les deux vitesses 𝒗𝟏 et 𝒗𝟐 s'égalent, le système n'évolue plus. C'est l'état d'équilibre dynamique.
Exercice d’application :
On dissout une masse 𝒎 = 𝟏, 𝟒 𝒈 d’acide propanoïque pur 𝐶2 𝐻5 𝐶𝑂𝑂𝐻 dans l’eau distillée, et on obtient une
solution aqueuse d’acide propanoïque de concentration molaire 𝑪 et de volume 𝑽 = 𝟒𝟎𝟎 𝒎𝑳.
La mesure du pH, à 25 °C, a donné la valeur : 𝒑𝑯 = 𝟑, 𝟎𝟗 .
On donne : La masse molaire de l’acide propanoïque : 𝑴 = 𝟕𝟒 𝒈. 𝒎𝒐𝒍−𝟏 .
❶ Calculer la quantité de matière initiale de l’acide propanoïque et déduire sa concentration.
❷ Ecrire l’équation de la réaction.
❸ Dresser un tableau d’avancement de la réaction, y indiquer l’état final.
❹ Montrer que le taux d’avancement final 𝝉 de la réaction s’écrit:
𝟏𝟎−𝒑𝑯
𝝉=
𝑪
❺ Calculer la valeur de 𝝉 et en déduire si la réaction est totale ou limitée.
Prof : CHOUIKHI OTMANE Page 5 sur 5
Vous aimerez peut-être aussi
- Transformations Chimiques S Effectuant Dans Les 2 Sens Cours 1Document5 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Cours 1Ahmed Yassine NaciriPas encore d'évaluation
- Cours de ChimieDocument13 pagesCours de Chimiekawaiialways9Pas encore d'évaluation
- 6 Réactions Acido-BasiqueDocument6 pages6 Réactions Acido-Basiqueateich simohamedPas encore d'évaluation
- 1 Bac Les Reactions Acido Basiques Cours 1Document6 pages1 Bac Les Reactions Acido Basiques Cours 1rihabPas encore d'évaluation
- Equilibre D'un Système ChimiqueDocument8 pagesEquilibre D'un Système ChimiqueNouhad KaisPas encore d'évaluation
- Les Reactions Acido Basiques Cours 1Document6 pagesLes Reactions Acido Basiques Cours 1منةيصةبصسكبةPas encore d'évaluation
- Activités 1Document4 pagesActivités 1LAILA ASLOUZIPas encore d'évaluation
- 1 - Transformations Rapides Et Transfomations Rapides-Pr SaadiDocument4 pages1 - Transformations Rapides Et Transfomations Rapides-Pr SaadiibtihalmelloukPas encore d'évaluation
- Cours Thermodynamique-ConvertiDocument45 pagesCours Thermodynamique-ConvertiRedOne DerrouazinPas encore d'évaluation
- Chimie 5Document11 pagesChimie 5LAILA ASLOUZIPas encore d'évaluation
- Examen National Physique Chimie 2 Bac SVT 2017 Normale CorrigeDocument10 pagesExamen National Physique Chimie 2 Bac SVT 2017 Normale CorrigeMohamed SaidiPas encore d'évaluation
- Correction Examen 2016-2020Document68 pagesCorrection Examen 2016-2020Mohamed SaidiPas encore d'évaluation
- Cours 1 - Suivi Temporel D'une TransformationDocument7 pagesCours 1 - Suivi Temporel D'une TransformationsalhiPas encore d'évaluation
- CC-Exos1 1011Document11 pagesCC-Exos1 1011Dabo100% (1)
- 2 Suivi Temporel D'une Transformation Chimique - Vitesse de RéactionDocument40 pages2 Suivi Temporel D'une Transformation Chimique - Vitesse de Réactionyunuabou3Pas encore d'évaluation
- Le Suivi Temporel D Une Transformation Chimique La Vitesse de Reaction Cours 1Document7 pagesLe Suivi Temporel D Une Transformation Chimique La Vitesse de Reaction Cours 1Boualem Talbi100% (1)
- Cours-Les Réactions chimiques-FR PDFDocument6 pagesCours-Les Réactions chimiques-FR PDFhakima032100% (1)
- 8 - Les Transformations Chimiques S'effectuant Dans Les Deux SensDocument10 pages8 - Les Transformations Chimiques S'effectuant Dans Les Deux Senspro alixPas encore d'évaluation
- Fiche Sur Loi Daction de Masse Conditions Dévolution Spontanée 1Document4 pagesFiche Sur Loi Daction de Masse Conditions Dévolution Spontanée 1chadaPas encore d'évaluation
- ACIDE BASE Equilibre D'un Systeme Janvier 2004Document3 pagesACIDE BASE Equilibre D'un Systeme Janvier 2004David BéliardPas encore d'évaluation
- Correction TD1 Génie Des Procédés Alimentaires LP IA (EST) 2020-2021Document10 pagesCorrection TD1 Génie Des Procédés Alimentaires LP IA (EST) 2020-2021Hassan lachgarPas encore d'évaluation
- Suivi Temporel Et Vitesse de Reaction Cours Corrige Et CompleteDocument7 pagesSuivi Temporel Et Vitesse de Reaction Cours Corrige Et CompleteYassine RabikPas encore d'évaluation
- 7 Réactions Acido-BasiquesDocument8 pages7 Réactions Acido-BasiquesMed yahyaPas encore d'évaluation
- Cours DosageDocument5 pagesCours DosageTEST - TESTPas encore d'évaluation
- Résumé .Chp 3.Transformations Associées à Des Réactions Acido-basique ..Document3 pagesRésumé .Chp 3.Transformations Associées à Des Réactions Acido-basique ..ayamazouz962Pas encore d'évaluation
- Corrigé Serie 3Document4 pagesCorrigé Serie 3Imane Bsr100% (1)
- Série 1 - Transformation ChimiqueDocument14 pagesSérie 1 - Transformation ChimiquemedPas encore d'évaluation
- 9 - État D'équilibre D'un Système 2Document8 pages9 - État D'équilibre D'un Système 2pro alixPas encore d'évaluation
- Potentiel - PHDocument3 pagesPotentiel - PHKahil LaibPas encore d'évaluation
- Chap V - Equilibre Liquide - VapeurDocument3 pagesChap V - Equilibre Liquide - VapeurHAMMOUPas encore d'évaluation
- BTS Chimie 1 Équilibre ChimiqueDocument10 pagesBTS Chimie 1 Équilibre Chimiquekarpla69Pas encore d'évaluation
- Révision N°1 Correction (MR KH Bessem) (Lycée Maknassy) PDFDocument2 pagesRévision N°1 Correction (MR KH Bessem) (Lycée Maknassy) PDFFakhri KlaiPas encore d'évaluation
- DS 6 SM Aet B 2018Document3 pagesDS 6 SM Aet B 2018Med BriniPas encore d'évaluation
- 5a. Essentiel A8Document6 pages5a. Essentiel A8chuyamadzenPas encore d'évaluation
- Correction de L'examen Des Enseignants Cadres Des Académies 2023 Matière: Physique Et ChimieDocument32 pagesCorrection de L'examen Des Enseignants Cadres Des Académies 2023 Matière: Physique Et ChimieMohamed AIT KASSIPas encore d'évaluation
- CHimie 1.2 - Réactions Acide - BasesDocument4 pagesCHimie 1.2 - Réactions Acide - Basessaadbouzid79Pas encore d'évaluation
- Dynamique Des Fluides ParfaitsDocument21 pagesDynamique Des Fluides ParfaitsAyoubPas encore d'évaluation
- Série 1Document7 pagesSérie 1chadaPas encore d'évaluation
- Dev de Synthese N°1 4eme SC Technique 1 FinalDocument5 pagesDev de Synthese N°1 4eme SC Technique 1 FinalMouhamed Ali SahbaniPas encore d'évaluation
- Les Reactions D Oxydo Reduction Exercices Corriges 1 3Document8 pagesLes Reactions D Oxydo Reduction Exercices Corriges 1 3chayma rebai100% (1)
- SN°4 MFluidesDocument7 pagesSN°4 MFluidesrachida lakaazPas encore d'évaluation
- 3 - Bilan D'energie D'un Système Réactif - 2Document22 pages3 - Bilan D'energie D'un Système Réactif - 2meriemmalika.aibPas encore d'évaluation
- Cedyna CHM 3Document17 pagesCedyna CHM 3Jonah LJDPas encore d'évaluation
- 02-Vitesse SerieDocument5 pages02-Vitesse SerieboustakatbPas encore d'évaluation
- Transformation Acide BaseDocument10 pagesTransformation Acide BaseNouhad KaisPas encore d'évaluation
- Biophysique Des Solutions 2023Document26 pagesBiophysique Des Solutions 2023zaki taleb100% (1)
- CH2Document4 pagesCH2drissboum1bacPas encore d'évaluation
- Extraction Ionique Exposé Final BonDocument26 pagesExtraction Ionique Exposé Final BonSurbroPas encore d'évaluation
- Devoir 2-s1 1BAC FR P.khaldoune (WWW - Pc1.ma)Document2 pagesDevoir 2-s1 1BAC FR P.khaldoune (WWW - Pc1.ma)saifeddinebenichou0Pas encore d'évaluation
- 2022 Examen 1 Chimie Solutions Corrigé LDDocument10 pages2022 Examen 1 Chimie Solutions Corrigé LDLaurent KeletaonaPas encore d'évaluation
- Transfo Thermo 11Document2 pagesTransfo Thermo 11stellaabossolo04Pas encore d'évaluation
- Examen National Physique Chimie 2 Bac SVT 2018 Normale CorrigeDocument9 pagesExamen National Physique Chimie 2 Bac SVT 2018 Normale CorrigeMohamed SaidiPas encore d'évaluation
- Examen Blanc SM Inter2222 PDFDocument8 pagesExamen Blanc SM Inter2222 PDFMouad ChakerPas encore d'évaluation
- Cours Final Biophys 2020 2021Document19 pagesCours Final Biophys 2020 2021afaf gouPas encore d'évaluation
- Chapitre 1 Réacteurs HomogènesDocument8 pagesChapitre 1 Réacteurs HomogènesGp GpPas encore d'évaluation
- S6 Chapitre 7 Equilibre ChimiqueDocument12 pagesS6 Chapitre 7 Equilibre ChimiqueMortadha RabahPas encore d'évaluation
- Correction Ds1 Bac SC 2018Document3 pagesCorrection Ds1 Bac SC 2018Anis DahnenPas encore d'évaluation
- TP 20 TSP Synthse Ester Odeur de Banane CorrectionDocument3 pagesTP 20 TSP Synthse Ester Odeur de Banane CorrectionEF YoPas encore d'évaluation
- Activités 1Document4 pagesActivités 1LAILA ASLOUZIPas encore d'évaluation
- Chimie 5Document11 pagesChimie 5LAILA ASLOUZIPas encore d'évaluation
- Chimie 3Document5 pagesChimie 3LAILA ASLOUZIPas encore d'évaluation
- Chapitre 7Document7 pagesChapitre 7LAILA ASLOUZIPas encore d'évaluation
- Chapitre 6Document9 pagesChapitre 6LAILA ASLOUZIPas encore d'évaluation
- Fabrication PDFDocument9 pagesFabrication PDFAymen RakroukiPas encore d'évaluation
- TD 2019Document32 pagesTD 2019Yc Yacine100% (1)
- TP 1 TractionDocument9 pagesTP 1 TractionMohcine EcharrifiPas encore d'évaluation
- Résumé: OH LibreDocument5 pagesRésumé: OH LibreLINDA CHABANEPas encore d'évaluation
- 1bac Biof ds1 Prof - ElyaagoubiDocument4 pages1bac Biof ds1 Prof - ElyaagoubiazezaPas encore d'évaluation
- Filtration 2Document3 pagesFiltration 2Imane RamadanePas encore d'évaluation
- Essai Au Scléromètre (SCHMIDT)Document3 pagesEssai Au Scléromètre (SCHMIDT)omar100% (1)
- Analyse Multivariée Des Relations Structures-Activités Dans Des Nouveaux Composés Organiques À Utilisation Médicinale SOUALMIA FatimaDocument130 pagesAnalyse Multivariée Des Relations Structures-Activités Dans Des Nouveaux Composés Organiques À Utilisation Médicinale SOUALMIA Fatimaazou korbaPas encore d'évaluation
- Inj Chiter LamriDocument79 pagesInj Chiter LamriHichem HamdiPas encore d'évaluation
- Usinage Des Materiaux SpéciauxDocument166 pagesUsinage Des Materiaux SpéciauxPerce NeigePas encore d'évaluation
- RamanDocument6 pagesRamanuyuyiuiuiPas encore d'évaluation
- TD1: Les Solutions Aqueuses (2 Séance) : Exercice 1Document2 pagesTD1: Les Solutions Aqueuses (2 Séance) : Exercice 1Tulay TurkanPas encore d'évaluation
- Cinétique ChimiqueDocument15 pagesCinétique ChimiqueYounes JaaidaniPas encore d'évaluation
- Calendrier Des Examens 1 Semestre de L'année Universitaire 2019-2020 Session 2Document3 pagesCalendrier Des Examens 1 Semestre de L'année Universitaire 2019-2020 Session 2Bergoug BahaPas encore d'évaluation
- Chap3-4 Lp105Document22 pagesChap3-4 Lp105lile aichaPas encore d'évaluation
- Etude de La Regularite Du Cru - BAKKAS Soukaina - 114Document43 pagesEtude de La Regularite Du Cru - BAKKAS Soukaina - 114Lamiae100% (2)
- Drain AxDocument10 pagesDrain AxaborazanePas encore d'évaluation
- Chapitre 18 - Eurocode 2 PDFDocument94 pagesChapitre 18 - Eurocode 2 PDFAhmed Skendraoui100% (1)
- M06 Application Notins Général RDM AC CCTP-BTP-CCTPDocument47 pagesM06 Application Notins Général RDM AC CCTP-BTP-CCTPGhassane Elhihi100% (10)
- Réactions Spécifiques DesDocument4 pagesRéactions Spécifiques Desmechergui mariemPas encore d'évaluation
- Ex 5p51Document5 pagesEx 5p51saraibnsoudaPas encore d'évaluation
- TP EnzymologieDocument9 pagesTP EnzymologieHamza WELGO50% (2)
- ComapDocument8 pagesComapslawny77Pas encore d'évaluation
- 1txh000097c0301 PDFDocument84 pages1txh000097c0301 PDFchahbounnabilPas encore d'évaluation
- Penetrant Rouge Dp-51Document3 pagesPenetrant Rouge Dp-51ALP69Pas encore d'évaluation
- Travaux Partique 2 de Chimie PDFDocument7 pagesTravaux Partique 2 de Chimie PDFBenouna Rajae AminaPas encore d'évaluation