Académique Documents
Professionnel Documents
Culture Documents
QCM Bioch 3ème
Transféré par
yousrabel990 évaluation0% ont trouvé ce document utile (0 vote)
42 vues30 pagesTitre original
QCM bioch 3ème
Copyright
© © All Rights Reserved
Formats disponibles
DOCX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
42 vues30 pagesQCM Bioch 3ème
Transféré par
yousrabel99Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 30
Dyslipidémie et athérosclérose Au-delà de 80 ans, la réalisation systématique Si TG>3.
4 => dosage de Apo B100 : 0,55-1,25
d’un bilan lipidique de dépistage n’est pas justifiée. g/L pour la femme et 0,55-1,35 g/L pour
Les lipoprotéines : 07 l’homme
- le chylomicron est le + volumineux , Obésité : excès de TG et non pas de Ch LPa : LDL + Apo A et Apo B (athérogène et
considérée comme exogène Dans les cas où les TG > 3,5g/l, le dosage est thrombogène)
- LDL => B100 seule impératif) le calcul ne suffit pas - On dose systématiquement le taux de la Lp(a)
- HDL => ApoA Valeurs Nle : chez les personnes présentant une
Le RCp LDL ou RCP B/E : est ubiquitaire foie + CT < 2 g/l ; LDLc < 1,60 g/l ; TG < 1,5 g/l ; HDLc hypercholestérolémie familiale.
+=> lie avec Apo B > 0,40 g/l (quel que soit le sexe ). - son taux est génétiquement déterminé
Rcp VLDL ou Rcp E => Apo E Analyse du sérum : - LDLc vrai] ou [LDLc sensible aux statines) =
Rcp ABC-A1 : TM ATP dépendant => HDL Sa limpidité ne peut être associée à une [LDLc mesuré] – [C - Lp(a)].
Rcp SR-BI => l’ ApoA1 =>HDL hypertriglycéridémie (hyper TG) sauf en cas - LPa ↑=> pseudo R° au statines (malgré qu’elle
Le Rcp Scavenger R sur les macrophage => LDL d’Hyperglycérolémie : sérum clair + fausse n’agit pas sur la LPa)
oxydé Hyper-TG (déficit de la glycérol kinase : une TAR Action des statines : régulent la HMG CoA
Lipase pancréatique dégrade le lipides en ou liée à l’X ). réductase, ils l’inhibent provoquant ainsi une
Chylomicron et VLDL => LPL( de la paroi Vx) => Sérum clair : Normal ou hypercholestérolémie diminution de la synthèse endogène
AG + Glycérol =< vers le T. adipeux pure type IIa. (principale) du cholestérol.
Régulé par : (L’Apo C-II est un cofacteur Le sparamètres spécifique à doser sont : Formule de Friedwald
activateur de LPL. CIII agit comme inhibiteur • L'Apo A1 est la principale apolipoprotéine des LDLc = cholesterol total (CT) – (HDLc + VLDLc)
La lipase hépatique fait la mm chose dans le lipoprotéines de densité élevée (HDL) qui sont VLDLc = TG/5 si TG en g/l (ou TG/2,2 TG en
foie antiathérogènes. mmol/l).
VLDL : 20% CH / 60% de TG • L'Apo B est contenue dans les lipoprotéines - HDLc = chléstérol TOT- cholésterol non HDL
Le Ch est amphiphile (si estérifié=> apolaire) de basse densité (LDL) et de très basse densité Le cholestérol total et le HDLc sont dosés
Le LDL c est le 1er fac athérogène (VLDL) qui sont athérogènes n’est valable que si le taux des TG est < à 3,5
Un bilan lipidique de base : • Lp(a) Contient une particule LDL dans sa g/l.
o Aspect du sérum structure (présence d’Apo B) : elle est Si Tg ≥3.5 : dosage de LDL et calcul de
o Taux de triglycérides (TG des VLDL) athérogène ; Elle a une forte analogie cholestérol non HDL :
o Taux de cholestérol total (CT) (LDL, HDL et structurale avec le plasminogène : elle est Cholestérol non-HDL = LDLc + 0,30g/l.
même VLDL). thrombogène - Le cholestérol non HDL correspond bel et bien
- Le dosage de l'Apo A1 permet de confirmer à la somme : LDL, Chylomicrons, IDL et Lp(a).
En cas de “normalité” , ne pas refaire avant 3 à des valeurs basses de l’HDLc0. les meilleurs marqueurs des particules
5ans Chez l’homme : 1,10 – 2,00 g/L ; chez la athérogènes : LDLc , Apo B , C-non HDL
femme : 1,2 – 2,2 g/L. la relation : TG ↑ => le taux de HDLc ↓à cause
Si HDL < 1.30 => dosage des ApoA1 de CETP / les gens avec hyper Tg => HDL bas
On a remarqué que les gens avec des taux
élevés de gros LDL ont moins de risque par
rapport aux gens qui accumulent des petites
LDL.(psq les ptt ne sont pas eliminé)
Chez les DT : TG↑, LDL faussement bas
Le pronostic est favorable si : Chol T/ HDLc < 5
pour les hommes et < 4,5 pour les femmes ;
LDLc / HDLc < 3,5 pour les hommes et < 3,2
pour les femmes ; Apo B / Apo A < 1 (on ne
trouve pas un taux de Apo B > taux d’Apo A)
Indication de lipidogramme :
- En cas de présence de lipoprotéines
anormales (type LpX, Lpa) :
- En cas de dyslipidémie mixte : type IIb (↑
concomitante de CT et de TG) ou type III (↑ des
IDL )
-En cas d’hypertriglycéridémies (chylomicrons
et/ou VLDL)
Il permet une analyse qualitative et
pseudoquantitative des lipoprotéines.
l’Hypercholestérolémie familiale HF :
- génétique AD , mut de LDLR (90%), APOB (5%)
et PCSK9 (1%)(prot de dégradation du LDLR) /La
mutation de l’Apo B est la moins sévère
- Maladie héréditaire la plus fréquente au
monde : 14 et 34 millions / mais méconnue
- clinique : exanthèmes tendineux, des arcs
cornéens avant 45 ans.
- il existe 2 formes :hétérozygote heFH ( + Fq)
et l’homozygote hoFH
- sérum clair , un pic de beta lipoprotéine
- c un type II selon Freidrikson
La maladie de Tangier 03 stades de formation de la plaque o Le LDL enrichi en TG subit l’action de la
- TAR , déficience du gène d’ABCA1 , quasi - strie lipoprotéine lipase et rentre dans le foie,
absence de HDL et d’Apo A1=> dépôt tissulaire - plaque o la lipase hépatique va agir sur les TG qu’il
du Ch => amygdale orange - complication renferme aussi, le transformant ainsi en sd-LDL
Déficience en Apo A1 QCM : (petites et denses LDL), et on aura une
- délétion complète du cluster génétique HF évoquer devant : LDL > 1 .90 H / LDL > 1.60 dégradation rapide de l’Apo A1 qui va être
ApoA1/Apo C3/Apo A4 Enf / le risque de IDM précoce est 20* éliminée par le rein.
- HDL tres bas , risque coronarien ↑ les chylomicrons sont plutôt les plus pauvres en D’où la relation : TG ↑ => le taux de LDLc ↓ :
Déficience en LCAT et maladie des yeux de protéines et les plus riches lipides Comment savoir alors que le taux LDLc est
poissons HLP IIB => est mixte mais le HDL n’est pas ↑ / faussement bas ?
- déficit de l'estérification du cholestérol HLP III => IDL Méthode n° 1 :
plasmatique un taux de TG élevée va augmenter l’activité de Dosage ApoB : : on sait que chaque lipoprotéine
- HDL plasmatique effondré la CETP, et donc le taux de sdLDL va augmenter, possède ses propres Apo. Les LDL et les sd-LDL
- d'opacités cornéennes on aura dans ce cas un taux de LDLc faussement possèdent tous des Apo B ;
- hypertriglycéridémie bas Le sujet avec LDLc faussement bas et donc sd-
- une anémie hémolytique normochrome Les récepteurs des LDL modifiées (Scavenger R) LDL élevé présente une ApoB plus élevée (voir
- une protéinurie sont des récepteurs éboueurs exprimés à la image)
Déficience en CETP surface des macrophages : ils ont une faible Méthode n°2 : on aura recours au calcul du
- TAR , HDL plasmatique ↑, affinité pour les LDL natives mais une forte cholestérol-non-HDL, ceci serait beaucoup plus
Athérosclérose affinité pour les LDL modifiées sans élevé chez un patient présentant un taux LDL
une « association de remaniements de l'intima rétrocontrôle négatif. faussement bas/ normal (tout simplement parce
des artères de gros et moyens calibres La Lp-PLA2 (Lipoprotéine associée à la qu’on dose ici tout le cholestérol excepté celui de
consistant en une accumulation focalisée de phospholipase A2) libère des médiateurs pro- HDL).
lipides, glucides complexes, de sang et de inflammatoires par hydrolyse de Dans l’HF : les mutations du gène LDLR sont
dépôts calcaires, avec remaniements de la phospholipides présents sur les (LDL). Elle est fatales, tandis que la mutation de l’Apo B est la
média ». produite essentiellement par les monocytes moins sévère
physiopath : macrophages et par les lymphocytes T. Elle est CT = CL-non-HDL + HDL
agression chronique => les LP transportent les exprimée dans le centre nécrotique des plaques
lipide de réparation d’athérosclérose
les LDL ^plasmatique ↑↑=> oxydation => non Relation LDLc- TG:
plus capté par le foie => reconnue par les o Une réaction impliquant la CETP va enrichir le
macrophage => cl spumeuse qui n’obéit pas au LDL en TG, et les VLDL en CE.
Rétrocontrôle –
Augmentation de Apo B100 et Ch non HDL =>
↑de Sd LDL
1. Conditions du prélèvement : La validité du bilan
lipidique dépend de quelques règles :
Sérum +++ : prélever sur un tube sec : les
anticoagulants sous-estiment le dosage des
lipides ( le CT++ jusqu’à 20% ) ;
Jeûne de 12 h : pas pour tous les paramètres
A distance d’une grossesse, 3 mois après
accouchement ; 2 à 3 mois après un processus
infectieux, chirurgical, sauf en cas d’IDM
(nouvelle recommandation).
Certains médicaments peuvent modifier les
concentrations sériques des lipides :
anticonvulsivants, oestro-progestatifs et
hypolipémiants
Des taux ↑ en Vit C (agent réducteur) et en
BRB entraînent une sous-estimation de la
concentration en CT : compétition avec le
substrat chromogénique lors de la réaction de
peroxydation. Exploration biochimique du LCR
Des concentrations importantes en Hb LCR nle : éléments <5 (monocyte ,LT) , eleveé chez le nné, GR absent
entraînent une surestimation de la Prot : tres faible, 0.20-0.45/ varie selon l’age, meme composition que le plasma
concentration en CT par interférence Gluc : 60% du gluc sanguin , hypo = hypoglycémie ou infection bact
colorimétrique. Ion : cl ↑117 , (↓en cas de méningite purulente) , H , vit, médiateurs chimique , lactate(0.25-1.5)
La prise chronique de l’alcool influence surtout La Pr du LCR : 90-180mmH2O / Volume : 120-150
sur GGT gamma glutamyl transpeptidase Le PH n’est pas plus alcalin que la plasma
Les VLDL : TG endogène, / Apo B100 et Apo Dans la méningite purulente : liquide trouble , elémt PNN++↑, gluc ↓, prot ↑, CL peut être Nle ou ↓
C ,dans certain situation elles peuvent etre lactate 3-10* la norme
athérogène Dans la méningite à liquide clair : TBK soit virale /prot ↑, elemt LT, gluc lactate :Nle ou ↓ ,CL nle
Le risque athérogène peut etre apprécier par le La TBK donne une méningite à liquide clair
rapport : Apo B / Apo A La glycorachie ↓ dans l’H méningé
Normalement, le liquide céphalo-rachidien est légèrement alcalin, pH 7,35 -7,40, en cas d’une méningite
bactérienne ; le pH diminue à 7,0-7,1.
La protéinorachie est définie comme la L'ANALYSE DU LCR: néoplasiques. o Hypertension
concentration en protéines dans le liquide Analyse cytologique: recherche de cellules, en Hypoglyémies endocrânienne
céphalo-rachidien. Elle ne doit pas être particulier globules blancs ; Ménigites purulentes
Méningites
confondue avec l'albuminorachie qui est la Analyse bactériologique: mise en culture pour
tuberuleuses
concentration de la seule albumine. identifier un éventuel germe en cause et Tumeurs méningées
L'électrophorèse du LCR : réaliser un antibiogramme. Syndrome de
pré-albumines : 6%, Analyse biochimique: dosage du glucose, des Rye(hépato-
albumines : 58,5%, protéines, des ions chlorures ; des lactates encephalpathie aigue
alpha-1-globuline 4,5%, Analyse macroscopique: étude de l'aspect et la Hémorragie sous
arachnoidienne
béta-1-globuline : 10%. couleur
Méningite rhumatoide
gammaglobulines : 9,5%. De nombreuses maladies inflammatoires ou
La glycorachie est ↑ en cas de HIC infectieuses du système nerveux central sont Les liquides sanglants ou jaunes (appelés
Le LCR Sa perméabilité est faible dans le sens responsables d’une synthèse intrathécale xanthochromiques) dans les trois tubes
sang → LCR. / Sa perméabilité est grande dans d’immunoglobulines (Ig). Ex SEP évoquent plutôt une hémorragie méningée,
le sens LCR → sang. - L’index d’IgG permet de mettre en évidence sans toutefois éliminer systématiquement une
Synthèse dans le plexus choroide et résorption une synthèse intrathécale d’IgG: méningite. La coloration jaune s’explique par la
villosité arachnoidienne de Paccioni Index de Delpech et Lichtblau : (IgG/Albumine transformation de l’hémoglobine en pigments
Le LCR subit une circulation passive du lieu de LCR )/(IgG/Albumine sérum) N<0,65 hématogènes ( tels que la bilirubine) au cours
sa production à son lieu d’élimination avec un d’une hémorragie méningée
clair trouble
débit de 20 cm3 /h. l pourrait être transsudatif en cas de
les méningites virales, méningite bactérienne
Il est renouvelé 3 fois par jour. compression mécanique ou d'un AVC.
tuberculeuses, méningée
Le LCR passe dans les sinus duraux et dans les néoplasiques, inflammatoire Physiologiquement d’aspect limpide
veines Spinales et à un moindre degré dans la mycosiques amicrobie
lymphe, le long des nerfs. leptospires et
Exploration du métabolisme glucidique
La composition du LCR est proche de celle du méningites décapitées
Le métabolisme glucidique comporte 2 phases :
plasma avec :
Hypoglycorachie Hyperglyorachie - Phase absorptive = glycolyse +
- pH plus acide (7,32) ➜ PaCO2 plus élevée ;
Diminue glycogénogénèse.
- Moins de : glucose, protéines, k+ ;
indépendamment de la o Diabète sucré - Phase post absorptive = glycogénolyse +
- Plus de : Cl- ;
glycémie au cours des o Encéphalite néoglucogenèse.
- Même concentration en Ca2+ ; méningites épidémique Index glucidique : 50-70
- Principal tampon : HCO3-. bactériennes et o Méningites - Glycémie à jeun = entre 0,7 et 1,1g/l.
mycosiques, et dans séreuses et
l’infiltration du LCR par urémiques
des cellules
L’insuline agit sur la phase absorptive/ glucagon test statistique test dynamique= en milieu H surveillance
en post absorptive glycémie à jeun : hépariné, épreuve hyperglycémiante : HGPO , HbA1c :EDTA , gly des 6-8S , VN : 4-
régulation métabolique - enz :HK HGPIV , test au glucagon(Explore la 6-7
absorptive post A jeun - colorimétrique :GOP/POD capacité de libération du glucose fructosamine : Alb (lysine), 200-
Glycolyse. Glycogénolyse Lipolyse. glycémie post prandiale : 2h hépatique (glycogénolyse) + section 265µmol/l ou 2.8 à 3.9µmol/g de
Lipogenèse. (hépatique + Cétogenèse. apres , VN=<1.40 résiduelle d’insuline après protéine./ 2-3S
Glycogénèse. musculaire). Protéolyse glycosurie : semi-quantitatif , l’hyperglycémie.) Microalbiminurie (pour les Cplx+
Insuline +++ Néoglucogenèse musculaire. réagit au GOD / quantitatif epreuve hypoglycémiante : test à +) :néphropathie DT,
hépatique. Adrénaline +++ GOD/POD , Glycémie insuline(0.1UI/Kg) , test au microangiopathies , VN :30-300
Lipolyse. >10mmol/l → glucosurie tolbutamine (sulfamide) => insuline ↑
Glucagon +++ apparait => hypogly (Explore la fonction Oses+ prot plasmatiques →
régulation nerveuse dosage de l’insuline : EDTA, endocrine du pancréas.) fructosamines
ELISA sandwitch , 10-20mUI/L insulinome : hypo importante Oses + hémoglobine →
sympa para S
dosage du peptide C : de la absence d’hypo => DT1 ID hémoglobine glyquée.
Hyperglycémiant. Hypoglycémiant.
pro-insuline , reflète l’insuline - c une liaison non enzymatique
Active le glucagon. Inhibe le glucagon.
endogène
Inhibe l’insuline. Active l’insuline.
dosage de glucagon :EDTA ,
régulation hormonale
par IC 80-120 pg/ml
hypo hyper
insuline HT, CTC, glucagon ,
adrénaline
- HT et CTC agit à long terme en modifiant l’ADN
- es autres à court terme en changeant la voie
La glycémie capiliare prend en compte l’Hte ( Hte ↑=> gly ↓)
métabolique par l’AMPc
Lecture des BU : Lecture faussée par vitamine C, dakin, eau de javel….
TEST au glucagon :
o Absence d’hyperglycémie => épuisement des réserves hépatiques de l’insuline ou déficit enzymatique
dans la voie métabolique.
o Retour à la normale retardé => diabète.
o ↑ anormale de la sécrétion d’insuline => insulinome
Exploré les hyper par l’insuline / les hypo par le glucagon
Glycogénoses ou endocrinopathie => hypo glycémie par insuline prolongée =hypersensibilité des tissu
diabète, déficit en récepteurs d'insuline et hypersécrétions des hormones hyperglycémiantes=> insulinoR°
l’HbA1c ↑ avec l’Age
Troubles du métabolisme glucidique o 0.92 – 1.25 g/l => DG. o >1.26 g/l => DT. Dgt : Epreuve de charge au fructose (30g /m²) et on
l’insuline et le peptide C => utile pour - Glycémie à 2 heures (après le début des dose fructose et glucose / ou l’activité de la F L-P
l’exploration des hypo Gly spontanée repas) ; < 1,20 g/L. aldolase sur biopsie de foie
peptide C =< l’activité résiduelle du pancréas - HbA1 c < 6,5%. Résultats : fructosémie Nle : 0,15 à 0,20 g/l
DT1 Hypoglycémie : Si intolérance : > 0.2-1 g/l + hypo Gly
pro insuline => intoxication au sulfamides, Glycogénose :
adénome à pro-insuline -déficit enz dans le métabolisme de glycogène
DT est une hyperglycémie chronique o Glycogénose de type 1 (maladie de Von gierke).
DT1 : o Glycogénose de type 3b (Forbes/Cori).
Elle peut etre par QCMs :
- Au moins l’un des auto-anticorps est présent :
- déficit enzymatique Hypogly :
o Anticorps anti-ilots (ICA).
- défauts de substrats - déficit en G6P
o Anticorps anti-GAD.
- hyperinsulinisme - intolérence au fructose
o Anticorps anti-insuline.
- déficits endocriniens - hyperinsulinisme
o Anticorps anti- IA2.
- autres : toxique , IHC - insuffisance hypophysaire Tm
o Anti ZnT8.
Galactosémie DG : dépistage au T1, > 0.92 / ou > 1.53 apres
A l’état normal : la fixation de l’insuline sur son
- TAR, rare, HGPO
récepteur induit une translocation des GLUT4
-Galactosémie classique : déficit en GALT : La gly est majoré par l’alcool et le froid
vers la membrane → capture du glucose
(- Cataracte. - Retard mental. – Cirrhose) La glycogénose I : Von Gierk : hypo gly sévère ,
- dans le pré DT => les Cl devient + R°
- Déficit en galactokinase : cataracte. acidose à TA normale , hyper Tg hyper Ch ,
Dans le DT1 => Histoire de MAI
Bio : L’identification du GAL urinaire par hyper Uricémie / déficit en G6P (no G6PD) Ch17
Dans le DT2 =< Histoire de diabète familiale
chromatographie. - clinique : Le début survient généralement dès
DT2 :
Dgt : Dosage du GAL 1-P érythrocytaire par la les premières semaines de vie avec la
Insulino-R° => hyperinsulinisme + intolérence
galactokinase. - Mesure de l’activité GALT. découverte d'une hépatomégalie ++
au gluc => ↓le l’activité des Cl β = DT2 apparait
Intolérance héréditaire au fructose : La tolérance au jeûne est très limitée
Diabète IIair :
- déficit en fructose 1-P aldolase Convulsions dues à l'hypoglycémie
- pancréas exocrine
- peut etre mortelle L'hyperlactacidémie, responsable d'une acidose
- trisomie 21
-Après la diversification → vomissements + métabolique sévère et d’une hyperuricémie
- cirrhose, hémochromatose , hépatite C
hypoglycémie sévère (goutte)
Diabète mono-génique :
- jamais de diarrhée et, il ne se développe ni Faciès poupin, dû au dépôt de graisses dans le
Mody: le plus fréquent, dû à la mutation de 6
troubles oculaires ni retard mental tissu sous-cutané
gènes./ DT néonat
contrairement à la galactosémie. Les complications rénales débutent par une
DG
Bio : hypo gly PP / fructosurie (par liqueur de protéinurie → l'insuffisance rénale.
- Glycémie à jeun : < 0,95 g/L [Normal]
Fihling)
Glycogénose Type I : déficit en glucose 6P et non pas Glycogène 6P Attention
La fructosamine est un composé qui se forme lorsque le glucose se combine avec l’albumine
Fructosamine => 1-3semaine / HbA1c => 2-3 mois
Indications cliniques de dosage de la fructosamine
- Surveiller la glycémie moyenne au cours des 1-3 dernières semaines ;
- Évaluer la réponse à l'insulinothérapie ;
- L'établissement ou la modification d'un plan de soins du diabète en observant leur efficacité;
- Diabète gestationnel
DIAGNOSTIC BIOCHIMIQUE DE DIABETE
- Glycémie à jeun ≥ 7,0 mmol/L = aucun apport Confirmation Dgt de la galactosémie : Dans la maladie de Wilson pas de glycosurie
calorique depuis au moins 8 heures à 2 reprises o Épreuve de charge en Galactose : abandonnée Les glycogénose Type I et III qui s’accompagne de
- Ou Taux d’HbA1c ≥ 6,5 % (chez les adultes) car mal tolérée hypoglycémie
mesuré à l’aide d’un test normalisé et validé, o Dosage du Gal 1-P érythrocytaire par la Sd métabolique :
en l’absence de facteurs compromettant la galactokinase ;
fiabilité du taux d’HbA1c o Mesure de l’activité GALT.
- Ou Glycémie 2 heures après l’ingestion de 75 g Les méthodes de référence dans le dosage de
de glucose ≥ 11,1 mmol/L (HGPO) ; HbA1c : les méthodes de référence sont : les
- Ou Glycémie aléatoire ≥ 11,1 mmol/L (2g/l). techniques chromatographiques,
Conversion : g/l x 5.55 = mmol/l immunologique et l'électrophorèse
Galactosémie : - EP capillaire est performante en matière de
- classique : TAR , déficit en GALT galactose 1- détection des fractions anormales d’Hb.
phosphate uridyl transférase=> Ch 09 - chez l’insuffisant rénale => surestimation
- IIair : déficit en galactokinase et non pas - Les résultats d’HbA1c doivent être exprimés soit
glucokinase Attention en unités IFCC (mmol/mol) soit en unités NGSP
Clinique : dérivées (pourcentage d’Hb totale et non pas de
Refus de biberons, vomissement, perte de prot sérique ) par un calcul utilisant l’équation
poids ; directrice IFCC-NGSP
Un ictère, une hépatomégalie ; sur estimation s/ estimation
La cataracte n'est habituellement pas L’hypertriglycéridémie ; Vit C et E ;
présente à la naissance mais se développe L’insuffisance Maladie hépatique
petit à petit sur une période de quelques rénale/hyperuricémie chronique ;
(Hb carbamylée) ; Hémodialyse ;
semaines à quelques mois (accumulation
Déficit en fer, vit B12, B9 Hémolyse ;
du galactitol) ; Splénectomie ; Transfusion sanguine ;
Un retard mental (difficile à détecter et ne Abus d’opiacés, d’alcool Présence d’HbS et C ;
devient réellement évident qu'après 6 à 12 ou d’acide acétylsalicique Splénomégalie ; Le peptide C :c la production endogène de
mois d'évolution) Hyperbilirubinémie ; Médicaments : dapsone, l’insuline , il l y équimolaire, on peut le doser
Sensibilité aux infections bactériennes Présence d’hémoglobine antiviraux, interféron, dans le sérum ou dans les urines, c de la pro-
(principalement du type Escherichia Coli), fœtale (Hbf) ; fer, EPO... ; insuline, DID est fortement abaissé
Ethnie (Africain/Africain- Grossesse. Note : Quand la dégradation sous l'influence de
causes principales de la mortalité..
Américain).
la phosphorylase atteint un point de
branchement (liaison 1- 6), une enzyme
particulière est nécessaire qui s'appelle Le glucagon :
l'enzyme débranchante. - par les Cl alpha, agit sur les Cl hépatocytes et
L'enzyme débranchante permet la libération de les adipocytes, n’a pas de Rcp musculaire ,
glucose libre, non phosphorylé. Une fois que favorise l’activation de la phosphorylase
l'enzyme débranchante a accompli son rôle, la Glycogénose de pompe :
phosphorylase active peut à nouveau agir pour - déficit en Maltase acid, atteinte musculaire ++,
dégrader les chaînes de glycogène. Dgt par l’activité alpha glucosidase au niv des
En l'absence d'enzyme débranchante, le leucocytes et fibroblaste
glycogène a une forme particulière, avec des Selon l'âge de début de la maladie de Pompe, on
branches courtes, appelées dextrine limite distingue trois formes:
- ca se voit dans les glycogénose => La forme infantile est la plus fréquente et la plus
Le dépistage du DG peut se faire en post Partum grave.
pr le dosage du HbA1c Elle débute avant 3 mois et se manifeste
Si premier desage de glycémie revenant hyper => par une hypotonie ;
* refaire un 2ème dosage On peut noter une pseudo hypertrophie
* demander une HbA1c musculaire ;
L’INTOLERANCE AU GLUCOSE est définie comme L'atteinte des muscles respiratoires se
- Une glycémie à jeun entre 1.10 et 1,26 g/L ; traduit par une insuffisance respiratoire ;
- Une glycémie élevée après une HPO : entre Le cœur est rapidement défaillant avec
1,40 et 2 g/L ; cardiomégalie ;
- Une HbA1c entre 5.7 et 6.4%. => Maladie de Pompe à début tardif ;
HbA1c : correspond à la fixation de glucose sur la => La forme adulte de la maladie :
valine N-terminale de la chaine B de Hb/ sans survient au-delà de 20 ans sans atteinte
intervention enzymatique cardiaque,
- l’intensité de la glycosilation est corrélée au Faiblesse musculaire lentement évolutive.
taux de glycémie La glycogénose de type V : maladie de Mc
On demande HGPO devant une intolérence au Ardele, déficit en Myophosphorylase, attinet
gluc , et devant la présence de FDR diabétique musculiare ++, rhabdomyolyse + myoglobine ↑
La glycogénose de type III est due au mauvais => IRA , CPK ↑
fonctionnement de l'enzyme débranchante Les CPK sont ↑ dans : glycogénose type II, III, V
dans les muscles, dans le foie ou dans ces deux Glycogénose type IX : déficit en phospho kinase
tissus à la fois
Exploration du remodelage osseux
métabolisme hyper hypo
Ca Calcémie : 88-104 mg/l soit 2,20 – 2,60 mmol/l. Calcémie > 2,63 mmol/l < 2,25 mmol/l
Calcium ionisé: 47,2 – 52 mg/l soit 1,18 – 1,30 Ca2+> 1,40 mmol/l. - Signes d’hyperexcitabilité = crise de
mmol/l etio : tétanie = signe de Trousseau avec
le CA2+ est 50% de la Calcémie tot - Excès d’apports calciques (iatrogène). paresthésies et convulsions.
- Acidose : ↑ proportion Ca ionisé /Ca Total (inverse - Insuffisance rénale chronique - Hypervitaminose D -par défaut d’absorption digestive
pour alcalose) - Syndrome BURNETT( exes de lait ) => néphrocalcinose + IRC -par défaut de réabsorption rénale,
- Hyperprotidémie : ↑ calcémie total mais ↓ part de - néo : Kc ostéophiles+ MM paranéo par sécrétion d’un peptide exemple l’IRC.
Ca ionisé. PTH-like -déficit en vitamine D +++++
- Hyperphosphorémie : ↓ Ca ionisé et ↑ proportion - non néo : d’hyperPTH primitive, Immobilisations prolongées , TRT → hypoparathyroïdie primitive
Ca complexé. par lithium . idiopathique ou chirurgicale .
CaC=CaM+0.025* (40- albuminémie) - Granulomatoses : sarcoïdose++(↑calcitrol) → pseudo hypoparathyroïdiene
Sachant que : - Iatrogène : diurétique thiazidique . Par résistance à la PTH.
la calcémie : en mmol/L - Maladie de Paget .
la protidémie : en g/l - Insuffisance surrénalienne aigue.
On aurait divisé par 40 ( ou x0.025) si on souhaitait - Phéochromocytome .
avoir un résultat en mmol/l - Hypercalcémie familiale bénigne .
Ph 0,8 -1,45mmol/l > 1,45 mmol/l Pas de Sg clinique < 0,80 mmol /l.
-Insuffisance rénale -SNC : tremblements, irritabilité, …..
-Maladies endocriniennes -Musculaire : Faiblesse
-Hypoparathyroïdie -Cardiaque : ↓ du contractilité myocardique .
-hypervitaminpse D -Respiratoire : ↓ de la contractilité du diaphragme
- pseudo hypoparathyroïdie. -Os : ↑ de la résorption osseuse
-Hyperparathyroïdie . -Diabète phosphoré . -Avitaminose D. -
Perfusion de glucose. -Ostéomalacie.
Mg 0,75 à 0,90 mmol/l -l’insuffisance rénale avec DFG< 30 ml/mn. < 0,6 mmol/L.
-les surcharges iatrogènes (antiacides). : Diabète, Alcoolisme, Stress
Syndrome de Laron : résistance des tissus-cibles à la GH (GH augmenté) Les corticoïdes diminuent l'absorption intestinale du calcium et la réabsorption
Dgt biochimique de GHD : rénale avec comme effet hypocalcémie et hyperparathyroïdisme secondaire
- dosage d’IGF1 - Trou osmolaire = Osmolarité mesurée - Osmolarité calculée
- utilisation des tests de stimulation combinée (2 agents pharmaco ) - Osmolarité plasmatique = (Na + K)*2 + Urée + Glycémie ( pas de HCO3-)
- utilisation du test de tolérence de l’insuline en 1re intension( non utilisée L'hypercalcémie tout comme l'hypokaliémie sont responsables d'un diabète
chez l’enfant > 5ans) insipide néphrogénique par inhibition de la sécrétion d’ADHsur le tubule
Marqueur de la formation osseuse : rénale
- PAL osseuse spécifique Les diurétiques thiazidiques augmentent la réabsorption rénale de calcium =<
- ostéocalcine CI dans l’hyperCa
- P1CP / P1NP Les phases du cycle du remodelage osseux : en plus
Le diagnostic biologique des états de carence et de surcharge en vitamine D de la phase de quiescence on a :
repose sur le dosage dans le plasma ou le sérum de 25(OH)D 3 et de
1. Phase d’activation
25(OH)D 2 .
Le dosage de la vitamine D 2 (ergocalciférol) et de la vitamine - A la surface de la matrice osseuse, recrutement des
D 3 (cholécalciférol) dans le sérum est d'un intérêt limité; il ne permet pas précurseurs mononucléés des ostéoclastes.
d'évaluer les réserves car leur hydroxylation est très rapide 2. Phase de résorption
De même, la production de 1,25(OH) 2 D 2 et 1,25(OH) 2 D 3 étant étroitement
-Adhérence des ostéoclastes qui creusent un trou =
contrôlée, leur dosage dans le sérum ne renseigne pas sur l'état de carence
lacunes de Howship
ou de surcharge en vitamine D.
Dosage de la vit D se fait par chimiluminescence -Relargage des ions H+
-Digestion de la matrice collagénique (cathepsine K et
les métalloprotéases).
3. Phase d’inversion
-Remplacement des ostéoclastes par des Cellules
mononucléées type macrophages.
Noter que la disparition des ostéoclastes est un signal
de reformation osseuse.
4. Phase de reconstruction (néo formation osseuse)
-Recrutement des ostéoblastes dans la lacune, qu’ils
comblent en apposant une nouvelle matrice organique,
qui sera ensuite minéralisée.
le Calcium osseux représente 99% du calcium total, sous forme de cristaux - Initialise la formation de cristaux d’hydroxyapatite et inhibe la minéralisation
d’hydroxyapatite (≈ 1000gr). après l’atteinte d’un seuil de saturation en sel.
- Ca osseux échangeable : 4gr (100mmoles), (réserve de calcium pour le maintien - Permet la liaison entre la matrice organique (fibres de collagène) et la matrice
de l’homéostasie calcique). inorganique (cristaux d’hydroxyapatites) de l’os.
- Ca du tissu osseux profond non échangeable. - Passe dans circulation sanguine.
- A une grande spécificité ostéoblastique
L’acidose peut donner une hyper Ca
- La liaison calcium-albumine dépend du pH. Lors d'une acidose par exemple (pH
diminué), il y a une altération de la liaison calcium-albumine ce qui va engendrer La PTH rp :
une augmentation de la fraction ionisée(compétition entre les H+ et les Ca2+ au - PTH-rP is composed of 141 amino acids and shows significant homology with
niveau de la fixation à l’albumine) PTH in the first 13 amino acids (extrémité N-terminale)
- Its actions include binding to and activating the PTH receptor, thus simulating
Pour la résorption = Vit D + PTH + RANKL + MCF + PGE2 + IL1,6,1 the PTH biological effects on bone, kidney, and intestine. Similar to PTH, PTH-rP
formation = Calcitonine + sexuelles + OPG + BMP + TGF- β + IGF + IL4,10,13 increases bone resorption by stimulating osteoclasts and promotes renal tubular
le calcium ionisé est PLASMATIQUE reabsorption of calcium. The net effect is elevated serum calcium concentration.
la vit D est résorptive à dose élevée - La principale différence entre la PTH et la PTHrP est que la PTH a une action
La phase organique de la matrice extracellulaire du tissu osseux est composé de : endocrine : véhiculée par le sang elle agit à distance de son lieu de sécrétion alors
*Collagène type 1 (90% de la matrice organique) organisé en fibre de collagène que la PTHrP agit localement, elle a une action paracrine
participant aux propriétés mécaniques de l’os. - Increased PTH-rP is seen in squamous cell carcinomas of the lung, esophagus,
Le Collagène est caractérisé surtout par la présence de résidus
cervix, and skin, as well as in other malignancies (e.g., islet cell carcinomas, T-cell
hydroxyproline. Il synthétisé par les ostéoblastes sous forme de and B-cell lymphomas, multiple myeloma).
procollagène qui après clivage libère un propeptide N-terminal (PINP) et - PTH-rP is measured by immunometric assay. The reference interval for PTH-rP
un propeptide C-terminal (PICP). is method dependent. In normal individuals, PTH-rP levels range from
La rigidité et les propriétés mécaniques du collagène sont assurées par
undetectable to around 2 pmol/L.
des ponts intercollagènes formant des liaisons croisées (=cross links). GH n’a pas d’action phosphaturiante/ les CTC sii
Les enzymes ostéoclastiques dégradent les ponts intercollagènes, ce qui
L’absorption intestinale du Ph :
entraine la libération de produits de dégradation : (biomarqueurs) - se fait d’une part par un processus d’absorption passif non saturable et
- sous forme libre (40%): Pyridinoline (PYP) et Desoxypyridinoline (DPD). d’autre part par un processus actif saturable.
- sous forme liées (60%): Télopeptide N-ter du collagène I (NTX) et Télopeptide C- Le processus passif est le plus utilisé dans les conditions physiologiques,
ter du collagène I (CTX). c’est un gradient de concentration entre la lumière intestinale et le
*Protéines non collagéniques (PNC) (10%): ostéocalcine – ostéonectine, liquide interstitiel.
fibronectine, servent à l’induction de la minéralisation. Le processus actif est un cotransport Na+ /Pi (via le cotransporteur
Ostéocalcine:
NPT2b exprimé au niveau de la membrane apicale des entérocytes) qui
est stimulé par la 1-25(OH)2 vitamine D
La PTH a un effet indirect sur l’absorptoon du Ph Dosage de l’alb urinaire : urines des 24h ou spot matinale, (pas de censervation
on dose au labo le phosphore inorganique (Pi) = phosphate des urines) , en dehors des infection , il est recommendé de faire 03 dosage
80 à 90 % sont réabsorbés et seulement 10 à 20 % sont excrétés ; - la
Hémochromatose : Hypersidérémie => Hyperferritinémie avec CSF élevé et
réabsorption a lieu essentiellement au niveau du tube contourné
proximal (pour 85 % contre 15 % environ au niveau des tubules plus TIBC basse
distaux).
Hypo Ca : Sd néphrotique , hypo PTH, hypo Mg 2+ sévère, IRC
Hyper Ca : + NEM1, leucémie aigue
Dans l’hypo PTH Iair :hyper Ph, hypo Ca, hypo Ca urie, concentration faible en
vit D active
pour diagnostiquer la maladie de Wilson on dose : céruléoplasmine + du cuivre
Hypert PTH Iair =< rétention du Ph > 0.9
sanguin + cuivre urinaire.
La calcitonine est une H polypeptidique , hypo Ca ,sécrété par les Cl C , tres
-la maladie de Wilson est une maladie autosomale récessive en rapport avec
elevée dans le CMT , inhibe l’action des ostéoclaste
une mutation dans le transporteur ATPasique du cuivre ATP7B ;
PTH favorise la réabsorption de Ca2+ ionisé / ↓la réabsorption du Ph , elle
-Biologiquement on aura : l’effondrement de céruléoplasmine ; baisse de la
permet une 2ème OH de la vit D3,
cuprémie ; augmentation de la cupriurie
PTH est une H polypeptidique , 84 Aa , libération IIair à la stimulationdu CaSR /
-Mécanisme : diminution de l’incorporation du cuivre dans l’Apo
agit sur un Rcp qui présente une similitude avec le Rcp de la calcitonine et la
céruléoplasmine → diminution de la céruléoplasmine sérique →
sécrétine
accumulation du cuivre, surtout dans le foie, la cornée, les reins et la peau
Hypoprotidémie : ↓ calcémie total mais ↑ part de Ca ionisé
( Il faut savoir que c'est la cuprémie totale qui est diminuée (par diminution
(Inversement pour l’hyperprotidémie)
du taux du Cu liée à la céruléoplasmine ) tandis que la fraction libre du Cu
Jamais de calcémie sur EDTA , Le tube EDTA contient du potassium et un
dans le sérum est augmentée )
chélateur de calcium (qui peut baisser la calcémie)
- l’anneau de Keiser Fleicher n’est pas pathognomonique
Dysprotéinémie
↓ du pic α1g sur EPP => evoque en premier une baisse de α1AT
Sd néphrotique : ALb et α1g et Ca ↓, α2g ↑, hyper lipidémie
α1AT : C'est la protéine la plus importante quantitativement parmi les
Famille des α1g : antitrypsine, antichymotrypsine, orosomucoide, transcortine
globulines α1.
Marqueurs de la dénutrition : préalb , alb , RBP, transferrine (mechi
- C’est une glycoprotéine positive de la réaction inflammatoire
l’haptoglobine ni CRP)
- Elle présente une action anti-protéasique
=> Un déficit est associé à des pathologies : (cofacteur de la LPL) qui, normalement, assure
- Pulmonaires chez l’adulte : emphysème ; leur épuration
- Hépatiques chez l’enfant : cirrhose. Hypocalcémie : par diminution de la fraction du
calcium liée aux protéines.
=> Une augmentation se voit lors de la phase aiguë de la réaction
Généralement, toutes les fractions diminuent
inflammatoire.
(même la ferritine migrant en β) à l’exception
=> Elle présente un grand polymorphisme génétique. Les α1 AT ont une du bloc α2 qui augmente ;
variation interindividuelle même s’ils ont tous le même rôle. Le chapeau mexicain est la conséquence de
=> Plusieurs gènes sont impliqués dans sa biosynthèse : il existe 23 allèles l’augmentation de synthèse par le foie de
différents soit 23 génotypes différents. l’alpha 2 macroglobuline. Cette synthèse a pour
but de lutter contre la baisse de la pression
SYNDROME NÉPHROTIQUE: oncotique.
L’installation progressive ou explosive d`un LES GAMMAPATHIES
syndrome œdémateux ; Elles forment un groupe hétérogène de
Protéinurie abondante ; pathologies caractérisées par la présence d’un
nombre accru d’Ig dans le sang ;
Les œdèmes : mous, blancs, prennent le godet,
prédominent dans les territoires déclives. Elles sont polyclonales ou monoclonales selon la
distribution relative de la zone g à
Biologie :
l’électrophorèse.
Hypoprotidémie associée à une
Parmi les gammapathies monoclonales: Myélome
hypoalbuminémie <30g/dl
multiple = maladie de Kahler: C’est une
Electrophorèse des protéines sériques : prolifération maligne des plasmocytes.
o Elévation de α 2 globulines, des beta o Sur le plan biologique :
globulines et du fibrinogène
Accélération de la vitesse de
o Diminution des gammaglobulines sédimentation > 100 mm /1ere H ;
L`hyperlipidémie est fréquente : augmentation Protéines totales > 80 g/L voire
de la synthèse des LDL (VLDL transformés par 100 à 120 g/L
la lipase hépatique en LDL) migrant en α2 aussi.
Électrophorèse sérique : pic
Ceci est due à une fuite de l’orosomucoïde
monoclonal
Immunofixation et/ou
immunoélectrophorèse :
augmentation des Ig G +++ ou des
IgA. Très rarement IgD ou IgE.
o Le tableau clinique est dominé par les
douleurs osseuses et l'altération de l'état
général
o Sur le plan radiologique: Lacune osseuse
ou géode dite à l'emporte pièce:
Zone d'ostéolyse arrondie, à
contours nets, sans condensation
périphérique ni réaction
périostée.
Multiples et disséminées sur la
totalité du squelette (crâne /
côtes).
o Groupe des albumines | Albumine
o Les α1 globulines: C’est un groupe hétérogène et on y trouve
α 1 antitrypsine ;
Orosomucoïde ;
AF1 (α 1 foetoprotéine) ;
Antichymotrypsine ;
α 1 lipoprotéine ;
Transcortine, TBG (thyroxin binding globulin).
o Les α2 globulines
L’haptoglobine :
L’α2 Macroglobuline
Céruléoplasmine
o Les β globulines :
β1 globulines
Transferrine | sidérophiline
Ferritine
CRP
β2 globulines :
C3 et C4 du complément
Fibrinogène
o Les gammaglobulines
ÉLECTROPHORÈSE DES PROTÉINES SÉRIQUES:
Séparation des protéines sériques sous l’action d’un champ électrique en
tampon alcalin
Migration de la cathode vers l’anode (+)
Vitesse de migration selon la taille des particules, la force ionique et la
porosité du support.
Les fractions de protéines distribuées de l'anode vers la cathode en
o Groupe des albumines | PA et RBP: Il est le plus anodique à
l'électrophorèse (migre le plus vite)
La pré-albumine (PA)
La RBP
o L'albuminémie chez L'IGF1 est un peptide de 7 500 Da ,
L'albumine: C'est la protéine majeure du plasma l'homme est 5% supérieure synthétisé par Foie (+++), sous le contrôle de
: 55-60 % des protéines totale : à celle chez la femme. la GH , il a une homologie structurale avec la
proinsuline.
C'est une holoprotéine. PM 69 kDa ; Variations physiologiques :
-La sécrétion d'IGF1 peut être modifiée par :
Sa structure est uni peptidique et o Nouveau-né : 30 g/l ; - une insuffisance hépatique,
globulaire ; - une insuffisance rénale,
o Grossesse : diminution d'environ
Son pH isométrique est bas : pHi = 4,7 25% par hémodilution et - la dénutrition,
ce qui explique qu'elle migre stabilisation à la limite inférieure - le diabète sucré
rapidement à l'électrophorèse ; de la normale ; Dans le plasma on dose la Vit D tot
(D2+D3)par chimiluminescence
Sa synthèse est active (10 à 12 g/j), o Sujet âgé après 60 ans: l'angiotensine II est un
principalement au niveau du foie ; diminution à 30-35 g/l. octapeptide actif ( l'angiotensine
Sa 1/2 vie biologique est de 15 à 19 Variations pathologiques : I est un decapeptide inactif )
jours. - apres conversion de l’Ang I
o Représentées uniquement
Rôle : par les hypoalbuminémies - stimule le syst orthosympathique , et stimule
Maintien de la pression oncotique dont les mécanismes sont
o la sécrétion de l’ADH , et la sécrétion des
(Po) du plasma ; génétiques ou acquises.
Les hyperlabuminémies minéraloCTC par le cortex surrénalien
o L'albumine est un transporteur non
spécifique : n’existent pas. Les concentrations sériques de la TSH et de la
La transferrine est, avec l'albumine et la
Bilirubine (protecteur de
préalbumine, l'une des trois protéines T4L présentent une relation inverse log-
la sérumalbumine) ;
négatives de la réaction inflammatoire. Sa linéaire= exponentielle , de sorte que des
Acides gras non
diminution est due à un hypercatabolisme
estérifiés (5% des acides protéique au profit de la synthèse des protéines modifications légères de la T4L entraînent une
gras) positives (CRP, haptoglobine, orosomucoïde).
Hormones ; réponse plus large (amplificatrice) de la TSH
Glucose ;
Endocrinopathies
sérique.
Médicaments ; Cause de l’insuffisance de H : insuffisance de
Calcium.
production, émission retardée baisse des
-Les variations individuelles étroites des valeurs
Valeur normale :
transporteurs, occlusion des Rcp par des Ac
des dosages thyroïdiens (observées dans des
o L'albumine sériques 40-45
Les H à Rcp membranaire : GH, prolactine, FSH,
g/l ; études chez des jumeaux) suggèrent que
adrénaline
chaque individu a un niveau propre de T4L
génétiquement prédéterminé.
- Il s’ensuit que dans les stades débutants d’un corticotrope) ou sd de cushing ectopique IGF1 => comme l’insuline => hypo G
dysfonctionnement thyroïdien, les anomalies (sécrétion paraneoplasique)... GH => hyper G
de la TSH sérique précéderont l’apparition ACTH ⬇si sd de cushing ACTH-indépendant :
d'une T4L anormale, en raison de la réponse tumeurs surrénalienne (bénigne/maligne),
exponentielle de la TSH à des modifications, hyperplasie micronodulaire bilatérale des Acide urique
même subtiles de la T4L, alors que cette surrénales L'hyperuricémie peut être en rapport avec des
dernière reste encore dans les normes de - Le cortisol a 8h n'a aucun intérêt pour le mutations génétiques qui altèrent le
référence d’une population diagnostic d'un hypercorticisme endogène, car fonctionnement de certaines enzymes on cite :
La TSH est + informative que la T4 il y a chevauchement des chiffres normaux et - Fructose 1-P aldolase (intolérance héréditaire
Hypothyroidie néonat : ictère nné tardive, hernie élevés. au fructose)
ombilicale, cri caractéristique Rappel sur le diagnostic biochimique de - G6-phosphatase ( glycogénose de type 1 )
Les HT qui traverse la Barrière materno- l’Acromégalie : - Hypoxanthine phosphoribosyl transférase
fœtale :LT4, Ac Anti TSH, Ac anti TPO (la TSH et L’HGPO constitue le test biochimique « gold (HPRT) : DEFICIT
la T3 ne passe pas ) standard ». - La phosphoribosyl-pyrophosphate synthétase
Sd de cusching : perte du cycle nyctéméral de Elle consiste à administrer 75 g de glucose oral (PRPP synthétase) : HYPERACTIVITE
CTC , Dgt exclue devant une cortisolémie à 8H < chez le patient à jeun, à 9h.
50 apres un test d’inhibition 1-2j Le glucose et la GH sériques sont dosés aux
- le test au Synachtene est réalisé en cas de temps T0, 30, 60, 90, 120 et 150 mn après le
suspicion d'une insuffisance surrénalienne. début de l’épreuve.
- il ne faut pas confondre maladie et sd de Chez les sujets sains, les taux sériques de GH
Cushing baissent jusqu’à devenir indétectables
le dosage de l'ACTH est utile dans le diagnostic (classiquement < 0,2 ng/ml).
étiologique : Chez l’acromégale, la GH sérique est mesurable;
ACTH ⬆si sd de cushing ACTH-dépendant : dans 30% des cas, la GH est paradoxalement
maladie de cushing (adénome hypophysaire augmentée.
- en cas de déficit => test à insuline
Sont souvent Acide => vaux mieux alcaliniser les
urines en cas de présence de cristaux d’AU
L’allopurinol rduit le risque d’hyperurécémie
Au cours de l’acces goutteux l’AU peut etre Nle
L’insuline + la réabsorption proximale =>
↓l’élimination
hyper U Iair II air
Sd de Lesch Nyhan hémopathies, IRA, psoriasis,
(liée au sexe , éthylisme, toxémie gravidique ,
recessif ) HTA, DU thiazidique , ACD , acidose
goutte primitive lactique
idiopathique
hypo AU
- Dans les urines : l'A.U est non ionisé. grossesse, déficit en Xanthine oxydase , défaut en Glut9
Est un puissant antiO2
- Dans le sang : l'A.U est sous forme estérifiée d'un sel, appelé urate, dont le cation peut être le sodium ou
Dans le plasma la forme libre est ++/ peut etre
l'ammonium
liée à l’Alb et β2g
L'urate est 18 fois plus soluble que l ‘acide urique dans un milieu aqueux
Urucolyse intestinale ne se fait pas chez l’homme
Clearence de 8.7+/- 2.5
Il est 100% filtré par le glomérule
Source de l'A.U :
- catabolisme des purines :: adénine, guanine, hypoxanthine et xanthine Transporteurs au niv du rein :
- produit terminal du métabolisme de l'azote (comme l'urée et sécrétion réabsorption
l'ammoniaque).
MPR4, galactine 9, URAT1 , Glut 9 , OAT
- La voie des pentoses phosphate et le catabolisme du fructose peuvent
donner de l'acide urique ABCG2, NPT1 et NPT2
Hyperuricémies est souvent assocée à : Il est actuellement bien admis que l'hypertriglycéridémie est L’acideurique est le produit terminal de Damp
athérogène et que 30 à 40% des sujets hypertriglycéridémiques ont une hyperuricémie. L' Hyperuricémie peut être due à :
Le mécanisme associant ces deux métabolismes n'est pas clair, cependant le risque cardiovasculaire au cours La consommation excessive de purines
de leur association est très fort alimentaires :
Urate monosodique => organisme - Anchois, Sardine, Thon en boite…
Acide urique => urines
- Bœuf, dinde, poulet, les abats…
- Lentilles, pois chiches, haricots... L’allopurinol agit en inhibant la xanthine oxydase
- Thé, cacao, chocolat, bière. Le syndrome de Lesch-Nyhan (SLN) est la forme
la consommation excessive d'aliments riches en la plus sévère du déficit en hypoxanthine-
fructose : guanine phosphoribosyl-transférase (HGPRT),
- Dattes, figues sèches, raisins secs, pommes, miel, une maladie héréditaire du métabolisme des
sodas. purines, et il associe une surproduction en
L’uricolyse a lieu essentiellement au niveau acide urique (SAU) à des troubles neurologiques
=> Equation de la MDRD (Modification du
intestinal. Elle est active sur l’acide urique et comportementaux
régime dans une maladie rénale :pds- / race
déversé dans l’intestin par voie passive, par Les normes :
+ , la + utilisée , meilleur si DFG <60
l’intermédiaire des sécrétions digestives homme : 50 - 60 mg/l
(salivaires, biliaires, pancréatiques et femme : 40 - 52 mg/l
intestinales). enfant : 35 -40 mg/l
Dans des conditions normales, les bactéries
'urate est 18fois plus solubles que l'acide urique
intestinales, pourvues d’uricases, dégradent
en milieu aqueux
totalement l’acide urique en allantoïne, et
même au-delà, en dioxyde de carbone et en Bilan rénale
ammoniac, éliminés ensuite dans les selles ou A une Fct endocrine (calcitriol, EPO, rénine) =>Pour l’enfant il faut utiliser la formule de
consommés pour leur propre métabolisme. Analyse d’aspect , couleur , odeur Schwartz :
Le rôle des bactéries est prouvé par la réduction Phénylcétinurie :odeur de souris
considérable de l’uricolyse à la suite d’ingestion Leucinose : odeur de moisi
d’antibiotiques. 1. Dosage de l’urée :voie d’elimination de
Hypourécémie type 2 est due à :mut SLC2A9 l’azote , produit dans le foie , eliminer par
La maladie de VON GIERKE est due à un déficit l’intestin aussi, en dehors de IRA , urée ↑
de la glucose 6 phosphatase : dans la DSH et ingestion de viande /urée ↓
- Le glucose 6p qui n’a pas pu rejoindre le glucose dans l’IHC ,
est alors métabolisé en acide lactique. 2. Dosage de la créat : creatine ( de l’arginine
- Le glucose 6p accumulé peut se transformer aussi et glycine)créatinine ( produit endogène ,
4. Ionogramme urinaire et sanguin
en ribose5p, qui rejoint le PRPP, catabolisé en acide musculaire, per Créatine phosphatase ,
5. Protéinurie
urique en passant l’IMP et l’hypoxanthine. Une marquer de la filtration glomérulaire )
baisse de la sécrétion urinaire de l’acide urique 3. Calcule du DFG , estimation de la clearance
consécutive à l’accumulation des lactates et des Clairance créatinine (ml/min) =U.V/P
corps cétoniques contribue également à augmenter
l’uricémie. VN : 120 ± 20 ml/min/1.73 m2.
C une produit de dégradation de l’ATP - les formules :
L’age avancée est un FDR => Équation de Cockroft-Gault (C-G)
Les produits laitiers n’ont pas de influence
La probénécide agit en ↓la rébsorpton rénale de
l’AU
si < 1 => IRF
Urée plasmatique/ Créatinine plasmatique : tres
↑=> IRF / Par contre in n’est pas très élevée
dans l’IRC
Nouveaux marqueurs de l’insuffisance rénale
permettant un diagnostic plus précoce, plus
sensible et plus spécifique. C’est le cas de :
• La cystatine C .
• La NGAL .
• L’IL 18 .
• La kidney injury molecule-1 (Kim 1).
• La N-acétyl-D-glucosaminidase .NADG
Insuffisance rénale chronique :> 3mois
Urée , créat ↑, DFG↓ < 60
- dans IRC on retrouve : rein de petite taille, anémie normocytaire normochrome, hyperPh, hypoCa++,
augmentation de la PAL
La formule de Cockrofft ne prend pas en compte
la race
Il existe 3 principaux stimulateurs de la rénine :
l’hyperkaliémie ; l’hyponatrémie ;
Insuffisance rénale aigue : l’hypovolémie
IRF : urée ++, par hypovolémie souvent la rénine est une enzyme sécrétée par une zone
IRO : du rein située près des glomérules et nommée
- intrinsèque : glomérulaire, Vx, tubulaire 85% , interstitielle appareil juxtaglomérulaire.
- post rénale : LR , HBP - La rénine n'a pas d'effets physiologiques directs,
Le sodium urinaire : très ↓ dans l’IRA fct / peu ↓dans l’atteinte chronique mais elle fait partie de ce qu'on appelle le système
Fraction excrétée du sodium FEN RAA dont le rôle est majeur dans le contrôle de la
pression artérielle : elle permet la formation de
Surface corporelle du sujet -----> Clairance mesurée ascendante de l’anse de Henlé, elle a un rôle anti-
l'angiotensine I, elle-même transformée à son tour, du sujet infectieux
grâce à l'enzyme de conversion, en angiotensine II, Si sa surface corporelle était de 1,73m2 ------> - L’uromoduline est synthétisée dans des cellules
une protéine qui a pour effet principal la Clairance corrigée du sujet épithéliales tubulaires épaisses à membres
vasoconstriction, ce qui élève la pression artérielle. l'équation MDRD n’exige pas une correction du ascendants (TAL)
L'angiotensine II active la sécrétion de l'aldostérone DFG retrouvé, elle le calcule directement pour - Des mutations dans le gène UMOD causent des
par les glandes surrénales ; cette hormone, en une surface corporelle de référence de 1,73 m2 maladies rénales
permettant à l'organisme de retenir du chlorure de Chez les patients avec un DFG < 60 - ne passe jamais la barrière vue son PM (en etat
sodium et de l'eau, provoque une augmentation du ml/min/1,73m2, MDRD est plus performante et physio ou patho)
volume sanguin circulant et, par ce biais, de la précise que Cockcroft et Gault Alcaptonurie : accumulation de l’ac
pression artérielle L’urée est synthétisé à partir de l’ammoniac , homogentisique dans le sang et les urines, cet
role du rein : néoglucogenèse , erythropoèse, CO2 et aspartate acide provient du catabolisme de
secrétion des Fc de croissance , synthèse des Le TCP est le siège du catabolisme de ++ prot de l’aa‘’tyrosine’’
PE2 faible PM Seuil de détéction de la protéinurie par BU : 150-
La bilirubine retrouvée dans l’urine est de la La rabsorption du Na au niv du TCP se fait 200 /Faussement positives en cas de
bilirubine conjuguée hydrosoluble librement leucocyturie, urines alcalines, hématies,
La production de la créatinine est l'appareil juxta-glomérulaire est constitué de : médicaments (chlorhexidine), BU immergée
proportionnelle à la masse musculaire, d’où la Artériole glomérulaire afférente trop longtemps), sperme, pus.
difficulté de fixer des valeurs normales./ son Macula densa : Différenciation pariétale du TCD => Faussement négatives en cas de chaînes légères
sécrétion n’est ps influencer par l’alimentation Lacis cellulo-conjonctif : sépare l’artériole et urines diluées.
Les med donnant une IRA pré rénale : glomérulaire afférente de la macula densa Evaluation par : Urines des 24h / ou les Spot
- AINS , IEC , ARAII Les néphrons corticaux sont + nombreux que les (dosage de prot/ alb par rapport à la créat)
La sévérité de l’IRC est estimer par l’estimation juxta médullaire c’est le rapport P/C «protéines/créatinine » ou A/C
du débit de filtration glomérulaire « albumine/créatinine » qui doit être réalisée à
Chez les sujets agé => on utilise la MDRD Protéinurie partir d’un échantillon urinaire pouvant être
Le dosage de la créat : basé sur la R° de jaffé ou La valeur limite habituellement reconnue est de prélevé à tout moment de la journée (celui du
la créat réagit avec l’acide picrique donnant une 150 mg/24 heures (l’albumine ne dépasse pas matin est préférable). C’est le Spot,
coloration orange en milieu alcalin à 520nm les 30 mg parmi ces 150 mg) Et calculé le rapport : Prot / créat =< suivie des
Conditions à respecter pour une bonne Faite de prot avec PM > 69000 Da, proteinurie modérée / Alb / Crat =< néphropathies
réalisation de la clairance : glomérule laisse passer 5g de protéine --puis DT et HTA
- Le sujet doit boire deux litres d’eau, au minimum, 99% sont réabsorbées par les tubules - La confirmation d’une microalbuminurie nécessite
durant la récolte des urines des 24 heures ; 500 mg/24 h chez l’enfant (+ elevée que l’adult) 2 tests positifs sur 3.
- Bien récolter et chiffrer la diurèse des 24 heures ; Les prot qui peuvent passé : => elle peut etre soit :
- Le prélèvement sanguin doit se faire le même jour AlbumineHaptoglobine- Orosomucoide transitoire fièvre , DSH, exercices,
où le prélèvement urinaire est ramené au Transferrine- α1 microglobuline -ß2 IC, convulsion
laboratoire ; microglobuline permanante chaines légères, LR, Tm ,
- Calculer la surface corporelle du sujet à partir de - Tamm-Horsfall. : uromoduline : Cette protéine atteinte glomérulo-
son poids et sa taille. n’est pas filtré, elle est sécrétée par la branche tubulaire
orthostatique sujet jeune, age < 30ans La protéinurie physiologique n’est pas favorisée - on dose au labo la BT , et BC
<2g/j, bénigne , touche par la pression oncotique de la capsule de - sur prélèvement sur tube sec ou hépariné
3-5% , réversible , Bowen - son disage oriente vers l’intensité de l’ictère
n’apparait pas en L’origine : - subi ctère 15-20 / ictère >20/ bilirubine à 180
décubitus - Si le glomérule laisse passer des à 200 mg/l
La microalb : ne veux pas dire atteinte rénale protéines : protéinurie La Blr est photosensible
- d’albumine plus de 30 g/24h => Alarme de glomérulaire ; ↑de la BNC défaut de ↑ de la BC
Microangiopathies conjugaison
QCM : - Si le tubule ne réabsorbe pas les hémolyse ++ BNC ↑BC↓ hépatique
PU < 150 mg/24h et prot / créat <0.2 protéines : protéinurie tubulaire ; BC et BNC ↑ stercobiline obstruction
TCP : prot de bas PM urobiline ↑ ↓ des VB
Les Ig M ne traverse en aucun cas
- Si les deux coexistent : protéinurie stercobiline
La recherche de la protéinurie orthostatique se mixte. ↑
fait de la manière suivante : Les BU sont imprégné d’un chromogène
- Les premières urines du matin sont éliminées ; dans un milieu acide Lait maternelle et novobiocine inhibe l’ UDPGT
- Recueillir les urines durant toute la journée (16 Risue de l’ictère nucléaire par la BC = B libre
heures), en demandant au patient d'avoir une Exploration biochimique de la La PAL est principalement d’origine Osseuse 60%
activité normale. La collecte se poursuivra en fonction hépatique o ↑ chez l’enfant et la femme enceinte à cause de
recueillant les urines juste avant le couché (premier Le bilan hépatique repose Sur l’étude des : (la croissance et le placenta)
échantillon). Au matin recueil des urines de la nuit • Syndrome de cytolyse. o ↑franche de PAL => rétention++
(deuxième échantillon). • Syndrome de cholestase. o ↑ modérée => Kc , Cirrhose, hépatite
- Si la protéinurie est normale => la nuit / et ↑ f la • Syndrome d’insuffisance hépatocellulaire. o Situé au niv des villosité canaliculaire
journée => c une PPO • Syndrome d’induction hépatique o Sont des enz qui catalyse la libération d’un
- elle est réversible Cytolyse : LDH , OCT , et transames phosphate inorganique à partir d’ester
- ALAT = TGP(P héPatique) / ASAT =TGO phosphate en milieu alcalin
- TGP/TGO > 1 : toutes les hépatites sauf γGT ↑ isolément => alcoolisme chronique, Sd
l’hépatites alcoolique. d’induction hépatique (med ++)
- IDM , EP => ↑de TGO o elle est ubiquitaire
Le dosage ne se fait pas seulement sur des o tres ↑ dans : hépatite méd , cholestase , méta
- LDH : 5 isoenz :
Urines de 24H , il peut etre fait sur un Spot
- LDH ↗↗↗ dans les hépatites , les ictères hépatique
La protéinurie ne veut pas dire forcément
hémolytiques, les métastases hépatiques. les Sd d’IHC :
atteinte rénale
intoxications aiguës graves et IDM . - hypo Alb => tardive
La protéine de Tamm-Horsfall est très grosse, ne
- LDH1 => 4H => heart - hypo fac de coagulation => précoce
traverse pas la barrière. Elle n’est pas filtrée
- LDH => 4M => muscle strié et foie - ↓ de l’urée
mais sécrétée plutôt par la branche large
- OCT : Ornithine carbamoyl transférase : Très - ↑ de l’ammoniac
ascendante de l’anse de Henlé.
spécifique du foie mais difficile à doser. - hypo gly et hypo Ch par déficit en LCAT
Cholestase : PAL , Blr , Sels biliaire, - TP↓, Facteur V ↓
5’nucléotidase , γGT, leucine aminopeptidase - Des signes de cholestase : PAL et γGT ↑ .
- Des signes de cytolyse : Transaminases ↑. - peut s’accompagner de fièvre : c'est le cas du - ↑ précoce de la Blr
Sd d’induction hépatique : ↑de la synthèse par paludisme par exemple - au stade terminale : EPP montre une soudure
le syst microsomale : Alcool, rifa , - selles de coloration Nle , pas de prurit β-γ
phénobarbitale, amiodarone - il peut etre chronique Marqueurs tumoraux
- ↗↗ isolé de GGT Lors d'un infarctus du myocarde, l'augmentation
- sans aucun signe de cholestase ou de cytolyse, du taux de LDH débute à la 10e heure, atteint
Fonction de détoxification et transformation des son maximum de la 48e heure à la 72e heure, le
xénobiotiques : retour à la normale s'effectuant en 15 jours.
- produits + polaire et + soluble LDH : 5 types d’isoenzymes separes par
=>Test d’épuration plasmatique: clearence de électrophorèse :
BSP et l’ICG => les deux sont anormaux dans la -LDH-1 (4H) - principalement dans le coeur.
cholestase -LDH-2 (3H1M) - principalement dans le systeme
=>Test de détoxication : Épreuve de L’acide
reticulo-endothelial.
Hippurique (AH), Tests de la
glucuronoconjugaison -LDH-3 (2H2M) - principalement dans les poumons
=>Tests de la fibrose hépatique : -LDH-4 (1H3M) - principalement dans les reins
-Fibrotest : α2 Macroglobuline , bilirubine -LDH-5 (4M) - principalement dans le foie et les
totale, haptoglobine, Apo A1, GGT. muscles stries
-Actitest = fibrotest + ALAT
Le syndrome fonctionnel kupfferien ou
Causes de l’hyperbilirubinémie :
syndrome mésenchymateux ou bien syndrome Bilirubine non-conjuguée (indirecte)
inflammatoire o Augmentation de la production de bilirubine:
• Il est du à une activation du système - Hémolyse
macrophagique (essentiellement) avec production - Erythropoïèse inefficace: destruction des
de cytokines. précurseur eryth dans la MO
• Et d’autre part une hypergammaglobulinémie o Défaut de conjugaison:
- Immaturité hépatique,
polyclonale repérée sur l’électrophorèse des
- Anomalies génétiques (maladie de Gilbert, Crigler
protéines (IgM, IgG, IgA). Najjer)
Bilirubine conjuguée (directe)
L’œuf ne contient pas de purines - Anomalies hépatocellulaires: cirrhose, hépatite,
Sd d’IHC : hypo (Alb , Ch, gly , Orosomucoide) néoplasie
mais ↑ de l’ammoniac - Obstruction mécanique des voies biliaires
Cholestase post hépatique : urobiline est ↓ • Extra hépatique: Lithiase, atrésie biliaire,
Cirrhose , hépatite, occlusion des VB => ictère à néoplasme
Blr mixte • Intra hépatique: Cirrhose
L’ictère hémolytique : La cirrhose :
- c'est un ictère à bilirubine libre (indirecte) - prot plasmatique sont ↓ au stade avancé
ACE GP, superfamilles des Ig , ADK CR ,
PM↑ M : CCR, Kc de sein , ovaire, poumon , CMT
B : TBk , fumeurs, MICI, hépatopathies
AFP GP , homologue à l’Alb ,
production Nle : hépatocytes fœtaux, sac
vitellin, tractus digestif et le rein
↑ dans : CHC , Tm testiculaire, Kc du
pancréas et bronchique
hCG α+β = non covalente
α comme :Lh , FSH , TSH
↑ dans : Kc testiculaire,maladies
trophoblastique, Kc mammaire,
Pulmonaire , gastro intestinale
PSA protéase (kalikréine)
peut etre produite par le sein et les Gld
salivaire/ app précoce dans le Kc de
prostate
PSA libre / PSA tot < 25% => malin
CA125 GP , PM ↑, Kc de l’ovaire
↑M : poumon, endomètre, sein,foie,
pancréas
↑B : pleurésie, péritonite, pancréatite,
cirrhose, IC congestive
CA15-3 PM le + Gd , GP mucineuse , Kc du sein
CA19-9 GP , Kc du pancréas, CCR , et Kc gastrique
NSE isoenz de l’enolase , trouve ↑ dans les
neurones et le cerveau,
↑ : Kc pulmonaire à ptt Cl ,
neuroblastome, Tm neuroendocrines
β2mg faible Pm , CMH 1 ,
↑M : lymphomes, MM, LMC,
↑B :MAI , IRC , rejet de greffe
Critères de light :
Vous aimerez peut-être aussi
- Exploration Du Mtabolisme LipidiqueDocument27 pagesExploration Du Mtabolisme Lipidiquegnomon dayang layePas encore d'évaluation
- Merged 20200614 004637Document4 pagesMerged 20200614 004637yaya camaraPas encore d'évaluation
- Les Hypercholestérolémies Familiales Aspects Génétiques Et AnalytiquesDocument67 pagesLes Hypercholestérolémies Familiales Aspects Génétiques Et AnalytiquesTaha Amine CherrabenPas encore d'évaluation
- Oméga 3 Et Maladies Cardiovasculaires-Etudes CliniquesDocument35 pagesOméga 3 Et Maladies Cardiovasculaires-Etudes Cliniqueslapetiterennaise56Pas encore d'évaluation
- DYSLIPIDEMIESDocument59 pagesDYSLIPIDEMIESCheick SANOUPas encore d'évaluation
- Hyperlipoproteinemie Version Imprimable (Du DR - Abdi)Document3 pagesHyperlipoproteinemie Version Imprimable (Du DR - Abdi)djamil1Pas encore d'évaluation
- Dyslypoprotéinémies - Chapitre Nutrition - BTS 2 EpmsDocument13 pagesDyslypoprotéinémies - Chapitre Nutrition - BTS 2 EpmsClément AdamPas encore d'évaluation
- Item 23 DyslipidemiesDocument22 pagesItem 23 Dyslipidemiessafa HADFIPas encore d'évaluation
- Dyslipidemies Nouvelles Therapeutiques 2006Document30 pagesDyslipidemies Nouvelles Therapeutiques 2006megenniPas encore d'évaluation
- Exploration Du Metabolisme LipidiqueDocument30 pagesExploration Du Metabolisme LipidiqueMohamed AminePas encore d'évaluation
- C6 - Dyslipidémies PowerPointDocument58 pagesC6 - Dyslipidémies PowerPointmalekmeabahPas encore d'évaluation
- Ligne Directrice 2021 - DyslipidémieDocument1 pageLigne Directrice 2021 - Dyslipidémiesara harvey vachonPas encore d'évaluation
- Item-R2c 223 - DyslipidémieDocument6 pagesItem-R2c 223 - DyslipidémieKenza ZahouilyPas encore d'évaluation
- Recos Dyslipidémies 2019 PDFDocument20 pagesRecos Dyslipidémies 2019 PDFSimona IonitaPas encore d'évaluation
- Item 23 Dyslipidemie-Residanat PDFDocument124 pagesItem 23 Dyslipidemie-Residanat PDFSyrine Boughzala0% (1)
- Biochimie3an Cardio-Exploration Lipides Lipoproteines2022semraDocument8 pagesBiochimie3an Cardio-Exploration Lipides Lipoproteines2022semramohamed labedPas encore d'évaluation
- 09 - Lipoprotéines PlasmatiquesDocument4 pages09 - Lipoprotéines PlasmatiquesdrjamaikenzaPas encore d'évaluation
- Dyslipidémie 2020Document41 pagesDyslipidémie 2020Jarraya RahmaPas encore d'évaluation
- Fiche Dyslipidémie - Artérosclérose À PublierDocument6 pagesFiche Dyslipidémie - Artérosclérose À Publierfichesevc100% (1)
- TD N 2 BC Sophie MARYDocument6 pagesTD N 2 BC Sophie MARYandriePas encore d'évaluation
- Metabolisme Des LipoproteinesDocument30 pagesMetabolisme Des LipoproteinesSpike NortonPas encore d'évaluation
- Exploration Du Métabolisme Lipidique-2 PDFDocument13 pagesExploration Du Métabolisme Lipidique-2 PDFahmed djellabPas encore d'évaluation
- 4 - Exploration Des DyslipoprotéinémiesDocument62 pages4 - Exploration Des DyslipoprotéinémiesFairouz Tou100% (1)
- Bilan Lipidique Et Classification Biochimique Des Hyperlipoprotéinémies VIDocument6 pagesBilan Lipidique Et Classification Biochimique Des Hyperlipoprotéinémies VImaxim200025Pas encore d'évaluation
- Dyslipidémieartérosclérose RevisionpaecardioDocument6 pagesDyslipidémieartérosclérose Revisionpaecardiofichesevc100% (1)
- Etude Des Métabolismes Par Modélisation CompartimentaleDocument25 pagesEtude Des Métabolismes Par Modélisation Compartimentalelapetiterennaise56Pas encore d'évaluation
- Fiche Dyslipidémie - ArtéroscléroseDocument6 pagesFiche Dyslipidémie - Artérosclérosefichesevc100% (1)
- Biochimie2an-Exploration Metabolisme LipidesDocument9 pagesBiochimie2an-Exploration Metabolisme Lipidesaya prodigePas encore d'évaluation
- BSIS12-F HDLC P 2012 FRA 2013Document1 pageBSIS12-F HDLC P 2012 FRA 2013Amine AminePas encore d'évaluation
- 2010 Rouen Dubus CoursBiopchimieAn2P2 PDFDocument13 pages2010 Rouen Dubus CoursBiopchimieAn2P2 PDFrahilPas encore d'évaluation
- Troubles Du Métabolisme LipidiqueDocument12 pagesTroubles Du Métabolisme LipidiqueSamir HPas encore d'évaluation
- Explorations Biochimiques Du Métabolisme Des Lipides Lipoproteines Atherogenese OffiDocument7 pagesExplorations Biochimiques Du Métabolisme Des Lipides Lipoproteines Atherogenese Offizouaoui kaoutherPas encore d'évaluation
- DYSLIPIDEMIEDocument4 pagesDYSLIPIDEMIEsara amarPas encore d'évaluation
- Hyperlipoprotéinémies (Dr. Kedad)Document47 pagesHyperlipoprotéinémies (Dr. Kedad)Elixir'sPas encore d'évaluation
- Lipoproteines & Plaque D'atheromeDocument15 pagesLipoproteines & Plaque D'atheromescaren efonaPas encore d'évaluation
- 1.3 - Les Lipides - FicheDocument1 page1.3 - Les Lipides - FicheMarie BrelPas encore d'évaluation
- 05 DyslipidemieDocument41 pages05 Dyslipidemiebasma KhawlaPas encore d'évaluation
- MTB Des LipoproteinesDocument22 pagesMTB Des Lipoproteines130660LYC OMAR BENABDELAZIZ NEDROMA100% (1)
- DyslipoprotéinémiesDocument2 pagesDyslipoprotéinémiesAhmedmahPas encore d'évaluation
- Métabolisme LipidiqueDocument2 pagesMétabolisme LipidiqueAro Manda100% (1)
- Biochimie Clinique 2 - Rouen - 4e Annee PDFDocument24 pagesBiochimie Clinique 2 - Rouen - 4e Annee PDFdeziri mohamedPas encore d'évaluation
- 220 Dyslipidémies - 0Document1 page220 Dyslipidémies - 0Abderraouf Benziane100% (1)
- 220 Dyslipidémies - 0Document1 page220 Dyslipidémies - 0cammganeshPas encore d'évaluation
- Normolipemiants & Antithyroidiens PDFDocument63 pagesNormolipemiants & Antithyroidiens PDFhp pcPas encore d'évaluation
- Etude Du Lactate Déshydrogénase LDHDocument3 pagesEtude Du Lactate Déshydrogénase LDHAmiraBenhammouPas encore d'évaluation
- Item 220 DyslipidémiesDocument6 pagesItem 220 DyslipidémiesDi BenamoPas encore d'évaluation
- 9 HypolipemiantsDocument14 pages9 HypolipemiantsWhat are youPas encore d'évaluation
- Minimal 2017-2018 Physiopath-S2Document36 pagesMinimal 2017-2018 Physiopath-S2karim sabarPas encore d'évaluation
- Taitement Des DyslpipdemiesDocument14 pagesTaitement Des DyslpipdemiesAlberto GeorgePas encore d'évaluation
- LES Dyslipidemies: DR Khlafa MDocument78 pagesLES Dyslipidemies: DR Khlafa MdrsoulyPas encore d'évaluation
- Exploration Du Metabolisme LipidiqueDocument40 pagesExploration Du Metabolisme LipidiqueAbdoulaye sebyPas encore d'évaluation
- Correction 2 TD Diabète 2Document3 pagesCorrection 2 TD Diabète 2Mey StudyPas encore d'évaluation
- Glyc EmieDocument3 pagesGlyc EmiezlimitounePas encore d'évaluation
- Dosage - Du Cholestérol HDL Ldl..Document5 pagesDosage - Du Cholestérol HDL Ldl..noorPas encore d'évaluation
- Beis45-F GPT (Alt) - LQ 2016Document1 pageBeis45-F GPT (Alt) - LQ 2016Riadh BenyoucefPas encore d'évaluation
- Item 220 - DyslipidemieDocument4 pagesItem 220 - DyslipidemieYakoub Hamdi0% (1)
- Fichier Produit 2121Document53 pagesFichier Produit 2121précieuse NgueloloPas encore d'évaluation
- Examens Biologiques en CardiologieDocument10 pagesExamens Biologiques en CardiologienawarPas encore d'évaluation
- Item-R2c 61 (Ex-59) - Classification Des Troubles MentauxDocument3 pagesItem-R2c 61 (Ex-59) - Classification Des Troubles MentauxIsabel VPas encore d'évaluation
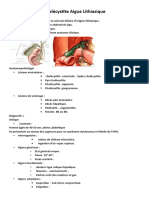
- Cholécystite Aigue LithiasiqueDocument4 pagesCholécystite Aigue Lithiasique68758kbdbmPas encore d'évaluation
- Lisa 118Document8 pagesLisa 118Balosin MarinaPas encore d'évaluation
- Maladies Et PoisonsDocument5 pagesMaladies Et PoisonsZurak Draken BorgPas encore d'évaluation
- PéritonitesDocument16 pagesPéritonitesMohamed BoudouPas encore d'évaluation
- Echos de La MicronutritionDocument8 pagesEchos de La Micronutritionanis100% (1)
- Soins Infirmiers en Ophtalmologie - CompressDocument39 pagesSoins Infirmiers en Ophtalmologie - CompressBadr Abou AliaPas encore d'évaluation
- 2-Psychologie de L'enfantDocument17 pages2-Psychologie de L'enfantMikael Ishak100% (1)
- Gériatrie, Maltraitance & IsolementDocument2 pagesGériatrie, Maltraitance & IsolementMohamed IkbalPas encore d'évaluation
- Master PPRDocument31 pagesMaster PPRAn ĪsPas encore d'évaluation
- Protocole Nat PEC Nutrition - Niger 2016 - VFDocument181 pagesProtocole Nat PEC Nutrition - Niger 2016 - VFAlberto George87% (15)
- 1-Les Schistosomes Et SchistosomosesDocument21 pages1-Les Schistosomes Et SchistosomosesYahia BenaliPas encore d'évaluation
- 5 Calcul de Dose Et Debit Exercices Et CorrigersDocument30 pages5 Calcul de Dose Et Debit Exercices Et CorrigersChristian Ngala100% (2)
- Guide Relais Prévention Combinée Au Pres Des PCDocument83 pagesGuide Relais Prévention Combinée Au Pres Des PCDjibril SyPas encore d'évaluation
- Diarrhées Chroniques - PPTX Cours 2019Document51 pagesDiarrhées Chroniques - PPTX Cours 2019maroua aouadiPas encore d'évaluation
- TD 1-Psycologie CliniqueDocument4 pagesTD 1-Psycologie CliniqueépineusePas encore d'évaluation
- Conduite À Tenir Devant Une ProtéinurieDocument28 pagesConduite À Tenir Devant Une ProtéinurieStu DentPas encore d'évaluation
- Les Echelles D Evaluation en Psychopathologie Depression-AngoisseDocument6 pagesLes Echelles D Evaluation en Psychopathologie Depression-AngoissemcTovar100% (1)
- Correction Devoir de Génétique MoléculaireDocument3 pagesCorrection Devoir de Génétique MoléculairessggnfPas encore d'évaluation
- Prévention Risque Au CimentDocument5 pagesPrévention Risque Au CimentANDRIA TatukiiPas encore d'évaluation
- PR Punga Syllabus Uro Volume 1Document80 pagesPR Punga Syllabus Uro Volume 1Anou KalengaPas encore d'évaluation
- Formation Es TH Ét I QueDocument56 pagesFormation Es TH Ét I QuemakiessPas encore d'évaluation
- Exploration Du Métabolisme Lipidique-2 PDFDocument13 pagesExploration Du Métabolisme Lipidique-2 PDFahmed djellabPas encore d'évaluation
- Adverbe de ModDocument12 pagesAdverbe de ModAlecs ChiriacPas encore d'évaluation
- National Geographic France Hors-S 233 Rie - 09 2018 - 10 2018Document128 pagesNational Geographic France Hors-S 233 Rie - 09 2018 - 10 2018pinocle.pablooPas encore d'évaluation
- Pathologie de L'appareil LocomoteurDocument103 pagesPathologie de L'appareil LocomoteurAïssatou TouréPas encore d'évaluation
- Fractures de L - EnfantDocument34 pagesFractures de L - EnfantGeorgePanaitPas encore d'évaluation
- La Fin DalzheimerDocument34 pagesLa Fin Dalzheimermetoui62100% (1)
- Module Politiques Programmes de SantéDocument40 pagesModule Politiques Programmes de SantétadayePas encore d'évaluation
- HematologieDocument4 pagesHematologiePalemero Naj NordeusPas encore d'évaluation