Académique Documents
Professionnel Documents
Culture Documents
97 765
Transféré par
hizballah27Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
97 765
Transféré par
hizballah27Droits d'auteur :
Formats disponibles
Néphrologie-urologie
125
Déshydratation
et hyperhydratation
cellulaires
et extracellulaires
Étiologie, physiopathologie, diagnostic, traitement
Dr Anne BLANCHARD, Dr Pascal HOUILLIER, Pr Michell PAILLARD
Service d’explorations fonctionnelles et radio-isotopes, CHU Broussais, 75674 Paris cedex 14
Unité INSERM U 356, université Pierre et Marie-Curie, Paris
Points Forts
à comprendre
● ● ● ● ● ● ● ● ● ● ● ● ● ● ● ●
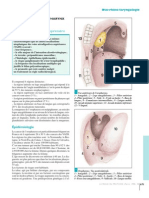
Hyperhydratation et déshydratation intracellulaires
• Les troubles de l’hydratation
extra et (ou) intracellulaire sont
toujours secondaires Conduite à tenir devant une hyponatrémie hypotonique
à la constitution d’un bilan sodé (hyperhydratation intracellulaire)
et (ou) hydrique déséquilibré. L’hyponatrémie hypotonique est définie par une concentration plasmatique de
Ces troubles, rarement liés sodium inférieure à 135 mmol/L associée à une osmolalité plasmatique mesu-
au dépassement des capacités rée inférieure à 280 mOsm/kg d’eau. Elle reflète toujours une hyperhydratation
physiologiques rénales intracellulaire. Cette hyponatrémie associée à une hypo-osmolalité plasmatique
d’adaptation aux variations est expliquée par un contenu en eau relatif supérieur au contenu en sodium, ce
des entrées d’eau et de sodium, dernier pouvant être normal, augmenté ou diminué.
reflètent le plus souvent L’hyponatrémie hypotonique doit être différenciée :
une altération de la fonction – des hyponatrémies isotoniques dans lesquelles l’osmolalité plasmatique est
d’excrétion du rein. Ce défaut normale. Ces « fausses hyponatrémies » sont liées à la présence anormale de
d’adaptation peut être d’origine macromolécules dans le plasma (dans les hyperprotidémies et hyperlipidémies
intrarénale (tubulopathie, majeures essentiellement) qui diminuent le contenu en eau plasmatique. La natré-
diurétiques) ou extrarénale mie est normale si elle est mesurée par litre d’eau plasmatique (par électrode
[déficits ou excès de sécrétion(s) spécifique, comme c’est le cas dans un nombre croissant de laboratoires). Ce
hormonale(s)]. diagnostic ne peut donc être évoqué que lorsque la natrémie est mesurée par litre
• Schématiquement, de plasma (photométrie de flamme) ;
il est pratique de retenir
– des hyponatrémies hypertoniques secondaires à la présence anormale d’un
les correspondances suivantes :
soluté osmotiquement actif autre que le sodium, et à l’origine d’une déshydra-
– trop d’eau : hyperhydratation
tation intracellulaire (cf. chapitre correspondant).
intracellulaire-hyponatrémie;
– pas assez d’eau : 1. Étiologie
déshydratation intracellulaire-
hypernatrémie ; L’apparition d’une hyponatrémie nécessite la constitution d’un bilan d’eau posi-
– pas assez de sodium : tif (entrées transitoirement supérieures aux sorties).
déshydratation extracellulaire- Les diverses causes d’hyponatrémies sont résumées dans le tableau I.
hypovolémie ;
– trop de sodium : 2. Physiopathologie
hyperhydratation • Création de l’hyponatrémie : en l’absence d’une insuffisance rénale avancée
extracellulaire-hypervolémie. (DFG < 20 mL/min) et d’accès de potomanie, l’apparition d’une hyponatrémie
signe généralement une incapacité à supprimer la sécrétion d’ADH malgré la
LA REVUE DU PRATICIEN (Paris) 765
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
TABLEAU I
Étiologie des hyponatrémies
• Apports d’eau en excès, dépassant la capacité normale d’excrétion rénale
– Troubles primaires de la soif : potomanie
– Apports d’eau augmentée avec apports osmotiques faibles : tea and toast
syndrome
• Excrétion rénale insuffisante d’apports d’eau physiologiques
A. Défaut majeur d’excrétion rénale d’eau : insuffisance rénale chronique avancée
(DFG < 20 mL/min)
B. Stimulus volémique de l’ADH :
– déplétion sodée avec hypovolémie
– syndromes œdémateux avec hypovolémie efficace (insuffisance cardiaque,
cirrhose, certains syndromes néphrotiques)
C. SIADH associé à une endocrinopathie :
– hypothyroïdie
– insuffisance glucocorticoïdes
D. SIADH
– Cancers :
. bronchiques
. digestifs (duodénum, pancréas, estomac)
. urologiques (vessie, prostate, uretère)
. autres (thymome, mésothéliome, lymphome, tumeur d’Ewing)
– Affections neurologiques :
. infectieuses (méningites, encéphalites, abcès)
. vasculaires (accident vasculaire cérébral)
. divers : traumatisme crânien, sclérose en plaques, neuropathies et polynévrites
– Affections pulmonaires :
. infectieuses (pneumopathies bactériennes ou virales, tuberculoses, abcès)
. cancers
. divers : ventilation mécanique, pneumothorax
– Reset de l’osmostat
E. Causes médicamenteuses :
– hormones peptidiques : analogues de la vasopressine, ocytocine, somatostatine
– diurétiques : thiazidiques
– psychotropes : phénothiazines, antidépresseurs tricycliques, halopéridol,
Fluoxétine
– antinéoplasiques : vincristine, cyclophosphamide, ifosfamide
– divers : tolbutamide, clofibrate, carbamazépine, morphiniques
diminution de l’osmolalité plasmatique. Cette sécrétion persistante d’ADH peut
être secondaire à un stimulus volémique, s’intégrer dans une endocrinopathie
(insuffisance glucocorticoïde, insuffisance thyroïdienne) ou définir un syndrome
de sécrétion inappropriée d’hormone antidiurétique (SIADH).
• Conséquences de l’hyponatrémie : la diminution de l’osmolalité plasmatique
entraîne un flux d’eau du volume extracellulaire vers les cellules, de manière à
équilibrer les osmolalités intra- et extracellulaires. Du fait que les cellules céré-
brales sont situées dans une boîte crânienne inextensible, le tableau clinique des
hyponatrémies aiguës est dominé par des symptômes neurologiques d’hyper-
tension intracrânienne : céphalées, troubles digestifs (nausées, vomissements),
syndrome confusionnel, coma et crises convulsives, et, à l’extrême, décès du
patient par engagement cérébral. Lorsque cette hyponatrémie se constitue len-
tement, elle est bien tolérée cliniquement. En effet, la diminution progressive de
l’osmolalité plasmatique est équilibrée par une diminution parallèle du contenu
intracellulaire en divers composés : ions (principalement potassium et anions) et
solutés organiques appelés osmolytes (inositol, glutamine, taurine). Cette adap-
tation permet aux cellules de maintenir un volume proche de la normale. La cor-
rection des hyponatrémies chroniques doit être lente pour permettre l’adaptation
766 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
inverse. Une correction trop rapide de la natrémie expose à un risque de déshy-
Répartition de l’eau dratation intracellulaire aiguë, et sa complication neurologique classique : la
de l’organisme myélinolyse centropontine associée cliniquement au syndrome de verrouillage
• L’eau représente entre 55 et 60 % du poids (ou locked-in syndrome : tétraplégie, diplégie faciale, perte de la latéralité du
du corps chez l’homme 45 et 60 % chez la regard, conscience normale). Le décès du patient est également possible.
femme.
• Le secteur intracellulaire représente 2/3 de 3. Diagnostic positif
l’eau totale (40 % du poids du corps).
• Le secteur extracellulaire représente 1/3 de • Diagnostic clinique et biologique : en dehors des signes neurologiques non
l’eau totale (20 % du poids du corps) et se spécifiques décrits précédemment, l’hyperhydratation intracellaire se traduit clas-
subdivise en secteur plasmatique (5 % du siquement par une prise de poids, l’existence de muqueuses humides, d’une
poids du corps) et liquide interstitiel (15 %
du poids du corps).
langue turgescente gardant l’empreinte dentaire.
Les échanges d’eau entre secteur intracellu- Le diagnostic d’une hyperhydratation intracellulaire repose sur la découverte
laire et secteur extracellulaire dépendent d’une hyponatrémie sur un ionogramme qui motive la mesure d’osmolalité plas-
essentiellement de la différence d’osmola- matique qui est diminuée.
lité qui peut s’établir de part et d’autre de la • Le diagnostic étiologique d’une hyponatrémie hypotonique comporte plusieurs
membrane cellulaire, et donc des variations
de la concentration extracellulaire des étapes successives et s’appuie sur l’évaluation de l’état d’hydratation extracel-
osmoles « efficaces » constituées à plus de lulaire, de la fonction rénale, et la mesure de l’osmolalité urinaire (et éventuel-
95 % par l’ion sodium et les anions qui l’ac- lement de la concentration plasmatique d’ADH) contemporaine(s) de l’hypo-
compagnent: natrémie :
osmolalité extracellulaire efficace =
[Na+]p x 2 – reconnaître les hyponatrémies secondaires à des apports dépassant la capacité
Les flux nets d’eau et d’électrolytes qui rénale d’excrétion d’eau :
s’établissent à travers la paroi du capillaire . du fait d’une insuffisance rénale avancée (DFG < 20 mL/min) ;
entre le secteur plasmatique et le secteur . du fait d’une augmentation primitive des apports d’eau (potomanie primaire) :
interstitiel, sont déterminés par 2 forces
opposées : la différence de pression hydro-
l’hyponatrémie s’accompagne d’une osmolalité urinaire appropriée, inférieure
statique « décroît » le long du capillaire, et à 100 mOsm/kg d’eau (150 chez le sujet âgé). La diurèse est élevée. La poto-
induit un flux liquidien du capillaire vers manie vraie (essentiellement rencontrée chez les schizophrènes) conduit à des
l’interstitium qui dilue progressivement les apports d’eau massifs, compulsifs, pouvant dépasser 15 L/24 h voire plusieurs
protides plasmatiques ; la différence de pres- litres sur un bref intervalle de temps dans quelques formes psychotiques graves.
sion oncotique induit un flux de sens opposé.
Elle s’accentue le long du capillaire avec la Elle expose à des accidents hyponatrémiques aigus pouvant entraîner la mort ;
diminution de la concentration protidique . le plus souvent, l’apparition d’une hyponatrémie est favorisée par la conjonc-
intracapillaire. Le flux net dirigé vers l’in- tion de plusieurs facteurs : une soif conservée ou augmentée (parfois d’origine
terstitium au début du capillaire, s’inverse organique), une altération modérée de la capacité rénale de dilution et des apports
au-delà du pojnt d’équilibre de filtration.
NB : La concentration d’albumine, élément osmotiques faibles qui limitent la diurèse maximale possible : par exemple, si
important des échanges entre secteur plas- l’osmolalité urinaire minimale atteinte est égale à 80 mOsm/kg d’eau, la diurèse
matique et interstitiel, constitue une part maximale sera de 10 L/24 h ; si les apports osmotiques sont de 800 mOsm/24 h,
négligeable des osmoles extracellulaires de 5 L/24 h si les apports osmotiques sont de 400 mOsm/24 h, de 2,5 L/24 h si
(moins de 1 mOsm/kg d’eau pour 40 g/L).
Elle n’intervient donc pas dans les échanges
les apports osmotiques sont de 200 mOsm/24 h. L’hyponatrémie du tea and toast
entre secteurs intra- et extracellulaires. syndrome est observée chez les personnes âgées et (ou) anorexiques qui ont un
régime très hypoprotidique et se nourrissent de tartines et de boissons chaudes
(tisanes ou thé). L’apport hydrique modérément élevé (3 à 4 L/j) ne peut pas être
excrété du fait des faibles apports osmotiques par cette alimentation pauvre en
sel et en protides ;
– reconnaître les hyponatrémies avec osmolalité urinaire inappropriée à l’hypo-
osmolalité plasmatique (supérieure à 150 mOsm/kg d’eau), en rapport avec un
stimulus volémique de l’ADH :
. du fait d’une hypovolémie efficace : l’examen clinique doit rechercher un syn-
drome œdémateux et l’existence d’épanchements séreux pouvant orienter vers
une insuffisance cardiaque congestive, un syndrome néphrotique ou une décom-
pensation cirrhotique. Dans ces syndromes, la pathogénie de l’hyponatrémie est
complexe, intriquant à des degrés divers une sécrétion d’ADH stimulée par l’hy-
povolémie efficace, et un maintien ou une stimulation de la soif ;
. du fait d’une hypovolémie vraie : il est parfois difficile de diagnostiquer, recon-
naître cliniquement une déshydratation extracellulaire à l’origine d’un stimulus
volémique de l’ADH. La réalisation d’une charge sodée permet de retenir ce dia-
gnostic lorsque la correction de la volémie entraîne la correction de la natrémie.
À l’inverse, lorsqu’une natriurèse supérieure à 80 mmol/24 h est obtenue, et que
l’osmolalité urinaire demeure inappropriée (> 100 mOsm/kg d’eau) à l’hypo-
natrémie qui persiste, le diagnostic d’hyponatrémie par stimulus volémique de
l’ADH peut être écarté ;
LA REVUE DU PRATICIEN (Paris) 767
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
– reconnaître les causes endocriniennes d’hyponatrémie : insuffisance surrénale
Régulation du bilan (par un test à l’ACTH), hypothyroïdie (par un dosage de TSH) ;
de l’eau – avant d’aboutir au diagnostic d’exclusion qu’est le syndrome de sécrétion inap-
Le bilan de l’eau est maintenu équilibré proprié d’ADH (SIADH) dont les étiologies sont résumées dans le tableau I.
grâce à une double régulation portant sur les Dans ce cadre, il est classique de distinguer un tableau clinique très particulier
entrées (modification de la soif) et l’excré-
tion rénale d’eau sous le contrôle de l’hor- nommé « reset de l’osmostat ». Ce dernier se définit par l’apparition d’une hypo-
mone antidiurétique (ADH). La valeur régu- natrémie stable, modérée, associée à une sécrétion d’ADH inappropriée. Cette
lée est l’osmolalité plasmatique dont les sécrétion d’ADH est freinable lorsqu’une hyponatrémie plus profonde est induite
variations déterminent les flux d’eau entre par une charge aqueuse et stimulable par la restriction hydrique. Cette patholo-
secteurs intra- et extracellulaires et donc le
volume cellulaire.
gie est donc caractérisée par un décalage de la relation reliant la natrémie à la
En situation physiologique, le stimulus sécrétion d’ADH vers des natrémies plus basses. Les patients atteints de ce syn-
essentiel de la sécrétion d’ADH et de la soif drome doivent être identifiés car l’hyponatrémie qu’ils présentent ne peut pas
est l’osmolalité plasmatique : très faible (la natrémie retournant inéluctablement à sa valeur d’équilibre) et ne doit pas
lorsque l’osmolalité plasmatique est < 280 être traitée.
mOsm/kg d’eau, la sécrétion d’ADH
s’élève, au-delà de ce seuil, proportionnel-
lement à l’élévation de l’osmolalité plasma- 4. Traitement
tique. En l’absence d’ADH, l’osmolalité du Le degré d’hyponatrémie est corrélé à la fois à l’importance des apports d’eau
fluide tubulaire, très basse à la fin du seg-
ment de dilution (qui comprend la branche et au degré d’altération de la capacité rénale à excréter cette eau, l’apparition
large de Henle et le tube contourné distal), d’une hyponatrémie signant obligatoirement un bilan d’eau positif relativement
est maintenue jusqu’à l’urine définitive. La au bilan de sodium.
fixation de l’ADH à son récepteur V2 induit Les bases thérapeutiques de l’hyponatrémie sont la restriction hydrique seule,
l’insertion d’une aquaporine dans la mem-
brane cellulaire apicale du tube collecteur l’administration de chlorure de sodium dans le but de corriger une hypovolémie
rénal. Cette protéine confère à l’épithélium vraie responsable d’un stimulus volémique de la sécrétion d’ADH, ou encore
une perméabilité à l’eau importante. Une une restriction hydrosodée. Le choix de la thérapeutique dépend essentiellement
équilibration osmotique avec l’interstititum de la pathologie d’origine :
hypertonique conduit à la concentration pro-
gressive des urines dont témoigne l’éléva- • une restriction hydrique associée à une restriction sodée est indiquée chez
tion de l’osmolalité urinaire. les patients présentant un syndrome œdémateux. On y adjoindra si possible le
Un sujet qui a un apport hydrique de 2 L/24 h traitement de sa cause : insuffisance cardiaque congestive, syndrome néphro-
et un apport osmotique de 800 mOsm/24 h a tique ;
une osmolalité urinaire moyenne de 400
mOsm/kg. Lorsqu’une charge aqueuse pro-
• l’administration de chlorure de sodium par voie orale ou par perfusion isoto-
longée (10 L/24 h) est administrée, le rein éli- nique permet de corriger les hyponatrémies secondaires aux hypovolémies vraies,
mine transitoirement une quantité d’eau infé- quelle qu’en soit l’origine ;
rieure aux entrées, l’osmolalité plasmatique • une restriction hydrique isolée est indiquée chez les patients potomanes ou
diminue, le volume intracellulaire tend à aug-
menter. La diminution de l’osmolalité plas-
atteints de SIADH. Dans ce cas, du fait du phénomène d’échappement rénal, un
matique inhibe la sécrétion d’ADH. L’osmo- apport hydrique modéré et fixe est toléré ;
lalité urinaire atteint progressivement une • les hyponatrémies apparaissant au cours des insuffisances thyroïdiennes ou
valeur minimale (80 mOsm/kg d’eau) qui glucocorticoïdes se corrigent avec l’instauration d’une opothérapie substitutive.
définit le pouvoir de dilution, tandis que la
diurèse devient égale aux apports d’eau. Si Les hyponatrémies chroniques doivent être corrigées lentement. Si l’existence
une restriction hydrique prolongée est ensuite de symptômes témoigne du caractère aigu d’une hyponatrémie, il convient de
instituée, le rein élimine transitoirement une corriger relativement rapidement la natrémie jusqu’à ce que le patient soit asymp-
quantité d’eau supérieure aux entrées, l’os- tomatique puis plus lentement : l’élévation de la natrémie conseillée est de 1,5
molalité plasmatique s’élève et le volume
intracellulaire tend à diminuer. L’élévation de
à 2 mmol/h sans dépasser 2,5 mmol/h, 15-20 mmol/24 h. L’administration de
l’osmolalité plasmatique stimule la sécrétion chlorure de sodium en solution hypertonique (513 mmol/L) associée aux diuré-
d’ADH. L’osmolalité urinaire augmente pro- tiques de l’anse est alors généralement utilisée, ajustée de sorte à maintenir un
gressivement pour atteindre, lorsque la natré- bilan sodé nul et un bilan hydrique négatif.
mie est O 145 mmol/L, une valeur maximale
(entre 850 et 1 200 mOsm/kg d’eau) qui défi-
Les hyponatrémies aiguës avec augmentation du volume extracellulaire peuvent
nit le pouvoir de concentration. La diurèse est bénéficier d’une épuration extrarénale, en raison du risque de surcharge extra-
alors inférieure à 0,75 L/24 h. cellulaire induit par la solution hypertonique de chlorure de sodium.
L’osmolalité urinaire maximale (la diurèse
minimale) est normalement atteinte lorsque
l’osmolalité plasmatique devient supérieure Conduite à tenir devant une déshydratation intracellulaire
ou égale à 300 mOsm/kg d’eau, valeur qui Les déshydratations intracellulaires sont toujours secondaires à une élévation de
correspond au seuil physiologique de la soif l’osmolalité efficace plasmatique. Elles s’accompagnent généralement d’une
intense. Ainsi, la régulation des entrées
d’eau dans l’organisme par la stimulation du hypernatrémie, définie par une concentration plasmatique de sodium supérieure
centre hypothalamique de la soif prend le à 145 mmol/L. La natrémie peut cependant diminuer lorsque l’hyperosmolalité
relais de l’adaptation rénale d’excrétion plasmatique est secondaire à la présence anormale en concentration élevée d’un
d’eau en cas de déshydratation intracellu- soluté autre que le sodium, de bas poids moléculaire et osmotiquement actif. Ce
laire importante.
.../... soluté est responsable d’un « trou osmotique », défini par la différence entre l’os-
molalité mesurée et calculée. Ce soluté peut être d’origine endogène (glucose
768 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
au cours de la décompensation diabétique) ou exogène (mannitol, glycocolle,
.../... éthylène glycol).
En physiopathologie, les stimulus non osmo-
tiques, essentiellement la baisse de volémie Ces états hyperosmolaires avec hypertonicité plasmatique doivent être distin-
artérielle, prennent une importance primor- gués des états hyperosmolaires sans hypertonicité plasmatique liés à la présence
diale : en cas de diminution de plus de 10 % plasmatique en concentration élevée d’un soluté de bas poids moléculaire mais
de la volémie efficace, la neurosécrétion osmotiquement inactif car librement diffusible dans les cellules : principalement
hypothalamique d’ADH est stimulée par des
afférences provenant des barorécepteurs l’urée ou l’éthanol. Dans ces états hyperosmolaires, le « trou osmotique » est
carotidiens et volorécepteurs atriaux. Elle augmenté mais la tonicité plasmatique, et donc le volume intracellulaire, sont
induit une sécrétion d’ADH inappropriée à normaux.
l’hyponatrémie qu’elle entraîne.
1. Causes
• Déshydratations intracellulaires avec hypernatrémie : elles sont le plus sou-
vent liées à l’existence de pertes rénales d’eau non compensées, plus rarement,
à l’administration ou l’ingestion accidentelle d’une solution hypertonique de
chlorure de sodium. Les pertes d’eau pouvant favoriser l’apparition d’une hyper-
natrémie sont multiples et peuvent être divisées en 3 catégories : l’augmentation
des pertes insensibles par la respiration et la sueur (favorisées par l’hyperventi-
lation et l’hyperthermie), les pertes rénales (diabètes insipides centraux ou
néphrogéniques, diurèses osmotiques) et gastro-intestinales.
• Hyponatrémies hypertoniques : le soluté responsable du trou osmotique peut
être d’origine endogène : la situation clinique la plus fréquente d’hyponatrémie
hypertonique est la décompensation diabétique. Plus rarement, le soluté est d’ori-
gine exogène au décours des intoxications par mannitol, glycocolle, éthylène
glycol.
2. Physiopathologie
• Création de l’hyperosmolalité extracellulaire : l’apparition d’une hyperna-
trémie est généralement due à la constitution d’un bilan d’eau négatif (entrées
transitoirement inférieures aux sorties). Physiologiquement, toute augmentation
de l’excrétion rénale d’eau (ou apparition de pertes extrarénales) entraîne une
stimulation de la soif qui suffit, par l’adaptation des entrées d’eau, à maintenir
la natrémie dans les limites de la normale. Ainsi, la plupart des patients atteints
de diabète insipide neuro- ou néphrogénique adaptent leur prise de boisson à
leur diurèse et régulent leur natrémie. L’apparition d’une hypernatrémie signe
donc soit un défaut d’accès à l’eau (vieillards, enfants, ou patients ne pouvant
ni boire d’eux-mêmes, ni exprimer leur soif), soit plus rarement un défaut pri-
mitif de la sensation de soif associé. Ce défaut de la soif doit faire rechercher,
par tomodensitométrie ou imagerie par résonance magnétique (IRM), une lésion
hypothalamique du centre de la soif (tumeur, anomalies vasculaires essentielle-
ment).
Au cours de la décompensation diabétique, l’élévation de la concentration extra-
cellulaire de glucose non diffusible entraîne un flux d’eau de la cellule vers le
liquide extracellulaire et donc une déshydratation intracellulaire associée à une
hyponatrémie. Secondairement, l’élévation de la concentration plasmatique de
glucose est tellement importante que la charge filtrée de glucose dépasse la capa-
cité de réabsorption rénale. Ce glucose non réabsorbé entraîne avec lui de l’eau
par un mécanisme de diurèse osmotique. Cette perte d’eau entraîne l’élévation
progressive de la natrémie, jusqu’à l’apparition d’une hypernatrémie.
• Conséquences de l’hyperosmolalité extracellulaire : l’élévation de l’osmola-
lité plasmatique entraîne un flux d’eau des cellules vers le liquide extracellu-
laire. L’hypernatrémie aiguë induit des symptômes neurologiques de gravité
variable (léthargie, perte de connaissance, coma) pouvant aller jusqu’au décès
du patient. Lorsqu’elle se constitue lentement, l’élévation de l’osmolalité plas-
matique est équilibrée par une augmentation du contenu en osmolytes intracel-
luaires qui permet de réguler le volume cellulaire au cours des hypernatrémies
chroniques. Cette adaptation expose à un risque d’hyperhydratation intracellu-
laire aiguë (potentiellement mortelle) en cas de correction trop rapide de l’hy-
pernatrémie.
LA REVUE DU PRATICIEN (Paris) 769
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
3. Diagnostic
Le diagnostic étiologique d’une hypernatrémie commence par un interrogatoire
soigneux du patient et de l’entourage à la recherche notamment d’antécédents
évocateurs (diabète sucré) de la prise ou de l’administration récente de solution
hypertonique ou de médicaments apportant une grande quantité d’osmoles (par
exemple, apports sodés massifs au cours de certaines antibiothérapies), d’un
contexte infectieux, d’épisodes diarrhéiques et de vomissements.
La diurèse doit être grossièrement quantifiée, ainsi que la sensation de soif, la
capacité à l’exprimer et à la satisfaire.
Une diabète sucré décompensé doit systématiquement être recherché par la
mesure de la glycémie et d’une glycosurie à la bandelette, puis par dosage de
laboratoire.
La mesure de l’osmolalité urinaire contemporaine de l’osmolalité plasmatique
supérieure à 300 mOsm/kg permet de juger du caractère adapté ou non de la
réponse rénale à l’hypernatrémie : l’hypernatrémie doit normalement entraîner
une hypersécrétion d’ADH et l’élévation de l’osmolalité urinaire. Schémati-
quement, une osmolalité urinaire supérieure ou égale à 850 mOsm/kg témoigne
d’une réponse rénale normale à une sécrétion d’ADH appropriée. À l’inverse,
lorsque l’osmolalité urinaire contemporaine d’une hypernatrémie est inférieure
à 300 mOsm/kg, il existe une anomalie majeure soit de la sécrétion, soit de la
réponse rénale à l’action de l’ADH.
Grâce à divers éléments on pourra :
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique, secon-
daires à des pertes d’eau pure ou très pauvre en sodium :
– par apport d’eau insuffisant pour compenser les pertes extrarénales normales
(osmolalité urinaire appropriée) :
. sujets ayant des troubles de conscience ou ne pouvant exprimer leur soif (sujets
déments, nourrissons),
. trouble primaire de la soif : l’absence de sensation de soif contemporaine d’une
osmolalité plasmatique supérieure à 300 mOsm/kg chez un individu pouvant
l’exprimer doit faire rechercher une lésion hypothalamique du centre de la soif.
Les troubles primitifs de la soif sont fréquemment associés à un diabète insipide
neurogénique partiel ;
– au cours de la polyurie des diabètes insipides : l’osmolalité urinaire contem-
poraine de l’hypernatrémie est inappropriée. L’administration par voie sous-cuta-
née ou nasale de dDAVP (agoniste des récepteurs V2 de l’ADH) permet de dis-
tinguer entre :
. un diabète insipide d’origine neurogénique (défaut de sécrétion hypothalamique
d’ADH) lorsque l’osmolalité s’élève de plus de 50 % dans les 2 h qui suivent
l’administration de dDAVP ;
. un diabète insipide d’origine néphrogénique (absence de réponse rénale à l’ac-
tion de cette hormone) lorsque l’osmolalité urinaire varie de moins de 30 % en
cas d’origine néphrogénique ;
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique secon-
daires à des pertes d’eau pure avec perte relativement plus faible de sodium :
– au cours des polyuries osmotiques, des substances de faible poids moléculaire
librement filtrées et peu réabsorbées entraînent la disparition du gradient cor-
tico-papillaire intrarénale. L’osmolalité urinaire est proche de celle du plasma
mais la concentration en électrolyte est beaucoup plus faible. La perte d’eau et
de sodium ainsi engendrée entraîne une déshydratation globale. Le soluté res-
ponsable peut être le glucose (la glycosurie élevée du diabète déséquilibré est la
première étiologie de polyurie osmotique), l’urée (polyurie osmotique de la
réduction néphronique avancée), le mannitol… ;
– au cours des pertes extrarénales (osmolalité urinaire appropriée) :
. pertes par vomissements, aspiration gastrique, diarrhée non compensées ;
. pertes extrarénales autres, augmentées par l’hyperventilation et l’hyperthermie ;
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique, secon-
daires à une surcharge en solutés non diffusibles (osmolalité urinaire appro-
priée) :
770 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
. la surcharge aiguë accidentelle en sodium : le plus fréquemment par apport
Hyperhydratation excessif de bicarbonate molaire au cours d’un arrêt cardiorespiratoire ou d’une
et deshydratation hyperkaliémie, entraîne un état d’hyperhydratation globale,
extracellulaires . hyperglycémie aiguë, principalement à la phase aiguë initiale de la décom-
pensation diabétique, avant apparition de la diurèse osmotique.
Aspects physiopathologiques
• Syndromes œdémateux : la formation d’œ- 4. Traitement
dèmes généralisés nécessite une altération
d’une ou de plusieurs forces de l’équilibre • Hypertonicité plasmatique secondaire à des pertes d’eau pures ± pertes de
de Starling qui régit les échanges périphé- sodium : comme pour l’hyponatrémie, la correction de l’hypernatrémie, lors-
riques entre secteurs plasmatique et inter- qu’elle est chronique et bien tolérée, doit être effectuée lentement, par adminis-
stitiel, l’équilibre étant déplacé en faveur
d’une augmentation nette de la filtration. Les
tration d’eau. Une hypernatrémie aiguë et symptomatique est corrigée plus rapi-
œdèmes sont le plus souvent dus à une aug- dement par l’administration orale d’une plus grande quantité d’eau ou en ajoutant
mentation de la pression hydrostatique capil- une perfusion intraveineuse de solution glucosée hypotonique à 2,5 %. Il est
laire (secondaires à une élévation de la pres- conseillé, en dehors de situations exceptionnelles, de ne pas diminuer la natré-
sion veineuse essentiellement, ou à une mie de plus de 1 mmol/h et 15 mmol/j. La voie orale est toujours privilégiée. Un
vasodilatation artériolaire), plus rarement à
une diminution de pression oncotique plas- apport de sodium et de potassium est effectué en fonction du degré de déshy-
matique (insuffisance hépatique, syndrome dratation extracellulaire qui est pratiquement constamment associé, et de la déplé-
néphrotique, entéropathies exsudatives) ou tion potassique.
une élévation de la pression oncotique inter- Le déficit hydrique peut être estimé grossièrement à partir du poids corporel du
stitielle (hypothyroïdie). La constitution
d’œdèmes suppose également une rétention sujet à l’état stable (PDC) et de la natrémie mesurée ([Na]p), par la formule sui-
majeure et prolongée de sodium par le rein, vante :
soit parce que le rein est anormal et ne déficit hydrique = 0,60 x PDC x (([Na]p/140)-l)
répond plus à l’expansion (œdèmes primi- • Le traitement de la décompensation diabétique associe la réhydratation extra-
tifs) soit parce que l’expansion s’associe à
une hypovolémie efficace. Les mécanismes et intracellulaire à l’administration d’insuline et de glucose.
compensateurs de cette hypovolémie effi- • La correction des hypernatrémies aiguës, en particulier celles secondaires à
cace sont à l’origine et soutiennent la réten- l’administration accidentelle de sodium ou s’accompagnant d’une insuffisance
tion sodée par un rein par ailleurs normal rénale, peut être assurée par hémodialyse.
(œdèmes secondaires).
• Œdèmes primitifs :
– la glomérulonéphrite est l’exemple type
des œdèmes primitifs : dans les syndromes Hyperhydratation
néphritiques, la rétention rénale primitive
provoque un bilan positif de sodium et d’eau
et déshydratation extracellulaires
(la natriurèse très faible est inférieure aux
apports habituels, oligurie) secondairement
responsable d’une expansion extracellulaire Conduite à tenir
vasculaire (responsable d’une élévation du devant une hyperhydratation extracellulaire
débit cardiaque et d’une HTA) et intersti-
tielle. La rénine et l’aldostérone plasma- Le volume extracellulaire est déterminé par le contenu (et non la concentration)
tiques, l’activité sympathique sont dimi- en sodium extracellulaire. L’hyperhydratation extracellulaire est toujours secon-
nuées. Le mécanisme de la rétention sodée daire à un bilan sodé positif (entrées supérieures aux sorties) qui s’accompagne
est mal connu. Dans la majorité des cas, il d’une rétention rapide d’eau du fait de la régulation de la natrémie (l’osmolalité
n’existe pas de syndrome néphrotique, l’al-
buminémie étant supérieure à 30 g/L, la pro- plasmatique) maintenue constante par l’ADH (cf. encadré régulation du bilan
téinurie inférieure à 3 g/24 h ; de sodium, page 773).
– la déplétion sélective en potassium pro-
voque une augmentation de la réabsorption 1. Causes
tubulaire proximale de sodium responsable
d’une expansion du volume extracellulaire. Les états d’hyperhydratation extracellulaire sont répertoriées dans le tableau II.
Des syndromes œdémateux ont été décrits Ils peuvent être subdivisés, si on écarte la situation particulière de l’insuffisance
au cours de déplétions potassiques sévères rénale avancée, en 2 catégories :
(supérieures à 500 mmol).
• Œdèmes secondaires : l’anomalie primitive – les hyperminéralocorticismes primitifs dont l’hyperaldostéronisme primaire
est une diminution de la volémie efficace qui est la principale cause, s’expriment cliniquement par une hypertension artérielle.
peut être définie par la volémie effectivement L’hyperhydratation extracellulaire est trop limitée pour entraîner un syndrome
présente dans le lit artériel. La stimulation œdémateux du fait du phénomène d’échappement du rein à l’hypersécrétion d’al-
des mécanismes régulateurs (dont témoigne
l’élévation de la rénine et de l’aldostérone
dostérone ;
plasmatique) met en jeu les barorécepteurs à – les causes de rétentions hydrosodées majeures qui entraînent l’apparition d’œ-
haute pression et entraîne un bilan cumula- dèmes généralisés.
tif de sodium responsable de l’expansion,
mais incapable de restaurer la volémie arté- 2. Physiopathologie (cf. encadré)
rielle. Selon l’origine, la diminution de la
volémie artérielle est associée ou non à une Hyperminéralocorticismes primitifs et tableaux assimilés : l’excès de minéralo-
diminution du volume vasculaire ; corticoïdes circulants, par leur action sur le tube collecteur cortical, induisent
.../...
une rétention rénale de sodium. Dans 90 % des cas, le stéroïde responsable est
LA REVUE DU PRATICIEN (Paris) 771
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
TABLEAU II
.../...
– dans l’insuffisance cardiaque chronique
congestive, la diminution de la volémie arté- Causes des hyperhydratations extracellulaires
rielle est secondaire à la diminution du
volume d’éjection systolique et du débit car- • Expansion du secteur extracellulaire sans œdèmes
diaque ;
– dans les insuffisances cardiaques à débit
Régulation du bilan du sodium
élevé (anémie, fistules artérioveineuses, A. Syndromes d’hyperminéralocorticorticismes primitifs ou apparentés :
béribéri) la diminution de la volémie arté- – syndrome de Conn
rielle est secondaire à la diminution des – hyperplasie bilatérale des surrénales (hyperplasies nodulaires, déficits
résistances artérielles périphériques, et en 11β-hydroxylase, 17 α-hydroxylase)
contraste avec l’élévation du débit cardiaque – intoxication par la glycyrrhizine (réglisse, Antésite)
et du volume sanguin total, caractéristique – pseudohyperaldostéronisme (syndrome de Liddle)
de ces pathologies ; – excès de glucocorticoïdes
– l’hypovolémie artérielle au cours de la cir- B. Insuffisance rénale avancée
rhose hépatique répond de plusieurs méca-
nismes : au stade précoce de la cirrhose • États œdémateux généralisés
expérimentale, l’hyperpression intrahépa-
tique, par l’intermédiaire de barorécepteurs Régulation du bilan du sodium
intrahépatiques, semble responsable de la A. Augmentation de la pression hydrostatique capillaire :
rétention rénale de sodium (réflexe hépato- – cirrhose hépatique
rénal). La diminution des résistances péri- – insuffisance cardiaque congestive
phériques induite par la vasodilatation – néphropathies glomérulaires
splanchnique et apparition d’angiomes stel- – toxémie gravidique
laires cutanés et viscéraux et diverses fis-
tules artérioveineuses, explique l’hypovolé- B. Augmentation de la perméabilité capillaire :
mie artérielle et le débit cardiaque élevé – choc anaphylactique, septique, œdème angio-neurotique familial
contemporains. Ce syndrome hyperkiné- – médicaments vasodilatateurs (minoxidil, inhibiteurs calciques)
tique participe à la création et à l’entretien C. Augmentation de la différence de pression oncotique:
de la rétention hydrosodée. La rétention – diminution de la pression oncotique plasmatique (albuminémie < 15-20 g/L)
hydrosodée se distribue de façon préféren-
. syndrome néphrotique sévère
tielle dans le péritoine à partir des capillaires
sinusoïdaux et à travers la capsule hépatique. . insuffisance hépatique
Rapidement, l’augmentation du retour lym- . gastro-entéropathies exsudatives
phatique vers la circulation systémique est – augmentation de la pression oncotique interstitielle : hypothyroïdie
dépassée et une ascite apparaît. Lorsque la D. Mécanisme indéterminé : œdèmes cycliques idiopathiques
rétention hydrosodée est majeure, un syn-
drome œdémateux généralisé s’installe ;
– au cours des syndromes néphrotiques, défi-
nis par l’association d’une protéinurie supé-
rieure à 3 g/24 h, d’une hypoalbuminémie l’aldostérone. Dans l’intoxication par la réglisse, la rénine et l’aldostérone sont
(30 < g/L) et d’un syndrome œdémateux. La diminuées. La réglisse inhibe la 11β-hydroxystéroïde-déshydrogénase qui cata-
rétention hydrosodée est induite par une aug- lyse le cortisol en cortisone dans le rein. L’inhibition de cette enzyme démasque
mentation primitive de la réabsorption tubu- l’action minéralocorticoïde du cortisol qui est physiologiquement absente.
laire de NaCl (tubule collecteur) et par les
mécanismes régulateurs de l’hypovolémie
efficace secondaire à la diminution de la 3. Diagnostic
pression oncotique. Une diminution isolée • Diagnostic clinique et paraclinique : il cherche à déterminer l’extension et les
de la pression oncotique ne semble cepen-
dant pas pouvoir entraîner à elle seule une
conséquences de la rétention hydrosodée :
hypovolémie efficace tant que l’albuminé- – la pression artérielle est plutôt basse dans l’insuffisance cardiaque et la cir-
mie demeure supérieure à 20 g/L. En effet, rhose, et élevée dans les hyperminéralocorticismes primitifs ;
l’hypoalbuminémie plasmatique s’accom- – la prise de poids, surtout si elle est rapide, amène une donnée quantifiable et
pagne d’une diminution proportionnelle de précoce, le syndrome œdémateux n’apparaissant cliniquement qu’au-délà de
la concentration interstitielle d’albumine ce
qui maintient la différence de pression onco- 3 kg, les épanchements sérieux au-delà de 6 kg. Dans les syndromes œdémateux
tique constante. majeurs, la prise de poids peut être massive (parfois > 30 kg en quelques
En réalité, la pathogénie semble un conti- semaines) ;
nuum entre des tableaux proches de la glo- – la recherche d’œdèmes au cours d’une rétention hydrosodée modérée se fera
mérulonéphrite aiguë associant un volume
plasmatique élevé, une activité rénine et une
au niveau des membres inférieurs (jambes en poteaux) chez un sujet ambula-
aldostéronémie basses, et des tableaux avec toire, et au niveau des zones déclives chez un sujet couché (empâtement lom-
hypovolémie vraie prédominante, associés à baire, de la face postérieure des cuisses, rétrotibial). Ces œdèmes blancs, mous,
une activité rénine et sympathique et à une indolores, gardent l’empreinte du doigt à la pression (signe du godet) ;
aldostéronémie élevées. La diminution de la – la recherche clinique d’une anasarque (extension aux séreuses) sera aidée par
pression oncotique, éventuellement d’autres
mécanismes non élucidés (anomalies de la la pratique orientée de radiographies (épanchements pleuraux, œdème pulmo-
perméabilité capillaire) seraient à l’origine naire interstitiel) et d’échographies (recherche d’ascite, d’un épanchement péri-
d’une hypovolémie et de sa persistance mal- cardique).
gré la rétention hydrosodée. • Diagnostic biologique : l’hyperhydratation extracellulaire s’accompagne d’une
diminution des protides et de l’hématocrite. Cependant, une hypoprotidémie
772 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
majeure doit faire rechercher une cause particulière, notamment un syndrome
Régulation du bilan néphrotique et une cirrhose.
du sodium Dans les syndromes œdémateux, la natrémie est normale lorsque l’hyperhydra-
Le volume extracellulaire est déterminé par le tation est restreinte au secteur extracellulaire. Une hyponatrémie signe l’exis-
contenu (et non la concentration) en sodium tence d’une hyperhydratation intracellulaire associée, le plus souvent liée à une
extracellulaire. En effet, une augmentation du
contenu en sodium induite par un déséquilibre sécrétion d’ADH entraînée par l’hypovolémie efficace.
du bilan sodé (entrées supérieures aux sorties) Les hyperminéralocorticismes primitifs se traduisent par une hypertension arté-
s’accompagne d’une rétention proportionnelle rielle, une légère hypernatrémie, une hypokaliémie et une alcalose métabolique.
d’eau car la natrémie (l’osmolalité plasma- Les dosages de rénine et d’aldostérone plasmatiques en position couché et débout,
tique) est maintenue constante par la sécrétion
d’ADH. Ainsi, chez un sujet sain, une aug- de la cortisolémie à 8 h et 16 h, d’aldostérone et de cortisol dans le recueil des
mentation du contenu en sodium de 140 mmol urines de 24 h motivés par une HTA, associés à des arguments cliniques et (ou)
s’accompagne nécessairement d’une aug- biologiques et (ou) par une HTA sévère résistante à un traitement bien conduit
mentation du volume extracellulaire de 1 L et permettent d’établir le diagnostic d’hyperminéralocorticisme et d’orienter les
d’une prise de 1 kg.
La valeur régulée est la volémie efficace, para-
examens complémentaires nécessaires au diagnostic étiologique.
mètre non mesurable qui peut être défini Dans les états œdémateux, la natriurèse est généralement effondrée, reflétant la
comme la part de la volémie qui participe effec- rétention sodée rénale (une natriurèse peut cependant être maintenue sous trai-
tivement à la perfusion tissulaire. Cette volé- tement diurétique). À l’inverse, au cours des hyperminéralocorticismes primtifs,
mie efficace représente normalement 15 % de
la volémie, soit la fraction de volume sanguin
il existe un phénomène d’échappement du fait de l’hypertension artérielle, et la
située dans le système artériel. Elle est un déter- natriurèse est rapidement égale aux apports. Cet échappement explique l’absence
minant majeur de la pression artérielle. Bien de syndrome œdémateux dans les hyperminéralocorticismes primitifs.
que l’hypovolémie efficace varie normalement
parallèlement aux volumes plasmatique total
et extracellulaire, elle peut être indépendante 4. Traitement
de ces volumes : une hypovolémie efficace
peut résulter d’une diminution primitive du • Le traitement des syndromes œdémateux repose sur le traitement étiologique
débit cardiaque ou des résistances vasculaires lorsque celui-ci est possible, et le traitement symptomatique du syndrome œdé-
périphériques. L’hypovolémie efficace est mateux :
alors à l’origine d’une stimulation des sytèmes
hormonaux capables d’induire une rétention
– la restriction sodée et hydrique constitue l’élément essentiel du traitement
hydrosodée, et donc un état de rétention hydro- puisque, pour entraîner le bilan négatif d’eau et de sodium souhaité, il convient
sodée avec syndrome œdémateux. de restreindre au maximum les apports ;
Une diminution de volémie efficace entraîne – le repos au lit avec surélévation des membres inférieurs aide à la résorption
l’activation des systèmes rénine-angiotensine-
aldostérone et sympathique qui stimulent la
locale des œdèmes et surtout diminue le tonus des systèmes sympathique et
réabsorption rénale de sodium : rénine-aldostérone et la sécrétion d’ADH, favorisant ainsi l’excrétion rénale
– la stimulation des volorécepteurs veineux ou d’eau et de sodium ;
atriaux, et des barorécepteurs artériels sen- – le plus souvent, l’utilisation de diurétiques est indispensable pour obtenir la
sibles aux variations de pression, active le sys-
tème sympathique. cette activation sympa-
résorption des œdèmes ; le furosémide (Lasilix) est le traitement d’attaque de
thique contribue directement à la rétention choix des syndromes œdémateux majeurs. Utilisé à la dose de 40 à 160 mg/j
rénale de sodium ; (puis 20 à 60 mg/j en dose d’entretien) lorsque la fonction rénale est préservée,
– la libération de rénine est provoquée par des il reste actif au cours de l’insuffisance rénale à condition d’augmenter la poso-
stimulus systémiques (activation du système logie. Il expose au risque d’hypokaliémie qu’il convient de prévenir par une sup-
sympathique) ou intrarénaux (activation des
barorécepteurs de l’appareil juxtaglomérulaire, plémentation potassique.
diminution du débit de chlore dans le fluide Lorsque les œdèmes sont induits par un hyperaldostéronisme secondaire (cir-
tubulaire délivré à la macula densa). La rénine rhose) on utilisera un diurétique épargneur du potassium tels que l’amiloride, le
entraîne la production locale et systémique
d’angiotensine II. L’angiotensine II systémique
triamtérène, ou la spironolactone disponibles sous différentes formes pharma-
stimule la libération surrénalienne d’aldosté- cologiques, seuls ou en association. Ces traitements sont contre-indiqués en cas
rone. Ces deux hormones, par leurs effets tubu- d’insuffisance rénale en raison du risque d’hyperkaliémie ;
laires (augmentation de la réabsorption de • Le traitement des hyperminéralocorticismes repose sur:
NaCl du tube proximal pour l’angiotensine II,
du tube collecteur pour l’adostérone) et glo- – le traitement étiologique : arrêt de la prise de réglisse, traitement chirurgical
mérulaires (baisse du DFG) entraînent une d’une tumeur surrénalienne, traitement substitutif au cours des blocs enzyma-
rétention sodée rénale. tiques… ;
Une augmentation de volémie efficace induite – le traitement symptomatique de l’hyperminéralocorticisme fera appel à des
par exemple par une perfusion aiguë de sodium
va entraîner la production d’hormones natriu- diurétiques épargneurs de potassium comme l’amiloride ou le triamtérène, ou à
rétiques : le facteur atrial natriurétique (ANF) un analogue inactif de l’aldostérone : la spironolactone.
est produit par les oreillettes cardiaques sous
l’effet d’une élévation de la tension pariétale.
L’ANF induit une augmentation du débit de Conduite à tenir
filtration glomérulaire et diminue la réabsorp-
tion tubulaire (essentiellement au niveau du
devant une déshydratation extracellulaire
canal collecteur). Par ailleurs, l’ANF inhibe la
synthèse de rénine et d’aldostérone.
L’apparition d’une déshydratation extracellulaire nécessite la constitution d’un
bilan sodé négatif (entrées transitoirement inférieures aux sorties).
LA REVUE DU PRATICIEN (Paris) 773
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
TABLEAU III
Causes principales des états
de déshydratation extracellulaire
Pertes extrarénales de sodium
A. Gastro-intestinales :
– diarrhée
– fistules ou drainages biliaires, pancréatiques, intestinaux
B. Cutanées :
– sueurs excessives (mucoviscidose)
– brûlures, affections cutanées inflammatoires
C. Création d’un « troisième secteur » :
– occlusion intestinale, péritonite
– pancréatite
D. Autres : ponctions péritonéales ou pleurales
Pertes rénales de sodium
A. Rein normal :
– vomissements, fistules ou aspirations gastriques
– diurétiques, diurèse osmotique
– déficit en minéralocorticoïdes
– hypercalcémie, acidose métabolique
B. Rein pathologique :
– insuffisance rénale chronique (retard à l’adaptation lors de la réduction brutale
des apports sodés)
– insuffisance rénale chronique avec syndrome d’hyporéninémie et hypoaldosté-
ronisme
– néphropathie avec perte de sel : néphropathies interstitielles, acidose tubulaire
distale et proimale
– syndrome de levée d’obstacle, reprise de diurèse d’insuffisance rénale aiguë
– pseudo-hypoaldostéronisme
1. Étiologie
Les causes des déshydratations extracellulaires peuvent être subdivisées en pertes
rénales et extrarénales de sodium, elles sont résumées dans le tableau III.
2. Physiopathologie
Les capacités d’adaptation rénales à un régime pauvre en sodium sont très impor-
tantes (la natriurèse pouvant être quasi nulle). L’apparition d’un bilan sodé néga-
tif suppose donc, soit la perte de sécrétions extrarénales riches en sodium, soit
une altération primitive des capacités rénales de réabsorption du sodium.
• Pertes extrarénales :
– lors des diarrhées ou lors de pertes de liquide de sécrétions intestinales, biliaires
ou pancréatiques : par fistules ou drainages, la perte de bicarbonate de sodium
et de chlorure de sodium aboutit à la création d’une contraction des volumes
extracellulaires et d’une acidose métabolique. On peut en rapprocher les séques-
trations liquidiennes non extériorisées, et donc difficiles à quantifier, qui peu-
vent survenir au cours d’occlusions intestinales, péritonites ou pancréatites. Dans
toutes ces situations, l’apparition d’une hypovolémie entraîne une réponse rénale
appropriée (natriurèse < 10 mmol/L ou par 24 h) ;
– la perte (par vomissement, fistule ou aspiration) de liquide gastrique, riche en
acide chlorhydrique : elle entraîne une alcalose métabolique. Initialement, cette
alcalose induit une perte rénale de sodium, car la quantité de bicarbonate de sodium
filtrée dépasse les capacités tubulaires de réabsorption aboutissant à une perte
rénale de bicarbonate de sodium. Cette alcalose entraîne également une hypoka-
liémie (par transfert intracellulaire et par stimulation de l’excrétion rénale de
potassium). À l’arrêt des vomissements, la concentration de bicarbonate s’équi-
774 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
libre à une valeur permettant sa totale réabsorption par le rein. La natriurèse s’ef-
fondre (< 10 mmol/24 h). La chlorurie très faible signe la déplétion chlorée ;
– pertes sudorales : la sueur contient 50 à 80 mmol/L de NaCl. Une perte notable
de sodium par sudation peut se produire dans certaines circonstances comme
l’exposition brutale à des températures élevées ou l’exercice physique intense.
Lorsqu’un sujet est exposé chroniquement à la chaleur, la concentration en NaCl
s’adapte et diminue. Cependant, les patients atteints d’insuffisance surrénale
chronique ou de mucoviscidose ont des concentrations de sodium dans la sueur
plus élevées que la normale et un défaut d’adaptation à la chaleur.
• Pertes rénales : d’une façon générale, deux phases peuvent être distinguées
lors de pertes de sodium d’origine rénale : lors de l’installation du trouble, l’ex-
crétion urinaire de sodium est supérieure aux apports, à l’origine d’un bilan néga-
tif de sodium et de la création de la contraction des volumes extracellulaires.
Secondairement, la charge sodée filtrée diminue du fait de cette contraction et
les systèmes de régulation stimulent les capacités de réabsorption sodée dans les
différentes parties du néphron encore fonctionnelles. Progressivement, la natriu-
rèse devient égale aux apports, mais demeure inappropriée à la déshydratation
extracellulaire, et un état stable s’instaure.
– L’administration de diurétiques entraîne une perte rénale de sodium et expose
à divers troubles hydroélectrolytiques associés, fonctions du site d’action de diu-
rétique : l’abus des diurétiques de l’anse (type furosémide) et les diurétiques thia-
zidiques qui inhibent la réabsorption dans le tube contourné distal entraînent une
contraction des volumes cellulaires associée à une alcalose métabolique et à une
hypokaliémie. À l’inverse, l’abus de diurétiques agissant sur le tube collecteur
cortical (amiloride, spironolactone, triamtérène) ou leur utilisation malgré l’exis-
tence d’une réduction néphronique entraîne une contraction des volumes cellu-
laires associée à une acidose métabolique et à une hyperkaliémie.
– Les diurèses osmotiques abordées dans le chapitre des déshydratations intra-
cellulaires, entraînent une perte d’eau supérieure à celle de sodium. La contrac-
tion extracellulaire est alors accompagnée d’une déshydratation intracellulaire.
– Déficits en aldostérone : la diminution de la réabsorption de sodium dans le
tube collecteur cortical, entraîne une contraction du volume extracellulaire asso-
ciée à une acidose métabolique et à une hyperkaliémie. Le déficit en aldostérone
peut être d’origine surrénalienne (insuffisance surrénalienne globale, bloc enzy-
matique aboutissant à un déficit spécifique en minéralocorticoïdes), ou secon-
daire à un déficit en rénine associé à certaines insuffisances rénales (syndrome
d’hyporéninémie et hypoaldostéronisme au cours de la néphropathie diabétique,
de la néphropathie aux antalgiques et AINS par exemple). Rarement, la rénine
et l’aldostérone sont très élevées, mais ni l’aldostérone endogène ni l’adminis-
tration de minéralocorticoïde n’entraînent l’effet rénal attendu. Cette pathologie
rare de l’enfance est décrite sous le nom de pseudo-hypoaldostéronisme.
– L’hypercalcémie et l’acidose métabolique diminuent la réabsorption tubulaire
de sodium et peuvent être responsables d’une contraction des volumes extra-
cellulaires.
3. Diagnostic
• Examen clinique : la déshydratation extracellulaire modérée peut s’accompa-
gner de sensations vertigineuses, majorées par l’orthostatisme. Cliniquement,
une perte de poids modérée, la diminution du tonus des globes oculaires, un pli
cutané, un aplatissement des veines périphériques et jugulaires en position cou-
chée devront être recherchés, ainsi qu’une exagération de la réponse à l’ortho-
statisme (lors du passage de la position couchée à la position debout, la fréquence
cardiaque s’élève de plus de 20 batt/min et les pressions artérielles diastolique
et systolique baissent de plus de 20 mmHg). Ces signes indicatifs sont cepen-
dant inconstants et non spécifiques. Une contraction sévère des volumes extra-
cellulaires entraîne une stimulation du système sympathique traduite clinique-
ment par une tachycardie (pouls filant) une vasoconstriction périphérique
(marbures, extrémités froides).
LA REVUE DU PRATICIEN (Paris) 775
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
Points Forts • Examens biologiques : plusieurs modifications biologiques peuvent témoigner
de la contraction : élévation de la protidémie et de l’hématocrite, apparition d’une
à retenir insuffisance rénale fonctionnelle (élévation de l’urée plasmatique proportion-
● ● ● ● ● ● ● ● ● ● ● ● ● ● ● ●
nellement supérieure à celle de la créatininémie), hyperuricémie provoquée par
• Les volumes intra- l’augmentation de la réabsorption de l’acide urique.
et extracellulaires sont maintenus Le dosage de rénine et d’aldostérone plasmatiques dans certains cas permet de
dans les limites physiologiques diagnostiquer un état d’hyperaldostéronisme secondaire, témoin d’une contrac-
grâce à l’ajustement tion volémique parfois modérée et infraclinique, ou de poser le diagnostic d’hy-
permanent, indépendant poaldostéronisme primaire (rénine élevée, aldostérone basse) ou secondaire
et coordonné des sorties d’eau (rénine et aldostérone basses).
et de sodium aux entrées. Cette L’analyse de l’ionogramme urinaire (sur les urines de 24 h ou à défaut sur échan-
double régulation (volume tillon) oriente vers le mécanisme : la natriurèse est généralement inférieure
intracellulaire/volume à 10 mmol/L lorsque la perte sodée est extrarénale (sauf dans les vomissements
extracellulaire) met en jeu à la phase initiale) et supérieure ou égale aux apports, et inappropriée lorsque la
des valeurs régulées (osmolalité perte est d’origine rénale. Dans cette dernière circonstance, la natriurèse devient
plasmatique contre volémie appropriée si la cause s’arrête brutalement : ainsi, à l’arrêt d’un traitement diu-
efficace), des récepteurs rétique, il existe une période transitoire au cours de laquelle la contraction per-
(osmorécepteurs/barorécepteurs siste, mais la natriurèse est appropriée (< 10 mmol/L), malgré l’origine initiale-
carotidiens et de l’artère rénale ment rénale de la perte sodée.
afférente-volorécepteurs La recherche de diurétiques dans les urines à jeun ou sur le recueil de 24 h est
atriaux) et des systèmes de indispensable si la cause de la contraction n’est pas claire, et qu’une prise cachée
régulation hormonaux ou non de diurétiques est envisageable.
hormonaux différents (hormone
antidiurétique – soif contre axe 4. Traitement
rénine angiotensine- Le traitement d’une déshydratation extracellulaire commence si possible par le
catécholamine, facteur atrial traitement étiologique et la correction des facteurs aggravants : traitement de la
natriurétique) permettant (des) cause(s) d’une diarrhée ou de vomissements, arrêt des traitements diuré-
la régulation de l’excrétion tiques, arrêt d’un régime pauvre en sel, correction d’une hypercalcémie…
rénale de l’eau et du sodium. L’arrêt de la perte de sodium permet d’éviter l’aggravation de la contraction. La
• Les troubles de l’hydratation, correction de la volémie suppose alors la constitution d’un bilan positif égal au
rarement liés au dépassement bilan sodé négatif responsable de la contraction. Cette correction doit être favo-
des capacités physiologiques risée par une supplémentation sodée orale.
rénales d’adaptation aux Lorsqu’il existe des signes hémodynamiques préoccupants (marbrures, extré-
variations des entrées d’eau mités froides, pouls filant, hypotension artérielle) il faut avoir recours à l’admi-
et de sodium, reflètent le plus nistration intraveineuse de succédanés de plasma (Plasmagel, Plasmion) qui vont
souvent une altération permettre de restituer une volémie efficace suffisante pour rétablir la perfusion
des fonctions d’excrétion du rein. tissulaire périphérique. L’utilisation de ces solutés doit rester limitée et laisser
• Le caractère adapté place, dès que les signes hémodynamiques s’améliorent, à une réhydratation par
de la réponse rénale à une perfusion de solution de NaCl isotonique (9 ‰). ■
modification du bilan de l’eau
est jugé sur l’osmolalité
urinaire (< 150 mOsm/kg
en charge aqueuse aiguë,
et > 800 mOsm/kg en restriction POUR EN SAVOIR PLUS
hydrique prolongée). Offenstadt G, Maury E. États hyperosmolaires. In : Offenstadt G, Brunette MG
(eds). Désordres acido-basiques et hydroélectrolytiques. Coll. Réanimation, eds
• La réponse rénale Blackwell, 1996 : 90-105.
à une variation de la volémie
Rose BD, Rennke HG. Régulation du bilan de l’eau et du sodium. In : Physiopa-
efficace est jugée sur la natriurèse thologie des affections rénales et des désordres hydroélectriques. Collection l’Es-
(< 10 mmol/24 h en déplétion sentiel, éditions Pradel, 1995 : 32-74.
sodée, natriurèse égale aux Désordres du bilan de l’eau. Ibid, 74-107.
apports en charge sodée aiguë).
776 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
inverse. Une correction trop rapide de la natrémie expose à un risque de déshy-
Répartition de l’eau dratation intracellulaire aiguë, et sa complication neurologique classique : la
de l’organisme myélinolyse centropontine associée cliniquement au syndrome de verrouillage
• L’eau représente entre 55 et 60 % du poids (ou locked-in syndrome : tétraplégie, diplégie faciale, perte de la latéralité du
du corps chez l’homme 45 et 60 % chez la regard, conscience normale). Le décès du patient est également possible.
femme.
• Le secteur intracellulaire représente 2/3 de 3. Diagnostic positif
l’eau totale (40 % du poids du corps).
• Le secteur extracellulaire représente 1/3 de • Diagnostic clinique et biologique : en dehors des signes neurologiques non
l’eau totale (20 % du poids du corps) et se spécifiques décrits précédemment, l’hyperhydratation intracellaire se traduit clas-
subdivise en secteur plasmatique (5 % du siquement par une prise de poids, l’existence de muqueuses humides, d’une
poids du corps) et liquide interstitiel (15 %
du poids du corps).
langue turgescente gardant l’empreinte dentaire.
Les échanges d’eau entre secteur intracellu- Le diagnostic d’une hyperhydratation intracellulaire repose sur la découverte
laire et secteur extracellulaire dépendent d’une hyponatrémie sur un ionogramme qui motive la mesure d’osmolalité plas-
essentiellement de la différence d’osmola- matique qui est diminuée.
lité qui peut s’établir de part et d’autre de la • Le diagnostic étiologique d’une hyponatrémie hypotonique comporte plusieurs
membrane cellulaire, et donc des variations
de la concentration extracellulaire des étapes successives et s’appuie sur l’évaluation de l’état d’hydratation extracel-
osmoles « efficaces » constituées à plus de lulaire, de la fonction rénale, et la mesure de l’osmolalité urinaire (et éventuel-
95 % par l’ion sodium et les anions qui l’ac- lement de la concentration plasmatique d’ADH) contemporaine(s) de l’hypo-
compagnent: natrémie :
osmolalité extracellulaire efficace =
[Na+]p x 2 – reconnaître les hyponatrémies secondaires à des apports dépassant la capacité
Les flux nets d’eau et d’électrolytes qui rénale d’excrétion d’eau :
s’établissent à travers la paroi du capillaire . du fait d’une insuffisance rénale avancée (DFG < 20 mL/min) ;
entre le secteur plasmatique et le secteur . du fait d’une augmentation primitive des apports d’eau (potomanie primaire) :
interstitiel, sont déterminés par 2 forces
opposées : la différence de pression hydro-
l’hyponatrémie s’accompagne d’une osmolalité urinaire appropriée, inférieure
statique « décroît » le long du capillaire, et à 100 mOsm/kg d’eau (150 chez le sujet âgé). La diurèse est élevée. La poto-
induit un flux liquidien du capillaire vers manie vraie (essentiellement rencontrée chez les schizophrènes) conduit à des
l’interstitium qui dilue progressivement les apports d’eau massifs, compulsifs, pouvant dépasser 15 L/24 h voire plusieurs
protides plasmatiques ; la différence de pres- litres sur un bref intervalle de temps dans quelques formes psychotiques graves.
sion oncotique induit un flux de sens opposé.
Elle s’accentue le long du capillaire avec la Elle expose à des accidents hyponatrémiques aigus pouvant entraîner la mort ;
diminution de la concentration protidique . le plus souvent, l’apparition d’une hyponatrémie est favorisée par la conjonc-
intracapillaire. Le flux net dirigé vers l’in- tion de plusieurs facteurs : une soif conservée ou augmentée (parfois d’origine
terstitium au début du capillaire, s’inverse organique), une altération modérée de la capacité rénale de dilution et des apports
au-delà du pojnt d’équilibre de filtration.
NB : La concentration d’albumine, élément osmotiques faibles qui limitent la diurèse maximale possible : par exemple, si
important des échanges entre secteur plas- l’osmolalité urinaire minimale atteinte est égale à 80 mOsm/kg d’eau, la diurèse
matique et interstitiel, constitue une part maximale sera de 10 L/24 h ; si les apports osmotiques sont de 800 mOsm/24 h,
négligeable des osmoles extracellulaires de 5 L/24 h si les apports osmotiques sont de 400 mOsm/24 h, de 2,5 L/24 h si
(moins de 1 mOsm/kg d’eau pour 40 g/L).
Elle n’intervient donc pas dans les échanges
les apports osmotiques sont de 200 mOsm/24 h. L’hyponatrémie du tea and toast
entre secteurs intra- et extracellulaires. syndrome est observée chez les personnes âgées et (ou) anorexiques qui ont un
régime très hypoprotidique et se nourrissent de tartines et de boissons chaudes
(tisanes ou thé). L’apport hydrique modérément élevé (3 à 4 L/j) ne peut pas être
excrété du fait des faibles apports osmotiques par cette alimentation pauvre en
sel et en protides ;
– reconnaître les hyponatrémies avec osmolalité urinaire inappropriée à l’hypo-
osmolalité plasmatique (supérieure à 150 mOsm/kg d’eau), en rapport avec un
stimulus volémique de l’ADH :
. du fait d’une hypovolémie efficace : l’examen clinique doit rechercher un syn-
drome œdémateux et l’existence d’épanchements séreux pouvant orienter vers
une insuffisance cardiaque congestive, un syndrome néphrotique ou une décom-
pensation cirrhotique. Dans ces syndromes, la pathogénie de l’hyponatrémie est
complexe, intriquant à des degrés divers une sécrétion d’ADH stimulée par l’hy-
povolémie efficace, et un maintien ou une stimulation de la soif ;
. du fait d’une hypovolémie vraie : il est parfois difficile de diagnostiquer, recon-
naître cliniquement une déshydratation extracellulaire à l’origine d’un stimulus
volémique de l’ADH. La réalisation d’une charge sodée permet de retenir ce dia-
gnostic lorsque la correction de la volémie entraîne la correction de la natrémie.
À l’inverse, lorsqu’une natriurèse supérieure à 80 mmol/24 h est obtenue, et que
l’osmolalité urinaire demeure inappropriée (> 100 mOsm/kg d’eau) à l’hypo-
natrémie qui persiste, le diagnostic d’hyponatrémie par stimulus volémique de
l’ADH peut être écarté ;
LA REVUE DU PRATICIEN (Paris) 767
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
– reconnaître les causes endocriniennes d’hyponatrémie : insuffisance surrénale
Régulation du bilan (par un test à l’ACTH), hypothyroïdie (par un dosage de TSH) ;
de l’eau – avant d’aboutir au diagnostic d’exclusion qu’est le syndrome de sécrétion inap-
Le bilan de l’eau est maintenu équilibré proprié d’ADH (SIADH) dont les étiologies sont résumées dans le tableau I.
grâce à une double régulation portant sur les Dans ce cadre, il est classique de distinguer un tableau clinique très particulier
entrées (modification de la soif) et l’excré-
tion rénale d’eau sous le contrôle de l’hor- nommé « reset de l’osmostat ». Ce dernier se définit par l’apparition d’une hypo-
mone antidiurétique (ADH). La valeur régu- natrémie stable, modérée, associée à une sécrétion d’ADH inappropriée. Cette
lée est l’osmolalité plasmatique dont les sécrétion d’ADH est freinable lorsqu’une hyponatrémie plus profonde est induite
variations déterminent les flux d’eau entre par une charge aqueuse et stimulable par la restriction hydrique. Cette patholo-
secteurs intra- et extracellulaires et donc le
volume cellulaire.
gie est donc caractérisée par un décalage de la relation reliant la natrémie à la
En situation physiologique, le stimulus sécrétion d’ADH vers des natrémies plus basses. Les patients atteints de ce syn-
essentiel de la sécrétion d’ADH et de la soif drome doivent être identifiés car l’hyponatrémie qu’ils présentent ne peut pas
est l’osmolalité plasmatique : très faible (la natrémie retournant inéluctablement à sa valeur d’équilibre) et ne doit pas
lorsque l’osmolalité plasmatique est < 280 être traitée.
mOsm/kg d’eau, la sécrétion d’ADH
s’élève, au-delà de ce seuil, proportionnel-
lement à l’élévation de l’osmolalité plasma- 4. Traitement
tique. En l’absence d’ADH, l’osmolalité du Le degré d’hyponatrémie est corrélé à la fois à l’importance des apports d’eau
fluide tubulaire, très basse à la fin du seg-
ment de dilution (qui comprend la branche et au degré d’altération de la capacité rénale à excréter cette eau, l’apparition
large de Henle et le tube contourné distal), d’une hyponatrémie signant obligatoirement un bilan d’eau positif relativement
est maintenue jusqu’à l’urine définitive. La au bilan de sodium.
fixation de l’ADH à son récepteur V2 induit Les bases thérapeutiques de l’hyponatrémie sont la restriction hydrique seule,
l’insertion d’une aquaporine dans la mem-
brane cellulaire apicale du tube collecteur l’administration de chlorure de sodium dans le but de corriger une hypovolémie
rénal. Cette protéine confère à l’épithélium vraie responsable d’un stimulus volémique de la sécrétion d’ADH, ou encore
une perméabilité à l’eau importante. Une une restriction hydrosodée. Le choix de la thérapeutique dépend essentiellement
équilibration osmotique avec l’interstititum de la pathologie d’origine :
hypertonique conduit à la concentration pro-
gressive des urines dont témoigne l’éléva- • une restriction hydrique associée à une restriction sodée est indiquée chez
tion de l’osmolalité urinaire. les patients présentant un syndrome œdémateux. On y adjoindra si possible le
Un sujet qui a un apport hydrique de 2 L/24 h traitement de sa cause : insuffisance cardiaque congestive, syndrome néphro-
et un apport osmotique de 800 mOsm/24 h a tique ;
une osmolalité urinaire moyenne de 400
mOsm/kg. Lorsqu’une charge aqueuse pro-
• l’administration de chlorure de sodium par voie orale ou par perfusion isoto-
longée (10 L/24 h) est administrée, le rein éli- nique permet de corriger les hyponatrémies secondaires aux hypovolémies vraies,
mine transitoirement une quantité d’eau infé- quelle qu’en soit l’origine ;
rieure aux entrées, l’osmolalité plasmatique • une restriction hydrique isolée est indiquée chez les patients potomanes ou
diminue, le volume intracellulaire tend à aug-
menter. La diminution de l’osmolalité plas-
atteints de SIADH. Dans ce cas, du fait du phénomène d’échappement rénal, un
matique inhibe la sécrétion d’ADH. L’osmo- apport hydrique modéré et fixe est toléré ;
lalité urinaire atteint progressivement une • les hyponatrémies apparaissant au cours des insuffisances thyroïdiennes ou
valeur minimale (80 mOsm/kg d’eau) qui glucocorticoïdes se corrigent avec l’instauration d’une opothérapie substitutive.
définit le pouvoir de dilution, tandis que la
diurèse devient égale aux apports d’eau. Si Les hyponatrémies chroniques doivent être corrigées lentement. Si l’existence
une restriction hydrique prolongée est ensuite de symptômes témoigne du caractère aigu d’une hyponatrémie, il convient de
instituée, le rein élimine transitoirement une corriger relativement rapidement la natrémie jusqu’à ce que le patient soit asymp-
quantité d’eau supérieure aux entrées, l’os- tomatique puis plus lentement : l’élévation de la natrémie conseillée est de 1,5
molalité plasmatique s’élève et le volume
intracellulaire tend à diminuer. L’élévation de
à 2 mmol/h sans dépasser 2,5 mmol/h, 15-20 mmol/24 h. L’administration de
l’osmolalité plasmatique stimule la sécrétion chlorure de sodium en solution hypertonique (513 mmol/L) associée aux diuré-
d’ADH. L’osmolalité urinaire augmente pro- tiques de l’anse est alors généralement utilisée, ajustée de sorte à maintenir un
gressivement pour atteindre, lorsque la natré- bilan sodé nul et un bilan hydrique négatif.
mie est O 145 mmol/L, une valeur maximale
(entre 850 et 1 200 mOsm/kg d’eau) qui défi-
Les hyponatrémies aiguës avec augmentation du volume extracellulaire peuvent
nit le pouvoir de concentration. La diurèse est bénéficier d’une épuration extrarénale, en raison du risque de surcharge extra-
alors inférieure à 0,75 L/24 h. cellulaire induit par la solution hypertonique de chlorure de sodium.
L’osmolalité urinaire maximale (la diurèse
minimale) est normalement atteinte lorsque
l’osmolalité plasmatique devient supérieure Conduite à tenir devant une déshydratation intracellulaire
ou égale à 300 mOsm/kg d’eau, valeur qui Les déshydratations intracellulaires sont toujours secondaires à une élévation de
correspond au seuil physiologique de la soif l’osmolalité efficace plasmatique. Elles s’accompagnent généralement d’une
intense. Ainsi, la régulation des entrées
d’eau dans l’organisme par la stimulation du hypernatrémie, définie par une concentration plasmatique de sodium supérieure
centre hypothalamique de la soif prend le à 145 mmol/L. La natrémie peut cependant diminuer lorsque l’hyperosmolalité
relais de l’adaptation rénale d’excrétion plasmatique est secondaire à la présence anormale en concentration élevée d’un
d’eau en cas de déshydratation intracellu- soluté autre que le sodium, de bas poids moléculaire et osmotiquement actif. Ce
laire importante.
.../... soluté est responsable d’un « trou osmotique », défini par la différence entre l’os-
molalité mesurée et calculée. Ce soluté peut être d’origine endogène (glucose
768 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
au cours de la décompensation diabétique) ou exogène (mannitol, glycocolle,
.../... éthylène glycol).
En physiopathologie, les stimulus non osmo-
tiques, essentiellement la baisse de volémie Ces états hyperosmolaires avec hypertonicité plasmatique doivent être distin-
artérielle, prennent une importance primor- gués des états hyperosmolaires sans hypertonicité plasmatique liés à la présence
diale : en cas de diminution de plus de 10 % plasmatique en concentration élevée d’un soluté de bas poids moléculaire mais
de la volémie efficace, la neurosécrétion osmotiquement inactif car librement diffusible dans les cellules : principalement
hypothalamique d’ADH est stimulée par des
afférences provenant des barorécepteurs l’urée ou l’éthanol. Dans ces états hyperosmolaires, le « trou osmotique » est
carotidiens et volorécepteurs atriaux. Elle augmenté mais la tonicité plasmatique, et donc le volume intracellulaire, sont
induit une sécrétion d’ADH inappropriée à normaux.
l’hyponatrémie qu’elle entraîne.
1. Causes
• Déshydratations intracellulaires avec hypernatrémie : elles sont le plus sou-
vent liées à l’existence de pertes rénales d’eau non compensées, plus rarement,
à l’administration ou l’ingestion accidentelle d’une solution hypertonique de
chlorure de sodium. Les pertes d’eau pouvant favoriser l’apparition d’une hyper-
natrémie sont multiples et peuvent être divisées en 3 catégories : l’augmentation
des pertes insensibles par la respiration et la sueur (favorisées par l’hyperventi-
lation et l’hyperthermie), les pertes rénales (diabètes insipides centraux ou
néphrogéniques, diurèses osmotiques) et gastro-intestinales.
• Hyponatrémies hypertoniques : le soluté responsable du trou osmotique peut
être d’origine endogène : la situation clinique la plus fréquente d’hyponatrémie
hypertonique est la décompensation diabétique. Plus rarement, le soluté est d’ori-
gine exogène au décours des intoxications par mannitol, glycocolle, éthylène
glycol.
2. Physiopathologie
• Création de l’hyperosmolalité extracellulaire : l’apparition d’une hyperna-
trémie est généralement due à la constitution d’un bilan d’eau négatif (entrées
transitoirement inférieures aux sorties). Physiologiquement, toute augmentation
de l’excrétion rénale d’eau (ou apparition de pertes extrarénales) entraîne une
stimulation de la soif qui suffit, par l’adaptation des entrées d’eau, à maintenir
la natrémie dans les limites de la normale. Ainsi, la plupart des patients atteints
de diabète insipide neuro- ou néphrogénique adaptent leur prise de boisson à
leur diurèse et régulent leur natrémie. L’apparition d’une hypernatrémie signe
donc soit un défaut d’accès à l’eau (vieillards, enfants, ou patients ne pouvant
ni boire d’eux-mêmes, ni exprimer leur soif), soit plus rarement un défaut pri-
mitif de la sensation de soif associé. Ce défaut de la soif doit faire rechercher,
par tomodensitométrie ou imagerie par résonance magnétique (IRM), une lésion
hypothalamique du centre de la soif (tumeur, anomalies vasculaires essentielle-
ment).
Au cours de la décompensation diabétique, l’élévation de la concentration extra-
cellulaire de glucose non diffusible entraîne un flux d’eau de la cellule vers le
liquide extracellulaire et donc une déshydratation intracellulaire associée à une
hyponatrémie. Secondairement, l’élévation de la concentration plasmatique de
glucose est tellement importante que la charge filtrée de glucose dépasse la capa-
cité de réabsorption rénale. Ce glucose non réabsorbé entraîne avec lui de l’eau
par un mécanisme de diurèse osmotique. Cette perte d’eau entraîne l’élévation
progressive de la natrémie, jusqu’à l’apparition d’une hypernatrémie.
• Conséquences de l’hyperosmolalité extracellulaire : l’élévation de l’osmola-
lité plasmatique entraîne un flux d’eau des cellules vers le liquide extracellu-
laire. L’hypernatrémie aiguë induit des symptômes neurologiques de gravité
variable (léthargie, perte de connaissance, coma) pouvant aller jusqu’au décès
du patient. Lorsqu’elle se constitue lentement, l’élévation de l’osmolalité plas-
matique est équilibrée par une augmentation du contenu en osmolytes intracel-
luaires qui permet de réguler le volume cellulaire au cours des hypernatrémies
chroniques. Cette adaptation expose à un risque d’hyperhydratation intracellu-
laire aiguë (potentiellement mortelle) en cas de correction trop rapide de l’hy-
pernatrémie.
LA REVUE DU PRATICIEN (Paris) 769
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
3. Diagnostic
Le diagnostic étiologique d’une hypernatrémie commence par un interrogatoire
soigneux du patient et de l’entourage à la recherche notamment d’antécédents
évocateurs (diabète sucré) de la prise ou de l’administration récente de solution
hypertonique ou de médicaments apportant une grande quantité d’osmoles (par
exemple, apports sodés massifs au cours de certaines antibiothérapies), d’un
contexte infectieux, d’épisodes diarrhéiques et de vomissements.
La diurèse doit être grossièrement quantifiée, ainsi que la sensation de soif, la
capacité à l’exprimer et à la satisfaire.
Une diabète sucré décompensé doit systématiquement être recherché par la
mesure de la glycémie et d’une glycosurie à la bandelette, puis par dosage de
laboratoire.
La mesure de l’osmolalité urinaire contemporaine de l’osmolalité plasmatique
supérieure à 300 mOsm/kg permet de juger du caractère adapté ou non de la
réponse rénale à l’hypernatrémie : l’hypernatrémie doit normalement entraîner
une hypersécrétion d’ADH et l’élévation de l’osmolalité urinaire. Schémati-
quement, une osmolalité urinaire supérieure ou égale à 850 mOsm/kg témoigne
d’une réponse rénale normale à une sécrétion d’ADH appropriée. À l’inverse,
lorsque l’osmolalité urinaire contemporaine d’une hypernatrémie est inférieure
à 300 mOsm/kg, il existe une anomalie majeure soit de la sécrétion, soit de la
réponse rénale à l’action de l’ADH.
Grâce à divers éléments on pourra :
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique, secon-
daires à des pertes d’eau pure ou très pauvre en sodium :
– par apport d’eau insuffisant pour compenser les pertes extrarénales normales
(osmolalité urinaire appropriée) :
. sujets ayant des troubles de conscience ou ne pouvant exprimer leur soif (sujets
déments, nourrissons),
. trouble primaire de la soif : l’absence de sensation de soif contemporaine d’une
osmolalité plasmatique supérieure à 300 mOsm/kg chez un individu pouvant
l’exprimer doit faire rechercher une lésion hypothalamique du centre de la soif.
Les troubles primitifs de la soif sont fréquemment associés à un diabète insipide
neurogénique partiel ;
– au cours de la polyurie des diabètes insipides : l’osmolalité urinaire contem-
poraine de l’hypernatrémie est inappropriée. L’administration par voie sous-cuta-
née ou nasale de dDAVP (agoniste des récepteurs V2 de l’ADH) permet de dis-
tinguer entre :
. un diabète insipide d’origine neurogénique (défaut de sécrétion hypothalamique
d’ADH) lorsque l’osmolalité s’élève de plus de 50 % dans les 2 h qui suivent
l’administration de dDAVP ;
. un diabète insipide d’origine néphrogénique (absence de réponse rénale à l’ac-
tion de cette hormone) lorsque l’osmolalité urinaire varie de moins de 30 % en
cas d’origine néphrogénique ;
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique secon-
daires à des pertes d’eau pure avec perte relativement plus faible de sodium :
– au cours des polyuries osmotiques, des substances de faible poids moléculaire
librement filtrées et peu réabsorbées entraînent la disparition du gradient cor-
tico-papillaire intrarénale. L’osmolalité urinaire est proche de celle du plasma
mais la concentration en électrolyte est beaucoup plus faible. La perte d’eau et
de sodium ainsi engendrée entraîne une déshydratation globale. Le soluté res-
ponsable peut être le glucose (la glycosurie élevée du diabète déséquilibré est la
première étiologie de polyurie osmotique), l’urée (polyurie osmotique de la
réduction néphronique avancée), le mannitol… ;
– au cours des pertes extrarénales (osmolalité urinaire appropriée) :
. pertes par vomissements, aspiration gastrique, diarrhée non compensées ;
. pertes extrarénales autres, augmentées par l’hyperventilation et l’hyperthermie ;
• reconnaître les états hyperosmolaires avec hypertonicité plasmatique, secon-
daires à une surcharge en solutés non diffusibles (osmolalité urinaire appro-
priée) :
770 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
. la surcharge aiguë accidentelle en sodium : le plus fréquemment par apport
Hyperhydratation excessif de bicarbonate molaire au cours d’un arrêt cardiorespiratoire ou d’une
et deshydratation hyperkaliémie, entraîne un état d’hyperhydratation globale,
extracellulaires . hyperglycémie aiguë, principalement à la phase aiguë initiale de la décom-
pensation diabétique, avant apparition de la diurèse osmotique.
Aspects physiopathologiques
• Syndromes œdémateux : la formation d’œ- 4. Traitement
dèmes généralisés nécessite une altération
d’une ou de plusieurs forces de l’équilibre • Hypertonicité plasmatique secondaire à des pertes d’eau pures ± pertes de
de Starling qui régit les échanges périphé- sodium : comme pour l’hyponatrémie, la correction de l’hypernatrémie, lors-
riques entre secteurs plasmatique et inter- qu’elle est chronique et bien tolérée, doit être effectuée lentement, par adminis-
stitiel, l’équilibre étant déplacé en faveur
d’une augmentation nette de la filtration. Les
tration d’eau. Une hypernatrémie aiguë et symptomatique est corrigée plus rapi-
œdèmes sont le plus souvent dus à une aug- dement par l’administration orale d’une plus grande quantité d’eau ou en ajoutant
mentation de la pression hydrostatique capil- une perfusion intraveineuse de solution glucosée hypotonique à 2,5 %. Il est
laire (secondaires à une élévation de la pres- conseillé, en dehors de situations exceptionnelles, de ne pas diminuer la natré-
sion veineuse essentiellement, ou à une mie de plus de 1 mmol/h et 15 mmol/j. La voie orale est toujours privilégiée. Un
vasodilatation artériolaire), plus rarement à
une diminution de pression oncotique plas- apport de sodium et de potassium est effectué en fonction du degré de déshy-
matique (insuffisance hépatique, syndrome dratation extracellulaire qui est pratiquement constamment associé, et de la déplé-
néphrotique, entéropathies exsudatives) ou tion potassique.
une élévation de la pression oncotique inter- Le déficit hydrique peut être estimé grossièrement à partir du poids corporel du
stitielle (hypothyroïdie). La constitution
d’œdèmes suppose également une rétention sujet à l’état stable (PDC) et de la natrémie mesurée ([Na]p), par la formule sui-
majeure et prolongée de sodium par le rein, vante :
soit parce que le rein est anormal et ne déficit hydrique = 0,60 x PDC x (([Na]p/140)-l)
répond plus à l’expansion (œdèmes primi- • Le traitement de la décompensation diabétique associe la réhydratation extra-
tifs) soit parce que l’expansion s’associe à
une hypovolémie efficace. Les mécanismes et intracellulaire à l’administration d’insuline et de glucose.
compensateurs de cette hypovolémie effi- • La correction des hypernatrémies aiguës, en particulier celles secondaires à
cace sont à l’origine et soutiennent la réten- l’administration accidentelle de sodium ou s’accompagnant d’une insuffisance
tion sodée par un rein par ailleurs normal rénale, peut être assurée par hémodialyse.
(œdèmes secondaires).
• Œdèmes primitifs :
– la glomérulonéphrite est l’exemple type
des œdèmes primitifs : dans les syndromes Hyperhydratation
néphritiques, la rétention rénale primitive
provoque un bilan positif de sodium et d’eau
et déshydratation extracellulaires
(la natriurèse très faible est inférieure aux
apports habituels, oligurie) secondairement
responsable d’une expansion extracellulaire Conduite à tenir
vasculaire (responsable d’une élévation du devant une hyperhydratation extracellulaire
débit cardiaque et d’une HTA) et intersti-
tielle. La rénine et l’aldostérone plasma- Le volume extracellulaire est déterminé par le contenu (et non la concentration)
tiques, l’activité sympathique sont dimi- en sodium extracellulaire. L’hyperhydratation extracellulaire est toujours secon-
nuées. Le mécanisme de la rétention sodée daire à un bilan sodé positif (entrées supérieures aux sorties) qui s’accompagne
est mal connu. Dans la majorité des cas, il d’une rétention rapide d’eau du fait de la régulation de la natrémie (l’osmolalité
n’existe pas de syndrome néphrotique, l’al-
buminémie étant supérieure à 30 g/L, la pro- plasmatique) maintenue constante par l’ADH (cf. encadré régulation du bilan
téinurie inférieure à 3 g/24 h ; de sodium, page 773).
– la déplétion sélective en potassium pro-
voque une augmentation de la réabsorption 1. Causes
tubulaire proximale de sodium responsable
d’une expansion du volume extracellulaire. Les états d’hyperhydratation extracellulaire sont répertoriées dans le tableau II.
Des syndromes œdémateux ont été décrits Ils peuvent être subdivisés, si on écarte la situation particulière de l’insuffisance
au cours de déplétions potassiques sévères rénale avancée, en 2 catégories :
(supérieures à 500 mmol).
• Œdèmes secondaires : l’anomalie primitive – les hyperminéralocorticismes primitifs dont l’hyperaldostéronisme primaire
est une diminution de la volémie efficace qui est la principale cause, s’expriment cliniquement par une hypertension artérielle.
peut être définie par la volémie effectivement L’hyperhydratation extracellulaire est trop limitée pour entraîner un syndrome
présente dans le lit artériel. La stimulation œdémateux du fait du phénomène d’échappement du rein à l’hypersécrétion d’al-
des mécanismes régulateurs (dont témoigne
l’élévation de la rénine et de l’aldostérone
dostérone ;
plasmatique) met en jeu les barorécepteurs à – les causes de rétentions hydrosodées majeures qui entraînent l’apparition d’œ-
haute pression et entraîne un bilan cumula- dèmes généralisés.
tif de sodium responsable de l’expansion,
mais incapable de restaurer la volémie arté- 2. Physiopathologie (cf. encadré)
rielle. Selon l’origine, la diminution de la
volémie artérielle est associée ou non à une Hyperminéralocorticismes primitifs et tableaux assimilés : l’excès de minéralo-
diminution du volume vasculaire ; corticoïdes circulants, par leur action sur le tube collecteur cortical, induisent
.../...
une rétention rénale de sodium. Dans 90 % des cas, le stéroïde responsable est
LA REVUE DU PRATICIEN (Paris) 771
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
TABLEAU II
.../...
– dans l’insuffisance cardiaque chronique
congestive, la diminution de la volémie arté- Causes des hyperhydratations extracellulaires
rielle est secondaire à la diminution du
volume d’éjection systolique et du débit car- • Expansion du secteur extracellulaire sans œdèmes
diaque ;
– dans les insuffisances cardiaques à débit
Régulation du bilan du sodium
élevé (anémie, fistules artérioveineuses, A. Syndromes d’hyperminéralocorticorticismes primitifs ou apparentés :
béribéri) la diminution de la volémie arté- – syndrome de Conn
rielle est secondaire à la diminution des – hyperplasie bilatérale des surrénales (hyperplasies nodulaires, déficits
résistances artérielles périphériques, et en 11β-hydroxylase, 17 α-hydroxylase)
contraste avec l’élévation du débit cardiaque – intoxication par la glycyrrhizine (réglisse, Antésite)
et du volume sanguin total, caractéristique – pseudohyperaldostéronisme (syndrome de Liddle)
de ces pathologies ; – excès de glucocorticoïdes
– l’hypovolémie artérielle au cours de la cir- B. Insuffisance rénale avancée
rhose hépatique répond de plusieurs méca-
nismes : au stade précoce de la cirrhose • États œdémateux généralisés
expérimentale, l’hyperpression intrahépa-
tique, par l’intermédiaire de barorécepteurs Régulation du bilan du sodium
intrahépatiques, semble responsable de la A. Augmentation de la pression hydrostatique capillaire :
rétention rénale de sodium (réflexe hépato- – cirrhose hépatique
rénal). La diminution des résistances péri- – insuffisance cardiaque congestive
phériques induite par la vasodilatation – néphropathies glomérulaires
splanchnique et apparition d’angiomes stel- – toxémie gravidique
laires cutanés et viscéraux et diverses fis-
tules artérioveineuses, explique l’hypovolé- B. Augmentation de la perméabilité capillaire :
mie artérielle et le débit cardiaque élevé – choc anaphylactique, septique, œdème angio-neurotique familial
contemporains. Ce syndrome hyperkiné- – médicaments vasodilatateurs (minoxidil, inhibiteurs calciques)
tique participe à la création et à l’entretien C. Augmentation de la différence de pression oncotique:
de la rétention hydrosodée. La rétention – diminution de la pression oncotique plasmatique (albuminémie < 15-20 g/L)
hydrosodée se distribue de façon préféren-
. syndrome néphrotique sévère
tielle dans le péritoine à partir des capillaires
sinusoïdaux et à travers la capsule hépatique. . insuffisance hépatique
Rapidement, l’augmentation du retour lym- . gastro-entéropathies exsudatives
phatique vers la circulation systémique est – augmentation de la pression oncotique interstitielle : hypothyroïdie
dépassée et une ascite apparaît. Lorsque la D. Mécanisme indéterminé : œdèmes cycliques idiopathiques
rétention hydrosodée est majeure, un syn-
drome œdémateux généralisé s’installe ;
– au cours des syndromes néphrotiques, défi-
nis par l’association d’une protéinurie supé-
rieure à 3 g/24 h, d’une hypoalbuminémie l’aldostérone. Dans l’intoxication par la réglisse, la rénine et l’aldostérone sont
(30 < g/L) et d’un syndrome œdémateux. La diminuées. La réglisse inhibe la 11β-hydroxystéroïde-déshydrogénase qui cata-
rétention hydrosodée est induite par une aug- lyse le cortisol en cortisone dans le rein. L’inhibition de cette enzyme démasque
mentation primitive de la réabsorption tubu- l’action minéralocorticoïde du cortisol qui est physiologiquement absente.
laire de NaCl (tubule collecteur) et par les
mécanismes régulateurs de l’hypovolémie
efficace secondaire à la diminution de la 3. Diagnostic
pression oncotique. Une diminution isolée • Diagnostic clinique et paraclinique : il cherche à déterminer l’extension et les
de la pression oncotique ne semble cepen-
dant pas pouvoir entraîner à elle seule une
conséquences de la rétention hydrosodée :
hypovolémie efficace tant que l’albuminé- – la pression artérielle est plutôt basse dans l’insuffisance cardiaque et la cir-
mie demeure supérieure à 20 g/L. En effet, rhose, et élevée dans les hyperminéralocorticismes primitifs ;
l’hypoalbuminémie plasmatique s’accom- – la prise de poids, surtout si elle est rapide, amène une donnée quantifiable et
pagne d’une diminution proportionnelle de précoce, le syndrome œdémateux n’apparaissant cliniquement qu’au-délà de
la concentration interstitielle d’albumine ce
qui maintient la différence de pression onco- 3 kg, les épanchements sérieux au-delà de 6 kg. Dans les syndromes œdémateux
tique constante. majeurs, la prise de poids peut être massive (parfois > 30 kg en quelques
En réalité, la pathogénie semble un conti- semaines) ;
nuum entre des tableaux proches de la glo- – la recherche d’œdèmes au cours d’une rétention hydrosodée modérée se fera
mérulonéphrite aiguë associant un volume
plasmatique élevé, une activité rénine et une
au niveau des membres inférieurs (jambes en poteaux) chez un sujet ambula-
aldostéronémie basses, et des tableaux avec toire, et au niveau des zones déclives chez un sujet couché (empâtement lom-
hypovolémie vraie prédominante, associés à baire, de la face postérieure des cuisses, rétrotibial). Ces œdèmes blancs, mous,
une activité rénine et sympathique et à une indolores, gardent l’empreinte du doigt à la pression (signe du godet) ;
aldostéronémie élevées. La diminution de la – la recherche clinique d’une anasarque (extension aux séreuses) sera aidée par
pression oncotique, éventuellement d’autres
mécanismes non élucidés (anomalies de la la pratique orientée de radiographies (épanchements pleuraux, œdème pulmo-
perméabilité capillaire) seraient à l’origine naire interstitiel) et d’échographies (recherche d’ascite, d’un épanchement péri-
d’une hypovolémie et de sa persistance mal- cardique).
gré la rétention hydrosodée. • Diagnostic biologique : l’hyperhydratation extracellulaire s’accompagne d’une
diminution des protides et de l’hématocrite. Cependant, une hypoprotidémie
772 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
majeure doit faire rechercher une cause particulière, notamment un syndrome
Régulation du bilan néphrotique et une cirrhose.
du sodium Dans les syndromes œdémateux, la natrémie est normale lorsque l’hyperhydra-
Le volume extracellulaire est déterminé par le tation est restreinte au secteur extracellulaire. Une hyponatrémie signe l’exis-
contenu (et non la concentration) en sodium tence d’une hyperhydratation intracellulaire associée, le plus souvent liée à une
extracellulaire. En effet, une augmentation du
contenu en sodium induite par un déséquilibre sécrétion d’ADH entraînée par l’hypovolémie efficace.
du bilan sodé (entrées supérieures aux sorties) Les hyperminéralocorticismes primitifs se traduisent par une hypertension arté-
s’accompagne d’une rétention proportionnelle rielle, une légère hypernatrémie, une hypokaliémie et une alcalose métabolique.
d’eau car la natrémie (l’osmolalité plasma- Les dosages de rénine et d’aldostérone plasmatiques en position couché et débout,
tique) est maintenue constante par la sécrétion
d’ADH. Ainsi, chez un sujet sain, une aug- de la cortisolémie à 8 h et 16 h, d’aldostérone et de cortisol dans le recueil des
mentation du contenu en sodium de 140 mmol urines de 24 h motivés par une HTA, associés à des arguments cliniques et (ou)
s’accompagne nécessairement d’une aug- biologiques et (ou) par une HTA sévère résistante à un traitement bien conduit
mentation du volume extracellulaire de 1 L et permettent d’établir le diagnostic d’hyperminéralocorticisme et d’orienter les
d’une prise de 1 kg.
La valeur régulée est la volémie efficace, para-
examens complémentaires nécessaires au diagnostic étiologique.
mètre non mesurable qui peut être défini Dans les états œdémateux, la natriurèse est généralement effondrée, reflétant la
comme la part de la volémie qui participe effec- rétention sodée rénale (une natriurèse peut cependant être maintenue sous trai-
tivement à la perfusion tissulaire. Cette volé- tement diurétique). À l’inverse, au cours des hyperminéralocorticismes primtifs,
mie efficace représente normalement 15 % de
la volémie, soit la fraction de volume sanguin
il existe un phénomène d’échappement du fait de l’hypertension artérielle, et la
située dans le système artériel. Elle est un déter- natriurèse est rapidement égale aux apports. Cet échappement explique l’absence
minant majeur de la pression artérielle. Bien de syndrome œdémateux dans les hyperminéralocorticismes primitifs.
que l’hypovolémie efficace varie normalement
parallèlement aux volumes plasmatique total
et extracellulaire, elle peut être indépendante 4. Traitement
de ces volumes : une hypovolémie efficace
peut résulter d’une diminution primitive du • Le traitement des syndromes œdémateux repose sur le traitement étiologique
débit cardiaque ou des résistances vasculaires lorsque celui-ci est possible, et le traitement symptomatique du syndrome œdé-
périphériques. L’hypovolémie efficace est mateux :
alors à l’origine d’une stimulation des sytèmes
hormonaux capables d’induire une rétention
– la restriction sodée et hydrique constitue l’élément essentiel du traitement
hydrosodée, et donc un état de rétention hydro- puisque, pour entraîner le bilan négatif d’eau et de sodium souhaité, il convient
sodée avec syndrome œdémateux. de restreindre au maximum les apports ;
Une diminution de volémie efficace entraîne – le repos au lit avec surélévation des membres inférieurs aide à la résorption
l’activation des systèmes rénine-angiotensine-
aldostérone et sympathique qui stimulent la
locale des œdèmes et surtout diminue le tonus des systèmes sympathique et
réabsorption rénale de sodium : rénine-aldostérone et la sécrétion d’ADH, favorisant ainsi l’excrétion rénale
– la stimulation des volorécepteurs veineux ou d’eau et de sodium ;
atriaux, et des barorécepteurs artériels sen- – le plus souvent, l’utilisation de diurétiques est indispensable pour obtenir la
sibles aux variations de pression, active le sys-
tème sympathique. cette activation sympa-
résorption des œdèmes ; le furosémide (Lasilix) est le traitement d’attaque de
thique contribue directement à la rétention choix des syndromes œdémateux majeurs. Utilisé à la dose de 40 à 160 mg/j
rénale de sodium ; (puis 20 à 60 mg/j en dose d’entretien) lorsque la fonction rénale est préservée,
– la libération de rénine est provoquée par des il reste actif au cours de l’insuffisance rénale à condition d’augmenter la poso-
stimulus systémiques (activation du système logie. Il expose au risque d’hypokaliémie qu’il convient de prévenir par une sup-
sympathique) ou intrarénaux (activation des
barorécepteurs de l’appareil juxtaglomérulaire, plémentation potassique.
diminution du débit de chlore dans le fluide Lorsque les œdèmes sont induits par un hyperaldostéronisme secondaire (cir-
tubulaire délivré à la macula densa). La rénine rhose) on utilisera un diurétique épargneur du potassium tels que l’amiloride, le
entraîne la production locale et systémique
d’angiotensine II. L’angiotensine II systémique
triamtérène, ou la spironolactone disponibles sous différentes formes pharma-
stimule la libération surrénalienne d’aldosté- cologiques, seuls ou en association. Ces traitements sont contre-indiqués en cas
rone. Ces deux hormones, par leurs effets tubu- d’insuffisance rénale en raison du risque d’hyperkaliémie ;
laires (augmentation de la réabsorption de • Le traitement des hyperminéralocorticismes repose sur:
NaCl du tube proximal pour l’angiotensine II,
du tube collecteur pour l’adostérone) et glo- – le traitement étiologique : arrêt de la prise de réglisse, traitement chirurgical
mérulaires (baisse du DFG) entraînent une d’une tumeur surrénalienne, traitement substitutif au cours des blocs enzyma-
rétention sodée rénale. tiques… ;
Une augmentation de volémie efficace induite – le traitement symptomatique de l’hyperminéralocorticisme fera appel à des
par exemple par une perfusion aiguë de sodium
va entraîner la production d’hormones natriu- diurétiques épargneurs de potassium comme l’amiloride ou le triamtérène, ou à
rétiques : le facteur atrial natriurétique (ANF) un analogue inactif de l’aldostérone : la spironolactone.
est produit par les oreillettes cardiaques sous
l’effet d’une élévation de la tension pariétale.
L’ANF induit une augmentation du débit de Conduite à tenir
filtration glomérulaire et diminue la réabsorp-
tion tubulaire (essentiellement au niveau du
devant une déshydratation extracellulaire
canal collecteur). Par ailleurs, l’ANF inhibe la
synthèse de rénine et d’aldostérone.
L’apparition d’une déshydratation extracellulaire nécessite la constitution d’un
bilan sodé négatif (entrées transitoirement inférieures aux sorties).
LA REVUE DU PRATICIEN (Paris) 773
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
TABLEAU III
Causes principales des états
de déshydratation extracellulaire
Pertes extrarénales de sodium
A. Gastro-intestinales :
– diarrhée
– fistules ou drainages biliaires, pancréatiques, intestinaux
B. Cutanées :
– sueurs excessives (mucoviscidose)
– brûlures, affections cutanées inflammatoires
C. Création d’un « troisième secteur » :
– occlusion intestinale, péritonite
– pancréatite
D. Autres : ponctions péritonéales ou pleurales
Pertes rénales de sodium
A. Rein normal :
– vomissements, fistules ou aspirations gastriques
– diurétiques, diurèse osmotique
– déficit en minéralocorticoïdes
– hypercalcémie, acidose métabolique
B. Rein pathologique :
– insuffisance rénale chronique (retard à l’adaptation lors de la réduction brutale
des apports sodés)
– insuffisance rénale chronique avec syndrome d’hyporéninémie et hypoaldosté-
ronisme
– néphropathie avec perte de sel : néphropathies interstitielles, acidose tubulaire
distale et proimale
– syndrome de levée d’obstacle, reprise de diurèse d’insuffisance rénale aiguë
– pseudo-hypoaldostéronisme
1. Étiologie
Les causes des déshydratations extracellulaires peuvent être subdivisées en pertes
rénales et extrarénales de sodium, elles sont résumées dans le tableau III.
2. Physiopathologie
Les capacités d’adaptation rénales à un régime pauvre en sodium sont très impor-
tantes (la natriurèse pouvant être quasi nulle). L’apparition d’un bilan sodé néga-
tif suppose donc, soit la perte de sécrétions extrarénales riches en sodium, soit
une altération primitive des capacités rénales de réabsorption du sodium.
• Pertes extrarénales :
– lors des diarrhées ou lors de pertes de liquide de sécrétions intestinales, biliaires
ou pancréatiques : par fistules ou drainages, la perte de bicarbonate de sodium
et de chlorure de sodium aboutit à la création d’une contraction des volumes
extracellulaires et d’une acidose métabolique. On peut en rapprocher les séques-
trations liquidiennes non extériorisées, et donc difficiles à quantifier, qui peu-
vent survenir au cours d’occlusions intestinales, péritonites ou pancréatites. Dans
toutes ces situations, l’apparition d’une hypovolémie entraîne une réponse rénale
appropriée (natriurèse < 10 mmol/L ou par 24 h) ;
– la perte (par vomissement, fistule ou aspiration) de liquide gastrique, riche en
acide chlorhydrique : elle entraîne une alcalose métabolique. Initialement, cette
alcalose induit une perte rénale de sodium, car la quantité de bicarbonate de sodium
filtrée dépasse les capacités tubulaires de réabsorption aboutissant à une perte
rénale de bicarbonate de sodium. Cette alcalose entraîne également une hypoka-
liémie (par transfert intracellulaire et par stimulation de l’excrétion rénale de
potassium). À l’arrêt des vomissements, la concentration de bicarbonate s’équi-
774 LA REVUE DU PRATICIEN (Paris)
1997, 47
Néphrologie-urologie
libre à une valeur permettant sa totale réabsorption par le rein. La natriurèse s’ef-
fondre (< 10 mmol/24 h). La chlorurie très faible signe la déplétion chlorée ;
– pertes sudorales : la sueur contient 50 à 80 mmol/L de NaCl. Une perte notable
de sodium par sudation peut se produire dans certaines circonstances comme
l’exposition brutale à des températures élevées ou l’exercice physique intense.
Lorsqu’un sujet est exposé chroniquement à la chaleur, la concentration en NaCl
s’adapte et diminue. Cependant, les patients atteints d’insuffisance surrénale
chronique ou de mucoviscidose ont des concentrations de sodium dans la sueur
plus élevées que la normale et un défaut d’adaptation à la chaleur.
• Pertes rénales : d’une façon générale, deux phases peuvent être distinguées
lors de pertes de sodium d’origine rénale : lors de l’installation du trouble, l’ex-
crétion urinaire de sodium est supérieure aux apports, à l’origine d’un bilan néga-
tif de sodium et de la création de la contraction des volumes extracellulaires.
Secondairement, la charge sodée filtrée diminue du fait de cette contraction et
les systèmes de régulation stimulent les capacités de réabsorption sodée dans les
différentes parties du néphron encore fonctionnelles. Progressivement, la natriu-
rèse devient égale aux apports, mais demeure inappropriée à la déshydratation
extracellulaire, et un état stable s’instaure.
– L’administration de diurétiques entraîne une perte rénale de sodium et expose
à divers troubles hydroélectrolytiques associés, fonctions du site d’action de diu-
rétique : l’abus des diurétiques de l’anse (type furosémide) et les diurétiques thia-
zidiques qui inhibent la réabsorption dans le tube contourné distal entraînent une
contraction des volumes cellulaires associée à une alcalose métabolique et à une
hypokaliémie. À l’inverse, l’abus de diurétiques agissant sur le tube collecteur
cortical (amiloride, spironolactone, triamtérène) ou leur utilisation malgré l’exis-
tence d’une réduction néphronique entraîne une contraction des volumes cellu-
laires associée à une acidose métabolique et à une hyperkaliémie.
– Les diurèses osmotiques abordées dans le chapitre des déshydratations intra-
cellulaires, entraînent une perte d’eau supérieure à celle de sodium. La contrac-
tion extracellulaire est alors accompagnée d’une déshydratation intracellulaire.
– Déficits en aldostérone : la diminution de la réabsorption de sodium dans le
tube collecteur cortical, entraîne une contraction du volume extracellulaire asso-
ciée à une acidose métabolique et à une hyperkaliémie. Le déficit en aldostérone
peut être d’origine surrénalienne (insuffisance surrénalienne globale, bloc enzy-
matique aboutissant à un déficit spécifique en minéralocorticoïdes), ou secon-
daire à un déficit en rénine associé à certaines insuffisances rénales (syndrome
d’hyporéninémie et hypoaldostéronisme au cours de la néphropathie diabétique,
de la néphropathie aux antalgiques et AINS par exemple). Rarement, la rénine
et l’aldostérone sont très élevées, mais ni l’aldostérone endogène ni l’adminis-
tration de minéralocorticoïde n’entraînent l’effet rénal attendu. Cette pathologie
rare de l’enfance est décrite sous le nom de pseudo-hypoaldostéronisme.
– L’hypercalcémie et l’acidose métabolique diminuent la réabsorption tubulaire
de sodium et peuvent être responsables d’une contraction des volumes extra-
cellulaires.
3. Diagnostic
• Examen clinique : la déshydratation extracellulaire modérée peut s’accompa-
gner de sensations vertigineuses, majorées par l’orthostatisme. Cliniquement,
une perte de poids modérée, la diminution du tonus des globes oculaires, un pli
cutané, un aplatissement des veines périphériques et jugulaires en position cou-
chée devront être recherchés, ainsi qu’une exagération de la réponse à l’ortho-
statisme (lors du passage de la position couchée à la position debout, la fréquence
cardiaque s’élève de plus de 20 batt/min et les pressions artérielles diastolique
et systolique baissent de plus de 20 mmHg). Ces signes indicatifs sont cepen-
dant inconstants et non spécifiques. Une contraction sévère des volumes extra-
cellulaires entraîne une stimulation du système sympathique traduite clinique-
ment par une tachycardie (pouls filant) une vasoconstriction périphérique
(marbures, extrémités froides).
LA REVUE DU PRATICIEN (Paris) 775
1997, 47
D É S H Y D R ATAT I O N E T H Y P E R H Y D R ATAT I O N C E L L U L A I R E S E T E X T R A C E L L U L A I R E S
Points Forts • Examens biologiques : plusieurs modifications biologiques peuvent témoigner
de la contraction : élévation de la protidémie et de l’hématocrite, apparition d’une
à retenir insuffisance rénale fonctionnelle (élévation de l’urée plasmatique proportion-
● ● ● ● ● ● ● ● ● ● ● ● ● ● ● ●
nellement supérieure à celle de la créatininémie), hyperuricémie provoquée par
• Les volumes intra- l’augmentation de la réabsorption de l’acide urique.
et extracellulaires sont maintenus Le dosage de rénine et d’aldostérone plasmatiques dans certains cas permet de
dans les limites physiologiques diagnostiquer un état d’hyperaldostéronisme secondaire, témoin d’une contrac-
grâce à l’ajustement tion volémique parfois modérée et infraclinique, ou de poser le diagnostic d’hy-
permanent, indépendant poaldostéronisme primaire (rénine élevée, aldostérone basse) ou secondaire
et coordonné des sorties d’eau (rénine et aldostérone basses).
et de sodium aux entrées. Cette L’analyse de l’ionogramme urinaire (sur les urines de 24 h ou à défaut sur échan-
double régulation (volume tillon) oriente vers le mécanisme : la natriurèse est généralement inférieure
intracellulaire/volume à 10 mmol/L lorsque la perte sodée est extrarénale (sauf dans les vomissements
extracellulaire) met en jeu à la phase initiale) et supérieure ou égale aux apports, et inappropriée lorsque la
des valeurs régulées (osmolalité perte est d’origine rénale. Dans cette dernière circonstance, la natriurèse devient
plasmatique contre volémie appropriée si la cause s’arrête brutalement : ainsi, à l’arrêt d’un traitement diu-
efficace), des récepteurs rétique, il existe une période transitoire au cours de laquelle la contraction per-
(osmorécepteurs/barorécepteurs siste, mais la natriurèse est appropriée (< 10 mmol/L), malgré l’origine initiale-
carotidiens et de l’artère rénale ment rénale de la perte sodée.
afférente-volorécepteurs La recherche de diurétiques dans les urines à jeun ou sur le recueil de 24 h est
atriaux) et des systèmes de indispensable si la cause de la contraction n’est pas claire, et qu’une prise cachée
régulation hormonaux ou non de diurétiques est envisageable.
hormonaux différents (hormone
antidiurétique – soif contre axe 4. Traitement
rénine angiotensine- Le traitement d’une déshydratation extracellulaire commence si possible par le
catécholamine, facteur atrial traitement étiologique et la correction des facteurs aggravants : traitement de la
natriurétique) permettant (des) cause(s) d’une diarrhée ou de vomissements, arrêt des traitements diuré-
la régulation de l’excrétion tiques, arrêt d’un régime pauvre en sel, correction d’une hypercalcémie…
rénale de l’eau et du sodium. L’arrêt de la perte de sodium permet d’éviter l’aggravation de la contraction. La
• Les troubles de l’hydratation, correction de la volémie suppose alors la constitution d’un bilan positif égal au
rarement liés au dépassement bilan sodé négatif responsable de la contraction. Cette correction doit être favo-
des capacités physiologiques risée par une supplémentation sodée orale.
rénales d’adaptation aux Lorsqu’il existe des signes hémodynamiques préoccupants (marbrures, extré-
variations des entrées d’eau mités froides, pouls filant, hypotension artérielle) il faut avoir recours à l’admi-
et de sodium, reflètent le plus nistration intraveineuse de succédanés de plasma (Plasmagel, Plasmion) qui vont
souvent une altération permettre de restituer une volémie efficace suffisante pour rétablir la perfusion
des fonctions d’excrétion du rein. tissulaire périphérique. L’utilisation de ces solutés doit rester limitée et laisser
• Le caractère adapté place, dès que les signes hémodynamiques s’améliorent, à une réhydratation par
de la réponse rénale à une perfusion de solution de NaCl isotonique (9 ‰). ■
modification du bilan de l’eau
est jugé sur l’osmolalité
urinaire (< 150 mOsm/kg
en charge aqueuse aiguë,
et > 800 mOsm/kg en restriction POUR EN SAVOIR PLUS
hydrique prolongée). Offenstadt G, Maury E. États hyperosmolaires. In : Offenstadt G, Brunette MG
(eds). Désordres acido-basiques et hydroélectrolytiques. Coll. Réanimation, eds
• La réponse rénale Blackwell, 1996 : 90-105.
à une variation de la volémie
Rose BD, Rennke HG. Régulation du bilan de l’eau et du sodium. In : Physiopa-
efficace est jugée sur la natriurèse thologie des affections rénales et des désordres hydroélectriques. Collection l’Es-
(< 10 mmol/24 h en déplétion sentiel, éditions Pradel, 1995 : 32-74.
sodée, natriurèse égale aux Désordres du bilan de l’eau. Ibid, 74-107.
apports en charge sodée aiguë).
776 LA REVUE DU PRATICIEN (Paris)
1997, 47
Vous aimerez peut-être aussi
- Hydraulique 2 Régimes Transitoires Coup de BelierDocument139 pagesHydraulique 2 Régimes Transitoires Coup de BelierSaid MrfPas encore d'évaluation
- CHAPITRE 7 Procedes de SeparationDocument17 pagesCHAPITRE 7 Procedes de SeparationHadizatou Dao100% (3)
- 1 Généralité RDMDocument7 pages1 Généralité RDMecomech100% (2)
- 98 1003Document7 pages98 1003hizballah27Pas encore d'évaluation
- 98 991Document7 pages98 991hizballah27Pas encore d'évaluation
- 98 913Document6 pages98 913hizballah27Pas encore d'évaluation
- 98 987Document3 pages98 987hizballah27Pas encore d'évaluation
- 98 919Document5 pages98 919hizballah27Pas encore d'évaluation
- 98 999Document4 pages98 999hizballah27Pas encore d'évaluation
- 98 1011Document7 pages98 1011hizballah27100% (1)
- 98 909Document3 pages98 909hizballah27Pas encore d'évaluation
- Antagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À ProtonsDocument6 pagesAntagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À Protonshizballah27Pas encore d'évaluation
- 98 881Document5 pages98 881hizballah27Pas encore d'évaluation
- 98 905Document4 pages98 905hizballah27Pas encore d'évaluation
- 98 887Document5 pages98 887hizballah27100% (1)
- 98 899Document6 pages98 899hizballah27Pas encore d'évaluation
- 98 805Document5 pages98 805hizballah27Pas encore d'évaluation
- 98 765Document5 pages98 765hizballah27Pas encore d'évaluation
- 98 875Document5 pages98 875hizballah27Pas encore d'évaluation
- 98 797Document5 pages98 797hizballah27Pas encore d'évaluation
- 98 787Document10 pages98 787hizballah27Pas encore d'évaluation
- 98 679Document6 pages98 679hizballah27Pas encore d'évaluation
- 98 802Document3 pages98 802hizballah27Pas encore d'évaluation
- 98 781Document5 pages98 781hizballah27Pas encore d'évaluation
- 98 689Document5 pages98 689hizballah27Pas encore d'évaluation
- 98 771Document6 pages98 771hizballah27100% (1)
- 98 685Document3 pages98 685hizballah27Pas encore d'évaluation
- 98 667Document4 pages98 667hizballah27Pas encore d'évaluation
- 98 657Document3 pages98 657hizballah27Pas encore d'évaluation
- 98 671Document4 pages98 671hizballah27Pas encore d'évaluation
- Lipothymie, Syncope Et Perte de Connaissance Brève: Orientation DiagnostiqueDocument4 pagesLipothymie, Syncope Et Perte de Connaissance Brève: Orientation Diagnostiquehizballah27100% (1)
- 98 661Document6 pages98 661hizballah27Pas encore d'évaluation
- 98 653Document4 pages98 653hizballah27Pas encore d'évaluation
- Cinetique 4Document22 pagesCinetique 4Souad BouafiaPas encore d'évaluation
- Pollution Et Qualite de L'Eau: GCI 515 Génie de L'environnement ©2009 A. Ndabigengesere, S. Narasiah Et R. Leduc 2-1Document89 pagesPollution Et Qualite de L'Eau: GCI 515 Génie de L'environnement ©2009 A. Ndabigengesere, S. Narasiah Et R. Leduc 2-1EL Hassania EL HERRADIPas encore d'évaluation
- CHap-II Solutions PropriétésDocument48 pagesCHap-II Solutions PropriétésDô FlamîîngoPas encore d'évaluation
- RapportDocument15 pagesRapportYc YacinePas encore d'évaluation
- Part Number Cilindros Hidraulicos Serie 2h ParkerDocument2 pagesPart Number Cilindros Hidraulicos Serie 2h ParkerJEFFRY CAÑON100% (1)
- EXP-PR-UT040-FR-R0 - Slides Eau DouceDocument48 pagesEXP-PR-UT040-FR-R0 - Slides Eau Doucefasert sarytghPas encore d'évaluation
- 2013tou32124 PDFDocument119 pages2013tou32124 PDFkhalidPas encore d'évaluation
- CTM 2 Dosage ÉtalonnageDocument3 pagesCTM 2 Dosage ÉtalonnageNatiPas encore d'évaluation
- BiblioDocument132 pagesBiblioimen kriaaPas encore d'évaluation
- CTNEDocument118 pagesCTNEElkhattabi AsmaePas encore d'évaluation
- Pression Vapeur D'eau Pression de Vapeur SaturanteDocument2 pagesPression Vapeur D'eau Pression de Vapeur Saturantechama chouPas encore d'évaluation
- 2018 TerpènesDocument40 pages2018 TerpèneskpemeoraPas encore d'évaluation
- Préparer Les Fonds Pour Mise en PeintureDocument82 pagesPréparer Les Fonds Pour Mise en PeintureBenoit LoiseauPas encore d'évaluation
- Éxposé PincipeDocument8 pagesÉxposé PincipeLouai AmairiPas encore d'évaluation
- Les RochesDocument10 pagesLes Rochesprecieusevolcy63Pas encore d'évaluation
- Cours de Biotechnologie Des MicroalguesDocument115 pagesCours de Biotechnologie Des MicroalguesSaida SweetPas encore d'évaluation
- PolyamideDocument13 pagesPolyamideJouini ZakariaPas encore d'évaluation
- SujetCAPB 2016 Sept PDFDocument11 pagesSujetCAPB 2016 Sept PDFBrahim OmariPas encore d'évaluation
- Effet Hall PDFDocument3 pagesEffet Hall PDFMassinoAissouPas encore d'évaluation
- Osmose - Recherche Google PDFDocument1 pageOsmose - Recherche Google PDFFrançois Désiré RazanadahyPas encore d'évaluation
- To 11Document12 pagesTo 11Adrien OfthestonePas encore d'évaluation
- Panne ZDocument1 pagePanne ZBlaise AtchomPas encore d'évaluation
- PCSIDS2Document6 pagesPCSIDS2Mouad MelloukiPas encore d'évaluation
- Ocl 2004116 P 454Document3 pagesOcl 2004116 P 454Silvia CalabresePas encore d'évaluation
- Concentration Molaire TRCF EleveDocument4 pagesConcentration Molaire TRCF EleveKAUZZOU FATIMAZZAHRAPas encore d'évaluation
- Pfe M570.513 SNVDocument108 pagesPfe M570.513 SNVyoucef RebbouhPas encore d'évaluation