Académique Documents
Professionnel Documents
Culture Documents
Analyse 3
Transféré par
ibrahimCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Analyse 3
Transféré par
ibrahimDroits d'auteur :
Formats disponibles
3OS
1. Les notions à acquérir
1.1 Vocabulaire à apprendre à maîtriser dans ce chapitre
réactif produit équilibre chimique
conditions expérimentales système système fermé
système ouvert réversible irréversible
état d’équilibre réaction directe réaction inverse
réaction complète réaction totale vitesse de réaction
milieu homogène milieu hétérogène loi d’action de masse
constante d’équilibre équilibre homogène équilibre hétérogène
principe de Le Châtelier catalyseur
1.2 Compétences à acquérir au cours de ce chapitre
A la fin de ce chapitre vous devrez être capable de
• Poser et équilibrer l’équation chimique d’une réaction réversible.
• Identifier les composants appelés produits et réactifs d’une réaction réversible.
• Déterminer, si une réaction est réversible ou totale, soit à partir de son équation
chimique, soit à partir de la description de la réaction.
• Identifier les réactions directe et inverse.
• Définir ce qu’est un état d’équilibre.
• Citer les caractéristiques d’un état d’équilibre.
• Citer les facteurs influençant la vitesse d’une réaction.
• Expliquer comment se comportent les vitesses des réactions directe et inverse hors
et à l’état d’équilibre.
• Poser les lois de vitesse de Guldberg et Waage, pour une réaction réversible.
• Appliquer la loi d’action de masse à un système à l’équilibre.
• Expliquer pour quelles raisons l’état d’équilibre n’est pas synonyme de l’arrêt des
réactions chimiques.
• Citer les facteurs pouvant perturber un état d’équilibre et discuter leur effet sur l’état
d’équilibre.
• Résoudre une équation du second degré à une inconnue.
• Ecrire l’expression de la constante d’équilibre d’une réaction réversible, en fonction
des concentrations des réactifs et des produits.
3OS
• Calculer la constante d’équilibre d’une réaction réversible à partir de concentrations
connues à l’équilibre.
• Exprimer et calculer la constante d’équilibre d’une réaction réversible dont les
coefficients stoechiométriques sont des multiples des coefficients les plus petits
possibles (§ 5.3 remarque point a)).
• Savoir que si Ke est définit pour A B, alors pour B A, Ke’ = 1/Ke.
• Citer le(s) facteurs influençant et n’influençant pas la constante d’équilibre.
• Calculer la concentration d’un des composants à l’équilibre en connaissant la valeur
de la constante d’équilibre et le nombre de mole ou la concentration des autres
composants à l’équilibre.
• Interpréter qualitativement la valeur de la constante d’équilibre et ainsi déterminer si
le mélange réactionnel à l’équilibre contient majoritairement des réactifs ou des
produits ou ni l’un ni l’autre.
• Calculer les concentrations des réactifs et/ou des produits, à l’équilibre, en
connaissant le nombres de moles ou la concentration des réactifs au départ, ainsi
que la valeur de la constante d’équilibre.
• Calculer les concentrations des réactifs, au départ, en connaissant le nombre de
moles ou la concentration des réactifs et/ou des produits à l’équilibre.
• Définir ce qu’est le quotient réactionnel.
• Déterminer les situations qui requièrent l’utilisation du quotient réactionnel.
• Ecrire l’expression du quotient réactionnel
• Comparer la valeur du quotient réactionnel avec la valeur de la constante d’équilibre
et ainsi déterminer et décrire la manière dont le système se comportera pour arriver
à l’état d’équilibre.
• Calculer la concentration des réactifs et/ou des produits, à l’équilibre, en connaissant
le nombre de moles ou la concentration des réactifs et des produits au départ, ainsi
que la valeur de la constante d’équilibre, après avoir utiliser le quotient réactionnel.
• Citer le principe de Le Châtelier.
• Déterminer l’effet de la modification d’un ou plusieurs facteurs influençant l’état
d’équilibre.
• Décrire qualitativement, mais de manière détaillée étape par étape, pour chaque
facteur influençant l’équilibre, l’impact sur le système et le comportement de ce
dernier, si un ou plusieurs de ces facteurs sont modifiés.
2. Introduction
Les réactions chimiques que vous avez rencontrées jusqu’à présent, sont des réactions
qui évoluent jusqu'à la disparition totale d’au moins un des réactifs. Ces réactions sont
dites réactions complètes ou totales.
En réalité, la majorité des réactions chimiques ne sont pas totales, car elles cessent de
progresser, alors que seule une partie des réactifs a été transformée. Lors de telles
réactions, les réactifs et les produits coexistent en permanence sans que l'on observe une
variation de leur concentration. On définit cet état en disant qu'il y a équilibre chimique.
Les équilibres chimiques 2
3OS
3. Les réactions réversibles
Si on étudie la réaction de l’acide chlorhydrique gazeux (HCl) et du gaz oxygène (O2),
l'expérience montre que, dans un système fermé :
• si on mélange, à chaud, les gaz HCl et O2, il se forme de l'eau et du gaz dichlore (Cl2).
• si on mélange, à chaud, c’est-à-dire dans les mêmes conditions expérimentales que la
réaction précédente, les produits de la réaction précédente H2O et Cl2, il se forme HCl
et O2.
Entre ces quatre corps purs, il peut donc se produire :
1) HCl et O2 donnent Cl2 et HCl : O2(g) + 4 HCl(g) 2 H2O(g) + 2 Cl2(g)
2) Cl2 et H2O donnent HCl et O2 : 2 H2O(g) + 2 Cl2(g) O2(g) + 4 HCl(g)
Autrement dit :
Si on fait réagir de l’acide chlorhydrique avec de l’oxygène, de l’eau et du chlore vont se
former
O2(g) + 4 HCl(g) 2 H2O(g) + 2 Cl2(g) (1)
Puis lorsque l’eau et le chlore seront formés, ils vont réagir ensemble pour former de
l’oxygène et de l’acide chlorhydrique.
2 H2O(g) + 2 Cl2(g) O2(g) + 4 HCl(g) (2)
Dans notre récipient, les deux réactions suivantes auront donc lieu en même temps.
1) O2(g) + 4 HCl(g) 2 H2O(g) + 2 Cl2(g) (1)
2) 2 H2O(g) + 2 Cl2(g) O2(g) + 4 HCl(g) (2)
Comme la réaction 2) est la réaction inverse de la réaction 1) et que les deux réactions ont
lieu dans les mêmes conditions expérimentales, on dit que la réaction est réversible. On
traduit cette réversibilité de la réaction par une double flèche dans l’équation chimique :
O2(g) + 4 HCl(g) 2H2O(g) + 2 Cl2(g) (3)
Remarques:
A) Voilà deux réactions:
2 H2O(l) 2 H2(g) + O2(g) et 2 H2(g) + O2(g) 2 H2O(g)
Ces dernières sont des réactions opposées, mais elles ne NE sont PAS réversibles,
car elles ne peuvent pas avoir lieu simultanément, dans les même conditions
réactionnelles et donc dans le même récipient.
B) Dans l’équation chimique d’une réaction réversible, la réaction représentée par la
flèche allant de gauche à droite , s’appelle la réaction directe. La réaction
représentée par la flèche allant de droite à gauche s’appelle la reaction
inverse.
Les équilibres chimiques 3
3OS
4. L’état d’équilibre
3.1 L’évolution des concentrations lorsqu’il y a un équilibre chimique
Continuons avec notre réaction 3). Puisque la réaction est réversible, les réactifs, ici HCl
et O2 côtoient en permanence les produits, Cl2, H2O et la réaction ne se termine jamais.
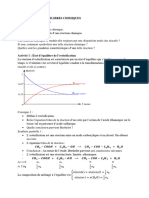
Si on mesure à intervalles réguliers, les concentrations des réactifs et des produits, on
obtient le résultat suivant:
Concentration
0 Temps1
Autrement dit:
Après un certain temps et, théoriquement pour une durée infinie, la réaction cesse
d’évoluer et toutes les concentrations restent constantes.
On dit alors que notre réaction aatteint l’état d’équilibre.
3.2 L’équilibre chimique est un équilibre dynamique
Il est TOTALEMENT FAUX de conclure que, puisque toutes les concentrations sont
constantes, alors les deux réactions se sont arrêtées.
EQUILIBRE = ARRET DU SYSTEME
Pour que les réactions chimiques aient lieu les molécules doivent entrer en collision, puis
échanger leurs atomes.
A l’état d’équilibre, les réactifs et les produits sont tous présents, ils entrent donc en
permanence en collision et échangent donc leur atomes pour former de nouvelles
Les équilibres chimiques 4
3OS
molécules. Les réactions chimiques ont donc toujours lieu. Des concentrations
constantes n’impliquent donc pas un arrêt des réactions.
Des concentrations constantes indiquent que la disparition des réactifs par la réaction
directe (1) se fait simultanément à leur formation par la réaction inverse (2). Idem pour les
produits.
Les deux réactions, la réaction directe (1) et la réaction inverse (2) continuent donc à
l’équilibre, mais elles ont lieu toutes les deux à la même vitesse.
3.3 Système ouvert versus système fermé
Nous avons spécifié au début de notre expérience que nous utilisions un système fermé.
En effet, si notre expérience est effectuée dans un système ouvert, les gaz formés
peuvent s’échapper du système et de ce fait la réaction inverse 2) ne peut plus avoir lieu.
La réaction directe (1) n’est plus réversible et l’état d’équilibre n’est jamais obtenu.
Exemples de systèmes fermés:
Une bonbonne aérosol est un exemple de milieu fermé. Il y a équilibre entre le liquide et le
gaz contenus dans la bonbonne. Si on laisse sortir le gaz en pesant sur la valve, le
système devient ouvert et il n'y a plus équilibre.
Une solution saturée de sucre est un exemple de milieu isolé. Les molécules de sucre ne
peuvent certainement pas quitter la solution
C12H22O11 (s) C12H22O11 (aq)
5. Vitesse de réaction
4.1 Introduction
Certaines réactions chimiques sont instantanées (réactions de précipitation, de
neutralisations, etc.), d'autres sont moins rapides (combustion du charbon, du pétrole dans
l'air), et certaines tellement lentes qu'elles peuvent se dérouler sur plusieurs heures voire
plusieurs jours (oxydation du fer, du cuivre).
D'une façon générale, la vitesse d'une réaction chimique est exprimée par la variation de
la concentration molaire des substances réagissantes par seconde.
var iation de la concentration ∆C mol
v= = =
var iation du temps ∆V l • s
4.2 Quelques facteurs influençant la vitesse de réaction
Chaque réaction s'effectue avec une vitesse qui dépend d'un certain nombre de facteurs
comme par exemple :
• La température :
Dans la majorité des cas la vitesse des réactions augmente avec la température (elle
double à peu près pour une élévation de 10°C). En effet l'agitation moléculaire croît
avec la température et les chocs entre molécules sont plus fréquents et plus violents
ce qui ‘’facilite’’ les réactions.
Les équilibres chimiques 5
3OS
• L'état physique des réactifs :
Le plus souvent une réaction ne pourra avoir lieu que dans un milieu où les molécules
ont un degré de mobilité qui leur permet d'entrer en contact les uns avec les autres :
état gazeux ou liquide.
Pour un réactif à l'état solide, plus la surface de contact avec le réactif gazeux ou
liquide est grande, plus la vitesse de réaction augmente. Tout le monde sait par
expérience qu'un feu s'allume plus rapidement avec des éclats de bois qu'avec des
bûches.
• La concentration
Il est évident que, quelle que soit la nature de la réaction, le nombre de moles
transformées par unité de temps et par unité de volume sera d'autant plus grand que le
nombre de moles de réactifs sera plus élevé.
En d'autres termes, la vitesse de réaction sera proportionnelle à la concentration
molaire.
4.3 Un exemple : La formation d’acide iodhydrique à partir de H2 et I2
Considérons la réaction suivante qui se déroule en milieu homogène gazeux à
température constante :
v1
H2 + I2 2 HI
v2
- On désigne par [H2], [I2], [HI], les concentrations molaires de H2 ; I2 et HI.
V1 est proportionnelle à [H2] et [I2] et donc
v1 = k1•[H2]•[I2]
k1 = constante de proportionnalité, appelée constante de vitesse de la réaction 1.
• k1 dépend de la nature des réactifs et de la température.
V2 est proportionnelle à [HI]••[HI]:
v2 = k2•[HI]•[HI] = k2•[HI]2
4.4 Loi des vitesses de Guldberg et Waage
Guldberg (chimiste et mathématicien norvégien : 1836-1902) et Waage (chimiste
norvégien : 1833-1900) ont généralisé, en 1867, l'influence de la concentration sur la
vitesse d'une réaction chimique par une loi qui s'énonce ainsi :
La vitesse d'une réaction chimique, en milieu homogène, est, à chaque instant,
proportionnelle au produit des concentrations molaires des substances réagissantes;
chaque concentration étant portée à une puissance égale au coefficient de l'équation
équilibrée.
Autrement dit, pour la réaction générale suivante,
v1
aA + bB cC + dD
v2
Les équilibres chimiques 6
3OS
les vitesses de réaction sont exprimées par les équations suivantes :
v1 = k1•[A]a•[B]b
v2 = k2•[C]c•[D]d
[X] = concentration de la substance sans les unités
6. La constante d’équilibre
5.1 La loi d’action de masse
Nous avons vu que l’équilibre chimique ne peut s'expliquer que si la vitesse de
transformation des réactifs en produits est égale à la vitesse de la réaction inverse
qui (re-)transforme les produits en réactifs.
Reprenons l'équation générale avec les équations des vitesses v1 et v2:
v1
aA + bB cC + dD v1 = k1•[A]a•[B]b
v2 v2 = k2•[C]c•[D]d
A l'équilibre on a : v1 = v2 ⇒ k1•[A]a•[B]b = k2•[C]c•[D]d
Cette expression peut être transformée et exprimée en fonction de k1 et k2. Le rapport
k1/k2 donne une nouvelle constante Kc.
k1 [C ]c [ D]d Kc est, pour chaque réaction et pour
= Kc = une température donnée, la constante
k2 [ A]a [ B]b d'équilibre.
Cette relation s’appelle la loi d’action de masse
5.2 Illustration par un exemple
Prenons la réaction suivante :
CO(g) + H2(g) CH4(g) + CO2(g)
But : Calculer la valeur de la constante d’équilibre de cette réaction à 20°C, sachant que
les concentrations à l’équilibre sont:
CO : 4,3 • 10 −6 mol/L CH4 : 5,14 • 10 4 mol/L
H2 : 1,15 • 10 −5 mol/L CO2 : 4,12 • 10 4 mol/L
Etape 1 : Equilibrer l’équation
2 CO(g) + 2 H2(g) CH4(g) + CO2(g)
Les équilibres chimiques 7
3OS
Etape 2 : Ecrire la constante d’équilibre
Kc =
[CH 4 ] • [CO2 ]
[CO]2 • [H 2 ]2
Etape 3 : Calculer la valeur de la constante d’équilibre
5,14 • 10 4 • 4,12 • 10 4
Kc = −6 2 −5 2
= 8,66 • 10 29
(4,3 • 10 ) • (1,15 • 10 )
Remarque : La constante d’équilibre, Kc, a une unité, mais celle-ci étant variable, on ne
l’utilisera pas. L’unité de Kc est [mol/L]x où x est un nombre entier positif ou
négatif.
5.3 Composition du mélange réactionnel à l’équilibre
Chaque réaction réversible possède sa propre constante d’équilibre, dont la valeur ne
change que si la température varie.
Autrement dit,
Pour une température donnée, quelle que soit sa composition initiale, la composition d’un
mélange réactionnel, à l’équilibre, correspondra toujours à la valeur de Kc.
Exemple:
On a préparé plusieurs mélanges de dioxyde de soufre et d’oxygène avec des
compositions initiales différentes.
On a laissé les réactions atteindre l’équilibre, puis on a mesuré toutes les concentrations.
2 SO2 + O2 2 SO3 à 1000 K Kc =
[SO2] mol/L [O2] mol/L [SO3] mol/L Kc
0,66 0,39 0,084
0,038 0,22 0,0036
0,11 0,11 0,0075
0,95 0,88 0,18
1,44 1,98 0,41
Remarques :
a) Habituellement, la valeur de la constante d’équilibre correspondant à l’équation
chimique ayants les coefficients stoechiométriques entiers les plus petits possibles.
Cependant, nous pouvons aussi déterminer la valeur de la constante d’équilibre pour
des multiples de ces coefficients.
Doublons les coefficients stoechiométriques de l’équation suivante:
2 CO(g) + 2 H2(g) CH4(g) + CO2(g)
4 CO(g) + 4 H2(g) 2 CH4(g) + 2 CO2(g)
x2
Les équilibres chimiques 8
3OS
[CH 4 ]2 • [CO2 ]2 = [CH 4 ]• [CO2 ]
2
= K c2
[CO ]4 • [H 2 ]4 [CO]2 • [H 2 ]2
La constante d’équilibre devient: Kc’ =
Si on multiplie les coefficients stoechiométriques par n, il faut élever Ke à la
puissance n.
b) La réaction suivante est réversible.
2 CO(g) + 2 H2(g) CH4(g) + CO2(g)
Le même équilibre peut donc être obtenu en utilisant les produits comme réactifs.
Notre équation devient :
CH4(g) + CO2(g) 2 CO(g) + 2 H2(g)
La constante d’équilibre est : Kc(rev) =
[CO]2 • [H 2 ]2 = 1
[CH 4 ] • [CO2 ] Ke
Les deux constantes d’équilibres sont donc l’inverse l’une de l’autre
7. Les équilibres hétérogènes
Les équilibres qui se produisent dans des systèmes comportant plusieurs phases
s’appellent des équilibres hétérogènes.
Prenons le cas de la dissociation de Ca(OH)2 dans l’eau. Ce dernier n’est que très peu
soluble dans l’eau. Aussi si l’on ajoute suffisamment d’hydroxyde de calcium, un précipité
restera au fond du récipient.
La dissociation/dissolution de l’hydroxyde de sodium se fera selon l’équilibre suivant :
Ca(OH)2(s) Ca2+(aq) + 2 OH-(aq)
[ Ca 2+ ][ OH - ] 2
avec la constante suivante : Kc =
[Ca(OH ) 2 ]
L’expression de la constante d’équilibre fait intervenir la concentration du sel non dissocié.
Le sel non dissocié étant à l’état solide, il est aberrant de parler de concentration. De plus,
seul les molécules à la surface du solide interviennent dans la réaction de dissociation.
Aussi [Ca(OH)2] n’intervient pas dans l’expression de la constante d’équilibre et cette
dernière devient :
Kc = [Ca2+][OH-]2
Ce raisonnement est vrai pour tous les solides et/ou les liquides purs qui apparaissent
dans les équations de réactions réversibles.
Les équilibres chimiques 9
3OS
8. Décoder les valeurs des constantes d’équilibre
La valeur de la constante d’équilibre nous indique si la concentration des produits dans le
mélange réactionnel à l’équilibre sera élevée ou faible.
Cette information nous permet de prévoir si un procédé industriel produira suffisamment
de produits pour être rentable ou non.
Si les concentrations des produits sont élevées à l’équilibre, la valeur du
numérateur de l’expression de la constante, sera grande et donc Kc sera grande.
Kc grande = mélange composé principalement de produits
Si les concentrations des produits sont faibles, à l’équilibre, la valeur du numérateur
de l’expression de la constante, sera petite et donc Kcsera petite.
Kc petite = mélange composé principalement de réactifs
Exemple 1
Réactifs = cases gris clair ; Produits = cases gris foncé
Kc =0,01 Kc = 1 Kc = 100
Exemple 2
H2(g) + Cl2(g) 2 HCl(g) Kc= 4 • 1031
Conclusion : L’équilibre favorise la formation de HCl
Exemple 3
N2(g) + O2(g) 2 NO(g) Kc= 4 • 10 −31
Conclusion : Les espèces prédominantes dans le mélange à l’équilibre sont N2 et O2.
Les équilibres chimiques 10
3OS
ATTENTION :
Ce raisonnement est qualitatif et il a des limites. Si le coefficient stoechiométrique d’un des
réactifs ou des produits est beaucoup plus élevé que celui des autres composants du
mélange à l’équilibre, le raisonnement est faussé.
Ainsi un mélange formé de 1/3 de produit et 2/3 de réactif,
1/ 3 1
- Si tous les coefficients stoechiométriques valent 1 Kc = = = 0.5
2/3 2
1
- Si le coefficient stoechiométrique du réactif vaut 10 Kc = = = 9,8.10-4
210
9. Calcul de la concentration d’un des composants d’un mélange à
l’équilibre
Reprenons la réaction de l’exemple 2 au paragraphe précédent :
H2(g) + Cl2(g) 2 HCl(g) Kc = 4 • 1031
But : Calculer la concentration d’acide chlorhydrique, à l’équilibre, si celle de H2 de 10-17
mol/L et celle de Cl2 de 2 • 10 −16 mol/L.
Exprimons Ke : Kc =
[HCl ]2 = x2
= 4 • 1031
[H 2 ] • [Cl2 ] 10 • 2 • 10
−17 −16
Nous devons donc résoudre une équation à une inconnue :
x2= 4 • 1031 • 2 • 10 −16 • 10-17
x = 8 • 10-2 ≅ 0,28 mol/L
Réponse : [HCl] = 0,28 mol/L
10. Déterminer les concentrations des composants d’un mélange à
l’équilibre à partir de la composition initiale
La constante d’équilibre peut être utilisée pour calculer la composition du mélange
réactionnel, à l’équilibre, à partir de n’importe quelle composition initiale.
But : Calculer la concentration de tous les composants du mélange à l’équilibre.
L’idée de base : La variation des concentrations du mélange est liée à la stoechiométrie
de la réaction.
Outil : Un tableau d’équilibre indiquant
- la composition initiale du mélange,
- les variations nécessaires pour atteindre d’équilibre,
- la composition à l’équilibre.
Les équilibres chimiques 11
3OS
La réaction:
Prenons la réaction de décomposition du pentachlorure de phosphore. La réaction a lieu
dans un réacteur de 500 ml à 250°C avec 1,5 mol de pentachlorure de phosphore.
PCl5(g) PCl3(g) + Cl2(g) Kc= 1,8
Marche à suivre
A) Calculons la concentration initiale de PCl5 : [PCl5] = 1,5/0,5= 3 mol/L 500 mL = 0,5 L
B) Remplissons le tableau d’équilibre
[PCl5] [PCl3] [Cl2]
mol/L mol/L mol/L
Mélange initial 3 0 0 Il n’y a pas de produit de réaction
x = variation de [PCl5]
Variation des concentrations -x +x +x
pour atteindre l’équilibre 1 mol PCl5 =1 mol PCl3
= 1 mol Cl2
Concentrations à l’équilibre 3-x +x +x
C) Posons Kc avec les concentrations à l’équilibre :
Kc =
[PCl3 ] • [Cl2 ] =
x2
= 1,8
[PCl5 ] 3− x
x2= 1,8 • (3 - x)= 5,4 – 1.8x
x2 + 1.8x - 5,4 = 0
D) Résolvons l’équation du second degré à une inconnue :
− 1.8 ± 1.8 2 − 4 • 1 • (− 5,4 )
x1,x2 = x1= 1,59 x2= -3.39
2
[…] > 0 x2 = impossible
x1 = x = 1,59 mol/L = [PCl3] = [Cl2]
E) Calculons la concentration du réactif à l’équilibre
[PCl5] = 3 – 1,59 = 1,41 mol/L
F) Réponses : [PCl3] = [Cl2] =1,59 mol/L [PCl5] = 1,41 mol/L
Les équilibres chimiques 12
3OS
11. Le quotient réactionnel Q
11.1 L’expression et l’utilisation du quotient Q
Si on prépare un mélange réactionnel contenant à la fois les réactifs et les produits d’une
réaction chimique donnée, il est possible de déterminer dans quel sens (consommation
des réactifs par exemple) va se déplacer la réaction pour atteindre l’équilibre.
Lorsque la concentration de l’un des réactifs ou produits est nulle, le système se déplacera
dans la direction qui permet la formation du composé manquant. Cependant, lorsque
toutes les concentrations initiales ne sont pas nulles, il est plus difficile de savoir dans quel
sens se déplacera la réaction pour atteindre l’équilibre.
Pour résoudre ce problème, on a recours au quotient réactionnel Q.
concentration des produits
Q=
concentration des réactifs
L’expression du quotient Q est la même que celle de la constante d’équilibre.
concentrations à N ' IMPORTE QUEL MOMENT DE LA REACTION des produits
Q=
concentrations à N ' IMPORTE QUEL MOMENT DE LA REACTION des réactifs
≠
concentrations A L' EQUILIBRE UNIQUEMENT des produits
Kc =
concentrations A L' EQUILIBRE UNIQUEMENT des réactifs
Cependant les concentrations utilisées pour calculer Q sont les concentrations à
n’importe quel moment de la réaction, alors que Kc est calculée en utilisant les
concentrations à l’équilibre uniquement.
11.2 L’interprétation de la valeur de Q
Trois cas peuvent se présenter :
I) Q = Kc Le système est à l’équilibre ; il n’y a aucun déplacement.
II) Q > Kc
Le rapport entre les concentrations initiales des
produits et les concentrations initiales des réactifs
est trop élevé. Pour atteindre l’équilibre, il doit y
avoir une transformation des produits en réactifs.
La réaction évoluera de droite à gauche (réaction
inverse favorisée) pour atteindre l’équilibre.
III) Q < Kc
Le rapport entre les concentrations initiales des
produits et les concentrations initiales des réactifs
est trop faible.
Les équilibres chimiques 13
3OS
Pour atteindre l’équilibre, il doit y avoir une transformation des réactifs en produits.
La réaction évoluera de gauche à droite (réaction directe favorisée) pour atteindre
l’équilibre.
11.3 Illustration par un exemple
Le monoxyde de carbone réagit avec la vapeur d’eau pour produire du dioxyde de
carbone et du gaz hydrogène selon l’équilibre suivant :
CO(g) + H2O(g) CO2(g) + H2(g)
A 700 °K, la constante d’équilibre vaut 5,1.
But : Calculer les concentrations à l’équilibre de toutes les espèces lorsqu’on mélange,
dans un ballon de 1 litre, 0,5 mole de CO et 0,5 mole H2O avec 2 moles de CO2 et 2
moles de H2.
A) Calcul de Q :
2•2
Q= = 16
0 .5 • 0 .5
B) Comparaison de Q et Kc :
Q > Kc Conclusion : La réaction évoluera de droite à gauche
C) Remplissage du tableau d’équilibre
[CO] [H2O] [CO2] [H2]
mol/L mol/L mol/L mol/L
Mélange initial 0.5 0.5 2 2
Variation des concentrations Les produits sont
+x +x -x -x consommés -x
pour atteindre l’équilibre
Concentrations à l’équilibre 0.5 + x 0.5 + x 2-x 2 -x
D) Posons Kc avec les concentrations à l’équilibre :
Kc =
[CO2 ] • [H 2 ] =
(2 − x) 2
= 5.1
[CO] • [ H 2O] (0.5 + x) 2
E) Résolution de l’équation et calcul des concentrations comme décrit dans le §9.
12. Les facteurs influençant l'équilibre d'une réaction (Principe de Le
Châtelier)
12.1 Introduction
Considérons la réaction réversible suivante :
v1
A + B C + D
v2
Les équilibres chimiques 14
3OS
On a vu que l'équilibre est atteint lorsque v1 = v2.
• Nous dirons que l’équilibre est déplacé vers la droite lorsque, pour une raison
quelconque, v1 devient plus grand que v2, c’est-à-dire que la réaction directe est
favorisée par rapport à la réaction inverse, et donc que les concentrations des
produits C et D, augmentent.
• Inversement, nous dirons que l’équilibre est déplacé vers la gauche lorsque, pour
une raison quelconque, v2 devient plus grand que v1, c’est-à-dire que la réaction
inverse est favorisée par rapport à la réaction directe, et donc que les concentrations
des réactifs A et B, augmentent.
Dans les deux cas, l’état d’équilibre initial est rompu et le système cherche à atteindre un
nouvel état d’équilibre.
Les facteurs pouvant modifier les vitesses de réaction vont donc également avoir un
impact sur l'état d'équilibre !
ATTENTION !
La constante d’équilibre sera toujours la même après modification des vitesses.
Autrement dit, le rapport entre les concentrations des réactifs et des produits de l’état
équilibre initial, sera le même que celui du nouvel état d’équilibre.
Seules les valeurs des concentrations auront varié !
Pour une réaction donnée, ces facteurs sont la variation de:
a) la concentration ou de la pression pour les gaz.
b) la température.
c) la surface de contact
d) la catalyse
12.2 Le principe de Le Châtelier
En 1884, le chimiste français Henry le Châtelier énonça un principe général qui permet
de prévoir le sens de déplacement d’un équilibre lorsque l’on modifie un de ces facteurs.
« Un système, soumis à une modification d’un des facteurs régissant son équilibre, évolue
vers un nouvel état d’équilibre, dans le sens qui tend à s’opposer à cette
modification. »
Remarque : Le principe de Le Châtelier ne fait que suggérer le sens du déplacement de
l’équilibre ; il ne fournit pas d’explication ni ne permet des prévisions
quantitatives.
Les équilibres chimiques 15
3OS
12.3 Quelques-uns des facteurs pouvant modifier l'état d'équilibre.
12.3.1 La concentration
Lorsque la concentration de l'une des substances d'un système à l'équilibre varie, le
système réagit de façon à s’opposer à la modification de la concentration de cette
substance.
Exemple : Supposons le système fermé à l’équilibre suivant :
(1)
N2(g) + 3 H2(g) 2 NH3(g) Kc =
(2)
• Si on augmente la concentration de dihydrogène gazeux, le système va favoriser la
formation d’ammoniac, c’est-à-dire la réaction directe (la réaction 1) de manière à
diminuer la concentration d’hydrogène et cela jusqu’à ce qu’il atteigne un nouvel
état d’équilibre. La réaction directe étant favorisée, on dit que l’équilibre est déplacé
à droite.
• Si au contraire, on diminue la concentration d’hydrogène, l’équilibre sera déplacé à
la gauche de façon à augmenter la concentration de dihydrogène.
Remarque
L’explication est simple, puisque la constante d’équilibre n’est pas modifiée, si on
change la valeur du dénominateur de la constante d’équilibre en modifiant par exemple la
concentration d’hydrogène, le système réagit dans un sens tel que Kc reste constante.
Application
Ce principe permet de faire tendre une réaction réversible vers une réaction irréversible
(ou complète).
Un bon moyen de s’assurer qu’une réaction continue à produire une substance, consiste à
enlever un des produits au fur et à mesure qu’il se forme.
Dans le cas de la synthèse du méthanoate d’éthyle par estérification, la température
d’ébullition de ce dernier est inférieure à tous les autres composés du mélange
réactionnel. En effectuant une distillation continue de l’ester, l’équilibre est poussé à droite
et la formation de l’ester est favorisée.
L’équilibre est donc
constamment déplacé vers la
formation de l’ester ce qui rend
la réaction complète.
Les équilibres chimiques 16
3OS
12.3.2 La pression (dans un système fermé)
Augmenter la pression pour un gaz, peut être mis en parallèle à une augmentation de la
concentration. Si la pression monte, le système réagira de façon à diminuer la
concentration des molécules.
Exemple : Prenons l’équilibre de la synthèse de l’ammoniac
(1)
N2(g) + 3H2(g) 2NH3(g) Kc =
(2)
1 mole 3 moles 2 moles
On remarque que :
• Dans le sens (1) (formation de NH3), la réaction entre N2 et H2 conduit à la
diminution du nombre de molécules gazeuses (on passe de 4 moles à 2 moles) et,
par conséquent, pour un récipient à un volume constant, à la diminution de la
pression du mélange réactionnel.
• A l’inverse la réaction (2) produit un plus grand nombre de molécules gazeuses et
ainsi une augmentation de la pression du mélange.
Dans le cas d’une augmentation de la pression (compression) du mélange
réactionnel, l’équilibre va être déplacé vers la droite, afin de réduire la
pression en diminuant le nombre de molécules.
Un déplacement de l’équilibre en sens inverse sera provoqué par une
diminution pression (dilatation).
Les équilibres chimiques 17
3OS
12.3.3 La température
La variation de la température est le facteur entraînant une modification de la valeur
de la constante d'équilibre, car Ke est fonction de la température.
Il y a 2 types de réactions au cours desquelles la température varie :
• Une réaction exothermique est une réaction au cours de laquelle on assiste à un
dégagement de chaleur.
Exemple : H2 + ½ O2 → H2O ∆H = -286 kJ
∆H = -286 kJ: L’énergie du système à diminué de 286 kJ d’où le signe
négatif. Cette énergie est dégagée par le système sous forme
de chaleur.
• Une réaction endothermique est une réaction au cours de laquelle il faut fournir
de la chaleur pour que la réaction ait lieu.
Exemple : H2O → H2 + ½ O2 ∆H = +286 kJ
• Dans le cas d’une réaction réversible, une réaction exothermique dans un
sens est endothermique dans l’autre sens.
Dans un système à l'équilibre, la chaleur dégagée par une réaction, est absorbée par la
réaction en sens inverse.
• Ainsi, si la température du système augmente, celui-ci va s'opposer à ce
changement en absorbant la chaleur : on favorise la réaction endothermique.
• A l'inverse, on favorise la réaction exothermique en diminuant la température.
Exemple : la synthèse de l’ammoniac
N2(g) + 3 H2(g) 2 NH3(g) ∆H = -22 kcal
Un ∆H négatif indique que la réaction directe est exothermique et donc que la
réaction inverse est endothermique.
Les équilibres chimiques 18
3OS
Par conséquent, une augmentation de la température favorisera la décomposition
de NH3 et un abaissement de température favorisera la production NH3.
12.3.4 La catalyse
Un catalyseur est une substance qui augmente la vitesse d’une réaction chimique. Le
catalyseur n’est pas consommé lors de la réaction.
La réaction de formation d’alcools primaires part hydrogénation des aldéhydes est une
réaction catalytique où le catalyseur est le nickel.
Les réactions chimiques ayant lieu dans le corps humain sont presque toutes des
réactions catalytiques. Les catalyseurs sont les enzymes.
Dans le cas de réaction réversible, le catalyseur accélère la vitesse à laquelle la réaction
atteint l’équilibre, mais il n’influence pas la composition de l’équilibre.
Au niveau moléculaire, nous pouvons considérer que le catalyseur accélère de la même
façon la réaction directe et la réaction inverse. Par conséquent, l’équilibre dynamique n’est
pas modifié.
Les équilibres chimiques 19
Vous aimerez peut-être aussi
- GeoradarDocument41 pagesGeoradargeonourePas encore d'évaluation
- Processus irréversibles non linéaires en thermodynamique: Les Grands Articles d'UniversalisD'EverandProcessus irréversibles non linéaires en thermodynamique: Les Grands Articles d'UniversalisPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- ZZZ Suppexos Me3 Me4 Energetique-3Document10 pagesZZZ Suppexos Me3 Me4 Energetique-3Maryam MaryamPas encore d'évaluation
- CinetiqueDocument50 pagesCinetiquesidi mohamed el amine nekkalPas encore d'évaluation
- Fiche Smart Grids PDFDocument5 pagesFiche Smart Grids PDFthe.diable.tristrePas encore d'évaluation
- Compensation de L'énergie RéactiveDocument1 pageCompensation de L'énergie RéactiveSarahSaidiPas encore d'évaluation
- Cours 13 Équilibres ChimiquesDocument4 pagesCours 13 Équilibres ChimiquesArti80% (5)
- Réactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Document63 pagesRéactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Oumayma IkhlefPas encore d'évaluation
- TP EquilibrechimiqueDocument8 pagesTP Equilibrechimiquecherazer67% (3)
- ch2 - Transformation Chimique Dun Systã Me - complétéDocument24 pagesch2 - Transformation Chimique Dun Systã Me - complétéd.xw.wx3Pas encore d'évaluation
- Les Equilibres ChimiquesDocument7 pagesLes Equilibres Chimiquesdembamamadou274Pas encore d'évaluation
- CR Equilibre ChimiqueDocument3 pagesCR Equilibre Chimiquemohamed mohPas encore d'évaluation
- Transformation Chimiquebilan de MatièreDocument3 pagesTransformation Chimiquebilan de MatièreKamal LaourdaniPas encore d'évaluation
- Chapitre 3 Equilibres Chimiques 3ème Génie Des ProcédésDocument23 pagesChapitre 3 Equilibres Chimiques 3ème Génie Des ProcédésCherif LaifaPas encore d'évaluation
- CM CHI 201 - 2022 Royal Partie 1Document53 pagesCM CHI 201 - 2022 Royal Partie 1Vera Legba-MonyPas encore d'évaluation
- Résumé Équilibre ChimiqueDocument4 pagesRésumé Équilibre ChimiqueMehdi BnmssdPas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Document2 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Fatima Zahrae El BouhmidiPas encore d'évaluation
- 06 Evolution Spontanee D Un Systeme ChimiqueDocument7 pages06 Evolution Spontanee D Un Systeme ChimiqueElec FoPas encore d'évaluation
- 5e Chimie Chapitre 7corrigéDocument24 pages5e Chimie Chapitre 7corrigéFolake AgardPas encore d'évaluation
- Cours Chimie II 1ère SNV v2 PDFDocument38 pagesCours Chimie II 1ère SNV v2 PDFSamsouma BkPas encore d'évaluation
- Cinetique Chimique (PR Belaribi)Document17 pagesCinetique Chimique (PR Belaribi)Zidani LinaPas encore d'évaluation
- Rappels Cinetique ChimiqueDocument22 pagesRappels Cinetique ChimiqueSaid Soilihi ZayadPas encore d'évaluation
- 2 5 A Term-Enthalpie Libre StandardDocument7 pages2 5 A Term-Enthalpie Libre StandardoumaroumarietouPas encore d'évaluation
- Equilibre Chimique, Word 1Document2 pagesEquilibre Chimique, Word 1Lourdes Gerges0% (1)
- Cinétique ChimiqueDocument10 pagesCinétique Chimiquearfpower100% (2)
- Evolution SpontanéeDocument3 pagesEvolution SpontanéeNoury AbkPas encore d'évaluation
- 1 Cours DescriptionDunSystemeFermeEnTransformationChimiqueCours VFDocument2 pages1 Cours DescriptionDunSystemeFermeEnTransformationChimiqueCours VFMed RhaiouzPas encore d'évaluation
- Chapitre 1 CS ENSA 2021Document26 pagesChapitre 1 CS ENSA 20213freefire 3gamePas encore d'évaluation
- Chapitre I. Généralités Et DéfinitionsDocument8 pagesChapitre I. Généralités Et DéfinitionsOum NiaPas encore d'évaluation
- Cours SM4001 PDFDocument105 pagesCours SM4001 PDFbentouamiPas encore d'évaluation
- Chapitre 9Document17 pagesChapitre 9Belinda DancheuPas encore d'évaluation
- Chp. Transformation ChimiqueDocument5 pagesChp. Transformation ChimiqueyvancharlesmendoumeessengPas encore d'évaluation
- Cinétique ChimiqueDocument7 pagesCinétique ChimiquehajPas encore d'évaluation
- Equilibre ChimiqueDocument7 pagesEquilibre ChimiquecherazerPas encore d'évaluation
- Chapitre 2Document4 pagesChapitre 2Moustapha Bassirou NianePas encore d'évaluation
- CHAPITRE 1 Partie 2Document14 pagesCHAPITRE 1 Partie 2hamid ibbakhPas encore d'évaluation
- Calcul Des Reacteurs Chimiques HomogeneDocument16 pagesCalcul Des Reacteurs Chimiques HomogeneجعدبندرهمPas encore d'évaluation
- II 04 CinetiqueDocument3 pagesII 04 CinetiqueMohamed ElouakilPas encore d'évaluation
- 1 Equilibres ChimiquesDocument6 pages1 Equilibres ChimiquesMira MslPas encore d'évaluation
- Suivi Temporel D'une Transformation ChimiqueDocument10 pagesSuivi Temporel D'une Transformation ChimiqueMhamed LaihemPas encore d'évaluation
- La Cinétique ChimiqueDocument7 pagesLa Cinétique ChimiqueAS asPas encore d'évaluation
- Description D'un Système Chimique en Réaction (1029)Document6 pagesDescription D'un Système Chimique en Réaction (1029)AxellePas encore d'évaluation
- Avancement D Une Reaction ChimiqueDocument4 pagesAvancement D Une Reaction ChimiqueFitouri MoncefPas encore d'évaluation
- Https0330088s.index Education - netpronoteFichiersExternes8aDocument7 pagesHttps0330088s.index Education - netpronoteFichiersExternes8athomasPas encore d'évaluation
- Avancement Dune RéactionDocument4 pagesAvancement Dune RéactionFanomezana RakotomalalaPas encore d'évaluation
- Equilibre ChimiqueDocument13 pagesEquilibre ChimiquememtolombernaPas encore d'évaluation
- GFTHKFDocument101 pagesGFTHKFFedoua BenamerPas encore d'évaluation
- Chapitre 04Document7 pagesChapitre 04الغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- 1 Cinétique ChimiqueDocument12 pages1 Cinétique ChimiqueYoucef KrPas encore d'évaluation
- 2022 Tle Spã© Chapitre 14 Cinétique ChimiqueDocument6 pages2022 Tle Spã© Chapitre 14 Cinétique Chimiquemavrinissue4Pas encore d'évaluation
- SN2-Chapitre 04 H2024Document40 pagesSN2-Chapitre 04 H2024alyssiamorrissette7Pas encore d'évaluation
- Chimie Corrige ch7 Partie1Document2 pagesChimie Corrige ch7 Partie1api-278378684100% (2)
- Les Réacteurs Idéaux Homogènes (Partie 2)Document16 pagesLes Réacteurs Idéaux Homogènes (Partie 2)OùSsàmà EL MàsmoùdiPas encore d'évaluation
- Chapitre 1 Cours Cinétique - 2021Document40 pagesChapitre 1 Cours Cinétique - 2021Li NaPas encore d'évaluation
- Chap 2 Rappel de Cinétique Chimique Stœchiométrie Et Notion D'avancementDocument14 pagesChap 2 Rappel de Cinétique Chimique Stœchiométrie Et Notion D'avancementAPas encore d'évaluation
- Prépa 2 - HamidiDocument8 pagesPrépa 2 - Hamidifatima chtoukiPas encore d'évaluation
- Cours À Recopier 05Document2 pagesCours À Recopier 05jean valjeanPas encore d'évaluation
- Chimie AnalytiqueDocument90 pagesChimie Analytiqueismaelsienou7Pas encore d'évaluation
- Cours CinetiqueDocument12 pagesCours CinetiqueArthur TigreatPas encore d'évaluation
- Solutions Et Expression de ConcentrationDocument11 pagesSolutions Et Expression de ConcentrationNicoleta ChivuPas encore d'évaluation
- Chap 01-Cinétique-Durée-RéactionDocument5 pagesChap 01-Cinétique-Durée-Réactionmube 75Pas encore d'évaluation
- Activité D'apprentissage Du Principe de Le Chatelier - Document D'étudeDocument5 pagesActivité D'apprentissage Du Principe de Le Chatelier - Document D'étudeRayan AllachePas encore d'évaluation
- 2023A - GCH2525 - Thermodynamique II - Chapitre 04 - Equilibre Thermo (Partie I)Document23 pages2023A - GCH2525 - Thermodynamique II - Chapitre 04 - Equilibre Thermo (Partie I)Rim Ben othmanPas encore d'évaluation
- Rapporte 1 Ayoub BakhtiDocument24 pagesRapporte 1 Ayoub BakhtiAyoub BakhtiPas encore d'évaluation
- Pollution Du Sol Assia YamounDocument92 pagesPollution Du Sol Assia YamounYamounAssia100% (4)
- Etude D'impact Sur L'environnementDocument13 pagesEtude D'impact Sur L'environnementmohammed amine qaouriPas encore d'évaluation
- TD #01 Limites de La Théorie ClassiqueDocument2 pagesTD #01 Limites de La Théorie Classiquemahfoud1254Pas encore d'évaluation
- AAASession 13 - CamerounDocument32 pagesAAASession 13 - CamerounDaniel Ndob boum100% (1)
- Rockwool Catalogue Solutions Isolation Bâtiment 2011Document200 pagesRockwool Catalogue Solutions Isolation Bâtiment 2011Hervé AngPas encore d'évaluation
- Article Carbone Jatropha 2014Document21 pagesArticle Carbone Jatropha 2014Gouhoungou RogatienPas encore d'évaluation
- Programmes FASA Avec Descriptifs Final Final XXXDocument185 pagesProgrammes FASA Avec Descriptifs Final Final XXXN LislaurePas encore d'évaluation
- Correction de Lexercice 3 de La Série 1Document10 pagesCorrection de Lexercice 3 de La Série 1medmm200430Pas encore d'évaluation
- Rapport Finale Boubaker 2020Document38 pagesRapport Finale Boubaker 2020Mohamed LamraniPas encore d'évaluation
- Corrosion Des Metaux M1Document18 pagesCorrosion Des Metaux M1Lkl HadjerPas encore d'évaluation
- Chapitre 1 Géologie Minière (L3 Valo)Document6 pagesChapitre 1 Géologie Minière (L3 Valo)Blanckoo BlanckooPas encore d'évaluation
- Human GeographyDocument2 pagesHuman GeographySimple IdeaPas encore d'évaluation
- TP17 PileHydrogene2018Document4 pagesTP17 PileHydrogene2018physalpPas encore d'évaluation
- Universite Kasdi MerbahDocument5 pagesUniversite Kasdi MerbahKaouachi Ahmed LouayPas encore d'évaluation
- GEI Physique 2021Document8 pagesGEI Physique 2021qzc4sstkgxPas encore d'évaluation
- THERMODYNAMIQUE II Chapitres FondamentauxDocument262 pagesTHERMODYNAMIQUE II Chapitres FondamentauxDavi Nordel NgondzaPas encore d'évaluation
- GBEE-2013-JPTshibangu QUALITE DE TIRDocument39 pagesGBEE-2013-JPTshibangu QUALITE DE TIRAbdelali Ait bendraPas encore d'évaluation
- These Nouacer Sana PDFDocument143 pagesThese Nouacer Sana PDFSoussou PerlaPas encore d'évaluation
- BLANC - PUGHE - CHARTHIER - Littérature Et Écologie - Vers Une Écopoétique PDFDocument12 pagesBLANC - PUGHE - CHARTHIER - Littérature Et Écologie - Vers Une Écopoétique PDFMarcelo SpitznerPas encore d'évaluation
- Historique de EddDocument17 pagesHistorique de EddChaima MarzoukPas encore d'évaluation
- HOUSSAMATOU - DOUDOUA Ligne PDFDocument93 pagesHOUSSAMATOU - DOUDOUA Ligne PDFAlassane KeitaPas encore d'évaluation
- m14 Systeme ThermiqueDocument3 pagesm14 Systeme ThermiqueMohamed LaribiPas encore d'évaluation
- 3 HakkouDocument8 pages3 HakkouMahaPas encore d'évaluation