Académique Documents
Professionnel Documents
Culture Documents
ch2 - Transformation Chimique Dun Systã Me - complété
Transféré par
d.xw.wx3Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
ch2 - Transformation Chimique Dun Systã Me - complété
Transféré par
d.xw.wx3Droits d'auteur :
Formats disponibles
Transformations de la matière
CH2. TRANSFORMATION CHIMIQUE
D’UN SYSTÈME
OBJECTIFS
Notions et contenus Capacités exigibles
Transformation chimique d’un système
Modélisation d’une transformation par une ou • Écrire l’équation de la réaction (ou des réactions) qui
plusieurs réactions chimiques. modélise(nt) une transformation chimique donnée.
Équation de réaction ; constante thermodynamique • Déterminer une constante thermodynamique
d’équilibre. d’équilibre et tester l’influence de différents
paramètres sur l’état d’équilibre d’un système.
Évolution d’un système lors d’une transformation • Décrire qualitativement et quantitativement un système
chimique modélisée par une seule réaction chimique dans l’état initial ou dans un état
chimique : avancement, activité, quotient de réaction, d’avancement quelconque.
critère d’évolution. • Exprimer l’activité d’une espèce chimique pure ou
dans un mélange dans le cas de solutions aqueuses très
diluées ou de mélanges de gaz parfaits avec référence à
l’état standard.
• Exprimer le quotient de réaction.
• Prévoir le sens de l’évolution spontanée d’un système
chimique.
Composition chimique du système dans l’état final : • Identifier un état d’équilibre chimique.
état d’équilibre chimique, transformation totale. • Déterminer la composition chimique du système dans
l’état final, en distinguant les cas d’équilibre chimique
et de transformation totale, pour une transformation
modélisée par une réaction chimique unique.
Dans le cas le plus général, dans un système physico-chimique évoluant entre un état donné et
un état différent, la variation de la quantité de matière d’une espèce physico-chimique Bi est
due à la fois :
- aux échanges de l’espèce Bi avec le milieu extérieur, à travers la surface Σ séparant
le système avec le milieu extérieur ;
- à la transformation chimique se déroulant à l’intérieur du système.
Si le système est fermé, il n’y a pas d’échange de matière entre le système et le milieu
extérieur : les variations de quantité de matière des espèces physico-chimiques sont alors
uniquement dues à la transformation chimique.
Dans la suite de ce chapitre, on se limite à l’étude de systèmes physico-chimiques
FERMÉS.
Autrement dit, les variations de quantités de matière des différentes espèces
physico-chimiques ne sont dues qu’à la transformation chimique se déroulant à l’intérieur du
système.
C. de Saint-Aubin PCSI3 2023-2024 1/24
Transformations de la matière
I. MODÉLISATION D’UNE TRANSFORMATION PAR UNE OU
PLUSIEURS RÉACTIONS CHIMIQUES
A. TRANSFORMATION CHIMIQUE
On rappelle qu’un système siège d’une transformation chimique voit la réorganisation des
atomes des espèces chimiques qui le constituent : certaines liaisons entre atomes se rompent,
d’autres liaisons entre atomes se forment. Il peut aussi y avoir des échanges d’électrons.
Autrement dit :
Une transformation chimique est une transformation d’un système physico-chimique au
cours de laquelle des espèces physico-chimiques sont modifiées.
exemple :
B. RÉACTION CHIMIQUE
Une transformation chimique peut être modélisée par une ou plusieurs réactions chimiques.
Une réaction chimique est un MODÈLE pour rendre compte, au niveau macroscopique,
d’une partie ou de l’ensemble d’une transformation chimique.
exemple :
Une même réaction chimique peut modéliser plusieurs transformations chimiques différentes.
exemple :
C. ÉQUATION DE RÉACTION
Une équation de réaction donne une écriture symbolique d’une réaction chimique.
C. de Saint-Aubin PCSI3 2023-2024 2/24
Transformations de la matière
Elle donne donc des informations au niveau macroscopique, mais rien au niveau
microscopique.
Elle se représente de manière très générale par :
0= 𝜈𝑖 𝐵𝑖
𝑖
où = montre bien qu’on a à faire à une équation
𝐵𝑖 représente soit l’espèce physico-chimique Bi
(lorsque l’on se focalise sur la nature de cette espèce)
soit une mole de cette espèce
(lorsque l’on se focalise sur les proportions en quantité de matière des
espèces intervenant dans l’équation i.e. sur la stœchiométrie*) ;
𝜈𝑖 est le NOMBRE stœchiométrique de Bi dans cette équation
est une grandeur ALGÉBRIQUE
est une grandeur adimensionnée (et donc sans unité).
S’il est positif, Bi est appelé produit,
s’il est négatif, Bi est appelé réactif.
* la stœchiométrie est l’étude des relations de proportionnalité qui existent entre les quantités
de matière des espèces intervenant dans la transformation chimique.
1 1
exemple : H2 (g) + O2 (g) = H2O(g) peut s’écrire 0 = – H2 (g) – O2 (g) + H2O(g)
2 2
1
on a donc : H 2O( g ) = + 1 ; H2( g ) = – 1 et O2( g ) = – .
2
Lorsque les nombres stœchiométriques sont ajustés,
la conservation des atomes
et
la conservation de la charge électrique
sont réalisées de part et d’autre du signe =.
exemple : Na(s) + H2O(l) = Na+(aq) + HO-(aq) + ½ H2 (g).
Remarques :
- lorsque le nombre stœchiométrique vaut 1 ou -1, on ne l’écrit pas dans l’équation
- le système peut contenir des espèces ne participant pas à la transformation chimique :
ces espèces sont appelées espèces spectatrices.
A priori, rien n’impose les valeurs des nombres stœchiométriques lorsqu’on écrit la réaction.
exemple : on peut aussi bien écrire 2 H2 (g) + O2 (g) = 2 H2O(g)
1
que H2 (g) + O2 (g) = H2O(g).
2
C. de Saint-Aubin PCSI3 2023-2024 3/24
Transformations de la matière
D. CONSTANTE THERMODYNAMIQUE D’ÉQUILIBRE
Système
Soit un système physico-chimique fermé à la température 𝑇.
Hypothèse réactionnelle
Supposons que ce système soit soumis à une transformation chimique modélisée par une seule
réaction chimique d’équation (1) suivante :
0= 𝜈𝑖 𝐵𝑖 (1)
𝑖
avec i nombre stœchiométrique algébrique de l’espèce physico-chimique Bi dans
l’équation (1).
Constante thermodynamique d’équilibre à 𝑻
À la réaction symbolisée par l’équation (𝟏), on associe un nombre strictement positif,
noté 𝐾°, appelé constante thermodynamique d’équilibre ou constante d’équilibre,
dépendant uniquement de la température 𝑻.
exemple : à la température 𝑇, la transformation d’une espèce A(g) en B(g) peut être modélisée
par la réaction unique suivante
d’équation (1) : A=B (1) 𝐾°1
ou d’équation (2) : 3A=3B (2) 𝐾°2
On montre (à l’aide de la RGW, cf. plus loin) que :
𝐾°2 = (𝐾°1 )3 à 𝑇
autrement dit 𝐾°2 ≠ 𝐾°1 à𝑇
la valeur à 𝑇 de la constante d’équilibre associée à une réaction dépend de l’équation
choisie pour symboliser cette réaction.
À la température 𝑇, la constante thermodynamique d’équilibre 𝐾°(𝑇) associée à (1) est
calculable à partir de données tabulées dans les tables thermodynamiques (cf. cours de
deuxième année).
exemple :
C. de Saint-Aubin PCSI3 2023-2024 4/24
Transformations de la matière
II. GRANDEURS DESCRIPTIVES DE L’ÉTAT D’UN SYSTÈME
PHYSICO-CHIMIQUE SOUMIS À UNE TRANSFORMATION
CHIMIQUE MODÉLISÉE PAR UNE SEULE RÉACTION
A. AVANCEMENT DE RÉACTION ASSOCIÉ À L’ÉTAT DU SYSTÈME
1. Exemple
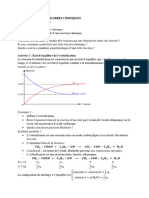
On étudie un système fermé dans lequel la formation d’eau gazeuse à partir de dihydrogène
gazeux et de dioxygène gazeux est modélisée par l’unique réaction d’équation suivante :
2 H2(g) + O2(g) = 2 H2O(g).
À l’état initial EI du système, l’expérimentateur décide d’introduire dans le système 𝑛𝐻2,0 mol
de dihydrogène gazeux, 𝑛𝑂2,0 mol de dioxygène gazeux et 𝑛𝐻2 𝑂,0 mol d’eau gazeuse.
1. Donner les quantités des espèces présentes dans le système lorsque 2 mol de
dihydrogène ont été consommées (état 1) ?
2. lorsque 1 mol de dihydrogène a été consommée (état 2) ?
3. lorsque 3 mol dihydrogène ont été consommées (état 3) ?
∆𝑛
4. Pour chacun de ces trois états, comparer les 𝜈 𝑖 des trois espèces physico-chimiques
𝑖
présentes.
2 H2 (g) + O2 (g) = 2 H2O(g)
𝒏 (EI) 𝑛𝐻2,0 𝑛𝑂2,0 𝑛𝐻2 𝑂,0
(mol)
𝒏 (E) 𝑛𝐻2 𝑛𝑂2 𝑛𝐻2 𝑂
(mol) = 𝑛𝐻2,0 + ∆𝑛𝐻2 = 𝑛𝑂2,0 + ∆𝑛𝑂2 = 𝑛𝐻2 𝑂,0 + ∆𝑛𝐻2 𝑂
𝑛 (E1)
(mol)
𝑛 (E2)
(mol)
𝑛 (E3)
(mol)
où E représente un état quelconque du système
et ∆𝑛 = 𝑛(𝐸∀) − 𝑛(𝐸𝐼)
car l’opérateur représente la différence entre une grandeur dans son état
final et celle dans son état initial.
Les variations de quantités de matière des espèces intervenant dans la réaction ne sont pas
indépendantes mais liées par la stœchiométrie de la réaction, et uniquement par celle-ci
lorsque le système est fermé.
C. de Saint-Aubin PCSI3 2023-2024 5/24
Transformations de la matière
2. Avancement de réaction associé à l’état du système
Système
Soit un système physico-chimique fermé à la température 𝑇.
Hypothèse réactionnelle
Supposons que ce système soit soumis à une transformation chimique modélisée par une seule
réaction chimique d’équation (1) suivante :
0= 𝜈𝑖 𝐵𝑖 (1)
𝑖
avec i nombre stœchiométrique algébrique de l’espèce physico-chimique Bi dans
l’équation (1).
Avancement
Entre l’état initial EI et un état quelconque E du système, on a pour tout constituant Bi :
∆𝑛𝑖 𝑛𝑖 − 𝑛𝑖,0
= = 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒 = Δ𝜉 = 𝜉(𝐸∀) − 𝜉(𝐸𝐼)
𝜈𝑖 𝜈𝑖
en posant par convention
𝜉(𝐸𝐼) = 0
il vient
pour tout constituant physico-chimique Bi participant à la réaction d’équation (1) :
∆𝑛𝑖 𝑛𝑖 − 𝑛𝑖,0
= =𝜉
𝜈𝑖 𝜈𝑖
où 𝜉 représente l’avancement de la réaction d’équation (1) associé à un état quelconque
donné E du système.
𝜉 est homogène à une quantité de matière et s’exprime donc en moles.
NB : c’est bien le symbole 𝜉 qui est recommandé internationalement par l’UICPA pour désigner un avancement
de réaction.
Attention, pour un état donné du système, dépend de l’écriture de l’équation de la
réaction : si les nombres stœchiométriques de (1) sont tous multipliés par un nombre a,
l’avancement dans cet état du système est divisé d’autant.
exemple :
C. de Saint-Aubin PCSI3 2023-2024 6/24
Transformations de la matière
Si > 0, la réaction a évolué dans le sens direct (sens ) entre EI et E.
Si < 0, la réaction a évolué dans le sens inverse (sens ) entre EI et E.
On comprend donc que les appellations « réactifs » et « produits » sont de pures conventions d’écriture, puisque
les notations adoptées autorisent la réaction à pouvoir évoluer a priori dans les deux sens.
démonstration :
3. Conséquence
Pour tout constituant physico-chimique Bi intervenant dans (1) :
∆𝑛𝑖 𝑛𝑖 − 𝑛𝑖,0
= =𝜉
𝜈𝑖 𝜈𝑖
d’où
𝑛𝑖 = 𝑛𝑖 ,0 + 𝜈𝑖 ξ Bi de (1)
Cette relation est très importante, puisqu’elle est utilisée à chaque fois qu’il s’agit
d’établir un bilan de quantité de matière, première étape incontournable lorsqu’il s’agit de
faire de la chimie quantitative.
exemple :
à partir de l’état initial ci-dessous, qui relève d’un libre choix de l’expérimentateur, on peut
donner le bilan des quantités de matière pour un avancement quelconque de la réaction :
2 H2 (g) + O2 (g) = 2 H2O(g)
𝑛 (EI)
3 5 4
(mol)
𝑛 (E)
3–2𝜉 5–𝜉 4+2𝜉
(mol)
C. de Saint-Aubin PCSI3 2023-2024 7/24
Transformations de la matière
Si l’expérimentateur choisit de changer d’état intial pour le suivant, il vient :
2 H2 (g) + O2 (g) = 2 H2O(g)
𝑛 (EI)
8 4 0
(mol)
𝑛 (E)
8–2𝜉 4–𝜉 2𝜉
(mol)
4. Bornes de 𝝃
𝜉 peut varier entre deux bornes, qui dépendent du choix de l’état initial EI par
l’expérimentateur :
𝝃𝒎𝒊𝒏 ≤ 𝝃 ≤ 𝝃𝒎𝒂𝒙
la borne supérieure max est la valeur qui serait atteinte si la transformation pouvait être
totale dans le sens direct i.e. si elle pouvait épuiser le réactif limitant.
et la borne inférieure min est la valeur qui serait atteinte si la transformation pouvait être
totale dans le sens inverse i.e. si elle pouvait épuiser le produit limitant.
Pour trouver 𝜉𝑚𝑖𝑛 ou 𝜉𝑚𝑎𝑥 , on commence, pour chacune des espèces Bi de (1), par la
recherche de l’avancement maximum (en valeur absolue) 𝜉𝑚𝑎𝑥,𝑖 auquel il pourrait donner lieu,
i.e. celui qui annulerait la quantité de matière de Bi.
Et donc :
Pour les réactifs :
le réactif limitant est celui d’avancement maximum le plus faible : c’est lui qui fixe la
valeur de 𝜉𝑚𝑎𝑥 .
Pour les produits :
le produit limitant est celui d’avancement maximum le plus faible en valeur absolue : c’est
lui qui fixe la valeur de 𝜉𝑚𝑖𝑛 .
exemple :
pour le premier exemple ci-dessus, on commence par chercher l’avancement maximum
auquel chaque espèce pourrait donner lieu :
3
𝑛𝐻2 = 0 𝑚𝑜𝑙 = 3 𝑚𝑜𝑙 − 2𝜉𝑚𝑎𝑥,𝐻2 d’où 𝜉𝑚𝑎𝑥,𝐻2 = 2 𝑚𝑜𝑙 : H2 est le réactif limitant
𝑛𝑂2 = 0 𝑚𝑜𝑙 = 5 𝑚𝑜𝑙 − 𝜉𝑚𝑎𝑥,𝑂2 d’où 𝜉𝑚𝑎𝑥,𝑂2 = 5 𝑚𝑜𝑙
𝑛𝐻2 𝑂 = 0 𝑚𝑜𝑙 = 4 𝑚𝑜𝑙 + 2𝜉𝑚𝑖𝑛,𝐻2 𝑂 d’où 𝜉𝑚𝑖𝑛,𝐻2 𝑂 = −2 𝑚𝑜𝑙 : H2O est le produit limitant
(de toute façon, puisqu’ici, il n’y en a qu’un !)
3
et donc finalement : 𝜉𝑚𝑖𝑛 = −2 𝑚𝑜𝑙 ≤ 𝜉 ≤ 𝜉𝑚𝑎𝑥 = 2 𝑚𝑜𝑙.
C. de Saint-Aubin PCSI3 2023-2024 8/24
Transformations de la matière
5. Rendement de réaction 𝜼 associé à un état du système
Le rendement de réaction 𝜼 d’une réaction qui avance dans le sens direct (𝜉 > 0) est
défini par :
𝜉
𝜂= × 100
𝜉𝑚𝑎𝑥
C’est un nombre important à suivre au cours d’une synthèse ou à calculer à l’issue d’une
synthèse, au laboratoire ou dans l’industrie : il permet en effet d’évaluer combien on a obtenu
de produit synthétisé par rapport à ce que l’on aurait pu avoir si la réaction avait été totale (ce
qui est rarement le cas).
Si le rendement d’une réaction est trop faible, on peut essayer de l’améliorer grâce à des
techniques d’optimisation (cf. chapitre suivant).
On définit également le taux d’avancement 𝝉 associé à un état du système avec :
𝜂 𝜉
𝜏= =
100 𝜉𝑚𝑎𝑥
En pratique, on calcule le rendement d’une réaction à partir de la quantité de matière de l’un
des produits Ai obtenus. En supposant qu’il n’y ait pas de Ai dans le système à l’état initial
(𝑛𝑖,0 = 0), il vient :
𝜉
𝜂= × 100
𝜉𝑚𝑎𝑥
avec
∆𝑛𝑖 𝑛𝑖 − 𝑛𝑖,0 𝑛𝑖
𝜉= = =
𝜈𝑖 𝜈𝑖 𝜈𝑖
où 𝜈𝑖 représente le nombre stœchiométrique associé à Ai
et
∆𝑛𝑖,𝑚𝑎𝑥 𝑛𝑖,𝑚𝑎𝑥 − 𝑛𝑖,0 𝑛𝑖,𝑚𝑎𝑥
𝜉𝑚𝑎𝑥 = = =
𝜈𝑖 𝜈𝑖 𝜈𝑖
d’où
en pratique
𝑛𝑖
𝜂= × 100
𝑛𝑖,𝑚𝑎𝑥
où 𝑛𝑖,𝑚𝑎𝑥 représente la quantité maximale de produit Ai, initialement absent, que l’on
aurait obtenue si la réaction avait été totale.
C. de Saint-Aubin PCSI3 2023-2024 9/24
Transformations de la matière
exemple :
6. Coefficient de dissociation 𝜶 associé à l’état du système
Dans le cas d’une réaction qui, mis à part un éventuel solvant, ne fait intervenir qu’un seul
réactif Ai, on peut définir son coefficient de dissociation 𝛼 et suivre l’évolution de l’état du
système en transformation chimique à l’aide du coefficient de dissociation 𝛼 au lieu de le
suivre à l’aide de son avancement 𝜉.
Par définition, pour l’unique réactif Ai :
𝑛𝑖,0 − 𝑛𝑖
𝛼=
𝑛𝑖,0
En pratique, on commence à effectuer un bilan en quantité de matière en fonction de
l’avancement 𝜉, puis on remplace par l’expression de 𝜉 en fonction du coefficient de
dissociation 𝛼, pour obtenir finalement un bilan de quantité de matière en fonction de 𝛼.
exemple :
C. de Saint-Aubin PCSI3 2023-2024 10/24
Transformations de la matière
7. Mélange stœchiométrique
Définition
Le système contient un mélange stœchiométrique si Bi et Bj intervenant dans la
réaction d’équation (1) :
𝑛𝑖 𝜈𝑖
=
𝑛𝑗 𝜈𝑗
c’est-à-dire que les quantités de matière des espèces physico-chimiques Bi et Bj intervenant
dans la réaction d’équation (1) sont dans les proportions données par la stœchiométrie de cette
réaction.
exemples :
Conséquences
Si un mélange est stœchiométrique à l’état initial, il le reste à n’importe quel stade de la
transformation.
démonstration :
𝑛𝑖,0 𝜈
si pour i, j espèces quelconques = 𝜈𝑖 pour EI
𝑛𝑗,0 𝑗
𝑛𝑖,0 𝑛𝑗,0
alors =
𝜈𝑖 𝜈𝑗
𝑛𝑖 𝑛𝑖,0 +𝜈𝑖 𝜉 𝑛𝑖,0 𝑛𝑗,0 𝑛𝑗
d’où = = +𝜉 = +𝜉 = pour E
𝜈𝑖 𝜈𝑖 𝜈𝑖 𝜈𝑗 𝜈𝑗
L’avancement maximal d’un système initialement en mélange stœchiométrique est le même
pour tous les réactifs.
démonstration :
𝑛𝑖 = 0 = 𝑛𝑖,0 + 𝜈𝑖 𝜉𝑚𝑎𝑥,𝑖
d’où
𝑛𝑖 − 𝑛𝑖,0 𝑛𝑗 − 𝑛𝑗,0
𝜉𝑚𝑎𝑥,𝑖 = = = 𝜉𝑚𝑎𝑥,𝑗
𝜈𝑖 𝜈𝑗
pour i, j réactifs quelconques.
Si le système est initialement en mélange stœchiométrique, tous les réactifs sont épuisés si
la transformation est totale.
B. ACTIVITÉ ASSOCIÉE À UNE ESPÈCE PHYSICO-CHIMIQUE
DANS UN ÉTAT DONNÉ DU SYSTÈME
On suppose désormais que le système physico-chimique étudié est de plus constitué de phases
uniformes.
C. de Saint-Aubin PCSI3 2023-2024 11/24
Transformations de la matière
Pour un état donné de ce système, on peut définir, pour chaque espèce physico-chimique Ci
intervenant ou non dans la transformation modélisée par la réaction d’équation (1), un nombre
appelé activité de Ci dans cet état du système et noté 𝒂𝑪𝒊 .
Lorsque l’espèce Ci est seule dans sa phase :
𝑎𝐶𝑖 𝑠𝑒𝑢𝑙 𝑑𝑎𝑛𝑠 𝑠𝑎 𝑝ℎ𝑎𝑠𝑒 = 1
Lorsque l’espèce Ci est un gaz présent dans un mélange gazeux supposé idéal
(en pratique, on considérera toujours les mélanges gazeux idéaux cette année),
on a :
𝑝𝐶𝑖
𝑎𝐶𝑖 𝑔𝑎𝑧 𝑒𝑛 𝑚é𝑙𝑎𝑛𝑔𝑒 𝑔𝑎𝑧𝑒𝑢𝑥 𝑖𝑑é𝑎𝑙 =
𝑝°
avec 𝑝𝐶𝑖 : pression partielle de Ci dans le mélange, exprimée en bar
et 𝑝° : pression standard : 𝒑° = 1 bar exactement.
Lorsque Ci est le solvant d’une solution aqueuse diluée idéale (en pratique
lorsque les solutés ont tous des concentrations inférieures ou égales à 1 mol.L-1),
c’est-à-dire lorsque Ci est l’eau liquide solvant :
𝑎𝑒𝑎𝑢 𝑠𝑜𝑙𝑣𝑎𝑛𝑡 = 1
Lorsque Ci est un soluté d’une solution aqueuse diluée idéale :
𝐶𝑖
𝑎𝐶𝑖 𝑠𝑜𝑙𝑢𝑡é 𝑒𝑛 𝑠𝑜𝑙𝑢𝑡𝑖𝑜𝑛 𝑎𝑞𝑢𝑒𝑢𝑠𝑒 𝑑𝑖𝑙𝑢é𝑒 𝑖𝑑é𝑎𝑙𝑒 =
𝑐°
avec 𝐶𝑖 : concentration en quantité de matière de Ci dans la solution,
exprimée en mol.L-1
et 𝑐° : concentration de référence : 𝒄° = 1 mol.L-1 exactement
(attention à bien distinguer c0, concentration initiale d’une
espèce, et c°, concentration de référence !).
exemples :
C. de Saint-Aubin PCSI3 2023-2024 12/24
Transformations de la matière
C. QUOTIENT DE RÉACTION ASSOCIÉ À L’ÉTAT DU SYSTÈME
Il est possible de caractériser chaque état E du système par un nombre 𝑸𝑬∀ attaché à la
réaction (1)
0= 𝜈𝑖 𝐵𝑖 (1)
𝑖
appelé quotient de réaction ou quotient réactionnel attaché à (1) dans cet état E :
𝜈𝑖
𝑄𝐸∀ = 𝑎𝐵𝑖 ,𝐸∀
𝑖
avec 𝑎𝐵𝑖 ,𝐸∀ : activité de l’espèce physico-chimique Bi intervenant dans (1) dans l’état E du
système.
𝑄𝐸∀ est un quotient : au numérateur, on trouve les activités des produits de la réaction (pour
lesquels 𝜈𝑖 > 0) ; au dénominateur, les activités des réactifs (pour lesquels
𝜈𝑖 < 0).
𝑄𝐸∀ est un produit de nombres, les activités 𝑎𝐵𝑖 ,𝐸∀ : c’est donc bien lui-même un nombre.
𝑄𝐸∀ est attaché à l’équation (1) de la réaction : il faut donc écrire l’équation (1) avant de
pouvoir écrire l’expression de 𝑸𝑬∀ !
exemple :
III. ÉVOLUTION D’UN SYSTÈME LORS D’UNE
TRANSFORMATION CHIMIQUE MODÉLISÉE PAR UNE SEULE
RÉACTION CHIMIQUE
Système
Soit un système physico-chimique fermé à la température 𝑇 et constitué de phases uniformes.
Hypothèse réactionnelle
Supposons que ce système soit soumis à une transformation chimique modélisée par une seule
réaction chimique d’équation (1) suivante :
0= 𝜈𝑖 𝐵𝑖 (1)
𝑖
avec i nombre stœchiométrique algébrique de l’espèce physico-chimique Bi dans
l’équation (1).
C. de Saint-Aubin PCSI3 2023-2024 13/24
Transformations de la matière
A. ÉQUILIBRE CHIMIQUE
Le système est dit dans un état d’équilibre chimique ou encore à l’équilibre chimique
de la transformation modélisée par la réaction d’équation (1) lorsque son état est tel
qu’il n’y a pas de variation temporelle des quantités de matière des espèces
physico-chimiques Bi apparaissant dans l’équation (1) alors que TOUTES ces espèces
sont encore présentes dans le système (au moins en quantité infinitésimale).
Il est à noter que cet état est dynamique : à l’équilibre, les transformations des réactifs en
produits et des produits en réactifs ont toujours lieu au niveau microscopique, mais les
quantités formées de produits sont compensées par celles des réactifs reformés à partir d’eux.
Au final, au niveau macroscopique, « tout se passe comme s’il ne passait plus rien ».
exemple :
B. CRITÈRE D’ÉVOLUTION CHIMIQUE SPONTANÉE (OU NATURELLE)
Critère d’évolution
Si pour un état E du système à la température 𝑇 :
𝑸𝑬∀ < 𝑲° :
le système n’est pas à l’équilibre et va évoluer de manière à faire tendre le quotient
de réaction vers 𝐾° : le numérateur va augmenter, le dénominateur diminuer :
il y a évolution spontanée (ou naturelle) dans le sens direct , des réactifs vers
les produits.
𝑸𝑬∀ > 𝑲° :
le système n’est pas à l’équilibre et va évoluer de manière à faire tendre le quotient
de réaction vers 𝑲° : le numérateur va diminuer, le dénominateur augmenter :
il y a évolution spontanée dans le sens indirect , des produits vers les réactifs
𝑸𝑬∀ = 𝑲° :
il n’y a pas d’évolution, le système est dans un état d’équilibre chimique.
NB : on parle d’évolution spontanée ou naturelle lorsque le système évolue chimiquement
sans que cela ne nécessite d’autres travaux que celui des forces de pression avec l’extérieur
(pas d’échange de travail électrique, par exemple).
C. de Saint-Aubin PCSI3 2023-2024 14/24
Transformations de la matière
exemples :
Validité et limites
La thermodynamique est la science qui traite de la production, du stockage, du transfert et de
la conversion de l’énergie.
Le critère d’évolution chimique spontanée donné ci-dessus est d’origine purement
thermodynamique. Son origine sera explicitée en deuxième année.
C. de Saint-Aubin PCSI3 2023-2024 15/24
Transformations de la matière
Lorsque la thermodynamique, par l’intermédiaire du critère d’évolution, interdit
l’évolution chimique spontanée d’un système dans un certain sens, ce système ne peut en
aucun cas évoluer spontanément dans ce sens.
Par contre, si la thermodynamique prévoit une évolution chimique spontanée dans un sens
donné, cette évolution peut ne pas se produire pour des raisons cinétiques.
Le système se maintient alors dans un état hors équilibre chimique parce l’évolution
prévue par la thermodynamique est de vitesse trop faible. On dit alors que le système
persiste dans un état métastable.
L’obtention de systèmes dans des états métastables est parfois recherchée par le chimiste.
On peut par exemple l’atteindre par l’opération de trempe : il s’agit d’une brusque et
importante diminution de la température d’un système qui, pour des raisons cinétiques, se
maintient à basse température dans l’état qu’il avait à haute température,.
exemple :
C. ÉQUILIBRE CHIMIQUE : UN ÉTAT PARTICULIER DU SYSTÈME
1. Relation de Guldberg et Waage
Le troisième cas du critère d’évolution vu en III.B constitue la relation de Guldberg et Waage.
Relation de Guldberg et Waage
À l’équilibre chimique à la température 𝑇 de la transformation modélisée par la réaction
d’équation (1), les activités des diverses espèces physico-chimiques Bi intervenant dans
(1) s’ajustent de manière à ce que :
𝑄 = 𝐾°(𝑇)
où 𝑄 représente, à l’état d’équilibre chimique, le quotient de réaction attaché à (1).
Notation
Dans CE cours, le symbole d’une balance sera attaché à la description d’une grandeur
descriptive d’un système dans un état d’équilibre chimique. Toutefois, cette notation n’est pas
normalisée : elle doit être utilisée à l’écrit seulement après avoir été clairement explicitée.
De même, on utilisera dans CE cours l’abréviation RGW pour « Relation de Guldberg et
Waage » : cette abréviation est à expliciter si on doit l’écrire ailleurs.
C. de Saint-Aubin PCSI3 2023-2024 16/24
Transformations de la matière
Remarque essentielle
Il s’agit de bien comprendre la signification profonde de la relation de Guldberg et Waage :
lorsque la température 𝑇 du système est fixée, la relation de Guldberg et Waage nous enseigne
qu’un nombre lié à la composition du système (son quotient de réaction 𝑄) évolue vers une
valeur cible (la valeur de sa constante thermodynamique d’équilibre à 𝑇) :
- cette cible « ne bouge pas » : 𝐾° est fixée à une certaine valeur dès que 𝑇 est fixée ;
- c’est uniquement la composition du système et donc son quotient de réaction 𝑄
« qui bouge ».
𝑲°
Énoncer qu’« à l’équilibre, 𝐾° va valoir 𝑄 » n’a donc aucun sens : ce n’est pas 𝑄 la cible
mais 𝐾° !
2. En pratique
Il est essentiel lorsque l’on écrit la relation de Guldberg et Waage de toujours :
- vérifier l’homogénéité de l’expression ;
- faire attention à la possible présence d’espèces spectatrices qui interviennent dans
les fractions molaires des espèces actives (« Stop ntot » en faisant attention aux
phases dans lesquelles se trouvent les constituants).
exemple :
3. Intérêts de la relation de Guldberg et Waage
Détermination de l’état d’équilibre chimique d’un système
Lorsque l’on connaît l’état initial d’un système à température 𝑇 soumis à une
transformation chimique modélisée par une seule réaction chimique, il ne reste plus
qu’une inconnue à déterminer pour connaître, s’il peut être atteint, l’état d’équilibre
chimique du système : son avancement à l’équilibre 𝜉 . En effet, dans un bilan en
quantité de matière, toutes les quantités des espèces à l’équilibres sont exprimées en
fonction des quantités initiales 𝑛𝑖,0 de ces espèces, quantités connues, et de l’avancement
à l’équilibre 𝜉 , seule inconnue.
C. de Saint-Aubin PCSI3 2023-2024 17/24
Transformations de la matière
La relation de Guldberg et Waage est l’équation qui permet de trouver la valeur de
l’inconnue 𝜉 .
exercice :
Soit un système à la température 𝑇 formé initialement d’une solution aqueuse très diluée
du soluté A(aq).
Le soluté A(aq) peut se transformer en soluté B(aq) selon une transformation chimique
modélisée par l’unique réaction suivante :
A (aq) = B(aq) 𝐾°(𝑇)
Sachant qu’à l’état initial, on introduit sans dilution n0 mol de A dans un volume V d’eau,
ξ
déterminer la valeur de l’avancement volumique x = V lorsque l’équilibre chimique est
atteint.
solution :
A (aq) = B(aq)
𝑛 (EI)
𝑛0 0
(mol)
𝑛 (E)
𝑛0 − 𝜉 𝜉
(mol)
𝑛 (E)
𝑛0 − 𝜉 𝜉
(mol)
c (EI) 𝑛0
= 𝑐0 0
(mol.L-1) 𝑉
𝑛0 − 𝜉 𝜉
c (E)
(mol) 𝑉 𝑉
= 𝑐0 − 𝑥 =𝑥
c (E)
𝑐0 − 𝑥 𝑥
(mol.L-1)
la seule inconnue qu’il reste à déterminer est x : cela se fait aisément en utilisant la
relation de Gulberg et Waage.
En effet, à l’équilibre, on a :
𝑄 = 𝐾°(𝑇)
i.e.
𝑎𝐵(𝑎𝑞),
= 𝐾°
𝑎𝐴(𝑎𝑞),
csoluté,
en modélisant la solution par une solution aqueuse diluée idéale asoluté, = c°
et donc
𝑥
= 𝐾°
𝑐0 − 𝑥
d’où il vient
𝐾°
𝑥 = 𝑐
1 + 𝐾° 0
C. de Saint-Aubin PCSI3 2023-2024 18/24
Transformations de la matière
La relation de Guldberg et Waage est souvent de degré élevé et possède donc plusieurs
racines. Toutefois :
l’équilibre chimique d’un système à température 𝑇 et d’état initial donné est unique :
seule une des racines de l’équation de Guldberg et Waage convient.
Cette racine se trouve aisément : c’est la seule qui ait un sens chimique c’est-à-dire
dont la valeur trouvée pour 𝜉 se situe dans l’intervalle [𝜉min , 𝜉max ] des valeurs
autorisées de 𝜉 .
Toutes les autres racines se situent en-dehors de l’intervalle [𝜉min , 𝜉max ] et n’ont pas
de sens physique.
exemple :
Position de l’équilibre chimique et valeur de 𝑲°
Pour la transformation modélisée par une seule réaction d’équation (1), si l’on suppose
qu’aucun produit n’est présent à l’état initial, on peut calculer les deux bornes entre lesquelles
varie l’avancement 𝜉 pour un état initial donné (cf. plus haut) :
0 ≤ 𝜉 ≤ 𝜉𝑚𝑎𝑥
ou encore
0 ≤ 𝜏 ≤ 1.
Si 𝐾° est « grand », 𝜉 est « proche » de 𝜉𝑚𝑎𝑥 (ou encore 𝜏 est « proche » de 1).
Si 𝐾° est « petit », 𝜉 est « proche » de 0 (ou encore 𝜏 est « proche » de 0).
Évidemment, il serait intéressant d’avoir un critère absolu permettant de préciser ce qu’on
entend par « grand » ou « petit ». Ceci n’est malheureusement pas possible de manière
générale.
En effet, tout dépend de ce que l’on appelle « proche ».
Et aussi et surtout
la position de l’équilibre chimique dépend ET de la stœchiométrie de la réaction ET de
l’état initial du système.
exemples :
C. de Saint-Aubin PCSI3 2023-2024 19/24
Transformations de la matière
Si à l’équilibre, on suppose que la réaction modélisant la transformation chimique étudiée
a un avancement très faible, on la qualifie de « peu avancée » et on écrit :
𝜉 ~𝜀 ou 𝜏 ~𝜀
en supposant qu’aucun produit de la réaction n’a initialement été introduit.
Si à l’équilibre, on suppose que la réaction modélisant la transformation chimique étudiée
est quasi-totale, on la qualifie de quantitative et on écrit :
𝜉 ~𝜉max ou 𝜏 ~1
en supposant qu’aucun produit de la réaction n’a initialement été introduit.
L’une ou l’autre de ces hypothèses simplificatrice permet alors d’abaisser le degré de la
relation de Guldberg et Waage à résoudre et d’en trouver plus facilement la racine.
Bien sûr, il faut ensuite vérifier que la racine trouvée est cohérente avec l’hypothèse faite. Si
ce n’est pas le cas, il faut reprendre le calcul sans hypothèse simplificatrice.
4. K° : un nombre associé à une équation de réaction donnée
C. de Saint-Aubin PCSI3 2023-2024 20/24
Transformations de la matière
D. ÉTAT FINAL D’UN SYSTÈME EN TRANSFORMATION CHIMIQUE
1. Position du problème
Dans le système étudié,
on ne peut avoir de transformation chimique totale que si le réactif limitant disparaît
complètement du système, autrement dit que si la transformation modélisée par la réaction
d’équation (1) n’est pas à l’équilibre chimique.
En effet, une quantité strictement nulle pour un réactif revient à une activité nulle pour
celui-ci, ce qui donne un quotient de réaction associé à (1) infini.
Une réaction totale ne peut donc être un état d’équilibre chimique de la transformation
modélisée par la réaction d’équation (1) puisque le nombre 𝐾° n’est pas infini.
De même, une quantité strictement nulle d’un produit donne un quotient de réaction associé à (1) nul.
Une réaction qui n’a pas du tout avancé ne peut donc pas non plus être un état d’équilibre chimique de la
transformation modélisée par la réaction d’équation (1), puisque le nombre 𝐾° n’est pas nul.
exemple :
Cas (a)
On ajoute dans de l’eau une très faible quantité 𝑛0 d’hydroxyde de cuivre II solide
Cu(OH)2 (s).
On observe qu’on arrive à le dissoudre complètement.
On peut donc écrire :
Cu(OH)2 (s) = Cu2+(aq) + 2 HO-(aq) (1)
𝑛 (EI) (a)
𝑛0 0 0
(mol)
𝑛 (E)
𝑛0 − 𝜉 𝜉 2𝜉
(mol)
𝑛 (EF) (a)
0 𝑛0 2𝑛0
(mol)
L’état final EF du système est un état d’équilibre puisqu’il ne se passe plus rien (plus
d’évolution temporelle).
Par contre, cet état d’équilibre n’est pas un état d’équilibre chimique de la transformation
modélisée par la réaction d’équation (1). En effet, il manque le réactif Cu(OH)2 (s).
La transformation est donc totale et non pas quantitative. On dit dans ce cas qu’il y a rupture
de l’équilibre chimique de la transformation modélisée par la réaction d’équation (1).
Puisque la transformation modélisée par la réaction d’équation (1) n’est pas à l’équilibre
chimique, on ne peut évidemment pas écrire de relation de Guldberg et Waage associée.
Cas (b)
On ajoute dans de l’eau une quantité 𝑛0 d’hydroxyde de cuivre II solide Cu(OH)2 (s) beaucoup
plus importante que dans le cas (a).
On observe cette fois qu’à l’état final, il reste du solide Cu(OH)2 (s) dans le système.
C. de Saint-Aubin PCSI3 2023-2024 21/24
Transformations de la matière
On peut donc écrire :
Cu(OH)2 (s) = Cu2+(aq) + 2 HO-(aq) (1)
𝑛 (EI) (b)
𝑛0 0 0
(mol)
𝑛 (E)
𝑛0 − 𝜉 𝜉 2𝜉
(mol)
𝑛 (E) (b)
𝑛0 − 𝜉 𝜉 2 𝜉
(mol)
Cet état final est cette fois à l’équilibre chimique de la transformation modélisée par la
réaction d’équation (1).
Dans ce cas, la relation de Guldberg et Waage associée à (1) peut être écrite.
On remarque donc qu’en fonction des conditions initiales choisies par l’expérimentateur, le
système à l’équilibre à l’état final peut être à l’équilibre chimique ou non de (1) : la
transformation modélisée par la réaction d’équation (1) peut être soit à l’équilibre, soit totale.
2. Généralisation : transformation à l’équilibre chimique ou pas :
cas des systèmes hétérogènes
Dans le cas d’un système hétérogène, l’état final du système peut être tel que la
transformation modélisée par la réaction d’équation (1) n’est pas à l’équilibre chimique.
En effet
dans le cas d’un système hétérogène, le sens d’évolution prévu par le critère
d’évolution spontanée ne permet pas toujours d’atteindre l’équilibre à cause des
conditions initiales choisies :
- soit parce que l’évolution prévue par le critère d’évolution spontanée peut se
faire mais que l’équilibre est hors d’atteinte par épuisement prématuré d’une
espèce chimique.
L’état final EF est un état de rupture de l’équilibre chimique de la
transformation modélisée par la réaction d’équation (1) : la transformation est
totale ;
- soit parce que l’évolution prévue par le critère d’évolution spontanée ne peut se
faire parce qu’une espèce qui devrait réagir n’a pas été introduite dans le
système.
L’état final EF est alors identique à l’état initial, appelé état de repos
chimique : la transformation modélisée par la réaction d’équation (1) n’a pas
du tout avancé : son avancement à l’état final est strictement nul.
exemple :
C. de Saint-Aubin PCSI3 2023-2024 22/24
Transformations de la matière
3. Méthodologie de recherche de l’état final d’un système siège
d’une transformation chimique modélisée par une seule réaction
À partir de tout ce qui précède, voici la méthode, À PARFAITEMENT CONNAÎTRE, qui
permet de décrire l’état final EF d’un système en transformation chimique modélisée par une
seule réaction d’équation (1), à partir d’un état initial EI donné.
Définir le système physico-chimique étudié.
Préciser la température 𝑇 du système, éventuellement sa pression 𝑝.
Décrire ce système à l’état initial : espèces physico-chimiques introduites, quantités
introduites.
Écrire l’équation (1) de la seule réaction modélisant la transformation chimique
envisagée.
Dresser le tableau d’avancement (donc en quantité de matière) de cette transformation :
description des quantités présentes à l’état initial EI, puis dans un état quelconque E du
système.
En fonction des données du problème, compléter éventuellement le tableau par la
description de ces états à l’aide d’une autre grandeur de description (concentrations,
coefficient de dissociation, pressions partielles, …).
À partir de la valeur du quotient de réaction 𝑄𝐸𝐼 à l’état initial et de la valeur de la
constante thermodynamique d’équilibre 𝐾° associée à (1) à 𝑇, prévoir le sens de
l’évolution spontanée de la transformation (étude qualitative).
Si la transformation prévue est nulle, l’état final EF est un état de repos chimique faute de
la présence de certaines espèces.
Sinon, supposer a priori que l’état final EF est un état d’équilibre chimique E :
- écrire la relation de Guldberg et Waage associée à (1) en faisant apparaître les
grandeurs pertinentes par rapport aux données de l’énoncé
- au regard des conditions et de la valeur de K°, faire éventuellement une hypothèse
simplificatrice : réaction peu avancée ou réaction quantitative, pour simplifier
l’équation obtenue
- résoudre cette équation pour trouver l’état d’équilibre
- le cas échéant, vérifier la cohérence de cet état avec l’hypothèse simplificatrice
faite : s’il n’y a pas cohérence, recommencer la résolution de l’équation sans
hypothèse simplificatrice
- si toutes les quantités de matière trouvées en supposant que l’état final EF est un
état d’équilibre sont positives, cette hypothèse est validée.
Sinon, l’état final EF n’est pas un état d’équilibre chimique : la transformation est alors
totale et l’état final EF est un état de rupture d’équilibre.
C. de Saint-Aubin PCSI3 2023-2024 23/24
Transformations de la matière
CONCLUSION
Grâce aux outils thermodynamiques introduits dans ce chapitre, il est désormais possible de
prévoir l’état final d’un système en transformation chimique lorsque celle-ci est modélisée par
une seule réaction chimique.
Bien entendu, la chimie qui se déroule tous les jours autour ou à l’intérieur de nous ne se
limite pas à ce cas. Très souvent, une transformation chimique doit être modélisée par
plusieurs réactions se déroulant ensemble dans le système. La méthode présentée dans ce
chapitre peut se généraliser et l’état final de tels systèmes peut également être prévu.
Toutefois, la résolution analytique du problème n’est plus toujours possible : il faut alors
recourir à l’outil numérique.
Par ailleurs, une fois l’état final d’un système trouvé, il peut ne pas convenir à
l’expérimentateur, qui va alors mobiliser ses connaissance pour le changer et l’optimiser.
Ces deux sujets sont traités dans le prochain chapitre.
C. de Saint-Aubin PCSI3 2023-2024 24/24
Vous aimerez peut-être aussi
- Processus irréversibles non linéaires en thermodynamique: Les Grands Articles d'UniversalisD'EverandProcessus irréversibles non linéaires en thermodynamique: Les Grands Articles d'UniversalisPas encore d'évaluation
- Cours Physique-Chimie 1bac BIOF .S1Document47 pagesCours Physique-Chimie 1bac BIOF .S1الغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- Cours 13 Équilibres ChimiquesDocument4 pagesCours 13 Équilibres ChimiquesArti80% (5)
- Os Chimie Corrige ch3 PDFDocument24 pagesOs Chimie Corrige ch3 PDFf.B100% (1)
- Réactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Document63 pagesRéactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Oumayma IkhlefPas encore d'évaluation
- Les Equilibres ChimiquesDocument7 pagesLes Equilibres Chimiquesdembamamadou274Pas encore d'évaluation
- 1 Equilibres ChimiquesDocument6 pages1 Equilibres ChimiquesMira MslPas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Document2 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Fatima Zahrae El BouhmidiPas encore d'évaluation
- Transformation Chimiquebilan de MatièreDocument3 pagesTransformation Chimiquebilan de MatièreKamal LaourdaniPas encore d'évaluation
- Analyse 3Document19 pagesAnalyse 3ibrahimPas encore d'évaluation
- Thermodynamique PDFDocument18 pagesThermodynamique PDFKarim MegherfiPas encore d'évaluation
- Cours de Thermo - 2022Document28 pagesCours de Thermo - 2022Soro AchillePas encore d'évaluation
- Cours Chim 06Document28 pagesCours Chim 06fsqiypiyiherafzferkPas encore d'évaluation
- Chapitre I - THERMODYNAMIQUE DU PREMIER PRINCIPE - 22-23Document17 pagesChapitre I - THERMODYNAMIQUE DU PREMIER PRINCIPE - 22-23Soro AchillePas encore d'évaluation
- CM CHI 201 - 2022 Royal Partie 1Document53 pagesCM CHI 201 - 2022 Royal Partie 1Vera Legba-MonyPas encore d'évaluation
- TP EquilibrechimiqueDocument8 pagesTP Equilibrechimiquecherazer67% (3)
- Cinétique ChimiqueDocument10 pagesCinétique Chimiquearfpower100% (2)
- Rappels Cinetique ChimiqueDocument22 pagesRappels Cinetique ChimiqueSaid Soilihi ZayadPas encore d'évaluation
- 1ère S - Chimie - Révision - La Transformation ChimiqueDocument13 pages1ère S - Chimie - Révision - La Transformation ChimiqueFidel ْPas encore d'évaluation
- Calcul Des Reacteurs Chimiques HomogeneDocument16 pagesCalcul Des Reacteurs Chimiques HomogeneجعدبندرهمPas encore d'évaluation
- Support Chaptre I CinétiqueDocument19 pagesSupport Chaptre I CinétiqueAthmane LandjassaPas encore d'évaluation
- Deplacement EquilibreDocument14 pagesDeplacement Equilibremohsat100% (2)
- 1 Bioenergetique LAS 2020Document38 pages1 Bioenergetique LAS 2020Duvalier EkeguePas encore d'évaluation
- 1 Bioenergetique LAS 2020Document38 pages1 Bioenergetique LAS 2020hissein ousmanPas encore d'évaluation
- Cours SM4001 PDFDocument105 pagesCours SM4001 PDFbentouamiPas encore d'évaluation
- Avancement D Une Reaction ChimiqueDocument4 pagesAvancement D Une Reaction ChimiqueFitouri MoncefPas encore d'évaluation
- Chapitre 2Document4 pagesChapitre 2Moustapha Bassirou NianePas encore d'évaluation
- Bilan Titrage Colorimetrique Et OxydoreductionDocument2 pagesBilan Titrage Colorimetrique Et Oxydoreductionbazoly.rambeloPas encore d'évaluation
- ThermochimieDocument9 pagesThermochimietiti_canariPas encore d'évaluation
- Chapitre 5A Complété Quotient de Réaction Et Constante d' ÉquilibreDocument3 pagesChapitre 5A Complété Quotient de Réaction Et Constante d' Équilibreairfann67Pas encore d'évaluation
- 2nde - CH5 - Cours - Transformation ChimiqueDocument3 pages2nde - CH5 - Cours - Transformation Chimiqueemma.gueblePas encore d'évaluation
- Cours Equilibre Chimique PDFDocument7 pagesCours Equilibre Chimique PDFKTMPas encore d'évaluation
- Cours Partie 1 Chimie en Solution AqDocument27 pagesCours Partie 1 Chimie en Solution AqchoroukbenhammouPas encore d'évaluation
- Description D'un Système Chimique en Réaction (1029)Document6 pagesDescription D'un Système Chimique en Réaction (1029)AxellePas encore d'évaluation
- Cinetique Chimique (PR Belaribi)Document17 pagesCinetique Chimique (PR Belaribi)Zidani LinaPas encore d'évaluation
- Bilan Matiere 2PDocument8 pagesBilan Matiere 2PMaël SounaPas encore d'évaluation
- Cours Thermochimie 2021Document109 pagesCours Thermochimie 2021Hiba AmalouPas encore d'évaluation
- Support Cours ThermodDocument126 pagesSupport Cours ThermodABDOXX1aPas encore d'évaluation
- Chp. Transformation ChimiqueDocument5 pagesChp. Transformation ChimiqueyvancharlesmendoumeessengPas encore d'évaluation
- TD 1 Description D'un SystemeDocument3 pagesTD 1 Description D'un Systemechristraore998Pas encore d'évaluation
- Chapitre VII Thermochimie PDFDocument14 pagesChapitre VII Thermochimie PDFÇiçek KokusuPas encore d'évaluation
- Réacteurs Chimiques Et Catalyse - Cinétique Homogène-1Document43 pagesRéacteurs Chimiques Et Catalyse - Cinétique Homogène-1mehdi manaaPas encore d'évaluation
- Chimie C Chap9 Evolution - SpontaneeDocument5 pagesChimie C Chap9 Evolution - Spontaneemohamed laghribPas encore d'évaluation
- Exercices L2 SPS 2023-2024 EquilibresDocument3 pagesExercices L2 SPS 2023-2024 Equilibresj29024688Pas encore d'évaluation
- Cours TC1Document1 pageCours TC1mxmzllr2Pas encore d'évaluation
- Cinetique Chimique PDFDocument21 pagesCinetique Chimique PDFياسين السعدانيPas encore d'évaluation
- CHAPITRE 1 Partie 2Document14 pagesCHAPITRE 1 Partie 2hamid ibbakhPas encore d'évaluation
- CH3L.a.M. ModérationDocument6 pagesCH3L.a.M. ModérationAmen RouissiPas encore d'évaluation
- Solutions Aqueuses Nouveau 2023Document79 pagesSolutions Aqueuses Nouveau 2023Fannes DesignPas encore d'évaluation
- Chap 3 Bilan de Matière Dans Les Réacteurs IdéauxDocument15 pagesChap 3 Bilan de Matière Dans Les Réacteurs IdéauxAPas encore d'évaluation
- Equilibre Chimique, Word 1Document2 pagesEquilibre Chimique, Word 1Lourdes Gerges0% (1)
- Cours Chimie II 1ère SNV v2 PDFDocument38 pagesCours Chimie II 1ère SNV v2 PDFSamsouma BkPas encore d'évaluation
- Chapitre 04Document7 pagesChapitre 04الغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Chapitre 7 Evolution Spontanée D'un Système Chimique CoursDocument6 pagesChapitre 7 Evolution Spontanée D'un Système Chimique CoursfranbillesPas encore d'évaluation
- Projet Cinitique GP l3 Section BDocument126 pagesProjet Cinitique GP l3 Section BokyPas encore d'évaluation
- CoursDocument7 pagesCoursMohammed TahriPas encore d'évaluation
- 13-14 Cours CG2Document44 pages13-14 Cours CG2Boukalmoune IbrahimPas encore d'évaluation
- Cours 1 Cinétique - L2-2020-2021Document7 pagesCours 1 Cinétique - L2-2020-2021shakib mesbahiPas encore d'évaluation
- I-1 Réactions Chimiques - Rappels - Hafid2021Document27 pagesI-1 Réactions Chimiques - Rappels - Hafid2021Raih NabilPas encore d'évaluation
- Dosage Eau OxygeneeDocument2 pagesDosage Eau Oxygeneecosmixvj100% (1)
- Cours MP PDFDocument2 pagesCours MP PDFSimo BouzoPas encore d'évaluation
- Equilibres Chimiques Et Électrochimiques en Solution Aqueuse (PDFDrive)Document163 pagesEquilibres Chimiques Et Électrochimiques en Solution Aqueuse (PDFDrive)Samah Soltane0% (1)
- Fascicule Cinetique ChimiqueDocument42 pagesFascicule Cinetique ChimiqueBarhoumi Mourad100% (2)
- 05 06 Rapport de LaboratoireDocument4 pages05 06 Rapport de LaboratoireScribdTranslationsPas encore d'évaluation
- Correction ExoDocument4 pagesCorrection ExogueyePas encore d'évaluation
- Resume de SecondeDocument6 pagesResume de SecondeLachhab AbdellatifPas encore d'évaluation
- Chapitre IVDocument24 pagesChapitre IVAPas encore d'évaluation
- GFTHKFDocument101 pagesGFTHKFFedoua BenamerPas encore d'évaluation
- Serie 1 CH Avancement Vitesse Dune Réaction2 1Document1 pageSerie 1 CH Avancement Vitesse Dune Réaction2 1daddouPas encore d'évaluation
- Cinétique ChimiqueDocument10 pagesCinétique Chimiquearfpower100% (2)
- Polycopié - Les Réacteurs HomogènesDocument93 pagesPolycopié - Les Réacteurs HomogènesIm printPas encore d'évaluation
- 2003 Pondichery Correction Exo1 Esterification 6ptsDocument2 pages2003 Pondichery Correction Exo1 Esterification 6ptsDaniela DinicaPas encore d'évaluation
- 2D PC CHAP 03 ExercicesDocument93 pages2D PC CHAP 03 ExercicesSHARK VAVAPas encore d'évaluation
- Chapitre I IntroductionDocument19 pagesChapitre I IntroductionOussama amasouPas encore d'évaluation
- Cours 1 - TM-1Document5 pagesCours 1 - TM-1Mål ÆkPas encore d'évaluation
- Aspects Quantitatifs Et TDDocument10 pagesAspects Quantitatifs Et TDYvesson CHARLESPas encore d'évaluation
- PDF - 2023 XCHI564 EMINES 2 Réacteurs Homogènes Hydro Idéale Bilans MATIERE Optim Techn EcoDocument74 pagesPDF - 2023 XCHI564 EMINES 2 Réacteurs Homogènes Hydro Idéale Bilans MATIERE Optim Techn EcoMouncef AsryPas encore d'évaluation
- Fiche de Revision 2Document2 pagesFiche de Revision 2mv9zrfr85xPas encore d'évaluation
- Fiche Tableau AvancementDocument2 pagesFiche Tableau Avancementabdirahman abdillahiPas encore d'évaluation
- Exercices Et Problèmes CHIMIE - 1re Année MPSIDocument260 pagesExercices Et Problèmes CHIMIE - 1re Année MPSIAdil ALAOUIPas encore d'évaluation
- Yyy Suppexos cm4 cm5 Chimie Acides Bases PDFDocument16 pagesYyy Suppexos cm4 cm5 Chimie Acides Bases PDFKurosaki AimarPas encore d'évaluation
- Cours Complet R.CDocument385 pagesCours Complet R.CPRAIIIZ FouPas encore d'évaluation