Académique Documents
Professionnel Documents
Culture Documents
Ebulition de L'eau
Transféré par
aesthetic compteTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Ebulition de L'eau
Transféré par
aesthetic compteDroits d'auteur :
Formats disponibles
Leçon 14: Ebullition de l’eau pure
Objectifs de la leçon :
- Réaliser l’expérience d’ébullition de l’eau pure et noter les observations.
- Tracer la courbe de variation de la température en fonction du temps à fin d’étudier un
changement d’état de l’eau pure.
- Interpréter des résultats et tirer des conclusions.
Afin d’atteindre ces objectifs l’apprenant doit être capable de :
Faire de déductions et tirer des conclusions.
Interpréter des données.
Activité : Etude d’un changement d’état : la vaporisation de l’eau pure.
1/ J’observe et je m’interroge :
• Comment expliquer le séchage des vêtements exposés à l’air libre?
L’eau des vêtements s’évapore à l’air libre sous l’action de la chaleur du soleil.
• Pour cuire des pâtes, décrivez- moi ce qui se passe pour l’eau quand on la
chauffe?
L’eau commence à bouillir jusqu’à vaporisation (passage de l’état liquide à l’état
gazeux).
• Quand on soulève le couvercle pendant la cuisson des pâtes Que voit- on?
On voit de la buée: la vapeur d’eau se refroidit et elle redevient donc liquide (c’est
la liquéfaction).
2/ Je déduis :
- Un changement d’état est le passage d’un état physique à un autre.
- Le passage de l’état liquide à l’état gazeux s’appelle la vaporisation.
- L’évaporation est une vaporisation qui se fait par la surface du liquide à l’aide de la
chaleur et du vent.
- Le passage de l’état gazeux à l’état liquide s’appelle la liquéfaction.
Chapitre V : Les états physiques de la matière : propriétés, caractéristiques et changements d’états
Leçon 14 : Ebullition de l’eau pure 1
3/ J’expérimente et j’observe :
• J’introduis un thermomètre dans un ballon contenant une petite quantité d’eau
pure.
• Je commence à chauffer l’eau en même temps je déclenche le chronomètre.
• Je suis l’évolution de la température en notant sa valeur à chaque minute sur le
tableau ci- dessous.
• J’arrête les mesures 2 à 3 minutes après le début d’ébullition de l’eau.
• Je complète le schéma de l’expérience et je note les observations :
Observations : Chronomètre
……………………………….
Qu’observez- vous au cours du
chauffage?
- Quand on chauffe l’eau, sa température
Thermomètre
……………………………….
augmente.
- L’eau s’échauffe: des bulles de gaz Gouttelettes
………………………… d’eau
dissous dans l’eau se dégagent à partir
d’une température de 40 °C.
- Puis des bulles plus grosses constituées
Ballon
de vapeur d’eau apparaissent: c’est
l’ébullition.
Figure 1 : Expérience de l’ébullition
de l’eau pure
Au cours de l’ébullition, je présente à l’ouverture du ballon un bécher, qu’observez-
vous?
- J’observe des gouttelettes d’eau qui se forment sur les parois internes du bécher. C’est
la liquéfaction.
Chapitre V : Les états physiques de la matière : propriétés, caractéristiques et changements d’états
Leçon 14 : Ebullition de l’eau pure 2
Je trace la courbe sur un papier millimétré, représentant l’évolution de la température en
fonction du temps et j’indique dessus, les étapes du changement d’état liquide et gazeux.
Temps 0 1 2 3 4 5 6 7 8 9 10
(minutes)
T ( °C) 26 30 42 56 72 88 100 100 100 100 100
4/ J’interprète et j’analyse :
Après avoir tracé la courbe, je réponds aux questions suivantes :
- Comment varie la température au début de l’expérience de l’ébullition de l’eau pure ?
La température augmente au début de l’expérience.
- De combien de parties est constituée la courbe de l’ébullition de l’eau pure ? Noter sur
chaque partie de la courbe l’état physique de l’eau pure.
Deux parties: la 1ere partie : la température augmente, la 2eme partie :la température
reste constante.
- Comment varie la température pendant le changement d’état ?
Pendant le changement d’état, la courbe présente un palier donc la température reste
constante.
- A quel instant commence ce changement d’état selon la courbe ?
Le changement d’état commence à t= 6 Minutes.
- A quelle température se fait alors ce changement d’état ?
Ce changement d’état se fait à 100 °C.
Chapitre V : Les états physiques de la matière : propriétés, caractéristiques et changements d’états
Leçon 14 : Ebullition de l’eau pure 3
- Puisque la liquéfaction est la transformation physique inverse de la vaporisation, La
courbe de liquéfaction est représentée ainsi:
Figure 2 : Courbe de liquéfaction de l’eau pure
Selon la courbe ci- dessus, quelle est alors la température de liquéfaction de l’eau pure ?
La température de liquéfaction se fait aussi à 100°C.
- Lorsque l’eau n'est pas pure, comme c’est le cas d’une eau salée (mélange eau + sel),
on obtient la courbe ci-dessous :
Figure 3 : Courbes d’ébullition de l’eau pure vs eau salée
Quelle est la différence entre les deux courbes ?
La différence c’est qu’on n’observe pas de palier pour la courbe de l’eau salée.
Chapitre V : Les états physiques de la matière : propriétés, caractéristiques et changements d’états
Leçon 14 : Ebullition de l’eau pure 4
5/ Je conclus
L’eau passe, par ébullition, de l’état liquide à l’état gazeux: C’est la
vaporisation.
Pendant la vaporisation, la température reste constante, la courbe
présente un palier à une température de 100°C.
L’évaporation est une vaporisation qui se fait par la surface du liquide.
Elle se fait à toute température.
Lorsque la vapeur d’eau est refroidie elle passe à l’état liquide: c’est la
liquéfaction.
La liquéfaction et la vaporisation sont deux transformations physiques
inverses qui se font à la même température.
L’essentiel à compléter :
- Pour un corps pur, La vaporisation et la liquéfaction sont deux changements d’état
physique inverses qui se font à une même température.
- Pour l’eau pure, la température de vaporisation et de liquéfaction est de 100°C.
Synthèse : Représentation graphique des idées
Chapitre V : Les états physiques de la matière : propriétés, caractéristiques et changements d’états
Leçon 14 : Ebullition de l’eau pure 5
Vous aimerez peut-être aussi
- Chapitre 2Document17 pagesChapitre 2Vince DrePas encore d'évaluation
- 5 - La Chaleur Et La TempératureDocument19 pages5 - La Chaleur Et La TempératurePicasso BosePas encore d'évaluation
- Partie FrigorifiqueDocument54 pagesPartie FrigorifiqueMohamed LaribiPas encore d'évaluation
- Questions Changements D' ÉtatDocument4 pagesQuestions Changements D' Étatmanilou57Pas encore d'évaluation
- Chapitre 5 Version Corrigée PDFDocument6 pagesChapitre 5 Version Corrigée PDFAdame KhelkhalPas encore d'évaluation
- Physique 7eme Cour-N°3Document10 pagesPhysique 7eme Cour-N°3nadiaPas encore d'évaluation
- 5c4-Les Changements DetatDocument6 pages5c4-Les Changements Detatben mamiaPas encore d'évaluation
- La Chaleur Et La TempératureDocument3 pagesLa Chaleur Et La TempératureMajdouline KtPas encore d'évaluation
- La Température, La Chaleur Et Les Changements D'état Physique de LaDocument3 pagesLa Température, La Chaleur Et Les Changements D'état Physique de LaHome erriahiPas encore d'évaluation
- Aqua Marketing Plan - by SlidesgoDocument15 pagesAqua Marketing Plan - by Slidesgolobnabouazizi85Pas encore d'évaluation
- Cr2 - Temperature Et La ChaleurDocument3 pagesCr2 - Temperature Et La ChaleursouhailPas encore d'évaluation
- La Chaleur Et Les Changements D Etat Physique de La Matiere Cours 6Document3 pagesLa Chaleur Et Les Changements D Etat Physique de La Matiere Cours 6soubzm2001Pas encore d'évaluation
- Les États de La Matière (Unité 2)Document36 pagesLes États de La Matière (Unité 2)Dde DjdPas encore d'évaluation
- LA LYOPHILISATION Cours M2 2021 - 2022Document76 pagesLA LYOPHILISATION Cours M2 2021 - 2022wissldjjPas encore d'évaluation
- Thermo SiphonDocument2 pagesThermo SiphonartustPas encore d'évaluation
- Changements D'état de La MatièreDocument8 pagesChangements D'état de La MatièreRiadh ChouaibiPas encore d'évaluation
- Changement Etat EauDocument5 pagesChangement Etat EauRayane BEKKOUCHEPas encore d'évaluation
- ExtraitDocument8 pagesExtraitfar32lemPas encore d'évaluation
- 1 - La Chaleur Et Les Changements D'état PhysiqueDocument15 pages1 - La Chaleur Et Les Changements D'état PhysiqueKezmin BiksPas encore d'évaluation
- Sequences Sur L Eau Ce2Document2 pagesSequences Sur L Eau Ce2Rokaya Lachkhame100% (1)
- TP2 Chimie2Document2 pagesTP2 Chimie2Tøøp Føøtball0% (1)
- TP2 - TVS - Thermodynamique II - PR Lamrani Et DaoudiDocument10 pagesTP2 - TVS - Thermodynamique II - PR Lamrani Et DaoudiHafid El fdilPas encore d'évaluation
- Melange Et Corps PurDocument11 pagesMelange Et Corps PurkountiyouPas encore d'évaluation
- TP4 Distillation Fractionnée 2Document3 pagesTP4 Distillation Fractionnée 2Fouad MihoubPas encore d'évaluation
- Chimie EauDocument4 pagesChimie EauAllinco NasreddinePas encore d'évaluation
- CINQcoursn°5 15 16 ENTDocument4 pagesCINQcoursn°5 15 16 ENTAnonymous Qzjk6K9GTPas encore d'évaluation
- Polycopié TP S2Document14 pagesPolycopié TP S2mona lemkadem100% (1)
- tp11 1s9 Vaporisation Par EbullitionDocument2 pagestp11 1s9 Vaporisation Par EbullitionsaanounPas encore d'évaluation
- Compte Rendu Chimie: 1: Vaporisation de L'eau DistilléeDocument9 pagesCompte Rendu Chimie: 1: Vaporisation de L'eau DistilléeWalid Ouabas100% (3)
- Pdfjoiner 1Document16 pagesPdfjoiner 1Ray CharlesPas encore d'évaluation
- Activité Vaporisation de L'eau 2023-2024Document1 pageActivité Vaporisation de L'eau 2023-2024saintmichelecole12Pas encore d'évaluation
- CHAP9 - Chimie - TP1 Fusion CyclohexaneDocument2 pagesCHAP9 - Chimie - TP1 Fusion CyclohexaneFrancoise BERNARDPas encore d'évaluation
- Chapitre 4 Transition de Phase Version Simplifiée STDocument45 pagesChapitre 4 Transition de Phase Version Simplifiée STArmel YmgPas encore d'évaluation
- Chaleur Et Température FinDocument2 pagesChaleur Et Température FinKarim ObaissPas encore d'évaluation
- SCPH 5 19 Ebulition TemperatureDocument7 pagesSCPH 5 19 Ebulition TemperatureAyoub ArrarPas encore d'évaluation
- Distillation FRACTIONéeDocument5 pagesDistillation FRACTIONéecélia ferPas encore d'évaluation
- CPHY-212 Les Effets Thermiques Fiche EleveDocument9 pagesCPHY-212 Les Effets Thermiques Fiche EleveKenson DEROSANPas encore d'évaluation
- 5 ch7 ExDocument3 pages5 ch7 ExNessrine ZahiPas encore d'évaluation
- Utiliser Une Éprouvette Graduée Changements D'étatsDocument3 pagesUtiliser Une Éprouvette Graduée Changements D'étatsarmy82145Pas encore d'évaluation
- TemperatureDocument5 pagesTemperatureShabanianzuruni ShabaniPas encore d'évaluation
- Refrigeration Part 2Document33 pagesRefrigeration Part 2Sam TendryPas encore d'évaluation
- Séquence 5 Lafusion de l' Eau 3Document2 pagesSéquence 5 Lafusion de l' Eau 3Orlane CatalanPas encore d'évaluation
- Examen: SPC Niveau: 6e/5e Date: 09/12/2022: Exercice 1Document2 pagesExamen: SPC Niveau: 6e/5e Date: 09/12/2022: Exercice 1Amin Chakib0% (1)
- TP - Vaporisation Par ÉbulutionDocument1 pageTP - Vaporisation Par ÉbulutionDorra Doggui100% (1)
- 2 I-07 EtatsDocument5 pages2 I-07 EtatsssgPas encore d'évaluation
- TD 2 de ThermochimieDocument4 pagesTD 2 de ThermochimieCARDI BPas encore d'évaluation
- TP Distillaion SimpleDocument5 pagesTP Distillaion SimpleMïss MïmãPas encore d'évaluation
- 5ème PH - CH Fiche Dexercices Révision 2Document2 pages5ème PH - CH Fiche Dexercices Révision 2nch.choudharyPas encore d'évaluation
- Chapitre - 2 Sciance A AhananeDocument6 pagesChapitre - 2 Sciance A AhananeNessa AnnePas encore d'évaluation
- Difference Entre Temperature Et Chaleur ProfDocument4 pagesDifference Entre Temperature Et Chaleur ProfnandimodipliaPas encore d'évaluation
- TPsolidificationDocument4 pagesTPsolidificationIbtissem Ben MahmoudPas encore d'évaluation
- Initiaion Process Par Daverni Kombila +241 077 513 683Document35 pagesInitiaion Process Par Daverni Kombila +241 077 513 683daverni bourobou kombilaPas encore d'évaluation
- TP - La - Distillation 02Document6 pagesTP - La - Distillation 02Belmabedi MarouanePas encore d'évaluation
- 5 ch7 Exc PDFDocument3 pages5 ch7 Exc PDFNoureddine CherradPas encore d'évaluation
- 5 ch7Document3 pages5 ch7Anonymous FikOnlapPas encore d'évaluation
- Document 3Document6 pagesDocument 3Doublalig2008Pas encore d'évaluation
- Correction Des Exercices de C6-1-1Document2 pagesCorrection Des Exercices de C6-1-1jean valjeanPas encore d'évaluation
- La Chaleur Et Les Changements D Etat Physique de La Matiere Cours 1Document3 pagesLa Chaleur Et Les Changements D Etat Physique de La Matiere Cours 1Moataz Ben MustaphaPas encore d'évaluation
- Le Corps Pur Et Ses Caracteristiques Cours PPT 4 2Document17 pagesLe Corps Pur Et Ses Caracteristiques Cours PPT 4 2Nassif AnassPas encore d'évaluation
- Mc3a9langes Et Corps PursDocument2 pagesMc3a9langes Et Corps PursAngus Mak100% (1)
- Corrige Optique TD Serie 1 by Team VioletDocument4 pagesCorrige Optique TD Serie 1 by Team VioletStéphane LeundePas encore d'évaluation
- Copie de Sismique Réfraction PDFDocument59 pagesCopie de Sismique Réfraction PDFMarwa MessaadiPas encore d'évaluation
- Corrigé Type Physique 04Document5 pagesCorrigé Type Physique 04Omar LANGEURPas encore d'évaluation
- But de TPDocument20 pagesBut de TPHamza Amdouni0% (1)
- TD Interférences Lumineuses 2016Document8 pagesTD Interférences Lumineuses 2016Oumar Traoré100% (1)
- 2 Memoire Ben Toumi Gherabpdf Ovgyi78k1666640309Document86 pages2 Memoire Ben Toumi Gherabpdf Ovgyi78k1666640309bhoussamhoussam7Pas encore d'évaluation
- Exercice Ox RedDocument3 pagesExercice Ox Redاپن فلسىطين المتمرد شخصىيآPas encore d'évaluation
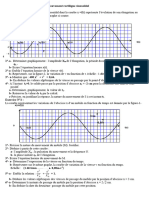
- Série Mouvement Rectiligne SinusoidalDocument2 pagesSérie Mouvement Rectiligne SinusoidalmanelbelhajlakdarPas encore d'évaluation
- Convection FDocument64 pagesConvection FHold YuhPas encore d'évaluation
- Thermique Du LaminageDocument4 pagesThermique Du LaminagePERRINPas encore d'évaluation
- Cours Chapitre 6 Transfert de Chaleur Et de Masse ApprofondiDocument7 pagesCours Chapitre 6 Transfert de Chaleur Et de Masse ApprofondiMohamed BelazilPas encore d'évaluation
- SC - Physiques Bac Blanc - Maths-2021 (Jlali Ammar)Document5 pagesSC - Physiques Bac Blanc - Maths-2021 (Jlali Ammar)Ali SkimaPas encore d'évaluation
- Chapitre1 Absorption-StrippageDocument8 pagesChapitre1 Absorption-StrippageLARDJOUN ElhabibPas encore d'évaluation
- Les Changements D'étatsDocument6 pagesLes Changements D'étatsHind BaddouPas encore d'évaluation
- Mouv Rect CoursDocument7 pagesMouv Rect Coursamine bouguernPas encore d'évaluation
- Mise A NiveauDocument16 pagesMise A Niveaughada el idirissiPas encore d'évaluation
- SP20 TE WB 05 19 - Retenir2Document5 pagesSP20 TE WB 05 19 - Retenir2Helena Ayala JamesPas encore d'évaluation
- FC.02 - Mouvement Vitesse AccelerationDocument3 pagesFC.02 - Mouvement Vitesse AccelerationDan CheridanPas encore d'évaluation
- Optique Physique 2021 PresentationDocument69 pagesOptique Physique 2021 PresentationNowe AhmadePas encore d'évaluation
- FT Panneau PIR AKDocument1 pageFT Panneau PIR AKKhadija OUKHAFPas encore d'évaluation
- OndesDocument125 pagesOndesTRAOREPas encore d'évaluation
- CH02 PropagationDocument27 pagesCH02 Propagationomarsahraoui240Pas encore d'évaluation
- TP1 - Capacité Thermique Massique Eau - CorrigéDocument3 pagesTP1 - Capacité Thermique Massique Eau - CorrigéSafa CHAGRENPas encore d'évaluation
- Dokumen - Tips - Travaux Diriges de Transfert Thermique Module En311Document39 pagesDokumen - Tips - Travaux Diriges de Transfert Thermique Module En311othman azPas encore d'évaluation
- Conduction ThermiqueDocument16 pagesConduction Thermiquehicham75% (4)
- Controle N1 Semestre 1 2BAC PC SM BIOFDocument134 pagesControle N1 Semestre 1 2BAC PC SM BIOFwaclapayPas encore d'évaluation
- Phys BâtimentDocument107 pagesPhys Bâtimentmbenzaconstructions2021Pas encore d'évaluation
- Chap-8 Bilans ThermiquesDocument28 pagesChap-8 Bilans Thermiquescherif003Pas encore d'évaluation
- ExtraitDocument8 pagesExtraitaq3446780Pas encore d'évaluation