Académique Documents
Professionnel Documents
Culture Documents
Corrigé PC TA4.
Transféré par
K.Tani-Eyatom PILINGATitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Corrigé PC TA4.
Transféré par
K.Tani-Eyatom PILINGADroits d'auteur :
Formats disponibles
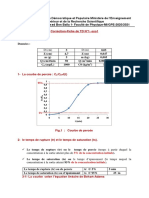
Année scolaire : 2022-2023 COMPOSITION RÉGIONALE DU 1ER SEMESTRE
Classe TA4
CORRIGE TYPE :
Chimie 1 : (4pts)
1. Définition
• Cinétique chimique : étude des vitesses de réactions chimiques (0,5pt)
• Catalyseur : une substance chimique qui augmente la vitesse d’une réaction sans intervenir dans
le bilan (0,5pt)
2. a) Equation bilan équilibrée : S2O82- + 2 I- ⎯⎯→ 2 SO42- + I2 (1pt)
b) Calcul des quantités de matière n1 d’ions peroxodisulfate et n2 des ions iodure
• n1 = C1 x V1 n2 = C2 x V2
= 0,2 x 0,5 = 0,4 x 0,5
n1 = 0,1 mol (0,5pt) n2 = 0,2 mol (0,5pt)
𝑛2 𝑛(𝐼)
c) n (S2O82-) = n1 = 0,1 mol = = 0,1 mol
2 2
𝑛2 𝑛1
= = 0,1 mol donc les réactifs sont dans les proportions stœchiométriques (1pt)
2 1
Chimie 2 : (6pts)
1. a) Réaction de substitution : réaction au cours de laquelle un ou plusieurs atomes monovalents se
substituent à un ou plusieurs atomes d’hydrogènes d’une molécule. (1pt)
b) Réaction qui nécessite la lumière pour s’effectuer est une réaction photochimique (0,5pt)
c) Noms et Formules des 4 dérivés chlorés du méthane et équations bilans. (0,5pt 4)
Noms Formules Equations bilans
monochlorométhane CH3Cl CH4 + Cl2 → CH3Cl + HCl
dichlorométhane CH2Cl2 CH3Cl + Cl2 → CH2Cl2 + HCl
trichlorométhane CHCl3 CH2Cl2 + Cl2 → CHCl3 + HCl
tétrachlorométhane CCl4 CHCl3 + Cl2 → CCl4 + HCl
2. a) Un fréon est un dérivé chlorofluoré du méthane ou d’éthane (1pt)
b) Usages du fréon : fluides réfrigérants et gaz propulseurs des aérosols (1pt)
c) Danger écologique : destruction de la couche d’ozone/gaz à effet de serre (0,5pt)
PHYSIQUE 1 : Gravitation (5pts)
1. a) Vrai (1pt) ; b) Faux (1pt) ; c) Faux (1pt).
2. a) iii (1pt) ; b) ii (1pt).
PHYSIQUE II (05 pts)
1. a) Calcul de la variation de température : Δθ = θ2 – θ1 ; Δθ = 60°C (1pt)
b) Quantité de chaleur reçue par l’eau : Q1 = mCeΔθ ; Q1= 125 700 J (0,75pt)
2. Energie électrique Q2 nécessaire pour le chauffage :
𝑸𝟏𝑿𝟏𝟎𝟎
Q2 = 𝟕𝟓 ; AN : Q2 = 167 600 J (1pt) car il y a 25% de perte.
3. Il s’agit de la transformation d’énergie électrique en énergie calorifique. (0,5pt)
4. Calcul de la durée t :
𝑸
Q2 = UIt sachant que P = UI on a Q2 = Pt soit t = 𝑷𝟐
A.N : t = 239,43 s = 3 min 59 s (0,75pt)
5) Calcul de l’intensité I :
𝒑 700
P = UI soit I = 𝒖 A.N : I = 220 ; I = 3,18 A (1pt)
Vous aimerez peut-être aussi
- Exercice Corrigé CinétiqueDocument13 pagesExercice Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- Examen 2er Semestre Mai 2017version Finale Enone Et CorrigeeDocument8 pagesExamen 2er Semestre Mai 2017version Finale Enone Et CorrigeeAziz JridiPas encore d'évaluation
- TD Cinetique ChimiqueDocument3 pagesTD Cinetique ChimiqueSimplice Assemien100% (3)
- TD de CinétiqueDocument14 pagesTD de CinétiqueDieu-donné Akin100% (2)
- Examen CB21 31 Mai 2012+corrigeDocument3 pagesExamen CB21 31 Mai 2012+corrigeOumaima El ImraniPas encore d'évaluation
- TD de Cinetique ChimiqueDocument6 pagesTD de Cinetique ChimiquefernandPas encore d'évaluation
- Résolutions Des TDDocument41 pagesRésolutions Des TDghislain AlowakinnouPas encore d'évaluation
- (C2) TDDocument4 pages(C2) TDMenePas encore d'évaluation
- Examen de Cin Et Cat Avec Correction Session de Ratt 2018-2019Document6 pagesExamen de Cin Et Cat Avec Correction Session de Ratt 2018-2019Chai MaePas encore d'évaluation
- Examen1 Réactivité Chimique FST-MeknèsDocument6 pagesExamen1 Réactivité Chimique FST-MeknèsayabourhdifaPas encore d'évaluation
- Exercices Cinétique (Loi de Vitesse) - EtingueDocument2 pagesExercices Cinétique (Loi de Vitesse) - EtingueLenz Daniel Jean PaulPas encore d'évaluation
- NormalDocument8 pagesNormalPhobos ElfaPas encore d'évaluation
- TD - Cpgo - 2023-2024 - Cinetique ChimiqueDocument4 pagesTD - Cpgo - 2023-2024 - Cinetique Chimiquedieudonnepooda71Pas encore d'évaluation
- Sciences-Physique S1-S3-1er-gr 2006Document5 pagesSciences-Physique S1-S3-1er-gr 2006Doro CisséPas encore d'évaluation
- TDcinét Chim.17-18Document3 pagesTDcinét Chim.17-18Joseph AmondPas encore d'évaluation
- Cinétique Chimique Exercices 01.TextMarkDocument4 pagesCinétique Chimique Exercices 01.TextMarkAbedPas encore d'évaluation
- Éaction Ersulfate - Odure: F D G D MDocument14 pagesÉaction Ersulfate - Odure: F D G D Mlamis b-zPas encore d'évaluation
- Electrochimie GP Ef 2017correctionDocument4 pagesElectrochimie GP Ef 2017correctionAbdelatif100% (2)
- Cinetique-chimique-Exercices 01 CompressedDocument4 pagesCinetique-chimique-Exercices 01 Compressedelmadani boutayebPas encore d'évaluation
- Corrigé S2 G1 2022Document5 pagesCorrigé S2 G1 2022yann.carly BoulinguiPas encore d'évaluation
- TD Equilibre 23-24Document2 pagesTD Equilibre 23-24diderPas encore d'évaluation
- Cinétique ChimiqueDocument1 pageCinétique ChimiqueCarla GastaldelloPas encore d'évaluation
- Examen de Cin Et Cat Avec Correction Session Normale 2018-2019Document6 pagesExamen de Cin Et Cat Avec Correction Session Normale 2018-2019Chai Mae100% (1)
- Chimie-1ereC D TI-Eval4Document13 pagesChimie-1ereC D TI-Eval4paulfrancoisngnintedemPas encore d'évaluation
- Tdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanDocument5 pagesTdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanAlassane TraorePas encore d'évaluation
- Exercices CINETIQUE L2-2016-2017Document4 pagesExercices CINETIQUE L2-2016-2017Fati Fleur100% (5)
- Exos CH 04Document3 pagesExos CH 04lol testPas encore d'évaluation
- TD Cin & Cat SMC S5 .Document32 pagesTD Cin & Cat SMC S5 .Chai Mae100% (3)
- EF1 Corrige Chimie3 19012016Document5 pagesEF1 Corrige Chimie3 19012016martin souman moulsiaPas encore d'évaluation
- C2Chim Suivi Cinetique ExercicesDocument8 pagesC2Chim Suivi Cinetique ExercicesMohamed El OuahdaniPas encore d'évaluation
- TD1 023 024Document7 pagesTD1 023 024ilyesfares49Pas encore d'évaluation
- Corrigé Du Devoir de Synthèse N°1: Chimie Exercice 1Document4 pagesCorrigé Du Devoir de Synthèse N°1: Chimie Exercice 1Riadh MarouaniPas encore d'évaluation
- Cinétique TDDocument5 pagesCinétique TDBadr MouslimPas encore d'évaluation
- M28 - Cinétique - TD1 - CorrectionDocument7 pagesM28 - Cinétique - TD1 - CorrectionHassan DriouachPas encore d'évaluation
- Vitesse 2Document5 pagesVitesse 2lemiaPas encore d'évaluation
- Serie de TD N°123 L2 Raff 22 23Document5 pagesSerie de TD N°123 L2 Raff 22 23Clash of Clans Bilal DzPas encore d'évaluation
- CC2 CorrectionDocument4 pagesCC2 Correctionbessama84Pas encore d'évaluation
- Compo2012SBT Facou 2ère PériodeDocument3 pagesCompo2012SBT Facou 2ère PériodeOumar TraoréPas encore d'évaluation
- 08 Evolution SpontaneeDocument3 pages08 Evolution SpontaneeChartier JulienPas encore d'évaluation
- Examen5 Réactivité Chimique FST-MeknèsDocument19 pagesExamen5 Réactivité Chimique FST-Meknèsyakubuojonugwa32Pas encore d'évaluation
- Cinétique Chimique Exercices 04.TextMarkDocument16 pagesCinétique Chimique Exercices 04.TextMarkAbedPas encore d'évaluation
- Bac PCDocument5 pagesBac PCOumar KakoroPas encore d'évaluation
- PC 2nde S, Tle A, Tle DDocument4 pagesPC 2nde S, Tle A, Tle DAGBANGBA AbdourahmanePas encore d'évaluation
- Série Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFDocument15 pagesSérie Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFSaifeddine MakniPas encore d'évaluation
- 0607DM2 PDFDocument3 pages0607DM2 PDFFoudil Laouici100% (1)
- Concours 2013 (+sol.) Proposition EPSTTDocument19 pagesConcours 2013 (+sol.) Proposition EPSTTNidal BestPas encore d'évaluation
- Correction Td3Document7 pagesCorrection Td3Harakat ElhoucinePas encore d'évaluation
- CO1 TS1 2024 Iadb - WahabdiopDocument4 pagesCO1 TS1 2024 Iadb - Wahabdioppapa samba sarrPas encore d'évaluation
- Revision T°s ChimieDocument4 pagesRevision T°s ChimiebipPas encore d'évaluation
- Cu Ag MG Cu Ag MG POCDocument3 pagesCu Ag MG Cu Ag MG POCorsiny clinton TCHAPTCHETPas encore d'évaluation
- TD2 Correction PDFDocument8 pagesTD2 Correction PDFKhadija LakhdiriPas encore d'évaluation
- Corrigé Sujet L2 Sciences Physiques Du 1er GROUPE Normal 19 PDFDocument1 pageCorrigé Sujet L2 Sciences Physiques Du 1er GROUPE Normal 19 PDFAlioune Fall BaPas encore d'évaluation
- Correction Epreuve de Chimie Au Probatoire C D Et E 2022Document3 pagesCorrection Epreuve de Chimie Au Probatoire C D Et E 2022possibradyPas encore d'évaluation
- 6-TDPCSIcinetique-2015Document8 pages6-TDPCSIcinetique-2015Nguissaly SonkoPas encore d'évaluation
- SP SUJET TS2-01-2022-iakaf-WahabDiopDocument4 pagesSP SUJET TS2-01-2022-iakaf-WahabDiopSerigne saliou GayePas encore d'évaluation
- Examen National Physique Chimie SPC 2019 Rattrapage SujetDocument7 pagesExamen National Physique Chimie SPC 2019 Rattrapage Sujethicham lahdissou100% (1)
- 6 Exc2001Document5 pages6 Exc2001Yassine RakchoPas encore d'évaluation
- Omega 13 (2010) - BoiloverDocument38 pagesOmega 13 (2010) - BoiloverAlain-Claude AMBOUROUEPas encore d'évaluation
- Al Hajjar HikmatDocument244 pagesAl Hajjar HikmatEya Hentati100% (1)
- PhotocatalyseDocument3 pagesPhotocatalyselaoliana0% (1)
- Traveaux Pratique OPU: Variation de La Perte de Charge Sur Une Colonne de Distillation DiscontinnueDocument9 pagesTraveaux Pratique OPU: Variation de La Perte de Charge Sur Une Colonne de Distillation Discontinnuenour nour100% (1)
- Extraction Des AromatiqueDocument69 pagesExtraction Des Aromatiquemoha khb88% (8)
- Chapitre 1 MRDocument12 pagesChapitre 1 MRClosed WayPas encore d'évaluation
- TP N° 5 (Oxydo-Réduction) PDFDocument7 pagesTP N° 5 (Oxydo-Réduction) PDFNacer NY Yahyaoui100% (1)
- Cours PDFDocument20 pagesCours PDFarezkibougareche2022Pas encore d'évaluation
- Dimensionnement D'une Nouvelle Colonne de Stabilisation de Condensat Hors Spécification (Dé-Isopentaniseur)Document115 pagesDimensionnement D'une Nouvelle Colonne de Stabilisation de Condensat Hors Spécification (Dé-Isopentaniseur)Tul IpePas encore d'évaluation
- Correction CombustionDocument4 pagesCorrection CombustionUmmah ClPas encore d'évaluation
- Chapitre 1 Combustion Et CombustibleDocument79 pagesChapitre 1 Combustion Et CombustibleRyad AsmaPas encore d'évaluation
- 12 Alimentation CarburationDocument20 pages12 Alimentation CarburationMarouane Sr4Pas encore d'évaluation
- Van Marcke - Verwarming/Chauffage - Cataloog/Catalogue 2010Document82 pagesVan Marcke - Verwarming/Chauffage - Cataloog/Catalogue 2010Van MarckePas encore d'évaluation
- Réactions Spécifiques DesDocument4 pagesRéactions Spécifiques Desmechergui mariemPas encore d'évaluation
- Corrigé Fiche N°1 Exo 1Document5 pagesCorrigé Fiche N°1 Exo 1Elaziouti AbdelkaderPas encore d'évaluation
- Thermodynamique Exercices T7 - ThermochimieDocument4 pagesThermodynamique Exercices T7 - ThermochimieIhsan Mokhlisse100% (9)
- Exposer de Physique ChimieDocument7 pagesExposer de Physique ChimieAkobe Urbain NdePas encore d'évaluation
- Thermo - Exercices Corrigés PDFDocument88 pagesThermo - Exercices Corrigés PDFayoub oubeddaPas encore d'évaluation
- Bechouni Med SifIslamDocument81 pagesBechouni Med SifIslamRá ÎdPas encore d'évaluation
- DM COI - Distillation Atmosphérique PDFDocument5 pagesDM COI - Distillation Atmosphérique PDFBOULAZREG RabahPas encore d'évaluation
- Synthèse de L'acide SulfuriqueDocument20 pagesSynthèse de L'acide Sulfuriquenabil_k5200100% (9)
- Projet PFEDocument2 pagesProjet PFEH'bibi MouhamedPas encore d'évaluation
- Nouveau Microsoft Office PowerPoint PresentationDocument11 pagesNouveau Microsoft Office PowerPoint PresentationHàm ZaPas encore d'évaluation
- Ds 2 CorrigéDocument22 pagesDs 2 CorrigéSouad BouafiaPas encore d'évaluation
- Catalogue E-Learning IAP 2021Document206 pagesCatalogue E-Learning IAP 2021sa3idPas encore d'évaluation
- Exposé GazDocument20 pagesExposé GazMustapha Mostapha AbidiPas encore d'évaluation
- Taxol PDFDocument38 pagesTaxol PDFYassine SabekPas encore d'évaluation
- Adsorbtion de L'Acide Chlorhydrique Par ArgileDocument8 pagesAdsorbtion de L'Acide Chlorhydrique Par Argilecélia fer100% (2)
- Charbon ActifDocument14 pagesCharbon ActifMedElazzPas encore d'évaluation
- La Pétrochimie Et Le Raffinage Du PétroleDocument3 pagesLa Pétrochimie Et Le Raffinage Du Pétrolemechergui75% (4)