Académique Documents
Professionnel Documents
Culture Documents
Obstétrique D1 U.ka-1
Transféré par
alexiskandeykom03Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Obstétrique D1 U.ka-1
Transféré par
alexiskandeykom03Droits d'auteur :
Formats disponibles
1
REPUBLIQUE DEMOCRATIQUE DU CONGO
MINISTERE DE L’ENSEIGNEMENT SUPERIEUR ET
UNIVERSITAIRE ET DE LA RECHERCHE SCIENTIFIQUE
FACULTE DE MEDECINE
DEPARTEMENT DE GYNECOLOGIE ET OBSTETRIQUE
NOTES DE COURS
D’OBSTETRIQUE
CT Dr MBANGAMA MUELA Andy
Gynécologue-Obstétricien
A l’usage des étudiants de 1er Doctorat
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
2
INTRODUCTION
Définition de l’obstétrique
Etymologie :
Ob = Devant
Stare = Etre debout
Au début l’obstétricien était considéré comme celui qui se tient debout devant la mère en travail
d’accouchement.
L’obstétrique est donc une partie de la médecine qui se consacre à l'étude de la grossesse et de
l'accouchement ainsi que des phénomènes qui leur sont associés.
Objectifs du cours d’obstétrique
A la fin de cette formation, l’apprenant doit être capable de :
1) Décrire l’anatomie et la physiologie des organes et autres structures impliqués dans la
reproduction chez la femme;
2) Décrire l’anatomie et les fonctions vitales du fœtus et des annexes fœtales;
3) Décrire les rapports anatomiques et physiologiques entre le fœtus et les structures
maternelles de la reproduction;
4) Reconnaître la grossesse en cas d’aménorrhée;
5) Distinguer les modifications physiologiques de grossesse de celles relevant des
pathologies gravidiques;
6) Proposer des examens paracliniques pour asseoir un diagnostic;
7) Assurer une CPN et une surveillance de la grossesse jusqu’à l’accouchement;
8) Décrire les principales étapes de l’accouchement normal et leur méthode de surveillance;
9) Choisir entre une PEC immédiate et un transfert de la patiente vers des meilleures
compétences;
10) Diriger un accouchement normal;
11) Organiser l’accueil du nouveau-né;
12) Surveiller le post-partum et la lactation.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
3
TABLE DES MATIERES
Ière PARTIE : GROSSESSE NORMALE ET ACCOUCHEMENT NORMAL
1. Fécondation, migration, nidation et croissance embryo-fœtale 5
2. Les modifications physiologiques maternelles pendant la grossesse 9
3. Le Bassin 13
4. Moteur utérin 24
5. Mobile fœtal 28
6. Annexes fœtales 40
7. Sémiologie obstétricale et surveillance d'une grossesse normale 45
8. Accouchement normal 53
9. Surveillance du travail et de l'accouchement 58
10. Les présentations 65
11. Accueil du nouveau-né 66
12. Le post-partum 68
13. La lactation et l’allaitement 71
IIème PARTIE : PATHOLOGIES GRAVIDIQUES
1. Petits ennuis de la grossesse 73
2. Placenta prævia 75
3. Hématome rétro-placentaire 79
4. Rupture utérine 81
5. Hémorragie de Benkiser 83
6. Rupture sinus marginal 83
7. Hypertension artérielle et grossesse 84
8. Eclampsie 88
9. HELLP Syndrom 94
10. Hématome sous-capsulaire du foie 95
11. Stéatose hépatique aigue gravidique 97
12. Grossesse multiple 98
13. Oligoamnios 103
14. Polyhydramnios 104
15. Rupture prématuré des membranes 108
16. Procidence du cordon 112
17. Menace d’accouchement prématuré 115
18. Accouchement prématuré 120
19. Dépassement de terme 119
20. Retard de Croissance Intra-Utérin ou souffrance fœtale chronique (SFC) 123
21. Mort fœtale in utero 126
22. Embolie amniotique 128
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
4
PATHOLOGIES MEDICO-CHIRURGICALES ASSOCIEES A LA GROSSESSE
1. Anémie et grossesse 129
2. Drépanocytose et grossesse 130
3. Diabète et grossesse 131
4. Obésité et grossesse 134
5. Infection urinaire et grossesse 135
6. Cardiopathies et grossesse 137
7. Pneumopathies et grossesse 139
8. Hépatopathies et grossesse 140
9. Hyperémèse et grossesse 141
10. Appendicite et grossesse 143
11. Néphropathies et grossesse 144
12. Vasculopathies autres que HTA et grossesse 145
13. IST et grossesse 146
14. Traumatismes et grossesse 149
15. Iso-immunisation materno-fœtale 150
16. Paludisme et grossesse 152
DYSTOCIES
1. Dystocie mécanique 154
2. Dystocie dynamique 155
3. Dystocie due aux parties molles : Utérus cicatriciel 157
4. Dystocie due au mobil fœtal 158
a. Présentation du siège 158
b. Présentation transversale 160
c. Présentations céphaliques autres que du sommet 160
d. Macrosomie fœtale 160
e. Souffrance fœtale aigue (SFA) 162
5. Dystocie due aux annexes fœtales 167
6. Lésions traumatiques maternelles 168
7. Inversion utérine 170
8. Pathologies du post-partum 171
a. Fièvre puerpérale 171
b. Hémorragie du post partum 172
c. Endométrite du post partum 178
d. Maladies thrombo-emboliques 178
e. Maladies liées à l’allaitement 178
9. Thérapeutique obstétricale 180
10. Soins obstétricaux et néonataux d’urgence (SONU) 180
11. Interventions obstétricales 181
a. Expression abdominale 181
b. Rupture artificielle des membranes 181
c. Episiotomie 182
d. Césarienne 184
e. Induction du travail d’accouchement 189
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
5
Ière PARTIE : GROSSESSE NORMALE ET ACCOUCHEMENT NORMAL
I.1. FECONDATION, MIGRATION, NIDATION ET CROISSANCE EMBRYO-FŒTALE
1. FECONDATION
La fécondation correspond à la fusion entre un gamète mâle (spermatozoïde) et un gamète femelle
(ovule mûre) généralement au niveau du tiers externe de la trompe pour donner une cellule
unique, l'œuf qui sera à l'origine de l'embryon.
Actuellement, il faut différencier la fécondation naturelle de la fécondation artificielle. Les
améliorations des techniques de procréation médicalement assistée (PMA) ont permis de réaliser,
aujourd’hui couramment, des fécondations in vitro, en dehors du corps de la femme.
La fécondation peut même être forcée par l'insertion du spermatozoïde directement dans l'ovocyte
(c'est l'injection intra-cytoplasmique de spermatozoïdes). FIVETE (= Fécondation In Vitro Et
Transfert d’Embryon) ou I.U.D (= Insémination intra-Utérine Directe).
2. LES ETAPES ET CONSEQUENCES DE LA FECONDATION
La fécondation naturelle humaine nécessite la présence d’un ovocyte, issu de l’ovaire par
ovulation (ovogénèse), et d’un spermatozoïde (issue de la spermatogénèse) au niveau de la
trompe de Fallope. La rencontre des deux gamètes et leur fusion n’est possible qu’après
reconnaissance de facteurs spécifiques sur les deux cellules, ce qui empêchera alors d’autres
spermatozoïdes de pénétrer dans l’ovule.
A la suite de la fécondation, il y aura amorce d’un processus de développement et de croissance
devant aboutir à un enfant à partir d’une structure microscopique, reconstitution du capital
chromosomique habituel de l’espèce humaine (= 46 chromosomes) et reproduction d’un individu
à partir des génotypes existants.
3. MIGRATION ET PRE-IMPLANTATION
Si la fécondation (qui a lieu dans la partie ampullaire de la trompe) est réussie, l'ovule migre le
long de la trompe jusqu'à la cavité utérine (cette migration dure six jours). Simultanément, le
zygote se divise plusieurs fois sans augmentation du volume total dans un premier temps car il est
encore enveloppé par la zone pellucide. Des cellules filles naissent de ces divisions et on parle
désormais du stade des blastomères. La compaction a lieu dès 16 cellules environ (la morula) ;
durant ce processus, les cellules externes (les trophoblastes) forment une paroi épithéliale
compacte. Elles sont liées entres elles par des complexes de liaison et des microvillosités croissent
sur leur surface externe. Les cellules internes sont ainsi abritées de l'influence du milieu externe et
elles peuvent se différencier indépendamment. L'embryoblaste se forme à l'intérieur.
Simultanément, une cavité remplie de liquide se constitue également, le blastocœle. On parle
désormais de blastocyste. Ce dernier s'extrait de la zone pellucide (hatching) et il se trouve
désormais à l'entrée de la cavité utérine en tant que blastocyste libre. On peut dès lors distinguer
deux couches cellulaires chez l'embryoblaste: l'épiblaste et l'hypoblaste. Par la suite, le blastocyste
libre se fixe à la muqueuse de l'utérus par le pôle où se trouve l'embryoblaste; ce processus est
appelé adplantation. Le blastocyste dégrade la muqueuse utérine à l'aide de ses enzymes et il y
pénètre progressivement. Ainsi débute l'implantation.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
6
4. IMPLANTATION ou NIDATION
Ce processus s'étend de la fin de la première semaine de développement embryonnaire au moment
de l'éclosion du blastocyste jusqu'à l'ébauche de la circulation placentaire primitive au milieu de la
seconde semaine de développement.
Au niveau de l’endomètre, alors que rien n’est à signaler au niveau de la couche basale et de la
couche spongieuse de l’endomètre, la couche superficielle (aussi appelée couche fonctionnelle =
la compacte) qui représente les 2/3 de l'endomètre, s´apprête à accueillir l´œuf. Elle subit 3 types
de modifications qui le font changer de nom (= DECIDUA ou CADUQUE) :
- il y a poursuite de l'évolution lutéale de l'épithélium glandulaire dont le glycogène devient
apical tandis que la sécrétion apparaît dans la lumière glandulaire; on peut dire que c’est la
constitution d’un stock alimentaire (glycogène) ;
- l’accentuation de l’œdème stromal périvasculaire ; c’est l’installation d’un coussin d´accueil ;
- l´accroissement de la congestion vasculaire ; c’est l’établissement d’une voie de
ravitaillement.
Les étapes de l'implantation commencent par une apposition du blastocyste à la muqueuse
utérine ce produisant dans une partie spécifique de la paroi utérine.
Une implantation du blastocyste hors de cette zone donne lieu à une grossesse extra-utérine, avec
des conséquences graves pour la santé. Les étapes de l'implantation du blastocyste dans
l'endomètre utérin se divisent en trois phases: l'apposition, l'adhésion, et l'enfouissement.
L'apposition ne peut se réaliser que dans une fenêtre temporelle précise au cours du cycle en
rapport avec la maturation de la muqueuse utérine. Lorsque l'adhésion à la muqueuse est réalisée,
les cellules périphériques du blastocyste, le trophophoblaste, sont différenciées en deux
populations: le syncytiotrophoblaste (ST, externe) et le cytotrophoblaste (CT, interne). Par leur
action lytique, les cellules du ST érodent plusieurs structures de la muqueuse utérine et induisent
la réaction déciduale de cette muqueuse. Ce processus conduit à l'enfouissement du blastocyste
dans la muqueuse qui est alors entièrement entouré par les cellules du ST. Au cours de la
deuxième semaine, des vacuoles extra-cytoplasmiques apparaissent dans le ST. Elles confluent
ensuite pour former des lacunes qui seront ultérieurement remplies par le sang maternel provenant
des vaisseaux érodés par l'activité lytique du ST. La mise en place de la circulation utéro-
placentaire primitive est ainsi achevée.
Les étapes de l'implantation résultent d'une cascade de mécanismes moléculaires d'interactions
entre les cellules trophoblastiques d'une part, et les cellules et la matrice extracellulaire de la
muqueuse utérine d'autre part. Ces interactions commencent déjà au moment de l'éclosion du
blastocyste (signaux pré-implantatoires) pour modifier les propriétés structurelles et
fonctionnelles de l'utérus qui favorisent le déplacement du blastocyste vers le site d'implantation
et la modification de ce dernier pour favoriser l'adhésion du blastocyste. Les interactions entre
blastocyste et épithélium utérin assurent l'orientation et l'adhésion à la paroi. Celles entre le
blastocyste et l'endomètre régulent l'invasion trophoblastique et l'enfouissement dans la
muqueuse.
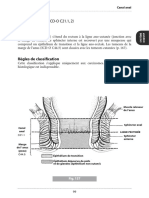
Adhésion du blastocyste Zone d'implantation normale
1. Cavité utérine ; 2. Isthme ; 3. Trompes ; 4. col
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
7
Plusieurs facteurs peuvent provoquer des anomalies de l'implantation. Plusieurs sites hors de la
zone d'implantation au niveau du corps de l'utérus ou même à l'extérieur de l'utérus permettent
une fixation et un développement du blastocyste (grossesse extra-utérine).
Zones possibles d'implantation ectopique
1. ovarienne 4. intersticielle 6. abdominale (sur une anse
2. infundibulaire 5. utérine basse (futur placenta intestinale)
3. tubaire (les plus fréquentes) praevia) 7. pelvienne
5. PERIODE EMBRYONNAIRE
La période embryonnaire correspond aux huit premières semaines de la grossesse.
Elle est divisée en une période pré-embryonnaire (de la 1e à la 3e semaine), occupée par la mise
en place des trois feuillets embryonnaires au cours de la gastrulation, suivie de la période
embryonnaire proprement dite (4e à la 8e semaine) pendant laquelle se développement les
différentes ébauches embryonnaires des organes.
Cette mise en place s'effectue grâce à l'interaction de facteurs génétiques et environnementaux,
coordonnés avec précision dans l'espace et dans le temps qui permettent d'établir des champs
d'induction tissulaire.
C'est pendant la période embryonnaire que les risques de malformations congénitales sont les
plus grands. Avant, les malformations conduisent le plus souvent à un avortement prématuré alors
qu'après l'incidence des malformations et leur gravité sont plus réduites.
Les facteurs tératogènes principaux sont les maladies infectieuses, les substances chimiques et
médicamenteuses et les radiations ionisantes.
6. PERIODE FŒTALE
La période fœtale englobe environ les deux derniers trimestres de la grossesse, c'est-à-dire 30
semaines durant lesquelles le fœtus développe ses systèmes d'organes. Durant cette période, la
femme subit un monitorage pour pouvoir rapidement saisir des anomalies de la grossesse. Il existe
aujourd'hui à cet effet diverses possibilités de diagnostic prénatal non-invasives et invasives en
fonction du résultat escompté. Le fœtus, et encore d'avantage l'embryon, sont très sensibles à des
substances tératogènes. Ces dernières peuvent provoquer des malformations des systèmes
d'organes en formation. La possibilité d'un diagnostic prénatal amène naturellement à la question
d'une interruption volontaire de la grossesse dans le cas où une maladie grave a été décelée.
7. CROISSANCE EMBRYO-FŒTALE
Les principales étapes (périodes) du développement sont embryonnaire et fœtale.
- La période embryonnaire va jusqu’à 8 semaines. Entre 36 et 48 h après, l’œuf est au stade de 4
cellules (= blastomères). Entre 48 et 72 heures, l’œuf a 8 cellules et entre 72 et 96 heures, il
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
8
atteint 16 cellules ; chaque division donne naissance à des grandes cellules (macromères) et à
de petites cellules (micromères). Les premières (macromères) s’organisent pour rester à
l’intérieur et les dernières (micromères) à la périphérie, ceci au stade de morula. Les grandes
cellules constituent le bouton embryonnaire tandis que les petites cellules le trophoblaste.
On peut retenir qu'à 8 semaines l'embryon pèse 1 g et mesure 2,1 à 2,5 cm; au 20e jour, on
assiste à l'ébauche cardiaque et à l'installation des premiers îlots vasculaires; au milieu de la 2e
semaine de grossesse, la nidation est effectuée, la différenciation cellulaire est amorcée, et le
sang maternel commence à baigner l'ébauche placentaire; vers le 25e jour, la circulation foeto-
placentaire est définitivement établie; au 26e jour, les bourgeons des membres apparaissent; au
30e, le pédicule embryonnaire est individualisé; au 45e s'effectue la différenciation génitale
des gonades; et au 60e a lieu le début de la différenciation des voies génitales mâles et
femelles. Cette période est dominée par les mitoses (c’est l’hyperplasie) ;
- La période fœtale va de 8 semaines jusqu’à terme. Elle commence avec la segmentation en
différentes parties du corps dès après 8 semaines, de sorte qu'à 12 semaines le fœtus a son sexe
déjà différencié et les ongles apparaissent nettement, tandis que le liquide amniotique atteint 30
ml. A 16 semaines, le fœtus dont le sexe est reconnaissable, pèse 100 g et mesure 14 à 17 cm.
A 20 semaines, il pèse 300 g, tandis qu'à 24 semaines, il pèse 600 g. A la fin de la 28e semaine,
il mesure 35 cm; cette taille sera de 40 cm à 32 semaines (1700 g), 45 cm à 36 puis 50 cm à
terme. Cette période comporte :
jusqu’à 16 semaines, une prolifération cellulaire sous l’influence conjointe de
facteurs génétiques, ovulaires intrinsèques et environnementaux ;
de 16 à 32 semaines, une hyperplasie associée à l’hypertrophie, avec prédominance
de cette dernière ; on note aussi un dépôt de graisses ;
de 32 à 40 semaines, une prédominance de l’hypertrophie cellulaire.
La régulation de la croissance fœtale est assurée par un système complexe de facteurs, les uns
probablement intrinsèques, les autres en rapport avec le placenta, et d’autres encore extrinsèques.
Parmi les facteurs intrinsèques de régulation de la croissance fœtale figurent :
- les dispositions génétiques propres à chaque individu, à chaque famille, à chaque tribu, et à
chaque race ;
- le sexe du fœtus ; c’est en fait au chromosome Y qu’on attribue la différence de 150 – 200
grammes en faveur du sexe masculin (effets des hormones testiculaires) ; des éléments soit
circulant dans le sang maternel, soit faisant partie de la structure cellulaire du fœtus ;
- les stimuli essentiellement hormonaux fœtaux ; il s’agit surtout des IGFs et leurs protéines
porteuses, ainsi que l’insuline fœtale (voir plus loin).
Parmi les facteurs placentaires on note :
- la qualité de l’implantation du trophoblaste (proportionnelle au degré d´invasion de
l’endothélium des artères spiralées de la Compacte) ;
- le rôle du placenta de transmetteur de nutriments au fœtus ;
- la fonction endocrinienne du placenta qui est pourvoyeur d´hormones (comme la HPL)
susceptibles de promouvoir la croissance fœtale.
- Parmi les facteurs extrinsèques de régulation de la croissance fœtale il faut citer la nutrition
maternelle, ou plutôt son état métabolique, notamment sa capacité à utiliser l’insuline. Etant
donné que le fœtus utilise le glucose comme nutriment principal, et qu’il le reçoit en majeure
partie de l'apport maternel par voie de diffusion facilitée à raison de 20 milligrammes/minute,
tout état de surcharge ou de déficience glucidique maternelle retentit sur la croissance fœtale.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
9
I.2. LES MODIFICATIONS PHYSIOLOGIQUES MATERNELLES PENDANT LA
GROSSESSE
Depuis la fécondation jusqu'à l'accouchement l'organisme maternel subit des changements
endocriniens ayant de grands retentissements au plan général. La grossesse entraîne non
seulement des modifications des organes pelviens mais de l’ensemble du corps. Ces modifications
permettent le meilleur environnement possible pour le fœtus.
Comprendre ces mécanismes est évidemment indispensable pour la compréhension des processus
pathologiques de la grossesse et du post partum. Ces adaptations peuvent parfois mimer une
pathologie ou masquer une pathologie préexistante.
1. Au niveau des organes génitaux
Il y aura au niveau de :
a. L’Utérus
- Augmentation poids et volume (non gravide 70 g, capacité 10 mL vs 1.100 g à terme et 5-20L.
- hypertrophie des cellules myométriales et augmentation de la vascularisation (peu
d’hyperplasie) stimulée par les œstrogènes (progestérone?) jusqu’à 12 semaines et ensuite par
la tension liée à la croissance fœtale et le liquide amniotique.
- Il y a également accumulation de tissu fibreux et élastique. La paroi de l’utérus, d’abord
épaisse, s’amincit pendant le troisième trimestre (≈1,5cm).
- Modification de la forme (poire en dehors de la grossesse, sphérique à 12 semaines, puis
ovoïde). A partir de 12 semaines l’utérus sort du pelvis et subit une dextrorotation
- Modification de sa contractilité : au 1er et 2ème trimestre, il existe des contractions sporadiques
et indolores (Braxton Hicks 1872), au 3ème trimestre, elles deviennent plus fréquentes, rythmées
entraînant un inconfort. Elles sont à la base d’un « Faux début de travail » si pas d’action au
niveau du col utérin et sont responsables d’une diminution du flux sanguin utérin sans effet sur
le flux ombilical.
b. Col utérin
- Ramollissement et cyanose liés à l’augmentation de la vascularisation et à l’œdème
- Hypertrophie-plasie des glandes endocervicales (à terme ½ du col), éversion ectopie
- Bouchon muqueux qui est la conséquence de la coagulation de la glaire cervicale
c. Ovaires
- Anovulation
- Corps jaune menstruel est transformé en corps jaunes gravidiques qui va continuer à synthétiser
la progestérone (6 – 7 semaines de grossesse) pour le maintien de la grossesse.
d. Vagin
- Hyperhémie, cyanose, augmentation des secrétions, pH 3,5 - 6 (glycogène, lactobacilles
acidophiles défense bactériologique)
2. Au niveau du système cardiovasculaire
On assiste à un surcroît de charge hémodynamique (+ 30%) au cours de la grossesse, du fait de
l'augmentation du volume de sang circulant. Ces modifications ont été attribuées aux hormones
stéroïdes de la grossesse.
- La grossesse s’accompagne d’une augmentation du lit vasculaire maternel. Qui concerne plus
le plasma (± 1000 ml, contre 450 ml seulement de globules rouges), il se crée un certain
déséquilibre entre contenant et contenu. C’est alors la fameuse Hémodilution.
- La grossesse implique de la part de l’œuf en général, du fœtus en particulier, une demande
impérative en fer du fait notamment de l’exigence de l’érythropoïèse fœtale des nouveaux
globules rouges ; le transfert du fer total est de ± 1 gramme de la mère vers le fœtus, que la
mère en soit suffisamment pourvue ou pas.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
10
- La grossesse implique également une exigence supplémentaire en acide folique, en vitamine
B12, et en fer, du fait de la synthèse des purines si nécessaires dans la réplication des molécules
d’ADN lors des mitoses ovulaires.
Ces 3 facteurs provoquent alors à une baisse des valeurs hématologiques réalisant le contexte
appelé Anémie physiologique de da la grossesse = ferriprive & folioprive = adaptation.
La pression artérielle produit du débit cardiaque par les résistances périphériques diminue de 20 à
30 % de façon proportionnelle à la baisse des résistances périphériques de 7 à 28 semaines de
grossesse puis ré-augmente. Le TA chez la femme enceinte doit être prélevée en position semi –
assise ou décubitus latéral.
3. Au niveau du système respiratoire
On observe une réduction de l'espace thoracique due à l'élévation diaphragmatique et à
l'horizontalisation des côtes (ce qui réduit la capacité respiratoire), mais cependant compensées
par l'évasement de la poitrine et l'augmentation de la fréquence respiratoire, avec accroissement
de près de 20 % de la consommation en oxygène (ce qui peut se traduire par une impression de
gêne respiratoire).
Au début de la grossesse la femme respire plus profondément mais pas plus fréquemment sous
l’influence de la progestérone. La ventilation alvéolaire est augmentée d’environ ½ par rapport à
avant la grossesse, l’O2 augmente et la CO2 diminue (l’alcalose respiratoire chronique est
compensée par une augmentation d’excrétion de bicarbonate par les reins). La capacité vitale est
ainsi maintenue avec une possible sensation d’essoufflement.
4. Au niveau du système urinaire
- Le ramollissement uretéro-vésical global dû aux œstrogènes favorise l’accumulation urinaire,
ce qui est propice à la pullulation microbienne. Ce même ramollissement est responsable d’une
certaine réduction de l’effet “ valve ” vésico-uretérale, ce qui crée des reflux vésico-uretéraux
épisodiques.
- L’augmentation sensible du taux de filtration glomérulaire (30-50%) ajoute à l’inflation
urinaire. Cet effet reste perceptible jusqu'à 2 mois après l’accouchement.
- La compression de l’utérus gravide sur les points urétéraux moyens ajoute à l’effet ci-dessus.
- L’accentuation de la dextroversion et de la dextrorotation de l’utérus au cours de la grossesse
favorise la dilatation de l’uretère droit, d’où la fréquence plus accrue de l’infection urinaire du
côté droit.
- Il faut aussi signaler l'abaissement du seuil rénal du glucose, ce qui peut donner lieu à la
présence de ce dernier dans l'urine alors que la glycémie est inférieure au taux de 180 mg/dl au
dessus duquel le sucre passe enfin dans l'urine chez tout individu.
5. Au niveau du tube digestif
- Diminution du transit lié à des facteurs hormonaux (progestérone) et mécaniques (déplacement
progressif – croissance de l’utérus) ;
- Reflux œsophagien, pyrosis, constipation
- Temps de vidange de l’estomac allongé (nausées) ! anesthésie générale
- Hémorroïdes (suite à l’augmentation de la pression au niveau de la veine porte)
- Gencives: cyanose, saignements, épulis
- Foie : surcharge métabolique des deux premiers trimestres avec comme conséquence la baisse
de la concentration des protéines sériques porteuses et la baisse de la pression oncotique, ce qui
va provoquer une accélération relative de la vitesse de sédimentation et l’apparition des
œdèmes ; accroissement de la synthèse de fibrinogène et de lipides (hyperlipidémie gravidique
responsable de l'hyperviscosité sanguine et de l’hypercoagulabilité au cours de la grossesse) ;
accroissement du taux de cholestérol dans la bile ainsi que l’hypotonie relative des voies
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
11
biliaires qui prédisposent à la cholélithiase et à la cholécystite ; il y a donc une possibilité de
stase vraie et donc d'ictère et prurit ; pas de modifications histologiques, synthèses protéines
(fibrinogène, globulines….)
- Pancréas : la glande produit plus d'insuline du fait de l'antagonisme de la progestérone, du
cortisol et de la HPL (donc la production est accrue) et de la mobilisation des réserves
périphériques (ce qui peut perturber l'épreuve de surcharge glucidique).
6. Au niveau du système endocrinien
a. Hypophyse
- Augmentation de la taille x 2 – 3
Lobe antérieur
- Production de la Prolactine avec pour rôle la préparation de la lactation, le transfert d’eau à
travers le placenta qui entraîne un feed back inhibiteur par HPL (hormone lactogène
placentaire), l’action lactotrope de la prolactine est inhibée par la progestérone et les
œstrogènes, ce qui justifie l’absence normale de la monté laiteuse au cours de la grossesse. Sa
présence devra faire suspecter entre autre une insuffisance placentaire.
- Diminution FSH et LH (feed-back négatif des œstrogènes).
- Hormone de croissance inhibée (HPL)
- ACTH augmentée malgré l’augmentation du cortisol, le feed back normal semble inhibé (?
Origine placentaire)
- TRH normale, les changements dans l’activité thyroïdienne ne sont pas liés à l’hypophyse
Lobe postérieur
- (stockage) ocytocine : secrétions pulsée pendant le travail
b. Thyroïde
- La glande s'hypervascularise en s'hypertrophiant, ce qui fait augmenter son volume. Elle
produit alors plus de T4 (thyroxine) totale. La concentration de thyroxine libre (la fraction
métaboliquement active) reste cependant inchangée, tandis que celle de la T3 diminue même
(surtout durant les 2 derniers trimestres). L'accroissement du métabolisme basal au cours de la
grossesse est donc imputable, non à la thyroïde, mais à 1) la morphogenèse fœtale et
placentaire, 2) la morphogenèse utérine, mammaire et graisseuse, ainsi qu'à 3) l'accroissement
du débit cardiaque.
- L'élévation du métabolisme basal, l'hypertrophie et l'hyperplasie glandulaires, associées à
l'augmentation de l'activité cardiaque (avec parfois souffle systolique, tachycardie et
palpitations) ont fait dire que la grossesse imite l'hyperthyroïdie. Ceci rend difficile le
diagnostic d'une hyperthyroïdie au cours de la grossesse et permet de comprendre le risque
d'aggravation de la maladie et de la grossesse (mortalité périnatale et hypotrophie fœtale).
7. Au niveau du métabolisme
a. Eau
- rétention d’eau
- diminution de l’osmolalité plasmatique de +/- 10 mOsm/kg
- sécrétion de vasopressine
- A terme : 3,5 L (fœtus, placenta, liquide amniotique) + 3L ( volume sanguin, utérus et seins)
= 6,5L rétention grossesse normale à terme.
b. Protéines
- 500g (fœtus + placenta) + 500g (utérus, seins, hémoglobine et protéines plasmatiques …)
c. Hydrates de carbone
- résistance à l’insuline (œstrogène? Progestérone? HPL), le « but » = permettre un plus grand
apport de sucre au fœtus (= principale source d’énergie du fœtus)
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
12
d. Lipides
- Les graisses constitue un mécanisme de stockage en théorie pour protéger la mère et l’enfant
de période de jeun prolongée et d’exercice physique intense. NB : La lactation accélère la
diminution des lipides après l’accouchement.
e. Sels minéraux
- Fer: la quantité absorbée dans la nourriture et celle stockée ne sont généralement pas
suffisantes pour rencontrer les besoins de la grossesse. Si pas de supplément, anémie
maternelle mais non fœtale
- diminution Ca et Mg
f. Poids
La grossesse est marquée du sceau de l'augmentation du poids corporel dont une part importante
est constituée d'eau (7 litres) et de sang (1,5 litre).
8. au niveau de la fonction de coagulation
- augmentation fibrinogène, facteurs V, VII, VIII et X
- augmentation VS
- le taux de plaquettes reste normal, elles sont plus larges, cela est due à l’augmentation de la
thrombocytopoïèse, l’augmentation de la consommation et une dilution.
- diminution fibrinolyse sui à une augmentation de plasminogène et une diminution de la
plasmine
Tout ce qui précède est responsable d’une hypercoagulatibilité potentielle.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
13
I.3. BASSIN OU FILIERE GENITALE
A. BASSIN OSSEUX OU FILIERE PELVIENNE
Le bassin est divisé en deux parties : le grand bassin et le petit bassin. Le grand bassin, sans
intérêt obstétrical, fait partie de la cavité abdominale. Il est constitué latéralement par les fosses
iliaques des os coxaux et, en arrière, par les ailes du sacrum.
Quant au petit bassin, il correspond au bassin obstétrical. Ce canal osseux est composé de deux
ouvertures : le détroit supérieur et le détroit inférieur et d'une excavation : l’excavation
pelvienne. Il a un rôle majeur en obstétrique.
1. Les éléments du bassin osseux
Le bassin est constitué :
- d’un élément central et postérieur : la colonne vertébrale constituée du sacrum et du coccyx,
- de deux os pairs et symétriques : les os coxaux (ancienne appellation : os iliaques).
Figure 20.
L’os Coxal est issu embryologiquement de la fusion de trois os : l'ischium (ischion), l'ilium (ilion)
et le pubis. Le sacrum est composé de 5 vertèbres soudées entre elles. La première vertèbre sacrée
s'articule avec la dernière vertèbre lombaire en formant une saillie appelée promontoire .
Os coxal
2. Les articulations du bassin
Les os coxaux, le sacrum et le coccyx sont réunis entre eux par cinq articulations :
- la symphyse pubienne en avant,
- les deux articulations sacro-iliaques en arrière et latéralement,
- l’articulation lombo-sacrée,
- l'articulation sacro coccygienne en arrière et en bas.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
14
1. DETROIT SUPERIEUR (DS)
= plan d’engagement de la présentation
Limites : en avant : le bord supérieur de la symphyse pubienne
latéralement : ligne innominée (ligne arquée)
en arrière : promontoire (jonction lombo-sacrée), c'est le bord antérieur de la face
supérieure de la première vertèbre sacrée.
Le DS est rétréci en arrière par la saillie du promontoire qui lui donne une forme en cœur de carte
à jouer. Pour cette raison, l'engagement n'est possible que dans un diamètre oblique du détroit
supérieur, la présentation étant orientée en OIGA ou OIDP, plus rarement en OIDA ou OIGP.
Le DS présente :
- un arc antérieur régulier de 6 cm de rayon environ,
- deux arcs postérieurs ou incisures (sinus) sacro-iliaques, séparés par le promontoire.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
15
Application en obstétrique :
- Lorsque la tête fœtale s’engage en variété antérieure, l’occiput bute sur l’arc antérieur, ce
qui entraîne la flexion.
- Lorsque la variété est postérieure, l’occiput est en regard d’un des sinus sacroiliaques. La
forme plus large de cette partie du bassin osseux favorise moins la flexion. Ceci explique
le nombre de présentations défléchies plus important, lorsque l’engagement de la tête
fœtale a lieu en variété postérieure.
Le plus grand diamètre est oblique (dû à la saillie du promontoire). Il est 12 cm.
Dans ce diamètre, ce fait l’engagement. ≡ DIAMETRE D’ENGAGEMENT
Diamètres du DS :
Diamètre promonto-sus-pubien (le diamètre conjugué anatomique) : mesuré du
promontoire au bord supérieur de la symphyse pubienne (11 cm).
Diamètre promonto-sous-pubien (le diamètre conjugué diagonale) : mesure la distance
entre le promontoire et le bord inférieur de la symphyse pubienne (12 cm).
Diamètre promonto-rétro-pubien (PRP) (ou le diamètre conjugué vrai ou obstétricale
ou sagittal utile de Pinard) : mesuré du promontoire au point le plus éminent de la face
postérieure du pubis (culmen rétro-pubien) (10,5 cm) .
Diamètre transverse maximum (TMx) ou anatomique du détroit supérieur : c'est la plus
grande dimension transversale du détroit supérieur (13,5 cm).
Diamètre transverse médian (TM ) : ou diamètre transverse utile du détroit supérieur ; il
est mesuré à mi-distance entre le promontoire et le bord supérieur du pubis (12,5 cm).
Diamètre oblique : c’est le diamètre d’engagement (12 cm (le G est supérieur au D), la
pointe postérieure est l'articulation sacro-iliaque ; la pointe antérieure est différente selon
les références :
o l'éminence ilio-pectinée de la branche ilio-pubienne du côté opposé ;
o Pour Magnin et Trillat : à égale distance de la symphyse pubienne en avant et des extrémités du
diamètre transverse maximum en arrière
o Pour P. Kamina : défini par la rencontre de la droite passant par le milieu du diamètre transverse
médian avec la branche horizontale du pubis (il l'appelle le diamètre oblique médian).
o Pour A. Bouchet et J. Cuilleret : au milieu de la ligne innominée du côté opposé.
Diamètre sacro-cotyloïdien : c'est la distance entre le milieu du promontoire à la partie
postérieure de la cavité cotyloïde (9 cm).
o La différence entre les deux diamètres sacro-cotyloïdiens = D
D
0,2 cm < D asymétrie moyenne ;
D = asymétrie forte
Diamètre sagittal postérieur : correspond à la distance séparant le milieu du diamètre
transverse maximum (du détroit supérieur) du promontoire (5 cm).
Diamètre sagittal antérieur : correspond à la distance séparant le milieu du diamètre
transverse maximum (du détroit supérieur) du bord supérieur de la symphyse pubienne
Indice de Magnin : (PRP + TM)
normal > 23 cm médiocre entre 20 cm et 21 cm
favorable > 22 cm et mauvais si < 20 cm
pronostic incertain entre 21 cm et 22 cm
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
16
Indice de Mengert : (TMx) x (PRP) :
Il est normalement de 140 environ.
Le pronostic serait favorable jusqu' à 120 et
très réservé au dessus de 100.
Inclinaison du bassin : 45° à 60° en moyenne.
1 = Promonto-Rétro-Pubien (PRP)
2 = Transverse médian (TM) ou utile
3 = Transverse maximal
4 et 4' = Diamètres obliques gauche et droit
5 et 5' = diamètre sacro-cotyloïdien gauche et droit
(Source Wikipédia et UVMaF)
2. DETROIT MOYEN ou EXCAVATION PELVIENNE (ou CANAL PELVIEN) :
Il est formée par la face postérieure du pubis et la face antérieure du sacrum et du coccyx et
prend la forme d'un cylindre à concavité antérieure dont la paroi postérieure mesure 10 à 11 cm
et la paroi antérieure mesure 4 à 5 cm ; sa section circulaire est pratiquement constant au
niveau de tous les plans (diamètre interne environ 12 cm).
Elle à la forme d'un segment de tore (cylindre incurvé) enroulé autour de la symphyse
pubienne.
Limites : avant : la face postérieure de la symphyse pubienne,
Latérale : la face interne des os iliaques.
Arrière : la face antérieure du sacrum
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
17
Diamètres :
Diamètre oblique antérieur de l'excavation : il va du bord inférieur de la symphyse
pubienne à l'épine sciatique (4,5 à 6,1 cm).
Diamètre oblique postérieur de l'excavation : il va de l'épine sciatique à la pointe du
sacrum (4,5 à 6,1 cm).
Diamètre bisciatique (ou bi-épineux): c'est la distance séparant les deux épines
sciatiques (10 à 10,5 cm).
Corde sacrée: mesurée du promontoire au bord inférieur du sacrum (10 à 13 cm, en
moyenne 11 cm).
Flèche sacrée: c'est la plus grande valeur de la droite abaissée perpendiculairement à la
corde sacrée (ou la distance entre la flèche sacrée et le point le plus profond de la
concavité sacrée qui se trouve en regard de S2- S3. Elle mesure l’amplitude de la
concavité sacrée (1,5 cm à 2,5 cm, en moyenne 2 cm).
A = promonto-rétro-publien ; B = sous-sacro-sous-publien ; H = flèche sacrée ; S : corde sacrée
Diamètre antéropostérieur : en moyenne 11,5 cm
Diamètre sagittal postérieur : en moyenne 5 cm
Axe de la symphyse : 35° à 45° en moyenne avec l'horizontale
Angle symphysaire : 85° à 100° en moyenne
Angle sacré : 30° en moyenne (variations importantes, limites 15° à 40°)
Application en obstétrique :
L'excavation pelvienne présente au niveau de son tiers inférieur un rétrécissement, appelé
détroit moyen (DM), marqué par la saillie des épines sciatiques. La saillance de ces épines
sera appréciée lors de l’examen clinique du bassin.
Le diamètre bi-épineux (ou bi-sciatique) mesure 10 à 11 cm.
Pour que l’accouchement par voie basse soit possible :
- en présentation céphalique, il faut que le diamètre bi-pariétal de la tête fœtale soit
supérieur au plus de 1 cm au bi-épineux,
- en cas de présentation podalique, le bi-pariétal doit être au maximum égal au bi épineux.
La courbure du sacrum : la concavité sacrée constitue un élément du pronostic obstétrical.
En effet, un sacrum plat ou en hameçon peut gêner la descente et la rotation de la tête fœtale.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
18
3. DETROIT INFERIEUR :
Le détroit inférieur forme l'orifice inférieur du bassin et se définit comme le plan de
dégagement de la présentation. C’est la zone d’insertion des muscles superficiels du périnée. Il
ressemble à un losange à grand axe antéro-postérieur. C'est un orifice ostéo-fibreux non
régulier.
Limites : avant : ogive pubienne (le bord inférieur de la symphyse pubienne)
Latérale : d'avant en arrière : le bord inférieur des branches ischio-pubiennes, le bord
inférieur des tuberosités ischiatiques, les grands ligaments sacro-sciatiques
Arrière : la pointe du coccyx
Les branches ischiopubiennes dessinent un triangle osseux à sommet antérieur. De plus, la
fente délimitée par les releveurs de l'anus est allongée d'avant en arrière. Pour ces raisons, le
dégagement n'est possible que si la présentation s'oriente dans le diamètre antéropostérieur du
détroit inférieur, en OP ou en OS.
Diamètres :
Diamètre bi-ischiatique ou intertubérositaire : c'est la distance mesurée entre les
faces internes des deux tubérosités ischiatiques (11 cm).
Diamètre sous-sacro-sous-pubien: mesuré de la pointe inférieure de la dernière pièce
sacrée au bord inférieur du pubis. Il représente le diamètre antéro-postérieur utile du
dégagement au niveau du détroit inférieur (11 cm à 11,5 cm).
Diamètre sous-coccy-sous-pubien : mesuré de la pointe inférieure du coccyx au bord
inférieur du pubis (9,5 cm).
Hauteur de l'arcade pubienne : c'est la perpendiculaire abaissée du sommet de
l'arcade au diamètre bi-ischiatique (6 cm à 7 cm).
Diamètre sagittal postérieur : 8 cm à 9 cm
Angle sous-pubien : 85° à 90°
Indice de Thoms = diamètre bi-ischiatique + diamètre sagittal postérieur = 15 cm
Indice de Fernstrôm ou Indice de Borell =
o Diamètre bisciatique + diamètre bi-ischiatique + diamètre sous sacro-sous-pubien
Il est normalement > à 31,5 cm ; le pronostic est réservé s'il est inférieur à 29,5 cm.
Application en obstétrique :
La rétropulsion du coccyx peut amener le diamètre sous coccy-sous-pubien à 12,5 cm.
L’ogive pubienne
L'ensemble formé par la symphyse pubienne et les branches ischio-pubiennes porte le nom
d'ogive pubienne. L'angle qu'elle forme oscille entre 85 à 90°.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
19
Ogive pubienne
Application en obstétrique :
Plus l'angle est fermé, plus le dégagement de la tête fœtale se fera au niveau du périnée
postérieur, entraînant un plus grand risque de déchirures périnéales.
B. PLANCHER PELVIEN OU DIAPHRAGME PERINEAL OU PARTIES MOLLES
Il se définit comme une espèce de plancher fibro-musculaire qui ferme l'excavation pelvienne
en bas. Il est de ce fait appelé PLANCHER PELVIEN ou encore DIAPHRAGME PERINEAL.
Il est percé de 3 lacunes par lesquelles passent l'urètre, le vagin et l'anus, et comprend 3 plans
tissulaires:
- le premier, périnée profond, est constitué de 2 muscles 1) le releveur de l'anus qui assure
une sangle musculaire plus ou moins tonique de chaque côté du vagin et 2) l'ischio-
coccygien; le releveur de l'anus ou LEVATOR ANI possède 3 parties, l'une iliaque =
muscle ilio-coccygien, une deuxième interne = pubienne, et une autre pubo-rectale; on y
signale aussi le fascia pelvien qui est à la fois pariétal et viscéral ;
- le second, périnée moyen, constitué de 2 muscles, le transverse profond, et le sphincter
externe de l'urètre;
- le troisième, périnée superficiel, est fait d'aponévroses et de 5 muscles du périnée au
nombre de 5; ce sont les muscles ischio-caverneux ou constricteur de la vulve, bulbo-
caverneux aussi appelé muscle constricteur du vagin (en forme de 8), transverse superficiel,
le tout convergeant vers le noyau fibreux qui sépare la commissure vulvaire et l'anus
entouré de son sphincter (muscle sphincter anal externe).
Les caractéristiques du périnée portent sur sa longueur (Normal = 3-8 cm) et sa souplesse.
Le plancher pelvien a un double rôle: d'abord soutenir les organes pelviens, ensuite fournir de
la résistance à la progression du fœtus, résistance que le fœtus doit refouler et écarter pour se
dégager.
C. VASCULARISATION ET INNERVATION
1) Vascularisation
C’est l’artère hypogastrique interne qui fournit l’artère utérine et l’artère vésico-vaginale, les
principales sources de sang au couple utéro-ovulaire. Quant aux lymphatiques, on reconnaît 3
groupes ganglionnaires : obturateur ; iliaque et hypogastrique ; aortique et inguinal. Leur
drainage s’effectue en suivant le ligament rond.
2) Innervation
Le ganglion hypogastrique de Lee & Frankenhauser est le point central de l’innervation
utérine. Il est un enchevêtrement de petits ganglions et de nerfs se nourrissant à la fois du
sympathique (D11, 12, et L1 === nerfs hypogastriques) et du parasympathique (S1-4
===== nerfs splanchniques pelviens et nerfs honteux).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
20
D. L'EVALUATION DU BASSIN
Il existe deux façons d'apprécier le bassin féminin: la pelvimétrie clinique et la pelvimétrie
radiologique ou radiopelvimétrie.
I. La pelvimétrie clinique
Elle s’effectue :
- soit à l'inspection du dos de la femme pour y tracer et étudier le losange de MICHAELIS
(défini par quatre points: début du sillon interfessier en bas - apophyse de la 5ème vertèbre
lombaire en haut - fossettes latérales correspondant aux épines iliaques postéro-supérieures)
dont les diagonales sont de 11 cm pour la plus grande (= verticale) et 10 cm pour la plus
petite (= horizontale); le croisement de ces diagonales permet d’obtenir deux parts égales de
5 cm pour l’horizontale, et une part de 4 cm au dessus + une part de 7 cm en desous pour la
verticale ;
- soit en utilisant un compas spécial appelé PELVIMETRE (surtout pelvimètre de Breisky),
pour réaliser la PELVIMETRIE EXTERNE; cette dernière est très facile, mais n'explore
que le grand bassin, ce qui réduit son intérêt; elle permet de fonder le soupçon d'un mauvais
(petit) bassin dont elle donne donc une idée approximative; les dimensions du grand bassin
chez la femme normale sont de 25 cm pour le BI-EPINEUX, 28 cm pour le BI-CRETE, et
31-32 pour le BI-TROCANTERIEN dans le sens frontal, tandis que dans le sens antéro-
postérieur on a le diamètre le plus utile de la pelvimétrie externe = CONJUGUE EXTERNE
DE BAUDELOCQUE (= 18-20 cm de la symphyse pubienne à la fossette marquant le
centre du losange de Michaëlis), ainsi que la HAUTEUR DU BASSIN (= 20-22 cm telle
que calculée entre l'ischion et la crête iliaque);
- soit par le toucher vaginal qui réalise la PELVIMETRIE INTERNE. L’examen clinique du
bassin obstétrical par toucher vaginal est réalisé à la 36-37ème semaine d’aménorrhée. Il est
un élément constitutif du pronostic obstétrical. La patiente doit être installée sur un plan dur,
en position gynécologique, vessie et rectum vides. La main et l’avant-bras de l’examinateur
doivent rester dans le même axe que le bassin.
L’exploration se fait toujours dans le même ordre et successivement.
a) Exploration du détroit supérieur
I. Étude du diamètre antéropostérieur ou PRP
Les doigts sont dirigés en direction du coccyx et de la dernière vertèbre sacrée. Puis ils
remontent le long de la concavité sacrée en direction du promontoire.
L’examen est normal lorsque le contact est perdu au niveau des 2 dernières vertèbres sacrées
(S2-S1) et le promontoire non atteint.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
21
II. Exploration des lignes arquées
Puis les doigts suivent les lignes arquées.
L’examen est normal lorsqu’elles ne sont suivies que sur les 2/3 antérieurs. Les sinus sacro-
iliaques sont inaccessibles.
b) Exploration du détroit moyen
- Appréciation de la hauteur et de l’inclinaison de la symphyse pubienne
- Recherche des épines sciatiques :
L’examen des parois latérales de l’excavation pelvienne permet d’apprécier la disposition des
épines sciatiques. Il faut apprécier leur orientation, leur écartement et leur éventuelle saillie.
Attention à une saillie trop importante des épines sciatiques ou à une symphyse basse.
c) Le détroit inférieur
- Examen de l’ogive pubienne :
L’ogive pubienne est définie par les branches ischio-pubiennes. Ces dernières sont situées dans
un plan qui fait avec l’horizontale en station debout un angle de 40°. L’angle de l’ogive
pubienne varie de 85 à 90°.
NB : la distance partant du promontoire au bord inférieur de la symphyse pubienne (= 12,5
cm), correspond au CONJUGUE DIAGONAL DU DETROIT SUPERIEUR ; on cherche ce
conjugué avec le doigt dirigé profondément vers le haut en direction du promontoire que
normalement on n'atteint pas (sauf doigts très longs ou forte laxité des parties molles ou encore
bassin anormal); c'est lorsqu'on l'atteint qu'on en prend la mesure tel qu'illustré sur la figure ci-
dessous (il faut ensuite en soustraire 1,5 cm représentant les tissus mous qui recouvrent l'os);
par la même occasion, on doit explorer les lignes innominées (normal = impossibilité
d'atteindre les 1/3 postérieurs), l'ogive sous-pubienne (normal = admet deux doigts), la
concavité sacrée (normal = profonde), et le épines sciatiques (normal = mousses = non
saillantes).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
22
Pelvimétrie interne.
II. Étude paraclinique du bassin obstétrical
Les examens paracliniques permettent d’obtenir les dimensions exactes des différents
diamètres du bassin, notamment les diamètres sagittaux et transversaux du détroit supérieur
(diamètre promonto-rétro-pubien (PRP) et diamètre transverse médian (TM)) et le diamètre bi-
sciatique au niveau du détroit moyen.
a) La pelvimetrie radiologique ou radiopelvimetrie
Elle a l'avantage de préciser les mesures et l'inclinaison des différents plans du bassin, ce qui
exige un personnel très qualifié et un coût relativement élevé.
Ses indications principales sont:
- l´antécédent de dystocie, notamment la Disproportion Foeto-Pelvienne (DFP);
- la découverte d'un Conjugué Diagonal < 12 cm;
- des épines sciatiques saillantes;
- Diamètre inter-tubérositaire < 9 cm;
- Présentation de Siège chez une primi;
- Tête Haute sur grossesse à terme chez une primi;
- Tête haute à dilatation de > 5 cm chez une primi.
Pour son exécution, elle exige 3 incidences:
- 1 face sur abdomen sans préparation (= incidence de Fabre) ;
- 3 faces respectivement de Thoms (position semi-assise, tronc incliné de 40-50 degrés en
arrière, permettant au DS de se retrouver parallèle au plan du film), de Colcher-Sussman
(position de décubitus dorsal, jambes jointes), et de Magnin et Naudin (jambes et cuisses
écartées de façon à bailler l'arcade pubienne qui est alors visée par les Rx) ;
- 1 profil (pour appréciation des diamètres antéropostérieurs).
La radiopelvimétrie comporte de nombreux inconvénients :
- irradiation fœto-maternelle,
- inconfort pour la patiente,
- nécessité d’utiliser des règles de correction des dimensions radiologiques,
- dispersion conique du faisceau des rayons avec agrandissement et déformation de l’image
réelle,
- visualisation parfois mauvaise.
b) La scannopelvimétrie
Trois clichés sont réalisés :
- cliché de profil pour étudier les diamètres sagittaux,
- 2 coupes transversales pour mesurer les diamètres transversaux.
Actuellement c’est la technique de choix. Elle présente de nombreux avantages :
- irradiation fœto-maternelle moindre,
- mesures directes avec interprétation plus précise,
- examen plus confortable pour la patiente et rapidité d’exécution (15 mn).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
23
c) La pelvimétrie par IRM
Deux séries de coupes sont réalisées. La patiente en décubitus dorsal, genoux légèrement
fléchis. Avantages: absence de mesures correctives (mesures directes) et absence d’irradiation
fœto-maternelle. Inconvénients: les risques de claustrophobie et le coût élevé.
E. CLASSIFICATION DES BASSINS FEMININS
1) Classification pratique des bassins féminins en Obstétrique
(Mécanique et Technique Obstétricale ; JP. Schaal, D. Riethmuller, R. Maillet).
Editeur : SAURAMPS Médical, 1998
Bassins PRP TM médian Indice de Magnin Bisciatique Biischiatique
Normaux > 10,5 cm > 11,5 cm > 22 cm > 9,5 cm > 9 cm
Limites < 10,5 - 8,5 cm < 11,5 - 9,5 cm < 22 - 20 cm < 9,5 - 8 cm < 9 - 8 cm
Chirurgicaux < 8,5 cm < 9,5 cm < 20 cm < 8 cm < 8 cm
2) Classification des bassins rétrécis symétriques non déplacés selon Merger
(Précis d'Obstétrique. Masson 1995)
Bassin aplati Diminution isolée du diamètre promonto-rétro-pubien
Bassin transversalement rétréci Diminution isolée du diamètre transverse maximum
o Forme ovale : bassin anthropoïde
o Forme triangulaire : bassin androïde
Bassin généralement rétréci Bassin bien proportionné mais :
o diamètre promonto-rétro-pubien diminué et
o diamètre transverse maximum diminué
Bassin généralement rétréci et aplati diamètre PRP et TMaximum diminués
prédominant sur le diamètre promonto-rétro-pubien
3) Classification des bassins selon Thoms
(selon les dimensions du détroit supérieur) (Précis d'Obstétrique. Masson 1995)
Les diamètres pris en compte :
au niveau du détroit supérieur : PRP et TMx
elle ne prend pas en compte la forme du bassin.
Bassin dolichopellique : PRP > TMx
Bassin mésatipellique : PRP = TMx ou PRP < TMx de 1 cm
Bassin brachypellique PRP < TMx de 1 à 3 cm
Bassin platypellique : PRP < TMx de plus de 3 cm
4) Classification de Caldwell - Moloy
d'après Caldwell WE Moloy HC, Am J Obstet Gynecol 1933 ; 26 : 479
Elle prend en compte la forme du bassin.
Technique de mesure
o Division du détroit supérieur par une ligne qui passe par le plus grand diamètre transverse (TMx)
o Comparaison des deux parties ainsi divisés antérieure et postérieure du détroit postérieur en comparant
le diamètre sagittal de la partie antérieure et celui de la partie postérieure
l'aspect de la réunion des deux parties antérieure et postérieure de la ligne innominée
Bassin gynoïde Diamètre sagittal postérieur légèrement inférieur au diamètre sagittal antérieur ;
la réunion des deux parties forme un cercle
PRP = TMx ou PRP < TMx
BIE (diamètre bi-épineux) > ou = 10 cm
Le plus fréquent des bassins
Bassin androïde Diamètre sagittal postérieur très inférieur au diamètre sagittal antérieur ;
la réunion des deux parties se fait à angle aigu
Bassin anthropoïde PRP > TMx
Il existe souvent une sixième vertèbre sacrée
Bassin platypelloïde TMx > PRP
Ces quatre types de bassin représentent 50 % des cas, les autres bassins sont des formes mixtes.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
24
I.4. MOTEUR UTERIN (FORCES EXPULSIVES)
L’utérus est en fait un muscle creux dont la paroi, appelée myomètre, est enveloppée par le
péritoine viscéral (= la séreuse) au dehors, tandis qu’elle est tapissée au-dedans par une couche
muqueuse mince et friable (= la muqueuse). Entre séreuse et muqueuse, la paroi utérine
comprend une couche de fibres musculaires (= la musculeuse). La musculeuse comporte 3
assises musculaires : celle qui est la plus externe est constituée de fibres longitudinales ; celle
qui est interne et se trouve en contact avec la muqueuse contient des fibres circulaires ; la
couche située entre les deux est beaucoup plus épaisse, et elle est dite plexiforme à cause de
l’enchevêtrement de ses faisceaux musculaires. Au niveau du col, les fibres longitudinales se
raréfient.
L´intérêt de la couche plexiforme est que, lors de la contraction, elle bloque littéralement les
vaisseaux sanguins qui traversent la paroi musculaire (d´abord les veines et puis, à des
pressions supérieures, les artères). Ceci peut donc provoquer, au cours du travail, une nette
réduction du transfert d´oxygène vers le fœtus.
1. Les modifications utérines au cours de la grossesse
Elles sont de type anatomique et histologique.
Au plan anatomique on a:
- une augmentation de volume; en dehors de la grossesse l'utérus pèse 50 g, et sa capacité est
de 10 ml; à terme, il pèse 900 à 1200 g, voire 1500 g, et a une capacité de près de 4 - 5
litres;
- un changement de forme, du fait que la fixité du col utérin d'une part et l'étirement de
l'utérus vers le haut d'autre part résultent en une structure très fonctionnelle, le SEGMENT
INFERIEUR, formé au dépens de l'isthme et de la partie la plus basse du corps de l'utérus ;
c’est une zone étirée et amincie qui devient une espèce de COIFFE sur laquelle vient
s'appuyer la partie fœtale en présentation; lors de l'opération césarienne, l'incision est
effectuée à cet endroit qui offre la résistance la plus moindre; sa proximité avec la vessie
rend cette dernière très vulnérable en cas de césarienne ou d'accouchement laborieux.
Au plan histologique on note des phénomènes de:
- hypertrophie musculaire;
- néoformation de fibres musculaires (hyperplasie);
- oedème interstitiel;
- distension (surtout dans le dernier trimestre);
- ramollissement qui correspond à la réduction (40 – 60 %) de son contenu en collagène, sous
l’effet des prostaglandines E et des modulateurs cellulaires, tels que le calmodulin, le Ca++
cellulaire et l´AMP cyclique ; c’est cela qui rend les fibres du col hydrophiliques ; c´est ce
qu´on appelle Mûrissement du col.
2. Physiologie du déclenchement des contractions utérines
La contraction de la cellule musculaire lisse utérine résulte du jeu des protéines contractiles
constitutives de cette cellule : actine et myosine, grâce à la libération d’énergie fournie de
l’Adénosine TriPhosphate (adénosine triphosphate) en présence d’ions Na+, K+, Ca++ surtout
qui serait mobilisé par les prostaglandines. La phosphorylation du complexe actine-myosine
est régulée par un système enzymatique faisant intervenir une phosphorylase et une
phosphatase.
a) Les influences inhibitrices sur les contractions utérines
Ce sont elles qui assurent le maintien de la grossesse; elles sont essentiellement hormonales, et
ont pour effet de bloquer la conductibilité de la fibre musculaire par l'onde contractile, grâce à
leur effet d'hyperpolarisation de la membrane cellulaire.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
25
Progestérone
HCG
Placenta: zone d'insertion représentant une zone passive de l'utérus.
b) Les influences excitatrices sur le muscle utérin
Elles coexistent avec les influences inhibitrices, mais voient leur ampleur s'accroître à mesure
que la grossesse avance en âge.
I. Influences excitatrices intrinsèques au myomètre (maturation)
- Augmentation progressive des protéines contractiles de type actine-myosine et des
phosphates à haute concentration énergétique de type ATP, à vocation contractile.
- Augmentation de récepteurs membranaires de surface de la fibre myométriale.
- Distension globale (corps utérin) et sectorielle (segment inférieur) du myomètre, avec
élévation du tonus de base, favorisant l’excitabilité et le déclenchement du réflexe utéro-
hypothalamique neuro-hormonal de FERGUSSON. Cette distension stimule également la
synthèse de prostaglandines du fait des modifications vasculo-motrices sur la decidua qui
est la grande pourvoyeuse de prostaglandines.
II. Influences excitatrices liées aux substances produites par la grossesse
- Œstrogènes d'origine placentaire, augmentant l'excitabilité de la fibre.
- Hormones utérotoniques telles que Cortisol (surrénales) et ACTH (hypophyse) fœtales -
ocytocine maternelle et fœtale – prostaglandines.
3. Initiation de la contraction utérine
L'initiation de la contraction utérine se fait au niveau de l'une et l'autre corne utérine près
desquelles se situe un "pace-maker". L'onde contractile se propage vers le bas (en direction du
col), et vers le milieu au niveau duquel les deux influx se rencontrent.
La contraction baisse d'intensité à mesure qu'elle descend le long de l'utérus, dans une espèce
de gradient dégressif se terminant au niveau de l'orifice interne du col. Etant donné que les
fibres qui se contractent ne retournent pas à l’état initial et voient donc leur longueur se réduire
après chaque contraction (= BRACHYSTASE), le col finit par s’ouvrir.
Sur le plan moléculaire la contraction consiste en une action de l´actine et de la myosine qui
s´entrecroisent pour former l´actinomyosine qui raccourcit la fibre musculaire sous l´effet de la
phosphorylation et la déphosphorylation enzymatique des chaînes légères de la myosine. Ces
séries de réactions enzymatiques ont besoin des ions calcium.
4. Caractéristiques cliniques des contractions utérines pendant le travail
Elles sont dues à l’activité du myomètre qui est composé de fibres musculaires lisses, de tissu
conjonctif et de nombreux vaisseaux. Elles correspondent aux contractions des fibres
élastiques.
Elles sont :
- involontaires
- intermittentes et rythmées : entre les contractions, l’utérus se relâche. La pression
enregistrée pendant cette phase définit le tonus de base ;
- progressives dans leur durée et leur intensité : elles surviennent toutes les 15 à 20 minutes et
durent de 15 à 20 secondes en tout début de travail. Elles surviennent toutes les 2 à 3
minutes et durent 30 à 45 secondes à la fin de la première phase de travail. Leur intensité
augmente au cours du travail.
- douloureuses : la douleur ne se manifeste qu’après une certaine durée de la contraction et se
termine avant la fin de celle ci. L’intensité de la douleur est sujette à des variations
individuelles. Elle augmente avec la progression du travail et est majorée par la crainte et
l’angoisse (utilité de la Préparation à la Naissance et à la Parentalité). Elle est le plus
souvent abdominale et pelvienne, mais peut également être ressentie dans la région
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
26
lombaire, notamment dans le cas des variétés postérieures. La pression à partir de laquelle la
douleur apparaît définit le seuil de Polaillon.
- totales : elles intéressent tout l’utérus.
Pour le diagnostic du travail, il faudra distinguer les contractions utérines de « travail » des
Contraction Utérine de Braxton-Hicks. Celles-ci peuvent s’observer dès 20 SA et devenir
douloureuses au cours du dernier mois de grossesse. Elles sont responsables du « faux travail
». L’étude de la pression intra-amniotique au cours d’une contraction utérine permet de mettre
en évidence :
- une phase ascendante rapide,
- une phase descendante plus longue qui ramène la pression au niveau du tonus de base,
- une phase de repos entre 2 contractions.
La contraction utérine
Elles se définissent donc par
- le tonus de base
- l’intensité
- la fréquence ou rythme
- la durée
- et le relâchement utérin
Le tonus de base est inférieur à 20 mm Hg (en moyenne de 10 à 18 mm Hg). Il objective
l’activité permanente du muscle utérin. Il est la traduction graphique du repos clinique de
l’utérus.
La pression maximale atteinte par la contraction définit son intensité. Celle-ci varie au cours
du travail ; elle est de 35 à 50 mm Hg à 3-4 cm de dilatation pour atteindre 50 à 80 mm Hg à
dilatation complète.
La différence entre pression maximale et tonus de base définit l’amplitude de la contraction.
Seule l’amplitude rend compte de l’efficacité de la contraction.
Les CU durent de 1 à 2 min (en moyenne 80 sec).
Elles constituent la force motrice permettant la formation du segment inférieur, la dilatation du
col utérin et la progression du fœtus dans le bassin, puis son expulsion hors des voies génitales.
5. Evaluation des contractions utérines
Elle se fait à l’examen clinique et par des examens paraclinique
1) À l’examen clinique
Le corps utérin devient plus cylindrique, se rapproche de la paroi abdominale antérieure, se
durcit progressivement empêchant de percevoir les parties fœtales, rendant plus difficile la
perception des bruits du cœur La palpation de l’utérus permet d’apprécier l’intensité et la durée
des CU, ainsi que le relâchement utérin.
Après la contraction, l’utérus se relâche, permettant à nouveau de percevoir les parties fœtales.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
27
2) Les examens paracliniques
L'évaluation des contractions utérines s'effectue à l'aide d´un tocodynamomètre qui est soit
interne (capteurs de pression directement posés dans la cavité utérine), soit externe (capteurs
posés sur l'abdomen). Les renseignements obtenus ont été codifiés depuis les travaux de
Caldeyro-Barcia (école de Montevideo). L'évaluation de la contraction utérine porte finalement
sur les éléments ci-dessous :
- son intensité
- son amplitude
- la durée de son relâchement
- l'intensité de base ou tonus de base de l'utérus
- la fréquence
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
28
I.5. MOBIL FOETAL
En mécanique obstétricale, on parle de mobile fœtal car le fœtus relié au placenta par son
cordon est relativement mobile dans la cavité utérine. Il va pouvoir progresser au travers de la
filière pelvienne sous l’influence des contractions utérines.
L’attitude générale physiologique en flexion du fœtus donne une forme globale d’ovoïde, dont
la petite extrémité est représentée par la tête. On parle d’ovoïde fœtal car la tête est le plus
souvent fléchie sur le tronc, les bras repliés sur le thorax, les cuisses fléchies sur l’abdomen et
les jambes fléchies sur les cuisses.
À terme le fœtus mesure environ 50 cm. Par rapport à son contenant, l’utérus qui mesure
environ 32-34 cm à terme, il est obligé d’appliquer une attitude générale en flexion. Cette
attitude au voisinage du terme est due à l’action prédominante des muscles fléchisseurs sur les
muscles extenseurs. En position fœtale, la longueur du fœtus est d’environ 30 cm.
1. ASPECT GÉNÉRAL DU FŒTUS
À terme, le fœtus pèse 3250 g et mesure 50 cm (talon-vertex) ce qui correspond au 50ème
percentile des courbes de Leroy. L'attitude générale du fœtus est la triple flexion des membres
et la double flexion céphalique (atloïdo-occipitale et cervicale).
2. ANATOMIE DU FŒTUS
L’anatomie du fœtus inclut désormais l’étude des formes et structures du fœtus à tous les âges
gestationnels, principalement lorsqu’elles reflètent des profils caractéristiques du bien-être
fœtal.
Au premier trimestre, 3 éléments anatomiques sont à considérer :
1) le sac vitellin (vésicule vitelline),
Son intérêt s´est encore accrue depuis que l´échographie a établi une corrélation
significative entre ses dimensions et le pronostic ovulaire ;
Ses dimensions normales augmentent rapidement de 3,5 millimètres (autour de 8 semaines)
à 6,5-10 millimètres (vers 11 semaines) avant sa disparition (sans doute parce que le
placenta vient alors assumer son rôle nutritionnel);
Trop petit, il signe une pauvreté des réserves, et donc une menace pour l’œuf;
Trop grand, il signe par contre soit une faible utilisation (anomalie chromosomique), soit
une incapacité d´utilisation (embryon déjà mort);
2) l´activité cardiaque, dont la présence doit être établie dès que la longueur crânio-caudale
est d´au moins 5 millimètres ; sinon, il faut suspecter une mort embryonnaire;
3) la morphologie d´ensemble, dont l´élément primordial semble être la transluminescence
de la nuque fœtale (Clarté nucale, Fetal nuchal translucency ou FNT), semble correspondre
à un œdème ne devant pas dépasser 2,4 millimètres pour certains, et 3 millimètres pour
certains autres; au-delà de ces limites, elle permet déjà d´évoquer une trisomie (surtout
21) ou faire redouter la survenue d’anomalies cardiaques ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
29
.
Aux 2ème et 3ème trimestres, l’anatomie du fœtus comprend des éléments classiques plus
ou moins figés (tête, colonne vertébrale, thorax avec cœur, diaphragme, abdomen et
membres), et 5 autres plus dynamiques (morpho-fonctionnels).
I. Tête fœtale: crâne - cerveau - face - nuque
La tête fœtale, si on la considère isolément, se présente sous forme d'un ovoïde à grosse
extrémité postérieure. La description qu’on fait généralement du crâne fœtal se rapporte au
fœtus à terme.
Les dimensions de la tête sont telles que si elle passe le reste suit sans difficulté; d'ou leur
importance en obstétrique. La tête fœtale possède les diamètres les plus grands du fœtus, ce qui
la rend la partie la plus difficile à expulser. Le crâne fœtal est constitué de 3 grandes parties: 1)
la face, 2) la voûte ou toit, et 3) la base.
Les os de la face et de la base sont plus ou moins soudés entre eux, tandis que ceux de la voûte
ne le sont pas. La mobilité de ces os peut aller jusqu'au chevauchement, permettant le
modelage de la tête. Ces os ne sont pas parfaitement ossifiés : seule leur portion centrale est
ossifiée, dure, en relief (bosse). Au fur et à mesure que l'on s'éloigne de ce centre, l'os devient
membraneux et s'amincit. Ceci donne à la tête fœtale la possibilité de se remodeler lors de son
passage à travers la filière génitale maternelle. Ce processus s'appelle ACCOMMODATION.
La voûte crânienne est constituée d'os plats issus de l'ossification d'une capsule membranaire
fœtale. Elle est formée de la profondeur vers la surface de 2 plans distincts :
le plan osseux, dont l’ossification est incomplète,
le plan du cuir chevelu, richement vascularisé.
La voûte qui est la partie la plus souvent exposée de la présentation se compose d’un
assemblage de 7 os formant une surface convexe. C’est un ensemble d’écailles osseuses,
mobiles les unes par rapport aux autres, séparées par des structures conjonctives fibreuses
représentant les sutures. Les 7 os sont : 2 os frontaux; 2 os pariétaux; 2 os temporaux et d'1 os
occipital. Les lignes de séparation de ces os sont Les SUTURES. Les zones d'abouchement
(rencontre) de 3 sutures sont faites de lacunes constituées de tissu conjonctif appelées
FONTANELLES, et que l'on peut palper sous forme de dépressions.
Les repères osseux de la tête sont situés sur la voûte crânienne et sont représentés par trois (3)
structures anatomiques:
- la suture sagittale, longitudinale ou grande suture, qui est en fait un sillon séparant les deux
os pariétaux;
- la fontanelle postérieure (située à l'extrémité postérieure de la suture longitudinale) = une
lacune de l'os à la jonction des 3 sutures de la voûte; cette fontanelle est aussi appelée petite
fontanelle ou lambda; elle est triangulaire et son repère est l'occiput; c'est elle qui se
présente au doigt examinateur dans la présentation du sommet ou VERTEX;
- la fontanelle antérieure, ou grande fontanelle, ou bregma, qui a la forme d'un losange des
angles duquel partent 4 sutures.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
30
Les sutures forment à leurs croisements des fontanelles. Les sutures et fontanelles servent à
diagnostiquer, lors d'un toucher vaginal, la variété de présentation et son degré de flexion.
Dans certains cas (anormaux), il existe une extension de la tête au lieu de la flexion tant
souhaitée. C'est alors la DEFLEXION qui, selon ses degrés, peut donner lieu à deux types de
présentation pathologique :
- la présentation du front (repère = nez);
- la présentation de la face (repère = bouche et l'arc du maxillaire inférieur).
Les sutures
Ce sont des espaces membraneux séparant entre eux les os de la voûte. On distingue 3 sutures
principales et 2 sutures accessoires. Les sutures principales sont accessibles au toucher vaginal
et sont facilement repérables.
sutures principales :
o la suture sagittale d'orientation antéro-postérieure sépare les 2 os pariétaux ;
o la suture coronale ou transversale antérieure croise perpendiculairement la suture
sagittale. Elle sépare les os frontaux en avant des os pariétaux en arrière ;
o la suture occipito-pariétale ou lambdoïde sépare l'écaille occipitale des 2 os pariétaux en
allant d'une écaille temporale à l'autre.
sutures accessoires :
o la suture métopique, inconstante, sépare les 2 os frontaux ;
o la suture pariéto-temporale ou squameuse.
Les fontanelles
Deux fontanelles ont leur importance en maïeutique.
La fontanelle bregmatique (bregma, grande fontanelle, ou fontanelle antérieure) est située
au croisement des sutures sagittale, métopique et coronale. C'est un espace membraneux
losangique à grand axe antéro-postérieur, et dépressible sous le doigt. Elle est limitée en
avant par les 2 os frontaux et en arrière par les 2 os pariétaux. En dehors de toute
accommodation, cette fontanelle mesure 2 cm de côté. Au moment de l'accouchement, le
toucher vaginal ne permet pas toujours de percevoir la forme losangique mais plutôt le
croisement des sutures. Elle sera comblée en général vers l'âge de 18 mois.
La fontanelle lambdatique (lambda, petite fontanelle, fontanelle occipitale ou fontanelle
postérieure) est située à la jonction de la suture occipito-pariétale et de la suture sagittale.
Elle a des dimensions plus réduite que le bregma. Elle est de forme triangulaire en « Y »
inversé ou lambda. Elle se comble vers l'âge de 2 mois.
Bien que d'existence constante, d’autres fontanelles sont accessoires par leur situation, leur
constance et leur peu d'intérêt obstétrical.
La fontanelle ptérique (ou ptérion) a une forme de « H » et unit les os frontal, pariétal,
sphénoïde et temporal. Elle est située à l’extrémité de la suture coronale.
La fontanelle astérique (fontanelle de Gasser ou astérion) réalise la jonction entre la suture
occipito-pariétale et l'os temporal.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
31
La fontanelle de Gerdy est située sur la suture sagittale à mi-chemin entre le bregma et le
lambda.
La fontanelle médio-frontale est située au milieu de la suture métopique en son milieu.
La fontanelle glabellaire (ou fontanelle médiane) est située à la jonction entre les os
frontaux et la racine du nez.
Les diamètres de la tête fœtale
L'apprentissage de la mécanique obstétricale nécessite la connaissance des différents diamètres
de la tête fœtale.
1 = sous-occipito-bregmatique 9,5 cm. 2 = sincipito-mentonnier=13,5 cm; 3 = occipito-frontal = 12 cm; 4 = sous-
mento-bregmatique = 9,5 cm; 5 = bi-pariétal = 9,5 cm; 6 = bitemporal = 8 cm (Source UVMaF)
a)Les diamètres antéropostérieurs
le sous-occipito-bregmatique : du bregma à la base de l'occipital. Il mesure 9,5 cm et
correspond à la position très fléchie de la tête.
l’occipito-mentonnier : du menton à l’occiput. Il mesure 13 cm et correspond à la
position intermédiaire de la tête ou plus exactement syncipito-mentonnier = 13, 5 cm (le
sinciput est à 1 ou 2 cm > de l’occiput)
l’occipito-frontal : de la glabelle à la partie supérieure de l'occipital. Il mesure 12,5 cm
le sous occipito-frontal : du sous-occiput au milieu du front. Il mesure 10,5 à 11 cm
b)Les diamètres verticaux
le sous mento-bregmatique : de la région bregmatique à la partie supérieure du cou près
du menton. Il mesure 9,5 cm et correspond à la présentation défléchie de la tête : la face.
le sous-occipito-bregmatique : déjà cité précédemment.
c) Les diamètres transverses
le bi-pariétal mesure 9,5 cm. C’est le plus grand diamètre qui 0000000000000000
s'étend d'une bosse pariétale à l'autre.
le bi-temporal mesure 8 cm. Il s’étend d’une fosse temporale à l’autre.
le bi-malaire mesure 7 cm.
Possibilités de réduction des dimensions du crâne fœtal
Certaines dimensions du crâne fœtal sont incompatibles avec un passage à l’intérieur du bassin
maternel. La tête ne peut présenter ses plus petites dimensions qu’à la condition qu’elle soit
totalement fléchie (sous-occipito-bregmatique) ou totalement défléchie (sousmento-
bregmatique).
Le passage dans la filière génitale impose parfois à la tête des déformations plastiques qui sont
rendues possibles par l’ossification incomplète du crâne. En effet le contenu minéral osseux
des os crâniens du nouveau-né est nettement inférieur à celui de l’adulte (1/30)
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
32
C’est ainsi que l’on peut voir :
le chevauchement des pariétaux (qui diminue le diamètre transversal)
le glissement de l’écaille de l’occipital sous les pariétaux (qui diminue le diamètre
antéropostérieur)
Il est évident que ces déformations doivent être modérées et il ne faut pas compter sur elles
pour amoindrir un trop grand diamètre lié à un défaut de flexion ou de déflexion de la tête.
II. Le cou
La grande mobilité du cou permet à la tête fœtale des mouvements de flexion, extension (ou
déflexion), d'inclinaison latérale. Ceci est dû à l’extensibilité de l’appareil ligamentaire des
vertèbres et à la hauteur considérable des disques cartilagineux intervertébraux. Les
mouvements ne sont limités que par la butée thoracique en avant et la butée vertébrale en
arrière. La torsion du cou chez le fœtus peut atteindre un degré extrême allant jusqu'à 180°.
III. Le tronc
Il présente ses plus grandes dimensions au niveau de la ceinture scapulaire et de la ceinture
pelvienne. Les diamètres transversaux sont donc plus grands que les diamètres antéro-
postérieurs.
a. Le thorax
C’est au niveau de la ceinture scapulaire que se trouve le diamètre le plus important du tronc :
le diamètre bi-acromial (allant d'un acromion à l'autre). Ce diamètre mesure 12 cm, mais il est
facilement réductible par tassement. Passant à 9,5 cm, il permet aux épaules de franchir
aisément le bassin maternel. La clavicule est l’os le plus soumis aux phénomènes de torsion et
de tassement lors de l'accouchement.
b. L’abdomen fœtal
L'abdomen du fœtus a ceci d'intéressant qu'il renferme les organes (foie - surrénales)
nécessaires à l'intégrité de l'unité foeto-placentaire (voir plus loin). On ne peut en outre ignorer
que beaucoup de malformations fœtales se signalent par une désorganisation de l'abdomen
fœtal. Dans ce dernier cas, l'abdomen peut avoir des dimensions responsables de dystocie, ce
qui fait des diamètres et circonférences de l’abdomen des mesures utiles à l'échographie:
diamètre, circonférence = [DAT + DAP] x 1,57, tube digestif - reins (cfr pelves < 5 mm,
sinon penser à une pyélectasie).
c. Les hanches
Le diamètre bi-trochantérien mesure 9,5 cm. Il est compatible sans accommodation avec les
diamètres du bassin maternel.
IV. Les membres
Les membres n'ont de l'importance en obstétrique que dans la mesure où :
- leur repérage par le toucher vaginal permet de préciser le diagnostic de certaines
présentations pathologiques, comme le SIEGE et l'EPAULE;
- leur présence à côté ou même au-devant d'une présentation céphalique peut réaliser une
dystocie plus ou moins grave; c'est alors la PROCIDENCE D'UN MEMBRE (rare);
- certains points d'ossification, notamment le point épiphysaire inférieur du fémur (POINT
DE BECLARD) et le point épiphysaire supérieur du tibia (POINT DE TODT),
permettent d'apprécier radiologiquement le degré de maturité du fœtus (ils correspondent
respectivement à 36 et 38 semaines de gestation).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
33
NB :
En marge des aspects anatomiques que nous venons d’évoquer, les membres participent à une
harmonie corporelle qui est représentée par les ratios morphométriques suivants:
Périmètre céphalique/Périmètre abdominal, ratio qui est âge-dépendant, et décroît de
manière linéaire de 16 à 40 semaines, et que l´on peut expliquer par le fait que
l´importance volumétrique de la tête fœtale par rapport au reste du corps diminue au fur
et à mesure que progresse la grossesse;
Longueur du Fémur/Périmètre abdominal, ratio indépendant de l´âge gestationnel, et
dont la valeur d´indice attendue normalement est de 22 ± 2%.
Ces ratios ont l´avantage d´être mesurables de manière précise in utero, grâce à
l´ultrasonographie. Ils traduisent bien le rapport classique avec lequel on apprécie la croissance
fœtale, à savoir : Poids/Age. C´est ainsi que ces 2 derniers peuvent actuellement être déduits
par computérisation à partir des paramètres cliniques (Hauteur utérine + niveau de descente de
la tête fœtale), et ultrasonographiques simples (BIP, DAT, LF). Des courbes de référence sont
alors nécessaires pour rendre aisée l´interprétation des valeurs trouvées.
3. LES PRESENTATIONS
Le pôle fœtal (soit la tête, soit le siège) qui entre le premier en contact avec le D.S. pour s'y
engager et évoluer suivant un processus qui lui est propre s'appelle PRESENTATION. On
reconnaît 2 types de présentation:
- longitudinales ou verticales, qui peuvent être CEPHALIQUE ou DE SIEGE (dite aussi
présentation pelvienne);
- horizontale ou transversale (= absence de vraie présentation).
Selon la loi de « l'accommodation » qui veut que les parties les plus volumineuses du fœtus se
placent dans les parties les plus larges de l'utérus, la tête qui est la partie fœtale la plus
volumineuse dans les 2 premiers trimestres est fréquemment retrouvée vers le haut
(présentation du siège). La situation se renverse vers le 3ème trimestre, et c'est alors la
présentation céphalique qui est la plus fréquente. Heureusement!
Lorsqu’à l'engagement la tête se présente en orientant sa suture sagittale dans le sens du
diamètre transverse, on parle de SYNCLITISME. Dans le cas contraire, il y a
ASYNCLITISME. La persistance du synclitisme signe un mauvais bassin.
Lorsque la tête est bien fléchie, c'est le diamètre sous-occito-bregmatique (9,5 cm) qui se
présente au Détroit supérieur. Et, selon les différents degrés de déflexion, on peut noter le
diamètre occipito-frontal (12 cm = c'est la présentation bregmatique), puis le sous-mento-
bregmatique (9,5 cm = c'est la présentation de la face, avec accouchement possible si le
menton tourne en avant), et enfin l'occipito-mentonnier (13 cm = c'est la présentation du front
= césarienne).
4. LA POSITION
Elle est définie comme le rapport entre le repère pris sur la partie en présentation et les 4
quadrants du bassin maternel vu d'en bas. Les positions de la tête sont respectivement
désignées en considérant l'occiput pour la présentation du sommet, le nez pour la face, le
menton pour le front et le sacrum pour le siège.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
34
Ainsi selon les repères fœtaux, on distingue les présentations suivantes :
a. La présentation du sommet
Les diamètres d'engagement sont le diamètre bi-pariétal et le diamètre sous-
occipitobregmatique.
Le repère définissant la variété de présentation est le lambda. Et les variétés selon la position
de la tête sont :
- les variétés antérieures Occipito-Iliaque Gauche Antérieure (O.I.G.A.) et Occipito-
iliaque Droite Antérieure (O.I.D.A) qui ne posent en général pas de problème en
l’absence d’une disproportion fœto-pelvienne.
- les variétés postérieures Occipito-Iliaque Gauche Postérieure (O.I.G.P.) et Occipito-
iliaque Droite Postérieure (O.I.D.P) pour qui, par contre, l’évolution de la dilatation et
de l’engagement du mobile fœtal sont plus lentes. L’accoucheur devra se donner une
période d’observation plus longue que d’habitude sans cependant dépasser le délai
normal d’un travail l’accouchement.
Variétés de position de la tête fœtale
b. La présentation du bregma
Les diamètres d'engagement sont le diamètre bi-pariétal et le diamètre occipito-frontal.
Le repère définissant la variété de présentation est le bregma.
c. La présentation du front
Les diamètres d'engagement sont le diamètre bi-pariétal et le diamètre syncipitomentonnier.
Le repère définissant la variété de présentation est la racine du nez.
d. La présentation de la face
Les diamètres d'engagement sont le diamètre bi-pariétal et le diamètre sous-mentobregmatique.
Le repère définissant la variété de présentation est le menton.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
35
La présentation de face avec menton antérieur permet un accouchement par la voie basse
Lorsque le menton est en postérieur, il y a risque d’enclavement de la tête fœtale dans la
filière génitale maternelle
e. La présentation du siège
Le diamètre d'engagement est le diamètre bi-trochantérien. Le repère définissant la variété de
présentation est le sacrum. Et selon la position du siège, les variétés sont : SIGA (e), SIDA (b),
SIGP (d) et SIDP (c)
NB :
Les diamètres du mobile fœtal n'ont d'intérêt que s'ils sont confrontés aux dimensions du
bassin maternel. Les repères anatomiques permettent à la sage-femme de diagnostiquer les
variétés de présentation du mobile fœtal afin de pouvoir adapter les prises en charge aux
situations cliniques.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
36
5. PHYSIOLOGIE FŒTALE
1) Circulation sanguine du fœtus
Le contrôle du rythme cardiaque fœtal est, comme chez l'adulte, sous la dépendance de
deux mécanismes:
- le premier mécanisme est l’automatisme cardiaque (=la capacité du muscle cardiaque à se
contracter de lui-même); cette capacité lui est assurée par le nœud de KEITH-FLACK et le
NOEUD AURICULO-VENTRICULAIRE DE ASHOFF-TAWARA;
- le deuxième mécanisme est assuré par le centre cardio-respiratoire du SNC dont le
diencéphale (bulbe rachidien), via NERF VAGUE (= parasympathique), sert à freiner les
effets incitateurs des centres automatiques ; chez le fœtus, la variabilité du rythme
cardiaque est presque sous la dépendance du VAGUE (parasympathique) dont on sait le
caractère irrégulier de la décharge ; c'est ce qui explique que, à l'enregistrement, le rythme
cardiaque fœtal ou RCF affiche une image en dents de scie d'amplitudes différentes.
La circulation du sang fœtal tire son originalité de 3 (trois) particularités anatomiques :
- la non fonctionnalité des poumons, et donc l’inexistence de la petite circulation ou
circulation pulmonaire (elle est fermée) ;
- l’existence d’une suppléance anatomo-fonctionnelle représentée par le placenta, avec sa
chambre intervilleuse ;
- la simplification structurale de l’hémodynamique, représentée par les raccourcis (shunts)
ci-après : le Ductus venosus, le Foramen ovale et le Canal arteriel.
Ductus venosus (D.V.) ou canal veineux d’Arantius
La grosse veine ombilicale (V.O.) apporte l'oxygène et les éléments nutritifs en provenance
du placenta ; il aborde le foie par le ligament falciforme pour lui fournir des branches destinées
au lobe gauche et deviendra la veine porte gauche.
Mais juste après avoir donné naissance à ces branches, la V.O. donne le D.V. (de calibre = 1/3
de la V.O.) dans lequel va s’engager ± 50% de son sang, ce qui confère à ce sang une vélocité
exceptionnelle ; ce sang occupe la portion postéro-gauche de la V.C.I. qu’il rejoint au niveau
du vestibule veineux, pratiquement au même niveau d’abouchement que les veines hépatiques
véhiculant le sang qui s’est « attardé » dans le foie. Ce dernier sang, de faible vélocité, ne se
mélange pas avec celui venant du D.V., et occupe la portion antéro-droite de la veine cave
inférieure ; c’est donc avec une forte différence de vélocités que les 2 « sangs » arriveront au
cœur droit.
Foramen ovale ou Trou de Botal : Le sang avec forte vélocité (apporté par le D.V.)
franchit facilement la Crista Dividens (formant le bord supérieur du Foramen Ovale), tandis
que l’autre sang « tombe » dans l’oreillette puis le ventricule droit.
Canal artériel : C’est une communication entre l'artère pulmonaire et l'aorte par laquelle
le sang arrive dans l'oreillette droite puis dans le ventricule droit (et donc à faible vélocité), et
qui emprunte la portion initiale de l'artère pulmonaire, gagne aussitôt la crosse de l'aorte sans
passer par le poumon ; l'aorte transporte donc un mélange de sang oxygéné (venant
directement du placenta via le D.V.) et peu oxygéné (venant du secteur veineux du fœtus via le
foie ; le sang aortique est distribué à tout l'organisme fœtal et assure ainsi l'oxygénation et la
nutrition tissulaire fœtale.
Les artères ombilicales assurent le retour du sang vers le placenta. Elles sont branchées
sur les artères hypogastriques, elles-mêmes ramifications terminales de l'aorte.
Les artères cérébrales moyennes reçoivent leur sang des carotides, et, comme ces
dernières, voient leur résistance chuter fortement à partir de la 30 ème semaine. Cette période
semble bien correspondre à ce qu’on observe comme une réponse adaptative du fœtus qui
épargne le cerveau lors de la baisse graduelle de la pression partielle en oxygène du 3 ème
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
37
trimestre. Ce phénomène connu sous le nom de « Brain Sparing Effect » est exagéré en cas
d’hypoxie (il y a alors forte chute de résistance, ce qui permet alors à beaucoup plus de sang de
continuer à irriguer le cerveau).
N.B. : Contrairement à la règle qui veut que deux (2) veines accompagnent une (1) artère, chez
le fœtus, c'est une (1) veine (ombilicale) qui est chargée de sang riche en oxygène, et se fait
accompagner de deux (2) artères (ombilicales) véhiculant du sang pauvre en oxygène et riches
en déchets métaboliques que le fœtus renvoie pour élimination vers le placenta.
Shunts de la circulation sanguine fœtale
2) Oxygénation du sang fœtal
Le fœtus obtient de l’oxygène grâce aux mécanismes suivants :
- amincissement progressif de la surface d’échange materno-fœtal ;
- accroissement de la concentration sanguine en hémoglobine ;
- la présence de l’hémoglobine F (HbF),
La qualité des échanges gazeux qui assurent l'oxygénation correcte de l'enfant, va donc
dépendre de :
- la circulation fœtale;
- l'intégrité de la paroi villositaire; et surtout
- la circulation du sang maternel dans la chambre intervilleuse (= flux sanguin utéro-
placentaire, facteur essentiel de l'oxygénation fœtale).
Pendant le travail (l'accouchement), les contractions utérines diminuent le flux sanguin total,
notamment les contractions puissantes de la période d'expulsion.
3) Nutrition fœtale
La nutrition fœtale est variable selon l’âge gestationnel :
- au premier trimestre, c’est par la vésicule vitelline que le jeune embryon se nourrit ;
- aux deuxième et troisième trimestres le fœtus se nourrit surtout de nutriments provenant de
la mère, à la faveur de la perméabilité placentaire, ainsi que de nutriments en provenance du
placenta lui-même.
a. Nutriments en provenance de la mère via perméabilité placentaire
Apport en macronutriments
On retient que le fœtus utilise le glucose comme nutriment principal, mais ne le produit de
façon endogène qu'en quantité négligeable ; la glycémie fœtale est fonction de la glycémie
maternelle. Le passage materno-fœtal s'effectue via diffusion facilitée ; au minimum, la
glycémie fœtale représente les 2/3 de celle de la mère). Les protéines plasmatiques passent de
la mère au fœtus par transport actif (à l'encontre du gradient des concentrations).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
38
Apport en micronutriments
Le fœtus est servi par le biais de perméabilité placentaire, à peu à travers les mécanismes
passifs (oxygène, vitamine C si à très forte dose), et surtout par les mécanismes actifs
concernant les acides aminés, les minéraux (le fer, le calcium, le magnésium, l’iode, le
phosphate, et probablement d’autres cations), ainsi que les vitamines hydrosolubles (B et C).
Les substances soumises à ce mode de passage placentaire sont plus concentrées dans le sang
fœtal que dans le sang maternel ; ce mode de passage placentaire induit une véritable
spoliation maternelle. La spoliation maternelle est plus prononcée à certaines périodes de la
grossesse (surtout au 3ème trimestre pour le Fe, d’où l’importance de l’anémie ferriprive des
prématurés).
b. Nutriments en provenance du placenta à travers son propre métabolisme
Ceci concerne notamment le métabolisme intermédiaire du lactate que le placenta peut
recycler pour produire du glucose.
Le rôle que le placenta joue dans la production et l'utilisation de nutriments fœtaux concerne
également l'interconversion de la sérine et de la glycine grâce à une interaction avec le foie
fœtal. En effet, le foie fœtal et le placenta produisent un nombre important d'acides aminés,
assurant presque entièrement la couverture des besoins fœtaux en lysine et en glycine. Un
phénomène du même genre s'applique à l'échange glutamine-glutamate.
4) Adaptations cardio-vasculaires et respiratoire du nouveau-né
L'adaptation circulatoire et respiratoire à la naissance se fait de façon progressive pour la
première, et immédiate pour la dernière. Les stimulations externes qui jouent un grand rôle
dans l'apparition du premier mouvement respiratoire :
- la compression du thorax de l'enfant à travers la filière génitale maternelle au cours de
l'accouchement (Laminage);
- le passage brutal d'un milieu liquide à un milieu aérien;
- le changement brusque de température (37 degrés in utero à la température ambiante).
Quant à la circulation sanguine, il y a ARRET DE LA CIRCULATION PLACENTAIRE, ce
qui a pour effet la redistribution du sang dans le reste de l'organisme. La résistance artérielle
diminue progressivement par amincissement des parois artérielles (en une dizaine de jours). Le
résultat se traduit par un passage sanguin de plus en plus facile dans la petite circulation.
L'accroissement progressif du volume sanguin empruntant le ventricule gauche va entraîner la
FERMETURE DU FORAMEN OVALE (TROU DE BOTAL). Cette fermeture est d'abord
fonctionnelle, puis anatomique au bout d'un an. Il y aura ensuite OBLITERATION ET
ATROPHIE DU CANAL ARTERIEL (vers le 37ème mois). Enfin, oblitération et atrophie du
canal veineux d'Arantius.
5) Maturation fœtale
La maturation fœtale évolue parallèlement avec l'âge de la grossesse et s'exprime sur tous les
organes et systèmes. L'étude des certains produits du métabolisme de ces organes permet ainsi
d'apprécier le degré de maturité du fœtus.
L'appareil digestif du fœtus fonctionne très peu : le fœtus déglutit en permanence du liquide
amniotique. La bile et les sécrétions des muqueuses digestives forment dans l'intestin ce
contenu vert noirâtre qui constitue le méconium. C'est plutôt par le foie que l'on apprécie la
maturité digestive. La maturité hépatique se traduit par un taux de bilirubine amniotique de
plus en plus voisin de 0 mg/100 ml au voisinage du terme, ce qui signe alors une certaine
capacité du foie à conjuguer la bilirubine. Cette capacité n'est d'ailleurs entièrement acquise
qu'après plusieurs jours de vie, d'où la gravité de certains ictères du nouveau-né.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
39
L'appareil rénal excrète une urine très peu concentrée, ce qui se traduit par une teneur en
créatinine du liquide amniotique progressivement croissante, jusqu'à atteindre des valeurs
proches de 1,6 à 2 mg/100 ml (37 semaines de gestation).
La peau qui mûrit manifeste sa capacité au renouvellement (desquamation dont l'étude peut se
faire après coloration au ROUGE CONGO ou encore au SOUDAN III). La proportion des
cellules cutanées desquamées colorées en orange (cellules orangées provenant des glandes
sébacées) atteint ou dépasse 10 % au voisinage de 38 semaines. Cet indice de maturité fœtale
n'est pas lié au poids, ce qui peut constituer un net avantage lorsque, comme dans certaines
situations pathologiques, le petit volume du fœtus fait penser à une grossesse plus jeune que
l'âge gestationnel.
Les surrénales tirent leur importance, du point de vue de leur maturité, du fait qu'elles
participent pour beaucoup dans la production de l'œstriol (élimination prépondérante chez la
mère), lui-même témoin de la vitalité fœtale.
La maturité pulmonaire est finalement l'élément le plus important de la maturité fœtale. Elle
est à la base de la survie ou du décès de la plupart des prématurés. La maturation pulmonaire
se caractérise par une production de plus en plus croissante (dès la 34ème semaine) du
SURFACTANT, une substance phospholipidique synthétisée par la paroi alvéolaire DONT
ELLE EMPECHE ALORS LE COLLAPSUS OU L'ATELECTASIE. C'est donc un agent
tensioactif dont le rôle est de diminuer les tensions de surface lors de l'expiration et d'éviter
que l'alvéole ne se vide complètement d'air (air résiduel).
Les deux (2) principaux phospholipides constitutifs du surfactant sont la lécithine et la
sphyngomyéline dont le rapport densimétrique constitue un excellent témoin de la maturité
fœtale. La maturité pulmonaire est donc atteinte si L/S ≥ 2. Elle est insuffisante si elle est < 2.
C'est dans ce dernier cas qu'il y a le plus grand risque de DETRESSE RESPIRATOIRE DU
NOUVEAU-NE OU MALADIE DES MEMBRANES HYALINES, du fait de l'atélectasie
progressive des alvéoles dont nous avons parlé plus haut.
La maturité squelettique du fœtus a longtemps été appréciée par la radiographie (mesure de
la longueur de la colonne lombaire selon SZEBOK, mesure de la longueur de la diaphyse
fémorale selon MAGNIN, point d'ossification épiphysaire fémoral inférieur ou BECLARD à
36 semaines, point d'ossification épiphysaire tibial supérieur ou TODT à 38 semaines, point
d'ossification de la tête humérale à 41 semaines, etc. Depuis quelque temps, l'échographie est
venue supplanter ces méthodes, grâce à la mesure, plus proche de la réalité, des diamètres
bipariétal et abdominal transverse, ainsi que celle de la longueur du fémur.
La capacité antigénique : la majeure partie des anticorps que le fœtus soit capable de
fabriquer sont des Ig M (au niveau de la rate). Les antigènes qui en stimulent le plus la
production sont d'origine bactérienne, ainsi que ceux du groupe Rhésus des globules rouges.
Les Ig G que possède le fœtus sont heureusement d'origine maternelle, et sont transférés en si
grand nombre que, vers la fin de grossesse, on retrouve des concentrations plasmatiques
équivalentes chez la mère et chez le fœtus.
La production des Ig A au niveau des intestins ne commence que quelques semaines après la
naissance, en réponse aux infections intestinales, d'où la très grande susceptibilité du nouveau-
né aux infections digestives.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
40
I.6. ANNEXES FŒTALES
I. LE PLACENTA
1) Anatomie du placenta
Le placenta est constitué de deux parties :
- une partie maternelle provenant de la transformation subie par la muqueuse utérine (appelée
alors CADUQUE) et qui correspond à la zone d'implantation (= PLAQUE BASALE);
- une partie ovulaire provenant de l'œuf (= PLAQUE CHORIALE).
Entre les deux plaques se trouvent les chambres intervilleuses, limitées par l'union des deux
plaques à la périphérie du placenta, formant ainsi ce qu'on appelle anneau obturant de winkler.
Figure : Chambre intervilleuse
Certaines des branches villositaires atteignent la plaque basale où elles s'insèrent par une ou
plusieurs boucles: ce sont les VILLOSITES CRAMPONS qui assurent l'adhérence du placenta
fœtal à la portion utérine. La plupart de ces villosités n'atteignent cependant pas la plaque
basale et constituent les VILLOSITES LIBRES qui flottent dans les lacs sanguins des espaces
intervilleux. Qu'elles soient libres ou crampons, les villosités se recourbent à leur extrémité qui
se termine toujours ainsi dans la chambre intervilleuse.
2) Physiologie du placenta
La circulation du sang maternel au niveau de la chambre intervilleuse s'établit au 18-21ème
jour. Le flux sanguin utéro-placentaire dépend de la pression artérielle maternelle et de la
pression intra-utérine. La circulation se fait de la manière suivante:
- le sang maternel est injecté dans la chambre intervilleuse sous forte pression, et sous la
forme d'un jet dirigé contre la plaque choriale ;
- le sang diffuse alors vers le sinus marginal ;
- le sang quitte enfin la chambre intervilleuse par les orifices veineux très larges, disposés
surtout à la base des septa intercotylédonnaires.
Les échanges respiratoires et nutritionnels au niveau de la chambre intervilleuse se passent
entre le sang fœtal des villosités placentaires (choriales) et le lac sanguin maternel remplissant
la chambre intervilleuse.
La perméabilité placentaire est sous la dépendance de:
- la valeur des flux sanguins materno-fœtaux ;
- la membrane placentaire (surface d'échange) ;
- la différence des pressions hydrostatiques de part et d'autre de cette membrane ;
- la différence des pressions osmotiques de part et d'autre de la membrane placentaire.
C’est ce qui confère un caractère sélectif à la paroi villositaire + la paroi vasculaire des
veinules ombilicales, base de la notion de BARRIERE PLACENTAIRE.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
41
NB : Alors qu’on a longtemps pensé que les sangs de la mère et du fœtus ne se mélangeaient
jamais, il a été démontré grâce au test de Kleihauer (frottis de sang maternel périphérique) que
près de 75% de femmes enceintes voient leur sang « contaminé » de cellules sanguines en
provenance du fœtus à l’un ou l’autre moment de la grossesse. Aussi bien la fréquence que
l’importance de cette « contamination » (= la quantité de sang passé du fœtus à la mère)
augmentent avec l’âge gestationnel, passant respectivement de 3% et 0,03 ml au premier
trimestre à 45% et 2,5 ml au troisième trimestre. Et en cas d’avortement spontané le risque est
de 1% et 0,1 ml ; le risque est de 20-25% en cas d’avortement provoqué.
3) Placenta : glande endocrine
Le placenta est capable de synthétiser :
- dès le début de la grossesse, les hormones polypeptidiques dont la structure rappelle celle
des stimulines hypophysaires : H.C.G. ou hormone chorionique gonadotrope ; H.P.L. ou
hormone lactogène placentaire ;
- dès qu'il prend le relais du corps jaune gravidique maternel, les hormones stéroïdes que sont
progestérone et œstrogènes ; le moment de ce relais (= fin du 3ème mois) a aussi été
identifié comme TROU HORMONAL, parce qu'il constitue une charnière importante (sorte
de remise reprise entre ovaire et placenta) dont la défaillance peut être à la base
d'avortement d'origine hormonale (progestérone).
a. Hormones peptidiques
L'H.C.G. est synthétisée par le chorion ovulaire ou trophoblaste. Sa sécrétion débute dès le 8-
12ème jour post ovulatoire. On n'en trouve plus trace dans la circulation maternelle au delà du
6ème jour après l'accouchement (sauf persistance d´une activité trophoblastique pathologique
ex. en cas maladie trophoblastique). Son action est essentiellement de stimuler la sécrétion
hormonale du corps jaune ovarien et d'assurer sa survie.
L'H.P.L. est aussi appelée hormone chorionique somato-mammotrophique (H.C.S.). Elle est
sécrétée par le syncytiotrophoblaste, et son apparition coïncide avec celle de l'H.C.G. (12 ème
jour de grossesse). Elle ne s'élimine que très peu dans les urines. L'H.P.L. possède 4 actions
(rôles, effets) biologiques dont l'effet global est de favoriser l'anabolisme du fœtus, à savoir :
- action lutéotrope : maintien du corps jaune de la grossesse;
- action lactogène : stimulation de la prolifération de l'épithélium glandulaire mammaire (=
effet mammotrophique); au cours de la grossesse, elle exerce avec les œstrogènes une
inhibition sur la sécrétion de prolactine hypophysaire, puisque leur chute conjointe après
l'accouchement déclenche la lactation (effet lactogène);
- action somatotrope = stimulation de la croissance fœtale en potentialisant les effets de la
somathormone hypophysaire, et en favorisant la synthèse des protéines;
- action métabolique au niveau des trois métabolismes fondamentaux (lipides, glucides et
protides) = lipolyse accrue avec libération de triglycérides et d'acides gras à partir des
graisses de réserve + baisse de consommation du glucose dont le rôle énergétique est
confisqué par les graisses, d'où l'effet DIABETOGENE + accroissement de la synthèse
protéique.
La SP1 ou Specific pregnancy glycoprotein ou encore ß1-GLYCOPROTEINE est une
production exclusive du placenta, essentiellement au niveau de la chambre intervilleuse. Sa
production est sous la régulation de la glycémie maternelle. Sa demi-vie est de 34 heures. On
lui attribue des propriétés immunosuppressives qui tiendraient à sa localisation (dans les
citernes du réticulum endoplasmique, sur la surface extracellulaire de la membrane plasmique
du syncytiotrophoblaste).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
42
Son intérêt en obstétrique tient à l'exclusivité de son site de production, les espaces
intervilleux, siège de l'essentiel des échanges materno-fœtaux. D'où son exploitation en cas de
RCIU où sa valeur prédictive et pronostique est souvent comparée à celle de l'HPL.
La RELAXINE est aujourd'hui reconnue comme une production du placenta favorisant le
relâchement ligamentaire dans le petit bassin.
b. Hormones stéroïdes
La PROGESTERONE, production habituelle de l'ovaire, au niveau du corps jaune menstruel,
devient une production essentielle du corps jaune gravidique, puis (à partir du 4ème mois de la
grossesse) du placenta.
La progestérone a un rôle connu : soutenir la grossesse en maintenant le myomètre dans un état
quiescent; elle a également un rôle putatif: servir d'agent immunosuppresseur en inhibant les
cellules T intervenant dans le rejet des tissus de greffe.
Les OESTROGENES produits par le placenta sont au nombre de trois (3): œstrone -
œstradiol - œstriol. Ce dernier occupe la plus grande part, et sa production s'effectue à partir
des androgènes fœtaux. C’est l'aromatisation de la testostérone par le placenta qui permet
d'obtenir l`œstrone et l'œstradiol ; pour obtenir l'œstriol, il faut l'intervention du foie et des
surrénales du fœtus; le placenta n'intervient qu'à la fin du processus pour désulfater puis
aromatiser les substrats ainsi traités au niveau du fœtus ; c'est alors que l'œstriol produit est
presque totalement (± 90%) renvoyé dans la circulation maternelle d'où il est excrété par les
urines maternelles.
4) Quant à la fonction immunologique du placenta,
Elle résulte de ce que la grossesse peut être considérée comme une greffe homologue
parfaitement tolérée pendant 9 mois d'un organisme étranger dans l'organisme maternel. Les
mécanismes intimes d'une telle tolérance sont mal connus. Les interrogations s'adressent aussi
bien à la durée exceptionnelle de la tolérance, à l'absence totale d'immunisation maternelle
contre la greffe (sauf cas d'iso-immunisation rhésus) et contre des grossesses ultérieures.
II. CORDON OMBILICAL
Le cordon ombilical est un fourreau (une tige) qui relie le fœtus (par l'ombilic) au placenta. Sur
ce dernier, il s'insère près du milieu de la face fœtale, mais parfois tout près du bord (insertion
marginale ou en raquette), et rarement directement sur les membranes (insertion
vélamenteuse). Au niveau de l'ombilic du fœtus la gaine du cordon se continue avec la peau du
ventre fœtal. Il est constitué de 3 éléments anatomiques essentiels:
- trois vaisseaux (une veine ombilicale unique centrale et volumineuse qui ramène vers le
fœtus le sang oxygéné chargé de nutriments; deux artères ombilicales enroulées en spirale
autour de la veine et qui proviennent des artères hypogastriques du fœtus en conduisant vers
le placenta le sang fœtal appauvri en oxygène et chargé de déchets);
- un tissu mésenchymateux de remplissage et de protection qu'on appelle GELATINE OU
GELEE DE WHARTON;
- une gaine extérieure formée par l'amnios.
A terme, le cordon ombilical est arrondi, turgescent, tordu en spirale blanchâtre et luisant. Sa
longueur est d’environ 30-70 cm en moyenne et son diamètre de 1,5 cm.
Les anomalies de longueurs peuvent être associées aux pathologies funiculaires : nœuds,
procidence, bretelles. La longueur du cordon peut également avoir des incidences sur le
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
43
déroulement de l'accouchement: trop court, il peut gêner la descente et la sortie du fœtus; trop
long, il peut facilement faire des boucles (= CIRCULAIRES) autour du cou et du corps du
fœtus où elles peuvent se serrer, soit au cours de la grossesse (parfois jusqu'à amputer un
membre), soit au cours de l'accouchement (avec gêne grave à la circulation sanguine dans le
cordon, correspondant à une véritable strangulation de l'enfant); de plus un cordon trop long
aura tendance à glisser plus facilement devant la présentation et à sortir avant le fœtus, ce qui
réalise l'entité dénommée PROCIDENCE DU CORDON.
III. MEMBRANES OVULAIRES
Elles sont constituées d'AMNIOS et de CHORION. Elles forment le sac ovulaire qui contient
le liquide amniotique.
L'amnios est d'origine ectodermique et tapisse l'intérieur du sac amniotique, y compris la face
fœtale du placenta et la gaine du cordon ombilical jusqu'au revêtement cutané du fœtus.
L'amnios est formé de plusieurs couches cellulaires très riches en mitochondries (ce qui
suggère une fonction sécrétoire).
Le chorion est une expansion du trophoblaste aux endroits où le placenta ne s'est pas
constitué.
Dès que l'orifice cervical s'ouvre, les membranes du pôle inférieur de l'œuf viennent, avec le
liquide amniotique qu'elles contiennent, former une espèce de hernie au contact de l'aire de
dilatation. Cette partie de l'œuf, représentée par le sac liquidien au contact de l'ouverture du col
(≥ 3 cm) porte le nom de POCHE DES EAUX.
IV. LIQUIDE AMNIOTIQUE
Il est contenu dans le sac amniotique et baigne le fœtus. Sa sécrétion débute assez tôt. De 30
ml à 10 semaines, sa quantité passe à 350 ml à 20 semaines, 1 litre à 38 semaines (500-1500
ml à terme).
Sa production est mixte: simple transsudation à partir des vaisseaux maternels au travers des
membranes surtout dans la première moitié de la grossesse - sécrétion active par la membrane
amniotique dont les assises cellulaires sont riches en mitochondries - déversement des urines
fœtales dans le sac ovulaire. Ce dernier mécanisme prédomine dans la deuxième moitié de la
grossesse, et explique la concentration en créatinine, en urée, et en acide urique du liquide
amniotique plus élevée que celle du plasma.
Sa résorption est constamment assurée par: la déglutition fœtale suivie de la résorption
partielle digestive, du passage sanguin et du retour vers le placenta - la résorption active de la
part de l'amnios.
Il est composé de 99 % d'eau et de 1 % de sels minéraux et de substances organiques
(protides, glucose, enzymes, etc.). Près du terme, le liquide amniotique contient en suspension
des cellules fœtales desquamées, des fins poils (=LANUGO ou fin duvet recouvrant la peau du
fœtus), des flocons de vernix caséeux, et de leucocytes. Il contient également de nombreux
métabolites fœtaux. Le fait que le liquide amniotique contienne des sels minéraux (notamment
le sodium) et les mucopolysaccarides est à la base de sa cristallisation particulière en feuilles
de fougère. Cette forme de cristallisation a donné lieu à un test (TEST DE
CRISTALLISATION ou FERN TEST) par lequel on sait distinguer le liquide amniotique des
autres écoulements liquides des voies génitales au cours de la grossesse.
Son rôle physiologique est à la fois mécanique, métabolique, et nutritionnel.
Il est mécanique parce que:
- il protège le fœtus contre les chocs;
- il réalise l’isolément thermique du fœtus ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
44
- il empêche le fœtus de coller aux parois du sac, ce qui prévient ainsi les adhérences, elles-
mêmes source de malformations;
- il donne au fœtus de bouger en tout sens, un peu indépendamment des lois de la pesanteur,
comme les astronautes dans l'espace.
Il est métabolique parce qu'il participe à l'hydratation fœtale. Il est nutritionnel parce que les
nutriments qu'il peut contenir peuvent passer au fœtus par déglutition et par imbibition au
niveau du cordon.
Son rôle médical et obstétrical vient de ce que:
- en le prélevant par amniocentèse et en analysant son contenu, il permet de surveiller un
grand nombre de paramètres de bien-être fœtal;
maturité fœtale par le rapport lécithine-sphingomyéline (L/S) ;
recherches génétiques ;
malaise fœtal en cas changement de coloration (liquide méconial = souffrance
fœtale ; rouge rosé = mort fœtale ; jaune = incompatibilité rhésus ou ABO ;
purulente = chorio-amniotite) ;
- il acquiert une signification particulière de lien avec le bien-être fœtal à partir de 16-20
semaines d’âge gestationnel, moment où le rein fœtal qui ne démarre la production d´urine
qu´après 12 semaines, constitue un appoint important à la production du liquide amniotique;
- il existe un autre lien, plutôt physiologique, qui tient au rôle de la diurèse fœtale dans la
production du liquide amniotique; cette fonction diurétique est perturbée en cas de stress
prolongé ; et le fait que les modifications de la quantité du liquide amniotique correspondent
au moment où la crise fœtale se précise, a fait que l’évaluation du liquide amniotique figure
au point de départ des plusieurs schémas de surveillance fœtale;
- à l’accouchement, il protège le fœtus contre l’infection, et il permet non seulement de
former un coussin = poche des eaux (une espèce de pare-choc) au fœtus qui fendille les
voies génitales maternelles, mais aussi de « lubrifier » la voie et éviter ainsi les « couches
sèches »; c‘est la raison pour laquelle il est souhaitable qu‘il ne s‘écoule pas (rupture de la
poche des eaux) avant une ouverture suffisante du col utérin.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
45
I.7. SEMIOLOGIE OBSTETRICALE ET SURVEILLANCE D'UNE
GROSSESSE NORMALE
1) Procédés de la sémiologie obstétricale
Les principales préoccupations de la sémiologie obstétricale portent sur:
- le diagnostic de la grossesse
- la détermination de l'âge de la grossesse
- le terme de la grossesse
- l'état de bien-être fœtal et néonatal
- l'état des annexes fœtales
- l'état de bien-être maternel
- le pronostic de l'accouchement et des suites de couches rapprochées et lointaines.
2) Sémiologie spécifique du 1er trimestre de la grossesse = diagnostic de la grossesse
Elle vise les points suivants:
- diagnostiquer la grossesse;
- déterminer les éléments qui feront l'objet d'une surveillance au cours de la grossesse, soit
parmi soit en plus du poids, de la tension artérielle, de la protéinurie, et de la glucosurie.
Le diagnostic de la grossesse au premier trimestre est aussi dit diagnostic de grossesse
débutante. Il comprend:
- l'anamnèse = Aménorrhée + Signes fonctionnels aussi appelés Signes sympathiques ;
- la clinique = signes généraux + SIGNES UTERINS;
- la paraclinique = TESTS DE GROSSESSE + EXAMENS SPECIAUX.
1) L’anamnèse
Elle achoppe sur l'AMENORRHEE dont la véracité, la durée, et la forme sont à préciser.
L’âge de la menarche peut être utile pour les primipares. Les signes sympathiques sont avant
tout digestives (nausées, vomissements, inappétence, inversion ou altération de goûts,
constipation), et est appuyée par une fatigabilité. Elle peut être aussi urinaire, ou psychique
(irritabilité). Ce sont des signes parasympathiques, mais plus connues sous le vocable de
« signes sympathiques de la grossesse ». L'ampleur de ces signes doit être estimée.
L’anamnèse se poursuit par une recherche systématique concernant l’identité de la femme, son
âge, son état civil, sa profession et ses antécédents.
- L’âge : les extrêmes d’âge constituent un groupe à haut risque ; les gestantes très jeunes (ex.
moins de 15 ans) peuvent souffrir de malnutrition, avoir une vie désordonnée et peuvent être
abandonnées par l’auteur de la grossesse et/ou la famille, ou avoir des complications osseuses
dues à l’immaturité de leur bassin. Les gestantes âgées de plus de 40 ans courent le risque de
malformations congénitales fœtales souvent dues au vieillissement des ovocytes et beaucoup
d’autres complications obstétricales (diabète, hypertension artérielle, hémorragie du post-
partum)
- L’Etat civil : célibataire et veuve de niveau socio-économique bas=élément de haut risque.
- La profession : certaines professions peuvent avoir des conséquences sur la grossesse :
exemple, les gestantes travaillant dans un laboratoire où on manipule des produits chimiques
ou viraux, ou dans un service de radiologie, courent un grand risque de malformation fœtale.
- Les antécédents familiaux : recherche des pathologies héréditaires dans la famille de la
gestante et celle de son mari : diabète, hypertension artérielle, drépanocytose homozygote
(anémie SS) ou drépanocytose hétérozygote (Hémoglobine AS) ainsi que les antécédents des
malformations congénitales dans les deux familles.
- Les antécédents personnels médico-chirgicaux : ils visent à connaître tout le passé médico-
chirurgical de la gestante avec insistance sur les pathologies qui peuvent influencer la
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
46
grossesse ou vice-versa : diabète, HTA, asthme, tuberculose, cardiopathie, traumatisme du
bassin, etc. on recherche également des intoxications à certaines substances nocives à la santé
de la mère et/ou du fœtus ; alcool, tabac, certaines drogues, allergies médicamenteuse,
alimentaires ou autres. Il est aussi important de connaître les immunisations soit par des
vaccins, soit par des maladies contractées : rougeole, rubéole, poliomyélite, tétanos, etc.
- Les antécédents personnels gynéco-obstétricaux : la date et l'issue des maternités antérieures
telles que révélées par le P G A (parité-gestité-abortus).
Parité = nombre d’accouchements d’enfants ayant atteint l’âge de viabilité (24-28 SA ou NN
ayant pesé 500 gr ou plus), vivants ou morts. Etant donné les difficultés d’élevage des
prématurissimes dans nos milieux (RDC) il est d’usage de considérer l’accouchement à partir
d’un nouveau-né pesant au moins 1 Kg ou une grossesse qui est arrivée à la 28ème semaine.
- Nullipare : c’est une femme qui n’a jamais accouché ;
- Primigeste : femme qui est à la toute première grossesse ;
- Primipare : femme qui a accouché une fois ou qui est au terme de sa première grossesse ;
Gestité = nombre de grossesses (intra-utérines, extra-utérines, molaires et les avortements).
- Multigeste : femme qui a été enceinte plusieurs fois ;
- Multipare : femme qui a accouché 3-4 enfants ;
- Grande multipare ; femme qui a 5 accouchements ou plus.
NB : le fait de connaître la gestité et la parité nous permet de catégoriser la gestante en groupe
à haut risque ou non. On s’intéresse aussi au type d’accouchements : eutocie (accouchement
normal) ou dystocie (accouchement difficile), au poids des enfants antérieurs, au nombre
d’enfants vivants ou décédés, au moment et à la cause de décès.
2) La clinique
L’examen clinique recherchera d'abord les signes du retentissement gravidique sur l'état
général, puis les signes utérins (= signes d’examen gynécologique).
i. Les signes généraux
Il s’agit de :
- l’hyperthermie de 3 semaines (pour celles suivies avec une courbe de température) ;
- la transformation de la ligne blanche en ligne noire (LINEA NIGRA) ;
- la turgescence mammaire (6-8 semaines);
- les stries abdominales ou vergetures (± 3 mois chez les primigestes, et plus tôt chez les
autres), hypertrophie de la papille gingivale ou épulis
- le "masque de la grossesse", lui, est plus tardif, soit ± 16 semaines, et correspond à une
hyperchromie luisante des parties saillantes du visage qui prend alors l'aspect en "écailles".
ii. Les signes d'examen gynécologique
a) A l'inspection (regard direct et spéculum)
- Humidité vaginale due à la congestion.
- Coloration vaginale virant au bleu ou au pourpre; ce signe mis en évidence pour la première
fois par Jacquemier est cependant appelé "signe de Chadwick".
- Hypersécrétion vaginale (tout à fait physiologique).
- Coloration cervicale virant aussi au bleu; c'est le "signe de Goodell".
b) A la palpation (toucher vaginal)
- Ramollissement cervical.
- Ramollissement de la jonction col-corps; d'abord limité à une petite zone circonscrite en
antérieur (= signe de "Ladin"); puis le ramollissement s'étend, permettant de délimiter le
globe utérin (= signe de "Hégar" à 6 semaines). Les doigts vaginaux placés en avant de lui
arrivent facilement au contact des doigts abdominaux, à tel point que le corps paraît, au
dessous de cette charnière, comme détaché du col et pourrait même être pris pour une masse
indépendante.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
47
- Autres signes: le "signe de Piskacek" (= tuméfaction asymétrique du fundus due à la
nidation = à distinguer d'un myome, d'une malformation utérine ou d'une masse annexielle
qui, eux, persistent après la 10ème semaine alors que ce signe disparaît).
- Augmentation du volume utérin, plus nette à partir de la 4ème semaine. A ce stade, il est
coutume de représenter le volume utérin en le comparant à certaines images bien connues
de la vie pratique: mandarine, orange, pamplemousse, poing etc. Les culs-de-sac sont alors
comblés par l'utérus = signe de Noble (= Le doigt qui suit le cul-de-sac latéral, au lieu de
s’enfoncer librement, bute contre le pourtour évasé de l’utérus).
- Palpation des annexes (trompes et ovaires) pour faire découvrir des masses soit
concomitantes à la grossesse, soit permettant d'expliquer l'aménorrhée qui a fait penser à la
grossesse (Kyste - abcès - GEU).
c) A l'auscultation RAS, sauf Sonicaid à partir de 8 à 10 semaines.
N.B. : Autres situations pouvant provoquer une aménorrhée : les affections psychologiques, les
dysfonctionnements ovariens et les anomalies structurales de l'endomètre (ex. synéchies).
3) La paraclinique
Les examens hormonaux et instrumentaux, ainsi que certains examens passés dans la routine.
Certains sont démodés, d'autres sont inaccessibles selon le milieu où l'on se trouve.
i. Les examens (tests) hormonaux biologiques
- L’examen extemporané des urines ou test de grossesse ou test à la bandelette : détecte la
présence de l’HCG dans les urines (qualitative) ;
- Le dosage plasmatique ou urinaire de l’HCG (quantitative) ;
Dans le temps, on recourait aux tests utilisant l'urine des femmes supposée enceintes injectée :
- soit chez le crapaud mâle (ce qui provoque la libération des spermatozoïdes = ±
éjaculation), c'est le "Frog test" de Galli-Mainini qui donne un résultat en 2 heures et qui
est valable entre la 8ème et la 16ème semaine de gestation (bufo-test).
- soit chez la rate impubère (cela produit une ovulation objectivable par la présence d'un
corps jaune = "test d'Ascheim-Zondek");
ii. Les examens (tests) hormonaux de type privatif (= test à la progestérone)
Le test à la progestérone ou Progest test consiste à administrer de façon brève (2-3 jours) 50
mg de progestérone/jour en I.M. En interrompant ainsi l’administration, si on est en l'absence
de grossesse, on provoque dans les 7-10 jours une hémorragie utérine dite de privation
progestéronique, signe d'un climat à prédominance œstrogénique. Donc il n’y a pas grossesse.
Il y a absence d'hémorragie en cas de grossesse, signe d'un climat à prédominance
progestéronique auquel la progestérone ainsi administrée ne fait que l’effet de renforcement.
iii. Les examens (tests) immunologiques
Ils exploitent la réaction d'agglutination (2 minutes à 2 heures). Leur sensibilité est très
variable d'un test à l'autre. Ils donnent des résultats faux positifs en cas de protéinurie + ou
d'usage de tranquillisants. Il y a également les tests radio-immunologiques plus spécifiques,
utilisant la sous unité β de l'HCG.
iv. Les examens instrumentaux
- L'échographie ou ultrasonographie permet de diagnostiquer la grossesse dès la 4è semaine,
avant l'augmentation du volume utérin;
- La cœlioscopie peut mettre en évidence une localisation extra-utérine de la grossesse.
v. Les examens spécifiques et non spécifiques
Les examens spécifiques et obligatoires: sérologie TORCH = toxoplasmose + rubéole +
cytomégalovirus + herpès, sérologie VDRL et VIH.
Les examens non spécifiques = Hb, Hc, GE, Cytobact urinaire et selles.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
48
3) Sémiologie spécifique du 2-3eme trimestre de la grossesse = vérification +
surveillance = organisation des consultations prénatales
a. Examen clinique
i. Examen clinique général
L’examen physique général vise à préciser l’état général de la gestante : une talle ≤ 150 cm
peut faire soupçonner un mauvais bassin ; un poids ≤ 50 kg fait penser à une dénutrition ou une
immaturité, tandis que ≥ 90 kg fait évoquer une obésité. Le poids, la taille, le pouls, la tension
artérielle (TA) ainsi que la température seront déterminés. L’état des conjonctives palpébrales
et bulbaires, la présence ou absence des œdèmes des membres inférieurs seront également
précisés. On recherchera les anomalies squelettiques comme la boiterie (cfr asymétrie du
bassin si la différence entre les deux diamètres obliques est > 1 cm), la cyphose, la scoliose, les
séquelles de poliomyélite et cicatrices traumatiques ou chirurgicales surtout au niveau du
bassin.
Pour être complet, l’examen physique doit également s’intéresser à l’inspection, la palpation,
la percussion et l’auscultation des différents organes comme le cœur, le poumon etc.
Il est conseillé de déshabiller la gestante progressivement au cours de ces différentes étapes de
l’examen afin de lui éviter d’être complètement nue durant tout l’examen.
ii. Examen gynéco-obstétrical
Inspection : on constatera les modifications gravidiques générales et locales (cfr. Supra)
Palpation : dépend de l’âge de la grossesse au moment où la gestante est examinée. A partir de
12 SA, le fond utérin (FU) devient facile à déterminer à la palpation abdominale.
Dans le dernier trimestre de la grossesse, la palpation de la masse utérine s’effectue suivant
une procédure définie comme « manœuvres de Léopold ». Les manœuvres de Léopold, au
nombre de 4, déterminent l’attitude fœtale par rapport au corps maternel.
1ère Manœuvre : on délimite le fond utérin et on détermine la partie
fœtale qui l’occupe. L’examinateur, placé à la droite de la gestante, le
regard tourné vers le visage de cette dernière, place ses deux mains
jointes pour cerner le fond, et il cherche à différencier le siège qui est
mou et irrégulier, de la tête qui est dure, ronde, régulière et ballotante.
C'est cette manœuvre qui précède la mensuration de la hauteur
utérine. La mesure se fait grâce à un ruban métrique, avec comme
repère en bas, le bord supérieur de la symphyse pubienne et en haut le
fond utérin, la gestante étant en décubitus dorsal, genoux fléchis.
2ème Manœuvre : consiste à chercher de quel côté se trouve le dos
fœtal. L’examinateur, dans la même position que ci-dessus, place les
2 mains de chaque côté de l’abdomen en s’appuyant sur ses bords
ulnaires; d’un côté, on palpe une formation linéaire, dure, qui
correspond au dos ; de l’autre, on palpe plusieurs parties nodulaires
qui correspondent aux membres. C’est cette manœuvre qui indique
l’endroit de prélèvement du rythme cardiaque fœtal.
Le prélèvement du rythme cardiaque fœtal (RCF) s'effectue au
niveau de l’un des 4 quadrants autour du nombril de la gestante, les quadrants supérieurs pour
le fœtus en siège, les quadrants inférieurs pour la présentation céphalique, et autour du nombril
pour la présentation transversale. Ce prélèvement s’effectue de 2 manières:
- prélèvement soit au stéthoscope de Pinard, soit au Sonicaid ;
- enregistrement continu (au moins 20 minutes), à l'aide d'appareillage électronique (ou
moniteur) ; c’est le Monitoring obstétrical.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
49
3ème Manœuvre : recherche la partie fœtale qui se trouve dans le
bassin. L’examinateur se positionne en tournant le dos à la gestante.
Il effectue les mêmes manipulations que lors de la recherche de la
partie fœtale qui occupe le fond de l’utérus. Si la tête n’est pas encore
engagée, on la reconnaît facilement car ronde, régulière et ballotante.
Dans la présentation du siège, cette partie est en continuité directe
avec la colonne vertébrale dans une position dorso-antérieure.
4ème Manœuvre : elle détermine le degré de descente de la partie
fœtale en présentation ; une seule main placée au dessus du pubis,
attrape entre le pouce et le médius la partie fœtale qui se trouve au
niveau de la symphyse pubienne. Ce sera donc une présentation
HAUTE ET MOBILE (sans aucun contact avec le bassin osseux),
AMORCEE (mobile mais butant contre les structures du D.S.),
FIXEE (non mobile parce que calée au niveau du détroit supérieur),
et ENGAGEE (à confirmer par le TV par le signe de Farabeuf).
L’examen au spéculum permet d’observer les modifications au niveau du vagin, du col, ainsi
que d’autres pathologies co-existantes avec la grossesse (exocervicite, polype, etc.)
Le toucher vaginal (TV) permet d’apprécier le vagin, le col, l’utérus ainsi que l’état du bassin
osseux de la gestante.
b. Age gestationnel
Après examen d’une femme enceinte, la conclusion doit toujours être tirée sur la date et le
pronostic de l'accouchement, ainsi que sur l'opportunité de la poursuite de la grossesse. D’où la
nécessité de connaître l’âge gestationnel. Ce dernier est aussi l’élément de base à partir duquel
toute évaluation de la croissance fœtale peut s’effectuer. Il est généralement établi grâce à des
paramètres non biométriques (anamnèse des dernières règles + anamnèse de la fécondation)
et biométriques (hauteur utérine + mensurations ultrasonographiques).
iii. Calcul de la date présumée de l'accouchement
La durée moyenne d'une grossesse dans l'espèce humaine est de 275 jours à partir de la
conception, qui correspond grosso modo à la date de l'ovulation. Si donc, théoriquement, on
ajoute 9 mois à cette date, on obtient la date probable de l'accouchement.
La règle consiste à ajouter 7 jours à la date, et à retrancher 3 mois (pour avril jusque décembre)
ou ajouter 9 mois (pour janvier, février et mars) au mois des dernières règles (exemples).
Lorsque le mois de février est compris dans le calcul, il est recommandé d’ajuter 9 jours plutôt
que 7 à la date.
iv. Règles pour apprécier l'âge gestationnel à partir de la clinique
- Règle de Mc Donald : Age (en mois lunaires) = Hauteur ut. (cm)/4 ; Age en semaines =
Hauteur utérine x 8/7.
- Règle de Naegele : Age (en mois lunaires) = [Hauteur ut./4] + 1.
- Règle des 4 de Bartholomew (Bartholomew's rule of fourths): elle consiste à diviser par 4
les distances entre symphyse et ombilic (si la hauteur utérine est comprise dans ces limites)
puis entre ombilic et pointe du xiphoïde (si c'est entre ces limites); chaque ligne correspond
à un mois; et en considérant ensuite que l'ombilic correspond à 5 mois de grossesse et la
limite supérieure à 9 mois, on estime l'âge gestationnel à partir du niveau où se trouve la
hauteur utérine.
- Formule de SPIEGELBERG : à partir du FU ou de la hauteur utérine (HU) : A 20 SA, le
FU est à l’ombilic. La progression du FU est ensuite de 4 cm par mois. A terme, il y a
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
50
régression de ± 2 cm due à la descente du mobile fœtal. Il existe cependant certaines
variations d’une femme à une autre.
Hauteur de l’utérus aux différents âges de la grossesse
- à 3 mois calendrier, la hauteur utérine est de 8 à 9 cm;
- à 4 mois calendrier, la hauteur utérine est de 16 cm;
- à 5 mois calendrier, la hauteur utérine est de 20 cm;
- à 6 mois calendrier, la hauteur utérine est de 24 cm;
- à 7 mois calendrier, la hauteur utérine est de 28 cm;
- à 8 mois calendrier, la hauteur utérine est de 30 cm;
- à terme, la hauteur utérine est de 32 à 34 cm.
v. Règles pour apprécier le volume fœtal à partir de la clinique
= Formule de Johnson : Poids fœtal (en grammes) = [Hauteur ut. - n] x 155 où la valeur de n
= 11 si le sommet est plus bas que les épines sciatiques (engagement), et 12 s'il est au niveau
ou au dessus des épines sciatiques
N.B. La meilleure façon d'estimer le poids fœtal est de recourir à l'échographie.
c. Organisation des consultations prénatales (CPN)
1) Le nombre et le calendrier de CPN
Le nombre total de CPN attendues est d'au-moins 3 (cfr OMS) pour prétendre assurer une
couverture acceptable de la grossesse, capable ainsi d’éviter la prématurité et la postmaturité,
surveiller les grands organes (circulatoire, digestif, urinaire) de la gestante, et prévoir les
modalités d'accouchement. L’idéal est d’en avoir 8 à 9.
Le calendrier des visites prénatales peut être conçu de façon à prévoir 1 CPN par mois jusqu'à
6 mois; 1 CPN par 2 semaines entre 6 et 8 mois; 1 CPN par semaine de 8 mois jusqu'à terme.
2) Le contenu des CPN
Parmi les éléments standards à prélever à chaque visite, on retient :
- le poids ; la croissance attendue est 400 – 500 g par semaine ;
- la pression artérielle ; elle doit rester constamment normale (< 135 / 85 mmHg), et devrait
même avoir tendance à baisser ; et une élévation de ≥ 30 pour la systolique et 15 pour la
diastolique doit être considéré comme la manifestation de l’hypertension ;
- la présence ou non des œdèmes (surtout des membres inférieurs) ; leur apparition, associée
à une élévation des chiffres tensionnels et à la présence d’une protéinurie fait poser le
diagnostic d’une pré-éclampsie qui est une des grandes pathologies de la grossesse ;
- les MFA, signe de vitalité du fœtus ;
- la HU, un des marqueurs de la croissance fœtale ; la croissance attendue est en moyenne de
4 cm par mois ;
- le RCF, preuve de vie fœtale, susceptible de révéler des anomalies qui poussent alors à
d’autres investigations ;
- la recherche d’une protéinurie et/ou une glucosurie.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
51
Les autres éléments spécifiques sont à adapter à chaque cas c. Ex. l’hyperglycémie
provoquée par voie orale (HGPO) chez les femmes avec glycémie à jeun élevée ou avec
antécédent de macrosomie ; le Coombs indirect chez les gestantes Rh négatif (cfr le Rhéso-
gamma chez les gestantes Rh négatif non immunisées peut être administré à la 28ème semaine
de grossesse).
3) La vaccination au cours des CPN
La vaccination obligatoire au cours des CPN concerne la vaccination antitétanique, en raison
de la future grande plaie que laissera le placenta à sa zone d’implantation (plaie cavitaire). Elle
devrait débuter à la 24ème semaine de gestation. Il faut un minimum de 2 vaccins (à 1 mois
d’intervalle) pour une couverture acceptable.
Si la gestante est sous vaccination pour l’Hépatite B, elle peut continuer et terminer sa cure. La
gestante exposée à l’Hépatite A peut recevoir sa sérothérapie avec immunoglobulines. La
vaccination antigrippale n’est pas contre-indiquée.
4) Les recommandations particulières au cours de la grossesse
Ces recommandations concernent l’hygiène alimentaire (régime varié et peu lipidique) et
vestimentaire (vêtements amples, aérés et confortables), l’activité physique (gymnastique
adaptée pour conserver une bonne sangle abdominale), et sexuelle (modération dans le premier
mois pour éviter les avortements, ainsi que dans le dernier mois pour éviter la rupture
prématurée des membranes).
d. Explorations fonctionnelles de l'œuf
A. Explorations fonctionnelles au premier trimestre
Au premier trimestre le bien-être ovulaire est essentiellement représenté par des signes
ultrasonographiques et hormonaux suivants:
- présence et dimensions du sac vitellin (variant entre 3,5 et 6,5 mm de diamètre) ;
- présence de battements cardiaques dès que la longueur crânio-caudale ou LCC =5 mm ;
- clarté de la nuque < 2,5 mm).
- taux d’HCG et d’HPL.
D’autres explorations (cordocentèse, biopsie du trophoblaste) peuvent aider à effectuer des
analyses cytogénétiques (ex. pour exclure une trisomie).
B. Explorations fonctionnelles aux deuxième et troisième trimestres
1) Comptage des mouvements fœtaux actifs (MFA)
Ce comptage peut se pratiquer 3 fois par jour pendant 30 minutes par séance. On additionne le
nombre de MFA par jour. Il y a risque fœtal quand il y a diminution des MFA jusqu’à 40 %
des MFA par rapport au jour précédent. Le comptage se fait par la gestante et la méthode varie
d’une école à l’autre.
2) Amnioscopie
Permet d’observer le liquide amniotique (LA) à travers les membranes par la voie du canal
cervical avec une source lumineuse lorsque la grossesse est) terme.
Si le liquide amniotique est clair, c’est normal, il est pathologique quand il est vert, verdâtre,
jaune ou sanguinolent. L’absence de vernix caseosa signifie que soit la grossesse n’est pas à
terme ou est à terme dépassé.
3) Cardiotocographie
a. Non Stress Test (N.S.T.) ou monitoring
Réalisé pour détecter une souffrance fœtale éventuelle par effet Döppler lors des MFA.
- N.S.T. réactif : tracé avec configuration régulière ;
o BCF entre 120 et 160 battements par minute
o Augmentation de ceux-ci (BCF) d’au moins 15 battements par minute durant au moins
20 secondes lors des MFA.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
52
- NST suspect : moins de 3 MFA pendant 40 minutes, durée de réaction fœtale moins de 20
secondes lors des MFA ou plus de 50 seconde sans configuration régulière.
- Tracé non satisfaisant : tracé non interprétable.
Indications du NST
1) Obstétricales :
- Dépassement de terme - Grossesse multiple
- Antécédent de mort in utéro - Oligohydramnios
- Dysgravidie - Isoimmunisation Rhésus
- Rupture prématurée des membranes (RPM)
- Diminution des mouvements fœtaux actifs
- Retard de croissance intrautérin (RCIU)
2) Médicales
- Diabète sucré - Cardiopathie
- HTA chronique - Néphropathie
- Malaria ou toutes autres pathologies fébriles
b. Tocodynamométrie
Réalisé pour étudier l’activité utérine (contractions)
Eléments à étudier :
1) tonus de base
2) fréquence, durée, intensité et amplitude des contractions utérines.
Indications de la tocodynamométrie
- Menace d’accouchement prématuré
- Induction de travail (ocytocine ou prostaglandine, cytotec…)
- Evaluation du traitement tocolytique
- Travail sur utérus cicatriciel
c. Contraction Stress Test (C.S.T.° ou test à l’ocytocine (O.C.T= oxytocin chalenge
test) ou monitoring dynamique.
Pratiqué pour évaluer les réserves respiratoires ou en oxygène du fœtus. On place un Théobald
(10 unités d’ocytocine dans 1 litre de sérum glucosé à 5 %). Dès qu’on obtient 3 contractions
utérines (C.U.) par 10 minutes, on prend les BCF au cours e ces CU. On peut ainsi avoir les
différentes décélérations (DIP) avec leur signification.
- DIP 1 : ralentissement précoce à l’acmé de la CU. Ceci correspond à la compression
crânienne entraînant un réflexe vagal avec bradycardie transitoire.
- DIP 2 : ralentissement tardif qui survient vers la fin de la CU. Ceci signifie une
réduction d’apport d’oxygène au fœtus soit par hypotension maternelle, soit par anémie
maternelle, soit par fibrose placentaire, … c’est le cas le plus grave.
- DIP 3 : ralentissement survenant à n’importe quel moment de la CU. Ceci signifie une
compression du cordon ombilical.
4) Amniocentèse
Permet de prélever le liquide amniotique pour des nombreux examens notamment la
détermination du rapport Lécithine/Sphingomyéline (L/S) pour la maturité pulmonaire, dosage
de la créatininémie, bilirubinémie dans l’incompatibilité Rhésus, examen des cellules fœtales
orangées pour la recherche de la maturité fœtale, etc ;
5) Le score biophysique de MANNING
Permet d’apprécier le bien-être fœtal ainsi que le risque encouru par le fœtus. Ce score
comporte 5 paramètres (4 éléments échographiques et le monitoring statique).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
53
Variable biophysique Normal (score = 2) Anormal (score = 0)
paramètres
1) Mouvements ≥ 1 épisode de durée > 30 sec pendant 30 min Absence ou présence d’un épisode de durée
respiratoires d’observation inférieur à 30 min pendant 30 min
d’observation
2) Mouvements > 3 en 30 min d’observation des épisodes des < 3 pendant 30 minutes
fœtaux actifs mouvements actifs continus = un seul épisode.
3) Tonus fœtal Attitude fœtale normale : flexion tête, colonne ½ flexion ou extension complète ou pas de
vertébrale, extrémité. retour en flexion.
Extension puis retour en flexion.
Au moins 1 épisode d’extension active plus
retour en flexion des membres fœtaux.
4) Liquide amniotique Etendu dans la cavité utérine ; la plus grande Absence du LA dans la plupart des surfaces
(LA) lame liquidienne > 1 cm dans le sens vertical au de la cavité utérine ; la plus grande lame
moins une poche de LA qui mesure au moins 2 liquidienne < 1 cm dans l’axe vertical ou
cm dans les deux plans perpendiculaires moins d’une poche > 2 cm dans des plans
perpendiculaires
5) NST Réactif Non réactif
Interprétation des résultats du score biophysique de Manning
Résultats Interprétation Décision
10/10 Risque d’asphyxie fœtale extrêmement rare Intervention
8/10 Préciser s’il existe un tissu rénal fonctionnel et
(LA↓) SFC probable membranes intactes. S’il en est ainsi, accoucher pour
indication fœtale.
6/10 (LA Si fœtus à terme → accoucher
normal) Test suspect, possibilité d’asphyxie fœtale Si prématurité → répéter test dans 24 h.
Si < 6/10 → accoucher
6/10 Accouchement pour indications fœtales
Asphyxie fœtale probable
(LA↓)
4/10 Haute probabilité d’asphyxie foetale Accouchement pour indications fœtales
2/10 Asphyxie fœtale presque certaine Accouchement pour indications fœtales
0/10 Asphyxie fœtale certaine Accouchement pour indications fœtales
6) Ultrasonographie Doppler
La technique d’ultrasonographie Doppler peut être appliquée dans l’étude du flux sanguin de
certains vaisseaux maternels ou fœtaux.
a. Doppler de l’artère utérine
La sonde doppler est placée au niveau de l’abdomen maternel en regard de l’artère utérine.
Normalement la valeur de la diastole (D) est la moitié de la systole (S). Index diastolique =
D/S = 50/100. Le Doppler de l’artère utérine est perturbé en cas de pathologie maternelle
comme la dysgravidie.
b. Doppler de l’artère ombilicale
Le curseur Doppler est placé au niveau de l’artère du cordon ombilical. Normalement la
diastole est le tiers de la systole. Index diastolique = D/S = 30/100. On a des valeurs anormales
quand la diastole tend vers zéro.
c. Doppler de l’artère cérébrale
Le curseur Doppler est placé au niveau de l’artère cérébrale. L’index diastolique et de 10 à 20
%. Ce doppler cérébral est perturbé quand la diastole augmente, le fœtus souffrant tendant à
privilégier la circulation cérébrale au détriment d’autres organes.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
54
I.8. ACCOUCHEMENT NORMAL OU EUTOCIE
On appelle accouchement l'expulsion hors des voies génitales maternelles du produit de
conception et de ses annexes à partir d'une période correspondant à la viabilité (28 semaines =
1000 grammes). Dans beaucoup de pays cependant, la survie néonatale est actuellement
atteinte dès que la grossesse arrive à 20 semaines (poids limite de 500 grammes). Avant 28
semaines il y a avortement. Entre cette limite de 28 semaines et la pleine maturité fœtale (37
semaines), on parle de prématurité (1700 gr à 32 semaines, 2400 gr à 34 semaines). Le mot
TERME est réservé à la grossesse qui progresse à partir de 37 semaines jusqu'à 42 semaines (≥
2500 gr). Après cette période on parle de post-terme ou de grossesse prolongée.
Les contractions utérines conduisant à l'accouchement = TRAVAIL.
La durée des contractions du travail ainsi que leur intensité sont croissantes. Au début du
travail elles surviennent toutes les 15 à 20 minutes et durent 15 à 20 secondes. En cours de
travail, toutes les 2 à 3 minutes durant 40 à 60 secondes. A la fin de l'expulsion, c'est à chaque
minute qu'elles surviennent durant 50 à 60 secondes. La douleur qui les accompagne est
ressentie (et exprimée) par la femme en fonction de plusieurs facteurs parmi lesquels il faut
citer: les rapports fœto-pelviens - la force des contractions - l'état physique et émotionnel de la
parturiente - et le niveau d'éducation.
Le déroulement du travail suit un cheminement classique qu'on reconnaît à travers les 3
PERIODES DE L'ACCOUCHEMENT: ouverture du col utérin (= DILATATION) - expulsion
du mobile fœtal (= EXPULSION) - et expulsion du placenta et des annexes (=
DELIVRANCE).
1. DILATATION
L'efficacité des contractions utérines est donc appréciée sur base de la progression de la
dilatation du col et de la descente fœtale qu'elles entraînent.
L'ouverture du col de l'utérus ou dilatation débute avec les contractions utérines. Le col perd
progressivement de sa longueur pour ne plus former qu'un simple orifice, c'est
l'EFFACEMENT du col qui se traduit par une disparition progressive du canal cervical que
l'on exprime en % en fonction du degré de cette disparition par rapport à la situation initiale
(qui est de 0 %). L’effacement précède donc généralement l’ouverture du col.
- Grossesse de 19
SA
- Col dilaté à 2 cm
sur toute sa
longueur
- poche des eaux
bombant dans le
vagin à travers
l’orifice externe du
col utérin
L’élargissement progressif de l'orifice du col une fois que celui-ci s’est effacé s’appelle
DILATATION, passant par les diamètres de 1 jusqu'à 10 centimètres; à son maximum, la
dilatation réalise une parfaite continuité de canal entre la cavité utérine et la cavité vaginale;
c'est le CYLINDRE UTERO-VAGINAL; c'est la période la plus longue du travail, soit 6 à 8
heures chez la multipare, et 8 à 12 heures chez la primipare.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
55
2. EXPULSION
L'expulsion peut commencer bien avant les contractions, mais elle débute généralement avec la
dilatation. Le fœtus progresse dans le détroit supérieur en présentant un de ses pôles dans une
situation favorable (tête bien fléchie en cas de présentation du sommet). Cette progression
s'effectue selon 3 mécanismes: ENGAGEMENT - DESCENTE - DEGAGEMENT.
L'ENGAGEMENT (entre tête et bassin), qui est le temps le plus essentiel de l'accouchement,
se fait par FLEXION de la tête fœtale et dans le diamètre oblique du bassin maternel
(généralement gauche). On parle d'engagement lorsque le diamètre le plus utile de la tête
fœtale (maximum = 9,5 à 10 cm) franchit le détroit supérieur.
ENGAGEMENT suivant le diamè
diamètre
oblique gauche
.
Il faut pour cela que le fœtus présente sa tête en oblique (OIGA - OIDA - OIGP - OIDP), et
que la flexion de la tête sur le tronc se maintienne de façon parfaite, au point que l'occiput soit
le sommet du fœtus. D'où le terme de PRESENTATION DU SOMMET.
La DESCENTE du mobile fœtal est fortement influencée par la force des contractions
utérines, la force de la presse abdominale, et la résistance du plancher pelvien. Le fœtus se voit
imposer une modification d'orientation (le sommet engagé dans un diamètre oblique se
dégagera dans un diamètre antéropostérieur), et une modification d'axe (engagement dans l'axe
ombilic-pointe du coccyx et dégagement par redressement suivant l'axe imprimé par la
courbure du sacrum).
DESCENTE suivi de ROTATION la tete
est dans l’l’axe anté
antéro-
ro-posté
postérieure
.
Ainsi, la descente s'effectue grâce à un mouvement de rotation du fœtus c'est la ROTATION
INTERNE, imposée par le contact avec les releveurs de l'anus - la saillie des épines sciatiques
- et les contre-pressions de l'arc antérieur du bassin sur la tête fléchie. Le résultat est le suivant:
- d'abord, il y a changement d'axe d'orientation du sommet qui tourne de la position Oblique à
la position P (postérieure), puis à T (transverse), puis A (antérieure), ou encore de A à P;
- ensuite, changement d'axe de progression selon la courbe parallèle à la concavité sacrée.
Le DEGAGEMENT de la tête fœtale ou le franchissement du détroit inférieur commence au
moment où la tête affleure l'orifice vulvaire et que le périnée commence à bomber.
Dès que la plus grande circonférence arrive sous l'ogive pubienne, la tête fait saillie au niveau
du détroit inférieur en présentant le diamètre sous-occito-bregmatique.
En se défléchissant, nuque calée sous la symphyse pubienne, le fœtus va alors se comporter
comme s'il redressait la tête, c'est la DEFLEXION. L'enfant naît en regardant le sol.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
56
EXPULSION DE LA TETE ROTATION DE RESTITUTION
. .
C'est un moment où les contractions utérines se voient renforcées par les efforts de poussée
maternels. C´est la classique PRESSE ABDOMINALE (envie de pousser déclenchée par le
contact de la tête fœtale avec le plancher pelvien).
Dès qu'elle est dégagée, la tête effectue spontanément une rotation de 90 degrés. C'est la
ROTATION EXTERNE qui est en fait le reflet du mouvement du dos fœtal qui correspond à
la rotation des épaules "obligées" de présenter un diamètre bi-acromial rapeti à 9 cm pour
passer au niveau du détroit supérieur.
L’EPAULE
ABAISSEMENT DE L’ L’EPAULE
ABAISSEMENT DE L’
ANTERIEURE POSTERIEURE
. .
L'épaule antérieure apparaît sous le pubis et se dégage, puis l'épaule postérieure racle le
périnée d'arrière en avant et se dégage.
3. DELIVRANCE
La délivrance est l’ensemble des phénomènes qui aboutissent à l’expulsion des annexes
fœtales (placenta, cordon ombilical et membranes) ou du délivre. C’est la période qui s’écoule
depuis la sortie du fœtus et la fin des 24 premières heures. L'accouchement ne peut pas être
considéré comme terminé tant que les annexes n'ont pas été expulsées.
La délivrance évolue en trois phases : décollement du placenta ; expulsion ou migration du
placenta ; hémostase.
A) Phase de décollement
Cette phase est sous la dépendance de la rétraction utérine qui la prépare et de la CU qui la
provoque.
1er temps préparatoire : la rétraction utérine est un phénomène passif et permanent
caractérisé par une diminution du volume de l’utérus après expulsion du fœtus, compensée par
l’augmentation de l’épaisseur de ses parois. Mais l’épaississement respecte la zone placentaire
qui reste mince. Il en résulte un enchatonnement physiologique du placenta. Au fond de la
cuvette ainsi circonscrite, le placenta est assez plissé, étirant les villosités crampons qui
l’amarrent à la caduque dont le clivage est ainsi préparé. Ce temps correspond à la phase de
rémission clinique et dure 10 à 15 minutes.
2ème temps = Décollement proprement-dit : la CU, phénomène actif, est la cause principale
du décollement placentaire. Dès que les contractions reprennent, elles accentuent l’effet de la
rétraction. Elles provoquent un clivage de la caduque soit à la jonction des deux couches
superficielles et profondes, soit en pleine zone superficielle, soit irrégulièrement suivant un
trajet qui emprunte ça et là l’un des plans précédents. Le clivage de la muqueuse en ouvrant le
sinus veineux détermine des foyers hémorragiques qui confluent en une nappe sanguine
continue : hématome rétroplacentaire physiologique qui à son tour aide à parfaire le
décollement.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
57
B) Phase de migration ou d’expulsion
Sou l’influence des CU puis de son propre poids, le placenta tombe dans le segment inférieur
qui déplisse en surélevant le corps utérin. Les membranes entraînées à leur tour se décollent en
se retournant en doigt de gant, puis la migration se poursuit vers le vagin et l’orifice vulvaire.
Dans les cas habituels où le placenta s’insère au fond de l’utérus ou à son voisinage, il sort par
sa face fœtale (mode SCHULTZE ou BAUDELOCQUE). Dans le cas où l’insertion est
basse, le placenta peut sortir par un bord ou la face utérine ou maternelle (mode DUNCAN).
Le sang ayant décollé le petit côté des membranes s’échappe lors même du décollement
placentaire. La délivrance paraît plus hémorragique.
C) Phase d’hémostase
Elle est assurée par :
- la rétraction utérine qui maintenant intéresse la zone placentaire, les vaisseaux sont
étreints et obstrués par les anneaux musculaires de la couche plexiforme ; mais la rétraction
n’est possible et durable qu’après évacuation totale de l’utérus, condition sine qua no d’une
hémostase rigoureuse et durable ;
- la coagulation sanguine : thrombose physiologique qui obstrue l’ouverture utérine des
sinus veineux ; pour que ces différents mécanismes puissent s’exécuter parfaitement, le
placenta doit être normal ; normaux aussi doivent être la contractilité et le processus de la
coagulation, sinon les complications de la délivrance risquent de se produire.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
58
I.9. SURVEILLANCE DU TRAVAIL ET DE L'ACCOUCHEMENT
1. SURVEILLANCE DU TRAVAIL
Elle intéresse les contractions utérines, le rythme cardiaque fœtal, la dilatation du col, et la
progression du fœtus.
a) Les contractions utérines
La contraction se manifeste au palper manuel comme un durcissement utérin caractéristique et
intermittent. Des détails plus précis peuvent être obtenus grâce à un enregistrement externe ou
interne des pressions intra-utérines. Les contractions utérines signent l'entrée en travail. Mais il
existe des faux travaux, des "fausses alertes" dont l'élément distinctif d'avec le vrai travail est
le manque d'effet notable sur le col. Elles sont accompagnées par des douleurs intermittentes et
rythmées. Ces douleurs (contractions) augmentent progressivement d'intensité, de fréquence et
de durée. L'ENTREE EN TRAVAIL est confirmée par la mise en évidence de l’un au moins
des signes objectifs suivants:
- émission à la vulve de quelques glaires, ± striées de sang (Bouchon muqueux); c'est la
preuve que le col commence à s'effacer et que la poche des eaux commence à se constituer,
ce qui chasse alors la glaire jusque là collectée au niveau du col;
- modification du col utérin, caractérisée par son raccourcissement progressif
(=Effacement du col), suivi ensuite de son ouverture (=Dilatation); mais chez la multipare,
les deux phénomènes vont souvent de pair;
- rupture des membranes, avec écoulement abondant et continuel de liquide amniotique, ce
qui peut également constituer un mode d'entrée en travail; lorsqu'elle survient tout au début
du travail, la rupture des membranes est dite PREMATEREE, tandis qu'elle est
TEMPESTIVE en fin de travail, à dilatation très avancée.
b) Le rythme cardiaque fœtal
Il doit être surveillé fréquemment (toutes les 15 minutes au-moins) au cours du travail, car la
contraction utérine, en réduisant la réserve en oxygène de la chambre intervilleuse, constitue le
stress par excellence et peut alors révéler une perturbation du rythme du cœur fœtal (souffrance
fœtale aiguë).
Le rythme cardiaque fœtal ou RCF entre les épisodes de contractions utérines varie
normalement entre 120 et 160 battements par minute (= 30 à 40 au 1/4). A plus de 160 on parle
d'ACCELERATION (si de durée < 5 minutes) ou de TACHYCARDIE (si de ≥ 5 minutes). A
moins de 120 il y a DECELERATION (< 5 minutes) ou BRADYCARDIE (≥ 5 minutes) dont
le pronostic est plus grave que l'accélération ou la tachycardie.
On utilise un monitorage électronique continu (Monitoring obstétrical dynamique) dont les
éléments d'appréciation portent sur : le rythme cardiaque fœtal de base, sa variabilité (en dents
de scie), et les modifications périodiques normalement attendues du RCF (accélération en cas
de mouvement fœtal ou de contraction utérine).
c) L'effacement puis la dilatation du col
C’est un important test d'efficacité des contractions utérines, il doit impliquer certaines
caractéristiques à rechercher (toutes les 3 heures au début, puis en fonction des circonstances
comme après RUPTURE SPONTANEE DE LA POCHE DES EAUX ou RSPE): souplesse du
col et vitesse régulière de dilatation. Normalement il faut 6 à 8 heures pour passer de col fermé
à 4 cm de dilatation (= PHASE PASSIVE DU TRAVAIL = LENTE), puis environ 1 cm par
heure pour atteindre la dilatation complète (= PHASE ACTIVE DU TRAVAIL = RAPIDE).
La formation de la poche des eaux devra être notée. On veillera à préserver le plus longtemps
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
59
possible la fonction de « pare-choc » de cette poche des eaux pour le fœtus qui fendille les
voies génitales maternelles (en principe jusqu‘à ce que la dilatation atteigne 6 centimètres). En
cas de rupture de cette poche, l'aspect du liquide amniotique devra être signalé: il doit être
clair, et doit rester clair durant toute la durée du travail (en cas de souffrance fœtale le liquide
devient teinté du vert de MECONIUM = liquide méconial).
d) La progression du mobile fœtal
Sa surveillance permet de reconnaître l'engagement de la présentation, en confrontant les
données de la palpation abdominale et du toucher vaginal. Il y a engagement lorsque la
présentation empêche, au moment du toucher, les deux doigts explorateurs d'atteindre la face
antérieure du sacrum. Ce signe (de FARABEUF) peut être faussé en cas d'œdème plus ou
moins important du cuir chevelu fœtal appelé bosse sero-sanguine ou Caput succedaneum.
Ce dernier se forme par appel d’eau sur le cuir chevelu au niveau de la calotte crânienne qui se
trouve en deçà de la zone de dilatation du col (= vers le vagin), au moment où la partie du
crâne fœtal se trouvant encore dans la cavité amniotique est soumise à la surpression des
contractions utérines. C’est donc une structure qui se constitue après avoir atteint une dilatation
d’au moins 3 cm, et signe une certaine stagnation du travail. Il peut signer une disproportion
fœto-maternelle.
Une autre manière d'apprécier le niveau de descente consiste à utiliser les PLANS de HODGE
(= 4 plans parallèles du DS au DI, l'engagement correspondant alors à HODGE III).
Diagnostic de l'engagement (signe de Farabeuf)
Il faudra également déterminer la variété de position de la présentation. Dans la présentation
du sommet, c'est l'occiput qui est le repère-clef, et on désignera cette position selon 4 variétés
possibles : OIGA (66 % des cas), OIDP (31 % des cas), OIGP (2 à 3 % des cas), OIDA (très
rare).
e) Le partogramme
C’est un diagramme (sous forme graphique) sur lequel on porte toutes les informations
concernant les paramètres de surveillance du travail. Le PARTOGRAMME permet ainsi de
mesurer le progrès du travail. Ses caractéristiques ont été codifiées par FRIEDMAN. Il
reprend :
- en abscisse, le temps écoulé depuis l'arrivée de la parturiente en salle de travail;
- en ordonnée, la dilatation d'une part, la hauteur de la présentation d'autre part.
On y distingue bien 2 phases :
- phase de latence ou phase lente ou phase passive ; elle s’applique à la dilatation du col de 0
à 4 cm ; c’est la plus longue (6 à 8 heures) ;
- phase active ; elle part de 4 cm à la dilatation complète ; elle correspond à une dilatation
horaire de 1 cm.
La phase de latence est celle qui pose le plus grand nombre d’erreurs diagnostiques, étant
donné que, chez une femme admise en travail, on ne connaît pas toujours avec exactitude à
quel moment le travail a débuté. Soucieuse d’aider le personnel de la salle d’accouchement,
l’OMS a proposé un partogramme simplifié qui débute dès que la dilatation de 4 cm est
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
60
atteinte. Cela ne signifie nullement que la femme n’est pas surveillée avant d’atteindre une
dilatation de 4 cm (voir plus loin).
Cervicogramme ou partogramme simplifié
Pour la dilatation du col 2 diagonales servant de repère sont tracées : la première en fonction
du minimum attendu (soit 1 cm/h) = ligne d´alerte. La 2 ème ligne est tracée parallèlement à
intervalle de 4 heures = ligne d´action. La surface à la gauche de la ligne d´alerte = zone A. La
zone B est entre les 2 lignes. La zone C est à droite de la ligne d´action = Césarienne.
Sur un mauvais travail la ligne symbolisant la dilatation va avoir tendance à croiser la ligne
d´alerte, entrant ainsi dans la zone B. Dans ce cas il faut activement chercher l´étiologie de la
lenteur dans l´évolution du travail et la corriger si possible (ex. vider la vessie, stimulation,
amniotomie, etc.). On s´accorde encore alors 2 heures d´observation.
En cas de normalisation du travail la parturiente va continuer à évoluer dans la zone B. Au cas
contraire, la ligne d´action va être croisée, et l´on se retrouve dans la zone C = Césarienne.
En ce qui concerne la descente du mobile fœtal, si elle s´effectue normalement l´amniotomie
se fera spontanément.
Utilisation pratique du partogramme
Diagnostic de travail confirmé? Parturiente à classer soit dans la phase de latence, soit dans la
phase active :
- de la phase de latence, elle doit entrer en phase active après 4 heures maximum;
- en phase active, elle doit atteindre la dilatation complète en progressant de 1 cm/h au min.
Partogramme simplifié = absence de la phase de latence.
- Durée de surveillance = 6 heures au maximum.
- Ligne d`alerte commence à 4 cm de dilatation, et monte en pente vers le niveau de 10 cm
qu’elle atteint à la 6ème heure (Figure ).
2. SURVEILLANCE DE L'EXPULSION (Accouchement proprement dit)
A) Recommandations générales
A dilatation complète, un matériel simple est préparé sur une table protégée d’un champ
stérile, 2 pinces de KOCHER, une paire de ciseaux et des compresses. A portée sont les
instruments d’extraction fœtale, de réparation d’épisiotomie et d’une façon générale, tout le
matériel pouvant être nécessaire aux interventions chirurgicales courantes. Sur une autre table,
ou mieux dans une salle attenante aux soins à donner au nouveau-né sont disposés : une pince
de Bar ou un matériel de ligature, une bande pour le pansement ombilical. Une solution
d’antibiotique avec un compte-goutte pour instillation interpalpébrale, un bracelet d’identité
qui sera fixé autour du poignet du nouveau-né et à côté tout le matériel de réanimation.
La règle de conduite consiste à obtenir un accouchement graduel (= non précipité), mais
continu (= sans arrêt).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
61
La précipitation peut provoquer:
- des déchirures maternelles parfois graves;
- un changement brusque de pression intracrânienne du fœtus, avec comme conséquence, une
hémorragie cérébrale;
- des lésions traumatiques sur le fœtus, notamment sous forme de fractures au niveau des
membres supérieurs;
- un "ETONNEMENT UTERIN" par vidange brusque de la cavité utérine, ce qui risque de
gêner les phénomènes adaptatifs assurant normalement les contractions utérines nécessaires
au décollement placentaire et à l'hémostase physiologique.
L'arrêt de la progression, par contre, signifie:
- la présence d'une résistance résultant soit de l'étroitesse de la voie (détroit moyen et détroit
inférieur), soit l'importance du volume fœtal ;
- l'augmentation de la durée de séjour du mobile fœtal dans les voies, avec conséquence
possible la nécrose des tissus maternels ainsi longtemps coincés; après passage du fœtus, il
peut en résulter des escarres qui, en tombant, créent des fistules;
- l'allongement de la durée d'expulsion, ce qui peut retentir sur la qualité des échanges
materno-fœtaux et avoir des retombées néfastes sur le développement du système nerveux.
B) Recommandations particulières
Les 3 principales parties du corps fœtal concernées sont: la tête - les épaules- le tronc et les
jambes. C'est par les deux premières parties que les complications sont les plus susceptibles
d'arriver.
Avant que la tête n’apparaisse à la vulve : rien à faire.
Au moment où le périnée se distend, et que la vulve s'entrouvre pour faire apparaître la tête,
chaque nouvelle contraction utérine et chaque effort de poussée imprime à la tête un léger
mouvement de va-et-vient. Le périnée peut alors être élargi vers le bas aux doigts, afin de
mieux visualiser et apprécier la progression de la tête. Parfois la presse abdominale peut être
renforcée par une pression modérée appliquée sur le fond utérin par un assistant (Manœuvre de
CRISTELLER).
Expulsion de la tête et trajet de l’épisiotomie
Au moment où la tête distend le périnée en restant calée à l'introïtus vaginal, on peut
pratiquer:
- la manœuvre de Ritgen "modifiée" qui consiste à favoriser la déflexion grâce à une pression
appliquée de bas en haut sur la région coccygienne;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
62
- une EPISIOTOMIE (incision périnéale médiane ou, de préférence médio-latérale de 3 - 5
cm) lorsque la menace de rupture (déchirure) devient imminente à cause de la fragilité
périnéale ou de l'exiguïté particulière de l'introïtus vaginal;
- un contrôle de la sortie du menton pour l'empêcher d'agir comme un "rasoir" qui peut ainsi
déchirer le périnée.
L'occiput est calé
calé sous la symphyse pubienne, on poursuit par Demander à la parturiente d'expirer pendant la poussé
poussée afin
pression le ralentissement de l'expulsion. d'en diminuer l'intensité
l'intensité et maintenir la pression sur la tête
. .
Continuer, avec la main occipitale, de contenir la tête afin de La pression occipitale est maintenue la main pé
périné
rinéale exerce une
ralentir l'expulsion afin de pré
prévenir la dé
déchirure du pé
périné
rinée, l'autre pression qui vise à "moucher le bé
bébé. Une fois la tête hors de la
main tentera sous le pé périné
rinée de crocheter le menton afin de vulve demander à la parturiente de ne plus pousser, visualiser le
contrôler lentement la progression cé céphalique. Demander alors à sens de rotation cé
céphalique qui sera complé
complété manuellement de
la parturiente de ne plus pousser 45°
45° dans le même sens (rotation de restitution)
. .
Au moment où la tête, sortie, n'a pas encore effectué la rotation externe, il est recommandé de:
- vérifier si le cordon ombilical ne s'enroule pas autour du cou (= CIRCULAIRE); s'il y a
circulaire, il faut repousser le cordon au delà des épaules en le glissant doucement; s'il est
serré et non refoulable, il faut le clamper et le sectionner entre deux pinces (attention !);
- exercer une traction modérée sur la tête en effectuant la rotation externe qui, comme on l'a
vu plus haut, permet aux épaules de s'engager dans le bon sens.
Au moment où les épaules se présentent au périnée, une traction contrôlée vers le bas
permet le dégagement de l'épaule antérieure, puis une traction vers le haut laisse dégager
l'épaule postérieure. Le reste du corps suit alors sans problème.
En exerç
exerçant la bascule de la tête vers le haut, l'é
l'épaule
Le dé
dégagement de l'é
l'épaule anté
antérieure est ré
réalisé
alisé posté
postérieure est dé
dégagé
gagée.
en excerç
excerçant la traction de la tête vers le bas Surveiller le pé
périné
rinée pendant cette phase
. .
Après l'expulsion, l'enfant est tenu par les pieds, donc tête en bas, pour faciliter le drainage
des mucosités accumulées dans l'arrière-gorge et des sécrétions bronchiques. L'enfant doit être
tenu plus bas que le placenta, pour favoriser le drainage du sang funiculaire en provenance du
placenta (environ 30-90 ml) vers l'enfant.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
63
N.B.:Le cordon doit être laissé battre jusqu'à cessation spontanée, sauf si l'enfant n'a pas
manifesté des signes d'activité (cri), auquel cas une hâte peut être mise à clamper le cordon à ±
10 cm de l'ombilic pour le sectionner entre deux pinces, et se préoccuper de la réanimation de
cet enfant.
3. SURVEILLANCE DE LA DELIVRANCE
La période de migration du placenta décollé s'accompagne d'un mouvement d'ascension
(montée) du fond utérin de 3 à 4 cm du fait de la distension du segment inférieur au passage du
gâteau placentaire; puis vient la redescente du fond utérin en dessous de l'ombilic lorsque, en
descendant dans le vagin, le placenta libère le segment inférieur qui se plisse alors de nouveau.
A l’examen, on constate une petite quantité de sang par la vulve, le FU remonte de 3 à 4 cm
au-dessus de l’ombilic. L'utérus alors rétracté forme au dessus du pubis une boule arrondie et
dure appelée GLOBE DE SECURITE parce que garant d'une bonne hémostase. En effet, la
quantité totale de sang que la parturiente perd dans ce cas est de l'ordre de 400 à 500 ml et ne
menace pas en principe la vie de l'accouchée. On dit alors que l'hémorragie est
PHYSIOLOGIQUE. RETRACTION UTERINE et COAGULATION SANGUINE forment
donc la base de l'hémostase au moment de la délivrance.
La délivrance comporte des gestes à éviter et d'autres à recommander.
a) Avant la mise sur pied de la technique de GATPA, l’accoucheur devait éviter:
- la traction sur le cordon, surtout avant le décollement placentaire, ce qui peut entraîner une
INVERSION UTERINE et une dilacération placentaire;
- se précipiter à agir alors qu'il n'y a pas d'hémorragie donc pas encore de PLAIE
CAVITAIRE (après décollement placentaire);
- s'inquiéter du retard de la délivrance avant 30-45 minutes.
Pour éviter cela, il était ainsi recommandé de :
- placer la pince de clampage du cordon juste au niveau de l’introïtus vaginal, afin de juger
du décollement placentaire dès que cette pince migre vers le bas ; il fallait alors vérifier
toutes les 5 minutes si la pince a migré de 2 à 3 centimètres vers le bas (c'est le signe
d'AHFELD qui signifie que le placenta est décollé);
- si le signe d'AHFELD est absent, il est toujours possible que le placenta soit décollé ; pour
en être sûr, il faut pratiquer la manœuvre de BRANDT-ANDREWS = cela se fait en
exerçant une pression abdominale sus-pubienne qui élève alors le fundus uteri, ce qui
permet à un placenta décollé de tomber; si le placenta n'est pas encore décollé, le cordon
remonte;
- exprimer le placenta décollé par pression intra-manuelle sur le fundus (manœuvre de
CREDE);
- placer sous la vulve un récipient pour recueillir le placenta, récolter et quantifier le sang dû
à l'hémorragie de la délivrance;
- administrer le méthergin (0,2 mg I.V. ou I.M.) ou l’ocytocine dès que la délivrance est
terminée, après avoir prélevé la TA ;
- examiner le périnée, à la recherche de lésion (éraillure-D1 à D3 ou déchirure du 1er degré,
2ème ou 3ème degré parfois compliquée d'une atteinte partielle ou totale du sphincter anal =
grave) ;
- examiner le placenta.
b) Avec la gestion active de la 3ème période de l’accouchement
Tout accoucheur est tenu de :
- écourter la délivrance et, ainsi assurer une économie de sang, en pratiquant la
DELIVRANCE ASSISTEE qui consiste à administrer 0,2 mg (= 1 ampoule) de Méthergin
I.V. à la mère au moment où la tête fœtale franchit le périnée;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
64
- A la place du Méthergin, on recommande de plus en plus l’Orasthin (10 unités IV) ; cette
mesure n’est pas nécessaire chez les parturientes déjà sous perfusion d’Orasthin ;
- et dès que l’enfant est sorti, application de la GATPA ou gestion active de la troisième
période de l’accouchement = la traction douce mais soutenue sur le cordon, à la manière de
la délivrance au cours de l’opération césarienne.
c) L'examen du placenta
Il fait partie intégrante de la surveillance de la délivrance.
Comme organe d'origine maternelle, le placenta peut, en se décollant mal, laisser béants des
vaisseaux maternels et ainsi provoquer une hémorragie maternelle grave, parfois mortelle.
Dans d'autres cas, des restes placentaires peuvent être à l'origine d'une infection post-partale.
Comme organe d'origine fœtale, le placenta traduit en partie les agressions subies par le
fœtus au cours de sa vie intra-utérine, et peut de ce fait expliquer une partie des anomalies de
croissance ou de comportement fœtal. Des prélèvements peuvent, à l'occasion, être effectués
sur lui pour des études plus approfondies.
Les éléments d'examen du placenta sont le poids et la forme, l'aspect de la face maternelle et
fœtale, le niveau d'insertion du cordon ombilical, la longueur et l'architecture du cordon
ombilical, ainsi que l'état des membranes fœtales.
Le dimensions et poids normal du placenta à terme mesure 15 à 20 cm dans son plus grand
diamètre, et 2 à 3 cm d'épaisseur dans sa partie la plus charnue; il pèse alors près de 450
grammes. Des placentas plus petits sont rencontrés dans les pathologies hypertensives qui
induisent un retard de croissance intra-utérin. Le poids du placenta représente le 1/5 à 1/6 du
poids fœtal. Ce rapport qui est appelé INDEX PLACENTAIRE peut atteindre les valeurs de
1/3 à 1/2 dans certaines pathologies comme la syphilis, l'érythroblastose grave et le diabète de
classe avancée).
La forme du placenta est discoïde. Sa face maternelle ne doit suggérer ni arrachements
tissulaires (= suspicion de rétention de cotylédon, justiciable d'une révision de la cavité
utérine), ni caillots sanguins (= hématomes), mais peut présenter des calcifications parfois sous
forme de larges plages (= suspect et non preuve de pathologie).
Le cordon ombilical mesure en moyenne 50 à 70 cm et doit être dépourvu de nœuds; il doit
comprendre trois vaisseaux (une veine et deux artères). Son insertion est généralement centrale
ou paracentrale, mais être franchement marginale (sur le bord = insertion en raquette = risque
de désinsertion vasculaire si traction intempestive lors de la délivrance), ou tout simplement
vélamenteuse (les vaisseaux funiculaires qui cheminent à travers membranes pouvant même se
positionner entre l'orifice interne du col et la présentation fœtale = VASA PRAEVIA).
L'état des membranes fœtales est intéressant à examiner tant pour le niveau de leur rupture
(bord le plus près du placenta ou PETIT COTE DES MEMBRANES < 10 cm = placenta
prævia), leur odeur (nauséabonde en cas de chorioamniotite), leur coloration (brun verdâtre en
cas de méconium), que pour la possibilité de découvrir des structures inhabituelles (cotylédons
aberrants, nodosités, kystes, etc.).
d) L’examen du périnée
Il constitue un autre temps important de la délivrance. Il permet de découvrir : soit qu’il est
resté intact ; soit qu’il porte des éraillures ; soit que ce sont des véritables déchirures. Il s’agit
alors des déchirures du 1er degré ou D1 (intéressant seulement les muqueuses), ou du 2ème
degré ou D2 (touchant aussi les plans musculaires), ou du 3ème degré ou D3 dont la D3 non
compliquée (atteignant la marge anale sans toucher le sphincter), ou encore D3 compliquée
(avec atteinte du sphincter).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
65
I.10. LES PRESENTATIONS
1. Définition
La présentation est la partie du fœtus qui occupe l’aire du détroit supérieur pour s’y engager et
évoluer ensuite suivant un mécanisme qui lui est propre.
2. Types de présentation
Le fœtus peut se présenter par :
- La tête : c’est la présentation céphalique
- Les fesses : c’est la présentation du siège
- Lorsqu’il se trouve en travers, c’est le tronc qui occupe l’aire du détroit supérieur (D.S),
quoique l’accouchement soit impossible si le fœtus est à terme, l’usage prévaut de
décrire la présentation de l’épaule alors qu’il s’agit plutôt d’une position transversale
ou oblique.
A. Présentation Céphalique
Elles sont les plus fréquentes (96 %). Mais il ne suffit pas qu’il se présente par la tête pour que
l’accouchement se réalise, encore faut-il que la tête fasse coïncider ses diamètres avec ceux du
bassin maternel.
La présentation de la tête fléchie est la présentation du SOMMET ; celle de la tête défléchie
(en extension) est la présentation de la FACE. Lorsque la tête reste en position intermédiaire
entre la flexion et la déflexion, c’est la présentation du FRONT.
a) Présentation du sommet
Définitions
C’est la présentation de la tête fléchie de sorte que la partie de la tête qui descend la première,
en même temps qui sert de repère pour la désignation de la variété de position est l’OCCIPUT.
Variétés de position
Lorsque le bassin est normal, le grand axe de la tête fléchie s’oriente toujours suivant l’un de
deux diamètres du bassin ; le gauche beaucoup plus souvent emprunté apparaît comme le
diamètre oblique normal de l’engagement. Suivant que l’occiput se trouve en avant vers
l’éminence iléo-pectinée ou en arrière vers le sinus sacro-iliaque.
Quatre variétés de position sont possibles :
Occipito-iliaque gauche antérieur (OIGA) et Occipito-iliaque droite postérieur (OIDP)
qui correspondent au diamètre oblique gauche du bassin.
Occipito-iliaque gauche postérieur (OIGP) et Occipito-iliaque droite antérieur (OIDA)
très rare et qui correspondent au diamètre oblique droit du bassin.
Ces 4 positions sont celles de l’engagement de la tête, les positions en occipito-iliaque gauche
ou droite transverse (OIGT ou OIDT) ne sont des positions d’engagement que dans certaines
formes du bassin (bassins plats), si non elles constituent des situations de malposition fœtale.
L’accouchement le plus eutocique est l’accouchement en présentation de sommet en OIGA.
b) Présentation de la face : a comme repère le menton.
c) Présentation du front : a comme repère le nez.
B. Présentation du siège : a comme repère le sacrum
C. Présentation transversale : a comme repère l’épaule.
NB : le déroulement de l’accouchement dans les présentations de la face, du front, du siège
ainsi que la présentation transversale sera décrit dans d’autres cours.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
66
I.11. ACCUEIL DU NOUVEAU-NE NORMAL ET ANORMAL
1) Exigences de la vie aérienne
Pour que la respiration s'installe de façon cyclique, il faut les conditions "sine qua non"
suivantes:
- intégrité, au niveau du cerveau, des centres respiratoires supérieurs (= bulbaires); cette
intégrité est d'autant plus acquise que le cerveau aura été très bien oxygéné durant la vie
fœtale et les premiers instants de la vie extra-utérine;
- maturité histologique pulmonaire;
- développement suffisant des muscles respiratoires, principalement inspirateurs;
- réserves énergétiques suffisantes sous forme de glycogène;
- liberté des voies respiratoires.
Dès son expulsion, le nouveau-né doit respirer. La première respiration fait dilater les alvéoles,
ce qui, avec la contraction diaphragmatique, déclenche une douleur qui fait que l'enfant crie
spontanément. L'absence de ce cri signifie qu'une réanimation immédiate est nécessaire.
2) Accueil du nouveau-né ayant bien crie spontanément (nouveau-né normal)
- la désobstruction des voies aériennes supérieures;
- la protection thermique;
- appréciation de l'état général du nouveau-né à travers 5 critères de cotation qui définissent
L'indice d'APGAR (nom de son auteur); c'est une cotation (à la 1ère, 5ème, et 10ème minute)
où chacun des 5 éléments (battements cardiaques - cri - coloration – réflexe à l’irritation
nasale - tonus) est noté de 0 à 2; le maximum = 10, le score étant estimé déprimé si < 7;
- ligature du moignon du cordon au moyen d'un fil stérile à ± 2 cm de la gaine ombilicale,
puis section de raccourcissement, suivi de la désinfection puis pansement stérile;
- soins des yeux (nitrate d'argent ou collyre aux AB (ex. chloramphénicol 0,5 %) ; ce geste
est aussi appelé CREDE;
- pesée et mensurations de la taille et du périmètre céphalique (crânien);
- vérification de l'état du nouveau-né, à la recherche des réflexes archaïques et d'éventuelles
malformations congénitales;
- mise en place du bracelet d'identité de l'enfant.
3) Accueil du nouveau-né sans cri ou avec cri faible
Lorsque le cri de l'enfant n'est pas obtenu ou ne l'est que très faiblement, l'indice d'APGAR est
inférieur à 7, et il y a DETRESSE NEONATALE qui nécessite une REANIMATION
NEONATALE. La réanimation néonatale peut donc être parfaitement prévisible dans les cas
de certaines pathologies maternelles ou fœtales connues, ou de certains types d'accouchement.
Le diagnostic de détresse respiratoire peut prêter à confusion. La cotation de l'indice (score)
d'APGAR permet de le faire de façon plus ou moins objective.
Tableau: Cotation de l'indice (score) d'APGAR (1958)
Cote Cœur Respiratoire=cri Tonus Coloration Irritation nasale Total
0 nul = 0 absent = 0 flasque= 0 Pâleur/cyanose= 0 sans réaction=0 0
1 Rythme<100= 1 faible = 1 membres fléchis=1 acrocyanose=1 grimace=1 5
2 >100 = 2 vigoureux=2 actif=2 rosée = 2 toux/éternuement=2 10
Il existe d'autres procédés d'évaluation comme celle de Silverman.
Les formes de DETRESSE RESPIRATOIRE sont:
- la maladie des membranes hyalines;
- l'inhalation amniotique résultant en une espèce de plâtrage des voies aériennes;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
67
- le pneumothorax;
- les situations diverses comme celles provoquées par l'infection, les affections neurologiques
et biologiques.
N.B. : Un diagnostic différentiel est à faire avec soit l'APNEE PHYSIOLOGIQUE et le
syndrome d'ENFANT ENDORMI (qu'il faut alors réveiller en le stimulant).
Le nécessaire pour une bonne réanimation doit toujours être prêt: table de réanimation -
chronomètre - aspirateur - sonde d'aspiration - inhalateur d'oxygène avec masque et valve de
sécurité - matériel d'intubation trachéale - appareil de ventilation manuelle adapté au nouveau-
né - matériel de perfusion et cathéter ombilical - médicaments divers tels que le sérum
bicarbonaté à 42 % semi molaire, le sérum glucosé hypertonique à 10-20 % (N.B. 10-20 cc/kg)
, la caféine, la nalorphine, le chlorure de calcium à 10 %, et la vitamine K (forme naturelle = 1
mg/kg, pas la synthétique, ex. Synkavit, qui possède des propriétés hémolysantes).
Le principe de la réanimation se résume en 3 points (=buts): 1) assurer une bonne ventilation -
2) assurer un bon régime cardiaque - 3) assurer un bon équilibre métabolique et un apport
hydro-électrolytique adéquat (= VeMaPe = ventiler + masser le cœur + perfuser).
Apgar 4 – 7 : désobstruer + oxygéner + perfuser.
Apgar < 4 : désobstruer + oxygéner + perfuser + intuber + réanimer.
4) Examen de l'enfant nouveau-né
Il vise à identifier:
- d'éventuelles déformations (ex. bosse séro-sanguine ou CAPUT) ou traumatiques (ex.
CEPHALHEMATOME - fracture surtout des membres supérieurs et du crâne),
- des malformations congénitales, et
- les effets de certaines pathologies gravidiques (ex. desquamation et longueur des ongles en
cas de grossesse prolongée - phlyctènes après épisode fébrile maternel ± prolongé).
A) L'inspection
Elle peut permettre de noter:
- un faciès caractéristique ; une anencéphalie; une microcéphalie; une micrognathie ; une
fente labiale et/ou palatine; une implantation basse des oreilles (Trisomique);
- une déformation thoracique suggestive d'une malformation interne;
- un abdomen avec hépatomégalie, splénomégalie, ou avec OMPHALOCELE; un
LAPAROCHISIS;
- une déformation des membres, ou leur amputation;
- des anomalies des organes génitaux externes;
- une imperforation anale et/ou de méat urinaire;
- le VERNIX CASEOSA, la teinte et les lésions cutanées diverses.
B) La palpation
Elle explore essentiellement les structures suivantes:
- la tête, à la recherche de sutures ou de fontanelles trop larges, de masses
- l'abdomen, pour le foie et la rate;
- les membres, à la recherche de déplacements osseux et de crépitement.
- Le tonus et les réflexes archaïques
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
68
I.12. POST-PARTUM
1. DEFINITION
Le POST-PARTUM est la période qui s'étend à partir de l'accouchement jusqu'à la 6 ème
semaine et au cours de laquelle s'effectue le retour physiologique vers l'état non gravide de
tous les organes ayant subi des modifications gravidiques. Une exception à ce retour : les seins
appelés plutôt à l'optimum de leur développement et de leur fonctionnement.
Elle se termine par le retour des menstruations ou retour des couches, sauf dans les cas
d’aménorrhée physiologique de lactation. A cette époque, l’organisme a retrouvé son équilibre
de non-gravidité et généralement le retour de l’ovulation rend possible une nouvelle grossesse.
Le post-partum est ainsi marqué par 3 types de phénomènes importants: réduction (restitution)
de volume des organes génitaux (= INVOLUTION) - établissement de la lactation ou montée
laiteuse - phénomènes généraux.
Le post-partum a été arbitrairement réparti de la manière suivante:
- post-partum immédiat = les 24 premières heures;
- post-partum précoce = jusqu'au 7e jour;
- post-partum tardif (éloigné) = jusqu'à 6-8 semaines.
2. PHYSIOLOGIE
Au plan général, l'eau accumulée dans le secteur extracellulaire diminue, si bien que durant
les 6 semaines, près de 4 kg vont être ainsi perdus, en grande partie par voie urinaire.
L'augmentation de l'excrétion urinaire + hypotonie résiduelle de l'arbre urinaire ==>
prédisposition à l'infection urinaire. Si œdème dans le post-partum, penser à l'existence ou le
début d'une dysgravidie.
Au plan psychologique, acceptation rôle de mère=>acceptation de l´enfant dans l´état où il
est.
Au plan utérin, le retour de l'utérus aux dimensions d'avant la grossesse s'appelle
INVOLUTION UTERINE. Elle s'effectue à la faveur des contractions utérines. L'involution
utérine est inaugurée par la constitution du globe de sécurité. Elle est rythmée par les
contractions utérines. Elle est localisée à l'hypogastre, mais peut irradier vers la région
lombaire. Dans certains cas, ces contractions sont d'une intensité très fortement ressentie par
l'accouchée. Les douleurs sont alors appelées TRANCHEES UTERINES. Elles correspondent
à des contractions intermittentes et douloureuses de l’utérus. Elles se traduisent par des
coliques utérines survenant les 2 ou 3 premiers jours de suites des couches, s’accompagnant
d’un écoulement sanguin ou d’une expulsion des caillots. Elles sont provoquées et exacerbées
par la tétée.
La réduction du volume utérin suit une certaine vitesse: au 1er jour, le globe utérin est à
l'ombilic; Le 6ème jour, il est à mi-distance entre l’ombilic et la symphyse pubienne. Après le
12ème jour, l’utérus est devenu pelvien. Un ralentissement ou un arrêt net de cette réduction
est dû soit à une mauvaise contractilité utérine, soit à une mauvaise vidange, soit encore à une
infection.
La cicatrisation de la plaie cavitaire est une composante majeure du POST-PARTUM. Elle
est favorisée par les contractions utérines qui rétrécissent aussi bien sa superficie que ses
vaisseaux. Ses sécrétions sont appelées LOCHIES. On entend sous ce nom l’écoulement
vulvaire des suites des couches. Sanglantes pendant les 2 ou 3 premiers jours, formées de sang
non-coagulé, les lochies s’éclaircissent et deviennent séro-sanguinolentes jusqu’au 8ème jour,
séreuses jusque vers le 15ème jour puis tarissent. Elles peuvent sans anomalie se prolonger plus
longtemps. Parfois aux environs du 12ème jour, l’écoulement redevient sanglant pendant 48
heures, c’est le petit retour des couches. L’odeur des lochies est plus ou moins forte suivant les
femmes. Leur abondance a été évaluée à 1400-1500 gr.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
69
Les lochies sont formées par les débris de la caduque, par de petits caillots venant de la plaie
placentaire, par l’exsudation des plaies cervicales et vaginales qui ont pu se produire pendant
l’accouchement. Dans l’utérus, les lochies sont stériles, au moins au début de suites de
couches. Les germes saprophytes ou les germes pathogènes des voies génitales inférieures
peuvent les infecter. En cas d'infection, elles deviennent purulentes.
La ré-fermeture du col utérin accompagne tout naturellement les contractions utérines. Si le
col n'a pas été ouvert avant l'accouchement, il ne s'ouvre pas davantage après l'accouchement.
De béant, flasque et congestionné qu’il était au début, régresse vite. Ses parois deviennent
fermes, épaisses et sa longueur diminue. L’orifice interne n’est plus perméable vers le 2ème
jour, l’orifice externe se referme plus lentement vers le 20ème jour.
Le sein : pendant la grossesse, les glandes mammaires sont le siège d’une prolifération active
qui se traduit par une augmentation de volume des seins et la sécrétion du colostrum. Pendant
les 2 ou 3 premiers jours des suites des couches, la sécrétion de colostrum augmente pour faire
place vers le 3ème jour à la MONTEE LAITEUSE. Sous ce nom, on désigne l’établissement de
la sécrétion lactée qui, à cette phase initiale, s’accompagne des phénomènes locaux et
généraux. Les seins deviennent turgescents, fermes, parfois durs et douloureux. Les veines
sous-cutanées forment un lacis bleuté. Au palper, le doigt perçoit le contour des lobules
mammaires et souvent le prolongement axillaire de la glande qui sous la forme d’un lobe
allongé et sensible, monte vers le creux axillaire. La pression du sein fait sourdre quelques
gouttes d’un liquide blanc-verdâtre : le lait.
Céphalées, malaises, bouffées de chaleur, soif, accélération de pouls, petite augmentation
thermique sont des signes généraux assez banals. La montée laiteuse dure de 24 à 48 heures.
Elle n’est qu’un phénomène préparatoire à la sécrétion lactée qui fait cesser les phénomènes
congestifs.
3. SEMIOLOGIE
La sémiologie du POST-PARTUM est dominée par l'hémorragie et les lochies, la douleur et
l'involution utérine, le sein et la lactation, ainsi que les plaies périnéales ou abdominales
éventuelles.
a) la douleur du post-partum : au niveau de l'hypogastre, elle peut signer une infection utérine
pouvant s'étendre aux trompes et au péritoine, une infection urinaire. Etendue latéralement,
cette douleur peut faire suspecter une atteinte ligamentaire du "large" telle qu'observée dans
les ruptures utérines latérales.
La douleur du post-partum, c'est parfois aussi au niveau du sein où elle peut être en rapport
avec une montée laiteuse ou une infection (mastite ou galactophorite).
b) L'hémorragie
Elle est la sécrétion naturelle de la plaie cavitaire, mais elle peut, lorsqu'elle est trop abondante,
signer une lésion du vagin et du périnée, du col utérin, ou de l'utérus même (atonie utérine,
déchirures, rétention placentaire, rupture utérine).
Les caractéristiques des lochies sont : leur couleur, leur quantité et leur odeur :
- trop abondantes==> rétention de débris placentaires, infection de la plaie cavitaire, lésion
utérine; l'anémie qui peut en résulter peut être profonde et nécessiter une transfusion;
- trop minimes==>obstacle cervical à l'écoulement (synéchies?); l'engorgement de l'utérus
par ces lochies qui ne s'éliminent pas (= HEMATOMETRIE) peut se solder par leur
déversement vers l'espace péritonéal;
- l'odeur normale de vieux sang; nauséabondes, elles font penser à une infection.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
70
c) Le sein
Le sein doit faire l'objet d'attention. Certaines anomalies sont parfois rencontrées:
- Lésions mamelonnaires de type crevasses et gerçures (rendant l'allaitement très
douloureux); mycosiques (= insalubres); rétractions (rendant la succion très laborieuse);
- absence de montée laiteuse après 5 jours, ce qui peut être le fait, soit d'une déshydratation
importante, soit d'une malnutrition sévère, soit d'une anémie profonde (ex. après
hémorragie grave), soit encore d'une oestrogénothérapie récente, ou tout simplement d'un
manque de succion; une forte émotion peut également retarder la montée laiteuse;
- défaut de vidange mammaire par obstruction canaliculaire ou alvéolaire, et pouvant
entraîner une mastite ou un abcès (généralement après 5 jours), une galactocèle (simple
dilatation kystique), ou une galactophorite (dilatation kystique infectée).
4. SURVEILLANCE DU POST-PARTUM
a) La température
Il faut prendre la température de l’accouchée deux fois par jour. Une élévation de température
accompagne habituellement la montée laiteuse. Si état fébrile, rechercher une infection de
l'endomètre (streptocoque et escherichia coli), des voies urinaires, des seins, mais aussi du
poumon.
b) La pression artérielle
La prise de la T.A. doit se faire journalièrement. Elle permet d’objectiver une pathologie
hypertensive du post-partum, ou une action iatrogène de certains médicaments comme le
méthergin. Dans ce cas, on fera également attention à la présente/persistance ou non des
œdèmes et ou d’une protéinurie.
c) L’involution utérine et soins locaux
Sa surveillance va de pair avec celle des lochies. Les membres inférieurs seront examinés à la
recherche d’une menace thrombo-embolique. Le lever doit être précoce entre la 12ème et la
24ème heure. Les mouvements au lit sont recommandés. Les soins locaux consistent à soigner
les plaies d’épisiotomie ou des déchirures du périnée.
d) L’alimentation
Elle doit être variée, habituelle, sans excès de quantité. La nourrice a grandement besoin d’eau,
elle augmentera donc la quantité habituelle des liquides sous formes d’eau, de lait, de thé et de
différentes boissons selon le goût individuel.
e) Les rapports sexuels et la contraception
Ils ne devraient être repris qu’après le retour de couches ou à la cessation des lochies. Si
l’accouchée demande à prendre des mesures anticonceptionnelles, certaines préconisent la voie
orale dès le 10ème jour des suites de couches pendant 21 jours sauf en cas d’allaitement, il est
préférable pour une nourrice d’attendre le retour de couches pour prendre la pilule. La
contraception à base de progestérone est la plus indiquée pendant cette période. La pilule
œstroprogestative est à déconseiller à cause du risque élevé de maladies thromboemboliques.
Entre temps, les préservatifs masculins ou féminins peuvent être utilisés.
5. CONSULTATIONS POST-NATALES
Entre le 6ème et la 8ème semaine qui suivent l’accouchement, le médecin fait l’examen postnatal
obligatoire. Par l’interrogatoire, il s’informe de la date et de la durée du retour de couches ou
s’il n’a pas eu lieu, s’enquiert des caractères de l’écoulement utérin lorsqu’il se prolonge de
façon excessive. On vérifie chez la nourrice la bonne marche d’allaitement. L’examen au
spéculum et le T.V. permettent de vérifier les organes génitaux. C’est pendant ces
consultations qu’on peut parler aussi de contraceptifs. La consultation postnatale est aussi
importante que prénatale. La majorité des femmes ne respectent pas cette consultation.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
71
I.13. LACTATION ET ALLAITEMENT
a)LA LACTATION ET ALLAITEMENT
Rappels sur l’anatomie du sein et la mammogénèse
1. Lactopoïèse
La Lactopoïèse ou synthèse des protéines et autres composants du lait (correspondant à la
montée laiteuse) a lieu lorsque l'inhibition due aux stéroïdes (surtout la progestérone) et au
HPL est supprimée, ce qui permet l'action de la PROLACTINE qui est d'initier la synthèse
intracellulaire d'ARN.
Au cours de la grossesse, la classique MONTEE LAITEUSE qu'on observe au 3 ème ou 4ème
jour du POST-PARTUM ne peut donc avoir lieu du fait de ce blocage de l'activité de la
prolactine sur la glande.
2. Galactopoïèse
La Galactopoïèse est l'entretien de la lactation et la vidange de la glande. Elle se fait d'abord
sous l'influence de la prolactine et des hormones post-hypophysaires (ADH et OXYTOCINE).
Elle se poursuit ensuite grâce à la succion par le bébé (ou un tire-lait) qui déclenche (via
REFLEXE NEURO-HORMONAL) la contraction des cellules myo-épithéliales des canaux
galactophores (.... et la contraction de l'utérus). C'est par ce mécanisme que s'effectue l'éjection
du lait maternel dans la bouche du bébé, et que la sécrétion du lait est auto-entretenue, en
même temps que l'involution utérine est favorisée.
3. Biochimie du lait
La sécrétion du lait est une sécrétion exocrine apocrine, c'est-à-dire qu'elle est libérée avec une
portion (apicale) du cytoplasme de la cellule épithéliale sécrétrice = forme intermédiaire entre
la sécrétion mérocrine comme le pancréas où la sécrétion quitte la cellule sans toucher à
l'intégrité de cette dernière, d'une part, et la sécrétion holocrine comme les glandes sébacées où
c'est la cellule-même sécrétrice qui est éliminée avec le produit qu'elle contient.
La sécrétion du lait s'effectue en suivant 2 étapes importantes:
- l'accumulation in loco (au niveau de la glande-même) des matériaux nécessaires à la
constitution de la sécrétion;
- la sécrétion proprement dite des composants; graisses (4%), protéines (1,5%), hydrates de
carbone (7%), eau (85%), et autres éléments à l'état de traces (minéraux et vitamines).
4. Régulation de la sécrétion lactée
Pour la régulation de la sécrétion lactée on retiendra les facteurs ci-après :
- apport énergétique;
- apport graisseux: rôle avéré;
- apport vitaminique et minéral: rôle douteux;
- apport hydrique: rôle très avéré ;
- poids du bébé: cfr hargne à la vidange de la glande;
- hormones: rôle démontré de GH, Thyroxine, Corticoïdes, ACTH.
5. Méthodes de blocage ou de prévention
Les méthodes de blocage ou de prévention de la lactation : abstention d'allaitement - bandage
compressif sur les deux seins - compresses froides ou camphrées -restriction des liquides - aux
diurétiques (si engorgement mammaire important) - les hormones (œstrogènes seuls -
androgènes seuls - œstrogènes associés aux androgènes - oestro-progestatifs) - les alcaloïdes de
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
72
l'ergot de seigle (BROMOCRYPTINE ou PARLODEL, à action dopaminergique qui inhibe la
prolactine).
b) INFLUENCES DE LA LACTATION SUR L'AXE HYPOTHALAMO-OVARIEN
1. Dans le post-partum (PP) immédiat et précoce (jusqu'à 1 semaine)
Les taux sanguins des hormones du cycle menstruel se trouvent à des niveaux défavorables
pour permettre la sélection d'un follicule destiné à l'ovulation. Les follicules dont le diamètre
est inférieur à 10 mm (tels que présents dans l'ovaire de l'accouchée) ont en effet une granulosa
réfractaire à l'action stéroïdogénétique de la FSH. On a donc:
- des taux bas d’œstradiol jusqu'à 3-4 semaines si pas d'allaitement, et jusqu'à 3-6 mois si
allaitement;
- des taux peu détectables de FSH et LH, mais qui remontent aux niveaux cycliques entre 2è
et 3è semaines PP, que la femme allaite ou pas;
- des taux résiduels de HCG (du fait de sa longue demi-vie) qui contribue à augmenter le
rapport LH/FSH, produisant ainsi une situation apparentée à celle de l'ovaire polykystique;
- des taux de PRL restant élevés jusqu'à la 2è semaine où ils amorcent une chute progressive
durant près de 2-3 semaines si pas d'allaitement (les taux élevés persistent si allaitement).
2. Dans le PP éloigné
- Si le nombre de tétées/jour est supérieur ou égal à 3, la décharge de PRL qu'elles
provoquent est si importante à chaque succion que les taux sanguins ne retournent à la
normale qu'en 6 mois.
- La PRL n'est cependant pas le principal facteur de l'anovulation par son action frénatrice sur
la FSH et la LH, puisque la première ovulation peut être détectée au 33è jour PP; on pense
que le retour au cycle fait intervenir un phénomène de "seuil pondéral critique comme celui
décrit pour la puberté (d'où le rôle de la suralimentation dans la précocité du retour des
couches).
- La lactation stimule la sécrétion de la Prolactine par le lobe antérieur de l'hypophyse;
- La Prolactine inhibe la sécrétion FSH et LH, ce qui résulte en un effondrement des taux
d'œstrogènes.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
73
IIème Partie : PATHOLOGIES GRAVIDIQUES
II.1. LES PETITS MAUX DE LA GROSSESSE
1. Nausées et vomissements
- Apparaissent en début de grossesse
- Dés 5 SA jusqu'à 14 SA
- Le plus souvent le matin
- Etat général conservé avec absence de prise de poids voir amaigrissement
- Examen clinique normal: surveiller le poids
- Si très importants rechercher une grossesse gémellaire ou une grossesse molaire.
Le traitement:
Rassurer la gestante, lui conseiller de se lever lentement et de fractionner les repas
Antiémétique 30mn avant les repas (per os ou voie rectale)
Si perte de poids supérieure à 10% ou égale à 5 kg prévoir une hospitalisation pour une prise
en charge psychologique avec réanimation et sédatifs.
La cause n'et pas connue: hypothèse de l'élévation des gonadotrophines chorioniques (+
fréquente si grossesse multiple ou molaire).
2. Le Reflux gastro-œsophagien
- Pyrosis : signe du lacet, décubitus dorsal +++
- Régurgitations
- Rarement hématémèse, dysphagie, anémie.
- Pas d'examen complémentaire systématique (fibroscopie si œsophagite patente)
Conduite à tenir?
- Les postures ; position verticale après les repas, surélévation de la tête de lit
- Eviter les mets épicés ou en sauce, le café, le thé les assaisonnements vinaigrés les boissons
gazeuses et surtout tabac et alcool +++
- Traitement médicamenteux avec Antiémétique 15 mn avant les repas et anti- acides, les anti
H2 sont efficaces, Ranitidine possible en cas de nécessité.
3. La constipation
- Pas de Bilan, sur le plan clinique un TR pour rechercher une constipation terminale.
- Conseils alimentaires : boire beaucoup, régime riche en fibre (légumes verts,fruits)
- Marche quotidienne 30 à 45 mn
- Se présenter à la selle à horaire régulier
- Eviter les laxatifs, les mucilages (risque de ballonnements), les huiles (une malabsorption
des vitamines), préférer le son et les fibres.
4. Les lombalgies
Elles représentent la première cause de douleur chez la femme enceinte et sont très fréquentes.
Elles sont bénignes mais entraînent une gêne fonctionnelle parfois importante nécessitant un
arrêt de travail.
Trois phénomènes sont imputés :
- le relâchement ligamentaire précoce,
- l’hyper lordose entraînée par l’augmentation du volume de l’utérus et
- la prise de poids.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
74
Les lombalgies apparaissent dès le deuxième trimestre de la grossesse pour disparaître après
l’accouchement.
Le diagnostic repose sur la plainte exprimée par la patiente et doit être complété par un examen
clinique minutieux afin d’exclure une autre pathologie.
Les examens complémentaires comme la radiographie, l’IRM sont contre-indiqués, il faut en
mesurer le bénéfice escompté avant de les prescrire.
Les moyens thérapeutiques sont les antalgiques (paracétamol), recommander des attitudes
posturales correctes afin de les prévenir. On retiendra les techniques physiques comme la
kinésithérapie, l’ostéopathie, l’acupuncture, et le port d’une ceinture lombaire, qui semble
réduire la douleur de façon significative.
5. Les crampes
Ce sont des contractions douloureuses localisées au niveau des mollets, d’apparition nocturne.
C’est la combinaison de deux minéraux, synergiques et antagonistes qui semble responsable de
ces troubles. La supplémentation en magnésium durant 3 mois semble efficace, une diminution
des crampes est observée.
6. Le syndrome douloureux des symphyses ou syndrome de lacomme
Ce syndrome douloureux ostéo-articulaire très fréquent, très douloureux, apparaît plus
particulièrement au cours des derniers mois de la grossesse. La patiente décrit une difficulté à
la marche, aux changements posturaux (debout/couché) et a l’impression que la présentation
fœtale est très basse, générant une sensation de pesanteur pelvienne permanente. Cette douleur
démarre du pubis mais peut irradier en avant vers les fosses iliaques, le périnée ou en arrière
vers les fesses, les fosses lombaires. Une des étiologies retenues serait due en partie à la
pression de la tête fœtale sur la symphyse pubienne dont les ligaments sont relâchés. La
relaxine hormone secrétée dés le début de la grossesse par le corps jaune voit sa production
maximale au troisième trimestre. Associée à l’action des œstrogènes elle joue un rôle non
négligeable sur les tissus conjonctifs des systèmes ligamentaires, pelviens et rachidiens.
Le traitement est essentiellement basé sur le repos strict. Les traitements médicamenteux à
l’exception du paracétamol et de l’acide uridine 5’hiphosphonique, n’ont pas démontré leur
intérêt thérapeutique.
7. Les œdèmes
Ils apparaissent au dernier trimestre et sont la conséquence d’une rétention hydrosodée et
d’une augmentation de la perméabilité capillaire.
On conseille:
- Marche quotidienne
- Surélévations des membres inférieurs la nuit
- Eviter les expositions au source de chaleur (voiture, radiateur d'appoint) et les bains
chauds prolongés.
Chaussettes ou bas de contention peuvent soulager mais n'empêche pas l'apparition de
varices (grade A) + + +
8. Les hémorroïdes
Prévention de la constipation
Même conseils que les œdèmes pour l'activité physique
Conseils alimentaires avec arrêt des épices.
Veinotoniques si besoin (grade C).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
75
II.2. PLACENTA PRÆVIA
A. DEFINITION
Le placenta prævia est l’insertion basse et vicieuse du placenta sur le segment inférieur en
totalité ou en partie, cette insertion étant source d'accidents hémorragiques. Normalement le
placenta s'insère sur l'une des faces et/ou le fond du corps de l'utérus. Le segment inférieur se
forme au 3ème trimestre de la grossesse. Il mesure 10 cm environ. De nombreux auteurs ne
retiennent comme placenta prævia qu'un placenta inséré en totalité ou en partie sur le segment
inférieur et entraînant des accidents hémorragiques, réservant le terme de placenta " bas
inséré " aux formes non hémorragiques, beaucoup plus fréquentes.
B. FACTEURS FAVORISANTS
multiparité ;
curetage et toutes les manœuvres endo-utérines ;
cicatrices utérines (myomectomie, cure de synéchie, césarienne, séquelle d'endométrite)
antécédents de placenta prævia ;
gémellité : placenta volumineux, très étalé, débordant sur le segment inférieur ;
fibromyomes sous-muqueux, des malformations utérines.
C. CLASSIFICATION
Classifications anatomiques : selon le rapport du placenta à l'orifice interne du col utérin :
- Placenta prævia latérale : le placenta est inséré sur le segment inférieur sans atteindre
l'orifice interne du col utérin, donc il reste à distance de cette orifice ;
- Placenta prævia marginale : le placenta est inséré sur le segment inférieur et son bord
approche sans recouvrir l'orifice interne du col utérin.
- Placenta prævia recouvrant partiel : le placenta recouvre partiellement l'orifice interne
du col utérin et à dilatation complète il ne recouvre qu'une partie de l'aire de la dilatation
cervicale.
- Placenta prævia recouvrant total ou centrale : le placenta recouvre complètement
l'orifice interne du col utérin et à dilatation complète du col utérin il recouvre la totalité
de l'aire de la dilatation cervicale.
Classification échographique d'après (BESSIS R, BRIGNON C, SCHNEIDER L. 1976)
Les placentas bas insérés antérieurs :
o de type I : la limite inférieur du placenta atteint le tiers supérieur de la vessie ;
o de type II : la limite inférieure atteint les deux tiers supérieurs de la vessie ;
o de type III : la limite inférieure atteint le col utérin ;
o de type IV : la limite inférieure dépasse le col utérin, c'est-à-dire atteint la face
postérieure de l'utérus
Les placentas bas insérés postérieurs :
o de type I : la limite inférieure de placenta se situe à moins de 4 cm en arrière du
col de l'utérus ;
o de type II : la limite inférieure du placenta atteint le col utérin,
o de type III : la limite inférieure du placenta atteint le tiers inférieur de la vessie
o de type IV : la limite inférieure du placenta recouvre totalement le dôme vésical.
Les placentas de type I et II correspondent aux placentas prævia latéraux.
Les placentas de type III correspondent aux placentas prævia marginaux.
Les placentas de type IV correspondent aux placentas prævia recouvrant.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
76
Placenta Prævia latéral (type I) : le bord Placenta Prævia marginal (type II): le bord
inférieur est loin de l’orifice interne inférieur atteint l’orifice interne
Placenta Prævia recouvrant partiel (type III) : Placenta Prævia recouvrant total (type
le bord inférieur recouvre partiellement IV) : le placenta recouvre totalement l’aire
l’orifice interne à 3 cm de dilatation de dilatation
D. MECANISME DES HEMORRAGIES DU PLACENTA PRÆVIA
- pour les variétés périphériques (latérales et marginales), les contractions physiologiques
de Braxton Hicks entraînent le décollement d'une languette placentaire, ouvrant ainsi les
sinus utérins qui saignent ;
- pour les formes recouvrantes, il s'agit plutôt d'un clivage entre le placenta et l'utérus dû à
la formation du segment inférieur au 3ème trimestre et à la dilatation progressive du col
pendant le travail.
- L'hémorragie fœtale est possible et assez fréquente : en effet, au cours du décollement
d'un bord placentaire, des villosités peuvent se déchirer, entraînant une hémorragie fœtale,
avec passage d'hématies fœtales non seulement dans le sang des pertes vaginales, mais aussi
dans la circulation maternelle, d'où deux conséquences possibles :
immunisation en cas d'incompatibilité Rhésus ;
et anémie fœtale rendant le fœtus beaucoup plus sensible à l'hypoxie.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
77
E. DIAGNOSTIC:
Plaintes:
Hémorragie indolore faite de sang rouge vif d’abondance variable avec tendance à se répéter
Parfois discrètes douleurs lombaires ou hypogastrique
Examen clinique:
Signes d’anémie et parfois de choc hypovolémique.
Présentation haute ou transversale et on objective parfois des contractions utérines
BCF. normaux ou bradycardes selon l’importance de la spoliation sanguine
Au spéculum: des caillots de sang dans le vagin et une hémorragie active ex-utéro
TV contre indiqué avant écho, sauf au bloc opératoire : sensation matelassée dans l’un des
culs-de-sac vaginaux (si placenta marginal ou recouvrant)
Après l’accouchement, l'examen du placenta et des membranes retrouve un petit côté des
membranes inférieur à 10 cm (taille du segment inférieur) témoignant donc d'un placenta
inséré en partie sur le segment inférieur
F. COMPLICATIONS
Procidence du cordon : après rupture spontanée ou artificielle des membranes, elle est
favorisée par une insertion excentrée, déclive ou vélamenteuse ;
Placenta accreta : adhérence anormale du placenta au myomètre due à l'absence partielle ou
complète de plaque basale. Elle est favorisée par la multiparité, les césariennes et curetages
antérieurs, les synéchies ; il peut se compliquer d'hémorragie massive, de CIVD, de rupture
du segment inférieur provoquée par la délivrance artificielle.
Coagulopathie de consommation (CIVD).
Anémie, choc hypovolémique, décès maternel
FSA et MIU
G. DIAGNOSTIC DIFFERENTIEL
a) Hémorragies d'origine cervico-vaginale ou vulvaire : ectropion, polype du col,
dysplasie et cancer du col.
b) Hémorragies d'origine endo-utérine au 3eme trimestre et au cours du travail
Rupture utérine :
- douleur très intense, pouvant être moins intense si rupture sur cicatrice utérine ;
- collapsus qui n'est pas expliqué par l'hémorragie externe modérée ;
- fœtus mort le plus souvent.
Hématome rétro-placentaire :
- Toxémie ou notion de traumatisme ; - mort fœtale parfois ;
- contracture utérine douloureuse ; - oligurie avec protéinurie ;
- métrorragies noirâtres peu abondantes ; - Coagulopathie de consommation (CIVD).
- état de choc ;
Hématome décidual marginal ou rupture de sinus marginal, avec hémorragie moins
importante, de bon pronostic materno-fœtal.
Hémorragie de Benkiser
Déchirure d'un vaisseau du cordon dont l'insertion est vélamenteuse, avec souffrance fœtale
aiguë et liquide amniotique sanglant
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
78
H. PRISE EN CHARGE :
Elle sera fonction de l’âge de la grossesse, du degré de dilatation du col, de la présentation, de
l’état du fœtus et surtout de l’importance de l’hémorragie
1) Hémorragie peu abondante
Hospitalisation : Repos strict et surveillance pouls, TA, hémorragie génitale et BCF
Bilan rapide : Hb, Ht, Gs + Rh (si non connu ou douteux)
Transfusion selon l’importance de l’anémie
Tocolyse si grossesse jeune (Spasfon, Salbutamol* sauf si près du terme)
Échographie pour vitalité fœtale et déterminer le type de placentation.
Si placenta latéral et grossesse jeune, hospitalisation jusqu’à l’arrêt de l’hémorragie, et
sortir avec RDV dans 2 à 4 semaines pour contrôle migration placentaire à l’échographie.
Si grossesse à terme et en travail, faire une rupture des membranes si la dilatation le
permet, si l’hémorragie s’arrêtait, on pourrait espérer un accouchement par voie basse. Si
par contre l’hémorragie ne s’arrêtait pas, pratiquer une césarienne urgente. Si la patiente
n’est pas en travail, attendre l’entrée spontanée en travail et procéder comme ci-dessus
Si placenta recouvrant : césarienne élective à 37-38 semaine ou plus tôt si l’hémorragie.
En l’absence d’échographie, si l’hémorragie s’arrête, attendre l’entrée spontanée en travail
et faire un TV en salle d’opération en présence de toute l’équipe opératoire prête.
Si placenta latéral, faire rupture des membranes et surveiller le travail comme
d’habitude. En cas d’hémorragie persistante, pratiquer une césarienne. Mais si
l’hémorragie ne se répète pas, espérer un accouchement par voie basse, sauf si SFA.
Si placenta recouvrant et grossesse à terme, pratiquer une césarienne d’emblée.
Césarienne d’emblé si membranes inaccessibles, Présentation transversale, Obstacle
prævia, Présentation siège, Grossesse précieuse, Utérus cicatriciel
2°) Si hémorragie génitale abondante:
Abord veineux en urgence avec 1l SP 0,9 % en attendant la transfusion.
prélèvement de sang pour le GS + Rh (si non connu), l’Ht et l’Hb.
Transfusion dès que possible du sang iso-groupe iso-rhésus frais
Echographie si possible pour vitalité fœtale, estimation du poids fœtal et placentation
TV en salle d’opération : si membranes accessibles, faire la RAPE pour minimiser les
pertes sanguines et pratiquer une césarienne urgente quel que soient l’âge de la
grossesse ou l’état du fœtus. Dans certains cas (arrêt hémorragie, fœtus mort ou non
viable, dilatation avancée, présentation céphalique de sommet), tenter un accouchement
par voie basse tout en étant prêt à pratiquer une césarienne urgente si hémorragie
importante menaçant la vie de la mère. Entre-temps on s’emploiera à corriger l’anémie.
Réanimation NN, prélever sang cordon pour GS+Rh, Hb, Ht, et transfuser si nécessaire.
- En post-partum:
Prévenir HPP par une perfusion ocytocine (20 UI + 1l SG 5 %).
Si hémorragie incoercible, pratiquer une hystérectomie d’hémostase.
Corriger l’anémie: transfusion ou traitement martial selon l’importance de l’anémie
Antibiothérapie + utérotoniques (Méthergin* ou Ergométrine*)
Surveiller pouls, TA, hémorragie génitale, globe de sécurité
recommander à l’accouchée un lever précoce pour prévenir les thromboembolies
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
79
II.3. HEMATOME RETRO-PLACENTAIRE
a. DEFINITION
Amas du sang entre le placenta et l'utérus dû à un décollement précoce, plus ou moins étendu,
du placenta au cours de la grossesse. Il s'agit d'une pathologie paroxystique des derniers mois
de la grossesse et du travail. Synonyme : Décollement prématuré du placenta normalement
inséré (DPPNI)
b. PHYSIOPATHOLOGIE
Décollement prématurément du placenta c'est-à-dire avant la naissance de l'enfant. Ce
décollement va entraîner la constitution d'une hémorragie qui ne va pas s'extérioriser le plus
souvent, s'épanchant entre placenta et utérus. Il se constitue donc un hématome dans l'espace
ainsi créé :
- le retentissement fœtal : la partie décollé du placenta ne participe plus aux échanges
fœto-maternels, il en résulte une hypoxie (diminution de l'oxygène) fœtale aiguë qui peut
être à l'origine d'une souffrance aiguë du fœtus pouvant conduire à la MIU ;
- le retentissement maternel pourra être dû à l'importance de l'hémorragie, mais surtout
aux troubles de la coagulation qui pourront survenir. En effet, l'ouverture de l'hématome
va entraîner le passage de thromboplastines placentaires dans la circulation maternelle,
responsables de CIVD, éventuellement associé à une fibrinolyse.
c. FACTEURS DE RISQUE :
- Hypertension gravidique ;
- Traumatismes : violent (ATR, chute) ou minime (version par manœuvres externes) ;
- Autres facteurs de risque plus accessoires : tabagisme, terme dépassé ;
d. CONSEQUENCES
Les complications vont se manifester chez le fœtus et chez la mère :
Chez le fœtus, la diminution des échanges → SFA → MIU ;
chez la mère : anémie, choc, troubles de la crase sanguine, nécrose de l'utérus (apoplexie
utéro-placentaire ou syndrome de couvelaire), mort maternelle.
e. DIAGNOSTIC
1. Forme frustre:
Douleurs abdominales modérées avec hypertonie utérine discrète se traduisant par un
mauvais relâchement utérin entre les CU.
Hémorragie génitale modérée ou absente
BCF souvent présents et normaux
2. Forme grave:
Douleurs abdominales en coup de poignard, de survenue brutale
Hémorragie génitale d’abondance variable faite de sang noirâtre
Signes d’anémie: tachycardie, pâleur conjonctivo-muqueuse, polypnée...
Signes de choc: soif intense, agitation, sudation profuse, collapsus cardio-vasculaire
Contracture utérine (utérus de bois) avec hypertonie de base
parfois la hauteur utérine augmente à chaque examen, témoin d’une hémorragie interne
Les BCF sont souvent absents sinon perturbés (bradycardie)
Au spéculum, hémorragie ex-utéro
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
80
Paraclinique : Echographie
Elle permet la recherche de la vitalité fœtale par la localisation de l'aire cardiaque.
Elle confirme le diagnostic, faisant le diagnostic différentiel avec le placenta prævia et
appréciant le volume approximatif de l'hématome rétro-placentaire dont l’image
caractéristique est une zone linéaire ou biconcave, bien limitée, vide d'écho.
Elle permet d'apporter également des précisions sur la taille du fœtus, sa présentation,
particulièrement difficiles à évaluer cliniquement en cas d'hypertonie utérine.
DPPNI sur placenta DPPNI sur placenta latéral
fundique avec hémorragie avec hémorragie extériorisée
interne
f. DIAGNOSTIC DIFFERENTIEL
Cfr placenta prævia.
g. PRISE E N CHARGE
Les gestes à poser devront être rapides et coordonnés, sans précipitation:
- Abord veineux en urgence avec 1l SP 0,9% en attendant la transfusion.
- Prélever le sang pour Hb, Ht, GS + Rh (si non connu), TS et TC, fibrinogène
- Obtenir rapidement du sang frais, du fibrinogène ou du plasma frais congelé afin
- Sonde vésicale à demeure pour évaluer la diurèse et prélever les urines pour albuminurie
- Evaluer les CU, la dilatation, l’état fœtal (BC.)
Si BCF présents, césarienne urgente sauf si fœtus non viable ou si dilatation très avancée
avec accouchement imminent. Si BCF absents : envisager l’accouchement par voie basse
Si col dilaté, RAPE pour diminuer la surdistention utérine et le passage vasculaire de la
thromboplastine
donner 10 mg Morphine ou 100 mg Péthidine en S/C pour calmer douleur et réduire
spasme utérin
placer un Théobald si le travail ne se déclenche pas spontanément ou en cas de dystocie
dynamique. Si la dilatation progresse rapidement, laisser évoluer le travail jusqu’à
l’accouchement. Entre-temps surveiller pouls, TA, évolution HU, l’hémorragie génitale
toutes les 15’, TS et TC toutes les 30’. L’intervalle entre début accident et délivrance ne
doit pas dépasser 6 heures, sauf si les paramètres de surveillance restent stables
- Pratiquer césarienne si hémorragie importante menaçant la vie de la mère, travail traînant et
signes vitaux s’altèrent, l’utérus ne répond pas à l’ocytocine
- Au cours de la césarienne, syndrome de Couvelaire (apoplexie utéro-placentaire qui
survient à la suite de la séparation prématurée du placenta. L'hématome formé envahit les
fibres musculaires de l'utérus) : utérotoniques.
- En post-partum:
Prévenir HPP par une perfusion ocytocine (20 UI + 1l SG 5 %). A défaut, massage de
l’utérus ou vessie de glace sur l’abdomen
Si hémorragie incoercible, pratiquer une hystérectomie d’hémostase.
faire bilan de coagulation (fibrinogène, taux de prothrombine, temps de Howell) et rénal
quantifier la diurèse horaire. Si anurie, forcer la diurèse avec le Furosémide (Lasix*,
Lasilix*) après correction des troubles hydro-électrolytiques et de l’anémie.
Antibiothérapie + utérotonique (ocytocine)
Surveiller pouls, TA, hémorragie génitale, globe de sécurité
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
81
III.4. LA RUPTURE UTERINE
a. DEFINITION
Urgence obstétricale définie comme une solution de continuité spontanée (non chirurgicale) du
muscle utérin. Elle peut être spontanée, c'est-à-dire survenir en dehors de toute intervention
obstétricale (sur utérus sain ou sur utérus cicatriciel) ou provoquée par une manœuvre
obstétricale. Elle survient pendant la grossesse ou pendant le travail.
b. Aspects anatomiques
Dans leurs formes cliniques, les ruptures peuvent être simples (corps utérin, segment
inférieur), ou carrément compliquées (s’étendant aux organes voisins comme le dôme vaginal,
la vessie, le col utérin).
Au plan anatomique, selon l’épaisseur de la paroi utérine intéressée, on parle de :
- rupture utérine incomplète, lorsque la musculeuse est atteinte, mais sans la séreuse ; le
péritoine pré-segmentaire est décollé mais reste intact, n’a pas cédé, et le sang épanché n’a
pas franchi la séreuse, d’où constitution d’hématome sous-péritonéal ;
- rupture utérine complète, avec ouverture de la séreuse et possibilité de déversement du
contenu utérin dans la cavité abdominale.
Au plan étio-pathogénique, on distingue deux types: rupture primitive (volontiers complète,
intéressant toutes les tuniques) et rupture secondaire (faisant suite à une cicatrice).
Par rapport au siège, la rupture siège généralement sur le segment inférieur, elle est
transversale ou longitudinale en cas de césarienne corporéale antérieure (fond ou face
antérieure de l'utérus) ou sur un des deux bords utérins (gauche le plus souvent).
c. ÉTIOLOGIES
Pendant la grossesse :
o soit spontanée (antécédents de césarienne corporéale, d'endométriose, de chorio-
carcinome, rarement après myotomie et en cas de malformation utérine)
o soit provoquée (traumatismes abdominaux)
Pendant le travail :
o soit spontanée (disproportion fœto-pelvienne négligée, épaule négligée, multiparité,
grossesse interstitielle, de la corne utérine, utérus malformé, césarienne corporéale
antérieure, myotomie, hystéro-plastie)
o soit provoquée (par VME, VMI, grande extraction, forceps, ocytociques, embryotomie)
d. CLINIQUE
Phase de pré-rupture (rétraction utérine)
- Stagnation du travail.
- Contractions utérines violentes, très rapprochées, avec hypertonie (contractions subintrantes).
- Anomalies de la dilatation du col qui s’œdématie.
- Anxiété et agitation de la parturiente.
- Imminence de rupture marquée par trois signes :
déformation de l’utérus en sablier ; segment inférieur très distendu, étiré ou allongé,
surmonté du corps utérin hypertonique rétracté moulant le fœtus ;
ascension de l’anneau de rétraction (anneau de Bandl- Frommel) séparant le corps utérin
et le segment inférieur ;
tension douloureuse et palpable des ligaments ronds sur les flancs utérins, mais difficile à
constater.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
82
Phase de rupture (survient brusquement)
Signes fonctionnels et généraux
- Douleur abdominale syncopale soudaine en coup de poignard souvent localisée à gauche et
accompagnée de sensation d’écoulement d’eau chaude dans le ventre.
- Etat de choc hémorragique : pouls rapide ou tachycardie ; chute de la tension artérielle ;
pâleur ; pincement des ailes du nez alors que les yeux se cernent ; la respiration devient plus
courte, et les extrémités et le nez se refroidissent.
Signes physiques ou d’examens
- Inspection : soit le ventre normal si le fœtus est encore dans l’utérus. Salie oblongue. Soit le
ventre prend des contours diffus et irréguliers si le fœtus a quitté l’utérus.
- Auscultation : BCF= négatif.
- Palpation : douleur exquise sur le bord utérin rompu ; fœtus sous la peau étalé et superficiel ;
masse ferme, utérus gravide débarrassé du fœtus.
- Toucher vaginal : douleur exquise sur le bord utérin rompu ; perte de sang noirâtre ;
disparition de la présentation, sauf si le fœtus est encore dans l’utérus ; brèche segmentaire
avec ses bords déchiquetés et parfois la sensation désagréable des anses intestinales ;
- Etat de choc.
NB : Il existe des formes insidieuses (à symptomatologie moins significative).
- avant l’accouchement, le fœtus reste in utéro, SFA sans cause apparente ;
- après l’accouchement (désunion d’une ancienne cicatrice de césarienne ou de perforation) :
choc (d’où révision utérine systématique si césarienne antérieure) ;
- ruptures utérines sous-péritonéales : état de choc plus variable, hématome unilatéral du petit
bassin ou de tout le paramètre et peut gagner la fosse iliaque et même la fosse lombaire ;
- ruptures méconnues, déchirures du col remontant vers le SI sans atteinte des vaisseaux.
e. COMPLICATIONS
Sont materno-fœtales :
Maternelles : déchirures cervicales et vaginales, rupture vésicale, mort maternelle par
état de choc ou péritonite puerpérale
Fœtales : mortalité de 0,05%, augmentée en cas de rupture spontanée complète au
moment de la rétraction ou après la rupture
f. CONDUITE A TENIR
Prophylaxie et diagnostic des disproportions fœto-pelviennes, attention aux manœuvres
obstétricales
Abord veineux en urgence avec 1l SP 0,9% en attendant la transfusion.
Prélever le sang pour Hb, Ht, GS + Rh (si non connu), et obtenir rapidement du sang
Sonde vésicale à demeure pour évaluer la diurèse
Si rupture totale, laparotomie pour soit suture simple si rupture non étendue et non
compliquée après parage des berges, soit hystérectomie totale si le col est atteint ou
subtotale après extraction du fœtus et correction du choc.
Si rupture sous-péritonéale ou si amincissement, soit surveillance simple si l'état
maternel est bon. soit laparotomie et suture simple si hémorragie de la délivrance.
Si la découverte de la rupture est faite au moment d'une césarienne, les sutures devront
être de bonne qualité. utérines devant toute hémorragie de la délivrance même minime !
La révision utérine devant un antécédent de cicatrice utérine est actuellement discutée.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
83
II.5. HEMATOME DECIDUAL MARGINAL
Il est dû à un décollement d’une portion périphérique du placenta. Le saignement est
typiquement noirâtre, de faible abondance, correspondant à l’évacuation de l’hématome.
L’examen clinique maternel est normal et il n’y a pas de signe de souffrance fœtale. Le
diagnostic est échographique, en précisant la taille et la localisation de l’hématome. L’aspect
est celui d’une zone hypoéchogène circonscrite, en périphérie du placenta le plus souvent situé
à son pôle inférieur.
Ce décollement de petite taille n’entraîne pas de réelle perturbation des échanges fœto-
maternels. L’hématome décidual marginal est de bon pronostic. La prise en charge repose sur
la mise au repos, une tocolyse est parfois nécessaire. La surveillance rapprochée est
indispensable.
II.6. HEMORRAGIE DE BENCKISER (Rupture d’un sinus marginal vaisseau prævia)
L’hémorragie de Benckiser est une hémorragie fœtale par dilacération d’un vaisseau prævia
lors de la rupture des membranes.
L’existence de ce vaisseau est le plus souvent due à la présence d’un cotylédon accessoire ou à
une insertion vélamenteuse du cordon. Elle est rare : 1 grossesse sur 4 000. Le risque pour le
fœtus est majeur.
Elle survient lors de la rupture spontanée ou artificielle de la poche des eaux. Les métrorragies
sont franches, indolores et de sang rouge. L’état maternel est conservé alors que la souffrance
fœtale est immédiate avec des anomalies sévères du rythme cardiaque fœtal. Elle conduit à
l’extraction fœtale en urgence par césarienne.
L’examen du placenta après la délivrance confirme le diagnostic en retrouvant le vaisseau
rompu.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
84
II.7. HYPERTENSION ARTERIELLE ET GROSSESSE
a. DEFINITION
Une HTA se définit par une pression artérielle systolique (PAS) supérieure ou égale à 140
mmHg et/ou une pression artérielle diastolique (PAD) supérieure ou égale à 90 mmHg, prise
en décubitus latéral gauche après un repos de 30 minutes. Ou une élévation de la PA habituelle
d’au moins 30 mmHg pour la systolique et 20 mmHg pour la diastolique.
La définition des désordres hypertensifs survenant au cours de la grossesse amène à distinguer
plusieurs types d’atteintes :
1) L'HTA gravidique HTA isolée sans protéinurie apparue à partir de la 20ème semaine
d’aménorrhée (SA) en l’absence d’antécédents.
2) L'HTA chronique ou permanente connue avant la grossesse ou apparaissant avant la 20 e
semaine d'aménorrhée et indépendante du rang de la grossesse.
3) La pré-éclampsie ou dysgravidie ou toxémie gravidique ou gestose éclamptogène associant
une à une protéinurie (0,3 g/l ou 0,50 g/24 h) et, de manière inconstante des œdèmes.
4) La pré-éclampsie surajoutée
5) La pré-éclampsie récidivante
b. ÉPIDEMIOLOGIE
Les données permettant de préciser l’incidence et les facteurs de risque de la prééclampsie sont
relativement difficiles à analyser, en raison de l’inhomogénéité des données de la littérature.
Cependant une étude multi-centrique portant sur la population générale en France retrouve une
incidence de 0,6%. En Europe, 10% des grossesses se compliquent de pré-éclampsie, et en
Afrique la fréquence varie de 10 à 13%.
Un certain nombre de facteurs de risque prédisposent à la pré-éclampsie :
1) Facteurs génétiques et familiaux : histoire familiale d’HTA ou de PE, l’antécédent
personnel d’HTA ou de PE
2) Facteurs de risque immunologiques : une maladaptation immunologique, la primiparité, le
changement de partenaire (primipaternité),
3) Facteurs de risque environnementaux : la toxicomanie au sens large du terme, la
consommation d’alcool, les conditions de vie (altitude), le travail stressant
4) Facteurs physiologiques : l’origine ethnique (noires), l’âge maternel ≥ 35 ans
5) Facteurs de risque maternels : les antécédents de dysgravidie, l’obésité, l’insulino –
résistance, les thrombophilies, les affections auto–immunes, l’HTA chronique, les
néphropathies chroniques, les infections urinaires
6) Facteurs de risque liés à la grossesse ou facteurs obstétricaux : intervalle long entre 2
grossesses, grossesses multiples, hydramnios, diabète, les anomalies chromosomiques ou
des malformations fœtales, l’anasarque fœtal, l’infection urinaire et la môle hydatiforme
c. PHYSIOPATHOLOGIE
La toxémie gravidique a pour étio-pathogénie un défaut de placentation, théorie étiologique
qui a battu en brèche toutes les autres jadis évoquées. La grossesse toxémique se caractérise
par une ischémie placentaire responsable d'une altération des cellules de l'endothélium
vasculaire. Ceci a trois conséquences : une sensibilisation accrue des vaisseaux aux substances
vasoconstrictives, une activation de la coagulation et de l'agrégation plaquettaire, et une
altération de la paroi capillaire responsable d'une fuite de liquide et de protéines. Il existe une
augmentation des résistances vasculaires et une hypovolémie relative liée à une redistribution
des liquides vers le secteur interstitiel. C'est donc une maladie générale qui débute dès la
placentation et qui peut atteindre tous les organes maternels et retentir également sur le fœtus.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
85
d. PRISE EN CHARGE
Elle est surtout fonction de l’importance des chiffres tensionnels qui conditionnent le
pronostic.
1. PREECLAMPSIE LEGERE ou MODEREE:
- 140/90 mmHg < TA < 160/100 mmHg
- Œdèmes modérés (+ ou ++) localisés au niveau des malléoles et disparaissant après repos.
- Albuminurie < 0,5 g/ L (+ ou ++)
- Diurèse > 600 ml/ 24 h.
Traitement en ambulatoire sauf si grossesse à terme ou proche du terme (> à 34 semaines)
Repos au lit en décubitus latéral gauche, et surélever jambes lorsque assise.
Régime sans sel déconseillé, sauf cas HTA essentielle ou insuffisance cardiaque associée.
Sédatif pour favoriser le repos : Diazépam
Anti-HTA en monothérapie : Aldomet
CPN rapprochées (1x/par semaine).
Contrôler chaque jour T. à domicile et si augmentation, revoir sans délais le médecin.
Bilan de retentissement materno-fœtal:
Mère : FO, ECG, Echo cardiaque, Rx thorax (après la 34ème SA), urée, créatinine et
surtout l’acide urique, SGOT, SGPT.
Fœtus : NST, Echo, Doppler, OCT, CMFA
Si la TA est contrôlée, on peut envisager un accouchement à terme (37-38ème semaine). Si
par contre la TA continue d’augmenter malgré le traitement, hospitaliser la gestante et
envisager un accouchement dans les meilleurs délais si la maturité pulmonaire est atteinte.
2. PREECLAMPSIE SEVERE:
- TA > 160/100 mmHg
- Œdèmes généralisés (+++ ou ++++)
- Albuminurie massive > 3 à 5 g / 24h (+++ ou ++++)
- Oligurie (diurèse < 500 ml/ 24 h ou 0,5 ml/ kg/ h)
- Parfois, céphalées, sensation de mouche volante, amaurose...
Hospitalisation dans chambre calme, peu éclairée, loin de bruit avec restriction des visites.
Repos au lit en décubitus latéral gauche, et surélever jambes lorsque assise.
Sédatif pour diminuer le stress et favoriser le repos : Diazépam
Anti-HTA en association : Aldomet + Adalat
Si la TA est très élevée, donner un anti-HTA par voie parentérale : Népressol, catapressan.
NB: diurétiques à proscrire sauf en cas de décompensation cardiaque et d’OAP.
Surveillance : TA toutes les 6 heures, conscience, Poids: 1x/sem, fonte des œdèmes,
Diurèse, Albuminurie: 1 x/jour et éventuellement la protéinurie des 24 heures
Etablir une courbe d’évolution de la TA, du Poids et de la diurèse pour juger de l’efficacité
du traitement.
Bilan de retentissement materno-fœtal:
Surveillance fœtale: BCF toutes les 6 heures, HU 1x/sem pour suivre la croissance fœtale,
CMFA, NST, Écho obstétricale (score biophysique de Manning), Doppler, OCT, selon les
moyens dont on dispose.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
86
Si l’évolution fœto-maternelle est favorable, on envisagera l’accouchement vers la 36-37ème
semaines. Si par contre la T.A. est mal contrôlée avec des signes évidents de souffrance fœtale
(N.S.T. non réactif, inversion du flux au Doppler ombilical, score biophysique de Manning <
4, acide urique > 360 µmol/l) on devra interrompre la grossesse dans les 48 heures, le plus
souvent par césarienne.
On devra s’assurer d’une collaboration étroite avec le néonatalogiste pour une bonne prise en
charge du nouveau-né.
En cas d’échec thérapeutique (T.A. très élevée malgré le traitement, F.O. au stade > III), on
décidera d’une interruption de la grossesse pour sauvetage maternel quel que soit l’âge
gestationnel.
Après la délivrance on évitera le Méthergin* ou l’Ergométrine* parce qu’ils entrainent une
élévation de la T.A. aggravant ainsi l’H.T.A (La méthylergométrine possède également une
activité vasoconstrictrice artérielle liée à la stimulation des récepteurs sérotoninergiques et/ou
alpha-adrénergiques). On donnera plutôt l’ocytocine 0,2 U.I. en I.M., ou 10 U.I. en perfusion
dans 500 cc de sérum glucosé à 5 %.
En post-partum, on continuera sans relâche la surveillance de la T.A. et de la conscience, ainsi
que le traitement anti-H.T.A. jusqu’à la normalisation de la T.A.
Une biopsie rénale sera envisagée 6 semaines après l’accouchement pour exclure une
néphropathie éventuelle.
A la prochaine grossesse, en l’absence d’une H.T.A. chronique on prescrira 75 à 100 mg
d’Aspirine Junior*/j p.o. à partir de la 13ème jusqu’à la 35ème semaine afin de prévenir la
récidive.
e. COMPLICATIONS
i. Maternelles
1) L'ECLAMPSIE
2) COMPLICATIONS HEPATIQUES
- HELLP SYNDROME
- STEATOSE HEPATIQUE AIGUË GRAVIDIQUE (SHAG)
- HEMATOME SOUS-CAPSULAIRE DU FOIE (HSC).
3) HEMATOME RETRO PLACENTAIRE
4) L’INSUFFISANCE RENALE
5) OEDEME AIGU DU POUMON (OAP)
6) LES TROUBLES DE COAGULATION : il s’agit d’une décompensation de l’état de
thrombopénie due à la consommation et /ou la destruction par processus micro
angiopathique de la grossesse, cette décompensation se voit quand il y’a un dépassement
des inhibiteurs physiologiques de la coagulation ou par leur défaut dans le cadre d’une
thrombophilie. Ceci est appelé la coagulation intra vasculaire disséminée chronique, qui se
voit la cause et la conséquence d’infarcissement, de nécrose et d’hémorragie au niveau des
différents organes. Elle se manifeste cliniquement par des signes de micro thrombocytose
(cytolyse, HELLP Sd, RCIU, MFIU …) et biologiquement par l’élévation du taux des D
dimères et des PDF. Le stade ultime est la CIVD hémorragique qui peut compliquer un
HRP et/ ou une éclampsie, est caractérisé par la diminution des facteurs de coagulation, du
fibrinogène, des plaquettes, de l’antithrombine, l’apparition des complexes solubles,
l’élévation des complexes thrombines anti thrombine, plasmine anti plasmine, des PDF,
des D dimères. Ces anomalies d’hémostase présentent un phénomène dynamique variable
dans le temps, nécessitant des bilans répétés et rapprochés.
7) LES COMPLICATIONS CARDIAQUES : ischémie myocardique, de nécrose ou de
complications mécaniques (insuffisance ventriculaire gauche) secondaires à la labilité des
chiffres tensionels.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
87
8) LES ACCIDENTS OCULAIRES : les troubles visuels peuvent aller depuis la baisse de
l’acuité visuelle à la cécité totale. Ils sont dus à un œdème rétinien ou à un décollement
rétinien ou des spasmes artériolaires entraînant une ischémie choroïdienne.
ii. Fœtales
1) RETARD DE CROISSANCE INTRA UTERIN
2) MORT FOETAL IN UTERO
3) PREMATURITE
4) DECES PERINATAL ET NEONATAL PRECOCE
f. IMPLICATIONS ANESTHESIQUES
La patiente toxémique sévère est, comme nous venons de l'exposer, hypertendue,
hypovolémique et susceptible de présenter des troubles de coagulation.
L'anesthésiste-réanimateur doit bien connaître cette pathologie car il y est confronté, soit en
pré-partum, soit dans le post-partum : à une éclampsie tardive, un OAP...
Deux situations sont à considérer, l'analgésie pour le travail et l'anesthésie pour césarienne.
1. Analgésie pour le travail
L'analgésie péridurale diminue les phénomènes douloureux et donc la sécrétion de
catécholamines et ses effets délétères sur le plan maternel et fœtal (diminution du flux utéro-
placentaire ; diminution de poussée hypertensive). Elle améliore la sécurité au moment de
l'accouchement et permet d'éviter l'anesthésie générale si une césarienne est décidée au cours
du travail.
L'anesthésiste-réanimateur doit disposer d'un bilan biologique (coagulation) de moins de 2
heures.
Le syndrome cave doit être prévenu systématiquement par un large décubitus latéral gauche.
Le niveau doit être environ D10-ombilic pour assurer une bonne analgésie.
2. Anesthésie pour une césarienne
L'anesthésie loco-régionale est la technique de choix. Le traitement anti-hypertenseur doit être
provisoirement arrêté. Le niveau d'anesthésie doit être obtenu en fractionnant les doses
d'anesthésiques locaux.
L'anesthésie péridurale est en théorie préférable à la rachianesthésie car ses effets
hémodynamiques sont moins brutaux.
L'anesthésie générale est nécessaire dans les formes sévères et/ou quand il existe une contre-
indication à l'anesthésie loco-régionale ou si urgence extrême : il faut se rappeler que le risque
d'intubation difficile est augmenté car les voies aériennes supérieures sont modifiées par
l'œdème. L'anesthésie doit être profonde et stable.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
88
II.8. ECLAMPSIE
1. Définition
Apparition au cours de la grossesse en pré, per ou post-partum de crises convulsives tonico-
cloniques suivies d’un coma chez une parturiente atteinte de prééclampsie, non liées à
l’épilepsie ou à d’autres maladies convulsivantes
2. Facteurs de risque
- facteurs liés à la grossesse : grossesse multiple, l’anasarque fœtale et l’infection urinaire ;
- facteurs non liés à la grossesse : l’hérédité, la primiparité, le statut socioéconomique,
l’obésité, le diabète, la race, le tabagisme et les conditions météorologiques.
3. Physiopathologie
L’éclampsie est la conséquence d’une prise en charge efficace de la pré-éclampsie non faite
qui peut aboutir à une micro-angiopathie avec possibilité d’œdème cérébro-méningé (les
artériographies cérébrales montrent des occlusions des artères distales de petit calibre sans
thrombose veineuse). Ces désordres entrainent chez la mère une hypovolémie relative associée
à une vasoconstriction, une altération de la perméabilité capillaire et des perturbations de la
coagulation. Ce syndrome peut ensuite entrainer des atteintes de tous les organes maternels.
Figure 1 : Physiopathologie de l’éclampsie
4. Classification
On distingue actuellement 4 types d’éclampsie,
- E. du pré partum : survenant avant le début du travail. Elle est dite précoce lorsqu’elle
survient avant la 28ème SA (38%) ;
- E. du per-partum : survenant pdt le travail (18%) ;
- E. du post partum : survenant dans les 7 jours suivant l’accouchement. Elle est dite tardive
lorsque survient entre les 3 à 4 sem (44%) ;
- E. intercurrente : survenant en pré-partum, mais s’arrêtant avec une amélioration clinique
suffisante pour permettre de poursuivre la grossesse pendant au moins 7jours.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
89
5. Clinique
Les signes prémonitoires :
- Céphalées frontales ou en casque pulsatiles avec adynamie, somnolence et vertiges, des
troubles oculaires avec diminution de l’acuité visuelle, phosphènes, amaurose
transitoire, des bourdonnements d’oreille.
- Des troubles digestifs avec nausées, vomissements, voire douleur épigastrique en barre
(signe de Chaussier), quasi pathognomonique de la crise.
- Dans le cas d’une toxémie gravidique en pleine poussée, l’œdème est parfois d’emblée
visible aux membres inférieurs, parfois encore latent, mais manifesté par une prise de
poids importante, anormale et rapide.
- L’hypertension artérielle qui est très fortement au dessus des chiffres limites de 140/90
mm/Hg a tendance à s’accroître encore souvent de façon brutale.
- L’albuminurie massive atteignant plusieurs grammes par litre.
- L’oligurie est constante.
Le traitement entrepris d’urgence dès l’apparition des signes prémonitoires de la toxémie
permet d’éviter la crise.
Signes d’éclampsie
La crise d’éclampsie évolue en quatre phases :
1-la phase d’invasion
Elle dure 5 à 30 secondes sans aura. Elle est marquée par des contractions fibrillaires et
rythmiques involontaires qui s’installent à la face (œil, paupière, mâchoire) et au cou. Les
globes oculaires roulent dans l’orbite et s’immobilisent latéralement, puis les contractions
atteignent les membres supérieurs qui s’enroulent en pronation sans toucher les membres
inférieurs.
2-la phase tonique
Elle dure 30 secondes, elle s’installe une minute après, elle associe :
- une hypertonie généralisée avec tête renversée et trismus (morsure de la langue), nuque
raidis, visage figé, yeux révulsés, membres supérieurs en flexion et les membres
inférieurs en extension.
- une apnée avec cyanose du visage et une mousse aux coins des lèvres.
3-la phase clonique ou convulsive
Elle dure 1 à 2 minutes. Elle débute par une longue inspiration qui met fin à la menace
d’asphyxie. Les mouvements convulsifs sont involontaires et désordonnés : face grimaçant, les
membres supérieurs sont projetés de façon anarchique, les muscles sont animés de
mouvements saccadés, les globes oculaires en nystagmus. Les membres inférieurs sont
relativement moins agités .Il est rare que la malade tombe et se traumatise.
4-la phase résolutive ou comateuse
S’installe un coma assez peu profond avec respiration stertoreuse d’une durée variable mais
assez courte (une demie heure à 2 heures) en fonction de l’intensité et de la répétition des
crises. Le réveil se fait à la fin de la crise et la malade ne garde aucun souvenir de l’accès ; il
n’y a ordinairement pas d’émission d’urine au cours de la crise.
Le caractère du coma : la profondeur du coma est un élément de gravité. Le plus souvent la
malade a des troubles de la vue, de l’intelligence tous ceux-ci sont dus à l’anoxie cérébrale.
Evolution de la crise d’éclampsie :
Dans l’immédiat on observe l’arrêt de la crise sous l’effet du traitement. En l’absence du
traitement, il y a répétition des crises avec état de mal éclamptique menaçant la vie de la mère :
asphyxie, défaillance cardiaque, œdème aigu du poumon, hémorragie cérébro-méningée.
Secondairement on peut retrouver une anurie par ischémie glomérulaire (régressive après
réanimation intense), un ictère par atteinte vasculaire disséminée, une psychose puerpérale
avec confusion.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
90
L’arrêt de la crise d’éclampsie ne survient souvent qu’après la mort du fœtus ou l’évacuation
utérine. Elle est assez rapide et le plus souvent complète d’où le caractère fœticide de la
maladie. L’éclampsie tue souvent le fœtus qui était dans un état de souffrance fœtale
chronique. S’il est vivant, il est le plus souvent prématuré ou hypotrophe.
Le pronostic materno-fœtal dépend de l’état clinique et des résultats des examens
complémentaires et les perturbations révélées par ces examens. En fonction de la date
d’apparition, plus l’éclampsie est précoce, plus elle est grave. Et concernant le caractère des
crises, l’éclampsie est d’autant plus grave que les crises sont subintrantes. Du point de vue
obstétrical, l’absence de travail est un élément de mauvais pronostic.
Signes associés
L’élévation de la température (témoignant d’un désordre au niveau du centre thermorégulateur
ou d’une infection), le sub-ictère (par suite d’une souffrance hépatique) sont de mauvais
paramètres ; la courbe de la tension artérielle élevée (due à la présence excessive de rénine,
d’aldostérone et de vasoconstricteur), la protéinurie massive et la diurèse basse ou effondrée
(par hypovolémie), l’hyperuricémie conduisant à une insuffisance rénale (le plus souvent
fonctionnelle) sont des mauvais indices.
L’œdème de la papille et les hémorragies rétiniennes (consécutives à une micro-angiopathie)
sont les éléments les plus graves.
Le pronostic materno-fœtal dépend aussi de l’apparition des complications et l’influence du
traitement.
6. Examens complémentaires
Le diagnostic étant fait, il est important de faire un bilan pour apprécier la gravité de
l’affection, de déterminer un pronostic, de suivre l’évolution à partir de ces repères. Le bilan
comporte le bilan sanguin (NFS), rénal (uricémie, créatinémie, protéinurie de 24 h), hépatique
(transaminases) et ophtalmique (fond d’œil).
Le Fond d’œil précisera le stade de l’atteinte rétinienne :
- Stade 1 : vasoconstriction artériolaire.
- Stade 2 : vasoconstriction plus intense avec tortuosité des artères et écrasements des
veines aux points de croisements.
- Stade 3 : stade 2 + Hémorragie et des exsudats.
- Stade 4 : en plus de l’œdème de la papille et de la rétine avoisinante réalise à l’extrême
une image de stase papillaire (neurorétinopathie).
Les résultats de ces différents examens vont guider la conduite à tenir et le pronostic.
7. Diagnostic différentiel
Thrombose veineuse cérébrale
Embolie artérielle cérébrale
Malformation vasculaire cérébrale (p.ex anévrisme)
Embolie amniotique
Le neuropaludisme
La méningo-encéphalite tuberculeuse.
La tumeur cérébrale
Autres qui sont facilement éliminées par l’anamnèse :
- l'épilepsie
- des Manifestations hystériques
- une intoxication par l’eau (au cours d’un traitement ocytocique),
- la toxicité des anesthésiques locaux,
- une syncope vagale et
- une hypoglycémie
8. Complications
Elles peuvent révéler la maladie ou compliquer son évolution.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
91
A. complications maternelles :
1) complications neurologiques
- L’œdème cérébral
- Hématomes Intra cérébraux
- Les lésions cérébrales ischémiques
2) les complications hépatiques : HELLP syndrome, la stéatose hépatique gravidique et
l’hématome sous capsulaire du foie.
3) hématome rétro placentaire
4) l’insuffisance rénale
5) œdème aigu du poumon (OAP)
6) les troubles de coagulation
7) le syndrome de Mendelson (inhalation)
8) Les complications cardiaques : ischémie myocardique, nécrose ou de complications
mécaniques (insuffisance ventriculaire gauche) secondaires à la labilité des chiffres
tensionnels.
9) les accidents oculaires : les troubles visuels peuvent aller depuis la baisse de l’acuité
visuelle à la cécité totale. Dans les cas graves, on observe un œdème de la rétine, des
hémorragies et plus rarement un décollement de la rétine.
10) les complications infectieuses : ils sont représentés essentiellement par les endométrites,
les pyélonéphrites, les pneumopathies nosocomiales, les chorioamniotites et les
infections pariétales.
11) Les complications thromboemboliques : Ce sont des complications fréquentes
survenant chez les patientes éclamptiques au cours du post partum favorisées par
l’allaitement et les troubles d’hémostase.
12) L’asphyxie : elle est une cause fréquente de syncope et de mort subite au cours de la
crise.
13) La morsure de la langue : elle est fréquente.
B. Les complications fœtales
1) le retard de croissance intra utérin
2) Mort fœtale in Utero
3) La prématurité
4) Le décès périnatal et néonatal précoce
9. Traitement
La prise en charge doit être précoce et comporte deux volets :
- la réanimation médicale des formes graves et de leurs complications,
- la prise en charge obstétricale.
Principes : une prise en charge multidisciplinaire qui vise à :
- assurer la liberté des voies aériennes,
- faire céder les convulsions,
- faire baisser la pression artérielle en conservant une PAM à 80 mmHg,
- provoquer l'accouchement (césarienne sauf multipare à terme avec col favorable).
NB : Il faut prévenir l'hypotension artérielle trop brutale.
La réanimation comprend la stabilisation de la PA, l'expansion volémique par cristalloïdes
(Ringer lactate) ou gélatines, un apport hydrique adéquat réduit au minimum (surcharge :
OAP), le maintien d'une diurèse. La surveillance associe pouls et PA, sondage urinaire,
prévention des morsures (canule), prévention de l'inhalation bronchique avec intubation si
score de Glasgow (GCS) inférieure ou égala à 9.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
92
Prise en charge
- Pendant la crise
Placer (sans se faire mordre les doigts) un mouchoir ou des compresses roulées entre les dents
pour éviter la morsure de la langue qu’on remplacera par une canule de Mayo après la crise
Protéger la gestante de toute chute pouvant entraîner fracture ou trauma crânio-encéphalique
Placera dès que possible une large voie veineuse par laquelle on donnera un anticonvulsivant :
R/Diazépam : 10 mg dilué en I.V. lent (2 minutes). Si les convulsions reprennent, renouveler
l’injection sans dépasser 30 mg en 1 h, sinon la patiente risque une dépression respiratoire. Si
nécessaire, instaurer une oxygénothérapie ou une ventilation assistée à l’aide d’un ballon
d’AMBOU.
Si les convulsions s’arrêtent, on poursuivra le traitement par une perfusion 40 mg de
diazépam dilué dans 500 ml de sérum physiologique ou Ringer lactate de manière à obtenir
une sédation tout en maintenant l’état de veille.
Ou R/ Diazépam par voie rectale si on ne peut le donner en I.V.. Donner 20 mg dilué dans
une seringue de 10 ml qu’on instillera dans le rectum à l’aide d’une sonde. Si on ne dispose
pas d’une sonde on introduira la seringue préalablement lubrifiée à moitié dans le rectum
après avoir retiré l’aiguille. On Injectera le contenu, tout en laissant la seringue en place et en
maintenant les fesses de la patiente serrées pendant 10 minutes pour éviter l’expulsion du
produit. Si les convulsions reprennent, on donnera encore 10 à 20 mg, par heure, en fonction
du poids de la patiente et de la réponse clinique.
N.B. : Ne pas dépasser 100 mg de diazépam en 24 h.
ou R/ Luminal*: ½ à 1 amp diluée en I.V. lent à renouveler si besoin
ou R/ Largactil*: 50 mg en I.V. lent, ensuite 25 mg I.M. toutes les 6 heures
ou R/ Sulfate de Magnésie selon le schéma de PRITCHARD :
Donnera 4 g de MgSO4 à 20% en IV lent (5 minutes), suivie de 5 g de MgSO4 à 50% en IM
profonde dans chaque fesse. Ensuite 5 g de sulfate de magnésium à 50% en IM toutes les 4 h,
dans la fesse gauche puis dans la fesse droite sans dépasser la dose totale de 39 mg en 24h.
Si on ne dispose pas de MgSO4 à 50%, on donnera 2g MgSO4 à 20% en I.V. lente, ensuite 1g
en I.V. lente toutes les heures.
Pendant le traitement on surveillera tout particulièrement les signes d’intoxication au sulfate de
magnésie (MgSO4)toutes les 15 minutes: F.R., diurèse, réflexes rotuliens.
En cas d’intoxication: F.R. (< 16 cycles/min.), oligurie (diurèse < 30 ml/h), abolition des
réflexes ostéo-tendineux, B.A.V. à l’E.C.G. , on arrêtera le traitement et on donnera 10 ml de
gluconate de calcium à 10 % en I.V. lente qu’on renouvellera si nécessaire jusqu’à la
disparition des troubles.
- Après la crise :
Aspiration oro-trachéale en cas d’encombrement des voie respiratoires. Une intubation peut
être nécessaire à cet effet surtout si la patiente est en coma;
Oxygénothérapie par intermittence et si nécessaire sous respirateur artificiel;
Sonde vésicale à demeure pour surveiller la diurèse horaire;
Sonde nasogastrique d’alimentation si la patiente est en coma.
Corriger les troubles hydro-électrolytiques (Lactate de Ringer) sous surveillance de la
pression veineuse centrale. Si on ne peut la mesurer, on donnera en moyenne 40 gttes/ min.
tout en surveillant la diurèse horaire (qui doit être de 30 à 50 ml/ h), et les signes d’O.A.P.
(dyspnée, toux grasse avec expectorations mousseuses...). On stoppera la perfusion dès
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
93
qu’apparaîtrons les signes d’encombrement de la petite circulation (dyspnée avec râles sous-
crépitants…) et on administrera 20 mg de Lasix* en I.V.D..
Surveiller conscience, T.A., diurèse et répétition des convulsions
Si la femme est enceinte, on évacuera la grossesse dès la stabilisation de l’état clinique (arrêt
des convulsions, lyse tensionnelle) quel que soit l’âge de la grossesse. Soit que le travail ne se
déclenche pas, on pratiquera alors une césarienne urgente après avoir maîtrisé les convulsions.
Soit que le travail se déclenche, il est en général rapide, et on tentera un accouchement par
voie basse (sauf si S.F.A., dystocie dynamique, poussée hypertensive, primipare du fait que sa
dilatation est généralement plus lente). Cependant si la crise se répète, on passera rapidement
par la voie haute.
Pour les grossesses trop jeunes, on est souvent tenté de laisser se poursuivre la grossesse
surtout si les convulsions s’arrêtent et que le fœtus est vivant. Nous pensons cependant qu’il
serait plus logique d’interrompre carrément la grossesse parce que l’éclampsie, complication
paroxystique de la prééclampsie, constitue déjà un signe de gravité; laisser la grossesse évoluer
exposerait inutilement la gestante à des complications encore plus graves.
On instaurera un traitement anti-hypertenseur: R/ Nepréssol*( amp. de 25 mg) : on injectera 5
mg en IV lente, toutes les 5 minutes, jusqu’à ce que la tension artérielle diastolique soit
redescendue jusqu’à 90 à 100 mmHg, ou 50 mg dans 500 ml de Lactate de Ringer qu’on fera
couler à un débit moyen de 4 gttes/min;
ou R/ Catapressan* ( amp. de 0,150 mg ) : 1 amp. en I.M. ou I.V. lente qu’on renouvellera
si nécessaire.
ou R/ Labétalol ; 10 mg en I.V. lente, si la tension diastolique reste supérieure à 110 mm Hg
après 10 minutes, on injectera encore 20 mg en IV lente. On augmentera la dose à 40 mg puis à
80 mg en I.V. lente si la T.A. diastolique reste élevée 10 minutes après la dernière injection
En cas de convulsions subintrantes, on procédera à une intubation et on placera la patiente sous
respirateur artificiel.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
94
II.9. HELLP SYNDROM
Hémolysis ELevoted liver enzymes Low Platelet count.
Il a été décrit pour la première fois par WEINSTEIN en 1982. Il s’agit d’une atteinte hépatique
compliquant la PE sévère. Elle se traduit par l’élévation des transaminases à laquelle
s’associent une hémolyse et une thrombopénie. L’incidence du HELLP syndrome varie entre 2
et 12% dans les PE et 20% dans les PE sévères.
Il n’existe pas dans la littérature de consensus concernant les valeurs retenues pour la
thrombopénie qui peut varier de 75000/mm3 à 150000/mm3 ainsi que les indicateurs de
l’atteinte hépatique utilisés. La définition reste biologique mais il y’a des controverses sur les
critères diagnostiques, dont le choix a été fait dans un souci de reproductibilité et de
comparaison des différentes séries.
Les critères retenus sont ceux de SIBAI :
- hémolyse : présence de schizophytes + Biluribine totale > 12mg/l, Ou LHD >600 UI/L
- augmentation des enzymes hépatiques ou cytolyse hépatique. ASAT (SGOT) > 70 UI/L
- thrombopénie : taux de plaquettes < 100 000 / mm3.
Le HELLP Syndrome augmente le risque de morbi-mortalité maternelle et fœtale. L’évolution
se fait spontanément vers la guérison après l’accouchement. Il s’agit d’une micro angiopathie
due à des lésions endothéliales diffuses, dont l’origine est multifactorielle (ischémie
placentaire ; migration de micro villosités syncitiales dans la circulation, activation des PNN).
70% des HELLP syndrome surviennent pendant la grossesse et 30% dans le post partum. Il est
important de noter que 80% des formes qui surviennent en post partum, concernent des
patientes traitées en pré partum pour éclampsie. Chez 20% qui restent, les signes de pré
éclampsie apparaissent après avoir identifié le HELLP Sd (HELLP Sd inaugural).
Ainsi HELLP Sd doit être recherché systématiquement chez toute patiente toxémique sévère à
l’admission mais aussi dans le post partum immédiat.
Cliniquement, le diagnostic du HELLP Sd est difficile, souvent il évolue de manière insidieuse
car les signes ne sont pas spécifiques et aboutissant à un retard diagnostic. Ceci peut être
responsable d’un pronostic désastreux. Les douleurs abdominales (au niveau de l’hypochondre
droit ou l’épigastre) prédominent (65% cas) et doivent être considérées, comme un signe
d’alerte. Les autres signes sont représentés essentiellement par les nausées ou vomissements,
les céphalées et les troubles visuels. L’hémolyse n’entraîne l’ictère que dans 50% des cas.
Le traitement et la surveillance du HELLP Sd sont ceux d’une PE sévère. La plupart des
auteurs, s’appuyant sur le mauvais pronostic materno fœtal de cette affection et les dangers que
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
95
fait courir la poursuite de la grossesse, prônent l’évacuation utérine. Toutefois le cas le plus
fréquent c’est l’association HELLP Sd - éclampsie. Elle constitue une indication formelle à
l’extraction fœtale vu la mortalité et la morbidité fœto-maternelle élevée comprenant CIVD
dans 21%, HRP 16% , IRA 8%, hémorragie cérébrale, OAP et un risque accru d’hémorragie de
la délivrance. En pratique, l’attitude logique chez une patiente présentant un HELLP Sd est
l’interruption de la grossesse quelque soit le mode de l’accouchement, si le terme est égal ou
supérieur à 34 SA ou si la maturité pulmonaire est acquise. Il est de même devant la
dégradation de l’état maternel, une souffrance fœtale ou l’existence d’une CIVD, quelque soit
l’âge gestationnel. A l’inverse, un traitement conservateur peut être proposé avant 34 SA pour
obtenir une maturité pulmonaire suffisante et faciliter le transfert vers un centre de
périnatalogie intégrant une unité de réanimation néonatale. Cependant cette attitude
expectative nécessite une surveillance tant sur le plan fœtal que sur le plan maternel, la
décision thérapeutique doit être évolutive, retenant que l’attentisme ne doit être inconsidéré. Le
bénéfice néonatal escompté étant souvent minime en regard des risques maternels encourus.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
96
II.10. HEMATOME SOUS-CAPSULAIRE DU FOIE (HSC).
L’hématome sous capsulaire du foie touche essentiellement la multipare et la primipare âgée.
Elle survient dans 60% des cas au 3ème trimestre. Mais parfois dans le post partum. Tous les
acteurs s’accordent sur la difficulté du diagnostic.
Dans les formes bénignes, les lésions sont les plus souvent asymptomatiques et leur prévalence
est inconnue. Dans les formes sévères, le diagnostic est rarement fait avant l’intervention.
Cependant il importe d’évoquer le diagnostic d’hématome s/s capsulaire du foie avant la
rupture hépatique de gravité redoutable, devant un syndrome douloureux abdominal haut chez
une multipare âgée, présentant un Sd toxémique.
- La biologie montre un HELLP Sd
- l’échographie abdominale est l’examen de choix. Elle permet de faire le diagnostic.
- La TDM permet de préciser l’étendue et d’assurer la surveillance ultérieure.
- L’artériographie mésentérique précise la topographie de la vascularisation artérielle
hépatique de manière à faciliter le geste d’hématose.
Néanmoins, dans le contexte de l’urgence, la laparotomie exploratrice confirme le diagnostic.
La conduite thérapeutique d’un hématome s/s capsulaire du foie est la surveillance sous
réserve :
- d’avoir une réserve de dérivés sanguins a la banque de sang.
- d’avis chirurgien viscéraliste.
- d’éviter la manipulation directe ou indirecte du foie.
- d’un monitorage hémodynamique continu.
- d’un traitement médical bien conduit avec :
o stabilisation tensionelle.
o Prévention des convulsions.
Si le HSCF est non rompu, le traitement doit rester conservateur avec transfusion de plasma
frais congelé décongelé. La patiente sera soumise à une surveillance rigoureuse de l’évolutivité
par des échographies hépatiques répétées ou des tomodensitométries.
La rupture de l’HSCF peut nécessiter une laparotomie en urgence, le geste va consister en :
- Application du spongel et de packing
- Ligature du segment hépatique qui soigne
- Drainage chirurgical.
Cette complication est responsable d’une lourde mortalité (50% dans la série de Sibaï). Dans
tous les cas, l’hospitalisation en réanimation en post opératoire s’impose.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
97
II.11. STEATOSE HEPATIQUE AIGUË GRAVIDIQUE (SHAG).
C’est une complication rare même très grave de la grossesse survenant le plus souvent au cours
du 3ème trimestre. Les signes cliniques sont peu spécifiques, associant nausées, vomissements,
pyrosis, fatigue intense et douleur épigastrique.
Sur le plan biologique, le bilan hépatique est perturbé avec augmentation des enzymes
hépatiques (LDH). L’hypoglycémie et l’effondrement des facteurs de coagulation signent les
formes évoluées. Elle pose le problème du DC différentiel avec le HELLP Sd (voir tableau I).
Le diagnostic est affirmé par l’histologie hépatique qui met en évidence des micro- vésicules
graisseuses au sein des hépatocytes.
Figure 8 : stéatose hépatique gravidique : le noyau reste au centre de l’hépatocyte et n’est pas refoulé par la
stéatose micro vacuolaire.
La gravité de l’association éclampsie-SHAG tient aux nombreuses défaillances viscérales
associées, en particulier à l’encéphalopathie hépatique et aux troubles d’hémostase.
En post partum, les complications secondaires à la SHAG sont représentées essentiellement
par :
- Les hémorragies génitales - l’infection
- l’insuffisance rénale aiguë - L’hypoglycémie
- le syndrome de rétention hydro-sodée (ascite)
La prise en charge après l’évacuation utérine n’est pas spécifique. Elle consiste à :
- la correction des troubles hydro-électrolytiques et l’apport de glucose.
- L’apport du PFC et de culots globulaires en fonction du bilan sanguin.
- Un traitement symptomatique de l’encéphalopathie hépatique par le lactulose et flumazénil
(anexate)
- La relance de la diurèse par des diurétiques après remplissage voir hémodialyse.
- La prévention de l’infection nosocomiale par des règles d’asepsie stricte.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
98
II.12. GROSSESSE MULTIPLE
1. DEFINITION :
Présence de plus d'un fœtus dans l'utérus.
2. CAUSES
- Fécondation de plusieurs ovules
- Division d'un ovule fécondé en deux fœtus distincts
- Facteurs prédisposants : antécédents familiaux de grossesse multiple, traitement de
l'infertilité à l'aide d'inducteurs de l'ovulation
3. CLASSIFICATION SELON LE NOMBRE DE ZYGOTES (œufs fécondés) :
a. Grossesse gémellaire dizygote ou les faux jumeaux :
C'est une grossesse issue de la fécondation de deux ovules (œufs). Les faux jumeaux sont
génétiquement différents, donc ils sont semblables à des frères et sœurs nés à différentes
époques ; Ils peuvent être du même sexe ou de sexe différents. La grossesse est toujours di-
amniotique dichoriale (ou bi-amniotique bichoriale). Il existe deux cavités amniotiques et
chaque fœtus se développe dans une cavité amniotique propre à lui. On trouve deux placentas
séparés mais on peut voir dans certains cas une seule masse placentaire par la fusion des deux
placentas (placenta synchorionique), même dans ce cas là, il y a toujours deux amnios et deux
chorions donc il n'existe pas de circulation sanguine commune par des anastomoses
vasculaires. La membrane qui sépare les deux cavités amniotiques (cloison inter-ovulaire) est
composée de quatre couches : deux amnios et deux chorions. La procréation médicalement
assistée (PMA) est parfois responsable de l'augmentation de ce type de grossesse.
Cas particuliers :
Grossesse hétérotopique ou ditopique ou combinée:
Grossesse gémellaire bi-ovulaire caractérisée par la nidation d'un œuf à l'intérieur de la cavité
utérine (grossesse intra-utérine) et la nidation d'un autre l'œuf à l'extérieur de l'utérus
(grossesse extra-utérine). La définition exclut les grossesses extra-utérines bilatérales.
La superfétation :
C'est l'implantation d'une nouvelle grossesse dans un utérus qui contient déjà une grossesse en
développement. Ce type de grossesse est déjà connu chez certains mammifères.
La superfécondation :
C'est la fécondation de deux ovules à peu près en même temps par des spermatozoïdes
provenant de deux mâles différents. Dans ce cas la les faux jumeaux ont deux pères différents.
b. Grossesse gémellaire monozygote ou les vrais jumeaux :
C'est une grossesse issue de la division d'un œuf fécondé unique. Les jumeaux sont
génétiquement identiques, donc ils ont les caractères apparents et latents, le même sexe, même
groupe sanguin, même couleur des yeux...
Selon la duré qui sépare la fécondation de la division de l'œuf fécondé on peut distinguer
plusieurs types de la placentation (le nombre des cavités amniotiques et la le nombre de
chorions) :
Grossesse gémellaire monozygote di-amniotique dichoriale :
La division de l'œuf unique fécondé survient rapidement, dans un délai inférieur ou égal à deux
jours par rapport à la fécondation ou la grossesse est encore au stade de 2 à 4 blastomères.
Chaque jumeau se développe dans une cavité amniotique propre à lui, la membrane qui les
sépare est composée de quatre couches : deux amnios ; deux chorions. Les deux placentas
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
99
peuvent être distincts, séparés, mais ils peuvent fusionner ensemble pour former une seule
masse placentaire. Elle représente 30 % des grossesses gémellaires monozygotes.
Grossesse gémellaire monozygote di-amniotique monochoriale :
La division de l'embryon survient dans un délai de supérieur à (2) jours et inférieur à 8 jours
par rapport à la fécondation (au stade de la morula ou blastocyste et avant la formation de
l'amnios). Chaque jumeau se développe dans une cavité amniotique propre à lui, la membrane
qui les sépare (la cloison inter-ovualire) est composée de deux couches qui sont les deux
amnios. Il y a une seule masse placentaire avec un seul chorion ; dans ce cas la une circulation
sanguine commune est possible par des anastomoses vasculaires artérielles ou veineuses.
Elle représente 70 % des grossesses gémellaires monozygotes.
Grossesse gémellaire monozygote mono-amniotique monochoriale :
La division de l'embryon survient dans un délai de supérieur à (7) jours et inférieur à (14) jours
par rapport à la fécondation (au stade de développement embryonnaire où la cavité amniotique
est déjà formée avec embryon à deux feuillets). Les deux jumeaux se développent ensemble
dans une cavité amniotique unique. Donc il existe une seule masse placentaire, un seul amnios
et un seul chorion. Si la séparation survient avant le 12ème jour de la fécondation il se forme
deux vésicules ombilicales et deux cordons. Si la séparation est survenue au 12ème ou 13ème
jour par rapport à la fécondation, il se forme une seule vésicule ombilicale et un seul cordon
bifurqué vers les deux jumeaux séparés.
Elle représente 1 à 2 % des grossesses gémellaires monozygotes.
Grossesse gémellaire monozygote mono-amniotique monochoriale avec
monstre double (jumeaux conjoints ou siamois) :
Deux théories expliquent la fusion des jumeaux conjoints :
- La division (scission) incomplète de la masse embryonnaire qui survient tardivement,
dans un délai égale ou supérieur à (14) jours par rapport à la fécondation.
- La théorie la plus récente voit la survenue des jumeaux conjoints par la fusion
secondaire et partielle de deux disques embryonnaires monozygotes déjà séparés. Dans
cette théorie il existe deux éventualités :
o la fusion des disques embryonnaire se fait à la surface sphérique de la vésicule
vitelline (théorie extra-sphérique).
o la fusion se fait à l'intérieur de la cavité amniotique (théorie endosphérique).
Selon cette théorie, les deux disques embryonnaires peuvent fusionner en différents points et
sous angles variés, et le résultat, une grande variété de types de fusion entre les jumeaux
conjoints.
Ces grossesses sont caractérisées par la présence d'un seul placenta, un seul chorion, un seul
amnios donc une seule cavité amniotique
4. CLINIQUE
1. Anamnèse
Il y a lieu de soupçonner une grossesse multiple chez les gestantes qui ont :
- des antécédents familiaux de grossesse multiple et chez celles qui sont traitées pour
l'infertilité.
- Exagération des signes sympathiques de la grossesse :
o Présence accentuée et précoce des désagréments de la grossesse
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
100
o Présence persistante et précoce de nausées, de brûlures d'estomac
o Plus tard au cours de la grossesse, dyspnée et indigestion accentuées
2. Examen obstétrical
- Hauteur du fond utérin supérieure à la normale, compte tenu du stade de la grossesse.
- Les mouvements fœtaux se manifestent sur une plus grande surface.
- On peut sentir un nombre excédentaire de membres à la palpation.
- On peut entendre deux cœurs distincts.
3. Examens paracliniques:
- La Rx. A.A.B. à partir de la 36è semaine montre 2 squelettes fœtaux
- L’échographie: confirme le diagnostic, décrit la morphologie des fœtus, leur croissance,
le nombre de sacs ovulaires, le nombre et l’insertion du (des) placenta(s)
NB : Un diagnostic échographique de gémellité posé précocement est la seule manière de
déterminer avec exactitude la chorionicité de la gémellité
5. DIAGNOSTIC DIFFERENTIEL
- Grossesse molaire - Hydramnios
- myome utérin - Un seul gros bébé (macrosomie)
- kyste ovarien
6. COMPLICATIONS
Complications pour la mère Complications pour le fœtus
- Pré-éclampsie - RCIU
- Anémie - Anomalies congénitales
- Travail et accouchement prématurés - Mort fœtale in utero
- Hydramnios - Naissance prématurée
- Vomissements de la grossesse
7. PRISE EN CHARGE
Pendant les C.P.N.:
On dépistera les signes de béance cervico-isthmique par un T.V. systématique à chaque
C.P.N. et si nécessaire on fera un cerclage du col utérin
On recherchera les signes de toxémie (H.T.A., protéinurie, O.M.I.)
On hospitalisera la gestante au moindre signe de menace d’avortement ou
d’accouchement prématuré
Pendant le travail :
Dès l’admission à la salle d’accouchement, après l’évaluation clinique on fera une Rx.
A.A.B. ou une échographie pour déterminer la présentation des 2 fœtus.
Si l’accouchement par voie basse est impossible ou risquée, on fera une césarienne. Ces
circonstances sont :
o Le 1er fœtus ou les 2 fœtus en présentation transversale
o Le 1er fœtus en présentation de siège (relative)
o Fœtus siamois
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
101
o Grossesse univitelline (risque d’accrochage des fœtus et d’enroulement des cordons
avec décollement prématuré du placenta)
o Utérus cicatriciel (risque important de déhiscence à cause de la surdistention utérine)
o Toutes les autres indications obstétricales de la césarienne.
Si l’accouchement par voie basse est possible, on surveillera l’évolution du travail
comme d’habitude. En cas de dystocie dynamique, on pratiquera une R.A.P.E. pour
diminuer la surdistention utérine et si nécessaire on placera un Theobald et en cas
d’échec, on passera par la voie haute. Si par contre le travail évolue bien, on prendra un
abord veineux avec 1l de sérum glucosé 5% en fin de dilatation. A dilatation complète, la
parturiente sera placée sur la table d’expulsion, deux trousses d’accouchement seront
préparées et on constituera une équipe suffisante pour accueillir les nouveau-nés. Après
l’expulsion du premier jumeau (en céphalique ou en siège), si la parturiente était sous
Theobald, on arrêtera la perfusion. L’accoucheur fera un T.V. de réévaluation et si
nécessaire l’aide accoucheur procédera à la verticalisation de la présentation par la
version par manœuvre externe.
Si la présentation est céphalique ou de siège, l’accouchement par voie basse sera
envisagé. On ajoutera 10 U.I. d’ocytocine dans la perfusion de sérum glucosé 5%, ou on
reprendra le Theobald, pour améliorer le régime contractile et écourter ainsi le délai
d’expulsion entre les 2 fœtus. Ce délai ne devra en aucun cas excéder 30 minutes, sinon
le fœtus restant court un risque plus grand de morbidité et de mortalité.
Si la dilatation est complète, l’accoucheur pratiquera une rupture artificielle des
membranes et dirigera l’accouchement comme pour une grossesse unifœtale. Si la
dilatation se rétréci, il attendra qu’elle soit à nouveau complète puis procédera comme ci-
haut.
Si la présentation est transversale et irréductible par la version par manœuvre externe ou
en cas de procidence du cordon, une césarienne urgente sera pratiquée.
N.B.: la version-extraction ne devra être faite que si la césarienne ne peut être pratiquée
urgemment, car elle est entachée d’une grande mortalité et morbidité même faite par des
mains expertes.
Après la délivrance on laissera couler la perfusion d’ocytocine pendant au moins 2 heures
afin de prévenir hémorragie de la délivrance.
Le post-partum sera géré comme pour toute grossesse.
CAS PARTICULIERS
1°) Un des fœtus est mort
On devra d’abord en rechercher la cause.
Si l’étiologie de la mort est évidente et menace la vie du fœtus encore vivant, on pratiquera
rapidement une césarienne si la maturité pulmonaire est atteinte.
Si l’étiologie de la mort n’est pas évidente on fera une échographie d’urgence pour
déterminer le nombre de placentas:
Si les placentas sont distincts et que la grossesse est encore jeune, on peut laisser
évoluer la grossesse tout en surveillant en hospitalisation la crase sanguine (T.S., T.C.,
fibrinogène toutes les 48 heures). Une échographie sera faite une fois par semaine
ainsi qu’un N.S.T. (si grossesse de plus de 28 semaines) jusqu’à l’accouchement.
Si la grossesse est à terme ou si la maturité pulmonaire est atteinte, l’accouchement
sera décidé dans les plus brefs délais de préférence par voie haute.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
102
Si le placenta est unique, on devra extraire rapidement le jumeau vivant s’il est viable,
car sa vie est inéluctablement menacée. Une prolongation de la grossesse entraînera
soit sa mort du fœtus soit lui laissera des séquelles neurologiques importantes après la
naissance.
2°) Grossesse triple
Si l’accouchement par voie basse est décidé, il sera dirigé comme pour la grossesse
gémellaire. Cependant la césarienne dans ce cas est plus souvent recommandée, car elle
permet d’améliorer le pronostic fœtal. Elle sera généralement pratiquée après la 36è semaine.
3°) Grossesse de plus de 3 enfants
Une césarienne élective sera pratiquée de préférence vers la 36è semaine ou dès que la
maturité pulmonaire est atteinte. Tout devra être mis en œuvre pour la réanimation néonatale
dès l’extraction des fœtus.
Une perfusion d’ocytocine (20 U.I. dans 1l de sérum glucosé à 5%) sera placée dans le post-
partum pour prévenir une hémorragie de la délivrance.
4°) Fœtus siamois
L’accouchement se fera toujours par césarienne si le diagnostic est connu d’avance.
Malheureusement, bien souvent dans notre milieu (faute d’échographie) c’est au moment de
l’expulsion fœtale qu’on est surpris par le blocage d’une partie du fœtus dans le vagin, ainsi
le taux de mortalité néonatale est très élevé.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
103
PATHOLOGIE DES ANNEXES FOETALES
II.13. OLIGOAMNIOS (OLIGOHYDRAMNIOS)
1. DEFINITION
C’est une insuffisance de liquide amiotique dont la quantité est estimée inférieure à 250ml.
Avec l’échographie cette appréciation passe par la détermination de l’Index de LA ≤ 5cm
(selon Phelan) ou la mesure de la plus grande poche de liquide amniotique (inférieure à 3
cm).
2. ETIOLOGIE
En dehors de la souffrance fœtale chronique, d’un effet médicamenteux (Indométacine), du
dépassement de terme, et de la rupture prématurée des membranes, il faut toujours suspecter
une malformation fœtale en cas d’oligohydramnios, jusqu’à preuve du contraire. Il s’agit
notamment de :
- lésions obstructives du système urinaire ;
- agénésie rénale ou autre dysplasies rénales ;
- malformations chromosomiques.
3. COMPLICATIONS
- Risque de décès périnatal lié à la pathologie sous-jacente (malformative ou non).
- Hypoplasie pulmonaire (perturbation de la dynamique des fluides intra pulmonaires). Le
rapport entre la circonférence thoracique et la circonférence abdominale est constant durant
la grossesse (0,94±0,05). Le rapport est utile pour prédire une hypoplasie pulmonaire
observée si ce rapport > 0,90).
- Absence des mouvements fœtaux qui peut entraîner des déformations squelettiques (pieds
bots, contractures articulaires…).
- Possibilité de brides pouvant entraîner des amputations de membres.
- Complications funiculaires : compression du cordon (décélération variables).
- Dystocie dynamique.
- Malprésentation (ex. siège).
- Couches sèches.
4. CLINIQUE
Sur le plan clinique, la hauteur utérine est inférieure à celle attendue pour l’âge de la
grossesse et sur le plan paraclinique (échographie), l’AFI est < 50.
5. CONDUITE A TENIR
- Rechercher la cause (échographie morphologique complète, caryotype).
- Amnio-infusion : remplacement échoguidé de liquide (sérum salé 0,9% à raison de 100ml
avant 24 semaines, 150-300ml après 24semaines) par voie transabdominale. Ceci améliore
la qualité des images échographiques des malformations éventuelles et permet une étude de
la dynamique urinaire, tout en restaurant le rôle protecteur du LA.
- Hydratation maternelle : l’apport d’au moins 2 litres d’eau en 2 heures par jour, avec une
eau faiblement minéralisée, permet une augmentation significative de liquide amniotique et
donc du bien-être fœtal. Parmi les mécanismes explicatifs de cet effet, on cite soit
l’amélioration de la perfusion des artères utérines et de la perfusion/oxygénation fœtale,
soit la diminution de l’osmolalité maternelle conduisant à un passage net d’eau dans le
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
104
plasma fœtal et donc une diminution de son osmolalité aboutissant à l’augmentation de la
production urinaire. Ce qui est sûr, c’est que la quantité de liquide amniotique est
fondamentalement liée à l’hydratation maternelle. Il faut donc assurer chez nos gestantes
un apport d’eau suffisant.
- Instillation transcervicale parfois également utilisée avec succès durant l’accouchement
pour prévenir les décélérations variables.
- Si le diagnostic est posé à terme (avant l’accouchement), l’oligoamnios qui traduit une
souffrance fœtale chronique, entre dans le score biophysique de Manning permettant
d’évaluer le bien être fœtale et il est ôté 0. La voie d’accouchement est haute car le rôle
d’amortisseur du LA pendant le travail ne sera pas assurer et donc le pronostic néonatal
incertain.
II.14. POLYHYDRAMNIOS
1. DEFINITION
L’hydramnios est classiquement défini par un excès de liquide amniotique supérieur à 2 litres
à l’accouchement. Cette définition est devenue un peu caduque depuis le développement de
l’échographie qui permet l’évaluation de la quantité du liquide amniotique au cours même de
la grossesse.
Il est important de savoir dépister l’hydramnios, car c’est un signe d’appel de malformation
fœtale : son apparition peut constituer une donnée importante du suivi évolutif d’une
pathologie (diabète, pathologie Rhésus, malformation fœtale connue), et il existe parfois une
indication à drainer cet hydramnios.
On reconnaît deux variétés : la forme aiguë et la forme chronique.
- Polyhydramnios aigu
Affection qui survient le plus souvent au 2ème trimestre et se caractérise par une
augmentation soudaine et rapide de la quantité de LA, accompagnée de symptômes
maternels importants (douleurs abdominales, nausée, vomissements, dyspnée, orthopnée).
- Polyhydramnios chronique
Affection qui survient plus tardivement (3eme trimestre) et à une évolution plus lente.
2. ETIOLOGIES
L’hydramnios est la conséquence d’un déséquilibre entre la production et l’élimination de
liquide amniotique.
Défaut d’élimination
Tout défaut d’absorption du liquide amniotique par le fœtus peut être à l’origine d’un
hydramnios : défaut de déglutition d’origine musculaire ou neurologique ou compressive,
obstacle digestif dont le retentissement sera d’autant plus important que l’obstacle est haut
situé.
Production excessive
La principale cause est la polyurie fœtale secondaire soit à des facteurs maternels (diabète),
soit à des facteurs fœtaux (cardiopathie, infection, syndrome transfuseur-transfusé).
Les anomalies ouvertes du système nerveux central (myéloméningocèle, anencéphalie)
peuvent être à l’origine d’un hydramnios secondaire à une fuite liquidienne.
Dans les anémies importantes, il se développe un syndrome de rétention hydrique généralisée
avec hypoprotidémie et hypervolémie dont le mécanisme est mal connu, mais qui aboutit à un
anasarque foeto-placentaire dont le premier signe est l’hydramnios associé à un
épaississement placentaire.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
105
Les différentes étiologies sont :
a) Ovulaires :
Malformations fœtales :
- Atrésie œsophagienne ou intestinale ; - Malformations chromosomiques ;
- Malformations du SNC ; - Fentes labio-maxillo-palatines ;
- Malformations cardiaques sévères ; - Omphalocèle.
Grossesses gémellaires. Tumeurs fœtales (poumons, reins).
Hydrops non immuns. Syndrome transfuseur transfusé.
Chorio angiomes.
b) Maternelles :
Diabète.
Infections (syphilis).
Incompatibilité fœto-maternelle.
c) Indéterminée.
3. DIAGNOSTIC
a. Clinique
Le diagnostic clinique d’hydramnios repose sur la mesure de la hauteur utérine, anormale pour
l’âge gestationnel. S’y associe éventuellement le classique signe du glaçon, témoin de la
mobilité du pôle fœtal au toucher vaginal. Les autres signes cliniques sont quasi inexistants en
cas d’hydramnios chronique.
En cas d’hydramnios aigu, la surdistension induit des signes de menace d’accouchement
prématuré (contractions, modifications cervicales) et des signes témoignant d’un
retentissement maternel : dyspnée d’effort, voire de décubitus ; douleurs abdominales à
irradiation lombaire, insomniantes ; utérus tendu, douloureux à la palpation ; présence d’une
circulation veineuse collatérale ; hypotension artérielle ; œdèmes des membres inférieurs.
b. Echographie
L’échographie permet de confirmer le diagnostic d’hydramnios, mais aussi d’en rechercher
l’étiologie. Les hydramnios modérés facilitent l’analyse de la morphologie fœtale.
1) Evaluation subjective du liquide amniotique
Dès la pose de la sonde d’échographie, l’opérateur éprouve l’impression d’une discordance
entre la taille du fœtus et les citernes de liquide amniotique avec un fœtus semblant
classiquement “nager librement dans un océan”, autrement appelé “fœtus suspendu”. Cette
approche peut suffire à poser le diagnostic et il a bien été montré une excellente corrélation
entre l’évaluation subjective par un opérateur entraîné et l’évaluation chiffrée à l’aide en
particulier de l’index amniotique. Cependant, une suspicion d’hydramnios doit motiver
l’échographiste à mesurer les grandes citernes ou l’index amniotique dans l’idée de quantifier
l’anomalie de liquide de façon précise et reproductible.
2) Méthodes semi-quantitatives d’estimation de liquide
Ces mesures permettent de confirmer le diagnostic d’hydramnios, d’en quantifier l’importance
et d’en réaliser une surveillance évolutive.
Mesure de la plus grande citerne
Elle a été proposée pour la première fois par Chamberlain et correspond à la mesure de la
profondeur (diamètre vertical) de la plus grande citerne de liquide amniotique, sans
interposition du cordon ombilical (fig).
o Utérus divisé en 4 quadrants
o Sonde parallèle au plan sagittal
o Mesure de la poche la plus profonde sans cordon dans les 4 quadrants
o Ne pas appliquer une pression trop importante avec la sonde
o Pratiquer la mesure à une période de relative inactivité fœtale
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
106
o Si IA pathologique, répéter la mesure 3 fois
o Une valeur > 8 définit l’hydramnios.
On distingue ainsi trois types d’hydramnios :
- modéré : plus grande citerne 8-12 cm,
- moyen : plus grande citerne 12-16 cm,
- sévère : plus grande citerne > 16 cm.
Index amniotique
Proposé par Phelan, il est préféré par la majorité des auteurs. L’utérus étant divisé en 4
quadrants à partir de 2 droites perpendiculaires au niveau de l’ombilic, on additionne les 4
hauteurs verticales des citernes de liquide amniotique les plus profondes. Dans un passé récent,
on distinguait les excès de liquide amniotique (20-25 cm) et les hydramnios vrais (> 25 cm).
Aujourd’hui, un consensus se dégage pour utiliser des courbes d’index amniotique en
percentile, en raison des variations physiologiques du liquide amniotique en fonction de l’âge
gestationnel.
En pratique, les deux techniques, “plus grande citerne” (PGC) et “index amniotique” (IA), sont
également utilisables en dépistage. Leur reproductibilité est bonne, de l’ordre de 0,5-1 cm en
intra-observateur et 1-2 cm en inter-observateur.
La sensibilité de la PGC est probablement meilleure, alors que la spécificité de l’IA est
meilleure.
c. Bilan biologique maternel
Il dépend bien entendu des données de l’examen échographique. Si l’échographie est
considérée comme normale, on pratiquera systématiquement une hyperglycémie provoquée
orale, une recherche d’agglutinines irrégulières, un test de Kleihauer et des sérologies
Parvovirus B19, CMV, herpès. D’autres sérologies pourront être demandées selon le contexte
(toxoplasmose). Devant des signes évocateurs d’anémie, on pratiquera en outre une
électrophorèse de l’hémoglobine si la patiente est d’origine africaine ou du bassin
méditerranéen.
d. Biologie fœtale
L’amniocentèse n’est pas systématique. On la réalisera pour caryotype fœtal dès lors
qu’existent des signes échographiques associés à l’hydramnios. Dans les hydramnios sévères,
et notamment lorsque l’état maternel nécessite la réalisation d’un amniodrainage, un caryotype
sera volontiers réalisé. Dans les hydramnios chroniques modérés, il n’y a pas d’indication
systématique. En cas d’amniocentèse, on fera la recherche d’une fœtopathie infectieuse, et un
dosage de l’alpha-foetoprotéine (AFP) et la réalisation d’une électrophorèse des
acétylcholinestérases (ACE) à la recherche d’une discrète anomalie de fermeture du tube
neural.
4. PRISE EN CHARGE
Devant toute suspicion clinique d’hydramnios, la conduite à tenir du praticien devra être
rythmée par trois interrogations :
- confirmer le diagnostic d’hydramnios,
- rechercher une étiologie maternelle, fœtale ou annexielle et essayer d’établir un pronostic
selon l’étiologie retrouvée,
- prendre en charge cet hydramnios afin d’éviter ces complications, au premier rang
desquelles l’accouchement prématuré.
La prise en charge se conçoit selon deux axes : la prise en charge de l’hydramnios qui peut être
menaçant et/ou gênant pour son propre compte, et la prise en charge de la pathologie retrouvée
le cas échéant.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
107
Prise en charge de la pathologie
Les pathologies fœto-maternelles accessibles à une thérapeutique seront traitées :
- équilibration d’un DID ou d’un diabète gestationnel,
- exsanguino-transfusion in utero en cas d’allo-immunisation fœto-maternelle,
- transfusion in utero en cas d’anémie fœtale secondaire à une infection par Parvovirus B19,
- instauration d’un traitement anti-arythmique en cas de tachyarythmie fœtale.
Une anomalie caryotypique sévère ou une poly-malformation fœtale incurable justifieront
d’accéder à une demande d’interruption médicale de grossesse (IMG).
Prise en charge de l’hydramnios
Un traitement sera indiqué en présence d’une mauvaise tolérance maternelle ou d’un risque
patent d’accouchement prématuré. Il fera appel aux amniodrainages et/ou aux
antiprostaglandines (Indométhacine).
o Amniodrainage
Il permet une normalisation du volume, mais surtout de la pression amniotique responsable des
signes d’intolérance maternelle et du retentissement fœtal. La technique choisie doit permettre
une évacuation rapide d’un volume au moins égal à 1 L, faute de quoi la procédure serait
rapidement inefficace et trop rapidement à refaire. En pratique, on choisira un système aspiratif
doux à l’aide d’un manomètre, branché sur une aiguille fine de 16 gauges par exemple, ou une
évacuation en déclive branchée sur une aiguille plus grosse de 14 gauges. Un repérage
échographique soigneux et continu est nécessaire pour éviter le fœtus et le placenta. Ce geste
nécessite une asepsie rigoureuse, mais ne nécessite pas de couverture antibiotique. Il peut être
utile d’administrer à la patiente au moment de la procédure un tocolytique et une analgésie, en
raison des contractions induites et des douleurs liées à la fuite péritonéale de liquide souvent
observée au décours du drainage. En cas d’hydramnios aigu et en fonction de la pathologie
sous-jacente, il est souvent nécessaire de réaliser des amniodrainages répétés, ce qui majore le
risque d’infections et de ruptures prématurées des membranes.
o Antiprostaglandines
L’indométacine agit par une diminution de la diurèse fœtale. L’hydramnios réapparaît
généralement à l’arrêt du traitement. L’indométacine est plus efficace en présence d’un diabète
maternel, d’obstructions digestives en aval de l’estomac et d’hydramnios idiopathique qu’en
cas de troubles de la déglutition. La posologie proposée est de 100 à 200 mg/jour en cures
courtes (48 h). La prescription doit respecter certaines contre-indications : grossesse dont le
terme est supérieur à 34 SA, contre-indications maternelles aux AINS.
Les bénéfices attendus de l’indométacine sont à mettre en balance avec les risques pour le
fœtus et le nouveau-né : fermeture prématurée du canal artériel responsable d’une hypertension
artérielle pulmonaire, insuffisance rénale, inhibition de l’agrégation plaquettaire, nécrose
ischémique de l’intestin grêle. L’hospitalisation est donc indispensable pendant le traitement
afin d’assurer une surveillance étroite :
- clinique : mesure de la hauteur utérine et enregistrement du rythme cardiaque fœtal
biquotidien,
- échographique : évaluation de la quantité de liquide amniotique bihebdomadaire associée à
une surveillance des flux du canal artériel. La fermeture partielle du canal artériel (5 à 10 %
des cas) impose l’arrêt immédiat du traitement. L’indométacine est toujours arrêté à 34 SA.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
108
L’ACCOUCHEMENT
Lorsqu’il existe une pathologie fœtale, il est souvent utile de programmer l’accouchement.
Compte tenu des complications obstétricales associées à la présence d’un hydramnios, la
connaissance de celui-ci impose de prendre systématiquement des précautions particulières.
o La voie d’accouchement
Ne dépend que de considérations obstétricales. Les indications de césarienne seront en rapport
avec une disproportion fœto-pelvienne, une malformation pouvant être source de dystocie ou
d’anomalies de la présentation. Exceptionnellement, une pathologie relevant d’une prise en
charge très spécialisée pourra nécessiter, outre son transfert vers une structure adaptée, un
accouchement programmé éventuellement au prix d’une césarienne. On retiendra cependant
que la macrosomie, éventuellement méconnue, est associée à la présence d’un hydramnios.
o La dystocie dynamique,
Volontiers associée à la surdistension, pourra être limitée par une ponction de liquide
amniotique préalable au travail, ou par une amniotomie précoce et prudente, ainsi que par
l’administration d’ocytociques.
o Le risque de procidence du cordon lors de la rupture des membranes
Justifie de contrôler la rupture en réalisant une amniotomie précoce et prudente à l’aiguille.
o La fréquence accrue d’hémorragies de la délivrance par atonie utérine
Justifie la pratique d’une délivrance dirigée et d’une surveillance post-partum renforcée.
NB : A la naissance, un examen complet du nouveau-né sera effectué à la recherche d’une
anomalie passée inaperçue en anténatal.
L’examen anatomopathologique des annexes fœtales complète l’enquête étiologique.
II.15. RUPTURE PREMATUREE DES MEMBRANES ou RPM
1. DEFINITIONS
La rupture prématurée des membranes (RPM) est une solution de continuité des membranes
(amnios et chorion) qui précède le travail.
Rupture de la poche amniochoriale : rupture de certaines poches liquides constituées entre
amnios et chorion.
Rupture précoce : c’est une rupture spontanée des membranes survenant au cours du travail
avant la dilatation complète.
Rupture tempestive : c’est une rupture spontanée des membranes à dilatation complète.
Poche des eaux : c’est une hernie des membranes au devant de la présentation qui se forme au
cours du travail d’accouchement
Rupture haute des membranes : c’est une rupture qui se situe à distance du col
2. MECANISMES DE LA RUPTURE DES MEMBRANES
Le sac amniotique est comme une sphère. La tension en un point quelconque peut être
calculée en fonction de la loi de La Place simplifiée : T= P/R
T= tension ; P= pression intra amniotique ; R= rayon de la sphère
La tension nécessaire pour obtenir la rupture est nettement supérieure à la tension créée par
la pression intra-amniotique. D’où l’augmentation de la pression intra-amniotique seule ne
peut expliquer la rupture des membranes, il faudra de ce fait qu’il s’y ajoute une anomalie de
la résistance des membranes.
Les trois mécanismes en cause dans la rupture prématurée des membranes sont :
1) une augmentation de la pression intra-amniotique par des causes mécaniques
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
109
2) une fragilité intrinsèque des membranes (Théorie de Widemann : déficit en vitamine C)
3) une fragilisation habituellement localisée des membranes.
Les deux causes des ruptures prématurées des membranes sont :
a. d’une part, l’altération des membranes (une anomalie localisée de la structure
membranaire au niveau du site de la rupture), c’est le fait d’une amniotite infectieuse en cas
de cervico-vaginite, d’infection urinaire ou d’insuffisance cervico-isthmique.
b. d’autre part, les causes mécaniques qui augmentent le tonus utérin qui fait céder les
membranes à l’endroit où elles présentent une fragilisation à savoir :
o une surdistension utérine par polyhydramnios, grossesses multiples, macrosomie ou par
présentation irrégulière (siège, transversale, composée, face) créant un défaut
d’accommodation.
o par mauvaise placentation (placenta circum vallé ou praevia).
Rupture haute des membranes
La paroi utérine joue un rôle protecteur des membranes. Celles-ci contractent des adhérences
étroites par l’accolement des deux caduques (pariétale et réfléchie). Le clivage ne se produisant
que lors de la formation de la poche des eaux. Dans d’autres cas les adhérences entre les deux
caduques sont serrées ; dans ce cas le jeu de glissement entre membranes et paroi utérine est
perturbé d’où la déchirure des membranes expliquant les cas de rupture haute des
membranes (à distance du col).
3. FACTEURS DE RISQUE D’UNE RPM (selon Allen)
Facteurs évitables Facteurs non évitables
1) cervico-vaginite 1) antécédents de RPM ou d’accouchement
2) insuffisance cervico-isthmique prématuré
3) moyen de diagnostic prénatal 2) hémorragie après le premier trimestre
(choriocenthèse,…) 3) pathologie placentaire (placenta prævia,
4) Malnutrition déficit en vit C, Zn, Cu hématome retro-placentaire, insertion marginale
5) touchers vaginaux du cordon)
6) Tabagisme 4) Grossesses multiples
7) Polyhydramnios (diabète déséquilibré) 5) chirurgie cervicale
4. FACTEURS FAVORISANTS LA RUPTURE PREMATUREE DES MEMBRANES
1) Age maternel avancé
2) Multiparité
3) Niveau socio-économique bas (cas de carence en vitamine C)
4) Profession : la RPM est plus fréquente chez les femmes exerçant un travail pénible (29%
chez les femmes débout, 17% chez les femmes assises)
5) Béance du col
6) Infection cervico-vaginale expliquant une chorioamniotite localisée, d’où l’intérêt du
traitement prophylactique des vaginites
7) Infection urinaire
8) Anomalies de la placentation.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
110
5. PHYSIOPATHOLOGIE DE LA RUPTURE PREMATUREE DES MEMBRANES
Les germes peuvent se propager par voie hématogène et descendante, l’infection préexiste
alors à la RPM. L’origine est souvent urinaire (MERGER). La RPM est consécutive à l’atteinte
du tissus conjonctif fibreux des membranes chorioamniotiques, en particulier du collagène de
type III. Il peut s’agir soit d’une action directe de la collagénase libérée par certains micro-
organismes, soit d’une action indirecte par l’activation des macrophages de la décidua qui
produisent des cytokines stimulant les collagénases (Interleukine 1, Tumor necrosis factor et
interleukine 6) ou qui libèrent l’interleukine 8 activant l’élastase des neutrophiles.
6. PATHOGENIE DE LA RUPTURE PREMATUREE DES MEMBRANES
L’irruption du L.A dans la cavité amniotique entraîne une alcalinisation du vagin, ce qui
entraîne une prolifération des germes qui jusque là étaient peu virulents en raison de l’acidité
du vagin. Par ailleurs, le L.A est un bon milieu de culture. Les germes apparaissent dans le
L.A dans les premières heures qui suivent la RPM. Leur propagation est ascendante souvent
après RPM ou après un travail prolongé.
7. COMPLICATIONS
- Maternelles : chorio-amniotite, endométrite, sepsis, décès maternel
- Fœtales : procidence du cordon, Souffrance fœtale, Mort in utero, présentation
vicieuse, prématurité.
- Néonatales : infection néonatale (méningite, sepsis), hypoplasie pulmonaire,
leucomalacie péri-ventriculaire, décès néonatal.
Facteurs favorisant la survenue de l’infection amniotique en cas de RPM:
1) le temps de latence : au bout de 24 heures de l’ouverture de l’œuf, toutes les études
montrent une augmentation de la fréquence des infections.
2) le nombre de touchers vaginaux
3) la présence dans le liquide du méconium, du sang et l’existence du matériel de cerclage.
Germe le plus rencontré : E. coli, les autres : S. fecalis, Klebsiella, Streptocoque α et β
hémolytiques, staphylocoque, Pseudomonas aeruginosa, Clostridium welchii, les bactéroïdes.
A l’hôpital St Luc (Kisantu), le S. aureus était le germe le plus rencontré au niveau de
l’endocol (40%) suivi de S. epidermidis (25%) puis E. coli (20%) (MAKENGO 2001).
Aux Cliniques Universitaires de Kinshasa, prédominance pour l’E. coli (28%) et Klebsiella
(28%) : germes isolés dans les urines, les lochies et le liquide amniotique (BULEDI 1986).
8. DIAGNOSTIC
a) Clinique
- Anamnèse : perte génitale des liquides (tiède opalescent) retrouvé dans 90% des cas.
- Examen au spéculum : visualisation d’un écoulement cervical. S’il n’est pas spontanément
visible, refouler avec la main sus-pubienne le mobile fœtal (manœuvre de Tarnier).
b) Paraclinique
- FERN test (cristallisation du LA) : mise en évidence d’image de feuilles de fougère sur un
frottis séché à l’air durant 5 à 7 minutes (test le plus fiable). La présence du sang en grande
quantité dénature la formation de fougères. Cette cristallisation est due à la présence du
sodium (Na Cl) dans le liquide amniotique.
- Fibronectine : la présence de cette glycoprotéine permet d’affirmer le diagnostic lorsque le
Fern test est négatif.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
111
- Echographie : la présence d’un oligohydramnios tend à confirmer le diagnostic de RPM.
Cependant une quantité de liquide amniotique normale n’exclut pas le diagnostic (en cas de
fissuration haute des membranes).
- Dans les cas douteux, la patiente sera mise en observation, avec une garniture propre.
- Parfois amnio-infusion avec des colorants intra-amniotiques : l’indigo carmin ou le rouge
congo. Ne jamais utiliser le bleu de méthylène, il provoque les hémolyses chez le fœtus.
9. DIAGNOSTIC DIFFERENTIEL
- RPM - perte involontaire d’urines
- rupture d’une poche amniochoriale - leucorrhée abondante
10. CONDUITE A TENIR
Bilan de départ
Le TV, discutable en dehors du travail, pour certains, n’apporte aucun renseignement
indispensable en plus de l’examen au spéculum et de l’échographie. Il peut cependant
permettre d’exclure une procidence du cordon. On évitera, après ce premier TV, les autres TV,
en dehors du travail. Et même pendant le travail, on évitera dans ce cas les TV intempestifs, en
raison du risque infectieux qu’ils comportent.
La Cardiotocographie peut aider à identifier des contractions utérines infracliniques et des
anomalies de RCF provoquées par une compression funiculaire.
Le bilan infectieux est indispensable :
- prélèvement du LA pour examens microbiologiques ;
- recherches des signes infectieux maternels (leucocytose, VS, CRP réactive, fièvre,
tachycardie, aspect des pertes…).
L’échographie permet la mesure de l’index amniotique ; l’estimation de l’age gestationnel et
du poids fœtal (2 à 20% de sous-estimation en présence d’oligohydramnios), la précision sur la
présentation, ainsi que l’examen morphologique complet du fœtus. La présence d’épisode de
mouvement respiratoire de plus de 30 secondes sur une observation de 30 min permet
d’exclure une infection. L’absence de mouvements respiratoires et corporels est presque
toujours associée à une infection. Enfin, une infection est mise en évidence dans plus de 50%
de cas lorsque les mouvements respiratoires observés durent moins de 30 secondes.
Une ammnio-infusion peut être envisagée.
Traitement proprement dit
Traitement préventif
- Cerclage du col et repos en cas de béance du col.
- Traitement des menaces d’accouchement prématuré.
- Traitement des infections cervico-vaginale.
Traitement curatif
- Toujours Hospitaliser la patiente.
- Quel que soit l’âge gestationnel, la présence d’une infection impose de terminer la grossesse
(tentative de déclenchement du travail ou césarienne selon le cas).
La césarienne se fait sur l’indication obstétricale seulement. Elle doit être entourée de
précaution d’asepsie en cas d’oligo-amnios, l’amnio-infusion pendant le travail permet de
diminuer l’incidence et la sévérité des décélérations. Elle améliore le pH, à la naissance, et
réduit considérablement le taux de césariennes pour souffrance fœtale sans augmenter le
risque infectieux.
- En l’absence d’infection, deux situations se présentent en fonction de l’âge gestationnel :
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
112
après 34 SA (âge de la maturation pulmonaire) : laisser le travail se déclencher (ce qui se
produit dans 80-90% des cas) ; sinon on déclenche le travail au bout de 24 heures ; le
travail sera induit par prostaglandines, car on enregistre beaucoup d’échec avec
l’ocytocine lorsque la grossesse est très jeune ; à défaut de prostaglandines, recourir au
Misoprostol (cytotec®) en utilisant le schéma oral après dilution, si non une perfusion de
glucosé 5% avec 20-40 UI d’ocytocine ;
avant 34 SA, il faut gagner du temps et prolonger la grossesse (en vue de permettre la
maturation pulmonaire) : hospitalisation ; repos au lit ; tocolyse (antispasmodique :
spasfon, papavérine) et bêtamimétiques (salbutamol) ; surveillance fœtale (monitorage,
score biophysique de Manning) ; prévenir l’infection (port des garnitures stériles, hygiène
corporelle, limitation du nombre des TV, contrôle réguliers de température, du pouls,
prélèvement des pertes (écouvillon), surveillance répétée des tests inflammatoires : VS,
GB, FL, fibrogène, si possible la protéine C réactive (CRP), surveiller la qualité des
pertes, l’odeur, ablation de matériel de cercle), usage des antibiotiques ( controversé en
dehors de l’infection, car pouvant sélectionner des germes, mais toutefois
l’antibiothérapie est obligatoirement en cas d’infection vaginale, urinaire ou amniotique).
NB.
La RPM survenant au 2ème trimestre comporte :
- une mortalité néonatale très importante (prématurité) ;
- une mortalité à court et long terme des survivants très élevée (infection) ;
- un risque d’infection maternelle non négligeable ; et étant donné le mauvais pronostic, la
décision doit être prise d’une manière collégiale avec le couple après une information
complète. Toujours songer à la possibilité d’un transfert in utero dans une formation
médicale possédant un service moderne de Néonatologie (Transfert en Afrique du sud, en
Europe, par exemple.
Au sujet de la corticothérapie en cas de RPM, le stress créé au fœtus par la rupture des
membranes accélère la maturation pulmonaire par des sécrétions de corticosurrénales. De
ce fait, l’administration des corticoïdes est jugée superflue lorsque la rupture dure depuis 24
heures. De même, les bêta-mimétiques souvent utilisés pour prolonger ces grossesses ont
une action favorable sur la maturation pulmonaire précoce.
Quant au nouveau-né, il sera pris en charge par le néonatologue s’il est prématuré. Des
prélèvements périphériques seront effectués à la recherche d’une infection (liquide
gastrique, oreille, nez, yeux, urines, anus) afin de traiter correctement l’enfant.
II.16. PROCIDENCE DU CORDON
1. DEFINITION
C'est la chute du cordon ombilical devant la présentation après rupture spontanée ou provoquée
de la poche des eaux. Elle est à différencier :
- du procubitus qui est une procidence du cordon sur membranes intactes, plus rare et moins
dangereuse, car il y a moins de compression et de dissécation cordonales mais qui est une
situation à haut risque de procidence vraie,
- de la latérocidence qui est une descente du cordon entre la paroi utérine ou vagino-pelvienne
et la présentation sans qu'il ne dépasse celle-ci. Elle est responsable de souffrance fœtale
aiguë par compression du cordon.
La procidence du cordon peut être, en fonction du degré de la descente, soit intra-cervicale (ne
dépasse pas l'orifice externe du col) correspondant à la latérocidence, soit intra-vaginale
(cordon dans le vagin), soit vulvaire (cordon à la vulve).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
113
2. ÉPIDEMIOLOGIE
- incidence 0,2-0,6 pour 100 accouchements selon l'inclusion des différents types de procidence,
- mortalité de 10 à 30% selon les équipes.
3. ÉTIOLOGIES
"Une présentation s'adaptant parfaitement au segment inférieur bien formé et au détroit
supérieur non rétréci ne peut engendrer de procidence". La procidence de cordon est donc
favorisée par un défaut d'accommodation fœto-maternelle :
- d'ordre fœtal : les présentations transversales (risque de 5 à 10%), podalique (++ dans les
complets avec un risque de procidence de 11%), céphalique (5%) défléchie haute et mal
accommodée, la grossesse gémellaire (9%), le petit poids fœtal (7% des prématurés), les
malformations fœtales,
- d'ordre maternel : la multiparité (par relâchement des parois utérines), les anomalies du
petit bassin (bassins rétrécis), les tumeurs pelviennes et prævia.
- d'ordre annexiel : l'hydramnios (3%), le placenta prævia avec insertion basse du cordon
(11%), une tumeur, un nœud du cordon ou un excès de longueur de celui-ci (facteur de
risque multiplié par 6 si > à 75 cm).
- La procidence peut être aussi iatrogène (20% des cas) quand la rupture de la poche des
eaux est brutale (10 à 20% des cas), lors d'une tentative de version interne avec refoulement
manuel, d'une VME (2,5% des cas).
4. DIAGNOSTIC CLINIQUE
S'il s'agit d'une procidence vraie, le diagnostic est facile et immédiat car le cordon est perçu au
doigt comme une tige turgescente pulsatile, synchrone au pouls fœtal (à différencier des
vaisseaux maternels). Le diagnostic est moins aisé, lors d'une latérocidence qui est suspectée
devant une bradycardie fœtale ou lors d'un procubitus où l'on perçoit à la palpation une masse
pulsatile dans la poche des eaux sur une présentation haute (diagnostic différentiel : vaisseaux
prævia avec insertion vélamenteuse du cordon). La procidence une fois reconnue, une question
se pose : le cordon bat-il ?
5. CONDUITE A TENIR
Il faut extraire le fœtus rapidement et calmement
- assurer une bonne oxygénation de la mère,
- faire appeler un anesthésiste en urgence,
- présence d'un aide dans la salle d'accouchement,
- selon le type de procidence, la conduite pratique est différente :
1) en cas de procubitus : certaines équipes font d'emblée une césarienne, d'autres préfèrent
l'expectative c'est à dire, mettre la patiente en position de Trendelenburg, attendre la
dilatation complète en surveillant le tracé et la présentation par échographie puis rompre la
poche des eaux et terminer l'accouchement soit par une version manœuvre interne soit par
une manœuvre instrumentale.
2) en cas de latérocidence : le mode d'extraction dépendra du tracé de monitoring et du pH
fœtal. Une perturbation est à considérer comme une souffrance fœtale au cours du travail.
3) en cas de procidence vraie : la conduite à tenir dépendra de l'état fœtal (tracé et
échographie), de la présentation, de la dilatation, et du travail
a. Présentation céphalique : le risque de compression est majeur :
mettre la patiente en position de Trendelenburg,
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
114
maintenir la présentation haute en refoulant manuellement celle-ci et non pas le cordon,
pour éviter toute compression cordonale jusqu'à l'extraction,
contrôler la vitalité fœtale,
si elle est bonne, la voie basse peut alors être acceptée avec extraction du fœtus par une
ventouse ou un forceps (abandonné par beaucoup) ceci d'autant plus qu'il s'agit d'une
multipare et que la présentation est engagée. Cette conduite n'est envisageable que s'il
n'existe pas de dystocie complexe, de bassin rétréci par exemple ou de souffrance fœtale.
Une césarienne ne se discute plus si les cas précités sont présents. Si la dilatation est
incomplète : la césarienne doit être réalisée rapidement d'autant plus qu'il s'agit d'une
primipare âgée, d'une primipare jeune en début de travail ou s'il existe des antécédents
obstétricaux difficiles. Lorsqu'une césarienne est l'attitude choisie, l'aide doit refouler la
présentation par un toucher vaginal appuyé le temps de l'extraction, une compresse humide
peut être posée sur le cordon (3ème degré) et une perfusion de ß mimétiques en IV par bolus
peut être mise en route pour augmenter la perfusion fœtale.
b. Autre présentations :
Épaule : la procidence du cordon doit conduire à une césarienne comme dans le cas d'une
épaule sans procidence (même si la compression cordonale est quasi inexistante dans ce cas),
Siège : si dilatation incomplète, césarienne indiscutable surtout s'il s'agit d'une primipare âgée.
Dans tous les cas, la conduite devra être rapide mais non précipitée. Elle dépendra surtout de
l'état du fœtus. Au moindre signe de souffrance fœtale, la césarienne doit être pratiquée.
La voie basse est actuellement acceptée surtout chez la multipare à dilatation complète avec
une présentation céphalique engagée ou si le fœtus est mort ou non viable.
6. COMPLICATIONS
Le pronostic fœtal dépend :
- de la compression du cordon par la présentation contre la paroi du bassin,
- de la prématurité,
- du délai d'extraction et des manœuvres employées.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
115
PATHOLOGIES LIEES A LA DUREE DE LA GROSSESSE
II.17. MENACE D’ACCOUCHEMENT PREMATURE
1. DEFINITION
La menace d’accouchement prématuré (MAP) survient entre 22 et 36 semaines d’aménorrhée
(SA) révolues et se caractérise par l’association de modifications cervicales et de contractions
utérines régulières et douloureuses qui conduiront à l’accouchement prématuré en l’absence
d’intervention médicale. L’accouchement prématuré peut être soit spontané (2 cas sur 3), soit
provoqué à la suite d’une décision médicale.
On parle de grande prématurité entre 28 et 32 SA et de très grande prématurité avant 28 SA
dans les milieux où la puériculture est très poussée.
L’augmentation des extractions précoces pour pathologie fœtale ou maternelle rendues
possibles par les progrès de la médecine périnatale ; l’augmentation de la fréquence de certains
facteurs de risque, notamment les grossesses multiples liées aux traitements de la stérilité. Le
risque de prématurité est 10 fois plus élevé pour ces enfants que pour ceux nés d’une grossesse
unique.
La menace d’accouchement prématuré est quantitativement la première cause d’hospitalisation
pendant la grossesse en sachant que le risque réel d’accouchements prématurés est très variable
selon les études de la littérature (entre 15 à 50 %).
2. ETIOLOGIES ET FACTEURS DE RISQUE
Les facteurs de risque d’accouchement prématuré de la mère concernent ses conditions socio-
économiques, ses antécédents gynécologiques et obstétricaux, ses conditions de travail et les
circonstances de sa grossesse. Ces facteurs sont résumés dans le coefficient de risque
d’accouchement prématuré établi par Papiernik, présenté dans le tableau 1.
Tableau 1 : Coefficient de risque d’accouchement prématuré (par Papiernik)
Conditions socio-économiques Atcd évocateurs Mode de vie Signes de l’examen
- Deux enfants ou plus sans aide - Un curetage - Travail à l’extérieur - Fatigue inhabituelle
1 familiale - Court intervalle après - Prise de poids excessive
- Conditions socio-économiques grossesse précédente (un an
médiocres entre accouchement et
fécondation)
- Grossesse illégitime non - Deux curetages ou plus - Plus de trois étages - Moins de 5 Kg de prise de poids
2 hospitalisée en maison sans ascenseur - Albuminurie
maternelle Plus de 10 cigarettes - Tension artérielle : maxima
- Moins de 20 ans par jour supérieure à 13 minima supérieur à 8
- Plus de 40 ans
- Mauvaises conditions socio- - Trois curetages ou plus - Long trajet quotidien - Chute de poids le mois précédent
3 économiques - Utérus cylindrique - Efforts inhabituels - Tête trop bas située pour un fœtus loin
- Moins de 20 ans - Travail fatiguant du terme
- Moins de 45 Kg - Grand voyage - Segment < déjà formé à une date
éloignée du terme
- Siège à plus de 7 mois
- Moins de 18 ans - Pyélonéphrite
4 - Métrorragie du 2ème trimestre
- Col court
- Col perméable
- Utérus contractile
- Malformation utérine - Grossesse gémellaire
5 - Un avortement tardif - Placenta praevia
- Un accouchement prématuré - Hydramnios
- Si le CRAP est inférieur à 5 : pas de danger de prématuré
- Si le CRAP est entre 5 et 10 : le risque est potentiel
- Si le CRAP est au dessus de 10 : le risque est certain
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
116
a) Causes utérines
- Béance du col.
- Malformations utérines : utérus hypoplasique ; utérus cloisonné ; utérus double.
- Fibromes utérins.
b) Causes ovulaires
- Grossesses multiples. - Placenta praevia.
- Polyhydramnios. - RPM.
c) Causes générales :
- Syndromes vasculo-rénaux. - Infections.
d) Causes socio-économiques
- Age maternel : < 18ans ; > 35ans. - Grossesses rapprochées.
- Mode de vie : fréquence accrue dans la classe pauvre ; alcoolisme ; longs voyages.
e) Les facteurs professionnels
- Travaux lourds. - Port de charges.
f) Facteurs nutritionnels
g) Causes chirurgicales et iatrogènes
- Chirurgie pendant la grossesse. - Prématurité induite.
h) Causes inconnues ou idiopathiques (50% des cas)
3. DIAGNOSTIC
La démarche diagnostique permet de confirmer la MAP, juger la gravité et préciser l’origine.
Elle repose sur un bilan complet qui doit comporter un interrogatoire pour préciser les
antécédents obstétricaux et rechercher les signes fonctionnels et généraux ; un examen
obstétrical avec l’évaluation des signes physiques ; des examens complémentaires dont
certains aident au diagnostic et d’autres seront utiles pour la recherche d’une étiologie.
Dans certains cas, l’accouchement prématuré est prévisible s’il existe : un facteur permanent
de risque d’accouchement prématuré ; une cause favorisante ; une rupture des membranes ;
enfin, si les modifications cervicales sont évidentes. Des mesures préventives immédiates
s’imposent.
Le plus souvent, la menace d’accouchement prématuré survient de façon inopinée et le
diagnostic est plus difficile, faisant appel aux données cliniques et aux données des examens
complémentaires.
a) Examen clinique
2 critères sont primordiaux : fréquence des contractions utérines (CU) et les modifications du
col utérin. Parler de MAP nécessite présence de CU non dépressibles et douloureuses, d’au
moins une toutes les 10 min et durant plus de 35 s. Elles peuvent être associées à une pesanteur
pelvienne et à une « envie de pousser », voire une sensation d’engagement fœtal. La notion de
facteur déclenchant peut être retrouvée : voyage récent, stress. Les modifications cervicales
sont appréciées par le TV. Il peut s’agir de raccourcissement, d’ouverture ou de changement de
consistance du col. L’ampliation du segment inférieur lié à la descente de la présentation est un
signe supplémentaire. Une hernie de la poche des eaux au travers du canal cervical constitue
un élément de gravité. Les autres éléments cliniques à prendre en compte sont : des lombalgies
périodiques ; des métrorragies plus ou moins intenses ; une RPM ; des diarrhées inexpliquées.
Toutes ces modifications peuvent être isolées ou plus ou moins associées entre elles ; elles sont
d’autant plus graves qu’elles surviennent chez une primipare et plus précocement pendant la
grossesse. Ces modifications permettent d’établir un score de tocolyse : score de Baumgarten
qui tient compte de 4 éléments, chacun étant coté de 0 à 4 : contractions utérines, modifications
cervicales, rupture prématurée des membranes, métrorragies (tableau 2).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
117
Tableau 2 : Indice de menace d’accouchement prématuré (SCORE DE BAUMGARTEN)
0 1 2 3 4
CONTRACTIONS 0 IRREGULIERES REGULIERES
UTERINES
MEMBRANES INTACTES RUPTURE RUPTURE
HAUTE BASSE
METRORRAGIES 0 MODEREES IMPORTANTES
DILATATION DU 0 1 cm 2 cm 3 4 cm
COL cm
SCORE :
≤ 4 : MAP LEGERE TOCOLYSE MINEURE
4 – 6 : MAP MODEREE TOCOLYSE MAJEURE
≥ 7 : MAP SEVERE TOCOLYSE MAJEURE
En pratique, la valeur diagnostique de l’examen clinique est bon dans les cas extrêmes (col très
modifié associé à des contractions utérines régulières ou, à l’inverse, col très peu modifié avec
des contractions rares).
Dans les situations intermédiaires, les plus nombreuses, la prédiction de l’accouchement
prématuré par l’examen clinique est médiocre, et des examens complémentaires semblent
utiles, notamment l’échographie du col utérin et la recherche de fibronectine fœtale dans les
sécrétions vaginales.
b) Examen paraclinique
Tocométrie externe
La tocométrie externe ne permet pas d’améliorer le diagnostic de menace d’accouchement
prématuré, même si elle permet de repérer davantage de contractions utérines.
Échographie du col utérin
Réalisée par voie endovaginale, elle est indispensable en cas de suspicion clinique de menace
d’accouchement prématuré. La longueur cervicale, la largeur de l’orifice interne ainsi que la
protrusion des membranes sont 3 critères à prendre en compte.
Les seuils de longueur cervicale les plus discriminants pour prévoir l’accouchement prématuré
se situent entre 26 et 30 mm.
En cas de signes d’accouchement prématuré, la valeur prédictive négative d’un col long à
l’échographie endovaginale (longueur > 30 mm) est forte. Cette valeur prédictive négative
forte peut permettre de diminuer le nombre d’hospitalisations et de traitements tocolytiques
inutiles.
Recherche de fibronectine fœtale dans les sécrétions vaginales
La fibronectine est une glycoprotéine sécrétée par le trophoblaste et les membranes fœtales.
Elle n’est plus libérée dans les sécrétions vaginales après 22 SA, lorsque les membranes
fusionnent. Elle réapparaît souvent en cas de rupture des membranes, mais aussi en cas
d’inflammation (due à une vaginose bactérienne p. ex.).
La technique fait appel a un écouvillonnage du cul-de-sac vaginal postérieur ou de l’exocol.
L’existence de rapports sexuels ou d’un toucher vaginal dans les 24 dernières heures ainsi que
la présence de métrorragies donnent des résultats faussement positifs.
En l’absence de fibronectine dans les sécrétions vaginales (taux inférieur à 50 ng/mL) chez des
femmes ayant des signes cliniques de menace d’accouchement prématuré, la probabilité d’un
accouchement dans les 14 jours est de 0,5 %, soit une valeur prédictive négative de 99,5 %.
En résumé, en cas de menace d’accouchement prématuré, la valeur diagnostique de
l’échographie et de la fibronectine apparaît supérieure à celle de l’examen clinique.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
118
Si l’on compare la fibronectine et l’échographie, leur valeur diagnostique semble identique.
Par ailleurs, il n’y a pas de preuve de l’avantage d’une association de ces 2 paramètres dans le
diagnostic de menace d’accouchement prématuré.
En cas de positivité de l’un ou de l’autre, le diagnostic de travail prématuré doit être considéré
comme probable et la patiente doit être hospitalisée pour une prise en charge adaptée en
fonction de son terme.
Autres examens complémentaires
Ils sont prescrits à la recherche d’une cause.
- La numération formule sanguine (NFS) recherche une anémie qui semble prédisposer à un
accouchement prématuré pour des taux d’hémoglobine inférieurs à 9 g et une
hyperleucocytose.
- L’examen cytobactériologique des urines (ECBU) recherche une infection urinaire. Le lien
entre une infection urinaire mais aussi une bactériurie asymptomatique (définie par la
présence de 100 000 germes/mL) et une menace d’accouchement prématuré est prouvé. La
bactériurie asymptomatique (3 à 5 % des femmes) doit être traitée en raison du risque de
pyélonéphrite et de prématurité.
- Les prélèvements cervico-vaginaux, en sachant que les infections amniotiques sont souvent
d’origine cervico-vaginale, recherchent des germes pathogènes qui sont retrouvés dans les
menaces d’accouchement prématuré (streptocoque B, E. coli…) et une vaginose bactérienne
en sachant que le risque relatif d’accouchement prématuré chez une patiente présentant à la
fois une MAP et une vaginose est multiplié par 2.
- Des hémocultures sont systématiquement pratiquées dans un contexte fébrile ou de poussée
fébrile résolutive à l’interrogatoire, à la recherche en particulier d’une listériose.
- L’examen échographique permet de déceler une grossesse multiple, un hydramnios, une
malformation fœtale, un placenta prævia, un fibrome. Il permet de réaliser une biométrie
fœtale en accord avec le terme théorique afin d’éliminer un retard de croissance intra-utérin
(RCIU) ou une macrosomie fœtale, s’assure de la présentation fœtale (céphalique, siège,
transverse) et du bien-être fœtal (mouvements actifs, mouvements respiratoires, vélocimétrie
artérielle et veineuse).
- L’enregistrement du rythme cardiaque fœtal permet de juger de la vitalité fœtale.
4. PRISE EN CHARGE
a) Bilan étiologique
C’est notamment la recherche d’un facteur déclenchant, surtout infectieux : paludisme (goutte
épaisse, frottis, test rapides) ; infection urinaire (ECBU) ; infection vaginale (prélèvements
endocervicaux). Les autres examens seront orientés par la clinique.
L’échographie obstétricale a une double visée : étiologique éventuelle (nombre de fœtus,
localisation du placenta) et orientative (biométrie fœtale, morphologie, liquide amniotique
résiduel).
b) Attitudes préventives
- Recherche et suppression des facteurs de risque dès la 1ere consultation.
- Cerclage du col en cas de béance cervico-isthmique démontrée.
- Repos maternel et tocolyse prophylactique avant, pendant et après traumatisme, notamment
chirurgical.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
119
c) Attitudes curatives
- Transfert « in utero » dans un hôpital ayant une unité néonatale adéquate (préférable à un
transfert néonatal). Il faut bien évaluer la situation (parité, état du col, contractions, réponse
à la Tocolyse) avant de prendre une décision de transfert car le pire est évidemment de
devoir précéder à l’accouchement durant le trajet.
- Repos au lit. Il peut, avec une bonne hydratation, suffire dans beaucoup de cas pour faire
cesser les contractions utérines. A ce repos on peut ajouter un anxiolytique du genre Valium
1 à 2 x 10 mg/jour.
- Stimulation de la maturation pulmonaire, moyennant recours aux corticoïdes. Ils diminuent
significativement le risque de syndrome de détresse respiratoire du nouveau né. Le bénéfice
maximum de la cure s’observe 24 heures après le traitement et dure une semaine.:
→ cortisol, prednisolone et prednisone traversent faiblement la barrière placentaire et sont
fortement inactivé par l’enzyme placentaire ==> utilisés dans le T3 des pathologies
maternelles (LED, asthme,…).
→ La dexamethasone et la betamethasone sont faiblement inactivés par l’enzyme 11 beta
hydroxysteroïde déshydrogénase ==> utilisées dans le traitement des pathologies fœtales.
Betamethasone 12 mg en IM à répéter après 24h et Dexamethasone 6 mg en IM toutes les
12h pdt 48h.
- Tocolyse, chaque fois qu’il est raisonnable d’arrêter l’accouchement. La tocolyse n’est pas
raisonnable par exemple dans les situations suivantes (contre-indications de la Tocolyse) :
o pré-éclampsie sévère ; o saignements importants ;
o chorio amniotite ; o Souffrance ;
o décollement placentaire ; o grossesse > 34 semaines.
o malformation fœtale létale ;
a) Les β mimétiques sont très utilisés. Leurs effets β2 stimulants provoquent une relaxation de
la musculature lisse (utérine et artériolaire) et une stimulation de la néoglucogenèse. Tous ils
possèdent des effets β1-stimulants (action inotrophe et chronotrope positive). Leurs effets
secondaires sont : tachycardie ; arythmie (d’où contre-indication si cardiopathie ou ECG
pathologique); nausées et vomissements, constipation ; céphalées ; hyperglycémie (d’où
contre-indication si diabète). On a également décrit des accidents comme œdème
pulmonaire (dans les grossesses multiples + administration de stéroïdes), ischémie
myocardique, tremor, nervosité, hypokaliémie, tachycardie fœtale.
b) L’indométacine, comme inhibitrice des prostaglandines diminue la contraction
myométriale et retarde l’accouchement de plusieurs jours (voie rectale ou orale) : 50 à
100mg par voie rectale, puis dose d’entretien de 25mg toutes les 4 à 6 heures durant 24 à
48 heures (sans dépasser 48heures). Les effets secondaires sont nombreux : ulcère peptique ;
hémorragies ; nausées, vomissements ; diarrhée ; thrombopénie ; allergies ; dyspepsie ;
céphalées. Chez le fœtus, l’indométacine peut provoquer une fermeture partielle du canal
artériel réversible à l’arrêt du traitement. Ce phénomène a peu d’influence sur l’oxygénation
fœtale à court terme. Lors d’usage prolongé, il semble y avoir un risque d’hypertension
pulmonaire. Risque d’oligo-amnios (voir polydramnios). L’insuffisance rénale fœtale est
transitoire et dose dépendante. Enfin, les effets sur l’agrégation plaquettaire peuvent être de
longue durée chez le nouveau-né qui élimine l’indométacine plus lentement que l’adulte. On
peut atténuer l’ampleur des effets secondaires en associant Indométacine et β mimétiques.
c) Les anticaliques, comme nifédipine (Adalat®) inhibent les contractions utérines spontanées
et induites par l’ocytocine : dose initiale de 3co à 10mg par voie orale ; dose d’entretien de
20mg toutes les 8heures durant 3jours puis 20mg 2x/jour. Son action est favorable dans le
cas où d’autres formes de tocolyse sont contre-indiquées. La nifédipine ne doit pas être
utilisée en association avec le sulfate de magnésium (risque d’hypotension). Ses effets
secondaires sont : érythème facial (flush), céphalées, rétention hydrosodée, nausée, allergie.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
120
d) Les antispasmodiques mineurs (Spasfon en perfusion, puis per os ou suppositoires,
Papavérine ampoules injectables, comprimés).
e) Mesures préventives pour une future grossesse.
II.18. L’ACCOUCHEMENT PREMATURE INELUCTABLE OU INEVITABLE
Il peut faire suite à une menace plus au moins longue non jugulée par le traitement, ou peut se
produire d’emblée. L’accouchement prématuré devient inéluctable (inévitable) lorsque :
- les contractions utérines deviennent de plus en plus fréquentes et régulières ;
- la rupture des membres intervient ;
- le col s’ouvre au-delà de 3 cm.
CONDUITE DE L’ACCOUCHEMENT PREMATURE
Les chances de survie des enfants de moins de 900g sont meilleures lors de l’accouchement
par césarienne. En dessous de 600g, la mortalité est telle qu’une césarienne est rarement
justifiée.
Pour les présentations céphaliques de plus de 900g ou plus de 27semaines, la survie est
meilleure par voie basse et la mortalité par maladie des membranes hyalines est plus faible.
Pour les présentations podaliques de moins de 2000g, la survie globale est nettement meilleure
par césarienne. Idéalement la décision concernant le mode d’accouchement doit se baser sur
l’âge gestationnel et le poids fœtal estimé par échographie. Pratiquement les informations
précises sur l’âge gestationnel (échographie précoce) manquent souvent, le critère décisionnel
prépondérant reste le poids de naissance.
- Césarienne pour les sièges de moins de 2000g.
- Pour les accouchements de jumeaux prématurés, la voie basse n’est envisagée que lorsque
les 2 fœtus sont en présentation céphalique.
NB : Une part importante de la prise en charge de l’accouchement prématuré consiste à le
prévenir au moyen d’une surveillance de toute la grossesse, notamment par la recherche des
facteurs étiologiques et par leur traitement éventuel (c’est le cas du cerclage dès qu’une béance
est soupçonnée).
II.19. DEPASSEMENT DE TERME OU PROSSESSE PROLONGEE
1. DEFINITION
Selon l’OMS et la FIGO, on parle de dépassement de terme pour des grossesses de 42
semaines révolues (dépassant 294 jours depuis la date des dernières règles). Il apparaît qu’une
augmentation de la morbidité néonatale s’observe déjà dès la fin de la 41 e semaine, c’est-à-dire
au-delà de 287 jours après la date des dernières règles.
2. FACTEURS FAVORISANTS
- Antécédents de dépassement de terme (risque de récidive =50%).
- Inertie utérine primaire.
- Malformations fœtales (responsables de 25% de la mortalité périnatale observée lors de
dépassement de terme. Au sujet de l’anencéphale : surrénales peu développées par
insuffisance de stimulation hypophysaire. On reconnaît aux surrénales fœtales le rôle dans le
déclenchement du travail).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
121
3. PHYSIOPATHOLOGIE ET COMPLICATIONS
La physiopathologie de la grossesse prolongée ou dépassement de terme est dominée par la
sénescence placentaire. Celle-ci est un phénomène physiologique qui débute normalement vers
la 36ème semaine. Elle est définie comme :
- une densification du stroma villositaire, avec épaississement de la membrane basale ;
- un rapprochement des capillaires vers la périphérie, c’est-à-dire, vers le syncytium ;
- un accroissement de plaques acidophilesdu syncytium, avec accumulation de noyaux en
dehors de ces zones.
On considère aussi généralement que les thromboses intervilleuses et les lésions de nécrose
ischémiques avec dépôt de substance fibrinoïde ou de fibrine, ainsi que la formation
d’’infarctus sont des témoins de la sénesence placentaire. Les précipités calciques souvent
associés au dépôt de substance fibrinoïde ont aussi souvent été pris pour une expression de la
sénescence.
Le problème soulevé par la sénescence placentaire est qu’il reste difficile de faire correspondre
à un âge donné de la grossesse un type de sénescence placentaire et un type de réaction fœtale,
ce qui gêne la prise en charge, puisque des 10% des grossesses prolongées, 1% seulement
posent problème. Et personne ne sait quel enfant se trouvera dans cette situation.
Les risques encourus par le fœtus portent sur :
- le liquide amniotique ; sa réduction entraîne une diminution des mouvements fœtaux et une
augmentation des risques de compression du cordon ombilical (décélérations variables au
monitoring) ;
- la sénescence placentaire responsable de l’hypoxie fœtale chronique, pouvant se terminer par
la mort in utero ; et il est toujours impossible de savoir quelle grossesse prolongée porte un
enfant qui va souffrir, ni si cette souffrance va être vite fatale ou pas ;
- le poids de naissance ; l’incidence des macrosomies est de 3 à 7 fois plus importante (environ
40% des enfants nés après 42 SA dépassent 4000g) et augmente le risque de dystocie des
épaules ;
- la détresse respiratoire néonatale, du fait que la maturité fœtale risque de faire déclencher à
ces enfants le réflexe d’inhalation du liquide amniotique, ce qui s’avérer d’une extrême
gravité si ce liquide est méconial (
- le syndrome de post-maturité ; ce terme s’applique aux enfants présentant un aspect clinique
évoquant une malnutrition intra-utérine (avec risque d’hypoglycémie néonatale).
Selon la classification de CLIFFORD on distingue 3 degrés de ce syndrome de post-maturité :
degré I = modifications des phanères (peau fripée, désquamante, ongles et cheveux
anormalement longs = « fœtus araignée ») ;
degré II = degré I + imprégnation méconiale de la peau et des membres ;
degré III = degré II + coloration jaunâtre de la peau et des annexes fœtales.
La mortalité périnatale est très élevée lorsqu’il y a cœxistence d’un dépassement de terme avec
un RCIU ou une pathologie maternelle.
4. DIAGNOSTIC
Le diagnostic est donc essentiellement anamnestique (chronologique) :
le début des règles est le repère classique ;
la date du rapport fécondant (si possible) ;
la courbe thermique indiquant le moment de l’ovulation ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
122
l’examen clinique en début de grossesse permet une approximation de 2 mois ; plus tard,
l’évolution de la HU ;
l’échographie avant 15SA est le moyen para-clinique le plus précis ;
l’amnioscopie n’apporte qu’un signe de valeur incertaine, la disparition des flocons.
En réalité, à défaut de disposer de repères irréfutables de dépassement de terme, on se contente
de réunir les preuves que la grossesse est au moins à terme, et que l’on ne court pas le risque
de provoquer un accouchement prématuré. Le diagnostic post-natal par l’examen de l’enfant
n’est pas pathognomonique car d’autres affections ont des tableaux similaires.
5. PRISE EN CHARGE
Une fois que le soupçon de grossesse prolongée se précise, il faut apprécier l’état fœtal par
plusieurs tests :
auto-contrôle des mouvements fœtaux (compte MF) ; la diminution des mouvements fœtaux
nécessite des tests diagnostics complémentaires ;
l’enregistrement du RCF (NST), un excellent test de bien-être fœtal ; on peut le rendre plus
sensible par l’épreuve à l’ocytocine (test à l’ocytocine ou OCT = oxytocin challenge test) ;
le profil biophysique de Manning, avec ses 5 points à explorer (MFA à l’écho, Tonus du
fœtus, Mouvements respiratoires fœtaux, Quantité du liquide amniotique, NST).
En pratique, selon notre attitude aux CUK :
expectative entre 40 et 41SA, période au cours de laquelle il faut soumettre le fœtus à la
surveillance soutenue ci-dessus décrite ;
Déclenchement systématique à 41SA révolue.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
123
II.20. RETARD DE CROISSANCE INTRAUTERIN (RCIU) OU YPOTROPHIE
FŒTALE – SOUFFRANCE FŒTALE CHRONIQUE
1. DEFINITION
Le RCIU est une anomalie dynamique de la croissance du fœtus. Il se traduit in utero par un
fœtus de taille insuffisante pour l’âge gestationnel. À la naissance, ce fœtus aura un poids
insuffisant selon des courbes de référence pour l’âge gestationnel.
Il faut 2 points pour juger une dynamique de croissance. Le 1e point est en général donné par
la biométrie de l’échographie du 1e trimestre qui confirme ou corrige l’âge gestationnel obtenu
à partir de la date des dernières règles. Le 2e point révélera l’anomalie de croissance par le
report sur des courbes de référence en fonction de l’âge gestationnel des divers paramètres
biométriques : diamètre bipariétal, périmètres crânien et abdominal, fémur.
Les courbes de référence sont exprimées en percentile ou en déviation standard (DS).
On tend à considérer tout fœtus dont la biométrie à l’échographie est inférieure au 10e
percentile (ou < 2DS) comme suspect de RCIU. En fait, cette définition statistique ne témoigne
pas obligatoirement d’une "pathologie".
On retrouvera en effet en dessous du 10e percentile :
- des enfants constitutionnellement petits avec un poids de naissance directement en relation
avec leur caractéristique génétique
- et des enfants présentant une véritable restriction de croissance. L'important est d'identifier
les fœtus présentant un ralentissement, voire un arrêt de croissance témoignant d'un
processus pathologique, car ce sont eux qui sont à risque de mort in utero ou de souffrance
fœtale chronique.
2. CLASSIFICATION
On distingue deux types de RCIU :
- les RCIU symétriques (harmonieux) qui sont précoces, rapidement sévères, et qui touchent
les paramètres (tête, abdomen, membres) ; ils font craindre une anomalie génétique ; le
RCIU symétrique a une valeur pronostique médiocre ; les troubles du développement
psychomoteur sont plus fréquents lors du RCIU symétrique ;
- les RCIU asymétriques (dysharmonieux), qui surviennent plus tardivement, et touchent au
début les paramètres abdominaux ; ils sont souvent d’origine vasculaire (le fœtus a tendance
à privilégier la vascularisation des organes nobles dont le cerveau, au déterminent du
territoire splanchnique) ; contrairement à ce qui aurait été postulé, la plupart des
malformations chromosomiques entraînent un RCIU asymétrique.
On distingue également divers dégrées de gravité :
- inférieur au 10° percentile = suspicion de RCIU ou RCIU modéré (peu sévère) ;
- inférieur au 5° percentile = RCIU sévère.
3. FACTEURS PREDISPOSANTS (DE RISQUE)
- Antécédent de RCIU - Toxicomanie
- Antécédent de mort in utero - Haute altitude
- Antécédent d’avortement à répétition - Prise de poids insuffisant pendant la
- Bas niveau socio-économique grossesse
- Primiparité - Malformation utérine
- Tabagisme - Petite taille (inférieur à 1,50m)
- Alcoolisme
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
124
- Age maternel (moins de 17 ans, plus de - Anomalies chromosomiques (trisomie
35 ans) 13, 18)
- Maladies cardio-vasculaires - Alpha-foeto-protéine élevé sans lésion
- Maladies chroniques (TBC) du tube neural.
- Facteurs fœtaux de risque
4. ETIOPATHOGENIE
Du point de vue physiopathologique, le RCIU est dû à :
- une diminution des échanges feoto-maternels par diminution quantitative et ou qualitative du
débit sanguin utéro-placentaire ; c’est la situation de pathologies maternelles chroniques
comme l’HTA, l’anémie, la dénutrition, les infections graves) ;
- une faiblesse d’utilisation des nutriments par le fœtus ; c’est le cas des anomalies
(malformations) du fœtus.
Parmi les causes, nous pouvons citer de manière exhaustive des causes maternelles, fœtales et
placentaires.
a) Causes maternelles
- Syndrome vasculo-rénal (HTA gravidique, pré-éclampsie, néphropathies…).
- Anémie, y compris la drépanocytose.
- Tabagisme ; alcoolisme ; toxicomanie.
- Insuffisance cardio-respiratoire.
- Déficit nutritionnel.
- Maladies chroniques (collagenoses).
- Malformations utérines.
- Infection : paludisme, rubéole, toxoplasmose, syphilis…
b) Causes fœtales
- Malformations chromosomiques.
- Malformations non chromosomiques.
c) Causes placentaires
- Insertion vélamenteuse du cordon, nœuds.
- Anomalies placentaires : placenta praevia, infarctus ; placentaires (pigment malarien)
chrorioangiome.
- Grossesses multiples.
- Pathologie dysimmunitaire.
- Infection materno-transmise.
5. DIAGNOSTIC
a) Diagnostic du RCIU
1) Clinique
La mesure de la hauteur utérine (HU) permet d'évaluer la croissance de l'utérus. Dans le
RCIU, elle est plus petite par rapport à celle attendu pour l’âge de la grossesse.
C’est la méthode la plus simple et efficace pour le dépistage du RCIU au cours de la
surveillance de la grossesse normale
4 cm par mois jusqu'à 32 SA : 7 mois = 28 cm = 32 SA,
4 mois = 16 cm, Puis, 2 cm par mois :
5 mois = 20 cm, 8 mois = 30 cm = 36,5 SA,
6 mois = 24cm = 28 SA, 9 mois = 32 cm = 41 SA.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
125
Technique de mesure
Le poids maternel est stationnaire, ou n’évoluant que trop lentement : se rappeler que la croissance
attendue est de 400 gr par semaine.
2) L’échographie
En cas de suspicion clinique de RCIU, ou dans le cadre de surveillance de la croissance fœtale
dans des grossesses à risque de RCIU, la biométrie fœtale réalisée par échographie est la plus
performante. Le périmètre abdominal est isolément le paramètre le plus intéressant.
La méthode la plus recommandée pour dépister et diagnostiquer l’hypotrophie est l’estimation de
poids fœtal (EPF), qui fait appel à plusieurs paramètres biométriques. Dans les grossesses
normales, c’est le plus souvent l’échographie de 32 SA qui permet de détecter les RCIU
cliniquement méconnus ; alors que dans les populations à haut-risque, on recherchera un RCIU
dès 24-26 semaines d’aménorrhée afin de dépister les hypotrophies précoces, rapidement sévères
et présentant un risque de mort in utero.
6. PRISE EN CHARGE
a) Après 34 SA
Il faut déclencher l’accouchement ou la césarienne (le maintien de la grossesse fait courir
beaucoup de risques, sans amélioration de la survie de façon significative).
b) Avant 34 SA
A titre préventif on peut affirmer que l’hypotrophie fœtale d’origine vasculaire peut être prévenue
grâce à un traitement par aspirine (100 mg/jour) de 14SA à 35SA, ainsi que celui par calcium (1-
2gp/jour).
c) Attitude expectative avec surveillance intensive
- Corticothérapie (maturation pulmonaire).
- Evaluation du risque de la mortalité et de la morbidité fœtale sur les paramètres susceptibles de
révéler la sévérité de l’hypotrophie, à savoir :
le caractère symétrique ou asymétrique du RCIU ;
l’importance du retard (<5°percentile = RCIU sévère) ;
l’infléchissement ou arrêt de la croissance ;
la vitalité fœtale (score biophysique de Manning).
- Les explorations Doppler.
- L’existence des malformations associées.
d) Accouchement proprement dit
L’accouchement doit se faire dans un centre ayant en son sein un service de périnatalogie et le
transfert « in utero » est toléré. Le mode d’accouchement est fonction de : la présentation, l’état
cervical, et la quantité de liquide amniotique.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
126
II.21. MORT FŒTALE IN UTERO
1. DEFINITION
La mort fœtale in utero représente souvent un drame mal vécu, parfois incompréhensible. Elle est
considérée comme l’échec du déroulement et de la surveillance de la grossesse. Il est difficile
d’opter pour une définition précise de la MFIU qui soit reconnue mondialement vu que les
conditions d’enregistrement de la mortalité fœtale varient sensiblement selon la période ou le pays
considéré, ce qui soulève le très important problème de compatibilité de statistique de cette
mortalité.
Sa définition varie d’un auteur à un autre. Plusieurs définitions ont été proposées par les auteurs.
Ainsi, J.M.THOULON définit la MFIU comme l’arrêt de toute activité cardiaque du fœtus après
28 semaines d’aménorrhée (180 jours de vie intra-utérine). Il élimine de cette définition les morts
intra partum (morts survenant pendant le travail et l’accouchement) et morts néonatales précoces
sans prendre en considération le poids du fœtus.
H.LERIDON a classé chronologiquement la MFIU en précoce, intermédiaire et tardive en
fonction de l’âge gestationnel, mais vu qu’il est parfois difficile de connaître celui-ci avec
précision, un comité d’experts a recommandé, en 1970, une nouvelle classification reposant sur le
poids de naissance. On parle alors de :
- mort fœtale précoce : survenant avant la 22ème semaine d’aménorrhée ou permettant
l’expulsion d’un fœtus décédé pesant jusqu’à 500g inclus.
- mort fœtale intermédiaire : survenant entre la 22ème et la 28ème semaine d’aménorrhée ou
permettant l’expulsion d’un fœtus décédé pesant de500 à 1000g inclus.
- mort fœtale tardive : survenant à partir de la 28ème semaine d’aménorrhée ou permettant
l’expulsion d’un fœtus décédé pesant >1000g.
Pour éviter les discordances terminologiques et donc statistiques, les experts de l’OMS ont
proposé la définition suivante : “On entend par « mort fœtale », la mort d’un produit de
conception lorsque ce décès est survenu avant l’expulsion ou l’extraction complète du corps de la
mère, indépendamment de la durée de la gestation, le décès est indiqué par le fait qu’après cette
séparation, le fœtus ne respire ni ne manifeste aucun signe de vie tels que le battement du cœur, la
pulsation du cordon ombilical ou la contraction effective d’un muscle soumis à la volonté ”.
Pratiquement aujourd’hui, la plupart des auteurs parlent de mort in utero à partir de 20SA. Pour
les grossesses jeunes < 20 semaines on préfère le terme « missed abortion » qui signifie
« grossesse morte et retenue ».
On cite parmi les facteurs de risque : l’âge maternel (> 35 ans), l’antécédent de MUI, les
conditions socio-économiques défavorables, l’alcoolisme, la toxicomanie, le tabagisme, et les
grossesses multiples.
2. ETIOLOGIE
a) Ovulaire
- Malformations chromosomiques (aneuploïdie, monosomie et trisomie, anomalies de structure
des chromosomes).
- Malformations non chromosomiques (absence de fermeture du tube neural, malformation liée
au diabète, syndrome des brides amniotiques, omphalocèle, laparoschischisis, hydrocéphalie,
malformation cardiaque, nanisme, etc.).
b) Maternelle
Il s’agit de toutes les situations susceptibles d’engendrer la souffrance fœtale chronique ou aiguë :
maladie rhésus (incompatibilité), collagénose (LED), pré-éclampsie, diabète, traumatisme,
cholestase gravidique, infection (parasitaire, bactérienne et virale).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
127
D’autres causes peuvent être envisagées : décollement placentaire, accidents du cordon, RPM et
chorio-amniotite, insuffisance placentaire (ex. dépassement de terme).
Comme pour la souffrance fœtale et le RCIU, dans un grand nombre de cas, aucune étiologie ne
peut être mise en évidence.
3. DIAGNOSTIC
Absence des MFA + BCF absents.
L’échographie confirme l’absence d’activité cardiaque.
Autres signes (radiographiques):
signe de Spalding (chevauchement des os du crâne) ;
signe de Robert (présence de gaz dans le système circulatoire)
angulation pathologique de la colonne vertébrale.
4. PRISE EN CHARGE
Le déclenchement immédiat n’a pas d’avantage par rapport à l’attitude expectative. Il faut 4 à 6
semaines avant l’apparition de troubles de la crase sanguine qui ne s’observent que chez 25% des
patientes.
Souvent confrontées aux problèmes psychologiques et émotionnels de la patiente, la plupart des
femmes n’acceptent pas d’attendre un déclenchement spontané.
En attendant le déclenchement, il faut :
- effectuer un contrôle des tests de coagulation, (temps saignement, Temps coagulation,
fibrinogène) + hémogramme (Hb et Ht);
- avoir du sang frais ;
- préparation psychologique de la maman pour accepter ce qui est arrivé ;
- statuer sur la méthode d’expulsion :
Théobald (perfusion glucosé 5% avec syntocinon 10UI) si col déclenchable ou favorable ;
Misoprostol (voix vaginale ou voie orale après dilution du médicament et administré par micro
doses fractionnées) ; les prostaglandines (PGE2) par voie vaginale (0,5 mg de PGE dans 2 ml
de gel toutes les 2 heures, maximum 6 doses par 24 heures), mais médicament non disponible,
très coûteux ;
Sonde de Foley couplée à la perfusion glucosé 5% avec syntocinon 10 UI si col peu favorable.
Après expulsion :
- discuter l’opportunité d’une révision utérine (aspiration ou curetage) ;
- remplir les documents annonçant le décès (certificat de décès) ;
- ne pas oublier le sevrage (pansement compressif des seins, Vitamine B6 comprimés, Parlodel) ;
- soins habituels du post-partum ;
- établir un programme de recherche étiologique (sérologie, microbiologie, glycorégulation,
etc.).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
128
II.22. EMBOLIE (DU LIQUIDE) AMNIOTIQUE
1. INCIDENCE :
Pathologie rare, ne survenant qu’après rupture des membranes (1 sur 50.000 accouchements),
mais très préoccupante.
2. FACTEURS PREDISPOSANTS
Multiparité, manœuvres obstétricales, polyhydramnios, travail de longue durée, décollement
placentaire, mort « in utero ».
3. PHYSIOPATHOLOGIE
La présence du LA dans la circulation est accompagnée d’une obstruction vasculaire aiguë au
niveau pulmonaire. Elle est due probablement à l’oblitération mécanique, mais aussi à l’action des
prostaglandines amniotiques. Les troubles de la coagulation sont déclenchées par des
thromboplastines amniotiques.
4. CLINIQUE ET DIAGNOSTIC
L’embolie amniotique est accompagnée des manifestations cliniques suivantes : hypertension
pulmonaire aigue, œdème pulmonaire (sans bronchospasme), défaillance cardiaque, cyanose,
hypoxie, convulsion, coma, CIVD et hémorragies.
Il faut donc évoquer ce diagnostic face à toute détresse cardio-respiratoire soudaine survenant
durant le travail ou peu après l’accouchement, chez une patiente par ailleurs en bonne santé.
Chez les patientes qui survivent, pour la plus part du temps, c’est un diagnostic de suspicion.
Même à l’autopsie, un diagnostic de certitude n’est pas toujours possible.
5. PRISE EN CHARGE
Le traitement en soins intensifs :
- intubation avec ventillation (oxygène) ;
- Dopamine ;
- corticoïdes ; hydrocortisone (ampoule 2ml = 100mg) 100mg IV ;
- traitement de CIVD = soutien transfusionnel (culot globulaire, plasma frais congelé,
thrombocytes = plaquettes) ; Héparine discutable (7500UI par 24heures en perfusion IV
continue).
Pronostic : sombre, mortalité maternelle très élevée jusqu’à 85% (dans de bonnes conditions de
travail) dont 25% meurent durant la 1ère heure.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
129
3ème partie : PATHOLOGIES MEDICO-CHIRURGICALES ASSOCIEES A
LA GROSSESSE
I.1. ANEMIE ET GROSSESSE
INTRODUCTION
Le terme anémie désigne un taux d'hémoglobine < 11 g par décilitre de sang durant la grossesse et
par un taux d'hémoglobine < 10 g par décilitre dans la phase du post-partum (après
l'accouchement).
On distingue plusieurs variétés d'anémie de la grossesse (liste non exhaustive) :
L'anémie ferriprive (Anémie microcytaire) qui se caractérise par un déficit en fer (apports
insuffisants avant la grossesse). La conséquence de l'anémie ferriprive chez la mère est une
diminution de la réserve totale du fer chez le nourrisson.
L'anémie par déficit en acide folique (Anémie macrocytaire), moins fréquente que l'anémie
ferriprive.
Les hémoglobinopathies dont il existe plusieurs variétés. Il s'agit essentiellement de la
drépanocytose et de la thalassémie.
INFLUENCES DE LA GROSSESSE SUR L’ANEMIE
La grossesse aggrave les anémies préexistantes dues à une carence nutritionnelle ou au paludisme
par exemple. La grossesse est donc en soi anémiante.
INFLUENCES DE L’ANEMIE SUR LA GROSSESSE
Risque plus accru d’hypoxie fœtale, avec possibilité de RCIU et la mort fœtale in utero. La
carence en acide folique, en vitamine B12, et en fer entraîne le risque de malformations
congénitales (surtout du tube neural). L’hypoxie placentaire va avoir, à la longue, comme
conséquence : avortement, prématurité, RCIU, mort in utero, DPPNI.
ETUDE CLINIQUE
- l’anamnèse : vertiges, fatigue, les palpitations cardiaques ;
- la clinique : pâleur conjonctivale et des muqueuses, dyspnée ou souffle systolique ;
- la paraclinique : Hb < 10 g/dl dans notre milieu et 11 g/dl pour l’OMS (< 8 g/dl = grave) ; bilan
étiologique : GE, ECBU en cas d’infection urinaire gênant l’action de l’érythropoïétine –
examen des selles révélant une parasitose).
Le diagnostic du retentissement : hauteur utérine, échographique.
TRAITEMENT
Préventif
Conseil alimentaire : Consommation de fer (viandes, poissons) ; Usage des activateurs de
l’absorption du fer pendant les repas (fruits) ; Proscrire les inhibiteurs de l’absorption du fer :
les tannins (thé), les polyphénols (mabélé), les fibres (mfumbwa).
Supplémentation en fer et en acide folique : dès fin 1er trimestre : Fer ferreux (40 – 120 mg/j
pendant 12 semaines. Acide folique (3 x 5 mg/j pendant 12 semaines.
Déparasitage sanguin et intestinal : Sulfadoxine-Pyriméthamine en DU (Fansidar 3
comprimés). Prise unique de Vermox 500 mg.
Curatif
Etiologique : C’est selon le résultat du laboratoire (sang, urines, selles).
Symptomatique : Fer ferreux si Hb ≥ 8 g% ; Transfusion si anémie grave après 36ème semaine
(signes fonctionnels : dyspnée, vertiges ; Hb < 7 g%), et retentissement sur le fœtus (RCIU).
En cas d’anémie sévère au 3ème trimestre : accouchement dans une structure capable de réaliser
correctement la délivrance dirigée ou une délivrance artificielle, transfusion si Hb ≤ 8 g/dl, même
si l’anémie est bien tolérée car risque de décompensation avec l’hémorragie de l’accouchement.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
130
I.2. DREPANOCYTOSE ET GROSSESSE
La drépanocytose est une anémie hémolytique héréditaire caractérisée par la survenue de
complications thrombotiques. C’est la polymérisation de l’hémoglobine S à l’état désoxygénée
responsable de la falciformation des globules rouges et de la perte de leur déformabilité qui est à
l’origine de l’augmentation de la viscosité sanguine et donc de la tendance à la thrombose et à
l’ischémie de territoires variés.
INFLUENCES DE LA GROSSESSE SUR LA DREPANOCYTOSE
La grossesse aggrave l’anémie du fait de l’anémie physiologique tendance à l’hypoxie
maternelle fréquence accrue des crises.
La densité du lit vasculaire placentaire (± 40 kilomètres !) lenteur de la circulation sanguine
placentaire = facteur favorisant l’obstruction vasculaire et les crises douloureuses.
Difficultés de diagnostic différentiel avec une infection urinaire, DPPNI, rupture utérine, MFC,
MAP, K.O. compliqué, GEU retard dans la prise en charge de la crise drépanocytaire.
INFLUENCES DE LA DREPANOCYTOSE SUR LA GROSSESSE
Les crises vaso-occlusives = source d’hypoxie = RCIU.
Les crises douloureuses drépanocytaires peuvent masquer une des pathologies ci-dessus évoquées
(diagnostic différentiel difficile) et retarder le traitement d’une vraie pathologie gravidique
accroissement de la morbidité et mortalité chez la drépanocytaire.
ETUDE CLINIQUE
Diagnostic souvent déjà posé dans l’enfance mais parfois aussi au cours de la grossesse (surtout
pour les formes hétérozygotes AS) à partir d’une crise vaso-occlusive ou d’une anémie très grave.
Le diagnostic de la crise chez une personne connue drépanocytaire doit tenir compte de l’existence
de 3 types :
- le type vaso-occlusif (avec micro-infarcissement et parfois lésions d’organes) douleur ;
- le type aplasique (fatigue médullaire) = anémie avec réticulopénie pâleur extrême + asthénie ;
- le type hémolytique (moins fréquent chez l’adulte) marqué par l’ictère.
Le diagnostic différentiel : pathologies gynécologiques et obstétricales déjà évoquées :
- Si douleur abdominale, penser à une crise vaso-occlusive mais sans oublier, selon la situation,
une infection urinaire, DPPNI, rupture utérine, MFC, MAP, K.O. compliqué, GEU ;
- Si pâleur profonde, penser à une crise aplastique, mais sans oublier la pseudo-pâleur gravidique ;
- Si ictère prononcé, penser à une crise hémolytique, mais sans oublier, selon la situation, un
ictère gravidique récidivant, une stéatose aiguë du foie, un paludisme, une hépatite virale.
PRISE EN CHARGE DE LA CRISE VASO-OCCLUSIVE
Suivi par obstétricien et hématologue. CPN plus précoce que pour une grossesse normale et se
feront toutes les 3 semaines. Supplémentation en acide folique et en fer.
Déterminer phénotype de l’Hb paternelle pour déduire le profil génétique possible du fœtus.
Attitudes établies : Hydratation glucosée 5%. Antalgiques et antiagrégants (aspirine, Nootropil,
Pyracétam). Vasodilatateurs (Hydergine). Transfusion. La transfusion a 3 effets principaux :
- diminuer le taux relatif de globules rouges avec hémoglobine S au dessous du seuil de 40% ;
- diminuer l’érythropoïèse maternelle ;
- augmenter la pression partielle en O2, ce qui réduit le risque de falciformation.
Il y a 2 options pour la transfusion :
a) transfusion systématique 1 fois toutes les 2 semaines à partir de la 16ème semaine ;
b) transfusion de manière conjoncturelle (= si urgence), N.B. exsanguino-transfusion de plus en
plus recommandée.
Attitudes conjoncturelles : AB, surtout dans formes aplasiques pour prévenir l’infection. O2, en
cas d’hypoxie. Antipaludique, en cas de paludisme.
Attitudes controversées : Bicarbonates cfr rareté de l’acidose systémique. Perfusions
hypotoniques. Diurétiques.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
131
I.3. DIABETE ET GROSSESSE
Le diabète sucré est une maladie métabolique chronique caractérisée par une hyperglycémie qui
peut s’accompagner des symptômes divers (polydipsie, pollakiurie, polyphagie, asthénie et
amaigrissement). Le diabète gestationnel est un trouble de la tolérance glucidique, de sévérité
variable, débutant ou diagnostiqué pour la première fois pendant la grossesse quelque soit le
traitement et l’évolution dans le post-partum. La différence entre les deux types au cours de la
grossesse est parfois difficile.
RAPPELS PHYSIOLOGIQUES
1. Glycorégulation chez la femme enceinte non diabétique
2 périodes successives : hypo-glycémie initiale puis hyperglycémie à partir du 2 trimestre.
a) 1ère moitié de la grossesse
- l’insulinémie et l’insulinosensibilité augmentent (phase d’anabolisme pour le développement
foetal). la glycémie baisse surtout la nuit et au réveil
b) 2ème moitié de la grossesse
- discrète insulinorésistance favorisée par les hormones placentaires et l’augmentation des
hormones de contre-régulation glycémique)
- diminution de la tolérance au glucose au cours de la grossesse normale : Si fonction
pancréatique normale = adaptation avec hyperinsulinisme réactionnel (surtout en post
prandial), qui permet le maintien de l’euglycémie ; si par contre fonction pancréatique déficiente
l’insulinosécrétion est insuffisante, en particulier en période post-prandiale, c’est le diabète
gestationnel.
2. Glycorégulation chez la femme enceinte à risque de diabète ou diabétique avant la grossesse
a) Variations métaboliques (2 périodes)
- 1 moitié tendance à l’hypoglycémie (phase d’anabolisme) et la cétose
ère
- 2ème moitié (20 SA) : l’insulinosécrétion est insuffisante, en particulier en période post-
prandiale+++ → hyperglycémie si diabète pré-gestationnel ou révélation d’un diabète
gestationnel
• En pratique : chez la femme dont le diabète préexiste à la grossesse : cette augmentation des
besoins en insuline nécessite une adaptation de doses
• En cas de diabète gestationnel la mise en route de l’insulinothérapie est fréquente à cette période
de la grossesse
b) Passage transplacentaire
Passent la barrière hématoplacentaire : Glucose, Corps cétoniques, les acides gras libres, les acides
aminés ; l’insuline ne passe pas la barrière hématoplacentaire
c) Seuil rénal de filtration du glucose
Physiologiquement abaissé, il souligne l’absence totale d’intérêt de la glycosurie
INFLUENCES DE LA GROSSESSE SUR LE DIABETE
La grossesse est diabétogène :
- elle produit des substances qui favorisent l’insulino-résistance, surtout après la 28ème semaine
= éclosion d’un diabète qui était jusque là caché ; moment propice pour le dépistage du
diabète sucré ;
- elle déséquilibre un diabète jusque là bien soigné.
- Elle s’accompagne d’un abaissement du seuil rénal du glucose.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
132
INFLUENCES DU DIABETE SUCRE SUR LA GROSSESSE
Chez la mère
- Aggravation des SYVARE = conséquences maternelles et fœtales ;
- La glucosurie fait de l’urine un milieu de culture microbienne = infections urinaires plus
fréquentes et même parfois graves avec vaginites fongiques;
- Macrosomie fœtale avec complications à l’accouchement = traumatismes (césariennes par
DFP, déchirures des parties molles en cas d’accouchement par voie basse), atonie utérine, avec
hémorragie grave du post-partum).
Au niveau de l’œuf
- Malformations chromosomiques = avortements ;
- L’hyperglycémie fœtale materno-transmise va induire
SFC par intoxication due au glucose ;
MIU, surtout vers la 36ème semaine (jadis appelée « mort subite », lorsqu’on ne savait pas
qu’elle était précédée de SFC) ;
Détresse respiratoire néonatale ;
Glucosurie et polyurie fœtale, responsable de polyhydramnios ;
Hyperinsulinisme fœtal secondaire + hypersécrétion de l’hormone somatotrope par les
cellules gamma du pancréas ; = hypertrophie fœtale + gigantisme fœtal = macrosomie
fœtale qui est responsable de traumatismes maternels signalées et de traumatismes
néonatals (dystocie des épaules avec risque de fracture de membres supérieurs et de
paralysie de membres supérieurs par élongation du plexus brachial) ;
Hyperinsulinisme néonatal résiduel = dysmétabolisme néonatal fait d’hypoglycémie +
hypocalcémie, entraînant parfois la mort du gros bébé.;
Polycytémie (polyglobulie) dont la réduction (par hémolyse) en période néonatale peut être
à la base d’un ictère nucléaire ;
Le contraste entre macrosomie et fragilité fait dire de ces enfants qu’ils sont des « colosses aux
pieds d’argile ».
ETUDE CLINIQUE
2 situations : soit diabète connu, soit découvert au cours de la grossesse.
Diabète est connu
L’histoire des antécédents contient des informations sur les complications du diabète.
Diabète découvert au cours de la grossesse = diabète gestationnel
Dépistage du diabète gestationnel : en présence des facteurs de risques :
- diabète chez les parents au premier degré,
- poids avant la grossesse de 90% ou IMC ≥ 25 kg/m2,
- âge maternel ≥35 ans,
- Antécédents de macrosomie,
- antécédent personnel de diabète,
- antécédent d’avortement spontané à répétition avant 10 semaines ou de MIU inexpliquée ou de
malformation, ou encore de polyhydramnios
Circonstance de découverte :
- hasard à tout moment (glycémie à jeun ≥ 126 mg/dL ou > 7 mmol/L, ou glycémie ≥ 140
mg/dL à 2 heures en post-prandial, ou encore glycémie casuelle ≥ 200mg/dL.
- Test de O’Sullivan : Charge 50 g glucose à n’importe quel moment de la journée avec un
dosage de la glycémie 1 h après. Si la glycémie > 2g/l diagnostic de diabète ; > 1,30 g/l le test
est positif une HGPO doit être réalisée ;
- HGPO : charge 100 g glucose chez une patiente à jeun ; glycémies dosées à 1h, 2h, 3h,
diagnostic de DG 2 chiffres de glycémies sont pathologiques
à jeun : ≥ 0,95 g/l 1h : ≥ 1,80 g/l 2h : ≥ 1,55 g/l 3h : ≥ 1,40 g/l
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
133
Une seule valeur pathologique Intolérance aux hydrates de carbone.
PRISE EN CHARGE
Objectifs
Au cours de la grossesse : obtenir une glycémie à jeun ≤ 95 mg/dl ou une glycémie post-
prandiale ≤ 120 mg/dl.
A l’accouchement : glycémie de 100-150 mg/dl et éviter la dystocie des épaules (césarienne).
Après l’accouchement :
- prévention du diabète si c’est le DGM = Conseil alimentaire + activité physique + Metformine ;
- contrôler tous les 3-6 mois et référer les vraies diabétiques chez diabétologue.
Mesures thérapeutiques
Non médicamenteuses : Conseil alimentaire (éviter sucres simples et graisses ; beaucoup de
résidus comme bananes plantain, les ignames, le maïs, les légumes, les fruits contenant peu de
fructose et beaucoup de fibres) + activité physique (2 km de marche/jour + activité des membres
supérieurs, ex. lessive – vaisselle – repassage – etc pour respecter l’apport sanguin au couple
utérus-foetus).
Médicamenteuses (Metformin 2x500 mg, insuline (posologie variable selon les taux de glycémie)
Attention !
Hospitaliser dès que complication obstétricale (infection urinaire à répétition, polyhydramnios,
pré-éclampsie, souffrance fœtale chronique) ou médicale (nécessité d’augmenter la dose
d’insuline).
Surveillance TA - Fond d’œil.
Collaboration avec internistes et pédiatres.
PREPARATION DE L’ACCOUCHEMENT
Programmation à 36 – 39 semaines, en préparant l’accueil du nouveau-né avec les pédiatres.
Mode d’accouchement = voie basse si dimensions fœtales normales (< 3500 g) et pas de S.F.
Si avant accouchement dose insuline < 10 U.I./jour, mettre 10 UI d’insuline ordinaire dans 1 litre
de glucosé 5%, à faire couler pendant 6-8 heures durant le travail.
Si avant accouchement dose insuline > 10 U.I./jour, il faut, soit la moitié de la dose de la veille (à
donner en 3 prises sous cutanées) + 1 litre de sérum glucosé 5% ; si travail provoqué on ajoute un
2ème litre de glucosé 5% contenant l’ocytocine; soit encore placer 1 l de glucosée 5% + 10 U.I.
Insuline ord. en prévoyant 5-10 U.I. toutes les heures tant que la glycémie est 200 mg/dl.
Après l’accouchement, faire attention à la dose d’insuline (à réduire de moitié!!) + ne pas utiliser
les ADO qui peuvent passer dans le lait et provoquer des hypoglycémies chez le nouveau-né.
Alimentation précoce du NN (car risque d’hypoglycémie).
Contraception définitive après 35 ans ou après la 5ème parité.
Risque après une grossesse avec DGM = Diabète surtout de type 2 définitivement dans 5 – 15 ans
40 – 60% (surtout si obésité et ou usage d’oestro-progestatifs).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
134
I.4. OBESITE ET GROSSESSE
L’obésité = excès pondéral, soit de poids absolu (> 90 kg, ou > poids idéal), soit d’index pondéral
de Quételet (BMI > 25). Elle comporte également un profond trouble métabolique intéressant
surtout les hydrates de carbone et les lipides, et aboutissant à un excès de tissu adipeux. Elle
consiste en 2 éléments successifs :
- une baisse du taux de récepteurs insuliniques au niveau des adipocytes insulino-résistance
hyperinsulinisme HGPO normale ou inversée ;
- un déclin progressif de la sécrétion insulinique (HGPO pathologique).
INFLUENCES DE LA GROSSESSE SUR L’OBESITE
L’insulino-résistance de la grossesse + celle de l’obésité amplification des troubles
métaboliques conduisant vers le diabète gestationnel, et plus tard vers le diabète.
INFLUENCES DE L’OBESITE SUR LA GROSSESSE
Au cours du premier trimestre
Difficultés diagnostiques à cause de l’importance du panicule adipeux qui rend le toucher vaginal
plus laborieux erreurs de terme (d’où l’échographie !).
Troubles du cycle chez les obèses s’ajoute aux difficultés à déterminer l’âge gestationnel.
Au cours de 2eme et 3eme trimestres
Fréquence accrue des syndromes vasculo-rénaux.
Intolérance aux hydrates de carbone.
Infections vaginales et urinaires.
Au cours du travail et de l’accouchement
Erreurs de présentation.
Difficulté d’apprécier correctement les contractions utérines.
Travail prolongé.
Macrosomie fœtale cfr diabète et grossesse.
Difficulté de cicatrisation de plaies éventuelles.
Au cours du post-partum
Risque thrombo-embolique.
ETUDE CLINIQUE
Calculer l'indice de Quetelet ou BMI, défini comme poids (en kg)/taille (en m)2, pour classifier
l’obésité. En 1981, Garrow a proposé la gradation suivante, l’obligation du traitement étant
reconnue à partir du grade II:
PRISE EN CHARGE
Le régime hypocalorique (± 1800 kcal/jour), à fractionner en 4-5 prises pour prévenir les
décharges hyperinsuliniques.
Eviter les sucres à absorption facile, les sauces et les graisses surtout d’origine végétale.
Prise en charge adaptée des complications obstétricales.
Attention aux β-mimétiques qui risquent de mobiliser les substrats glucidiques et graisseux
hyperglycémiques.
Le nouveau-né doit faire l’objet des mêmes précautions à l’accueil que celui de mère diabétique,
qu’il soit macrosome ou pas.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
135
I.5. INFECTION URINAIRE ET GROSSESSE
DEFINITION
La définition de l'infection du tractus urinaire (ITU) est purement bactériologique : c'est
l'existence d'une bactériurie associée de façon obligatoire à une réaction inflammatoire qui se
traduit par la présence de leucocytes dans les urines.
Les formes cliniques les plus rencontrées sont : la Bactériurie asymptomatique, la cystite aigue et
la pyélonéphrite aiguë.
INFLUENCES DE LA GROSSESSE SUR L’INFECTION URINAIRE
Déjà expliquées avec les modifications gravidiques de l’organisme maternel.
INFLUENCES DE L’INFECTION URINAIRE SUR LA GROSSESSE
La prématurité
Diagnostic différentiel difficile avec appendicite, DPPNI, rupture utérine, MFC, MAP, K.O.
compliqué, GEU, étirement d’adhérences génito-pelviennes.
L’infection périnatale ou néonatale, par voie hématogène maternelle.
ETUDE CLINIQUE
pyélonéphrite aiguë :
début le plus souvent brutal :
- survenant habituellement entre les 5e et 7e mois de la grossesse ;
- marqué par une fièvre entre 39°C et 40°C, parfois oscillante, avec frissons et altération de l'état
général ;
les signes fonctionnels orientent vers l'appareil urinaire :
- douleur lombaire dans la majorité des cas à droite, intense, permanente, fréquemment avec
paroxysmes, avec irradiation descendante ;
- parfois douleur iliaque isolée, sur le trajet de l'uretère ;
- associée à des troubles vésicaux : brûlures mictionnelles, pollakiurie... ;
l'examen clinique retrouve une fosse lombaire très douloureuse, ce qui, joint à la grossesse,
gêne la perception d'un contact lombaire. Le toucher vaginal peut retrouver une douleur dans
un cul-de-sac latéral. Les urines sont rares et troubles.
Cystite aiguë
apyrétique ;
se traduisant par des signes vésicaux :
- brûlure mictionnelle, surtout en fin de miction, avec besoin impérieux ;
- pollakiurie variable, moins significative durant la grossesse, de même que les douleurs sus-
pubiennes pendant ou après la miction ;
- moins souvent, hématurie terminale.
Bactériurie asymptomatique
Fréquente, la bactériurie peut survenir dès le 2ème mois de la grossesse.
Elle est décelée à l'ECBU.
Les examens paracliniques urinaires : Le diagnostic repose sur l'examen cytobactériologique
des urines (ECBU). Ils montrent :
- une albuminurie ;
- une pyurie (sédiment urinaire) ;
- une culture positive souvent aux colibacilles sensibles à la Furadantine et/ou à la Gentamycine
et/ou à la Kanamycine. D’autres germes peuvent également être isolés.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
136
Le diagnostic différentiel doit toujours faire penser aux pathologies gynécologiques et
obstétricales déjà évoquées.
PRISE EN CHARGE
Le traitement de l’infection urinaire repose sur 4 points :
- Durée ≥ 7 jours ; si pyélonéphrite aigue : 2-3 semaines, la forme chronique 4-6 semaines ;
- la précision des médicaments à utiliser ; sur base d’antibiogramme ; si non recourir à l’un des
médicaments les plus actifs contre les colibacilles (furadantine 3 x 100 mg/, gentamycine 1 x
160 mg/jour, ou kanamycine 2 x 500 mg/jour) ;
- la prudence à ne déclarer la guérison que si 2-3 cultures reviennent négatives à une semaine
d’intervalle ; si récidive fréquente ou récurrence, bilan pour exclure une anomalie structurale de
l’arbre urinaire ; en cas de pyélonéphrite, la surveillance doit se poursuivre pendant 6 mois ;
- la diurèse qui doit être soutenue par la prise de boissons abondantes ; il peut également être
envisagé d’acidifier l’urine avec du Chlorure d’ammonium ou de la Méthionine (10 g/jour) pour
la rendre hostile aux colibacilles.
La fièvre et les douleurs doivent être combattes avec les antipyrétiques et les analgésiques. Une
attention particulière est à attirer sur le fait que, en fin de grossesse, les sulfamides (cfr
Furadantine) peuvent, par compétition avec la bilirubine, empêcher sa fixation et favorise chez le
fœtus l’apparition d’un ictère nucléaire.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
137
I.6. CARDIOPATHIES ET GROSSESSE
Les maladies cardiaques ne sont pas rares chez la femme enceinte (0,5-1 %). Les cardiopathies
congénitales en constituent la première étiologie, avant les valvulopathies.
La grossesse entraîne une augmentation du débit cardiaque (+ 50 %). Lors du travail obstétrical, il
augmente encore de 10 à 40 %.
Un mauvais statut fonctionnel (stades NYHA III-IV), HTAP ou cardiopathie obstructive sévère
sont hautement prédictifs de complications graves (trouble du rythme, défaillance cardiaque,
accident thrombo-embolique) et de décès. La morbi-mortalité fœtale est également très élevée
dans ces situations.
Si la maladie cardiaque est contrôlée, l'accouchement par voie basse est souvent la meilleure
option. En revanche, une atteinte aortique menaçante (dissection, dilatation) ou une HTAP sévère
imposent l'extraction par césarienne.
La prise en charge d'une femme enceinte ayant une cardiopathie est multidisciplinaire et doit être
menée dans un centre spécialisé, permettant la réanimation de la mère et de l'enfant.
INFLUENCES DE LA GROSSESSE SUR LES CARDIOPATHIES
Surcroît de charge hémodynamique (+ 50%), du fait de l'augmentation du volume de sang
circulantfatigue du cœur.
Les maladies hypertensives de la grossessecomplication d’une cardiopathie préexistante.
Hypercoagulabilité sanguine due à l’hyperlipidémie gravidique + la synthèse accrue de facteurs de
coagulation. Si on ajoute le risque variqueux qui est augmenté au cours de la grossesse, on obtient
un accroissement du risque thromboembolique.
L’hémorragie de fin de grossesse comporte un risque de décompensation cardiaque d’une
cardiopathie qui était bien tolérée jusque là.
Le recours à des médicaments typiquement obstétricaux (ex.β-mimétiques) effets sur le cœur.
Les efforts expulsifs de la période d’accouchement peuvent hypoxie du myocarde.
Le vidange de l’utérus à l’accouchement grand appel de sang (a vacuo) vers le territoire
splanchnique (= au niveau de l’abdomen), réduisant gravement l’irrigation du myocarde. Sur un
système cardio-vasculaire déficient, la spoliation sanguine au niveau du cœur peut être telle qu’un
véritable choc peut en résulter : c’est le choc splanchnique.
La plaie cavitaire, élément clé du post-partum, renferme un risque important de greffe bactérienne
sur un cœur malade (Osler). Ce temps constitue donc une occasion propice des poussées
évolutives des cardiopathies, et le terrain favorable des complications thromboemboliques.
Il faut enfin signaler la cardiomyopathie péripartale dont on sait la fréquence particulièrement
accrue autour de l’accouchement, sans qu’on en ait trouvé l’explication.
INFLUENCES DES CARDIOPATHIES SUR LA GROSSESSE
Toxicité sur le fœtus de certaines drogues administrées à la mère cardiopathe. C’est le cas des
digitaliques, capables de se retrouver chez le fœtus.
Prématurité induite dont la fréquence est accrue du fait de l’obligation que l’on a parfois
d’interrompre la grossesse à cause de l’aggravation de l’état maternel.
ETUDE CLINIQUE
Le diagnostic positif d’une cardiopathie au cours de la grossesse repose sur les plaintes et
signes cardiaques.
- Plaintes:
Dyspnée Haleine courte
Palpitations cardiaques Précordialgies
La sévérité de ces symptômes est fonction du type et de l'importance de la cardiopathie.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
138
- Examen clinique
Inspection : éréthisme cardiaque
Palpation : trouble du rythme cardiaque
Auscultation : souffle cardiaque avec parfois un Thrill
Le diagnostic de la gravité fonctionnelle conditionne le pronostic aussi bien de la cardiopathie
que de la grossesse elle-même. Il s’effectue à travers le schéma de classification proposée par la
N.Y. Heart Association.
PRISE EN CHARGE
La prise en charge d’une cardiopathie au cours de grossesse repose sur 9 principes :
- repos et diète (régime hyposodé ou désodé dès la classe III) ;
- éviter et prévenir l’anémie, les β-mimétiques et la scopolamine ;
- petites doses de Pénicilline G retard (Extencilline) au long de la grossesse pour prévenir la
réactivation du R.A.A. et de la myocardite ;
- accouchement sans douleur par anesthésie péridurale (pour réduire le stress et éviter les efforts
expulsifs) + raccourcissement de l’expulsion (ventouse ou forceps) ;
- délivrance assistée ou tout simplement GATPA (pour limiter les pertes sanguines) ;
- pose d’un sac de sable (± 2 kg) sur le ventre (4-6 heures) afin de prévenir un choc splanchnique ;
- pas d’allaitement si classe III ;
- lever précoce pour limiter le risque thromboembolique ;
- limitation de naissances, étant donné que tout antécédent de décompensation cardiaque au cours
de la grossesse comporte un risque fort élevé de récurrence (stérilisation définitive si classe III).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
139
I.7. PNEUMOPATHIES ET GROSSESSE
La fonction pulmonaire maternelle est bien protégée au cours de la grossesse. Sauf atteinte
particulière des poumons, pas de grande influence de la grossesse sur les pneumopathies.
INFLUENCES DES PNEUMOPATHIES (GRAVES) SUR LA GROSSESSE
Baisse de la surface d’hématose maternelle hypoxie hypotrophie fœtale.
Toux persistante déclenchement des contractions utérines.
Les Radiographies diagnostic au premier trimestre risque de tératogenicité pour le fœtus.
Contagion néonatale surtout en cas de tuberculose ouverte.
En cas de césarienne, limite aux possibilités anesthésiques si pneumopathies graves.
ETUDE CLINIQUE + ATTITUDES THERAPEUTIQUES
Cette rubrique ne concernera que la tuberculose et l’asthme.
Pour la tuberculose :
- Attention à l’ototoxicité fœtale des aminosides, surtout si donnés de façon prolongée ;
- l’isolement du nouveau-né en cas tuberculose ouverte ;
- l’allaitement pouvant s’avérer épuisant pour la mère, est à éviter dans les formes sévères ;
- les signes inflammatoires doivent être recherchés chez le nouveau-né ; si présents de façon plus
moins nette, démarrer d’emblée un traitement aux tuberculostatiques chez l’enfant.
Pour l’asthme :
- faire attention à l’effet que peuvent avoir des médicaments comme l’adrénaline et les
corticoïdes, non seulement sur le risque tératogène et hémorragique, mais aussi sur l’apparition
ou l’aggravation des syndromes vasculo-rénaux ;
- lorsqu’une anesthésie est nécessaire, priorité est accordée à l’anesthésie épidurale ; si, malgré
tout, une anesthésie générale est requise, il faut recourir au cyclopropane.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
140
I.8. HEPATOPATHIES ET GROSSESSE
La fonction hépatique subit une forte surcharge métabolique au cours de la grossesse. Il existe des
atteintes hépatiques spécifiques de la grossesse (cholestase intra-hépatique, stéatose aiguë
gravidique, hépatopathie associée à l’hyperémèse gravidique, ainsi que l’hépatopathie associée à
la toxémie gravidique) et d’autres non spécifiques, parce qu’elles se rencontrent de façon fortuite
au cours de la grossesse ; c’est le cas de l’hépatite virale.
INFLUENCES DE LA GROSSESSE SUR LES HEPATOPATHIES
C’est essentiellement la prédisposition à la cholélithiase et à la cholécystite, ainsi qu’à
l’augmentation de la concentration de fibrinogène.
INFLUENCES DES HEPATOPATHIES SUR LA GROSSESSE
La première influence s’exerce par le biais de la toxicose maternelle avortement ;
prématurité ; RCIU. La deuxième influence concerne le risque de contamination fœtale ; c’est le
cas de l’hépatite virale.
ETUDE CLINIQUE
Nous ne présentons que les 2 grandes hépatopathies spécifiques de la grossesse, à savoir :
cholestase intra-hépatique, stéatose aiguë gravidique.
LA CHOLESTASE INTRA-HEPATIQUE DE GROSSESSE
Elle apparaît au 3ème trimestre (entre la 28ème et la 32ème semaine), sans notion de contamination
microbienne ou virale, ni de prise médicamenteuse suspecte (Tétracycline).
Sa pathogénie consiste en une rétention intra-hépatique de sels biliaires, donnant lieu à :
- un prurit intense (lésions de grattag) , sans fièvre, ni douleur hépatique ;
- des troubles digestifs (diarrhées et constipations) ;
- rarement un ictère qui apparaît alors 1 – 2 semaines après le début du prurit.
Sa biologie est marquée par des taux de phosphatases alcalines élevés (normal = 0 à 5,5 U/L),
transaminases normaux (SGOT et SGPT) ; des taux de bilirubine (directe) modérément élevés.
Son évolution comporte 3 caractéristiques principales :
- pas de régression avant l’accouchement ;
- pronostic maternel favorable, mais pronostic fœtal réservé (avortement, prématurité, RCIU) ;
- récidive dans 40 – 60% des cas au cours des grossesses ultérieures, ce qui prédispose alors aux
calculs biliaires ; cette marque a conféré à cette maladie le nom de Ictère gravidique récidivant.
Diagnostic différentiel : paludisme, hépatite virale et hépatite toxique.
Son traitement est symptomatique (Phénobarbital + Cholestyramine + Bilagol). Parfois, une
hospitalisation est requise pour surveiller étroitement l’état ovulaire.
LA STEATOSE AIGUE GRAVIDIQUE
On en distingue 2 sortes : une idiopathique, plus fréquente, qui apparaît au 3ème trimestre (entre la
28ème et la 32ème semaine), et une autre iatrogène et toxique, résultant de l’inhibition de la
synthèse protéique hépatique par des fortes doses de Tétracycline, et qui peut donc apparaître à
n’importe quel âge de la grossesse, ou même en dehors de la grossesse.
Sa pathogénie consiste en une inhibition de la synthèse protéique hépatique par des fortes doses
de Tétracycline, donnant lieu à un ictère évolutif, des douleurs épigastriques et lombaires, une
anorexie, des nausées et vomissements, une tachycardie. Le prurit y est rare. Parfois atteinte rénale
sévère d’emblée avec anurie. Le tableau peut même compter des diathèses hémorragiques.
Biologie : phosphatases alcalines normales, transaminases (SGOT et SGPT) élevés, bilirubine
(essentiellement directe) élevés.
Son pronostic est grave, aussi bien pour la mère que pour le fœtus.
Diagnostic différentiel : paludisme grave, hépatite virale sévère, empoisonnement, un HELLP
Syndrome, et même une crise drépanocytaire.
Son traitement est symptomatique.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
141
I.9. HYPEREMESE ET GROSSESSE
Les vomissements de la grossesse sont un signe banal faisant même partie des signes
« sympathiques » de la grossesse. Ils sont généralement accompagnés de sialorrhées et de nausées,
et se rencontrent surtout le matin, avec prédominance chez les primigestes. Il s’agit d’un
dérèglement fonctionnel déclenché par la présente de l’œuf fécondé.
Normalement, ces vomissements se manifestent vers la 4 - 6ème semaine et disparaissent vers la
14-16ème semaine, bien qu’on puisse parfois les observer jusqu’à terme. Ils sont provoqués par les
odeurs fortes. Leur contenu est variable : muqueux le matin après réveil, bilieux la journée, et
alimentaire après repas. Ils surviennent sans effort, sans intervalle de temps libre après le repas, et
ne s’accompagnent pas d’une vidange complète de l’estomac.
C’est lorsqu’ils deviennent trop fréquents et abondants qu’ils entraînent une dénutrition et
constituent alors une vraie maladie appelée Hyperémèse gravidique ou Hyperemesis gravidarum
ou Vomissements incoercibles ou encore Gestose émétisante.
INFLUENCES DE LA GROSSESSE SUR L’HYPEREMESE
2 pôles : un pôle nerveux, et un pôle ovulaire.
- Instabilité neuropsychique : les vomissements représentent dans ce cas une façon pour la
gestante d’attirer l’attention de son entourage sur elle.
- L’œuf fécondé sécrète de l’HCG qui induit un dérèglement fonctionnel de tout l’organisme.
INFLUENCES DE L’HYPEREMESE SUR LA GROSSESSE
Sur la mère
- déshydratation et troubles électrolytiques (hypokaliémie + hyponatrémie + hypochlorémie),
avec, dans les cas extrêmes, une insuffisance rénale et hépatique, ainsi qu’un décollement de la
rétine.
- Jeûne dénutrition de type hypoglycémique et hypoprotéique lypolyse compensatoire.
adipeuse (amaigrissement), et surtout, d’une production accrue de corps cétoniques = acidose
métabolique. A l’ombre d’un jeûne, une hypovitaminose (surtout B) touchant particulièrement la
vitamine B1 l’organisme va alors manquer un important facteur de la myélinisation des fibres
nerveuses, d’où les troubles neuro-psychiques qui vont entretenir le cercle vicieux de la maladie.
La polynévrite qui se manifeste dans le contexte de cette pathologie porte le nom de MALADIE
de WINIKOFF-KORSAKOFF. Par ailleurs, la carence en vitamine C, K, et en prothrombine va
déterminer des diathèses hémorragiques.
Sur l’œuf
Les effets sont plus tardifs : RCIU.
ETUDE CLINIQUE
Diagnostic aisé :
- vomissements déclenchés par toutes sortes d’aliments ;
- dénutrition ;
- prostration.
Score d’évaluation:
- durée de vomissements = 1 pour ≥ 5 jours ; 2 pour 6-7 jours ; 3 pour > 7 jours ;
- nombre de vomissements par jour = 1 pour ≤ 4 fois/jour ; 2 pour 5-7 fois/jour ; 5 pour 8-
9/jour ; 7 pour ≥ 10 fois/jour ;
- perte de poids = 2 pour < 2 kg ; 4 pour 2-4 kg ; 6 pour ≥ 5 kg ;
- acétonurie = 1 si positif à 1 + ; 2 si positif à ++ ;
- déshydratation = 1 pour un taux d’hématocrite ≤ 39% ; et 2 pour un taux > 39%.
Le score est dit modéré entre 6 et 12 ; il est sévère entre 13 et 20.
Paraclinique :
- hémoconcentration (Hb, Hc, GR) ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
142
- acidose métabolique (acétonurie, ionogramme, réserve alcaline) ;
- atteinte générale (prothrombine, fibrinogène, protidémie) ;
- le fond d’œil.
Son diagnostic différentiel:
- grossesse môlaire ;
- Trouble gastro-intestinale (gastrite, parasitose, ulcère gastro-duodénal, hernie hiatale).
PRISE EN CHARGE
Le traitement étiologique
Il s’attaque aux 2 pôles neuropsychique et ovulaire déjà évoqués.
Pour le pôle neuropsychique :
- repos dans l’isolement ;
- sédatifs;
- une psychothérapie.
Pour le pôle ovulaire, l’arrêt de la grossesse dans 2 situations : môle hydatiforme et aggravation
de l’état maternel (Ictère, oligurie, diathèse hémorragique, anomalies du fond d’oeil).
Le traitement symptomatique
Il comprend :
- repos digestif d’au - 48 heures ; puis reprise alimentaire avec des aliments secs (ex. biscuits) ;
- alimentation parentérale avec des perfusions glucosées hypertoniques parfois ponctuées de 5
U.I. d’insuline ;
- correction de troubles électrolytiques ;
- supplémentation en vitamine, surtout en vitamine B1 ;
- anti-émétiques (Primpréran®, Vogalène®).
NB : Si épine irritative (parasitoses intestinales, gastrite), appliquer actions spécifiques.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
143
I.10. APPENDICITE ET GROSSESSE
L’appendicite est une infection, généralement bactérienne, de l’appendice, consécutive à
l’obstruction de la lumière appendiculaire.
INFLUENCES DE LA GROSSESSE SUR L’APPENDICITE
- Déplacement de l’appendice vers le haut, en arrière de l’utérus gravide (modification
topographique) examen clinique plus compliqué et diagnostic plus difficile, car le point de
Mc Burney n’est plus évident ; abord et acte opératoire plus laborieux.
- Hypervascularisation pelvienne de la grossesse + l’accroissement du drainage lymphatique
favorisent la dissémination microbienne, la gangrène et la rupture de l’appendice.
- Montée du grand épiploon qui laisse l’appendice à découvert pas de possibilité de
cloisonnement en cas de gangrène et de rupture, ce qui favorise alors la péritonite.
- L’abaissement brusque de la masse utérine après l’expulsion du fœtus provoque un
« repositionnement » de l’appendice libération éventuel du cloisonnement du processus
inflammatoire autour de l’appendice. Une péritonite peut alors se généraliser en post-partum.
INFLUENCES DE L’APPENDICITE SUR LA GROSSESSE
- Déclenchement des contractions utérines avortement ou accouchement prématuré.
- Appendicectomie au cours de la grossesse constitue un stress locorégional et général pouvant
avoir les mêmes effets sur la motilité utérine.
- Incision médiane disproportionnée par rapport à l’idée que l’on se fait d’une plaie
d’appendicectomie.
- Cicatrisation définitive gênée et longtemps douloureuse du fait de la poussée de la croissance
utérine.
- Si appendicectomie près du terme (≥ 36 semaines) risque de césarienne.
ETUDE CLINIQUE
Le diagnostic de l’appendicite repose sur une anamnèse précise quant à la localisation et la
persistance, l’évolution de cette douleur ; cette douleur est progressive, sans rémission véritable, et
s’accompagne parfois de nausées, vomissements et constipation. La recherche de cette localisation
doit tenir compte des modifications topographiques déjà mentionnées..
Diagnostic différentiel :
- Sphère digestif : néoplasmes, diverticulite, parasitoses intestinales, occlusion intestinale ;
- Sphère génito-urinaire : kyste ovarien compliqué, MFC ou MAP, DPPNI, infection urinaire,
calcul urinaire, pyélonéphrite ;
- Systémique : pneumonie avec irritation diaphragmatique suivie d’irradiation abdominale de la
douleur. .
PRISE EN CHARGE
Le traitement est chirurgical, urgent et s’effectue par une laparotomie médiane sous-ombilicale, si
la grossesse est au-delà du premier trimestre. Il doit comprendre les précautions suivantes :
- chercher la collaboration de l’interniste et du chirurgien pour asseoir le diagnostic ;
- mettre en place une tocolyse dès que diagnostic est posé ; poursuivre cette tocolyse pendant
l’opération et durant les 10 jours qui suivent cette intervention ; mesure valable que s’il n’est pas
prévu de pratiquer une césarienne au décours de l’appendicectomie;
- administrer des gestagènes (Progestérone, Proluton, Utrogestan) si la grossesse est encore au 1er
et début 2ème trimestre).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
144
I.11. NEPHROPATHIES ET GROSSESSE
Les néphropathies de la grossesse se présentent sous 3 formes qui, toutes, menacent la vie de la
mère du fait de la diminution de la fonction rénale : formes glomérulaires ; formes vasculaires ;
formes polykystiques.
Le pronostic est tributaire de l’existence ou non de l’hypertension artérielle. Le critère d’atteinte
fonctionnelle est représenté par le taux de créatinine sérique. C’est lui qui détermine
l’autorisation ou non, ainsi que la poursuite ou non de la grossesse. Il n’existe cependant pas de
degré type d’atteinte rénale à partir duquel ces décisions peuvent se prendre. Signe particulier
d’aggravation = apparition d’une insuffisance rénale.
INFLUENCES DE LA GROSSESSE SUR LES NEPHROPATHIES
L’état gravidique prédispose à l’atteinte rénale par insuffisance rénale à travers les situations
suivantes :
- hémorragie, soit au cours de la grossesse, soit en fin ;
- syndromes vasculo-rénaux ;
- infection ;
- attitudes thérapeutiques (médicaments néphrotoxiques, accidents transfusionnels, excès
d’ocytociques cfr effet ADH).
Au cours de la grossesse, les néphropathies préexistantes présentent un léger risque
d’aggravation.
La protéinurie des glomérulonéphrites peut augmenter et accentuer l’œdème par le biais de
l’hypoalbuminémie consécutive.
INFLUENCES DES NEPHROPATHIES SUR LA GROSSESSE
Sont fonction de la présence / apparition ou non d’une insuffisance rénale troubles
hydroélectrolytiques, avec acidose métabolique ; cytolyse tissulaire provoquant de
l’hyperkaliémie (mortalité fœtale de près de 100%). Si pas d’insuffisance rénale, l’HTA
facilement contrôlable.
Les néphropathies protéinuriques entraînent une hypoprotéinémie responsable d’un RCIU.
PRISE EN CHARGE
Le traitement est causal + fluides + électrolytes + protéines alimentaires.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
145
I.12. VASCULOPATHIES AUTRES QUE HTA ET GROSSESSE
Il s’agit des phénomènes de thrombo-embolisation. Leur pathogénie se résume en 2 mots : stase
sanguine.
Le risque est le plus marqué en post-partum, notamment les 30 premiers jours. Les situations
prédisposant à l’aggravation de la stase sanguine sont :
- l’obésité ; - les syndromes vasculo-rénaux ;
- les varices ; - le travail prolongé.
- les cardiopathies préexistantes ;
La complication la plus redoutable en est l’embolie.
INFLUENCES DE LA GROSSESSE SUR LES TROUBLES THROMBO-
EMBOLIQUES
La grossesse réalise une situation propice à la thrombo-embolisation, protectrice contre le
danger hémorragique.
INFLUENCES DE TROUBLES THROMBO-EMBOLIQUES SUR LA GROSSESSE
En dehors du contexte post-partal, c’est le syndrome de la coagulation vasculaire disséminée.
ETUDE CLINIQUE
Elle comporte 3 formes principales : la thrombophlébite ; l’embolie ; l’afibrinogénémie.
La thrombophlébite est plus fréquente sur terrain de varices de la vulve et des membres
inférieurs. Manifestation : douleurs souvent au niveau des membres inférieurs (creux
poplitée) + fièvre et frisson + œdème inflammatoire du membre concerné + induration
turgescente du trajet veineux concerné.
L’embolie : drame pulmonaire, cérébral et cardiaque, qui menace la vie de la mère.
L’afibrinogénémie : drame hémorragique (cfr DPPNI).
PRISE EN CHARGE
Le traitement préventif :
- soins appropriés des varices (bas spéciaux, bandes élastiques de type Velpeau, veino-
toniques genre Daflon®, Phlébodia®, Venoruton®, Glyvénol®) ;
- Aspirine (= anti-agrégant plaquettaire) ;
- lever précoce.
Le traitement curatif : AB + Anti-inflammatoires + anticoagulant sanguine, à savoir :
Héparine : 1 ml = 50 mg = 5000 UI.
Début du traitement en i.v. à 5-7 mg/kg/jour, avec comme dose de départ le 1/12 ème de la
dose du jour ; exemple une femme de 70 kg 5 mg/kg/j = 350 mg/j = 1ère injection = 30
mg i.v.
les autres doses sont à adapter aux temps de Howell (TH) et de céphaline-kaolin (TCK)
pratiqués juste avant l’injection (cfr biologie clinique).
En cas de survenue d’une hémorragie, injecter le Sulfate de protamine à la dose de 0,5 mg/kg,
renouvelable au besoin après 20 minutes. En cas de travail, il faut diviser la dose de chaque
injection par 2 ou 3 jusqu’à 12 heures après l’accouchement.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
146
I.13. IST ET GROSSESSE
Les Infections sexuellement transmises ou I.S.T. sont celles qui sont principalement ou
secondairement transmises par voie sexuelle. Le terme « Infections» a remplacé celui de
« maladies » parce qu’il s’agit d’affection parfois sans manifestation clinique.
L’agent causal est soit bactérien (gonocoque - haemophilus vaginalis - chlamydia
trachomatis - etc), soit fongique (candida albicans), soit protozoaire (trichomonas vaginalis),
soit viral (herpès-virus type 2, virus du lymphogranulome vénérien, cytomegalovirus, virus
du condylome acuminé, virus de l’hépatite B, HIV). La contamination se fait avant ou
pendant la grossesse.
INFLUENCES DE LA GROSSESSE SUR LES I.S.T.
La grossesse favorise le développement microbien à cause de :
- l’humidité vulvo-vaginale particulière au cours de la grossesse ;
- la tendance à la fatigue de la grossesse ↓ vigilance de la femme aux pratiques
hygiéniques;
- l’immunodéficience de la grossesse, susceptible d’aggraver les lésions.
INFLUENCES DES I.S.T. SUR LA GROSSESSE
Au cours de la grossesse, la part des IST à la morbi-mortalité materno-périnatale provient
de :
- la toxicose maternelle (la mère intoxique le fœtus) via la fièvre et les médicaments
nécessités par l’infection en question ;
- l’hyponutrition maternelle RCIU;
- la contamination ovulaire avortement tardif, hyperplacentose, malformations
congénitales, polyhydramnios, prématurité, souffrance foetale, et MIU ; la potentialité de
transmission verticale du Sida (mère vers enfant) par l`exposition muqueuse, voie
transplacentaire (surtout si chorio-amniotite, RPM, lésions placentaires, contamination
ascendante) et voie orale (lait dans les 2 premiers mois);
- la fragilisation du pôle inférieur des membranes foetales RPM et chorio-amniotite.
Au cours de l’accouchement :
- la dystocie cervicale à cause des lésions organiques qui fait augmenter le risque de
césarienne ;
- césarienne aussi du fait que l’accouchement par voie basse n’est parfois toléré que si les
membranes restent intactes jusqu’à dilatation complète, ce qui est rarement obtenu ; d’où la
césarienne dès que la rupture des membranes intervient.
Au cours du post-partum et pour le nouveau-né :
- la conjonctivite gonococcique et/ou à chlamydia = ophtalmie néonatale;
- la contamination systémique du nouveau-né = transmission mère-enfant (VIH, Herpès);
- la compromission de l’allaitement;
- la compromission de la vaccination utilisant des vaccins avec virus atténués (ex. BCG).
ETUDE CLINIQUE
La symptomatologie :
- douleur génitale ou génito-urinaire spontanée ou provoquée (différentiel difficile KO et
GEU) ;
- prurit vulvaire ou vulvo-vaginal avec leucorrhée.
La clinique :
- Ecoulement vaginal avec son site précis de provenance;
- Congestion vulvaire et/ou vaginale;
- Parfois lésions organiques de type rougeur, tuméfaction, érosion, éruption, condylome;
- Odeur parfois indicative de l’étiologie ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
147
- Sensibilité localisée ou étendue (à l’examen de l’abdomen et au TV).
N.B. l’aspect et la couleur des sécrétions peuvent aider à l’identification des germes (lait
caillé pour candida, en grumeaux pour candida, mousseux ou spumeux pour trichomonas,
verdâtre pour gonocoque).
Le diagnostic étiologique est fait par la paraclinique :
- Le frottis vaginal, soit à frais (trichomonas vaginalis, levures, mycélium, entamoeba
hystolytica), soit avec 1 goutte de solution d’hydroxyde de potasse (dégagement de l’odeur
de poisson pourri quand il s’agit de l’hémophylus vaginalis), soit avec le Giemsa
(chlamydiae, lymphogranulome vénérien), soit avec le Gram (gonocoque, levures et
mycélium, trichomonas vaginalis), soit enfin avec microscopie sur fond noir (tréponème
pâle) ;
- l’acidité des sécrétions vaginales (acide à pH voisin de 4,5 = hémophylus vaginalis ou
candida albicans ; pH > 4,5 = trichomonas vaginalis);
- la sérologie (syphilis, HIV) ;
- la culture sur vésicule vitelline (chlamydiae), ou sur Sabouraud ou sur Nickerson (candida
albicans).
En l'absence de secrétions sur lesquelles il soit possible d'objectiver l'agent causal, penser au
gonocoque et au chlamydia.
PRISE EN CHARGE
Prévention faite de :
- dépistage anténatal par voie de frottis vaginal et de sérologie information à la gestante (au
sujet de l’hygiène génitale = sobriété de la toilette vaginale) pour respecter la défense anti-
bactérienne naturelle du vagin ;
- information au personnel soignant sur l’hygiène ano-urétrale + hygiène du post-partum ;
- information au personnel soignant sur la contamination transversale surtout en salle
d’accouchement (cfr lunettes de protection).
Traitement anti-infectieux précoce (gestante et son partenaire) :
- Vaginose bactérienne (clindamycine® + métronidazole® en ovules + en comprimés
pendant 10 jours) ; traitement de préférence spécifique aux germes en cause et à base
d’associations; par voie générale, (ex. ampi+aminoside, ampi+bactrim®) ; parfois drogues
spéciales (ex. Zovirax®,Podophylline®);
- VIH / Sida : PEC essentiellement préventive contre la transmission verticale et
transversale, pendant la grossesse (PTME) = diminuer la charge virale maternelle grâce
aux ARV (par exemple AZT 500 mg/j en 5 prises entre la 14 ème et la 34ème semaine de
gestation + 3TC à partir de la 32ème semaine + Didanosine comme Videx à 125 mg le matin
et 125 mg le soir pour les femmes de < de 60 kg et 200 mg matin et soir pour les plus de 60
kg); en fin de grossesse, diminuer l’exposition de l’enfant au virus CESARIENNE à
programmer à membranes intactes; le jour de la césarienne, on administre en perfusion de
l’AZT à raison de 2 mg/kg en 1 heure, puis 1 mg/kg/heure jusqu’à totaliser 5 mg/kg, puis
enfin pratiquer la césarienne; pour le nouveau-né, on administre du sirop d’AZT à raison de
8 mg/kg/j pendant 6 semaines ; supprimer l’exposition post-natale en contre-indiquant
l’allaitement au sein maternel.
Dans la pratique, la PTME applique la politique suivante :
- d’abord s’assurer si la gestante est éligible aux ARV ou pas ; pour cela, on dose le taux de
CD4 ; l’éligibilité est déclarée en dessous de 200 ;
- si éligible, on débute les ARV (au moins une association de trois) ; pas de traitement
particulier en début de travail ; et après l’accouchement, on traite l’enfant avec la
Zidovudine en sirop (2 x 4 mg/kg/jour pendant 1 mois) ;
- si la gestante est non éligible aux ARV, on débute à la 28ème semaine avec Zidovudine (2 x
300 mg/jour) que l’on poursuit jusqu’à l’entrée en travail ; dès le début du travail, on donne
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
148
l’association de Zidovudine (2 comprimés en une fois) + Lavucidine (2 comprimés de 150
mg) + 1 comprimé de Névirapine (200 mg) ; après l’accouchement, on donne à l’enfant la
Névirapine (0,2 mg/kg en dose unique), puis on poursuit son traitement avec la Zidovudine
(2 x 4 mg/kg/jour) pendant 7 jours ; la mère poursuit son traitement ;
- pas d’épisiotomie si accouchement par voie basse ;
- laver le nouveau-né de mère HIV avec une solution tiède de dakin.
- Nettoyage de tous les instruments utilisés et endroit souillé de sang de la gestante.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
149
I.14. TRAUMATISMES ET GROSSESSE
Le traumatisme signifie tout événement violent survenant sur tout ou partie de l’organisme.
INFLUENCES DE LA GROSSESSE SUR LE TRAUMATISME
- La grossesse par les vertiges et autres malaises favorise les chutes.
- La propension antérieure de l’abdomen au cours de la grossesse favorise le choc sur la
masse utérine en cas d’affrontement même mineur.
INFLUENCES DU TRAUMATISME SUR LA GROSSESSE
- La douleur due au trauma favorise la confusion diagnostique avec les pathologies
gynécologiques et obstétricales douloureuses (KO compliqué, MFC, MAP, DPPNI).
- Les radiographies diagnostiques en cas de traumatisme risque tératogène sur un œuf
jeune (grossesse non encore voyante).
- Le stress du traumatisme provoque la décharge de substances hautement utéro-excitantes, à
savoir : cortisol, catécholamines, ocytocine, ADH, prostaglandines risque d’avortement.
- Le choc, même léger, du traumatisme sur la masse utérine peut conduire au DPPNI ou à la
rupture utérine.
ETUDE CLINIQUE
- Anamnèse : horaire, la nature et le point d’impact du traumatisme;
- les lésions d’accompagnement : contusions, plaies, fractures, et hémorragie;
- l’état de l’abdomen (douleur?) et de l’utérus en particulier (contraction? Contracture?); le
retentissement materno-ovulaire.
ATTITUDES THERAPEUTIQUES
Elles sont fonction de :
- l’âge gestationnel;
- l’état clinique de la gestante;
- l’état ovulaire (relâchement utérin, intégrité utérine, RCF);
- les lésions associées.
Elles consistent en :
- Tocolyse préventive, curative si signes d’irritation utérine (tocographie SVP! si grossesse
≥16 semaines) ;
- Laparotomie exploratrice dès soupçon de rupture utérine;
- Interruption de la grossesse (par césarienne) en cas de DPPNI ou de mort maternelle;
NB : en cas de mort maternelle remontant à moins d’une minute, si la hauteur utérine dépasse
l’étendue d’une main d’adulte, une césarienne post-mortem est pratiquée avec le premier
instrument tranchant rencontré sur les lieux.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
150
I.15. ISO-IMMUNISATION MATERNO-FŒTALE
L’iso-immunisation sanguine materno-fœtale, aussi appelée érythroblastose fœtale, est une
maladie strictement fœtale, puisque la mère qui en est la cause n’en souffre pas. Elle est
caractérisée par une anémie hémolytique du fœtus, et dont le point de départ est une réaction
d’immunisation sanguine maternelle envers l’antigène fœtal Rhésus.
C’est en 1961 qu’avec la première transfusion sanguine réussie par Lilley par voie intra-
péritonéale, qu’elle devient la première maladie fœtale traitable in utero. Et en 1981 le taux
de survie périnatale est encore nettement amélioré avec la transfusion sanguine fœtale
« intravasculaire ».
PHYSIOPATHOLOGIE
On est en présence d’une mère Rhésus – et d’un enfant Rhésus + (ou même un enfant Rhésus
– mais Du+).
Il s’agit d’une allo-immunisation maternelle par voie d’hémorragie foeto-maternelle
transplacentaire ou par voie de transfusion sanguine (exclusivement pour les groupes non D).
Il faut un minimum de 0,1 ml de sang fœtal pour immuniser la mère. Cela a lieu en deux
temps :
- la mère entre en contact avec l’antigène en question (en l’occurrence l’antigène D) soit
lors d’un avortement ; soit lors d’un accouchement ; soit lors des ponctions ovulaires ; soit
au cours de la grossesse lors des manœuvres endo-utérines ou de version externe ; soit lors
d’une transfusion de sang Rhésus – mais Du+ ;
- cette femme est dite sensibilisée, et en gardera la mémoire toute sa vie durant ; si cela
arrive au cours d’une grossesse, celle-ci n’est généralement pas menacée, puisqu’il faut un
autre contact de réveil immunitaire pour produire les anticorps susceptibles d’aller nuire au
fœtus ;
- par un contact ultérieur (éventuellement au cours d’une autre grossesse, mais parfois au
cours de la même grossesse si les conditions s’y prêtent cfr ci-dessus), la sensibilisation
itérative provoque une stimulation du système immunitaire maternelle qui fabrique alors
des anticorps M complets (agglutinants en milieu salin, et ne traversant pas la barrière
placentaire), ainsi que des anticorps G incomplets (non agglutinants en milieu salin) qui
traversent la barrière placentaire ; et une fois arrivés dans le compartiment fœtal, ces Ig G
sensibilisent les hématies du fœtus qui vont alors être détruites dès que le système réticulo-
endothélial du fœtus atteint sa maturité (= à partir de la 16ème semaine de gestation) ; c’est
le début de la maladie fœtale.
Les Ig G passent la barrière placentaire à partir de la 12ème semaine, et le passage augmente
progressivement jusqu’à 24 semaines, puis fort rapidement jusqu’à terme. Le fœtus dont les
globules rouges sont détruits devient anémique (Hb < 10g/dl), d’où la survenue de la
décompensation cardiaque, avec oedèmes (= HYDROPS FETALIS puis, avec l’atteinte du
placenta HYDROPS FOETO-PLACENTAIRE ou ANASARQUE FOETO-
PLACENTAIRE); le fœtus devient également ictérique et va colorer le liquide amniotique en
jaune. Cette coloration figure parmi les éléments d’appréciation de la gravité de l’état fœtal.
N.B.
Il est possible que même en présence d’une mère Rhésus – et d’un enfant Rhésus + (ou même
un enfant Rhésus – mais Du+), l’immunisation maternelle ne se produise jamais. C’est un
mode de prévention naturelle de la maladie grâce au système ABO. Le sang fœtal du groupe
A, par exemple, qui arrive dans la circulation sanguine d’une mère certes Rhésus négatif
mains du groupe B n’a pas le temps d’être reconnu par la mère, tout simplement parce qu’il
est A et donc immédiatement détruit et réduit au silence par les agglutinines B (anti A), et
tout s’arrête là.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
151
ETUDE CLINIQUE
Le diagnostic repose sur les éléments anamnestiques maternels et ceux relatifs à la grossesse
en cours.
Les éléments anamnestiques maternels sont :
- antécédent d’enfant né ictérique ;
- antécédent d’enfant né mort de cause inexpliquée.
Les éléments relatifs à la grossesse en cours sont :
- le groupe sanguin Rhésus de la mère (rarement se fier au groupe sanguin du conjoint);
éventuellement un Coombs indirect positif; il faut se rappeler que le Coombs ne concerne
pas les Anti-A et Anti-B puisque le test nécessite des globules rouges quelconques O Rh +
auxquels on ajoute le sérum de Coombs (= sérum de lapin anti-gammaglobulines humaines)
susceptible de provoquer l’agglutination;
- un titrage d’anticorps faisant état d’une forte sensibilisation maternelle;
- la démonstration, à l’échographie, de l’anémie fœtale (via cordocentèse), de l’anasarque
foeto-placentaire, et de modifications importantes à l’étude doppler, ainsi que d’une
bilirubinamnie encore positive après 35 semaines de gestation.
PRISE EN CHARGE
La prévention médicale
C’est la seule qui donne des résultats sûrs, étant donné que, lorsque la maladie est déclarée,
les chances d’obtenir un enfant de bonne qualité sont forts minces. Il s’agit donc de prévenir
(empêcher) la sensibilisation maternelle chez une femme Rh - supposée non encore
sensibilisée. Elle consiste à administrer des gammaglobulines contenant des grands titres
d’anticorps anti-D (RhoGam®) chaque fois qu’il y a risque pour la femme Rh - d’entrer en
contact avec du sang Rh + (avortement, transfusion, accouchement). Cette administration doit
se faire dans les 72 heures qui suivent la situation à risque de contamination sanguine. La
dose de gammaglobulines à injecter est fixée empiriquement à 250-300 µg en supposant que
la quantité moyenne de sang fœtal passé à la mère ne dépasse pas 0,1 ml. Etant donné que
cette quantité peut être plus importante dans certaines circonstances, le RhoGam® risque de
ne pas suffire. Il est alors recommandé d’évaluer précisément afin de mieux adapter la dose à
administrer. On recourt pour cela au test de KLEIHAUER (= frottis de sang périphérique
maternel à recouvrir avec un acide faible == les cellules sanguines fœtales contenant une
hémoglobine plus résistante à la dénaturation que les hématies adultes vont être plus
facilement reconnues et comptées).
La surveillance gravidique
Elle s’effectue par la répétition du test de Coombs indirect :
- 1x/jr/mois à partir de la 12ème semaine jusqu’à la 32ème semaine, tant qu’il demeure négatif ;
- 1 fois toutes les 2 semaines jusqu’à terme, tant qu’il demeure négatif ;
- dès qu’il est positif, il faut en obtenir le titrage des anticorps; en dessous de 1/16 le fœtus
n’est pas encore en danger, et le titrage peut être répété 1 fois par semaine;
- dès que titre dépasse 1/16, on attend la 28ème semaine pour une amniocentèse tous les 15
jours en vue d’un dosage de bilirubine dans le liquide amniotique;
- on laisse poursuivre la grossesse tant que le taux de bilirubinamie se situe dans la zone
inférieure de Lilley;
- en cas de transfusion fœtale (= in utero) ou néonatale, le sang à donner est celui du groupe
O Rh négatif compatible avec le sang maternel, pour qu’il ne soit pas « attaqué » par les
anticorps maternels anti-Rhésus ayant provoqué la maladie;
- dès qu’on se situe dans la zone supérieure de Lilley, une exsanguino-transfusion est à
envisager in utero tant qu’on n’a pas encore atteint l’âge propice d’extraction fœtale (32 –
34 semaines).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
152
I.16. PALUDISME ET GROSSESSE
Le Paludisme ou Malaria est une maladie occasionnée par un parasite (le Plasmodium) qui
est inoculé à l’homme par un vecteur (l’anophèle). Des 4 types de Plasmodium (falciparum,
malariae, ovale, et vivax) le falciparum est le plus pathologique. Une fois dans le corps de
l’homme, le parasite se localise soit dans le sang (provoquant ainsi les signes de la maladie),
soit dans le foie (possibilité d’absence de signes de la maladie dans l’immédiat, avec risque
de reviviscence jusqu’à près de 6 mois plus tard).
INFLUENCES DE LA GROSSESSE SUR LE PALUDISME
- La grossesse offre des conditions de reviviscence ou d’aggravation du paludisme ; cfr
baisse de l’immunité.
- La potentialité de transmission verticale du paludisme (mère vers enfant) est réelle si le
plasmodium se concentre au niveau du placenta, donnant lieu au paludisme fœtal et/ou
néonatal.
- Une pathologie gravidique, en l’occurrence l’éclampsie, peut être faussement diagnostiquée
à la place d’un paludisme grave, ce qui péjore alors le pronostic.
- La confusion diagnostique peut encore intervenir en post-partum lorsqu’une fièvre
d’origine malarienne est mise au compte d’une montée laiteuse.
INFLUENCES DU PALUDISME SUR LA GROSSESSE
- Le parasitage puis la destruction des globules rouges maternels exposent à la bascule de
l’anémie physiologique de la grossesse vers l’anémie maladie dont nous avons déjà illustré
les effets sur la grossesse.
- La maladie maternelle alourdit les « signes sympathiques » de la grossesse et peut de ce fait
aggraver un tableau de dénutrition (possibilité de RCIU).
- Les formes graves de la maladie comportent des troubles de coagulation qui peuvent
précipiter un syndrome de type CIVD.
- La transmission verticale du paludisme (mère vers enfant) comporte ainsi un risque
d’anémie chez l’enfant.
- La toxicose maternelle de type fébrile (soit par libération des cytokines par le parasite, soit
du seul fait de la parasitémie) et médicamenteuse va engendrer une perturbation des
échanges materno-fœtaux ainsi que des contractions utérines avortement ou prématurité.
ETUDE CLINIQUE
Symptomatologie polymorphe, mais dominée par la fièvre, les céphalées, les courbatures et
les arthralgies.
Signes de gravité (P. falciparum) : changement de comportement – somnolence – altération
de la conscience – choc – convulsions – ictère sévère – hémoglobinurie – insuffisance rénale
aiguë – D.I.C. – œdème aigu du poumon.
Paraclinique repose sur l’examen de la GOUTTE EPAISSE dont cependant la négativité
n’exclue pas la maladie, et dont la positivité ne signifie pas non plus forcément nécessité de
traitement (puisque une malaria biologique peut être éradiquée par les anticorps de l’individu
concerné). Le frottis sanguin, pour évaluation de la DENSITE PARASITAIRE après avoir
identifié un champ microscopique de 100 ou de 200 globules blancs, = (nombre de parasites
x 100) / 6000 (correspondant à la leucocytose)
La détermination de cette densité constitue un puissant moyen de contrôle de l’efficacité du
traitement, surtout si la disparition des signes de la maladie est lente (faisant craindre une
résistance au médicament utilisé). C’est donc un examen qu’il faut alors répéter au fur et à
mesure du traitement. On recourt parfois aux tests immunologiques pour départager
certains cas douteux (suspects de résistance aux antipaludiques).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
153
PRISE EN CHARGE
Traitement symptomatique : antipyrétiques et antispasmodique
Traitement étiologique :
Pour la prévention : moustiquaire imprégnée + 1 dose curative de FANSIDAR® (3
comprimés en une fois) au 2ème trimestre puis au 3ème trimestre (les 2 prises étant espacées
d’au moins 4 semaines) = Traitement préventif intermittent (TPI).
Pour le paludisme simple :
Au 1er trimestre, Quinine en comprimé + Clindamycine
Au 2ème et 3ème trimestre : en 1ère intention Association Artesunate + Amodiaquine ou
Artémether + Lumefantrine ; et en seconde intention Quinine comprimé+ Clindamycine
Pour le paludisme compliqué le traitement est à instaurer à l’hôpital, dans un service de
soins intensifs, sous forme de perfusion de quinine (dose journalière en 4 heures de perfusion
de sérum glucosé à 10%) + un relais à la forme orale en association avec la Clindamycine.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
154
4ème partie : DYSTOCIES
IV.1. DYSTOCIE DUE AUX VOIES
1. DYSTOCIE DUE AU BASSIN OSSEUX
Il s’agit d’une perturbation essentiellement d’origine osseuse de la marche de l’accouchement
par les voies naturelles. Problème jadis important de l’obstétrique, la dystocie osseuse a perdu
son caractère dramatique grâce à l’hygiène de l’enfance qui limite actuellement les avancées
du rachitisme, les conséquences ostéo-articulaires de la tuberculose, la quasi suppression de
la luxation congénitale de la hanche, ainsi qu’au dépistage possible au cours des CPN et au
perfectionnement des techniques opératoires de la césarienne et de réanimation.
Des études radiologiques permettent de définir les indices de perméabilité du détroit
supérieur, notamment l’Indice de MAGNIN qui est la somme du diamètre transverse médian
et du diamètre antéro-postérieur utile, soit 12,5 cm + 10,5 cm = 23 cm. Cet indice apprécie
le pronostic de l’accouchement qui est bon si l’indice est à 23 cm et plus, incertain si entre
21 et 22 cm, mauvais si inférieur à 20 cm.
A) BASSINS PATHOLOGIQUES OU RETRECIS
Caractérisés par la réduction d’un ou de plusieurs diamètres au niveau d’un ou de plusieurs
étages du bassin. Le plus souvent cette diminution se trouve au niveau du détroit supérieur.
Elle y entraîne la réduction de l’aire d’engagement.
Les bassins pathologiques sont nombreux :
a) bassin rétrécis symétriques (généralement rétrécis ou Justo-minor, plats, transversalement
rétrécis, etc…);
b) bassins asymétriques (boiterie unilatérale, scoliose, atrophie pelvienne, bassin de
Naegelé) ;
c) bassins dystociques après traitement orthopédiques ;
d) bassins limites caractérisés par la réduction de quelques mm à 0,5 cm du diamètre
normal.
En dehors des situations où la césarienne est d’emblée de mise, la prise en charge des
anomalies du bassin comprend l’EPREUVE DU TRAVAIL. Il s’agit d’un essai
thérapeutique d’expectative attentive qui consiste à donner à la femme toutes les chances
d’accoucher par la voie basse si cela est raisonnablement possible. Il s’agit d’un
accouchement dirigé qui, pendant une certaine durée d’observation, permet de confronter
trois facteurs : la présentation et le bassin (confrontation céphalo-pelvienne) ; le troisième
facteur est justement celui qui confronte = l’action des contractions utérines. Cette
confrontation doit aboutir à l’engagement franc de la tête fœtale. Elle ne peut donc être
envisagée que si les préalables ci-après sont réunis : absence d’une viciation du bassin, un
fœtus en bonne vitalité, ainsi que la possibilité de mobiliser aisément tous les moyens
(chirurgiens, anesthésistes, pédiatres, etc…) pour une césarienne si échec de l’épreuve.
Elle s’adresse exclusivement à la présentation céphalique de sommet et exige :
- des bonnes contractions utérines ;
- une dilatation du col d’au moins à 5 cm, la poche des eaux étant rompue ;
- une surveillance attentive, avec des examens comparatifs et un timing d’évaluation.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
155
IV.2. DYSTOCIE DUE AUX FORCES EXPULSIVES = DYSTOCIE
DYNAMIQUE
1. DEFINITION
C’est l’ensemble des perturbations du fonctionnement du muscle utérin au cours du travail de
l’accouchement. Il s’agit des anomalies de la contraction utérine (C.U) et de la dilatation du
col utérin rendant un accouchement laborieux voire impossible.
Les dystocies dynamiques sont presque toujours utérines et intéressent très peu le col. Les
vraies dystocies qui intéressent le col sont rares et sont organiques = souvent secondaires à
une lésion discrète. Leur étiologie est donc à rechercher au niveau de :
- adhérences anormales et persistantes du pôle inférieur de l’œuf, empêchant le libre jeu du
segment inférieur sur le pôle fœtal inférieur ; cela fait généralement suite à une endométrite
déciduale du début de grossesse, ou à de antécédents d’avortement cureté ou infecté ; dans
ces cas la dilatation du pôle inférieur au doigt puis la rupture artificielle des membranes
résoud le problème ;
- cicatrices cervicales ;
- lésions infectieuses ex.herpétiques ou syphilitiques qui limitent l’ampliation cervicale.
Les dystocies dynamiques utérines sont fonctionnelles et se rapportent à :
- l'hypotonie = tonus de base normal, mais amplitude faible (FDT ? Obstacle?);
- l'hypocinésie = fréquence des contractions < 2 par 10 minutes; fréquente en cas de
présentation de siège, de cicatrice utérine, de polyhydramnios, et de présentation céphalique
dans la position occipito-postérieure; l’association d’hypocinésie d’intensité et de fréquence
caractérise l’INERTIE utérine ; ces états sont fréquents au début du travail. Il faut faire le
diagnostic différentiel avec le faux travail ;
- l’hypertonie; tonus de base élevée; relâchement insuffisant entre les C.U.; il peut s’agir soit
d’une contraction soutenue (contracture) comme on en trouve en cas de DPPNI, ou tout
simplement de pression interne soutenue (hyperdistension utérine) comme en cas de
polyhydramnios, du simple fait de la distension hydraulique, et non comme conséquence
d’un trouble intime de la fonction contractile; l’ouverture de l’œuf fait chuter le tonus de
base et la C.U devient normale;
- l'hypercinésie; fréquence des contractions > 2 par 10 minutes;
- l'incoordination des contractions (dyskinésie); non respect du triple gradient contractile
(début – propagation – intensité), généralement du fait soit d'un obstacle, soit d'une
disproportion, soit d'une cicatrice.
2. LES CONSEQUENCES DES TROUBLES DE LA DYNAMIQUE UTERINE
Ce sont :
- la non progression de la dilatation cervicale et de la descente fœtale;
- les troubles hémodynamiques aboutissant à l'œdème cervical;
- le syndrome de "lutte" entre d'une part l'utérus qui tente de chasser le mobile et d'autre part
les voies d'expulsion qui s'y opposent; cela se traduit par l'apparition d'un anneau de
rétraction à la jonction corps-segment inférieur = ANNEAU DE BANDL-FROMMEL
ayant la forme d'une dépression circulaire donnant "l'utérus en sablier" (diagnostic
différentiel avec un globe vésical); il y a dans ce cas un amincissement très étendu du
segment inférieur = pré-rupture utérine;
- la rupture utérine;
- l'infection;
- l'étonnement utérin.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
156
3. ETHIOPATHOGENIE
Selon des états pathologiques, on peut avoir plusieurs types :
- hypertonie par contracture dans l’hématome retro-placentaire(DPPN) ; le tonus de base
peut atteindre des valeurs 3 ou 4 fois supérieures à celles du tonus normal, mais avec des
C.U rythmées et des amplitudes presque normales de 20 à 25 mm Hg ;
- hypertonie par distension (Polyhydramnios) ; valeurs élévées de pression intra-amniotique
entre les C.U de faible amplitude ; l’ouverture de l’œuf fait chuter le tonus de base et la C.U
devient normale ; ici, l’élévation de pression intra-utérine est un simple fait de distension
hydraulique et non la conséquence d’un trouble intime de la fonction contractile. Ici
l’hypertonie est abusive ;
- hypertonie par hypercinésie (ou tachysystolie) ; elle résulte de l’injection de doses
excessives d’ocytocine, surtout en IM, et provoque l’hypercinésie d’intensité et de
fréquence avec élévation progressive de tonus de base ; elle se traduit par un mauvais
relâchement utérin entre les C.U, et risque d’aboutir à une contracture utérine ;
l’hypertonie résulte aussi d’un effort contractile contre un obstacle infranchissable ; dans ce
cas, la dystocie dynamique est la conséquence mécanique.
4. LE TRAITEMENT DES TROUBLES DYNAMIQUES
1) pour l'hypocinesie :
- s'assurer d'abord qu'il s'agit bel et bien d'un travail effectif;
- ensuite s'assurer qu'on n'est pas en présence d'une disproportion foeto-pelvienne;
- mettre la gestante au repos + Antispasmodiques en cas de dystocie de démarrage ou de faux
début de travail;
- stimuler (syntocinon) en cas d'inertie primaire ou de rupture des membranes;
- entreprendre une correction éventuelle de troubles électrolytiques;
- amniotomie si les membranes étaient restés jusque là intactes.
2) Pour l'hypercinésie utérine :
- retrait éventuel de l'ocytocique en cause;
- amniotomie si hématome rétro-placentaire;
- césarienne si anneau de Bandl.
3) Pour la dyskinésie utérine : orasthin sous PDA.
4) Pour la faiblesse de la presse abdominale à l'expulsion : ventouse ou forceps et/ou
Christeller sous conditions.
5) Cas particuliers
a. Hypertonies localisées
- Syndrome de DEMELIN : un anneau musculaire occupant une dépression entre deux
saillies fœtales à un étage quelconque de l’utérus. Signe : douleur permanente et irradiation
lombo-sacrée, Arrêt de la dilatation, relâchement médiocre de l’utérus. Le diagnostic est
tardif et se fait lors de manœuvre intra-utérine, instrumentale ou manuelle : le traitement
consiste en simples moyens médicamenteux ou par extraction difficile artificielle soit par
les voies naturelles ou par césarienne.
- Syndrome de SHICKELE : anneau musculaire du col utérin effacé = dernier anneau
musculaire constituant l’obstacle. Pendant le tonus l’orifice cervical reste tendu comme
cerclé par un fil de fer. Au cours de la C.U le col devient tendu et douloureux. Avec le
traitement l’anneau, cède et le travail se poursuit et se termine rapidement. Sans
traitement, le travail prolongé conduit à l’épuisement.
b. Dystocie de la phase d’expulsion
- Dystocie dynamique par défaut :
chez certaines grandes multipares à musculature utérine déficiente ;
chez certaines primipares après un travail difficile trop long qui les conduisent à un
état de fatigue et même d’épuisement.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
157
- Dystocies d’expulsion : Ocytocine en perfusion IV lente. Si apparition des signes de
souffrance fœtale extraction rapide du fœtus par Césarienne si la dilatation est incomplète
ou tête non engagée. Forceps si cela est possible.
IV.3. DYSTOCIE DUE A L’UTERUS ET AUX PARTIES MOLLES
Les malformations utérines (Hypoplasie d’un utérus cylindrique, bicorne ou didelphe), les
altérations acquises de la fibre utérine chez la primigeste âgée (myomatose), l’immaturation
du corps et du col chez des primipares très jeunes, tout comme l’utérus hypocontractile de la
grande multipare, peuvent constituer des causes soit d’absence, soit de mauvais travail, soit
encore d’obstacle à l’expulsion fœtale.
L’utérus cicatriciel
Un utérus cicatriciel est celui qui a déjà fait l`objet d`une opération chirurgicale : soit une
myomectomie, soit une réparation en cas de malformation ou de lésions iatrogènes abortives,
soit encore plus souvent une césarienne. Avec la montée du taux de césariennes dans le
monde et particulièrement en Afrique Noire, l`accroissement du nombre d`utérus cicatriciels
constitue une réalité obstétricale incontournable.
La cicatrice utérine constitue une zone de moindre résistance susceptible de céder lors des
fortes pressions internes provoquées par les contractions utérines du travail. On assiste donc a
une rupture utérine qui peut être incomplète (n`intéressant pas toute l`épaisseur du muscle
utérin ou myomètre), ou complète. Ceci survient plus fréquemment pendant le travail, mais
peut aussi s`observer en dehors du travail, comme en cas de traumatisme. C`est une situation
volontiers hémorragique qui menace immédiatement la vie de la mère et de l`enfant.
Les circonstances amenant la cicatrice utérine à céder, et donc à provoquer une hémorragie
qui peut tuer, sont multiples, les plus importantes étant :
- la multiplicité des cicatrices (antécédent de 2 césariennes et plus) ;
- l’étendue de cette (ces) cicatrice(s) (gros myomes dont l`ablation a conduit le chirurgien à
atteindre la cavité utérine) ;
- la grande multiparité (plus de 4 accouchements) ;
- la mauvaise qualité de la cicatrice (césarienne corporéale – infection post-césarienne –
indices importants de mauvaise cicatrice à hystérographie, à l'hystéroscopie et surtout à
l'échographie endovaginale) ;
- le mauvais bassin ;
- la hauteur utérine importante (plus de 34 cm) ;
- la présentation du siège ;
- l`absence de liquide amniotique (Rupture prématurée des membranes) ;
- les contractions provoquées par l`oxytocine, les prostaglandines et analogues (cytotec).
Ces circonstances constituent des motifs suffisants, pour une maternité de premier niveau,
d`envisager le transfert ou la référence.
Au niveau de l’hôpital général de référence la cicatrice utérine n`est pourtant pas une contre-
indication à l`accouchement par voie basse qui reste envisageable chez la paucipare dans
certaines conditions : une seule cicatrice de bonne qualité, le bassin bon, la présentation de
sommet, le volume fœtal moyen, et les contractions utérines spontanées.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
158
IV.4. DYSTOCIES DUES AU MOBILE FOETAL
A. LES MAUVAISES PRESENTATIONS
1. LA PRESENTATION DE SIEGE
On décrit 3 variétés: complète; incomplète; décomplétée (mode fesses, pieds, genoux).
Etiologie
- Hypotonie utérine multiparité, grossesse multiple; polyhydramnios).
- Malformation utérine (septum).
- Anomalie fœtale (hydrocéphalie, anencéphalie).
- Antécédent de siège.
- Anomalie du bassin maternel (angustie).
Risque
= Morbidité et mortalité périnatale accrues du fait de la fréquence de dystocie mécanique
(d'où la prolongation du travail), des difficultés liées à l'extraction de la tête dernière, et du
risque intrinsèque des manœuvres endo-utérines de la grande ou de la petite extraction.
Ce risque est d'autant plus accru que l'on se trouve en présence de:
- souffrance fœtale; - placenta praevia; - cicatrice utérine;
- prématurité; - malformation fœtale; - gros enfant;
- procidence du cordon; - grossesse multiple; - angustie pelvienne.
Diagnostic
Le diagnostic de la présentation de siège doit être posé bien avant le travail afin de prendre les
précautions qui s'imposent pour réduire les risques ci-dessus évoqués. Les éléments
diagnostiques se trouvent dans:
- l'examen clinique via Manœuvres de Léopold;
- l'échographie qui, non seulement authentifie la présentation, mais aussi renseigne sur la
morphologie et la position du fœtus ainsi que sur l'état des annexes (placenta, cordon et
liquide amniotique);
- le toucher vaginal au cours du travail doit faire le diagnostic différentiel avec une
présentation de face (voir différence entre anus fœtal et bouche fœtale); le toucher vaginal
permet également de déterminer la position du sacrum qui est le repère de la présentation.
Mécanisme d'accouchement
Dans l'accouchement eutocique (par présentation céphalique), une fois que la tête est sortie, le
reste suit presque sans problème (sauf dystocie des épaules). Dans l'accouchement de siège,
tant que la tête n'est pas encore sortie, tout reste à faire. Le déroulement s'effectue de la
manière suivante:
- le siège s'engage suivant le diamètre bitrochantérien (10 cm); la descente et la rotation dans
la concavité pelvienne suivent alors de façon à amener le dos fœtal vers l'avant de la mère
(l'enfant devant regarder le sol en naissant);
- le dégagement s'effectue en sacro-pubien; la hanche antérieure doit sortir la première (il y a
un déhanchement qui amène les fesses de l'enfant vers le haut;
- les épaules s'engagent selon le diamètre bisacromial ; le dégagement a lieu en transverse;
- la tête dernière doit rester totalement fléchie sur la poitrine, formant bloc.
Conduite à tenir
Au cours de la grossesse; il faut poser le diagnostic; oublier la tentation des manœuvres de
version!
Pratiquer la césarienne si enfant de faible poids de naissance, si poids fœtal estimé à plus de
3400 gr, si bassin limite, si rupture précoce des membranes, ou encore en cas de prématurité.
Au cours du travail, confirmer le diagnostic + s'assurer que la tête est bien fléchie
(échographie ou radiographie) + avoir une estimation du volume fœtal (hauteur utérine +
échographie) + être sûr que le bassin maternel est bon (antécédents obstétricaux +
radiopelvimétrie).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
159
Au début de l'expulsion; préparer un abord veineux (pour la perfusion éventuelle en vue de
corriger l'hypocinésie utérine) + assurer un élargissement des voies en pratiquant une large
épisiotomie + s'abstenir de toucher à l'enfant avant la sortie du nombril (qui est la preuve que
les épaules sont passées par le détroit supérieur); toute manipulation sur le fœtus avant ce
moment entraîne de la part du fœtus un relèvement des bras, ce qui hypothèque les chances
d'engagement de la tête dernière (cfr "qui est cet imbécile qui me cherche noise); il faut en
principe attendre que les épaules se dégagent d'elles-mêmes spontanément sauf si ARRET DE
PROGRESSION (= présomption que les bras sont en train de se relever) ou ROTATION DU
DOS FŒTAL VERS L'ARRIERE. Dans ce cas il faut pratiquer la petite extraction (appliquer
les mouvements physiologiques).
A la fin de l'expulsion; pratiquer la manœuvre de Bracht ( ) ou, si échec, de Mauriceau (2
doigt dans la bouche du fœtus ).
2. LA PRESENTATION TRANSVERSALE
Elle est aussi dite de l'épaule en raison de la tendance de cette dernière à vouloir forcer le
détroit supérieur pour s'y engager. Elle est parfois précédée d'une présentation oblique. Sa
fréquence varie de 0,3 à0,4%.
Les variétés de position sont dominées par celles du dos en antérieur (épaule droite ou gauche
dorso-antérieures, par opposition aux positions épaule droite ou gauche dorso-postérieure).
Etiologie (similitudes avec le siège)
- Hypotonie utérine multiparité, grossesse multiple; polyhydramnios).
- Malformation utérine (utérus cordiforme ou à éperon).
- Tumeurs utérines praevia.
- Antécédent de siège.
- Anomalie du bassin maternel (angustie).
Risque
Il tient au fait que, sauf correction spontanée (oublier la version par manœuvres externes), vers
la fin de la grossesse, il n'existe pour ce type de présentation aucune possibilité
d'accouchement par voie basse (MEMENTO: CONDUPLICATO CORPORE pour les petits
fœtus morts ou vivants avant la 20 - 24ème semaine de gestation).
L'évolution du travail en cas de présentation transversale s'effectue vers:
- l'instauration d'un syndrome de lutte, avec aboutissement logique vers la rupture utérine
(risque aggravé dès que les membranes sont rompues);
- la rupture prématurée des membranes;
- la procidence du cordon (sans beaucoup de gravité étant donné l'absence d'élément
compressif sur lui;
- l'engagement de l'épaule dès que les membranes sont rompues; c'est la classique situation
d'EPAULE NEGLIGEE, le bras venant presque saluer l'accoucheur à la vulve; c'est une
situation qui ne doit pas durer longtemps, sinon on arrive à la rupture utérine;
- la rupture utérine.
Diagnostic
Le diagnostic de la présentation transversale est obligatoire à temps. C'est ce qui permet
'effectuer une césarienne dans le calme bien avant l'entrée de la gestante en travail. Les
éléments diagnostiques se trouvent dans:
- l'examen clinique via Manœuvres de Léopold (orientation transversale de l'ovoïde fœtale); il
est typique de trouver le détroit supérieur "déshabité" (sans partie fœtale en présentation);
- l'échographie;
- le toucher vaginal au cours du travail accède au gril costal.
Mécanisme d'accouchement
C'est la césarienne qu'il faut pratiquer, et à temps!
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
160
3. LA PRESENTATION CEPHALIQUE OCCIPITO-POSTERIEURE
Son intérêt réside dans le fait qu'elle occasionne un accouchement traînant étant donné que la
rotation effectue plus qu'un demi-tour. Cette rotation est difficile sinon impossible à obtenir
dans 20% des cas, surtout si PDA (cfr trop grande laxité du bassin mou), ou en cas de bassin
androïde. On assiste alors à l'apparition d'un œdème cervical et d'un caput qui brouille les
repères de position. Elle fait alors indiquer une césarienne.
4. LA PRESENTATION CEPHALIQUE TRANSVERSE PROFONDE
Cette situation survient lorsque la tête n'effectue presque pas de rotation dans sa descente qui
se fait ainsi non comme une vis, mais plutôt comme un simple clou. On palpe alors les 2
fontanelles à la fois. La tête se trouvant bloquée dans la concavité sacrée, il faut la dégager à
l'aide d'une ventouse ou d'un forceps.
5. LA PRESENTATION DE FACE
Elle est fort rare (0,20%) et consécutive à une déflexion extrême de la tête fœtale, passant
progressivement par les présentations du front(repère = nez; diamètre de présentation = sous-
occipito-mentonnier = 13,5 cm; césarienne) et du bregma ou de la grande fontanelle
(césarienne).
Son étiologie peut être maternelle (bassin limite), fœtale (tumeur cervicale, macrosomie,
dolicocéphalie), ou annexielle (polyhydramnios, placenta relativement bas-inséré, circulaire du
cordon).
Le repère est le menton (diamètre sous-mento-bregmatique = 9,5 cm, ou bi-malaie = 5,5 – 9
cm). Le diagnostic différentiel peut être difficile à poser avec le siège, le front. L'échographie
et/ou la radiographie vient trancher.
Le mécanisme d'accouchement (très souvent eutocique):
- 4 variétés d'engagement, comme d'habitude, mais la plus fréquente se trouve être la mento-
iliaque droite postérieure (M.I.D.P.);
- le couple thoraco-céphalique (pr-sterno-syncipital dit aussi de solidarisation = 13,5 – 14,5
cm) ne peut pas passer le détroit supérieur, d'où la nécessité que la face se désolidarise,
tourne vers l'avant de manière à placer l'occiput dans la concavité sacrée et le menton sous la
symphyse;
- cette rotation vers l'avant est plus rapide en cas de position antérieure; en l'absence de
rotation antérieure une césarienne s'impose;
- le dégagement n'a donc lieu qu'en cas de rotation antérieure; c'est alors la poursuite de la
désolidarisation entre tête et thorax qui amène à la vulve tour à tour menton, front et occiput;
en cas d'expulsion traînante il est fait recours au forceps en mento-pubien;
- le visage du nouveau-né est en principe couvert d'un œdème hideux qui se résorbe sans
laisser de trace.
B. L'EXCES DE VOLUME OU MACROSOMIE FŒTALE
L'excès du volume fœtal peut être absolu; c'est le cas des macrosomies fœtales à terme (>4000
g – 4400g). Il peut également être relatif; c'est le cas de fœtus de volume normal, mais sur des
bassins maternels franchement ou relativement viciés. C'est la disproportion foeto-pelvienne
(DFP) ou encore céphalo-pelvienne.
En fait quatre situations sont susceptibles de se présenter:
- fœtus de volume normal et bassin limite;
- fœtus de volume normal et bassin rétréci;
- fœtus macrosome et bassin normal;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
161
- fœtus macrosome et bassin rétréci.
Le diagnostic du volume fœtal est fait à partir des antécédents de macrosomie fœtale + une
hauteur utérine importante par rapport à l'âge gestationnel + une évaluation échographique. De
plus il existe des excès de volume localisés (hydrocéphalie, kystes cervicaux, tumeur sacro-
coccygienne ou autre, les siamois), dont certains peuvent nécessiter des ponctions (kystes,
hydrocephalie), ce qui évite parfois une césarienne.
Le diagnostic d'anomalie pelvienne vient également par l'anamnèse (antécédent de dystocie)
+ une petite taille de la femme (150 cm ou moins) + une évaluation endopelvienne (on atteint
facilement le promontoire = présomption de diamètre promonto-sous-pubien et partant
promonto-rétro-pubien insuffisant) + Radiopelvimétrie).
Les risques
L'excès du volume fœtal constitue une occasion de:
- manque d'engagement de la tête fœtale;
- syndrome de lutte si l'anomalie n'est pas reconnue à temps;
- troubles de la dynamique utérine;
- rupture utérine;
- dystocie des épaules (après la sortie de la tête, celle-ci reste collée à la vulve et ne sait pas
effectuer la rotation externe, et le visage de l'enfant s'oedématie et se cyanose), avec son
cortège de complications (élongation du plexus brachial, fractures des bras, hémorragies
cérébro-méningées).
La conduite de l'accouchement en cas d'excès de volume fœtal est variable:
- en cas d'excès absolu (ce qui suppose un diagnostic très précis aussi bien du fœtus que du
bassin), la césarienne s'impose;
- en cas d'antécédent de césarienne, une autre césarienne est de règle;
- en cas de disproportion relative liée à une viciation modérée du bassin maternel, on recours à
une tentative d'accouchement par voie basse appelée EPREUVE D’ENGAGEMENT ; elle se
réalise sous certaines conditions sine qua non (présentation du sommet + membranes
rompues ou à rompre dès que l'épreuve démarre + contractions utérines régulières ou à
régulariser, l'épreuve devenant alors DYNAMIQUE); les premières raisons de poursuite de
l'épreuve sont évaluées après 2 – 3 heures de travail en fonction de la dilatation et de la
descente du mobile foetal); dans tous les cas, il est aujourd'hui possible de mieux décider de
l'épreuve du travail sur la base du DIAGRAMME DE MAGNIN (voir figure avec ses zones
de pronostic favorable d'accouchement par voie basse, d'incertitude indiquant l'épreuve, et de
césarienne d'emblée).;
- en cas de dystocie des épaules (plus fréquente si le fœtus pèse plus de 4000 grammes), il ne
faut pas tirer sur la tête! il ne faut pas non plus faire de Christeller! Il faut d'abord s'assurer
d'une largesse au niveau de la voie grâce à une large épisiotomie; Il faut procéder à la
MANŒUVRE DE MC ROBERTS (flexions-extension des cuisses sur l'abdomen + pression
supra-pubienne pour permettre à l'épaule antérieure de se dégager grâce au tassement du
diamètre bi-acromial); c'est lorsque cette manœuvre tarde à s'effectuer tout à fait qu'on
recourt à d'autres techniques malheureusement plus traumatisantes, avec fractures, comme la
manœuvre de COUDER (introduction de l'index de l'accoucheur sous la symphyse le long de
la face antérieure de l'humérus que l'on refoule ensuite vers l'arrière sur le dos du fœtus, ce
qui fléchit l'avant-bras sur le bras et fait extériorise le coude puis tout le bras correspondant),
ou encore la manœuvre de JACQUEMIER (= variante de la précédente, mais cette fois sur
l'épaule postérieure à laquelle on accède à la faveur de la concavité sacrée),
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
162
C. LA SOUFFRANCE FOETALE AIGUE
1) INTRODUCTION :
La souffrance fœtale aigue est un état pathologique synonyme d’asphyxie fœtale qui survient
le plus souvent au cours du travail. Elle menace la vie, l’avenir fonctionnel et psychomoteur du
fœtus
Elle serait responsable :
De mortalité périnatale dans 1/3 cas
De morbidité fœtale : les séquelles sont d’ordre neurologique : Infirmité psychomotrice et
retard intellectuel.
La SFA peut être inaugurale ou secondaire à une SF chronique
Elle est de gravité rapidement croissante
2) PHYSIOPATHOLOGIE :
La SFA est la conséquence de perturbations des échanges gazeux fœto-maternelles au cours de
l’accouchement.
Les échanges dépendent des conditions de circulation des 2 côtes de la membrane placentaire.
Il faut rappeler qu’il y a adaptation fœtale à l’anoxie jusqu’à un seuil donné en rapport avec :
Les variations au cours de contraction utérine (les besoins en O2↑) :
Si CU importante → hypoxie fœtale.
- Les variations tensionnelles : si état de choc → ↓ débit utéro-placentaire
- Les variations posturales : décubitus dorsal → compression de l’aorte, et de la veine cave
inférieur → ↓ de la circulation utéro-placentaire.
- Les variations en rapport avec une fièvre, un surmenage assimilé à un exercice physique
intense → les débits viscéraux et placentaires en détournent une partie de la masse sanguine
vers les territoires musculaires et cutanés.
Si pas de correction → hypoxie → acidose gazeuse.
Les variations métaboliques fœtales :
→ Les besoins en glucose ↑
→ Le fœtus fait appel à ses réserves en glycogène stockées dans le foie, myocarde et rein =
glycolyse anaérobie → Orientation du catabolisme glucidique vers voie anaérobique
→ Acidose métabolique, celle-ci s’ajoute à l’acidose gazeuse préexistante.
- La bradycardie constitue une réponse habituelle à l’anoxie fœtale. Cependant, il est possible
d’observer une tachycardie.
- La SFA sévère peut entraîner des lésions ischémiques parenchymateuses (redistribution du
sang fœtal aux organes nobles : cerveau, myocarde et surrénales).
- Au niveau de l’intestin, l’hypoxie entraîne une augmentation du péristaltisme intestinal
avec émission du méconium.
- Une atteinte fonctionnelle du foie ictère précoce et des troubles des facteurs de coagulation
- L‘hypoxie peut empêcher la fermeture du canal artériel.
3) ETIOLOGIES
A. Causes maternelles:
1. Perturbations locales:
- Dystocie dynamique avec hypercinésie et/ou hypertonie
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
163
- Travail prolongé : survient secondairement à des présentations céphaliques post mal
fléchies ou à une dystocie cervicale primitive.
2. Perturbations régionales:
Le décubitus dorsal peut entraîner un effet Poseiro : compression des vaisseaux abdomino-
pelviens (Aorte, Artère iliaque primitive droite) surtout au moment de la contraction utérine,
ceci entraîne une ↓ du flux utéro-placentaire.
3. Perturbations générales:
- Choc hémorragique
- Hypotension iatrogène : antihypertenseurs, analgésie péridurale
- Choc vagal
4. Hypoxie maternelle:
- Anémie sévère - Insuffisance rénale aigue
- Cardiopathie décompensée, insuffisance - Intoxication au CO
cardiaque - Apnée au cours d’une crise d’éclampsie
- Insuffisance respiratoire
B. Causes annexielles :
1. au niveau du placenta :
- Le chorio-angiome : peut réduire le passage trans-placentaire d’O2.
- Altérations membranes (infarctus placentaire) :
- Il y a réduction de la surface d’échange en cas de toxémie gravidique, HTA, Diabète ID,
Grossesse prolongée (le retentissement sur les échanges sera aggravé pendant le travail).
2. Au niveau du cordon : ↓ du courant circulatoire ombilical.
- Procidence du cordon, latérocidence, circulaire serré, bretelle du cordon.
- Anomalie de longueur (cordon court)
- Ou anomalie anatomique des vaisseaux (art ombilicale unique).
C. Causes fœtales:
Certains fœtus, du fait de leur fragilité propre, sont menacés de souffrance fœtale au cours de
l’accouchement :
- Prématurés - fœtus anémiés : Hgie (HRP, Hgie de
- Hypotrophes Benkiser, PP), Hémolyse : incompatibilité
- Jumeaux fœto-maternelle
- fœtus infectés (chorioamniotite) - Malformations fœtales
4) DIAGNOSTIC POSITIF
A. Clinique : Le diagnostic clinique repose sur 2 signes:
1. Modifications des BCF:
- Les BCF sont perçues par auscultation du cœur fœtal grâce au stéthoscope de Pinard ou au
Sonicaïd
- Rythme de base : 120 – 160 bat/min, les battements sont nets, bien timbrés en dehors des CU
- La SFA se manifeste par des troubles variés de la fréquence cardiaque :
o Tachycardie modérée ou légère 160-180 bat /min
o Tachycardie sévère ou marquée > 180 bat/min
o Bradycardie modérée ou légère 100 – 120bat/min
o Bradycardie Marquée ou sévère < 100 bat/min
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
164
2. Apparition du méconium dans le liquide amniotique :
En dehors de la présentation de siège, l’apparition de méconium frais dans le liquide
amniotique est considérée comme un signe de SFA.
Le liquide simplement tinté de vert traduit une SF chronique ou une SFA ancienne et
transitoire.
B. Examens paracliniques :
1. Monitorage obstétrical doit être systématique :
a. Enregistrement de la CU : tocographie externe ou interne (par mise d’un cathéter entre
la présentation et la paroi utérine). Les anomalies pouvant perturber les échanges fœto-
maternels :
- L’hypercinésie d’intensité : intensité totale des CU > 60mm Hg en début de travail et CU >
80mm Hg en fin de travail
- L’hypercinésie de fréquence : Fréquence des CU > 5cu / 10min
- L’hypertonie : correspond à un tonus de base > 11mm Hg en début de w et > 18mm Hg en
fin de travail (mais le diagnostic peut être clinique : Absence de relâchement de l’utérus).
b. Enregistrement de la fréquence cardiaque fœtale :
- Fréquence de base se situe normalement entre 120 et 160 bat/min
- Dans un tracé normal, il existe des oscillations dont l’amplitude est de l’ordre de 5 à 25
bat/min : tracé oscillant
- Les oscillations peuvent être absentes ou très réduites, inférieures à 5 bat/min : Il s’agit d’un
tracé plat. Ce type de tracé s’observe :
o devant une souffrance fœtale chronique sévère.
o devant un état de sommeil fœtal (le tracé devient normal après excitation fœtale).
o parfois en rapport avec l’action des médicaments utilisés pendant l’accouchement
comme les morphiniques, les barbituriques ou l’atropine.
Le rythme plat s’observe dans certaines anencéphalies, malformations cardiaques et en cas
de grande prématurité.
- Anomalies de fréquence de base :
o Bradycardie : modérée 100 – 120 bat / min, Sévère < 100 bat / min transitoires
durant plus de 3 min traduit en général une anoxie
o Tachycardie : modérée 160 – 180 bat/min, sévère > 180 bat/min
o Les tachycardies persistantes pendant tout l’accouchement sont en général
pathologiques.
o Les ralentissements périodiques : ce sont des ralentissements précoces de la
fréquence cardiaque fœtale déclenchés par les CU.
Il existe 3 types :
- Ralentissement(R) précoces ou Dip 1 : commencent avec le début de la CU
C’est un R dont le décalage est < à 20’, Ils sont synchrones avec la CU et
constitue parfois l’image en miroir.
- R tardifs ou Dip 2 : commencent après le début de la CU avec un décalage de
20-60 secondes.
Ils sont liés à l’hypoxie foetale induite.
- R. variables ou Dip 3 : débutent à des moments variables par rapport aux CU
association probable du Dip 1 et Dip 2, correspondent vraisemblablement à
l’acidose fœtale.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
165
2. Etude du pH et des gaz du sang par micro-prélèvement, au cours de la dilatation, le
prélèvement s’effectue, les membranes étant rompues, au niveau du scalp. Le sang fœtal est
recueilli dans un tube capillaire, le PH fœtal est mesuré par un PH mètre. Un pH ≥ 7,25 est
normal, 7,20 < pH < 7,25 est intermédiaire et un PH < 7,20 est pathologique.
Indiquée pour certains : en cas d’accouchement prématuré, RCIU
Si anomalie fréquence Cardiaque fœtale
Si liquide teinté en début de w
(Elle est de moins en moins utilisée car risque d’infection et de traumatisme du Scalp).
3. Dosage des lactates au Scalp fœtal :
Normal si < 5, Si > 5 : pathologique
5) DIAGNOSTIC DE LA SFA A LA NAISSANCE :
Grâce au score d’APGAR calculée à 1 min, 3 min, 5 min.
Paramètres 0 1 2
Rythme cardiaque Absent <100 > 100
Respiration Absente cri faible cri vigoureux
Tonus Flasque légère flexion bonne flexion
Réflexe Pas de réponse léger mouvement cri
Couleur Bleu ou blanc extrémités cyanosées tout rose
Si score > 7 : NNé normale, si Apgar < 3 : NNé en état de mort apparente, si 7> Apgar > 3 :
NNé souffrant.
6) PRISE EN CHARGE
A. Prise en charge prophylactique :
1. Avant le début du travail :
- Détecter les patientes dont l’accouchement par voie basse peut constituer un danger pour
l’enfant. C’est le cas des SF chroniques et des bassins chirurgicaux.
- Une césarienne prophylactique doit être décidée
- Parfois l’accouchement par voie basse peut être accepté sous surveillance rigoureuse
2. Pendant le W :
- Monitorage obstétrical systématique surtout si l’accouchement à risque
- Corriger la position maternelle :
o DLG est recommandé si non, au moins inclinée sur la gauche.
o Eviter le décubitus dorsal
- Lutter contre l’anxiété et la douleur.
o préparation psychoprophylactique à l’accouchement
o proposer parfois l’analgésie péridurale si nécessaire.
- Corriger les anomalies de la contraction utérine :
o expectative si CU régulières spontanément.
o perfusion de Sérum Glucosé + 5UI de Syntocinon pour régulariser les CU en cas
d’hypocinésie.
Dépistage précoce de la SFA :
- L’absence de trouble de la fréquence Cardiaque fœtale permet d’exclure une SFA
- La négativation des BCF ne survient jamais sans être précédée une période d’anomalie
importantes et en phase terminale d’une bradycardie sévère ± prolongée++
- L’apparition de trouble de la FCF est un signe d’alarme.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
166
B. Prise en charge obstétrical :
La SFA déclarée est une urgence, il consiste à extraire le nouveau-né par la voie la plus rapide
et dans les meilleures conditions (par voie naturelle ou par césarienne en fonction des
conditions obstétricales).
1. Moyens :
a. Césarienne :
- Rachianesthésie ou anesthésie générale
- L’analgésie péridurale est CI sauf si elle est déjà installée
- Patiente en DLG (15°)
b. Extractions instrumentales
- Les instruments utilisés, ventouse, forceps ou spatules doivent être non traumatiques.
- La prise doit être facile et l’extraction rapide
- L’opérateur doit être entraîné.
2. Indications :
a. SFA qui survient au cours de la 1ère partie du w : Césarienne
b. SFA qui survient au cours de la 2ème partie du w :
- Césarienne si conditions obstétricales défavorables (présentation haute ou mal
accommodée).
- Extraction instrumentale si dilatation complète ou presque et présentation engagée ++
- Elle permet parfois une extraction plus rapide que la césarienne.
c. Réanimation fœtale in utero ++
- Perfusion de Sérum Glucosé si w prolongé (> 8h)
- oxygénation 6 l/min
- Traitement de la pathologie maternelle : diabète, HTA, Anémie,….
7) LA SOUFFRANCE FŒTALE AU COURS DU TRAVAIL
Des arguments épidémiologiques soutiennent que les contractions utérines constituent la
circonstance idéale pour l'aggravation de la SOUFFRANCE FOETALE à cause notamment de
la compression des vaisseaux intra-myométriaux et funiculaires. Mais beaucoup d'autres
circonstances peuvent être à l'origine d'un trouble du rythme cardiaque fœtal, notamment:
- la compression de la tête fœtale au niveau du petit bassin; on a en effet calculé que la
pression pouvait atteindre 200 mmHg; et pour peu que le fœtus connaisse un problème
antérieur, une telle pression peut induire une hypoxie cérébrale;
- la compression funiculaire; elle induit une réaction polymorphe en raison de la diversité de
- vaisseaux intéressés (veine et artères); cette réaction a bien entendu une gravité fonction de
la durée, de l'importance de la pression, et de la prédominance des vaisseaux intéressés; ainsi
par exemple, la compression veineuse induit une baisse de flux sanguin vers le cœur, vers
l'aorte et la carotide (d'où l'activation des barorécepteurs et donc la tachycardie fœtale;
cependant, lorsque ce sont les artères qui sont comprimées il y a une surpression en amont
(c'est-à-dire au niveau du cœur lui-même ainsi qu'au niveau de l'aorte); on aura dans ce cas
bradycardie;
- l'hypoperfusion utéroplacentaire soit passagère soit durable; la réponse cardiaque foetale face
à cette agression, quelle qu'elle soit, est classique; l’agression retentit au niveau de la
chambre intervilleuse sous forme d'HYPOXIE + ACIDOSE; et dès qu'un certain seuil dans
les modifications physico-chimiques sanguines est atteint, on observe des phénomènes
adaptatifs sous forme d'une réaction directe (= la stimulation des baro-récepteurs et des
chémo-récepteurs) et une réaction indirecte (= stimulation du tissu nodal ou centres
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
167
automatiques du myocarde et du centre bulbaire ou centre vagal); d'où le mécanisme vaso-
moteur (VASOCONSTRICTION PERIPHERIQUE SELECTIVE et une HYPERTENSION)
tendant à protéger coeur - cerveau - surrénales - placenta qui sont des organes vitaux pour la
situation intra-utérine (la fameuse "Circulation préférentielle" au détriment des secteurs
comme la peau, et les intestins); lorsqu'elle est passagère l'hypoxie + l'hypercapnie +
l'acidose sont vite compensées; si l'hypoperfusion dure longtemps (exemple dans la
dysgravidie, l'hématome rétroplacentaire, la grossesse prolongée, le diabète sucré, et
l'incompatibilité iso-immune (Rhésus), elle provoque une réaction compensatoire de type
centralisation (brain-sparing effect + cœur) avec baisse des oscillations;
- l'effet Poseiro ou compression de la Veine-Cave inférieure; cet effet devient dangereux si la
tête est déjà engagée;
- certaines circonstances telles que l'anesthésie rachidienne induisent une hypotension, avec
hypoperfusion utéroplacentaire;
- la dysrégulation orthostatique observée durant la station debout ;
- toutes les dystocies surtout dynamique entrainant une prolongation du travail ;
- tout usage mal contrôlé d’ocytociques ;
- l’usage de médicaments antispasmodiques et analgésiques à la fin du travail car ils
provoquent la dépression de centres respiratoires du fœtus ;
- les anesthésiques généraux ont une action dépressive nécessitant une bonne oxygénation de
la mère, tandis que l’anesthésie régionale peut entrainer une hypotension maternelle qui peut
être grave pour le fœtus (d’où une perfusion IV des substances à grosses molécules).
Enregistrement du rythme cardiaque fœtal
Voici les modifications pathologiques les plus décrites au cours du ST (il s'agit en principes de
décélérations):
- précoces = débutant dès que débute la contraction utérine, c'est le DIP I ou type I
(compression de la tête ?);
- tardives = début de la modification après un petit temps de latence après le début de la
contraction, ou retard de retour au RCF de base après cessation de la contraction; c'est le Dip
II ou type II (danger|: souffrance foetale);
- variables et non systématiques = associant plusieurs types d'anomalies; c'est le Dip III ou
type III (compression du cordon ? malformation cardiaque ? ou tout simplement une bonne
réactivité du Vague si la déviation est < 20 bpm ?).
Le traitement de la souffrance fœtale au cours du travail
Il est fonction de l'état d'avancement de ce dernier.
A dilatation complète, la présentation engagée, on hâte l’expulsion grâce à une ventouse ou des
forceps.
IV.5. DYSTOCIE DUE AUX ANNEXES FOETALES
4.1. Les anomalies d’insertion placentaire
4.1.1. L’insertion basse du placenta = placenta praevia
4.1.2. L’insertion trop profonde du placenta (placenta increta et percreta)
4.1.3. L’hématome rétroplacentaire
4.1.4. Les anomalies des vaisseaux placentaires
Voir pathologies gravidiques.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
168
IV.6. LESIONS TRAUMATIQUES MATERNELLES
1. RUPTURE UTERINE
2. DECHIRURES
Du col, du vagin, de la vulve, du perinée, et les déchirures vulvo-périnéales.
3. HEMATOMES GENITAUX
Jadis thrombus génitaux, actuellement hématomes génitaux ou périgénitaux, ils sont constitués
au cours de l’accouchement sous forme de collections sanguines qui se développent sous
l’épithélium ou muqueuse vaginale, dans le tissus cellulaire de la vulve, du vagin ou du
paramètre. Ils ont une certaine tendance à la diffusion du fait du détachement et du glissement
du plan superficiel sur les plans profonds.
On distingue deux groupes
1. Hématome vulvo-vaginal ou bas- situé
Rare, il se constitue pendant l’accouchement, mais se manifeste cliniquement dans les
minutes ou les heures qui suivent l’accouchement ou la délivrance : tuméfaction vulvaire
unilatérale avec écchymose fessière.
2. Hématome vaginal
- Hématome vaginal pur : pas visible au niveau de la vulve mais senti au T.V. On note une
masse tumorale rénitente qui dévie la direction du col. Evolution vers une résorption lente
en quelques semaines. Infection rare, mais risques de rupture si gros hématome et provoque
alors une hémorragie générale qui peut s’extérioriser. Son traitement = abstention
opératoire : intervenir si augmentation surtout rapide de l’hématome, si l’hématome est cause
de dystocie, si l’hématome est douloureux, fissuré ou infecté. Dans ce cas l’incision de
l’hématome est réalisée + donner des antibiotiques + antalgiques et éventuelleement
transfusion.
- Hématomes pelviens ou haut-situés : localisés au-dessus des releveurs de l’anus. Graves,
très rares, ils sont liés à une fissure ou une déchirure du segment inférieur ; c’est une forme
de rupture utérine. Le traitement consiste en: coeliotomie + traitement de choc +
antibiothérapie.
4. DECHIRURES PERINEALES ET VULVAIRES (VULVO-PERINEALES)
Les déchirures vulvo-périnéales sont des solutions de continuité intéressant soit en même
temps et à la fois, le périnée, la vulve et le vagin (toujours en postérieur), soit isolément la
vulve seule latéralement ou antérieurement. Elles constituent des complications fréquentes de
l’accouchement, parfois graves, soit immédiatement du fait de l’incontinence du sphincter
anal, soit ultérieurement du fait du risque de développement d’un prolapsus.
1) Etiologies
Maternelles
- Atrophie périnéale (périnée mal étoffé) ou fragilité constitutionnelle.
- Pathologies : vaginite granuleuse ; périnée oedématié, infiltré ; périnée cicatriciel ;
périnées étirés des luxées.
Fœtales
- Grand volume de la tête.
- Trop grand diamètre bisacrromial.
- Certaines présentations : Occipito-sacrés (O.S) ; Déflexion ; Siège (lors de la tête dernière).
- Accouchement trop rapide.
Obstétricales
- Forceps ou ventouse.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
169
- Manoeuvres mal pratiquées ou brutalement.
2) clinique
Pas de signes fonctionnels. Seule l’inspection minutieuse de la région vulvo-périnéale
découvre ces lésions. Un examen clinique bien fait sous un bon éclairage en écartant les lèvres
vulvaires donne le diagnostic des déchirures qui sont de trois types : incomplète ou simple,
complète, et compliquée.
a) Déchirure incomplète ou simple (à 3 degrés)
- 1er degré : c’est l’atteinte de la muqueuse vaginale, du tissu conjonctif et de la musculeuse,
à partir de la fourchette vers l’anus, plus toutes ou une partie superficielle des fibres du
noyau fibreux central du périnée. Cette lésion est aussi appelée déchirure de la commissure
postérieure.
- 2ème degré : est caractérisé par des lésions de la muqueuse vaginale, du tissu conjonctif, de
la peau du périnée, des tissus du muscle bulbo-caverneux, plus la partie antérieure du
noyau fibreux central.
- 3ème degré : comporte des lésions de la muqueuse vaginale, du tissu conjonctif, de la peau
du périnée plus tous les muscles du noyau fibreux central du périnée sont lésés, mais le
sphyncter anal reste intact.
b) Déchirure complète
Lésions ci-dessus plus le sphyncter anal qui est aussi lesé : tous les tissus musculaires et
conjonctifs ont disparu, seule la muqueuse rectale reste intacte. Le toucher rectal ne soulève
que la muqueuse rectale.
c) Déchirure complète compliquée
C’est quand le sphyncter anal est aussi sectionné, plus une lésion plus ou moins étendue de la
muqueuse ano-rectale de 2 - 5 cm : les deux canaux (vagin et rectum) communiquent
largement. Cette lésion est appelée CLOAQUE.
5. DECHIRURE CENTRALE OU INTERSTITIELLE DU PERINEE
C’est une lésion rare, trompeuse, seule la peau du périnée est intéressée, éraillure, et
muqueuse vaginale est intacte. Suite à une mauvaise direction pendant le dégagement, la tête
foetale vient buter contre le milieu du périnée qu’elle rompt entre la commissure postérieure
et l’anus en laissant en avant un pont de tissu, la muqueuse vaginale intacte. Entre les deux
doigts pour palper le périnée postérieur, on sent :
- la rupture du noyau fibreux central du périnée associée à ;
- l’élongation des muscles transverses et ;
- une déchirure des élévateurs de l’anus, avec risque fréquent de prolapsus.
6. LESIONS VULVAIRES SEULES
Isolées ou associées aux lésions périnéales :
- déchirure hyménéale après la déformation on a des caroncules multiformes ;
- déchirure clitoridienne : mauvaise technique de dégagement, lésion très hémorragique ;
- déchirures latérales nymphéales : déchirure verticale de la petite lèvre ; rupture de la petite
lèvre.
Traitement
- Prophylactique : appliquer correctement la technique de l’expulsion ; épisiotomie au moindre
signe de déchirure.
- Curatif : suture de chaque lésion sous xylocaïne 2% ou sous anesthésie rachidienne +
antibiothérapie et soins locaux (ablation des fils non resorbables sur la peau au 7ème jour).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
170
IV.7. INVERSION UTERINE
1. INTRODUCTION
Incidence : 1 sur 10.000 à 20.000 accouchements.
2. ETIOLOGIE
- Pression sur le fundus ou traction sur le cordon lorsque l’utérus est relâché.
- Augmentation subite de la pression intra-abdominale lors d’efforts de toux ou de
Vomissements.
- Tentative d’extraction d’un placenta non clivé lors de la délivrance artificielle.
- Cordon court.
3. CLINIQUE
Une inversion incomplète (fundus restant dans la cavité utérine) peut être difficile à
diagnostiquer et se manifeste le plus souvent par de saignements persistant dans le post
partum. Rarement elle peut se transformer secondairement en inversion complète.
Le choc grave hypovolémique et neurogène est la manifestation la plus importante de
l’inversion complète et peut s’accompagner de douleurs abdominales sévères avec envie de
pousser.
4. TRAITEMENT
- Réduction manuelle : si elle a lieu immédiatement après l’inversion, elle peut se pratiquer
sans anesthésie ; sinon elle s’effectue sous narcose (Fluotane).
- Empaumer le fond utérin en plaçant les doigts à la jonction du col et du corps. Délivrance du
placenta avant ou après la manœuvre.
- Méthode de Johnson : empaumer le fond utérin le bout des doigts étant au niveau des culs-
de-sac cervico-corporeaux. Le tout est remonté en bloc au delà du petit bassin jusqu’au
niveau de l’ombilic. Maintenir cette position pendant 3 à 5minutes.
- Méthode de O’Sullivan (plus compliquée).
- Correction chirurgicale par laparotomie en cas d’échec : exercer une traction par la pince sur
la paroi postérieure ou les ligaments ronds :
o la technique de Haultain = inciser la face postérieure de l’anneau de contraction après
laparotomie
o la méthode de Spinelli = l’intervention se pratique par la voie vaginale. Inciser la face
postérieure de l’anneau de contraction sans pratiquer la laparotomie. Toute l’opération se
déroule dans le vagin.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
171
IV.8. PATHOLOGIES DU POST-PARTUM
I. FIEVRE PUERPERALE
1) ETIOLGIE
- Infection génitale
- Infection mammaire
- infection urinaire
- infection de plaies traumatiques
- paludisme
- Thrombophlébite
- Autres
Le texte n’abordera que les deux premières étiologies, les autres ayant déjà été traitées ailleurs.
A. Infection génitale
Il s’agit surtout de l’endométrite du post-partum, grande tueuse autrefois (cfr histoire de
Semmelweiss), et encore parmi les trois plus grandes causes de mortalité maternelle dans le
monde.
La porte d’entrée est représentée par la plaie cavitaire et des solutions de continuité réalisées
par les lésions des parties molles.
Les germes les plus incriminés sont essentiellement bactériens :
- bactéries endogènes (= présentes sur le corps même le la femme) ; ex. au niveau du périnée,
du vagin, et des intestin (anus – rectum) ; ce sont les coliformes, les entérocoques (=
streptocoque fécalis), les anaérobes (streptocoques), le gonocoque, le chlamydia, etc…
- bactéries exogènes (rencontrées sur le lieu du travail et de l’accouchement) ; ex. au niveau
des narines, de la gorge et des mains du personnel soignant ou d’autres parturientes ; c’est le
cas du streptocoque β-hémolytique du groupe A, et du staphylocoque doré.
La gravité de la maladie est fonction de la virulence du germe, de l’association microbienne
éventuelle, de la résistance propre de la parturiente, et de l’étendue des lésions constituant la
porte d’entrée microbienne.
Cette gravité est représentée comme suit :
- infection légère ; elle concerne le vagin, le col et l’utérus ;
- infection modérée ; elle concerne aussi les trompes et binetôt le pelvis ;
- infection sévère ou grave ; c’est soit une péritonite, soit une septicémie, soit les deux.
La clinique (symptomatologie et diagnostic) est généralement précédée d’un contexte
suggestif constitué des éléments ci-après :
- travail prolongé, avec multiplicité de touchers vaginaux ;
- conditions hygiéniques défectueuses dans la salle de travai et/ou d’accouchement ;
- lésions de parties molles ; ex. déchirures, épisiotomie ;
- rupture prématurée des membranes, avec risque de chorio-amniotite.
La symptomatologie comprend :
- la fièvre, souvent endéans les 24 premières heures (ce qui la distingue de la fièvre due à la
montée laiteuse), mais peut aussi apparaître plus tardivement ;
- l’élévation du pouls ;
- les signes loco-régionaux ;
- les lochies purulentes dans la forme purulente, et sanglantes dans la forme hémorragique
(plus tardive = à partir du 12ème jours.
La lochiculture vient identifier le ou les germes.
La prise en charge va consister en :
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
172
- une antibiothérapie préventive dans toutes situations à risque infectieux (voir ci-dessus) ;
antibiotiques dès la 6ème heure après RPM ; ou 30 minutes avant la délivrance, ou après
clampage du cordon lors de la césarienne) ;
- antibiothérapie curative (ampicillinine ou érythromycine ou céphalosporines, toutes les 6
heures, en association avec le 500 mg de métronidazole toutes les 8 heures ;
- anti-inflammatoires ;
- utérotoniques ;
- parfois benzoate d’oetradiol pour assurer une bonne trophicité de l’endomètre.
Attention ! Pas d’irrigation vaginale !!!!!
B. Infection mammaire
Elle est à distinguer de l’engorgement mammaire (2 – 3ème jour), qui s’accompagne de
circulation collatérale, de douleur, fièvre, avec parfois la présence de nodules douloureux. Son
traitement est fait d’antalgiques, de succion éventuellement soutenue par un tire-lait.
La mastite du post-partum peut débuter à tout instant ; Elle est provoquée par le staphylocoque
doré, et se manifeste par une tension mammaire douloureuse localisée et une fièvre. Il faut
stopper l’allaitement et donner antibiotiques et anti-inflammatoires. Elle peut prendre des
allures parfois susceptibles de semer la confusion avec le cancer, avec peau d’orange
(danger !!!!).
L’abcès mammaire est généralement consécutif à une rétention de lait au niveau des canaux
galactophores (galactocèle). La galactocèle se présente sous forme de kyste à aspirer ou à
inciser sous couverture d’antibiotique + examen cytobactériologique. L’abcès, lui, est à inciser
(incision radiaire ? aréocirculaire ?) sous couverture d’antibiotique, en veillant à ce que tous les
septa de l’abcès soient crevés au doigt.
Les raghades et le crévases au niveau du mamelon sont des lésions suceptibles de s’infecter.
On les soigne en badigeonnant les lésions avec de la glycérine boratée. Si la succion n’est pas
très douloureuse, l’allaitement peut se poursuivre durant le traitement.
II. HEMORRAGIE DU POST-PARTUM (OU DE LA DELIVRANCE)
1. DEFINITION
L'hémorragie de la délivrance est une perte de sang supérieure à la quantité physiologique
(500ml), survenant après l'accouchement et dans les 24 heures qui suivent celui-ci.
L'origine de celle-ci n'est pas forcément une hémorragie de la délivrance proprement dite
(saignements provenant d'une mauvaise hémostase au niveau de la zone d'insertion placentaire
intra-utérine), mais un élargissement de la définition couramment acceptée inclut :
- tous les saignements d'origine génitale, souvent traumatiques (utérus, col, vagin et périnée) ;
- ainsi que les troubles de l'hémostase qui peuvent être primitifs, mais aussi secondaires aux
précédents (conséquences et complications d'une hémorragie massive et/ou persistante).
2. DIAGNOSTIC
En cas d’hémorragie extériorisée :
Hémorragie génitale abondante après l’accouchement (> 500 cc en 24 heures),
l’accouchée baigne dans le sang sur son lit (la difficulté est la quantification)
s'organiser au cours de tout accouchement pour le recueil le plus complet possible des
pertes sanguines par voie génitale doit être un principe. Un récipient spécialement prévu
à cet effet existe sur les tables d'accouchement ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
173
la quantification ne doit pas négliger les pertes sanguines " camouflées " : champs,
linge, garnitures, compresses, qui doivent être pesées s'il y a une suspicion d'hémorragie
En cas d’hémorragie non extériorisée :
Le diagnostic de la perte sanguine peut être ignoré si les pertes ne sont pas ou sont
incomplètement extériorisées :
Circonstances :
→ inertie ou atonie utérine avec accumulation de caillots intra-utérins :
C'est le contrôle régulier du globe utérin (dit " globe de sécurité ") qui ne doit pas dépasser le
niveau de l'ombilic, mais surtout ne pas augmenter de volume ; un geste simple consiste à
l'exprimer afin d'extérioriser le contenu Éventuel (caillots que l'on peut peser) ;
→ formation d'hématomes pelviens dans les suites de lésions traumatiques.
Le saignement n'est alors pas toujours extériorisé, du fait qu'il est représenté par un hématome
péri génital dont le diagnostic n'est fait ni par le saignement extériorisé ni par la visualisation
objective de celui-ci au niveau périnéo-vulvaire.
Le diagnostic est alors fondé sur la survenue :
→ de douleurs devenant souvent intolérables (tension pelvi-périnéale) ;
→ surtout d'un retentissement maternel :
Autres signes :
Signes d’anémie (pâleur cutanéo-muqueuse, dyspnée), voire signes de choc (ho.T.A.,
soif, pouls rapide et filant) avec parfois un collapsus cardio-vasculaire.
Altération de l’état général
3. CAUSES DES HEMORRAGIES DE LA DELIVRANCE
Il existe trois causes principales :
une pathologie de la délivrance, le saignement provenant de la zone d'insertion
placentaire, dont l'hémostase ne s'est pas bien faite pour différentes causes ;
une lésion génitale traumatique (utérine, principalement cervicale et/ou vaginale
et/ou périnéo-vulvaire) ;
une pathologie de l'hémostase :
→ parfois conséquence de pathologies obstétricales graves (hématome rétroplacentaire,
mort fœtale, chorio-amniotite non traitée, embolie amniotique) ;
→ mais surtout d'hémorragies de la délivrance que l'on a laissées s'aggraver :
diagnostic non fait ou trop tardif ayant pour conséquence une perte sanguine
importante et des troubles de coagulation secondaires.
a) PATHOLOGIE DE LA DELIVRANCE
Elle est essentiellement représentée par la Rétention placentaire. Dans ce cas, l’hémorragie
peut être due à des :
1) Troubles dynamiques
l'inertie utérine est la conséquence d'une absence de délivrance physiologique : absence de
survenue des contractions utérines survenant dans la phase de décollement faisant suite la
période de repos dite " physiologique " :
o différents facteurs favorisants sont retenus :
Épuisement musculaire chez les grandes multipares du fait d'un travail prolongé,
atonie après un accouchement trop rapide,
surdistension de l'utérus (grossesse gémellaire, hydramnios, macrosomie fœtale),
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
174
pathologie utérine modifiant la contractilité de celui-ci (fibromes, malformations),
inertie iatrogène (utilisation des bêtamimétiques, anesthésie au fluothane, arrêt des
ocytociques après expulsion de l'enfant) ;
l'hypertonie utérine est responsable d'un enchatonnement placentaire (rétention du
placenta décollé au-dessus de la contracture) :
o cette contracture peut être cervicale (enchatonnement global) ou localisée, souvent au
niveau d'une corne ;
o cette hypertonie est souvent iatrogène : Injection inadéquate d'ocytociques (délivrance
dirigée trop tardive) ; ou expression utérine incongrue avant le décollement
placentaire (ne jamais effectuer avant que l'on ait confirmé le décollement placentaire
par la manœuvre du refoulement sus-pubien, remontant le fond utérin vers l'ombilic, sans
constater de ré-ascension du cordon au niveau de l'orifice vulvaire).
2) Anomalies placentaires
L'hémorragie peut être due à:
des anomalies d'insertion placentaire : adhérences anormales, essentiellement
représentées par le très rare placenta acreta (villosités placentaires adhérant au myomètre
sans interposition des caduques basales), ou percreta (avec villosités placentaires
traversant tout le myomètre jusqu' la séreuse utérine) :
o elle peut concerner une partie ou l'ensemble de la zone d'insertion placentaire ;
o certains facteurs sont considérés comme favorisants :
insertion placentaire sur une cicatrice utérine,
une synéchie,
une Adénomyose ;
séquelles d'endométrite ;
curetages abrasifs multiples) ;
les anomalies morphologiques du placenta :
o persistance de la totalité ou d'un fragment de placenta dans la cavité utérine ;
o cotylédons accessoires (aberrant) séparés du gâteau placentaire principal ;
les localisations anormales du placenta :
o principalement, l'insertion basse du placenta (objectivée par la mesure du petit côté des
membranes qui est inférieur à 10cm lors de l'examen du délivre). Les contractions
utérines ne font alors pas bien l'hémostase de la partie de l'insertion placentaire qui se
trouve sur le segment inférieur, celui-ci ne bénéficiant pas de la rétraction du corps utérin;
o plus rarement, l'insertion placentaire sur une cloison d'un utérus malformé.
3) Fautes techniques
Rappelons que certaines fautes techniques ou manœuvres intempestives pratiquées avant la
délivrance et souvent dans le but de l'accélérer peuvent être la base d'hémorragies :
arrêt des ocytociques utilisés pendant le travail, après expulsion de l'enfant, alors que ceux-
ci doivent être gardés au même débit ;
expression utérine avant le décollement placentaire ;
traction sur le cordon.
4) Inertie utérine
L'inertie utérine (atonie utérine) faisant suite à une délivrance normale peut être cause de
saignements après l'expulsion d'un placenta complet (surdistention utérine).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
175
5) Inversion utérine
Complication devenue rarissime, c'est l'invagination du fond utérin en doigt de gant dont on
décrit trois degrés : elle est souvent le fait de manœuvres intempestives (traction sur le cordon,
expression utérine violente).
b) LESIONS GENITALES TRAUMATIQUES
1. Ruptures utérines
Les ruptures utérines sont définies comme une solution de continuité non chirurgicale de
l'utérus.
Leurs causes sont :
une altération de la paroi utérine : principalement une cicatrice utérine
(césarienne, myomectomie avec ouverture de la cavité, antécédents de perforation
ou rupture suturée), ou un utérus fragilisé (grande multiparité, curetages répétés) ;
la disproportion fœto-pelvienne, la rupture survenant alors l'issue d'un travail
prolongé, mal surveillé, le plus souvent chez la femme multipare ;
les ruptures iatrogènes :
o manœuvres obstétricales (version par manœuvre interne principalement) ;
o extractions instrumentales (lors de la pose de cuillères ou avant dilatation complète en
particulier dans l'extraction de la tête dernière) ;
o administration intempestive d'ocytociques, dans les disproportions fœto-pelviennes.
2. Déchirures du col
Ce sont les solutions de continuité non chirurgicales du col utérin, survenues au moment de
l'accouchement ; même si elles ne remontent pas jusqu'au segment inférieur et qu'elles sont
strictement cervicales, elles peuvent être très hémorragiques.
Rarement dues à une pathologie du col (cancer), elles sont le plus souvent iatrogènes : la
parturiente ayant poussé trop tôt, une extraction instrumentale ayant été pratiquée avant
dilatation complète, en particulier sur la tête dernière dans la présentation du siège.
3. Déchirures du vagin
Les déchirures du vagin sont de diagnostic facile lorsqu'elles prolongent une déchirure
périnéo-vulvaire.
En fait, elles sont plus souvent diagnostiquées lors de la révision sous valves.
L'hémorragie qui en découle peut être sous-estimée, du fait de la constitution d'un
hématome dans les tissus celluleux périvaginaux.
Les facteurs favorisants sont :
o une malformation vaginale non diagnostiquée et non corrigée avant la grossesse ;
o une cicatrice vaginale antérieure ;
o une vaginite ;
o un accouchement dystocique souvent associé à des manœuvres instrumentales.
4. Déchirures vulvaires et périnéales
Les déchirures vulvaires et périnéales sont rarement responsables d'hémorragies graves, mais
la base d'une spoliation sanguine parfois non négligeable, surtout si l'on tarde les réparer. C'est
donc une cause cumulée plus qu'une cause directe.
c) TROUBLES DE L'HEMOSTASE
Les troubles de l'hémostase peuvent exister au cours de certaines pathologies
obstétricales :
o hématome rétroplacentaire, dans le cadre de dysgravidie ou non ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
176
o mort fœtale in utero ;
o chorio-amniotite ;
o embolie amniotique.
Ce sont, plus souvent, les complications d'une hémorragie grave de la délivrance, dont le
diagnostic a été tardif ou sous-estimé, ou qui a été mal jugulée.
Dans ces circonstances survient une coagulation vasculaire disséminée, dont découlera
une fibrinolyse.
4. TRAITEMENT ET CONDUITE TENIR
a. Traitement préventif
L'idéal est le traitement préventif qui est fondé sur le respect de certaines règles de sécurité.
Le traitement préventif de l'inertie utérine :
o peut être orienté par des facteurs de risque, surdistension utérine, grande multiparité
pour certains, systématique, pour d'autres auteurs ;
o consiste en l'injection de 10 unités d'ocytocine (Syntocinon*), par voie
intramusculaire directe lors du dégagement des épaules dans les présentations
céphaliques (délivrance assistée);
o l'utilisation de Méthergin*, de la même façon, est moins recommandée du fait des
contre-indications (hypertension artérielle, pathologie vasculaire, présence de
myomes utérins).
Respecter la physiologie de la délivrance, en évitant les tractions intempestives sur le
cordon, massage ou expression utérine inadéquats.
Pratiquer une délivrance artificielle en l'absence de délivrance spontanée 30 minutes
après l'accouchement.
Examiner très soigneusement le délivre qui, s’il est incomplet, doit faire pratiquer une
révision utérine sans tarder.
Rechercher et suturer immédiatement toutes les déchirures des parties molles.
b. Traitement curatif
1. Moyens thérapeutiques : les utérotoniques
Les ocytociques (Syntocinon*), utilisables sous forme :
o de perfusion (10 unités dans 1000ml de sérum glucosé 5%) ;
o d'injection IV directe (10 unités) ;
o d'injection IM (10 unités) dont l'effet n'est alors obtenu qu'au bout de 10 15 minutes ;
o d'injection intramurale (intramyométriale) au travers de la paroi abdominale sous contrôle de
la main introduite dans la cavité utérine, en cours de révision utérine ;
le Méthergin* est utilisé par certains auteurs, bien que contre-indiqué en cas de pathologie
vasculaire, d'hypertension artérielle ou de la présence de myomes utérins.
Les prostaglandines : prostaglandine E2 (Nalador*) :
o en perfusion à la seringue électrique (1 ampoule dans 50 cm3 passer en 2 à 5h), d'efficacité
immédiate ;
o les voies intramusculaire et intraveineuse directe sont strictement interdites.
2. Les moyens mécaniques
En cas d'échec des traitements médicaux et pour des hémorragies graves n'ont plus de place
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
177
dans les structures techniquement équipées ou l'embolisation artérielle peut être réalisée :
le tamponnement intra-utérin par des champs ou le poing ganté de l'opérateur ;
application de pince de Muzeux sur le col de l'utérus pour effectuer une traction avec ou
sans rotation pendant quelques heures (par diminution du débit artériel utérin) ;
Ces moyens peuvent Éviter une issue chirurgicale dans les hémorragies graves et rebelles,
permettant la constitution du clou plaquettaire.
3. Les traitements chirurgicaux
Rarement utilisés (lors de l'Échec des autres méthodes), peuvent être :
La ligature des artères hypogastriques, surtout chez les femmes jeunes désireuses de
grossesses ultérieures. Elle ne met pas en danger l'avenir de l'utérus ;
La ligature des artères utérines
Le B-Lynch
L'hystérectomie d'hémostase, solution radicale qui doit rester exceptionnelle ;
rappelons les sutures des lésions traumatiques : utérines, cervicales, vaginales et
Volvo-périnéales ;
actuellement, et à proximité d'un radiologue entrainé et équipé, l'embolisation
artérielle est une solution à privilégier.
4. Les traitements médicaux des troubles de la coagulation
traitement substitutif des facteurs manquants : plasma frais congelé ;
pour certains cliniciens, le fibrinogène garde encore des indications ;
la transfusion permet la compensation de la spoliation sanguine, mais doit être bien
réfléchie.
III. ENDOMETRITE DU POST-PARTUM
1. DEFINITION
C'est une infection puerpérale (l'inflammation de l'endomètre et du myomètre dans les suites
des couches). L'origine des germes peut être:
Exogène: la cavité utérine par le non-respect de l'asepsie (instruments souillés, les gestes de
l'accoucheur);
Endogène: les germes proviennent le plus souvent du vagin.
Certains facteurs favorisent l'infection:
La rupture prématurée des membranes;
La durée du travail;
L'attitude locale des tissus et les manœuvres endo-utérines.
2. DIAGNOSTIC
Il est essentiellement clinique
Signes cliniques:
La fièvre, les lochies fétides.
A l'examen: altération de l’état général, subinvolution utérine avec un col ouvert; douleur à la
palpation et à la mobilisation de l’utérus
NB : l’odeur nauséabonde dans la chambre de l’accouchée est un élément qui doit attirer
l’attention
Diagnostic biologique:
Culture des lochies.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
178
3. TRAITEMENT
a) Objectifs thérapeutiques
Juguler l'infection (AB)
Favoriser l’évacuation des lochies (utérotoniques)
Baisser la fièvre (antipyrétiques) et Calmer la douleur (antalgiques).
b) Conduite à tenir
i. Ce qu'il faut faire
Antibiothérapie probabiliste, à large spectre et en association (tenir compte des anaérobies)
β lactamines (amoxycilline) +Aminosides (gentamycine)
Céphalosporines (cefotaxime, ceftriaxone) + dérivés imidazolés (métronidazoles)
Quinolones (ciprofloxacine) + dérivés imidazolés (métronidazoles)
Antibiothérapie à adapter après culture et antibiogramme
ii. Ce qu'il ne faut pas faire
Ne pas faire de prélèvement (Hémoculture, examen de lochies) pour isolement et
identification de l'agent causal quand cela est possible.
Utiliser un seul antibiotique dont le spectre d'action n'est pas assez large
c) Mesures préventives
Asepsie strict pendant les accouchements;
Eviter les touchers répétés, la prolongation excessive de travail, les manœuvres utérines
traumatisantes.
IV. MALADIES TRHOMBOEMBOLIQUES DANS LE POST PARTUM
Terrain favorisant:
- ATCD maladies TBE - Anémie, hémorragie de la délivrance
- Infection puerpérale - Insuffisance veineuse
- Immobilisation prolongée - Césarienne
a) Phlébite du MI:
Survient vers le J5-J7, pouls grimpant de Malher, Fièvre à 38°C, douleur de la face post de
jambe ou de la cuisse.
b) Phlébite pelvienne:
Thrombose de la veine ovarienne, survenant vers le J5, T° 39-40°C, tableau septique sévère,
douleur au TV, le plus souvent localisation droite. Savoir y penser!
V. MALADIES LIEES A L’ALLAITEMENT
a) Engorgement : survient vers J2-J3 lors de la montée laiteuse :
Seins durs, tendus et douloureux
ttt = décongestion par massage et vidange sous douche tiède + antalgiques (paracétamol).
b) Crevasse : Fissurations rouges et douloureuses à la base ou au sommet du mamelon
Facteurs de risque : mauvaise position d’allaitement, problème d’hygiène
ttt préventif: nettoyage strict avant et après chaque tétée, protection sèche et
stérile, application en fin de tétée
ttt curatif: crème à base de Vitamine A et E avec anesthésique local, arrêter
l’allaitement du côté atteint
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
179
c) Lymphangite : inflammation du réseau lymphatique dermo-épidermique
Facteurs de risque : engorgement, crevasse
Diagnostic: J2-J8, T° 39-40°C, placard inflammatoire triangulaire allant vers
aisselle, sans signe d’abcès
ttt: l’allaitement maternel peut être poursuivi, localement cataplasmes
d’Antiphlogistine*, Antiinflammatoire (Aspirine), pas ATB.
d) Galactophorite : 1er stade de complication glandulaire
Diagnostic: douleur et rougeur du sein, signe de BUDIN (issue de pus à la
pression du mamelon), T° 38°C, germe staphylocoque,
ttt= suspension de l’allaitement du côté atteint avec désengorgement de ce
sein, Anti inflammatoire, ATB Rovamycine* secondairement adapté.
e) Abcès du sein : stade ultime de la complication glandulaire
Diagnostic: douleur vive, pulsatile et insomniante, T° 39°C, tuméfaction
inflammatoire
ttt: Arrêt AM, drainage chirurgical
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
180
IV.9. THERAPEUTIQUE OBSTETRICALE
1. INTRODUCTION
En dehors du fer, des vitamines, des anti-émétiques, anti-acides gastriques, antihistaminiques,
analgésiques, antimicrobiens, antihypertenseurs, tranquillisants, diurétiques et autres souvent
administrés à la femme enceinte, et dont les effets (y compris tératogène) doivent toujours
êtres connus, une mention particulière doit être réservée à la notion de SOINS
OBSTETRICAUX D’URGENCE.
En effet, chaque année dans le monde, près de 600 000 femmes meurent de complications
liées à la grossesse, et beaucoup d’autres encore sont rendues invalides par des conditions
telles que des douleurs chroniques, la fistule, une réduction de leur mobilité, des lésions de
l’appareil génital et la stérilité. Depuis plusieurs décennies, les programmes de santé
maternelle ont recours aux examens de dépistage prénatals pour tenter de repérer les femmes
qui courent un risque de complications. Quoique bénéfiques à bien des égards, ces efforts
n’ont pas permis de réduire les taux de mortalité maternelle, car c’est très souvent au cours de
l’urgence obstétricale que les plus graves complications surviennent, même chez des
gestantes reconnues sans risque jusque là.
Il a été identifié trois types de retards qui peuvent avoir une incidence sur les chances d’une
femme de survivre à une urgence obstétricale (Thaddeus et Maine, 1994). Les deux premiers
types (retard dans la décision de consulter un prestataire quand les signes d’alarme
apparaissent et retard à atteindre un établissement de santé) reflètent, du moins en partie,
des facteurs sociaux sous-jacents (manque de ressources, infrastructure déficiente, manque
d’établissements adéquats, statut dévalorisé des femmes, prise de décision familiale
concernant l’accouchement) qui interviennent en dehors de l’établissement et aboutissent
parfois à des urgences contre lesquelles le personnel médical ne peut rien faire. Ceci peut être
très frustrant.
Le troisième type de retard (retard de soins une fois que la femme arrive à
l’établissement) est souvent sous contrôle du personnel de santé. Et étant donné que les
causes physiques directes des décès maternels (hémorragie, complications de l’avortement
pratiqué dans des circonstances dangereuses, septicémie/infection, troubles hypertensifs,
dystocie par obstacle mécanique) peuvent être traitées, il a été défini un paquet de mesures de
base susceptibles de réduire la mortalité : ce sont les soins obstétricaux de base.
Les soins obstétricaux d’urgence sont souvent décrits en termes de soins « de base » et de
soins «complets» qu’un établissement peut offrir à une femme qui présente des complications
obstétricales.
Les services obstétricaux de base (SOU ou SONUB) comportent les fonctions capitales
suivantes :
- administration parentérale des antibiotiques ;
- administration d’ocytociques ;
- administration parentérale des anticonvulsivants pour la pré-éclampsie et l’éclampsie ;
- extraction manuelle du placenta ;
- extraction manuelle des produits non évacués (par exemple aspiration manuelle
intrautérine),
- accouchement naturel dirigé
Les services complets (SONUBC) comprennent ces 6 fonctions et ajoutent 2 autres fonctions,
à savoir :
- opération chirurgicale (par exemple césarienne) ;
- transfusion sanguine.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
181
Un établissement de SOU de base est un établissement qui peut exécuter à tout moment
toutes les fonctions 1 à 6, tandis qu’un établissement de SOU complets exécute toutes les
fonctions 1 à 8.
2. INTERVENTIONS OBSTETRICALES
A. EXPRESSION ABDOMINALE
C’est une manoeuvre appliquée par un aide pris parmi le personnel médical qui renforce les
contractions utérines vers la fin de l’accouchement et qui constitue une force supplémentaire
d’expulser le foetus. Pratiquée trop tôt ou trop longtemps, elle peut provoquer certains
accidents (complications) tels que :
- déchirures du périnée par sortie trop brusque du fœtus ;
- compression placentaire d’oû souffrance fœtale ;
- décollement du placenta et embolie amniotique.
Les conditions de son usage sont : la dilatation complète du col + la présence de la
présentation à la vulve.
Indication : manque de progression de mobile foetal pendant l’expulsion alors que la
présentation est au niveau du périnée, dans l’accouchement du Sommet ou du Siège. Elle est
aussi utilisée comme complément des autres méthodes telles que forceps, épisiotomie, et
ventouse.
Contre- indications :
- si toutes les conditions de l’expulsion sont favorables ;
- expulsion rapide spontanément ;
- manque d’ampliation progressive du périnée.
Technique
- Parturiente sur la table d’expulsion.
- L’aide exerce, uniquement à la demande de l’accoucheur, qui dirige l’accouchement,
l’expression sur le fond de l’utérus ; avec les paumes de ses 2 mains réunies en cupule
pendant les contractions utérines suivant l’axe du bassin jusqu’à la sortie de la tête de
l’anneau vulvaire. Le reste de l’accouchement est assuré par l’accoucheur seul. C’est la
manœuvre de Christeller.
B. RUPTURE ARTIFICIELLE DES MEMBRANES (RAM)
1. Définition
C’est une petite intervention obstétricale consistant à réaliser une solution de continuité des
membranes ovulaires à travers l’aire de dilatation du col, d’où suppression de l’intégrité de
l’oeuf avec sortie du liquide amniotique.
2. Indications
En dehors du travail, à condition que les membranes soient accessibles :
- déclenchement du travail ;
- placenta praevia latéral ou marginal saignant ;
- hématome retro-placentaire ;
- polyhydramnios (ponction des membranes).
Pendant le travail :
- dilatation stationnaire du col alors que les autres facteurs sont normaux notamment le
bassin, présentation régulière du foetus, les contractions utérines ;
- dilatation complète avant de faire pousser ou d’appliquer une ventouse ou forceps ;
- accouchement provoqué ;
- accouchement dirigé (Epreuve du travail qui ne commence qu’après l’ouverture de l’œuf) ;
- DPPNI ;
- dystocie dynamique.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
182
3. Contre-indications
- Présentation transversale ou oblique.
- Mort foetale in utéro car risque important d’infection amniotique.
- Présentation du siège ou de face.
- Dilatation du col moins de 4 cm sauf dans le DPPNI ou placenta prævia latéral ou marginal.
4. Complications
- Procidence du cordon.
- Présentation dystocique dans le polyhydramnios.
5. Technique
C’est en fonction de la dilatation du col utérin (TV)
- Mettre 1 ou 2 doigts dans le vagin jusqu’au contact et sous les membranes ou de la poche
des eaux.
- Introduire une demie-paire de la pince de Kocher ou de Pozzi ou un instrument pointu.
- Gratter sur les membranes pour les rompre.
- Freiner avec un doigt l’écoulement rapide ou brutal du liquide amniotique pour éviter une
procidence du cordon.
- Elargir l’ouverture des membranes.
C. EPISIOTOMIE OU PERINEOTOMIE
1. Définition
L’épisiotomie ou périnéotomie est une intervention obstétricale mineure par voie basse,
consistant en une incision aux ciseaux droits (longue de 2- 4 cm), au niveau de l’anneau
vulvaire et touchant le périnée et et le vagin, dans le but d’élargir l’ouverture vulvaire et de
permettre la sortie aisée de la présentation.
En outre l’épisiotomie représente ainsi un traitement véritable de prévention des déchirures
périnéales plus ou moins complexes délabrant la vulve et le périnée. Elle prévient aussi les
prolapsus de l’âge mur. La fréquence de l’épisiotomie est variable selon les écoles.
Il existe plusieurs types d’épisiotomie:
- épisiotomie médiane = section selon l’axe du milieu qui respecte les vaisseaux et les nerfs
de la vulve, mais elle ne met pas toujours à l’abri le rectum ; il y a donc risque de
l’élongation de l’incision vers le sphyncter anal;
- épisiotomie latérale; elle peut blesser la glande de Bartholin et la suture est plus difficile
vue la rétraction des muscles;
- épisiotomie médio-latérale ; c’est le type le plus couramment pratiqué et recommandé;
l’incision, part obliquement en angle de 45° de la commissure postérieure de la vulve ; cet
angle de 45° avec l’axe vulvo-anal rend la réparation aisée et épargne le sphyncter anal;
épisiotomie bilatérale, avec double incision droite et gauche, mais qui est à proscrire.
2. Les indications d’épisiotomie
Elles sont de 3 ordres : maternel, foetal et instrumental.
Elles ont dites maternelles en cas de risque de lésion du périnée maternel au cours de
l’expulsion :
- anomalies du périnée
o étroitesse de la vulve peu extensible;
o atrésie du périnée;
o excès de longueur du périnée vulnérable;
- menace de déchirure, comme fréquemment en cas de
o périnée court et tendu dans les bassins des luxées;
o périnée fragile des infectées;
o périnée oedématié des protéinuriques ou lors d’un travail prolongé;
o périnée cicatriciel;
o excès des diamètres fœtaux par excès de volume foetal ou lors de certaines
présentations (face, occipito-sacrée, bregma, siège, dystocie des épaules).
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
183
Elles sont foetales dans les circonstances suivantes:
- souffrance foetale due à la longueur exagérée de la période de l’expulsion ;
- fragilité du foetus prématuré, hypotrophe ou postmature ; l’épisiotomie permet la sortie
rapide de la tête foetale et de protéger le crâne du prématuré contre les butées périnéales.
Les indications instrumentales se rapportent aux cas où l’épisiotomie constitue un temps
complémentaire de certaines interventions : forceps, ventouse ou spatule, version par
manoeuvres internes.
3. Conditions d’application de l’épisiotomie
- Période d’expulsion fœtale.
- Périnée distendu et la tête apparente dans l’anneau vulvaire.
- Matériel de suture à portée de main (porte-aiguille, pince anatomique ou pincette, Kocher et
ciseaux, compresses stériles, anesthésie locale ou générale, de fils de suture absorbable
(catgut ou vycril) et non résorbable (nylon ou crin), une autre paire des gants que ceux qui
ont servi à l’accueil du nouveau-né, désinfectants.
4. Inconvenients
- Déchirure du périnée qui rend la réparation plus difficile si l’épisiotomie a été insuffisante.
- Hémorragie plus importante (surtout si la présentation est siège) par rapport à un
accouchement normal.
- Lâchage de l’épisiotomie si mauvaise technique ( bords non ajustés) ou mauvaise qualité
des Fils.
- Infection de la plaie de l’épisiotomie.
- Si la cicatrisation est inesthétique,elle détermine la vulve peu symétrique.
- La cicatrice est souvent douloureuse et constitue alors une cause de dysparéunie.
5. Technique
Au cours de l’expulsion, sur la table d’accouchement, les manipulations de l’épisiotomie se
résument comme suit ;
- incision de l’anneau vulvaire, du vagin et du périnée ; pour ce faire, on place deux doigts
de la main secondaire (p.ex. gauche) entre la présentation au-dessus et le périnée en sous ;
on place ensuite les ciseaux droits ouverts, une branche dans le vagin et l’autre branche
en dehors sur la peau du périnée ; attendre une contraction utérine au cours de laquelle
faire pousser la parturiente ; à ce moment précis où la femme pousse, sectionner
franchement 4-5 cm l’anneau vulvaire, le périnée et le vagin en partant de la commissure
postérieure de la vulve, en dirigeant les ciseaux latéralement en oblique à droite ou à
gauche ;
- la présentation se dégage ; expulsion du nouveau-né comme pour tout autre accouchement
par voie basse ; délivrance dans les délais habituels ;
- suture ou réparation de l’épisiotomie ;
anesthésie locale à la xylocaîne 1% (infiltrer le nerf honteux interne au niveau de la
face interne de la tubérosité ischiatique ;
mise dans la cavité vaginale d’une boule des compresses stériles (à former = « souris »
pour empêcher le sang provenant ex-utéro de la plaie placentaire de couler sur la zone
de réparation ;
réparation, soit en un bloc, soit mieux en 3 plans car plus anatomique (suture de la
muqueuse vaginale en commençant au-delà de 1 cm du V de l’incision vaginale, en
points séparés ou en surjet avec du catgut fin ou du vicryl, plans musculaire et de sous-
cutané avec catgut ou vicryl, et enfin peau avec du nylon ou crin) ;
- soins immédiats ;
retirer la » souris » du vagin ;
désinfecter la cavité vaginale et la plaie suturée ;
faire un pansement sec.
- assurer les soins habituels comme après tout accouchement et une antibiothérapie
prophylactique ;
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
184
- ablation des fils non-résorbables placés sur la peau au 7ème jour après l’accouchement puis
sortie de la maternité.
D. LA CESARIENNE
1) Définition
La césarienne est une intervention chirurgico-obstétricale qui consiste à réaliser
l’accouchement artificiel après ouverture chirurgicale de l’utérus.
Elle s’exécute par voie abdominale après cœliotomie ou par voie vaginale après décollement
de la vessie (cas de grossesse arrêtée très tôt avec petit fœtus).
La césarienne comme la césure, sont dérivés du verbe latin caedere qui veut dire couper.
2) Indications
La césarienne est indiquée chaque fois que l’état maternel ou l’état fœtal exige l’évacuation
rapide de l’utérus alors que la voie basse est interdite ou trop risquée. Ainsi, on est amené à
envisager l’accouchement par césarienne dans deux grands moments, soit pendant la
grossesse, soit pendant le travail. Les indications de la césarienne peuvent être :
- Maternelles, fœtales, annexielles ou mixtes
- Selon leur caractère impératif ou non, absolues = obligatoires (l’accouchement doit se
faire par césarienne) ou relatives (en certaines circonstances favorables
l’accouchement peut se passer par voie basse).
- Electives ou urgentes
- selon la récurrence, temporaires càd uniquement au cours de la grossesse actuelle ou
permanentes càd qu’elles surviennent à toutes les grossesses (ex. anomalies du
bassin).
Pendant la grossesse : au cours des CPN certains états pathologiques de la grossesse, vont
orienter vers la césarienne. On s’y prépare et décide en fin de grossesse (césarienne
programmée ou élective). C’est le cas de certaines grossesses à haut risque.
Pendant le travail : il s’agit souvent des indications d’urgence. La césarienne doit être
exécutée rapidement pour éviter le pire.
Ces indications sont de trois ordres : maternel, foetal et mixte.
Indications d’ordre maternel
- Dystocies mécaniques dues à :
bassin rétréci ou généralement rétréci ;
bassin limite (après échec de l’épreuve du travail) ;
obstacles ou tumeurs praevia (kystes, fibromes ou myome).
- Dystocies dynamiques = anomalies de la contraction utérine et de la dilatation du col utérin
(opérer après la correction non réussie) ; utérus cicatriciel.
- Indications maternelles générales, exemple :
o néphropathies gravidiques car risques élévés de mort foetale in utéro ;
o diabète à la 37ème semaine pour sauvetage fœtal ;
o cardiopathies cyanogènes ;
o cancer du col ;
o prolapsus opéré ;
Indication d’ordre foetal ou ovulaire (cas les plus fréquents)
- Souffrance foetale aiguë.
- Souffrance fœtale chronique sévère (enfant incapable de supporter le stress contraction
utérine).
- Présentations particulières : face si dystocie, transversale (épaule), front / bregma, siége
avec un fond utérin important.
- Insertion basse du placenta surtout centrale.
- Procidence du cordon sur présentation céphalique.
- Macrosomie (excès de volume) sans hydrocéphalie.
- Césarienne post-mortem si la femme enceinte meurt de mort brutale.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
185
- Antécédents de morti-natalité.
- enfant « précieux » !!!
Indications d’ordre mixte : association d’indications d’intérêt maternel et foetal à la fois
- Eclampsie.
3) Principes en préopératoires
• S’assurer que :
– la salle d’opération est propre (elle doit être nettoyée après chaque
intervention ;
– le matériel nécessaire est disponible, en particulier les médicaments et
l’oxygène ;
– le matériel d’urgence est disponible et en état de marche.
– il y’a suffisamment de champs, et des blouses chirurgicales.
– il y’a des consommables stériles (gants, gaz, instruments).
Préparer la patiente.
• Lui expliquer l’intervention dont elle va bénéficier et le bien fondé de cette
intervention.
• Si elle est inconsciente, expliquer à la famille de quoi il s’agit.
• La patiente ou la famille doit consentir à l’intervention en connaissance de cause.
• Aider la patiente ou la famille à se préparer à l’intervention.
• Envoyer un prélèvement de sang pour dosage de l’hémoglobine ou l’hématocrite,
groupe sanguin et le rhésus.
• Commander du sang pour le cas où une transfusion serait nécessaire, puis si besoin
faire une transfusion sans attendre.
• Nettoyer la zone à inciser avec un antiseptique type Bétadine.
• Ne pas raser la région pubienne car cela accroît les risques de l’infection. Si
nécessaire, il est possible de couper légèrement les poils pubiens.
• Surveiller les signes vitaux (TA, pouls, FR) et consigner les observations par écrit.
• Administrer une prémédication adaptée au mode d’anesthésie choisie.
• Poser une sonde urinaire et surveiller la diurèse.
• Veiller à ce que les autres membres de l’équipe (médecin, sage-femme, infirmière,
anesthésiste, aide, etc.) reçoivent les informations nécessaires.
Position
• Installer la patiente dans la position adaptée à l’intervention de façon à :
– exposer le champ opératoire le mieux possible ;
– permettre à l’anesthésiste d’accéder à la patiente sans difficulté ;
– permettre à l’infirmière de contrôler les signes vitaux et de surveiller les
injections IV et les perfusions ;
– assurer la sécurité de la patiente en prévenant les traumatismes et en
maintenant une bonne circulation sanguine ;
– préserver sa dignité et respecter sa pudeur.
Lavage mains avant l’intervention
• (Principe généraux de l’asepsie et de l’antisepsie)
• Retirer tous les bijoux.
• Garder les mains au-dessus du niveau du coude, les mouiller soigneusement et les
savonner.
• Savonner en un mouvement circulaire, en commençant par le bout des doigts ;
• Bien nettoyer entre les doigts ;
• Remonter jusqu’au coude en savonnant puis faire de l’autre côté.
• Se rincer les bras l’un après l’autre, en commençant par le bout des doigts et en
gardant toujours les mains au-dessus du coude.
• Frotter pendant 3 à 5 minutes.
• Sécher chaque main avec une serviette stérile différente.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
186
• Essuyer en commençant par le bout des doigts et en remontant jusqu’au coude puis
changer de serviette.
• Une fois les mains propres, veiller à ne pas les mettre en contact avec des objets (par
exemple, matériel, blouse de protection) qui ne soient pas désinfectés ou stériles.
• Si elles touchent une surface contaminée, les nettoyer à nouveau.
Préparation du champ opératoire
• Préparer peau avec antiseptique (Bétadine) :
• Badigeonner trois fois la zone à inciser avec solution antiseptique à l’aide d’une pince
porte tampons stériles ou désinfectée et d’une compresse, veiller à ne pas contaminer
gants en touchant zones cutanées.
• Commencer par l’endroit à inciser et travailler en direction de l’extérieur en un geste
circulaire ;
• Une fois arrivée terminer, jeter la compresse.
• Ne jamais revenir au centre de la zone à préparer avec la même compresse.
• Garder les bras et les coudes en hauteur et veiller à ce que la blouse ne touche pas la
zone à inciser.
Anesthésie et césarienne
• L’anesthésie pour une césarienne, classiquement, peut être obtenue de deux manières :
– une anesthésie générale ou
– une anesthésie locorégionale.
• Plusieurs autres techniques peuvent être utilisées : l’anesthésie péridurale et locale.
Anesthésie locorégionale
Les avantages :
– la mère est consciente, il n’y a pas de risque l’inhalation.
– le risque de la dépression du nouveau-né est diminué.
Les inconvénients :
– une hypotension liée au bloc sympathique, la prévention s’obtient par
remplissage vasculaire et administration des vasoplégiques.
Anesthésie générale
Les avantages :
– l’incision est rapide, c’est une technique fiable, contrôlable avec hypotension
modérée.
Les inconvénients :
– le risque d’inhalation est élevé dans ce cas-ci (syndrome de Mendel Son).
– la dépression du nouveau-né.
Modes d’ouverture pariétale
• L’accès à la cavité péritonéale peut se faire classiquement de deux façons :
– Soit par une laparotomie médiane : celle-ci peut se faire de deux manières,
en sous ombilicale ou en sus et sous ombilicale.
• La laparotomie médiane sous ombilicale est utilisée comme une des
voies d’abord dans la césarienne segmentaire
• tandis que la laparotomie sus et sous-omblilicale est utilisée pour la
césarienne corporéale.
– Soit par une laparotomie transversale basse ou incision de
PFANNENSTIEL : c’est une incision sus-pubienne transversale.
• Elle se situe à environ 3cm au-dessus du rebord supérieur du pubis.
• On réalise une incision obliquement vers le haut du tissu sous-cutané et
une section arciforme de l’aponévrose, qui est ensuite décollé du plan
musculo-aponévrotique, ceci permet d’exposer les muscles grands
droits dont la séparation le long de la ligne médiane donne accès au
péritoine qui sera incisé longitudinalement.
• Cette seconde technique est préférable à la laparotomie médiane pour trois raisons :
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
187
– résultat esthétique meilleur.
– incidence très basse des hernies cicatricielles ;
– Et meilleure résistance à une éventuelle mise sous-tension lors d’une grossesse
ultérieure.
• Cependant l’exécution de l’incision de PFANNENSTIEL prend beaucoup de temps,
d’où elle n’est pas conseillée en cas d’extrême urgence. Cette technique constitue une
des voies d’abord de la césarienne segmentaire.
Types d’hystérotomie
Hystérotomie segmentaire transversale.
– L’incision utérine se fait selon un tracé arciforme à concavité supérieur sur la
face antérieure du segment inférieur. C’est la technique la plus utilisée car elle
permet d’obtenir une bonne cicatrisation.
Hystérotomie segmentaire longitudinale
– Plus délicate que la segmentaire transversale, l’incision se fait
longitudinalement sur la face antérieure. Elle offre une cicatrice de moins
bonne qualité.
Hystérotomie corporéale
– Une technique abandonnée actuellement.
– L’incision se faisait longitudinalement sur le corps utérin à sa face antérieure.
Cette technique (Hystérotomie corporéale) est d’indication restreinte pour deux raisons :
– les risques septiques sont très élevés lorsque l’intervention survient après un
certain temps de travail à œufs ouvert. Notons qu’avec l’avènement de
l’antibiothérapie, ce risque est minimisé.
– la cicatrice obtenue est souvent de mauvaise qualité. Une nouvelle grossesse
est souvent mal venue car elle fait courir le risque d’une rupture utérine
inopiné au cours du travail d’accouchement.
Hystérotomie segmento-corporéale
– Commencée le plus bas possible (segment inférieur) l’incision utérine remonte
longitudinalement sur le corps utérin pour obtenir l’ouverture nécessaire et
suffisante à l’extraction fœtale. Cette technique est souvent décidée en «
peropératoire » devant l’impossibilité de réaliser une hystérotomie
segmentaire pure.
Césarienne itérative : Il s’agit d’une hystérotomie à faire sur un utérus cicatriciel, ayant
déjà subi une césarienne.
4) Techniques de la césarienne
• Les techniques ont été si nombreuses depuis les débuts de l’intervention jusqu’à
maintenant.
• Ne seront décrites ici que
– la césarienne segmentaire,
– la césarienne selon Misgav Ladach et
– la césarienne selon Stark.
a) La césarienne segmentaire
• Premier temps : mise en place des champs ; cœliotomie sous ombilicale ou transversale
dans un souci esthétique surtout.
• Deuxième temps : protection de la grande cavité par des champs abdominaux après mise
en place des valves.
• Troisième temps : incision transversale aux ciseaux du péritoine pré-segmentaire dont le
décollement est facile.
• Quatrième temps : incision transversale ou longitudinale du segment inférieur ;
• Cinquième temps : extraction de l’enfant
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
188
• Sixième temps : c’est la délivrance par expression du fond utérin, ou délivrance manuelle
par l’orifice de l’hystérotomie.
• Septième temps : suture du segment inférieur qui se fait en un plan avec des points
séparées croisées en x sur les extrémités et les points séparés extra-muqueux sur les
berges.
• Huitième temps : suture du péritoine pré segmentaire.
• Neuvième temps : on enlève les champs abdominaux et les écarteurs ou valves pour
ensuite pratiquer la toilette de la cavité abdominale.
• Dixième temps : fermeture plan par plan de la paroi sans drainage.
Avantages de la césarienne segmentaire
• Incision autonome du péritoine viscéral possible permettant une bonne protection de la
suture.
• Incision de l’utérus dans une zone qui redeviendra pelvienne
• Incision de la partie non contractile de l’utérus donc moins de risque de rupture
• La cicatrice est d’excellente qualité.
b) La césarienne selon la technique de Misgav Ladach
• Se basant sur la littérature, Michael Stark de l’hôpital Misgav Ladach de Jérusalem a
modifié et rationalisé ces nouvelles stratégies en mettant au point une technique qu’il
a appelé modestement méthode de Misgav Ladach. Elle consiste à :
• ouverture pariétale par une incision rectiligne transversale superficielle de la peau à
environ 3cm au dessous de la ligne inter iliaque unissant les 2 épines
antérosupérieures.
• ouverture transversale du péritoine pariétal
• pas de champs abdominaux
• hystérotomie segmentaire transversale
• suture de l’hystérotomie en un plan un surjet non passé
• non fermeture des péritoines viscéral et pariétal
• suture aponévrotique par un surjet non passé
• rapprochement cutané par quelques points de Blair-Donati très espacés.
Avantages de la technique de Misgav Ladach
• Limite des attritions tissulaires
• Elimine les étapes opératoires superflues
• Simplifie le plus possible l’intervention.
• La simplicité de cette technique et les résultats obtenus par différentes études font
penser qu’elle deviendra sous peu la référence en matière d’extraction fœtale par voie
haute.
• Il faut signer cependant que les techniques sus citées comportent des précautions
particulières et des modifications gestuelles dans certaines circonstances telles que le
placenta prævia antérieur et la césarienne itérative.
c) La césarienne de Stark
• Ouverture pariétale selon la méthode de Joël Cohen modifié ;
• Ouverture transversale du péritoine pariétal.
• Pas de champs abdominaux.
• Hystérotomie segmentaire transversale.
• Extraction fœtale avec délivrance artificielle.
• Suture de l’hystérotomie en un plan « extra muqueux »par un surjet non passé.
• Non fermeture des péritoines viscéral et pariétal.
• Suture aponévrotique par un surjet non passé.
• Rapprochement cutané par quelques points de Blair-Donnati très espacés.
5) Les temps complémentaires de la césarienne
Il s’agit là des interventions qui sont souvent associées à la césarienne. Parmi elles, les
plus fréquentes sont :
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
189
– la ligature des trompes
– la kystectomie de l’ovaire
– l’hystérectomie.
6) Les complications de la césarienne
a) Les complications per opératoires
• L’hémorragie
• Les lésions intestinales
• Les lésions urinaires (les lésions vésicales, les lésions urétérales).
• Les complications anesthésiques : Hypoxie, syndrome d’inhalation, collapsus cardio-
vasculaire, arrêt cardiaque à l’induction.
b) Les complications postopératoires
Les complications maternelles
• Les complications infectieuses : l’endométrite, les suppurations et abcès de la paroi,
voire la septicémie.
• Les hémorragies post-opératoires : hématome de paroi, saignement des berges
d’hystérotomie par hémostase insuffisante, hémorragie vers J10-J15 post-opératoire
après lâchage secondaire de la suture et nécrose du myomètre.
• Les complications digestives : iléus paralytique post opératoire fonctionnel, les
vomissements, la diarrhée, les sub-occlusions, voire occlusion.
• La maladie thromboembolique
• Les complications diverses : troubles psychiatriques (psychoses puerpérales), fistules
vésico-vaginales, embolie gazeuse, embolie amniotique.
Les complications chez le nouveau-né :
• Les complications liées aux drogues anesthésiques : dépression du nouveau-né
• Les troubles respiratoires : la détresse respiratoire.
• Les complications infectieuses.
• La mortalité du nouveau-né.
E. INDUCTION DU TRAVAIL
Définition
Le déclenchement induction du travail est l’induction artificielle des contractions utérines
avant leur survenue spontanée dans le but d’obtenir un accouchement par les voies naturelles
chez une femme qui n’était pas jusque là en travail.
Indication
- Maternelle : HTA, Diabète, insuffisance cardiaque, respiratoire, cancer ...
- fœto-annexielle : RPM, RCIU, terme dépassé (à ce jour on attend plus le dépassement
et on induit systématique à la 41ème semaine révolue pour améliorer le pronostic
néonatale), iso-immunisation
- De convenance : arrange la famille ou l’équipe médicale
Contre indications
- Accouchement voie basse impossible :
o bassin chirurgical,
o Obstacle prævia
- Souffrance fœtale chronique ou aigue
- Utérus cicatriciel ?
- Siège ? Jumeaux ?
- Placenta recouvrant
- Allergies aux prostaglandines
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
190
Conditions du déclenchement
- Accouchement par voie basse possible, pas de disproportion fœto- maternelle
- S’assurer du bien être fœtal par le score biophysique de Manning
- Evaluer la maturation du col par le score de Bishop qui oriente le choix de la méthode
d’induction
Moyens d’induction
- Médicamenteux
o Ocytocine
o Syntocynon
o Les prostaglandines ou ses dérivés : Prostine E2 gel à 1 ou 2mg (dans le cul de sac
postérieur du vagin), Dinoprostone (Prépidil®) 0,5mg (dans canal cervical),
Misoprostol (Cytotec ®).
o Les anti-progestérones : Mifégyne
- Non médicamenteux ou mécanique
o Sonde de Foley
o Amniotomie ou rupture artificielle des membranes
o Bougies et dilatateurs cervicaux (laminaires et Dilapans)
Schémas d’induction
1) Théobald (solution 1l Sérum glucosé 5% + 10 UI Ocytonine)
2) Sonde Foley à relayer avec le Théobald
3) Gel de prostaglandine à relayer par le Théobald
4) Misoprostol intravaginal
5) Misoprostol per os
Risque et complicationde l’induction
L`induction du travail comporte 2 principaux types de risque liés à l’éventualité d’une
hyperstimulation utérine :
- possibilité de souffrance fœtale aigue; elle est d’autant plus grande que le fœtus est à
risque ; les contractions utérines constituant la circonstance idéale pour l'aggravation de la
souffrance fœtale, à cause notamment de la compression des vaisseaux intra-myométriaux
et funiculaires ainsi que de la portion rétro-utérine de l'aorte (EFFET POSEIRO = qui
retentit sur la circulation utéro-placentaire), il est imprudent d’induire le travail chez une
femme dont l’état fœtal n’a pas été évalué quant à sa capacité à supporter les contractions
utérines ;
- possibilité de rupture de l`utérus, surtout si celui-ci est fragilisé par une cicatrice ou une
multiparité ; c`est ainsi que l`induction du travail ouvre la voie à l`hémorragie qui peut
tuer ; on peut également évoquer, en post-partum, les anomalies contractiles susceptibles de
conduire à une atonie utérine, donc à une hémorragie.
Choix et technique d’induction selon les différents schémas
Le choix du schéma d’induction dépend du score de Bishop qui est un score obstétrical qui
permet d’évaluer la maturité ou la déclenchabilité du col. Il correspond à la somme de
l’appréciation des cinq paramètres suivant :
- la dilatation du col utérin,
- l’effacement du col utérin,
- la consistance du col utérin,
- la position du col utérin,
- le degré d’engagement ou positionnement de la présentation fœtale par rapport
aux épines sciatiques.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
191
Paramètres 0 1 2 3
Dilatation du col utérin Fermé 1 - 2 cm 3 - 4 cm ≥ 5 cm
Effacement du col utérin 0 - 30% 40 - 50% 60 - 70% ≥ 80 %
Consistance du col utérin Ferme Moyenne Molle
Position du col utérin Postérieure Médian Antérieure
Degré d’engagement ou positionnement mobile amorcée fixée engagé
de la présentation fœtale par rapport aux (3 cm au (2 cm au (< 1cm au (1 - 2 cm au
épines sciatiques dessus) dessus) dessus) dessous)
Valeurs du score : de 0 à 13
Score ≥ 7 = Bishop Bon ou col déclenchable, pronostic favorable
Score < 7 = Bishop Mauvais ou col non déclenchable, pronostic défavorable ==> nécessite
une maturation du col (avec soit Sonde de Folley, gel de prostaglandine)
L`induction du travail constitue beaucoup plus qu`un geste. C`est donc un processus lourd de
conséquences qu`il convient d`initier seulement si :
- les conditions de son application sont réunies (accouchement par voie basse possible c.-à-d.
bonne présentation du fœtus et fœtus de poids normal – col favorable, c.-à-d. Bishop bon) ;
- consentement éclairé de la parturiente sur les risques éventuels) ;
- on dispose des possibilités de pratiquer une césarienne en urgence ; ceci suppose non
seulement des facilités pour poser le diagnostic d`hyperstimulation utérine ou de malaise
fœtal avéré (cardiotocographie), mais également un kit opératoire et un accès à l`anesthésie.
Si ces conditions ne sont pas réunies, il devient irresponsable d`induire le travail. La
prudence est encore plus à respecter s`il s`agit d`un utérus fragilisé, et une tocolyse est à
prévoir en cas d`hyperstimulation.
Lorsque le score de Bishop est mauvais, il faut réaliser une maturation du col au moins 24
heures auparavant, soit avec la Sonde de Foley, soit avec les gels de prostaglandines ou soit
avec benzoate d’œstradiol (actuellement de moins en moins utiliser)
Les méthodes ou schémas d’induction les plus utilisées dans notre milieu pour induire le
travail sont :
1) l`Amniotomie : elle n`est possible qu` à la faveur d`une certaine ouverture du col, ce qui
prédispose ainsi à sa réussite ; elle provoque une augmentation brutale de la synthèse des
prostaglandines au niveau de l`utérus et induit un travail proche du travail spontané ; il
fait donc courir moins de syndrome d`hyperstimulation que les drogues utérotoniques ; on
l`associe souvent à la perfusion d`ocytocine qui vient alors rendre le procédé moins
banal ;
2) le Théobald : on la débute très prudemment avec un débit de 4 gouttes/minute, puis l`on
augmente progressivement de 4 gouttes toutes les 30 minutes jusqu’à l’obtention des
bonnes contractions utérines, donc ne plus augmenter dès que les contractions sont jugées
bonnes, le débit maximal à ne pas dépasser est de 44 gouttes/minute ;
3) les prostaglandines : réputées d`un coût élevé (forme gel), sauf le Misoprostol (Cytotec,
en comprimés) ;
Misoprostol intravaginal : on dépose dans le fond du vagin (cul de sac ou fornix
postérieur) en raison de 25 microgrammes soit ¼ de comprimé toutes les 4 – 6 heures, en
veillant à ne pas dépasser 400 microgrammes ;
Misoprostol per os : on prépare une solution en diluant 1 comprimé de 200
microgrammes dans 100 cc d’eau plate et on administre 20 microgrammes soit 10cc de
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
192
solution toutes les 30 minutes jusqu’à l’obtention des bonnes contractions utérines (NB :
toujours bien homogénéiser avant l’administration. Dose maximale de misoprostol à
administrer 400 microgrammes soit deux comprimés.
4) la dilatation mécanique du col (= à éviter si cervicite), soit au moyen des laminaires
(chers), soit par pose d`une sonde de Foley numéro 18 dont on gonfle le ballonnet avec 30
– 50 ml de sérum physiologique ; les contractions utérines surviennent aussi bien par
réflexe neuro-hormonal (prostaglandines) de Fergusson que par production directe des
prostaglandines au niveau de la zone membranaire du pole inférieur de l`œuf qui est
décollée par le ballonnet ; on la relaye parfois avec la perfusion d`ocytocine dans les 24
heures qui suivent sa pose.
Notes de cours d’obstétrique CT Dr MBANGAMA MA UKA/KANANGA 2015
Vous aimerez peut-être aussi
- Obstetrique Complet Final 29 Mai1 - 2-2Document254 pagesObstetrique Complet Final 29 Mai1 - 2-2sando loic100% (3)
- Grossesses MultiplesDocument8 pagesGrossesses MultiplesWOGNIN100% (1)
- RPM Fine 1Document42 pagesRPM Fine 1FlaPas encore d'évaluation
- Réanimation NN UO Oct 2021Document41 pagesRéanimation NN UO Oct 2021Nabia ThomasPas encore d'évaluation
- Protocolesmaternite HUMaout 2013Document88 pagesProtocolesmaternite HUMaout 2013Marlee Rosy. A.Pas encore d'évaluation
- Prof Kakudji Obstetrique-2Document310 pagesProf Kakudji Obstetrique-2laurejacky5Pas encore d'évaluation
- Cours de Sonu Corr 1018Document105 pagesCours de Sonu Corr 1018Lukusa Maurice100% (1)
- 24 54666Document13 pages24 54666AlinaPas encore d'évaluation
- Manuel Pratique D'urgence ObstétriqueDocument219 pagesManuel Pratique D'urgence ObstétriqueS&M The perfect100% (3)
- I-2-17-Principales Complications de La GrossesseDocument35 pagesI-2-17-Principales Complications de La GrossesseNemo LuPas encore d'évaluation
- Rea Nouveau NeDocument38 pagesRea Nouveau NeSalimaPas encore d'évaluation
- Nursing en Obstétrique PDFDocument84 pagesNursing en Obstétrique PDFMuba100% (1)
- Macros OmieDocument3 pagesMacros OmieالهامPas encore d'évaluation
- 5.menace D'accouchement PrématuréDocument8 pages5.menace D'accouchement Prématuréaramediagne869Pas encore d'évaluation
- Rupture Prématurée Des Membranes: DR Chelha Maitre Assistante en Gynécologie Obstétrique Chu OranDocument14 pagesRupture Prématurée Des Membranes: DR Chelha Maitre Assistante en Gynécologie Obstétrique Chu OranOustite StetouPas encore d'évaluation
- Tunisie Med 2012 90 4 300 305Document6 pagesTunisie Med 2012 90 4 300 305matthieu kabeyaPas encore d'évaluation
- Cours de Chirurgie Ped MunyantwariDocument63 pagesCours de Chirurgie Ped MunyantwariStanley Pedos100% (1)
- Mémoire CEGLA CamilleDocument87 pagesMémoire CEGLA CamilleHamza BIKIPas encore d'évaluation
- Uterus Cicatriciel Sfe 3Document4 pagesUterus Cicatriciel Sfe 3Abdallah Ouedraogo100% (1)
- DFASMa 2c Programme 2018-19Document27 pagesDFASMa 2c Programme 2018-19Antoine DanvioPas encore d'évaluation
- Grossesse Extra-UterineDocument17 pagesGrossesse Extra-UterineMaryem Rhaimia100% (1)
- Patho Obstetriques N°1 & 2Document42 pagesPatho Obstetriques N°1 & 2Kabinè CONDEPas encore d'évaluation
- Menace D'accouchement Prématuré (MAP)Document39 pagesMenace D'accouchement Prématuré (MAP)BENGHENISSA SOUNDOUSPas encore d'évaluation
- Chapiter 1Document20 pagesChapiter 1kalda kidePas encore d'évaluation
- 20-Nephrologie 8e-Edition Chap20 PDFDocument12 pages20-Nephrologie 8e-Edition Chap20 PDFسيف الاسلام عبد الرحمانPas encore d'évaluation
- Placenta PraeviaDocument19 pagesPlacenta PraeviaYasmine BelguendouzPas encore d'évaluation
- Pré Eclampsie EclampsieDocument13 pagesPré Eclampsie EclampsieTouny YoroubaPas encore d'évaluation
- RDP - 2007 Fievre Et Grossesse 17Document5 pagesRDP - 2007 Fievre Et Grossesse 17hassenmedmahmoud8Pas encore d'évaluation
- Pronostic D-WPS OfficeDocument7 pagesPronostic D-WPS Officealexiskandeykom03Pas encore d'évaluation
- 61 Pré-Éclampsie - Collège Urgences 21Document14 pages61 Pré-Éclampsie - Collège Urgences 21ihatemedecine99Pas encore d'évaluation
- Soins ObstetricauxDocument149 pagesSoins ObstetricauxDjibo Adamou KoussangaPas encore d'évaluation
- Le Partogramme R1Document16 pagesLe Partogramme R1Fifi AyadiPas encore d'évaluation
- 4 - L'hémorragie Du Troisième Trimestre - Organisé PDFDocument10 pages4 - L'hémorragie Du Troisième Trimestre - Organisé PDFMohamed Ikbal100% (3)
- Rupture Prématurée Des MembranesDocument10 pagesRupture Prématurée Des MembranesHindou IlhemPas encore d'évaluation
- Guideline 449 FR 2022 11 08Document189 pagesGuideline 449 FR 2022 11 08Koudous OladimedjiPas encore d'évaluation
- VtementsDocument14 pagesVtementsimePas encore d'évaluation
- Enace D Accouchement PrématuréDocument52 pagesEnace D Accouchement Prématuréالوثائقية هل كنت تعلمPas encore d'évaluation
- Obstetrique Elongi Complet (DR - Kas) - 1Document364 pagesObstetrique Elongi Complet (DR - Kas) - 1prince.rommaPas encore d'évaluation
- Protocole de ServiceDocument78 pagesProtocole de ServiceMouniratou SAWADOGOPas encore d'évaluation
- Placenta PraeviaDocument10 pagesPlacenta PraeviaPrisca Amboyo100% (1)
- Anesthésie Pour CésarienneDocument13 pagesAnesthésie Pour CésarienneHãdjęr MėsPas encore d'évaluation
- HRP Ahlem PDFDocument13 pagesHRP Ahlem PDFtrick trickPas encore d'évaluation
- Protocole de Recherche1 ...Document13 pagesProtocole de Recherche1 ...salim nisrinPas encore d'évaluation
- Livret interne KB2014 Tome 4 (Maternité)Document95 pagesLivret interne KB2014 Tome 4 (Maternité)savinien.tobePas encore d'évaluation
- Cesarienne Cours M2 DR Kemfang 2015Document23 pagesCesarienne Cours M2 DR Kemfang 2015Valdes KPas encore d'évaluation
- cours d'obstétriqueDocument16 pagescours d'obstétriqueITS MEPas encore d'évaluation
- 32 Grossesse Extrauterine 2020Document17 pages32 Grossesse Extrauterine 2020karima karimaPas encore d'évaluation
- 60 EclampsieDocument20 pages60 EclampsieMolka HanabliaPas encore d'évaluation
- Urgences Chirurgicales Du Nouveau-Né Et Du NourrissonDocument10 pagesUrgences Chirurgicales Du Nouveau-Né Et Du Nourrissonasmae.mehdielyacoubiPas encore d'évaluation
- Hemorragie Du Premier TrimestreDocument28 pagesHemorragie Du Premier TrimestrematsfloriaPas encore d'évaluation
- Métrorragies 3è TrimestreDocument12 pagesMétrorragies 3è Trimestreavounvi100% (1)
- 32 Grossesse Extrauterine 2022Document18 pages32 Grossesse Extrauterine 2022Mohamed ArfaouiPas encore d'évaluation
- Cadiopathies-Et-Grossesse-Final 2Document59 pagesCadiopathies-Et-Grossesse-Final 2Manel KammounPas encore d'évaluation
- Gyneco5an Rpm2019bichaDocument5 pagesGyneco5an Rpm2019bichaRima BouallegPas encore d'évaluation
- 0 Obstétrique Pathologique IDocument94 pages0 Obstétrique Pathologique Iwassila silaaaPas encore d'évaluation
- Neuroped PSMDocument14 pagesNeuroped PSMYunes At YidirPas encore d'évaluation
- La CésarienneDocument43 pagesLa CésarienneMarevaPas encore d'évaluation
- La Menace DDocument7 pagesLa Menace Danis anisPas encore d'évaluation
- MS11 2 Betend Anne 0 DDocument34 pagesMS11 2 Betend Anne 0 DNathan PeaPas encore d'évaluation
- Uterus - Ligaments LargesDocument6 pagesUterus - Ligaments LargesAek BenguerrahPas encore d'évaluation
- Os CoxalDocument8 pagesOs CoxalAbd El AzizPas encore d'évaluation
- Accouchement en Presentation Du Sommet-DiaposDocument51 pagesAccouchement en Presentation Du Sommet-DiaposAghilas KingPas encore d'évaluation
- L'utérusDocument30 pagesL'utérusAbdul Koudouss KonePas encore d'évaluation
- APPAREIL URO-GENITAL-convertiDocument60 pagesAPPAREIL URO-GENITAL-convertiAmadou Marouba Sow100% (1)
- Livret PelvisDocument47 pagesLivret PelvisJojo AYATINPas encore d'évaluation
- Gyneco5an-Presentation Sommet2017belalaDocument4 pagesGyneco5an-Presentation Sommet2017belalaSarah EllePas encore d'évaluation
- POLY - PCEM2-THEME XIII 2016 Unlocked - BY MED - TMSSDocument136 pagesPOLY - PCEM2-THEME XIII 2016 Unlocked - BY MED - TMSSjehane oussamaPas encore d'évaluation
- Os CoxalDocument30 pagesOs CoxalMalek LarbiPas encore d'évaluation
- Le Cycle Menstruel de La FemmeDocument1 pageLe Cycle Menstruel de La Femmekharrat100% (1)
- PelvimétrieDocument11 pagesPelvimétrieyassin temoPas encore d'évaluation
- Chirurgie OrthopédiqueDocument40 pagesChirurgie OrthopédiqueCharlotte Taton100% (2)
- Anatomie de LuterusDocument9 pagesAnatomie de Luterusmt6341373Pas encore d'évaluation
- Canal Anal PDFDocument7 pagesCanal Anal PDFLAHLOU KHALIDPas encore d'évaluation
- Lee J Skandalakis Surgical Anatomy and Technique A Pocket Manual 458-550Document93 pagesLee J Skandalakis Surgical Anatomy and Technique A Pocket Manual 458-550Groupe 6 Internat UNDHPas encore d'évaluation
- Perinee Feminin-Dr KaboubDocument7 pagesPerinee Feminin-Dr KaboubOum SelmanePas encore d'évaluation
- Mes Actualités - MémoireDocument81 pagesMes Actualités - MémoirenguebiloPas encore d'évaluation