Académique Documents
Professionnel Documents
Culture Documents
2013 CtresEtrangers Exo2 Correction Esters 8pts
Transféré par
Haman Bello OumarouCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2013 CtresEtrangers Exo2 Correction Esters 8pts
Transféré par
Haman Bello OumarouDroits d'auteur :
Formats disponibles
Bac S 2013 Centres étrangers CORRECTION © http://labolycee.
org
Exercice II – L’estérification (8 points)
1. Mécanisme. O
1.1. L’éthanoate de butyle a pour formule semi-développée :
C CH3
CH3 CH2 CH2 CH2 O
(0,25 pt + 0,25 pt) O
Il a été formé lors de la réaction entre l’acide éthanoïque C CH3
(0,25 pt + 0,25 pt)
et le butan-1-ol CH3 CH2 CH2 CH2 OH HO
1.2. (0,75 pt) Il s’agit d’une réaction de substitution car le OH du groupe carboxyle de l’acide
carboxylique a été substitué par le groupe CH3 – CH2 – CH2 – CH2 –O de l’alcool.
1.3. Pour l’acide éthanoïque :
(0,25 pt) L’atome de carbone lié aux atomes d’oxygène est partiellement chargé positivement
car l’électronégativité de l’élément C est inférieure à celle de l’élément O. O
δ+
(0,25 pt) Cet atome C est un site accepteur de doublet d’électrons. C CH3
Pour le butan-1-ol (R2–OH) : HO
(0,5 pt) L’atome d’oxygène avec ses deux doublets non liants est un site donneur de doublets
d’électrons.
(0,25 pt) On peut imaginer comme première étape, le transfert de doublet schématisé par la
flèche courbe ci-après : O
C CH3 + CH3 CH2 CH2 CH2 OH
HO
2. Synthèse.
2.1. (0,75 pt) L’estérification est réalisée avec un montage de chauffage à reflux. Le chauffe-
ballon permet d’agir sur le facteur cinétique qu’est la température et ainsi de modifier la durée de
la réaction.
Le réfrigérant à boules condense d’éventuelles vapeurs nocives, maintenant constant le volume
du milieu réactionnel.
2.2. (0,5 pt) Le protocole proposé a pour objectif d’étudier la cinétique de la réaction
d’estérification.
La diminution de la température augmente fortement la durée de réaction.
Ainsi lors de l’étape 1, les réactifs en contact ne réagissent quasiment pas. On choisit l’instant de
début de réaction.
Lors de l’étape 2, la réaction d’estérification au sein du prélèvement qui pourrait se poursuivre
est bloquée par le refroidissement. Le titrage reflètera bien la composition du système chimique
à la date du prélèvement.
2.3. Calculons les quantités de matière des réactifs, afin de déterminer le réactif limitant.
m
ρ= soit m = ρ.V
V
m ρ.V
n= donc n = (avec ρ en g.mL-1 et V en mL)
M M
(0,25 pt) Quantité de matière d’alcool initiale :
On a introduit un volume V = 44,8 mL d’alcool.
0,81×44,8
n= = 0,49 mol d’alcool
74
(0,25 pt) Quantité de matière d’acide initiale :
On a introduit un volume V’ = 28 mL d’acide.
1,05×28
n' = = 0,49 mol d’acide
60
(0,25 pt) Réactif limitant :
Le mélange réactionnel est équimolaire (il contient la même quantité de chaque réactif), ainsi les
proportions stœchiométriques de l’équation de la réaction sont respectées. Il n’y a pas de réactif
en excès, ni en défaut.
D’après l’équation de la réaction, une mole d’acide fournit une mole d’ester.
(0,25 pt) On obtiendrait 0,49 mol d’ester si la réaction était totale.
2.4. (0,5 pt) « La solution d’hydroxyde de sodium permet de doser l’acide éthanoïque. »
Cela est vrai si la réaction de la base HO– avec l’acide CH3COOH est totale.
On remarque que l’acide est miscible avec la solution aqueuse d’hydroxyde de sodium, ce qui
facilite la réaction.
De plus il faut que les ions H3O+ apportés par l’acide sulfurique soient présents en quantité
négligeable face à la quantité d’acide éthanoïque.
(0,25 pt) « Le titrage de l’acide éthanoïque par la solution d’hydroxyde de sodium permet de
déterminer la quantité d’ester formée. »
équation chimique alcool + acide ester + eau
État du Avancement
(mol) Quantités de matière (mol)
système
État initial x=0 n n’ 0 0
En cours de
x n–x n’ – x x x
transformation
État final xfinal n – xfinal n’ – xfinal xfinal xfinal
À l’équivalence du titrage nHO− versée = nacide restant , donc on accède à nacide restant.
nacide restant = n’ – x, donc on accède à x.
Il disparaît autant d’acide qu’il se forme d’ester, soit x mol.
2.5. (0,25 pt) La température influence l’évolution temporelle d’une réaction chimique :
La comparaison des courbes relatives
aux variantes 1 et 3, montre qu’en
augmentant la température on obtient,
en une même durée, une plus grande
quantité d’ester.
(0,25 pt) Un catalyseur influence
l’évolution temporelle d’une réaction
chimique :
La comparaison des courbes relatives
aux variantes 1 et 2, montre que la
catalyseur permet d’obtenir, en une
même durée, une plus grande
quantité d’ester.
(0,25 pt) Excès d’un réactif :
La comparaison des courbes relatives
aux variantes 4 et 5, montre que
l’excès de butan-1-ol permet d’obtenir
davantage d’ester.
3. Extraction, purification et identification.
(5x0,25 pts)
On applique la règle des (n+1)uplet où n représente le nombre d’atomes d’hydrogène voisins.
Les protons portés par l’atome de carbone 1 n’ont pas d’atomes d’hydrogène voisins. Le signal
correspondant est un singulet.
Les protons portés par l’atome de carbone 2 ont deux atomes d’hydrogène voisins. Le signal
correspondant est un triplet.
Les protons portés par l’atome de carbone 3 ont quatre atomes d’hydrogène voisins. Le signal
correspondant est un quintuplet.
Les protons portés par l’atome de carbone 4 ont cinq atomes d’hydrogène voisins. Le signal
correspondant est un hexuplet.
Les protons portés par l’atome de carbone 5 ont deux atomes d’hydrogène voisins. Le signal
correspondant est un triplet.
Remarque :
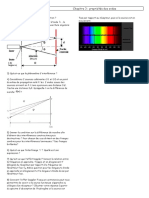
Voici le spectre de RMN réel de cette molécule.
On y trouve effectivement le triplet pour le carbone n°2 à 4,06 ppm et le singulet à 2,04 ppm pour
le carbone n°1, voire le triplet à 1,0 ppm pour le carbone n°5 ; par contre on a un massif autour
de 1,5 ppm qui ne correspond ni à un quintuplet ni à un hexupplet.
Pour les professeurs « Autoformation à la Résonance Magnétique Nucléaire du proton »
http://www.unice.fr/cdiec/cours/rmn_web/c_rmn.htm
Vous aimerez peut-être aussi
- Annale Chimie 1Document16 pagesAnnale Chimie 1Sinem SinemPas encore d'évaluation
- 2005 09 Antilles Correction Exo3 Menthe 4ptsDocument3 pages2005 09 Antilles Correction Exo3 Menthe 4ptsAnthea MallaPas encore d'évaluation
- 2003 09 National Correction Exo2 Banane 6 5ptsDocument2 pages2003 09 National Correction Exo2 Banane 6 5ptsHassan BelqaidPas encore d'évaluation
- Tdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanDocument5 pagesTdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanAlassane TraorePas encore d'évaluation
- C 02 Ab 1 eDocument5 pagesC 02 Ab 1 eMihnea GamanPas encore d'évaluation
- 2014 Pondichery Exo2 Correction SyntheseAcetateEthyle 5ptsDocument2 pages2014 Pondichery Exo2 Correction SyntheseAcetateEthyle 5ptsAbdeljalil LoudainiPas encore d'évaluation
- Exos CH 04Document3 pagesExos CH 04lol testPas encore d'évaluation
- TD Cinetiqueserie n07Document2 pagesTD Cinetiqueserie n07YASSINE AZNAGPas encore d'évaluation
- L2 TP CinChimDocument7 pagesL2 TP CinChimDa DiPas encore d'évaluation
- 6-TDPCSIcinetique-2015Document8 pages6-TDPCSIcinetique-2015Nguissaly SonkoPas encore d'évaluation
- Cinétique Expérimentale, Énoncés Des ExercicesDocument25 pagesCinétique Expérimentale, Énoncés Des ExercicesWafae LahjoujiPas encore d'évaluation
- Exos CinétiqueDocument16 pagesExos Cinétiqueayyoub dhbPas encore d'évaluation
- 2013 09 Metro Exo2 Correction Aspartame 10ptsDocument4 pages2013 09 Metro Exo2 Correction Aspartame 10ptsaa.aa1Pas encore d'évaluation
- Examen National Physique Chimie 2 Bac SVT 2017 Normale Sujet 2Document6 pagesExamen National Physique Chimie 2 Bac SVT 2017 Normale Sujet 2Othman HabtiPas encore d'évaluation
- TD HLCH420 Cinétique Chimique 16-17Document4 pagesTD HLCH420 Cinétique Chimique 16-17y_aitabdellahPas encore d'évaluation
- Cin ExoDocument10 pagesCin ExoHarakat ElhoucinePas encore d'évaluation
- الامتحان الوطني في مادة الفيزياء والكيمياء 2011 علوم رياضية ترجمة فرنسية الدورة الاستدراكيةDocument16 pagesالامتحان الوطني في مادة الفيزياء والكيمياء 2011 علوم رياضية ترجمة فرنسية الدورة الاستدراكيةFahmiPas encore d'évaluation
- DS 1 CorrigéDocument3 pagesDS 1 CorrigéFethi BorsaliPas encore d'évaluation
- TD (1) Cinétique ChimieDocument3 pagesTD (1) Cinétique ChimieAnass ZaouiPas encore d'évaluation
- Je Partage TP1-CC1 Avec VousDocument8 pagesJe Partage TP1-CC1 Avec Vousmenin noorPas encore d'évaluation
- C10Chim - Esterification - Hydrolyse - Equilibre - Exos - Fischer - 2 PDFDocument7 pagesC10Chim - Esterification - Hydrolyse - Equilibre - Exos - Fischer - 2 PDFAzizElheniPas encore d'évaluation
- Cinétique TDDocument5 pagesCinétique TDBadr MouslimPas encore d'évaluation
- Annalee 214Document16 pagesAnnalee 214Zineb KhadranePas encore d'évaluation
- Bestcours NS 28FDocument8 pagesBestcours NS 28Frobi jungkookPas encore d'évaluation
- TD - Cpgo - 2023-2024 - Cinetique ChimiqueDocument4 pagesTD - Cpgo - 2023-2024 - Cinetique Chimiquedieudonnepooda71Pas encore d'évaluation
- Killian - 2022 - Tp1Document9 pagesKillian - 2022 - Tp1amandine gaianiPas encore d'évaluation
- Examen National Physique Chimie Sciences Maths 2010 Normale SujetDocument8 pagesExamen National Physique Chimie Sciences Maths 2010 Normale SujetŤăhã ÊìîPas encore d'évaluation
- DM Nâ°1Document8 pagesDM Nâ°1grégoire beraudPas encore d'évaluation
- Série de Chimie - 4ème Année Sc. Exp - Technique & MathématiquesDocument3 pagesSérie de Chimie - 4ème Année Sc. Exp - Technique & MathématiquesأشرفالمبروكPas encore d'évaluation
- 2013 CtresEtrangers Exo2 Sujet Esters 8ptsDocument4 pages2013 CtresEtrangers Exo2 Sujet Esters 8ptsHaman Bello OumarouPas encore d'évaluation
- Sceance - de - Revisions - Avant - Concours CHIMI PDFDocument19 pagesSceance - de - Revisions - Avant - Concours CHIMI PDFKhawla El HamdaouiPas encore d'évaluation
- Examen National 2021 Session normal-SPDocument8 pagesExamen National 2021 Session normal-SPAmmar LokihiPas encore d'évaluation
- Exercice AvancementDocument5 pagesExercice AvancementMajid Nait LyassePas encore d'évaluation
- 201701271158125 (3)Document9 pages201701271158125 (3)Ali RammalPas encore d'évaluation
- Série D'exercices - Chimie Estérification Et Hydrolyse - Bac Math - 2010-2011 - MR AkkariDocument2 pagesSérie D'exercices - Chimie Estérification Et Hydrolyse - Bac Math - 2010-2011 - MR Akkariyouma009Pas encore d'évaluation
- Cinetique ConductimetrieDocument10 pagesCinetique ConductimetrieMouad Arrad100% (1)
- TD de Cinetique ChimiqueDocument6 pagesTD de Cinetique ChimiquefernandPas encore d'évaluation
- Devoir de Sciences Physiques N°4: Exercice 1: Dosage D'un CollyreDocument5 pagesDevoir de Sciences Physiques N°4: Exercice 1: Dosage D'un CollyreRyan BoucettaPas encore d'évaluation
- Exam BlanchDocument8 pagesExam Blanchاستاذك في الفيزياءPas encore d'évaluation
- Exercice Avance 1er S PDFDocument4 pagesExercice Avance 1er S PDFMajid Nait LyassePas encore d'évaluation
- Série 1 Cinétique 2020 2021Document4 pagesSérie 1 Cinétique 2020 2021Li Na0% (1)
- Chimie D Chap14 Correction ExosDocument4 pagesChimie D Chap14 Correction ExosSOULA CHAHINAZPas encore d'évaluation
- EstérificationDocument2 pagesEstérificationIlyes Ben Jemaa0% (1)
- Serie4 (Ben Amor)Document1 pageSerie4 (Ben Amor)Malek BerrguebPas encore d'évaluation
- Chimie - Bière Brune AromatiséeDocument6 pagesChimie - Bière Brune AromatiséeAbdel ElouaerPas encore d'évaluation
- DS1 2022-2023 Sujet Corrige BaremeDocument10 pagesDS1 2022-2023 Sujet Corrige Baremearnaud.bedouinPas encore d'évaluation
- Bac 2015 SM2 ofDocument8 pagesBac 2015 SM2 ofعذاب الهمة عذبPas encore d'évaluation
- 2005 09 Antilles Sujet Exo3 Menthe 4pts 2Document3 pages2005 09 Antilles Sujet Exo3 Menthe 4pts 2Youssef DahaniPas encore d'évaluation
- Chimie Baccalaureat Blanc N°2 - Session de Mai 2017Document5 pagesChimie Baccalaureat Blanc N°2 - Session de Mai 2017Junior NoulaPas encore d'évaluation
- blan 3Document7 pagesblan 3Ya Cin KhaldiPas encore d'évaluation
- Chapitre-9-Réaction D'ésterificationDocument11 pagesChapitre-9-Réaction D'ésterificationa houssPas encore d'évaluation
- Examen1 Réactivité Chimique FST-MeknèsDocument6 pagesExamen1 Réactivité Chimique FST-MeknèsayabourhdifaPas encore d'évaluation
- Epreuve_Chimie_1_Preparation_au_CNC_2021Document7 pagesEpreuve_Chimie_1_Preparation_au_CNC_2021Meriem El AbzazePas encore d'évaluation
- TP7 Cinétique Chimique Du Premier Ordre.Document14 pagesTP7 Cinétique Chimique Du Premier Ordre.Sellam Anis100% (1)
- Exercice 1 (7 Points) Odeur Désagréable de PoissonsDocument4 pagesExercice 1 (7 Points) Odeur Désagréable de Poissonsveronica.1.moussallemPas encore d'évaluation
- Examens de Chimie-1Document17 pagesExamens de Chimie-1Anas HajimPas encore d'évaluation
- Exercice 1 (7 Points) Propriétés D'un AlcoolDocument7 pagesExercice 1 (7 Points) Propriétés D'un AlcoolKeys of H.A.Pas encore d'évaluation
- Série D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienDocument2 pagesSérie D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienInass LayachPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Politique EconomiqueDocument12 pagesPolitique EconomiqueHaman Bello OumarouPas encore d'évaluation
- EX SN 2022 2023 Economie Internationale FrancaisDocument3 pagesEX SN 2022 2023 Economie Internationale FrancaisHaman Bello OumarouPas encore d'évaluation
- Politique EconomiqueDocument12 pagesPolitique EconomiqueHaman Bello OumarouPas encore d'évaluation
- Politique EconomiqueDocument12 pagesPolitique EconomiqueHaman Bello OumarouPas encore d'évaluation
- Politique EconomiqueDocument12 pagesPolitique EconomiqueHaman Bello OumarouPas encore d'évaluation
- Tchatat Nya RaoulDocument47 pagesTchatat Nya RaoulHaman Bello OumarouPas encore d'évaluation
- bacCD Chimie 2006Document2 pagesbacCD Chimie 2006Haman Bello OumarouPas encore d'évaluation
- bacCD Chimie 2005Document3 pagesbacCD Chimie 2005Haman Bello OumarouPas encore d'évaluation
- 2013 CtresEtrangers Exo3 Correction Pendule Ammoniac 5ptsDocument3 pages2013 CtresEtrangers Exo3 Correction Pendule Ammoniac 5ptsHaman Bello OumarouPas encore d'évaluation
- Bac CH 1999Document3 pagesBac CH 1999Haman Bello OumarouPas encore d'évaluation
- bacCD Chimie 2006Document2 pagesbacCD Chimie 2006Haman Bello OumarouPas encore d'évaluation
- Bac F1Document2 pagesBac F1Haman Bello OumarouPas encore d'évaluation
- 2015-Pondichery-Exo1-Correction-Vitamine C-9 PtsDocument3 pages2015-Pondichery-Exo1-Correction-Vitamine C-9 PtsHaman Bello OumarouPas encore d'évaluation
- Bac CH 2006Document3 pagesBac CH 2006Haman Bello OumarouPas encore d'évaluation
- Bac CH 2000Document2 pagesBac CH 2000Haman Bello OumarouPas encore d'évaluation
- TD de Chimie Tle C&DDocument21 pagesTD de Chimie Tle C&DHaman Bello OumarouPas encore d'évaluation
- 2014 Polynesie Exo1 Correction AcideCitrique 5 5ptsDocument2 pages2014 Polynesie Exo1 Correction AcideCitrique 5 5ptsHaman Bello OumarouPas encore d'évaluation
- TP1: Réflexion Et Réfraction-Lois de Snell-Descartes: Table N°Document5 pagesTP1: Réflexion Et Réfraction-Lois de Snell-Descartes: Table N°Sarah KhaderPas encore d'évaluation
- Séries 2 Constituants de La Matière 1er CP 2021-2022Document2 pagesSéries 2 Constituants de La Matière 1er CP 2021-2022ZITOUNI AdemPas encore d'évaluation
- Iso 5048 1979Document11 pagesIso 5048 1979hamza aircraft engineerPas encore d'évaluation
- EWDR983-985 CS (LX) Fre 3-05Document11 pagesEWDR983-985 CS (LX) Fre 3-05jean-sebastien CordierPas encore d'évaluation
- Présentation 1Document151 pagesPrésentation 1hamzaPas encore d'évaluation
- MIMODocument52 pagesMIMOJordan WilsonPas encore d'évaluation
- Dimensionnement Partie2Document41 pagesDimensionnement Partie2Imane SAHDAOUIPas encore d'évaluation
- Caquot ForfaitaireDocument38 pagesCaquot ForfaitaireBadra Ali SanogoPas encore d'évaluation
- PolissageDocument22 pagesPolissageYoussef JlassiPas encore d'évaluation
- Esquema Electrico Cuenod 100Document8 pagesEsquema Electrico Cuenod 100Rafael pozo ramosPas encore d'évaluation
- 4limites Zones Et Opérations LiéesDocument8 pages4limites Zones Et Opérations LiéesYoussaf El goussiPas encore d'évaluation
- Physique - WikipédiaDocument1 pagePhysique - WikipédiaAmariliPas encore d'évaluation
- Simulation Dune Cellule PVDocument12 pagesSimulation Dune Cellule PVZiko halloumiPas encore d'évaluation
- Puissances ExercicesDocument8 pagesPuissances ExercicesSiskoPas encore d'évaluation
- Dimensionnement Optimal Dun Entrainement Synchrone Pour Une Application de Pompage PhotovoltaiqueDocument9 pagesDimensionnement Optimal Dun Entrainement Synchrone Pour Une Application de Pompage PhotovoltaiqueadrarwalidPas encore d'évaluation
- Marrakech-Safi Examen Regional Maths 2019 SujetDocument1 pageMarrakech-Safi Examen Regional Maths 2019 Sujetwac 1978Pas encore d'évaluation
- ch3 Proprietes Ondes EssentielDocument2 pagesch3 Proprietes Ondes EssentielNajimou Alade Tidjani100% (1)
- CHAPITRE1 L'acier Dans La Construction MétalliqueDocument12 pagesCHAPITRE1 L'acier Dans La Construction MétalliqueMélissa KhelilPas encore d'évaluation
- CHAP1Document5 pagesCHAP1Firas AguirPas encore d'évaluation
- Quantité de MouvementDocument7 pagesQuantité de MouvementEasye Troublej100% (2)
- Examens Nationaux Bacpro Voitures PC 2018 RDocument9 pagesExamens Nationaux Bacpro Voitures PC 2018 RSaidPas encore d'évaluation
- Exemple Concours Medecine FMP Rabat 2014 CorrigeDocument10 pagesExemple Concours Medecine FMP Rabat 2014 Corrigee.maskarPas encore d'évaluation
- Examen D - Optique Géométrique Session Normale 2013Document8 pagesExamen D - Optique Géométrique Session Normale 2013boukredimidjamel1958Pas encore d'évaluation
- Chapitre4 CisaillementDocument9 pagesChapitre4 CisaillementDawoud MayoufPas encore d'évaluation
- Activite 3 CorrectionDocument4 pagesActivite 3 CorrectionYoman Arthur verdier AssuiPas encore d'évaluation
- TD-2 - Interaction Rayonnement Matière - ModifiéDocument2 pagesTD-2 - Interaction Rayonnement Matière - ModifiéLodvert T. POATYPas encore d'évaluation
- Coagulation FloculationDocument27 pagesCoagulation Floculationabderrahimn0% (1)
- TP 5 Etude Alternateur TriphaseDocument10 pagesTP 5 Etude Alternateur Triphaseomar ballalouPas encore d'évaluation
- On Asymptotic Analysis and Homogenization of PerioDocument135 pagesOn Asymptotic Analysis and Homogenization of PerioSMITIPas encore d'évaluation
- 07 R Régional PC Marrakech Safi 2021 (WWW - Pc1.ma)Document3 pages07 R Régional PC Marrakech Safi 2021 (WWW - Pc1.ma)Yassine El KassirPas encore d'évaluation