Académique Documents
Professionnel Documents
Culture Documents
Ai 99
Ai 99
Transféré par
ami rTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Ai 99
Ai 99
Transféré par
ami rDroits d'auteur :
Formats disponibles
Agrégation interne 1999 Corrigé
Partie B
Théorie de Hückel
I. Conjugaison et structure.
1.1.1. Un système est dit conjugué si les OM π (ou non-liantes) se recouvrent. Ce qui se produit
lorsque elles ont même symétrie et ne sont séparées que par une liaison σ.
1.1.2. A : oui ; B : oui ; C : non ; D : non ; E : oui ; F : oui ; G : oui ; H : oui ; I : oui ; N : oui ; K :
non ; L : non.
1.1.3. A : buta-1,3-diène ; D : cyclohexa-1,4-diène ; E : propénal ; H : vinylbenzène (ou
phényléthylène).
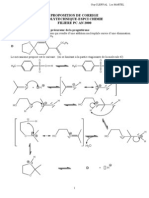
1.1.4.
- O
A E O
+ +
I - O O
1.1.5. Il y a deux conformations où la conjugaison est possible : s-cis et s-trans, mais on ne peut
pas parler de stéréoisomères.
1.2.1.1. Intégrale coulombienne : énergie de l’orbitale atomique « seule ». (α = <ϕΗϕ>)
1.2.1.2. Energie de stabilisation due au recouvrement des deux orbitales. (β = <ϕiΗϕ,j> i et j
atomes liés)
1.2.1.3. méthanal (CH2O) : 1 électron π ; méthoxyéthylène : 2 électrons π.
1.2.1.4 Le fluor est le plus électronégatif des éléments on trouve bien que les orbitales p sont
basses.
x 1 1
1.2.1.5. Déterminant : 1 x 1 = x3 – 3x + 2, on trouve les racines – 2, 1 (racine double).
1 1 x
Donc E1 = α + 2 β et E2 = α – β (niveau dégénéré, deux
orbitales)
coefficients des OM
OM N° 1 0.5774 0.5774 0.5774
OM N° 2 0.7071 – 0.0000 – 0.7071
OM N° 3 0.4082 – 0.8165 0.4082
1.2.2 On prend α = 0.
JM Toledano Page 1/6
Agrégation interne 1999 Corrigé
1.3.1. voir annexe
1.3.2. Pour l’éthylène l’énergie des 2 électrons est de ε0 = 2(α + β)
nb
επ επ’ επ – επ’
électrons
cyclobutadiène 4 4α + 4β 4(α + β) 0
hexa-1,3,5-triène 6 6α + 7β 6(α + β) β
octa-1,3,5,7-tétraène 8 8α + 9,52β 8(α + β) 1,52β
cycloocta-1,3,5,7-tétraène 8 8α + 9,64β 8(α + β) 1,64β
benzène 6 6α + 8β 6(α + β) 2β
butadiène 4 4α + 4,472β 4(α + β) 0,472β
fulvène 6 6α + 7,466β 6(α + β) 1,466β
acroléine 4 4α + 5,76β 4(α + β) 1,76β
1.3.3. β étant négatif on voit qu’il y a toujours stabilisation sauf dans le cas du cyclobutadiène
(ce cas et celui du cyclooctatétraène ne correspondent à rien de réel les molécules ne sont pas
planes et il n’y a pas de conjugaison).
1.3.4.1. benzène (comparé au hexa-1,3,5-triène) : ∆εres = 6α + 8β – (6α + 7β) = β < 0 aromatique
en accord avec le critère simple.
cycloocta-1,3,5,7-tétraène (comparé au cycloocta-1,3,5,7-tétraène) :
∆εres = 8α + 9,64β – (8α + 9,52β) = 0,12 β < 0 aromatique (c’est faux !) en désaccord avec le
critère simple.
fulvène (comparé au hexa-1,3,5-triène) : ∆εres = 6α + 7,466β – (6α + 7β) = 1,466β < 0
aromatique en désaccord avec le critère simple.
cyclopropénium (comparé à l’éthylène) : ∆εres = 2α + 4β – (2α + 2β) = β < 0 aromatique en
accord avec le critère simple.
1.3.5.1. énergie de délocalisation : – 3.119,7 + 206,3 = – 152,8 kJ/mol.
1.3.5.2. N : oui les deux cycles, A : oui, un seul cycle. La différence des énergies de combustion
est égale à la différence des énergies de résonance (même liaisons rompues) : N – A = 137 kJ/mol
c’est N qui a la plus forte énergie de résonance.
JM Toledano Page 2/6
Agrégation interne 1999 Corrigé
II. Application de Hückel à la réactivité chimique.
2.1.1.
H H H H
C
+
H Cl H Cl
2.1.2. OM π de l’éthène et 3p non-liante de Cl.
2.1.3. Cl : mésomère donneur. On voit un abaissement de la première orbitale, un relèvement de
la seconde (HO) et de la troisième (BV).
2.1.4. q1 = – 0,04 e ; q2 = 0,02 e ; q3 = 0,02 e. On voit une légère charge + sur le C2 correspondant
à un effet inductif attracteur.
2.1.5. L’attaque de H+ a lieu sur le C1 (charge –), on a :
H H +
H H
H +
C Cl CH3CHCl2
H Cl H Cl
2.2.1.1. On trouve q6 = 0,38 e.
2.2.1.2. On peut écrire :
+
_
la deuxième forme mésomère est aromatique (6 électrons conjugués dans un cycle), la charge –
se répartit sur les 5 C (d’après les formes mésomères, le calcul donne une différence entre les C).
2.2.1.3. Le nucléophile va sur la charge + du C6.
2.2.1.4. La charge – du cycle peut donner lieu à des attaques électrophiles sur les C les plus
chargés (d’après les calculs C2 et C5).
2.2.2. : le tableau donné par l’énoncé comporte des erreurs, voici les valeurs que j’ai calculé :
Énol :
O est l’atome 3
Energies : α + 2.336β α + 0.773β α – 1.108β
coefficients des OM
OM N° 1 0.1634 0.3816 0.9098
OM N° 2 0.7351 0.5680 -0.3702
OM N° 3 0.6580 -0.7292 0.1877
Déterminant
x 1 0
1 x 0.8
0 0.8 x+2
Énolate :
O est l’atome 1
JM Toledano Page 3/6
Agrégation interne 1999 Corrigé
Energies : α + 1.802β α + 0.445β α – 1.247β
coefficients des OM
OM N° 1 0.7370 0.5910 0.3280
OM N° 2 -0.5910 0.3280 0.7370
OM N° 3 -0.3280 0.7370 -0.5910
Déterminant
x+1 1 0
1 x 1
0 1 x
2.2.2.1. Charges partielles :
O : -2 e(0,737² + 0,591²) = -1,785 e soit δ- = - 0,785 e
C2 : -2 e(0,591² + 0,328²) = - 0,914 e soit δ- = + 0,086 e
C3 : -2 e(0,328² + 0,737²) = - 1,302 e soit δ- = - 0,302 e
2.2.2.2. Par l’atome O (je suppose que c’est l’énolate le nucléophile)
2.2.2.3. La HO (OM 2) a un plus fort coefficient sur C3 : c’est par là que ça réagit.
2.2.2.4. Deux réactions possibles :
O Br O
C
Br O
O
Le diméthoxyéthane (DME) solvate les alcalins par les oxygènes mais la DMF(c' est à dire le
diméthylméthanamide comme dit l' énoncé) est un solvant aprotique polaire qui est très bon
dissociant et qui solvate spécifiquement les cations : Donc dans la DMF l' oxygène ne sera pas
sous forme de paire d' ion, sera bien libre et on aura essentiellement de l'
O-alkylation. Dans la
DME, l' énolate sera moins dissocié, se trouvera plus ou moins sous paire d' ion et on observe
surtout de la C-alkylation (Merci à JM Kern)
2.3.1.1. Aucune !
2.3.1.2. Le second ne réagit pas en Diels Alder car la position trans
des doubles liaisons est bloquée.
2.3.1.3.1. On utilise la HO du diène et la BV du diénophile. Cette
position mène à K qui est majoritaire car il y a un recouvrement
secondaire favorable (flèches courbes) entre les OA des C des
esters et les deux C au fond du cycle. On forme le composé endo.
2.3.1.3.2. Le composé R R
minoritaire est le
composé exo :
O O
COOMe
COOMe
JM Toledano Page 4/6
Agrégation interne 1999 Corrigé
s2.3.1.4. Les substituants de la double liaison étant trans ils le restent dans le composé d’addition.
La molécule est chirale on l’obtient sous forme d’un racémique (2 énantiomères 50/50). La
réaction est stéréosélective (un stéréoisomère et pas l’autre) mais pas énantiosélective.
H3C CH2 MeOOC COOMe
H3C
CH2 COOMe
H3C COOMe H3C
H3C CH2 COOMe COOMe
H3C
CH2 COOMe
H3C MeOOC H3C
2.4.1.1. Soit butadiène + éthylène donne cyclohexène, soit 2 butadiène donne 4-
vinylcyclohexène. Isomère s-cis.
2.4.1.2. On reprend le dessin fait ci-dessus : on voit
que la BV du butadiène est plus proche de sa HO que
de celle de l’éthylène.
2.4.2.1.
dx
dt = k1 [ A ][ B] = k1 (a − x)(a − x − 2y)
dy = k [ B]2 = k (a − x − 2y) 2
dt 2 2
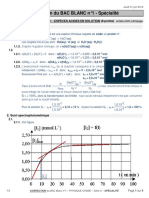
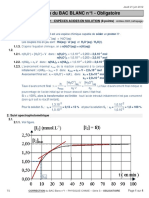
2.4.2.2. On aura quelque chose de ce genre, au dessus x,
y en dessous (j’ai pris k1 > k2, voir ci-dessous)
2.4.2.3. Chaque molécule d’acroléine réagit avec une
molécule de butadiène, donc les 78% de butadiène ayant
réagi se décomposent en 65% par la réaction 1 et 13%
par la réaction 2. Les OM de l’acroléine vues ci-dessus
sont plus basses on a un diènophile plus réactif.
2.5.1. La base conjuguée est aromatique (6 électrons dans un cycle).
2.5.2.1. C5H10 + H – → C5H9 – + H2↑. Le dihydrogène dégageant la réaction est totale.
2.5.2.2. Pour détruire le dimère qui s’est éventuellement formé.
2.5.2.3. Attaque nucléophile.
2.5.2.4. On a :
JM Toledano Page 5/6
Agrégation interne 1999 Corrigé
H3C
_ H3C
CH3
CH3
H3C CH3
OH
+ O-
H
H
O
H3C H3C CH3
CH3
OH
H
OH-
La facilité est due à l’obtention d’un système conjugué (cf la crotonisation des aldols).
2.5.3.1. Réaction d’acétalisation : N est le 3-bromopranal.
O Br HO Br
+
CH
+
H
HO OH
etc…
2.5.3.2. Oui en milieu acide avec un excès d’eau (c’est tout
son intérêt : protection réversible de la fonction aldéhyde)
2.5.3.3. Il y a SN du cyclopentadiènate sur le Br. O O
2.5.3.4. En milieu acide avec un excès d’eau l’acétal
redonne l’aldéhyde.
JM Toledano Page 6/6
Vous aimerez peut-être aussi
- Corrigé Centrale 2010 Acide OxaliqueDocument6 pagesCorrigé Centrale 2010 Acide OxaliquePascal FrajmanPas encore d'évaluation
- Exercices-Materiaux-Chapitre IDocument8 pagesExercices-Materiaux-Chapitre IJewel Slam100% (1)
- SMDocument26 pagesSMLghazi OumssadPas encore d'évaluation
- 2010 Pondichery Exo1 Correction Polonium 6ptsDocument2 pages2010 Pondichery Exo1 Correction Polonium 6ptsla physique selon le programme FrançaisPas encore d'évaluation
- 2013 Antilles Exo2 Correction Pommes 10ptsDocument3 pages2013 Antilles Exo2 Correction Pommes 10ptsYasmine HamichePas encore d'évaluation
- Corrigé Serie D Session 2015Document8 pagesCorrigé Serie D Session 2015inayalinah4Pas encore d'évaluation
- DS4 - Reactions Nucleaires - Cohésion Solides - DissolutionDocument3 pagesDS4 - Reactions Nucleaires - Cohésion Solides - DissolutionKARENPas encore d'évaluation
- Liaison ChimiqueDocument31 pagesLiaison Chimiquezdramane950Pas encore d'évaluation
- Controle 2020 QuantiqueDocument2 pagesControle 2020 QuantiqueRhm Gaming100% (1)
- Exercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le SoleilDocument3 pagesExercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le Soleilroudy100% (1)
- ch01 SolutionnaireDocument40 pagesch01 SolutionnaireWaqar BaigPas encore d'évaluation
- 5 - Effets ÉlectriquesDocument12 pages5 - Effets Électriqueshoussam.mouhtadiPas encore d'évaluation
- Atomistique Ex CorDocument2 pagesAtomistique Ex Coramirtrk80100% (1)
- Physique 2011 Principale Correction PDFDocument9 pagesPhysique 2011 Principale Correction PDFRoua ManiPas encore d'évaluation
- Alcènes Énoncés ExercicesDocument62 pagesAlcènes Énoncés ExercicesMaxime EidelsbergPas encore d'évaluation
- Cours Orga SMC S3 2021Document118 pagesCours Orga SMC S3 2021zniber.fatima2001Pas encore d'évaluation
- Corrigé Serie D 2021Document7 pagesCorrigé Serie D 2021ChristellePas encore d'évaluation
- PC 1D 1a Ta S2 2024Document4 pagesPC 1D 1a Ta S2 2024arsene BATAWUILAPas encore d'évaluation
- Examen National Physique Chimie SPC 2016 Normale Corrige 1Document9 pagesExamen National Physique Chimie SPC 2016 Normale Corrige 1othmane GbPas encore d'évaluation
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014)Document5 pagesDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014)AliMchirguiPas encore d'évaluation
- Corrigé CNC Chimie 2012 MPDocument6 pagesCorrigé CNC Chimie 2012 MPzazazaz2000100% (1)
- TS - BAC Blanc N°1 Corrigé - Spécialité PDFDocument4 pagesTS - BAC Blanc N°1 Corrigé - Spécialité PDFphytanjaPas encore d'évaluation
- Corrigé de L'épreuve de Sciences Physiques: Universite C A D DDocument5 pagesCorrigé de L'épreuve de Sciences Physiques: Universite C A D DLindeltaylor DioufPas encore d'évaluation
- Physique C PDFDocument4 pagesPhysique C PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Architecture Moléculaire Et StéréochimieDocument5 pagesArchitecture Moléculaire Et StéréochimielucatelliPas encore d'évaluation
- Concours 2012 (+sol.) Proposition EPST23Document19 pagesConcours 2012 (+sol.) Proposition EPST23Nidal BestPas encore d'évaluation
- ExamenDocument3 pagesExamenIheb DassiPas encore d'évaluation
- 1es Chap 1 Cours Poly CompleteDocument6 pages1es Chap 1 Cours Poly CompleteDavid LandellePas encore d'évaluation
- C 00 XP 1 CDocument13 pagesC 00 XP 1 CMihnea GamanPas encore d'évaluation
- 5351 Entrainement TSDocument6 pages5351 Entrainement TSmohammed laadili100% (1)
- 2010 Asie Exo3 Correction QROCChimie 6 5pts - 2Document3 pages2010 Asie Exo3 Correction QROCChimie 6 5pts - 2Youssef DahaniPas encore d'évaluation
- Corrige td1 ElectrochimieDocument7 pagesCorrige td1 Electrochimieayoub dahbi100% (1)
- CNC 2000 Chimie MP CorrectionDocument4 pagesCNC 2000 Chimie MP CorrectionNouhaila AfakirePas encore d'évaluation
- Sujets Pass2021Document4 pagesSujets Pass2021indien cheperPas encore d'évaluation
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Handoura NaceurDocument4 pagesDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Handoura NaceurMohamed SaidiPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - ObligatoireDocument4 pagesTS - BAC Blanc N°1 Corrigé - ObligatoirephytanjaPas encore d'évaluation
- Devoir Up PhysiqueDocument4 pagesDevoir Up PhysiquedianechibidouxPas encore d'évaluation
- Bacc PC Serie C 1999 - 2013Document55 pagesBacc PC Serie C 1999 - 2013riantsoaPas encore d'évaluation
- 1cm41mch1 245884Document5 pages1cm41mch1 245884Absa NdiayePas encore d'évaluation
- C Chtsi2021Document8 pagesC Chtsi2021Rose kalvine MougoulaPas encore d'évaluation
- Examen1 Réactivité Chimique FST-MeknèsDocument6 pagesExamen1 Réactivité Chimique FST-MeknèsayabourhdifaPas encore d'évaluation
- Hückel Elèves TDDocument3 pagesHückel Elèves TDami rPas encore d'évaluation
- Correction TD Chimie Générale Fiche1Document6 pagesCorrection TD Chimie Générale Fiche1comboudriPas encore d'évaluation
- Chap 4 EFFET S ELECTRONIQUESDocument8 pagesChap 4 EFFET S ELECTRONIQUESEL Menani NadiaPas encore d'évaluation
- Bac PCDocument5 pagesBac PCOumar KakoroPas encore d'évaluation
- Chimie-Bioch 1 2010Document17 pagesChimie-Bioch 1 2010raspberry najmPas encore d'évaluation
- Edlab PC 2017 CorreDocument2 pagesEdlab PC 2017 Corresaidouly95Pas encore d'évaluation
- Corrige Bac 2009Document2 pagesCorrige Bac 2009Claudy TsakengPas encore d'évaluation
- Devoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaDocument7 pagesDevoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaTawfiq Weld EL ArbiPas encore d'évaluation
- Chapitre IVDocument8 pagesChapitre IVYu-oh CrysisPas encore d'évaluation
- Cu Ag MG Cu Ag MG POCDocument3 pagesCu Ag MG Cu Ag MG POCorsiny clinton TCHAPTCHETPas encore d'évaluation
- TD Avec SolutionDocument21 pagesTD Avec SolutionAll AhmeDcia0% (1)
- Mecanisme Reactionnel SN1 SN2 OuziDocument33 pagesMecanisme Reactionnel SN1 SN2 Ouzisafae ziyatiPas encore d'évaluation
- DS05Document11 pagesDS05baatoutmbPas encore d'évaluation
- Effets Electroniques OrganiqueDocument21 pagesEffets Electroniques OrganiqueLahcen ElamraouiPas encore d'évaluation
- Homework Corrosion BekhdidjaDocument4 pagesHomework Corrosion BekhdidjaفتحيPas encore d'évaluation
- Cor Sujet ChimieDocument5 pagesCor Sujet ChimiefaridattallahPas encore d'évaluation
- Physique Bac MathDocument4 pagesPhysique Bac MathSofia BahriniPas encore d'évaluation
- Cours Techniques SpectroscopiquesDocument34 pagesCours Techniques Spectroscopiquesami rPas encore d'évaluation
- Examen Chimie Theorique SMC5 - Partie HuckelDocument4 pagesExamen Chimie Theorique SMC5 - Partie Huckelami rPas encore d'évaluation
- 3.systemes Polyelectroniques AtomesDocument21 pages3.systemes Polyelectroniques Atomesami rPas encore d'évaluation
- APCQ3Document16 pagesAPCQ3ami rPas encore d'évaluation
- Cours CQ CIDocument86 pagesCours CQ CIami rPas encore d'évaluation
- Simple Huckel CH404Document3 pagesSimple Huckel CH404ami rPas encore d'évaluation
- Chap3 Modele Ondulatoire de L'atomeDocument15 pagesChap3 Modele Ondulatoire de L'atomeami rPas encore d'évaluation
- 2021 sp1 Devoir01Document3 pages2021 sp1 Devoir01ami rPas encore d'évaluation
- Décoloration Du PH - PHDocument2 pagesDécoloration Du PH - PHami rPas encore d'évaluation
- 2014 01 26 TD3Document2 pages2014 01 26 TD3ami rPas encore d'évaluation
- امن المخبرDocument1 pageامن المخبرami rPas encore d'évaluation
- Hückel Elèves TDDocument3 pagesHückel Elèves TDami rPas encore d'évaluation
- Travaux Pratiques de Thermodynamique Et de Cinétique ChimiquesDocument18 pagesTravaux Pratiques de Thermodynamique Et de Cinétique Chimiquesami rPas encore d'évaluation
- Expériences ChimieDocument9 pagesExpériences Chimieami rPas encore d'évaluation
- Présentation Teneur en Eau Dans Les Huiles DiélctriquesDocument5 pagesPrésentation Teneur en Eau Dans Les Huiles Diélctriqueschichid2008Pas encore d'évaluation
- Extraction Liquide Liquide 20 - 210517 - 114623Document24 pagesExtraction Liquide Liquide 20 - 210517 - 114623Mahmoud MazboudiPas encore d'évaluation
- Extraction Liquide-LiquideDocument7 pagesExtraction Liquide-LiquideAbdou MiringhiPas encore d'évaluation
- UE CHM 4168 2022-2023 TD No1 SyntheseDocument2 pagesUE CHM 4168 2022-2023 TD No1 SyntheseIsocrate DourrawaPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - Spécialité PDFDocument4 pagesTS - BAC Blanc N°1 Corrigé - Spécialité PDFphytanjaPas encore d'évaluation
- DPS Iii - Q - Cis - Apd - CVD - Clim-Fte - Syn - Bat.02Document9 pagesDPS Iii - Q - Cis - Apd - CVD - Clim-Fte - Syn - Bat.02valdes zebazePas encore d'évaluation
- .Parties Du DiscoursDocument8 pages.Parties Du DiscoursKirby KjongPas encore d'évaluation
- Chapitre III Transitions Du Premier Et Second OrdreDocument13 pagesChapitre III Transitions Du Premier Et Second OrdreLamiae NouiguiPas encore d'évaluation
- Le Théâtre Classique, Module 18, Semestre 3, Aicha BouraisDocument7 pagesLe Théâtre Classique, Module 18, Semestre 3, Aicha BouraisAdil AmmariPas encore d'évaluation
- Des Melanges DangereuxDocument4 pagesDes Melanges Dangereuxproduction.assur2cPas encore d'évaluation
- Exercices 13 Suivi TemporelDocument1 pageExercices 13 Suivi Temporelالغزيزال الحسن EL GHZIZAL Hassane75% (4)
- Théorie Du Champ Cristallin 2019-2020Document2 pagesThéorie Du Champ Cristallin 2019-2020Roi AroufPas encore d'évaluation
- Fiche 1 - Principales Propriétés Des Différentes Classes de PolymèresDocument26 pagesFiche 1 - Principales Propriétés Des Différentes Classes de PolymèresManamba Dite Sisse TraoréPas encore d'évaluation
- DS2 3 Eme T 2023Document4 pagesDS2 3 Eme T 2023Riadh MarouaniPas encore d'évaluation
- Indicateurs ColoresDocument3 pagesIndicateurs ColoresWEMBE RAOULPas encore d'évaluation
- Xypex ConcentreDocument4 pagesXypex ConcentreAdel BouatayPas encore d'évaluation
- Sujet2015 Cap CDocument10 pagesSujet2015 Cap CpaulardPas encore d'évaluation
- Activité 3: L'élément Oxygène Dans Notre Atmosphère (Correction)Document2 pagesActivité 3: L'élément Oxygène Dans Notre Atmosphère (Correction)EvaPas encore d'évaluation
- Exploration Des Ressources Minerales Et Energetiques Bouabsa LDocument79 pagesExploration Des Ressources Minerales Et Energetiques Bouabsa LMohammed Larbi FaradjiPas encore d'évaluation
- TP Comment Synthétiser Et Caractériser Un PolymèreDocument3 pagesTP Comment Synthétiser Et Caractériser Un PolymèrealexbardonfrPas encore d'évaluation
- Projet DeclairageDocument7 pagesProjet Declairageabdelbasset elwaddaniPas encore d'évaluation
- Les Matériaux Nanostructurés PDFDocument49 pagesLes Matériaux Nanostructurés PDFmortadaPas encore d'évaluation
- 5-Structures AlternativesDocument16 pages5-Structures AlternativesOthman ShonePas encore d'évaluation
- Travaux Dirigés de Chimie N° 6: Exercice 1: Équations de Réaction Et Constantes D'équilibreDocument4 pagesTravaux Dirigés de Chimie N° 6: Exercice 1: Équations de Réaction Et Constantes D'équilibreAbderrahman IGHNIHPas encore d'évaluation
- Correction Exercices Chapitre N°8 - Oxydo-Réduction Dans Les Piles Et AccumulateursDocument3 pagesCorrection Exercices Chapitre N°8 - Oxydo-Réduction Dans Les Piles Et Accumulateursunsheatedsword55Pas encore d'évaluation
- Salim DouaaDocument220 pagesSalim DouaaAbdoPas encore d'évaluation
- InmunohistochimieDocument4 pagesInmunohistochimiepame RodriguezPas encore d'évaluation
- Evaluation Solides Cristallins Sujet A À FDocument10 pagesEvaluation Solides Cristallins Sujet A À Frania rejebPas encore d'évaluation
- Mig225syn FRDocument18 pagesMig225syn FRalain.broussyPas encore d'évaluation