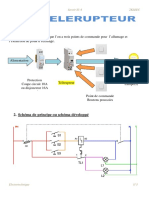
Académique Documents
Professionnel Documents
Culture Documents
Tpbinaire
Tpbinaire
Transféré par
Ämø ŰñåTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Tpbinaire
Tpbinaire
Transféré par
Ämø ŰñåDroits d'auteur :
Formats disponibles
1 – TP [TPBinaire.
tex] Sciences Physiques MP
TP : Diagramme binaire
Nous allons, dans ce TP, tracer le diagramme binaire d’un mélange liquide eau-propanol. Le propanol de formule
CH3 − CH2 − CH2 OH est un liquide de densité 0, 80 donc de masse volumique 0, 80 g · mL−1 qui possède une
température d’ébullition de 97, 2 ˚C sous la pression atmosphérique de 1 bar. Le diagramme de ce mélange
binaire possède l’allure donné à la figure 1. Le montage expérimental est photographié à la figure 5.
T en ˚C
100
p = 1 bar
98
97,2˚C
96
94
92
90
88
86
84
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1
fraction molaire en propanol
Fig. 1 – Diagramme binaire isobare eau-propanol
A. Principe de l’expérience
Le principe est le suivant : un mélange binaire va être porté à l’ébullition t0 ( ˚C). Lorsque cette ébullition est
atteinte, on note la température. De la vapeur s’est formée. Le réfrigérant à eau étant placé très près du ballon,
on admettra que la vapeur se liquéfie à t0 ( ˚C). On récupère une petite partie de la vapeur liquéfiée dans un
petit bécher. Cela va nous permettre de placer deux points sur le diagramme binaire : sur la droite horizontale
t0 ( ˚C), on placera un point de la courbe d’ébullition de fraction massique xL prop en propanol calculée à partir
des volumes mélangés. Pour le point de la courbe de rosée qui correspond à la liquéfaction de la vapeur, sa
fraction massique en propanol xVprop sera déterminée par mesure de l’indice de réfraction grâce au réfractomètre
d’Abbe. On peut ainsi construire les courbes de rosée et d’ébullition, voir la figure 2.
t(˚C)
t0 (˚C) b b b
b b
xL xVprop x
prop
Fig. 2 – Principe de construction du diagramme binaire
B. Réfractomètre d’Abbe
Le réfractomètre d’Abbe permet de mesurer de façon très précise l’indice de réfraction de la vapeur liquéfiée.
Il s’utilise en déposant quelques gouttes de liquide - issues directement du bécher où l’on recueille la vapeur
liquéfiée - sur la face horizontale en verre de l’appareil. On referme alors la partie mobile. Après avoir réglé
l’oculaire à sa vue, en tournant le plus gros bouton, on devrait voir une frontière horizontale entre une zone
éclairée et une zone sombre, comme sur la figure 3.
JR Seigne Fauriel St Etienne
Sciences Physiques MP TP [TPBinaire.tex] – 2
Mauvais réglage Bon réglage
Fig. 3 – Aperçu du disque observé dans le réfractomètre
Un bouton plus petit permet de supprimer les effets chromatiques et d’affiner la frontière. Lorsqu’on aura utilisé
le réfractomètre, il faudra aussitôt essuyer délicatement, avec un mouchoir fin, la surface de verre où on a déposé
le liquide. À partir de la mesure de l’indice, on déterminera xVprop par lecture sur la courbe d’étalonnage fournie,
car la relation entre l’indice et la fraction massique de propanol n’est pas linéaire, comme on peut le constater
sur le graphique de la figure 4.
n
1,39
1,38
1,37
1,36
1,35
1,34
1,33
0 10 20 30 40 50 60 70 80 90 100
x : fraction massique en propanol
Fig. 4 – Courbe d’étalonnage : évolution de l’indice
C. Expérience
Le montage expérimental est celui de la figure 5.
Nous allons réaliser deux expériences, l’une en commençant par l’eau pure et l’autre en commençant par le
propanol pur.
1. Mettre 30 mL d’eau distillée (30 g) dans le ballon avec de la pierre ponce (quelques grains).
2. Ajouter 0, 5 mL de propanol mesuré avec une pipette extrêmement fine.
3. Mettre en route l’eau du réfrigérant.
4. Mettre en route le chauffage au voisinage du maximum.
5. Lorsque l’ébullition se produit, observer l’évolution de la température, attendre que le système soit à l’équi-
libre et que de la vapeur se liquéfie et remplisse le tube d’écoulement muni du robinet, mesurer la température
t0 (˚C) grâce au thermomètre.
6. Lorsque le petit tube de verre d’écoulement avant le réfrigérant est plein, enlever le chauffe-ballon (sans
baisser son thermostat) et refroidir en mettant le ballon en contact avec un cristallisoir contenant un peu de
glace, on observera la baisse de température. Lorsque la température est de l’ordre de 70˚C, on peut arrêter de
refroidir.
7. Récupérer la vapeur liquéfiée dans un petit bécher, en verser avec précaution quelques gouttes directement
depuis le petit bécher sur la surface en verre du réfractomètre. Mesurer l’indice optique n du mélange binaire
prélevé.
8. Dévisser complètement le petit robinet, l’essuyer comme d’ailleurs le petit bécher. Refermer ce robinet.
9. Ajouter un nouveau volume de propanol.
10. Remettre le chauffe-ballon et ainsi de suite...
JR Seigne Fauriel St Etienne
3 – TP [TPBinaire.tex] Sciences Physiques MP
Fig. 5 – Montage d’étude du diagramme binaire
11. À chaque opération, on doit effectuer deux mesures : t0 (˚C) et n. On ajoutera le propanol selon le tableau :
vprop ( mL) ajouté 0,5 0,5 1 2 2 4 10 20
mprop ( g) ajoutée 0,4
mtotale 30,4
xLprop calculée en % 1,3
t0 (˚C) mesurée
n mesuré
xVprop mesurée en %
12. Recommencer l’expérience dans un nouveau ballon propre et sec avec 30 mL de propanol pur (24 g). Les
ajouts s’effectueront selon le tableau :
veau ( mL) ajouté 0,5 0,5 1 2 4 4 10
meau ( g) ajoutée 0,5
mtotale 24,5
xL
prop calculée en % 98,0
t0 (˚C) mesurée
n mesuré
V
xprop mesurée en %
D. Exploitation des mesures
13. Proposer dans le compte rendu des tableaux complétés sur le modèle de ceux des questions précédentes.
Pour les calculs, on ne tiendra pas compte des faibles volumes prélevés pour effectuer les mesures.
14. Réaliser sur un papier millimétré le diagramme binaire en choisissant intelligemment les échelles (la
température sera comprise entre 85˚C et 100˚C environ). On fera apparaı̂tre les points de la courbe d’ébullition
en une couleur et ceux de la courbe de rosée en une autre couleur.
15. À partir du tracé du diagramme binaire, décrire toutes les situations de refroidissement d’une vapeur ou
de chauffage d’un liquide (évolution de t(˚C)).
16. Décrire avec soin les différentes situations que l’on pourra rencontrer lors d’une distillation d’un mélange
binaire eau-propanol.
JR Seigne Fauriel St Etienne
Vous aimerez peut-être aussi
- TP ThermodynamiqueDocument10 pagesTP ThermodynamiqueBeto Trejo Avila100% (1)
- 6th Central Pay Commission Salary CalculatorDocument15 pages6th Central Pay Commission Salary Calculatorrakhonde100% (436)
- Fiche TD Opu N 1 l3 Gp2020 2021Document4 pagesFiche TD Opu N 1 l3 Gp2020 2021Mohamed Berber100% (1)
- Thermodynamique Exercices T6 - Equilibre D'un Corps Pur Sous Deux PhasesDocument5 pagesThermodynamique Exercices T6 - Equilibre D'un Corps Pur Sous Deux PhasesIhsan Mokhlisse100% (4)
- Manipulation 1Document5 pagesManipulation 1Debdoubi Abdel100% (1)
- Diagrame Binaire Eau PropanolDocument4 pagesDiagrame Binaire Eau PropanolMari MareqsdfPas encore d'évaluation
- Tpchaire 1Document2 pagesTpchaire 1Abdallah HachaniPas encore d'évaluation
- Poly TP Spectro de FlammeDocument5 pagesPoly TP Spectro de FlammeLaura Dijoux100% (1)
- TD Chimie Physique Appliquée 2022Document8 pagesTD Chimie Physique Appliquée 2022Ivan YamdjeuPas encore d'évaluation
- Exo de VacancesDocument2 pagesExo de VacancesKerherve JulienPas encore d'évaluation
- 1ère SérieDocument3 pages1ère SérieAbdallah abdellaouiPas encore d'évaluation
- 1ère SérieDocument3 pages1ère SérieAbdallah abdellaoui100% (1)
- Travaux Dirigés de Distillation-ConvertiDocument4 pagesTravaux Dirigés de Distillation-ConvertiSaâd Sardi100% (1)
- TP AdiabatiqueonDocument3 pagesTP AdiabatiqueonmajdoubPas encore d'évaluation
- Rattrapage S4 - Juin 2019 - SolutionDocument6 pagesRattrapage S4 - Juin 2019 - SolutionIm printPas encore d'évaluation
- TD 2 de ThermochimieDocument4 pagesTD 2 de ThermochimieCARDI BPas encore d'évaluation
- TP t2 Calorimetrie Mesures D Enthalpie Massique de Fusion Et D Enthalpie Standard de ReactionDocument4 pagesTP t2 Calorimetrie Mesures D Enthalpie Massique de Fusion Et D Enthalpie Standard de Reactionnawaramira59Pas encore d'évaluation
- Olympiades 2012Document102 pagesOlympiades 2012Stephan Lampert100% (1)
- TP Distillation Courbe de RoséeDocument9 pagesTP Distillation Courbe de RoséeKeryl Crawford100% (1)
- TDDIS2019Document8 pagesTDDIS2019Étoile D'or100% (1)
- °smc4 TD Thermodynamique Chimique Fsdm-Fes 19-20Document23 pages°smc4 TD Thermodynamique Chimique Fsdm-Fes 19-20Ayoub OuangliPas encore d'évaluation
- Exo T6liqvapDocument8 pagesExo T6liqvapجعدبندرهم100% (1)
- Recueil de Genie Chimique G3Document14 pagesRecueil de Genie Chimique G3MbuluPas encore d'évaluation
- Fiche TD Opu 2023 2024 GPDocument4 pagesFiche TD Opu 2023 2024 GPClash of Clans Bilal DzPas encore d'évaluation
- 07 Diagrammes Td-EnonceDocument4 pages07 Diagrammes Td-Enoncecours importantPas encore d'évaluation
- Serie 1 de TDDocument3 pagesSerie 1 de TDbouraiou nabilaPas encore d'évaluation
- Seq 7 ExercicesDocument4 pagesSeq 7 ExercicesMõ ÖnPas encore d'évaluation
- TD 1Document2 pagesTD 1forio_23Pas encore d'évaluation
- Binaires 2Document8 pagesBinaires 2محمد الفاتح100% (1)
- TD1-Dist 21Document1 pageTD1-Dist 21HPas encore d'évaluation
- Série #1 S2 PIC8 19-20Document6 pagesSérie #1 S2 PIC8 19-20SALIMA BOULAIDPas encore d'évaluation
- Série #3 - S4 2021 PDFDocument3 pagesSérie #3 - S4 2021 PDFYounesPas encore d'évaluation
- Examen 2022Document2 pagesExamen 2022salma ihssanPas encore d'évaluation
- Distillation FractionnéeDocument4 pagesDistillation FractionnéeImen FarhatPas encore d'évaluation
- TD de Thermodynamique CPGE1-2023Document5 pagesTD de Thermodynamique CPGE1-2023Ange Michel Romuald DjePas encore d'évaluation
- Exercices de La Thermodynamique Appliquée1Document3 pagesExercices de La Thermodynamique Appliquée1minhtuanbk202Pas encore d'évaluation
- TD1-Complèmentaire-Corps PurDocument5 pagesTD1-Complèmentaire-Corps PurmennanesalaheddinePas encore d'évaluation
- TRAVAILDocument4 pagesTRAVAILYa Cin KhaldiPas encore d'évaluation
- Soutien Pcsi 3 Vitesse Et Loi de VitesseDocument5 pagesSoutien Pcsi 3 Vitesse Et Loi de VitesseHarakat ElhoucinePas encore d'évaluation
- TPP2-1Spe-Sujet-Loi de MariotteDocument2 pagesTPP2-1Spe-Sujet-Loi de MariotteceliabenayPas encore d'évaluation
- 2010 11.cours.06 Changement de Phases Des Corps Purs - Powerpoint.thermoDocument18 pages2010 11.cours.06 Changement de Phases Des Corps Purs - Powerpoint.thermoloicdeezer2Pas encore d'évaluation
- Examen Blanc 5 - FinalDocument8 pagesExamen Blanc 5 - FinalBouchra100% (1)
- Serie 1 de TD 2022Document3 pagesSerie 1 de TD 2022bouraiou nabilaPas encore d'évaluation
- Série TD Distillation-Rectification 2020-2021Document6 pagesSérie TD Distillation-Rectification 2020-2021Algerie Cyrus100% (3)
- TP ThermoDocument21 pagesTP Thermosamirwane100% (1)
- Série 4 Esrérification 2021Document6 pagesSérie 4 Esrérification 2021safouen mejbriPas encore d'évaluation
- Lois PhysiquesDocument1 pageLois PhysiquesMartin SossouPas encore d'évaluation
- Exercices 14 Suivi Temporel PDFDocument2 pagesExercices 14 Suivi Temporel PDFYassir Ksakass50% (2)
- 10 - DistillationDocument14 pages10 - DistillationEtienne jeoffreyPas encore d'évaluation
- Exercices de TDDocument4 pagesExercices de TDWeld Saf100% (1)
- Cours TD'E 1et2Document2 pagesCours TD'E 1et2brahimza61Pas encore d'évaluation
- TP N 1 CaloriemetrieDocument6 pagesTP N 1 Caloriemetrieمحده عبد الرحمان100% (1)
- Pdfjoiner 1Document16 pagesPdfjoiner 1Ray CharlesPas encore d'évaluation
- TP2 - TVS - Thermodynamique II - PR Lamrani Et DaoudiDocument10 pagesTP2 - TVS - Thermodynamique II - PR Lamrani Et DaoudiHafid El fdilPas encore d'évaluation
- Cinetique ExercicesDocument15 pagesCinetique ExercicesGajo MouandzaPas encore d'évaluation
- (TP23) EnonceDocument4 pages(TP23) EnonceAdam Ait FarsPas encore d'évaluation
- Document AP Mecanismes Reactionnels Correction Final 2Document7 pagesDocument AP Mecanismes Reactionnels Correction Final 2louloute2883Pas encore d'évaluation
- TDT7Document2 pagesTDT7ridhajamel100% (1)
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Catalogue Mural 2021 - Essid Céramique Fabricant de Carrelage en TunisieDocument43 pagesCatalogue Mural 2021 - Essid Céramique Fabricant de Carrelage en TunisieAnis SouissiPas encore d'évaluation
- Atlanta GroupDocument60 pagesAtlanta GroupAnis SouissiPas encore d'évaluation
- Notion:: Formes JuridiquesDocument2 pagesNotion:: Formes JuridiquesAnis SouissiPas encore d'évaluation
- Revit NomenclaturesDocument6 pagesRevit NomenclaturesAnis SouissiPas encore d'évaluation
- CatalogueDocument1 pageCatalogueAnis SouissiPas encore d'évaluation
- Telerupteur PDFDocument3 pagesTelerupteur PDFAnis Souissi100% (2)
- Telerupteur PDFDocument3 pagesTelerupteur PDFAnis Souissi100% (2)
- Pronopers1 091219144144 Phpapp01Document5 pagesPronopers1 091219144144 Phpapp01Anis SouissiPas encore d'évaluation
- Prepositions 110913135812 Phpapp01Document8 pagesPrepositions 110913135812 Phpapp01Anis SouissiPas encore d'évaluation
- Matlab PDFDocument2 pagesMatlab PDFAnis SouissiPas encore d'évaluation
- A3520 PDFDocument35 pagesA3520 PDFAnis SouissiPas encore d'évaluation
- A3522 PDFDocument26 pagesA3522 PDFAnis SouissiPas encore d'évaluation
- A3466 PDFDocument17 pagesA3466 PDFAnis SouissiPas encore d'évaluation
- Sequence 14-C4 Actions Permanentes Et VariablesDocument12 pagesSequence 14-C4 Actions Permanentes Et VariablesAnis SouissiPas encore d'évaluation
- Conduites - Forcées Principe, Aménagement Et SécuritéDocument19 pagesConduites - Forcées Principe, Aménagement Et SécuritéIMARPas encore d'évaluation
- Chpitre 7 Stabilité Des PentesDocument9 pagesChpitre 7 Stabilité Des PentesmohamedPas encore d'évaluation
- Géo AffineDocument99 pagesGéo AffineOladé Ange Sèïvè LokoPas encore d'évaluation
- Calcul de Alpha-CrDocument10 pagesCalcul de Alpha-CrmihaidelianPas encore d'évaluation
- Progression P1 2024 MathsDocument19 pagesProgression P1 2024 MathskittynoumeaPas encore d'évaluation
- I-Existence Et Unicité: 2 - ConvexitéDocument4 pagesI-Existence Et Unicité: 2 - ConvexitéAmin Zekri100% (1)
- Aky013 4 04Document50 pagesAky013 4 04ggmarcosPas encore d'évaluation
- Biogreen FicheProdETIA UPX FRIGOMIX 2013 03 en FR GLCDocument1 pageBiogreen FicheProdETIA UPX FRIGOMIX 2013 03 en FR GLCmartin carchanoPas encore d'évaluation
- 7744 Le Procede de Moulage en Coquille Par Gravite EnspsDocument9 pages7744 Le Procede de Moulage en Coquille Par Gravite Enspslyes100% (1)
- Brevet de Maths 2023 Sujet Pour Reviser Le Brevet en LigneDocument7 pagesBrevet de Maths 2023 Sujet Pour Reviser Le Brevet en Ligneghislaine dug.armèdePas encore d'évaluation
- Ecoul Charge PermDocument39 pagesEcoul Charge PermAhmed MallekhPas encore d'évaluation
- Page de GardememoireDocument126 pagesPage de GardememoireMusta GuessPas encore d'évaluation
- Mode CalculatricesDocument30 pagesMode CalculatricesBennouna RedaPas encore d'évaluation
- Rapport Abandon Scolaire Last 2004 PDFDocument69 pagesRapport Abandon Scolaire Last 2004 PDFAdil TahraouiPas encore d'évaluation
- GéomorphologieDocument13 pagesGéomorphologieLubna TamsPas encore d'évaluation
- 139 S - Moteur de Base PDFDocument21 pages139 S - Moteur de Base PDFHamza RezguiPas encore d'évaluation
- Mon Cours SupDocument875 pagesMon Cours SupamenzouPas encore d'évaluation
- Complex It eDocument28 pagesComplex It ebilalPas encore d'évaluation
- MDS CH-21Document24 pagesMDS CH-21AyoubPas encore d'évaluation
- ElectroctatiqueDocument35 pagesElectroctatiqueIssam LfPas encore d'évaluation
- L'Éclairage Dans Les ÉcolesDocument52 pagesL'Éclairage Dans Les Écolesأحمد أمين العلويPas encore d'évaluation
- Cours TenseursDocument7 pagesCours TenseursGhy PouiPas encore d'évaluation
- NC Reservoir 006Document21 pagesNC Reservoir 006Hamou MelloulPas encore d'évaluation
- Qu'est-Ce Que La Méditation ?Document21 pagesQu'est-Ce Que La Méditation ?Didier Salvignol100% (1)
- Mécanique Des Sols II PDFDocument120 pagesMécanique Des Sols II PDFLordPas encore d'évaluation
- Valeur AbsolueDocument5 pagesValeur AbsolueraftoupinPas encore d'évaluation
- DS 6 SupDocument2 pagesDS 6 SupSara MarouchePas encore d'évaluation
- Travaux PratiquesDocument8 pagesTravaux PratiquesOsvaldo DOMINGOSPas encore d'évaluation
- T5-6 FluidesDocument69 pagesT5-6 FluidesOumaimaPas encore d'évaluation
- Espaces VectorielsDocument18 pagesEspaces VectorielsAMEZIANE MOHAMEDPas encore d'évaluation