Académique Documents
Professionnel Documents
Culture Documents
Chim 03 TP 1
Transféré par
Mouhieddine KhailiTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Chim 03 TP 1
Transféré par
Mouhieddine KhailiDroits d'auteur :
Formats disponibles
ETUDE CINETIQUE D’UNE TRANSFORMATION
Objectif : Etudier la vitesse volumique de la réaction de l’eau oxygénée avec l’ion iodure.
A. Matériel et réactifs
solution aqueuse d’iodure de potassium (K+ + I- ) ,
de concentration c1 = 0,3 mol.L-1 ;
acide sulfurique,
de concentration c2 = 0,5 mol.L-1 ;
solution aqueuse de thiosulfate de sodium
(2Na+ + S2O32- ), de concentration c3 = 0,5 mol.L-1 ;
eau oxygénée (H2O2 ),
de concentration c4 = 0,25 mol.L-1 ;
empois d’amidon ou thiodène.
erlenmeyer, …
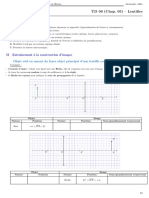
compléter le schéma en indiquant où sont les différentes
solutions , et en quelle quantité
B. Protocole expérimental
Dans un erlenmeyer, introduire 10,0 mL de la solution d’iodure de potassium prélevés à l’aide d’une pipette jaugée. A l’aide de la.
pipette graduée, ajoute 1 mL d’empois d’amidon dans la solution. Ajouter lentement, par petites quantités successives, 10 mL d’acide
sulfurique mesurés à l’éprouvette graduée.
ATTENTION ! L’acide sulfurique est à manipuler avec précaution : l’usage de lunettes et de gants est indispensable.
Remplir la burette graduée avec la solution de thiosulfate de sodium. Eliminer toute bulle d’air sous le robinet et ajuster le zéro. Placer
l’erlenmeyer sous la burette sur l’agitateur magnétique. Y verser 1,0 mL de thiosulfate de sodium et enclencher l’agitation
magnétique. Dans un bécher, introduire 10,0 mL d’eau oxygénée prélevés à l’aide d’une pipette jaugée. Verser rapidement le contenu
du bécher dans l’erlenmeyer et déclencher immédiatement le chronomètre (temps t 0 ). Attendre l’apparition de la teinte bleue dans la
solution pour la première fois et noter la date t 1 correspondante sans arrêter le chronomètre. Ajouter rapidement à nouveau 1,0 mL de
la solution de thiosulfate de sodium. Recommencer l’opération huit fois et compléter le tableau suivant.
C. Exploitation des résultats
1. Réaction entre l’eau oxygénée et l’ion iodure
L’eau oxygénée oxyde lentement l’ion iodure. Les demi-équations électroniques associées aux couples redox en présence sont
H2O2 / H2O :
I2 / I- :
Equation-bilan de la réaction étudiée :
réaction lente / rapide ?
2. Principe du dosage du diiode formé
à la date t = t0 = 0 s, on verse 1,0 mL de solution de thiosulfate de sodium dans le mélange réactionnel. L’ion thiosulfate réduit
instantanément le diiode qui se forme lors de la réaction entre l’eau oxygénée et l’ion iodure. Les demi-équations électroniques
associées aux couples redox en présence lors de cette réaction sont :
I2 / I- :
S4O62- / S2O32- :
Equation-bilan de la réaction de dosage :
réaction lente / rapide ?
3. Tableau descriptif de l’évolution du système chimique
Tableau d’avancement de la réaction étudiée
4. Quelques questions de réflexion
Donner la composition du mélange, en mmol, à t0 : n(I- ) = n (H2O2 ) = n (S2O32- ) =
Quels sont les 2 renseignements apportés par l’apparition de la teinte bleue ?
# #
Qu’arrive-t-il à l’eau oxygénée au cours de l’expérience ?
Qu’arrive-t-il aux ions iodure au cours de l’expérience ?
Qu’arrive-t-il au diiode au cours de l’expérience ?
Exprimer n (I2 ) dosé en fonction de n (S2O32- ) :
Puis n (I2 ) formé en fonction de x, d’après le tableau d’avancement de la réaction étudiée :
Au temps t1 , quelle quantité de diiode a été formée ?
Au temps t2 , quelle quantité totale de diiode aurait été formée ?
Quelle est la valeur de xmax ?
apparition
de la teinte 1ère fois 2ème fois
bleue
date t0 t1
(min, s) 0
n (I2 ) formé
0
(mmol)
avancement
x 0
(mmol)
C. Vitesse volumique de la réaction
Tracer la courbe représentant l’évolution de l’avancement au cours du temps x = f(t). S’aider du tableur en classe.
Calculer le volume réactionnel au début et à la fin de l’expérience. Peut-on le considérer constant ?
Déterminer la vitesse volumique de la réaction aux dates tA = min s et tB == min s.
Comment évolue cette vitesse au cours du temps ?
Déterminer le temps de demi-réaction.
Vous aimerez peut-être aussi
- Serie Avancement1Document2 pagesSerie Avancement1amine touatiPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- 02 TP Cinetique DosagesDocument3 pages02 TP Cinetique Dosagesssg100% (1)
- Série Révision Mars 23Document8 pagesSérie Révision Mars 23Ahmed Baba Mohameden HamdiPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- A. Etude Cinétique de La Transformation Des Ions Peroxodisulfate Et Des Ions IoduresDocument5 pagesA. Etude Cinétique de La Transformation Des Ions Peroxodisulfate Et Des Ions IoduresZahra Zahra50% (2)
- Chimie TP3 DosageDocument2 pagesChimie TP3 DosageKhadija KabatiPas encore d'évaluation
- Série N°3 Avec Correction Chimie Série Cinétique 2007 2008 (Tlili Touhami)Document14 pagesSérie N°3 Avec Correction Chimie Série Cinétique 2007 2008 (Tlili Touhami)Ltaief Chayma100% (2)
- TP5 SuivicinetiquepartitrageDocument2 pagesTP5 Suivicinetiquepartitragekabid1964Pas encore d'évaluation
- Série Cinétique Chimique 2bac: P T P T RDocument9 pagesSérie Cinétique Chimique 2bac: P T P T Rrkibi.khadija2006Pas encore d'évaluation
- TS-TP No4 - cinetique-H2O2 I2 Thios-EvalueDocument4 pagesTS-TP No4 - cinetique-H2O2 I2 Thios-EvalueMLAN Hesna100% (2)
- SerieDocument7 pagesSeriemehdi benmassoudPas encore d'évaluation
- C03 Cinetique ReactionDocument2 pagesC03 Cinetique ReactionmohPas encore d'évaluation
- Suivi CinetiqueDocument7 pagesSuivi CinetiqueMed BriniPas encore d'évaluation
- Correction Du TP - Suivi Temporel D'une Transformation Chimique Par ...Document3 pagesCorrection Du TP - Suivi Temporel D'une Transformation Chimique Par ...WaliD MerabeT0% (1)
- CH 1 ExostsDocument3 pagesCH 1 ExostsNajimou Alade Tidjani100% (1)
- Travaux Pratiques Cinétique: Faculté de Chimie Département de Génie Des MatériauxDocument4 pagesTravaux Pratiques Cinétique: Faculté de Chimie Département de Génie Des MatériauxmehalasmaaPas encore d'évaluation
- Éaction Ersulfate - Odure: F D G D MDocument14 pagesÉaction Ersulfate - Odure: F D G D Mlamis b-zPas encore d'évaluation
- TS2TDC42013Document4 pagesTS2TDC42013Najimou Alade TidjaniPas encore d'évaluation
- DM Chimie RevisionDocument2 pagesDM Chimie RevisionMolka HarbaouiPas encore d'évaluation
- Série Chimie Cinétique Chimique 2011 2012 (Dahmani Lotfi)Document4 pagesSérie Chimie Cinétique Chimique 2011 2012 (Dahmani Lotfi)Aicha DaouPas encore d'évaluation
- TP7 Cinétique Chimique Du Premier Ordre.Document14 pagesTP7 Cinétique Chimique Du Premier Ordre.Sellam Anis100% (1)
- Série D'exercices 1, Transformations Rapides Et Transformations Lentes, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDDocument1 pageSérie D'exercices 1, Transformations Rapides Et Transformations Lentes, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Chimievalution PDFDocument37 pagesChimievalution PDFAnis DahnenPas encore d'évaluation
- TP Chimie n1Document4 pagesTP Chimie n1Adel Laimeche100% (1)
- Serie C: Cinétique Chimie: 500 ML 2.10 500 ML 6.10 +2 H /H /I (H)Document4 pagesSerie C: Cinétique Chimie: 500 ML 2.10 500 ML 6.10 +2 H /H /I (H)Babacar NdiayePas encore d'évaluation
- DM 11 ChimieDocument4 pagesDM 11 ChimieMustapha BelmuftiPas encore d'évaluation
- DM Révisions 2006Document2 pagesDM Révisions 2006Daniela DinicaPas encore d'évaluation
- CinetiqueDocument9 pagesCinetiqueAnn OussPas encore d'évaluation
- Reaction Persulfate IodureDocument8 pagesReaction Persulfate Iodurelamis b-zPas encore d'évaluation
- Chimie TD 3 Cinétique ChimiqueDocument4 pagesChimie TD 3 Cinétique ChimiqueFranck Momo100% (1)
- Ob s1 Cinetique ChimiqueDocument2 pagesOb s1 Cinetique Chimiquemedabdellahisamba34Pas encore d'évaluation
- TP Cine TiqueDocument4 pagesTP Cine Tiquejaywalk100% (1)
- BIOF-Suivi Temporel D'une Transformation Et Vites 2018-ChajraouiDocument6 pagesBIOF-Suivi Temporel D'une Transformation Et Vites 2018-ChajraouiChajraouiAhmed50% (2)
- Série D'exercices 2, Suivi Temporel D'une Transformation Chimique - Vitesse de Réaction, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDDocument8 pagesSérie D'exercices 2, Suivi Temporel D'une Transformation Chimique - Vitesse de Réaction, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDMoulayMouly100% (6)
- PDF Ex7C1 Oxydation Des Ions Iodures Par Les Ions PeroxodisulfateDocument1 pagePDF Ex7C1 Oxydation Des Ions Iodures Par Les Ions PeroxodisulfateMohamedPas encore d'évaluation
- Vitesse 2Document5 pagesVitesse 2lemiaPas encore d'évaluation
- SUIVI TEMPOREL de L'avancementDocument2 pagesSUIVI TEMPOREL de L'avancementSahbi Mabrouki YamenPas encore d'évaluation
- Série D'exercices - Sciences Physiques Préparez Votre Baccalauréat Cinetique Chimique - Bac Sciences Exp (2013-2014) MR Sdiri Anis PDFDocument4 pagesSérie D'exercices - Sciences Physiques Préparez Votre Baccalauréat Cinetique Chimique - Bac Sciences Exp (2013-2014) MR Sdiri Anis PDFAzizElheniPas encore d'évaluation
- TSP2SP2Ch9T4-exos Resolus p245n11 246n15 250n25Document5 pagesTSP2SP2Ch9T4-exos Resolus p245n11 246n15 250n25mohPas encore d'évaluation
- Serie C1 PDFDocument4 pagesSerie C1 PDFMofid PC100% (3)
- Exercice 9 Suivi Temporel Dune Transformation ChimiqueDocument1 pageExercice 9 Suivi Temporel Dune Transformation ChimiqueCatuk Ella100% (2)
- Exercices 7 Suivi TemporelDocument1 pageExercices 7 Suivi Temporelكورة لايفPas encore d'évaluation
- tp7 (Chimie Dosage de 02)Document5 pagestp7 (Chimie Dosage de 02)Sabin SamPas encore d'évaluation
- Exos CH 04Document3 pagesExos CH 04lol testPas encore d'évaluation
- Cours Chimie 20102011 PDFDocument83 pagesCours Chimie 20102011 PDFالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Suivi Temporel D Une Transformation Chimique Vitesse de Reaction Activites 2Document1 pageSuivi Temporel D Une Transformation Chimique Vitesse de Reaction Activites 2lhoussine.bgPas encore d'évaluation
- SV Chim 2021 2 FRDocument7 pagesSV Chim 2021 2 FRanthony nehmePas encore d'évaluation
- TP Cinetique ChimiqueDocument3 pagesTP Cinetique ChimiqueNouara Amokrane100% (1)
- TP2 Cintique H2O2 06 07Document12 pagesTP2 Cintique H2O2 06 07Hoù Dà Mrt75% (4)
- 2003 Polynesie Sujet Exo2 Cinetique 2 5ptsDocument2 pages2003 Polynesie Sujet Exo2 Cinetique 2 5ptsAslan AntriPas encore d'évaluation
- C2Chim Suivi Cinetique ExercicesDocument8 pagesC2Chim Suivi Cinetique ExercicesMohamed El OuahdaniPas encore d'évaluation
- Chimie 4 SUIVI TEMPOREL D'UNE TRANSFORMATION CHIMIQUE PAR TITRAGEDocument1 pageChimie 4 SUIVI TEMPOREL D'UNE TRANSFORMATION CHIMIQUE PAR TITRAGELamsaaf MohamedPas encore d'évaluation
- TP CinetiqueDocument2 pagesTP Cinetiquefaiza77100% (1)
- Chap 01Document4 pagesChap 01touzalinePas encore d'évaluation
- Exercices 1 Suivi TemporelDocument2 pagesExercices 1 Suivi TemporelayoubbouuderqaPas encore d'évaluation
- Chimie-TP1 Facteurs CinetiquesDocument1 pageChimie-TP1 Facteurs CinetiquesChartier JulienPas encore d'évaluation
- TP2a Chimie Cinetique-ChimiqueDocument2 pagesTP2a Chimie Cinetique-ChimiquemohPas encore d'évaluation
- Exercice 1Document8 pagesExercice 1Mouhieddine KhailiPas encore d'évaluation
- DM03 Optique CompletDocument4 pagesDM03 Optique CompletMouhieddine KhailiPas encore d'évaluation
- Devoir Controle 1 - Physique - Lycée Pilote SfaxDocument3 pagesDevoir Controle 1 - Physique - Lycée Pilote SfaxMouhieddine Khaili100% (2)
- Etudiant: Frédéric Gaillard Professeur: Henning MüllerDocument114 pagesEtudiant: Frédéric Gaillard Professeur: Henning MüllerMouhieddine KhailiPas encore d'évaluation
- TD06 - Lentilles MincesDocument10 pagesTD06 - Lentilles MincesMouhieddine KhailiPas encore d'évaluation
- Determination A Sec Du Coefficient Micro-DevalDocument3 pagesDetermination A Sec Du Coefficient Micro-DevalL'acteur VictimePas encore d'évaluation
- 47K - Operating Manual - 10052472 - 09 - FRDocument39 pages47K - Operating Manual - 10052472 - 09 - FRAhmed HarratPas encore d'évaluation
- 10-Lesassemblages Par Éléments FiletésDocument9 pages10-Lesassemblages Par Éléments FiletésSegaAlainCoulibalyPas encore d'évaluation
- Fiche Métier - Employé de Station ServiceDocument11 pagesFiche Métier - Employé de Station ServiceCHEIKH ALIOU SOUANEPas encore d'évaluation
- Chapitre I: Formes Des Médicaments SolidesDocument22 pagesChapitre I: Formes Des Médicaments SolidesDjellal Zahariya mohammadPas encore d'évaluation
- Ec AntoineDocument28 pagesEc AntoineAlicia ZPas encore d'évaluation
- 3 MSPMChap 3Document26 pages3 MSPMChap 3soumia bouPas encore d'évaluation
- 17-Techniques de Biologie MoléculaireDocument76 pages17-Techniques de Biologie MoléculaireInsafPas encore d'évaluation
- Dosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)Document4 pagesDosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)theobromine100% (5)
- Règles FB (P92-701)Document71 pagesRègles FB (P92-701)Pan Panam100% (1)
- RAPPORT Final PDFDocument86 pagesRAPPORT Final PDFAnass El Kasmaoui100% (2)
- Catalogue Choix Vérins HydrauliquesDocument60 pagesCatalogue Choix Vérins HydrauliquesStephane Tchoriang100% (1)
- Revisions 2nd Atomes Et Molecules PDFDocument2 pagesRevisions 2nd Atomes Et Molecules PDFSaad MabchourPas encore d'évaluation
- Procédure de Réparation Par Demi-Coquilles NFTALDocument16 pagesProcédure de Réparation Par Demi-Coquilles NFTALTayyeb Ouis100% (1)
- LEVOTHYROX - Sommation Interpellative Extraits Sans Nom 02112017Document5 pagesLEVOTHYROX - Sommation Interpellative Extraits Sans Nom 02112017Christophe LèguevaquesPas encore d'évaluation
- GazochimieDocument9 pagesGazochimieHadjer zitPas encore d'évaluation
- Isolants ThermiquesDocument24 pagesIsolants Thermiquesmelisa kadiriPas encore d'évaluation
- Mémoire de PFEDocument67 pagesMémoire de PFEdjamalPas encore d'évaluation
- NotcompDocument37 pagesNotcompxxxPas encore d'évaluation
- STG C120Document14 pagesSTG C120bouabdallah laref100% (1)
- Solutions Ozone Eau Potable WedecoDocument8 pagesSolutions Ozone Eau Potable WedecoalainPas encore d'évaluation
- Pdf2star 1476439438 Manuscrit TH Se AG Sicaire FINALDocument227 pagesPdf2star 1476439438 Manuscrit TH Se AG Sicaire FINALHardy BONDAPas encore d'évaluation
- Element Standard Mecanique Information Technique PDF 842 Ko ESM LCAT1Document41 pagesElement Standard Mecanique Information Technique PDF 842 Ko ESM LCAT1razvan65Pas encore d'évaluation
- Version Tunnel Moteur Constructeur Conception Type PuissanceDocument24 pagesVersion Tunnel Moteur Constructeur Conception Type PuissanceLiebherr100% (8)
- Partie 6.2 - Coût de Fabrication PDFDocument17 pagesPartie 6.2 - Coût de Fabrication PDFamalPas encore d'évaluation
- UranuimDocument40 pagesUranuimOussama DhahriPas encore d'évaluation
- NF P 84-500 Géomombranes PDFDocument20 pagesNF P 84-500 Géomombranes PDFbastophePas encore d'évaluation
- Chapitre III ThermochimieDocument5 pagesChapitre III ThermochimieÀzïz LAPas encore d'évaluation
- CHIMIEDocument108 pagesCHIMIEdazePas encore d'évaluation
- ENAP CHLORIC CC Blanc F C Ref 218103901Document1 pageENAP CHLORIC CC Blanc F C Ref 218103901massiPas encore d'évaluation
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Conception & Modélisation CAO: Le guide ultime du débutantD'EverandConception & Modélisation CAO: Le guide ultime du débutantPas encore d'évaluation
- Semer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumeD'EverandSemer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumePas encore d'évaluation
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- L'Ombre à l'Univers: La structure des particules élémentaires XIIfD'EverandL'Ombre à l'Univers: La structure des particules élémentaires XIIfPas encore d'évaluation
- Histoire de la psychologie scientifique: De la naissance de la psychologie à la neuropsychologie et aux champs d'application les plus actuelsD'EverandHistoire de la psychologie scientifique: De la naissance de la psychologie à la neuropsychologie et aux champs d'application les plus actuelsPas encore d'évaluation
- Géologie de l'Amérique: Les Grands Articles d'UniversalisD'EverandGéologie de l'Amérique: Les Grands Articles d'UniversalisPas encore d'évaluation
- Jus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTD'EverandJus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTPas encore d'évaluation
- Enseigner une Langue Etrangère Par l’Apprentissage HybrideD'EverandEnseigner une Langue Etrangère Par l’Apprentissage HybridePas encore d'évaluation
- 500 secrets pour avoir un potager merveilleuxD'Everand500 secrets pour avoir un potager merveilleuxÉvaluation : 2 sur 5 étoiles2/5 (1)
- 160 ressources pour se lancer dans la vidéo quand on n’y connait rienD'Everand160 ressources pour se lancer dans la vidéo quand on n’y connait rienPas encore d'évaluation