Académique Documents
Professionnel Documents
Culture Documents
Capture D'écran . 2024-04-22 À 22.12.08
Capture D'écran . 2024-04-22 À 22.12.08
Transféré par
ksanetkibreab07Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Capture D'écran . 2024-04-22 À 22.12.08
Capture D'écran . 2024-04-22 À 22.12.08
Transféré par
ksanetkibreab07Droits d'auteur :
Formats disponibles
LE METABOLISME CELLULAIRE
Domaine professionnel santé 1ère année
Ecole de culture générale Biologie 2023
Domaine professionnel santé Le métabolisme 1ère année
Table des matières
1 Introduction ....................................................................................... 3
2 Utilisation des nutriments par les cellules ............................................... 4
3 Définitions .......................................................................................... 6
3.1 Métabolisme ................................................................................. 6
3.2 Anabolisme et catabolisme ............................................................. 6
4 Les enzymes....................................................................................... 7
4.1 Définitions .................................................................................... 7
4.2 Du gène à l'enzyme ....................................................................... 9
4.3 Les voies métaboliques ................................................................ 11
5 L’énergie .......................................................................................... 12
6 Métabolisme des nutriments contenant de l’énergie ............................... 13
6.1 La respiration cellulaire ................................................................ 15
6.1.1 Définition et équation bilan ..................................................... 15
6.2 L’ATP (adénosine triphosphate) ..................................................... 16
6.2.1 Structure et hydrolyse de l’ATP ............................................... 16
6.2.2 Utilisation de l’énergie libérée par l’hydrolyse de l’ATP ................ 18
6.2.3 Régénération de l’ATP ............................................................ 19
7 Travail pratique sur les réactions enzymatiques ..................................... 20
7.1 Réaction et principes de l’expérience .............................................. 21
7.2 Inhibiteurs enzymatiques ............................................................. 23
7.2.1 Pesticides ............................................................................. 23
7.2.2 Métaux toxiques .................................................................... 23
7.2.3 Médicaments inhibiteurs :....................................................... 23
7.2.4 Inhibiteurs de la dégradation de principes actifs ........................ 24
8 Sources ........................................................................................... 24
École de culture générale, 2023 2
Domaine professionnel santé Le métabolisme 1ère année
1 Introduction
La cellule est une usine chimique miniature où se produisent des milliers de
réactions dans un espace microscopique.
Les glucides associés à de l’azote peuvent être convertis en acides aminés qui se
lient pour former des protéines ; inversement, durant la digestion, les protéines
sont décomposées en acides aminés qui pourront à leur tour être convertis en
glucides. Les petites molécules se combinent pour former des polymères que la
cellule peut ensuite hydrolyser selon ses besoins.
Chez les organismes pluricellulaires, de nombreuses cellules exportent des
produits chimiques d’une partie de l’organisme vers d’autres parties. Le processus
chimique appelé respiration cellulaire assure le fonctionnement de la cellule en
utilisant l’énergie emmagasinée dans les monosaccharides et d’autres sources
d’énergie. La cellule se sert de cette énergie pour accomplir ses différentes
fonctions, comme le transport de solutés à travers la membrane plasmique.
Les réactions qui ont lieu dans une cellule sont coordonnées et régulées avec
précision. Par sa complexité, son efficacité, son intégration et sa sensibilité aux
moindres changements, la cellule présente une activité chimique sans égale.
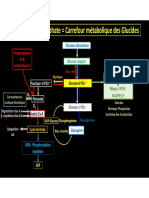
Carte métabolique
Glycogène
(n+1) Glycolyse Néoglucogenèse
Catabolisme des Anabolisme des Trans-énoyl-CoA
graisses (β-oxydation) graisses
D-Glucose Triglygéride
Glycogène (n) Glycogène (n) Cycle de Krebs Cycle de l’urée
Trans- / désamination Glycogénogenèse Acyl-CoA
des acides aminés et glycogénolyse
Corps cétoniques Fermentation lactique Acyl-CoA
Glucose-1- Utilisation des chaînes carbonées des acides aminés Acide gras β-hydroxyacyl-CoA
Glucose-6- phosphate (glucoformateurs, cétogènes, mixtes)
phosphate
Voie des pentoses phosphates
Voie des
pentoses
TRP
phosphates Lactate
β-cétoacyl-CoA
Glycérol CYS ALA
Fructose-6-
phosphate Glycérol-
phosphate THR GLY SER
Dihydroxyacétone- D-β-hydroxybutyrate
phosphate LEU / LYS
Acétoacétate
TRP / ILE
1,3-biphospho- 3-phospho- 2-phospho- Phosphoénol Pyruvate
Fructose-1,6- pyruvate LEU
biphosphate
glycérate glycérate glycérate TYR
Acétoacétyl-CoA
Glycéraldéhyde- Acétone
3-phosphate PHE
ASN ASP
Mitochondrie
Malonyl-ACP
Oxaloacétate Malonyl-CoA
α-cétoacide Acide aminé
Urée Pyruvate Acétyl-CoA
Glutamate α-cétoglutarate Acétyl-Malonyl-ACP
Malate Acétyl-ACP
Oxaloacétate
Ornithine Malate Citrate
Arginine
Butyryl-Malonyl-ACP
Butyryl-ACP
Fumarate Acyl-ACP
Fumarate Acétoacétyl-ACP
Isocitrate
Carbamoyl-
TYR
phosphate
PHE
GLU
Citrulline Succinate Crotonyl-ACP
α-cétoglutarate
Arginino- THR / MET
succinate Succinyl-CoA GLN / ARG
VAL / ILE β-hydroxybutyryl-ACP
Aspartate HIS / PRO
École de culture générale, 2023 3
Domaine professionnel santé Le métabolisme 1ère année
2 Utilisation des nutriments par les cellules
Objectifs d’apprentissage :
- Définir un nutriment et citer des exemples de nutriments
- Expliquer les différentes possibilités d’utilisation des nutriments par une
cellule
Une fois à l'intérieur des cellules de l'organisme, les nutriments passent par une
gamme extraordinaire de réactions biochimiques qui, ensemble, forment ce qu'on
appelle le métabolisme (metabolê : changement). Au cours du métabolisme, des
substances sont continuellement élaborées et dégradées. Les cellules consomment
de l'énergie pour pouvoir extraire des nutriments une plus grande quantité
d'énergie, puis elles utilisent cette énergie pour subvenir à leurs besoins. Même au
repos, l'organisme dépense beaucoup d'énergie.
Pour rappel, un nutriment est une petite molécule qui est directement assimilable
par nos cellules. Certains nutriments sont issus de la digestion de molécules plus
grandes alors que d’autres pas (ex. vitamines, eau, sels minéraux). Ils
appartiennent tous à une des six catégories de molécules citées ci-dessous.
Les nutriments appartiennent à des catégories de molécules organiques ou
inorganiques (minérales) qui constitue la nourriture :
Molécules organiques Molécules inorganiques
- Les glucides dont les nutriments principaux sont
- L’eau
le glucose, fructose et galactose, ribose et xylose
- Les lipides dont les nutriments sont le glycérol et
les acides gras, ainsi que les stéroïdes comme le - Les sels minéraux
cholestérol
- Les protéines dont les nutriments sont les acides
aminés
- Les vitamines
École de culture générale, 2023 4
Domaine professionnel santé Le métabolisme 1ère année
Les nutriments, en provenance de notre alimentation, sont utilisés pour construire
et faire fonctionner notre organisme. Ils remplissent trois grands rôles :
1) Energie : la dégradation des nutriments permet la production et la mise en
réserve d’énergie (ex : graisses, glycogène)
2) Structure : les nutriments peuvent être utilisés pour construire des structures
cellulaires (ex : actine/myosine, phospholipides, calcium)
3) Fonction : ils permettent de fabriquer des molécules ayant rôle fonctionnel
(ex : enzyme, hormone, anticorps) dans le but de réguler le métabolisme
cellulaire et nos processus physiologiques.
École de culture générale, 2023 5
Domaine professionnel santé Le métabolisme 1ère année
3 Définitions
Objectifs d’apprentissage :
- Définir le métabolisme et son rôle ;
- Citer et décrire les deux voies du métabolisme (catabolisme et
anabolisme) ;
- Donner des exemples pour illustrer ces deux voies.
3.1 Métabolisme
Le terme métabolisme correspond à l’ensemble des réactions chimiques qui
se déroulent à l'intérieur des cellules.
Le rôle du métabolisme consiste à gérer les ressources énergétiques et
matérielles de la cellule.
3.2 Anabolisme et catabolisme
Le métabolisme présente deux aspects :
a) L’anabolisme : ensemble des réactions permettant la synthèse de
molécules complexes à partir de molécules plus simples. Les voies
anaboliques consomment de l’énergie. On parle alors de réaction
endothermique.
Ex : synthèse d’une protéine à partir d’acides aminés.
b) Le catabolisme : ensemble des réactions permettant la décomposition des
grosses molécules en plus petites, susceptibles d’être éliminées. Les voies
cataboliques libèrent de l’énergie. On parle alors de réaction exothermique.
Ex : dégradation d’une molécule de graisse en glycérol et acides gras.
Ex : lors de la respiration cellulaire, le glucose est décomposé en dioxyde de
carbone et en eau.
L'énergie libérée par les réactions cataboliques peut être emmagasinée, puis servir
aux réactions anaboliques.
École de culture générale, 2023 6
Domaine professionnel santé Le métabolisme 1ère année
4 Les enzymes
Objectifs d’apprentissage :
- Définir une enzyme ;
- Citer deux exemples d’enzymes ainsi que la réaction catalysée par ces
enzymes ;
- Expliquer la spécifié enzyme-substrat et l’importance du site actif dans cette
spécificité ;
- Expliquer le lien gène-enzyme ;
- Expliquer ce qu’est une voie métabolique ;
- Expliquer l’importance des enzymes dans une voie métabolique. Expliquer
les conséquences en cas de déficit d’un gène.
4.1 Définitions
Les enzymes sont des protéines qui servent de catalyseurs biologiques. Elles
sont capables, à faible dose, d’accélérer considérablement les réactions du
métabolisme, sans y participer vraiment ; on les retrouve intactes, à la fin de la
réaction.
L’organisme humain compte environ 75'000 sortes d’enzymes différentes.
Le réactif sur lequel une enzyme agit s’appelle substrat. L’enzyme se lie à son
substrat (ou à ses substrats, lorsqu’il y a deux ou plusieurs réactifs). Pendant que
les deux sont réunis, l’action catalytique de l’enzyme convertit le substrat en
produit(s) de la réaction :
Enzyme
Substrat(s) Produit(s)
Par exemple, l’enzyme appelée saccharase (la plupart des noms d’enzymes se
terminent par –ase) scinde le saccharose (disaccharide) en ses deux
monosaccharides, le glucose et le fructose :
Saccharase
Saccharose Glucose Fructose
École de culture générale, 2023 7
Domaine professionnel santé Le métabolisme 1ère année
Une enzyme peut reconnaître son substrat même parmi des composés très
apparentés, de sorte que chaque enzyme catalyse une réaction spécifique. Par
exemple, la saccharase n’agit que sur le saccharose : elle ignore les autres
disaccharides, comme le maltose.
Cette spécificité enzyme-substrat est possible grâce à la forme
tridimensionnelle unique de chaque enzyme. En fait, seule une petite partie
de la molécule d’enzyme se lie au substrat. Cette partie, appelée site actif, forme
habituellement une poche ou un sillon à la surface de la protéine. La spécificité
d’une enzyme réside dans le fait que la forme de son site actif correspond
exactement à la forme de son substrat. Cependant, le site actif n’est pas un
réceptacle rigide dans lequel le substrat s’emboîte. Lorsque celui-ci y entre, il
provoque une légère modification structurale de l’enzyme. Le site actif épouse
encore mieux le contour du substrat.
L’image ci-dessous montre l’ajustement induit entre une enzyme et son substrat.
Dans une réaction enzymatique, le substrat se lie au site actif de l’enzyme pour
former un complexe enzyme-substrat. Une fois la transformation du substrat
en produit terminée, le produit quitte le site actif. Ce dernier est donc libre
d’accepter une autre molécule de substrat. Le cycle entier se produit tellement vite
qu’une seule molécule d’enzyme transforme habituellement un millier de
molécules de substrat par seconde.
La plupart des réactions métaboliques étant réversibles, une enzyme peut
catalyser les réactions directe et inverse. La réaction qui prédomine dépend surtout
des concentrations des réactifs et des produits.
École de culture générale, 2023 8
Domaine professionnel santé Le métabolisme 1ère année
La figure ci-dessous illustre le site actif et le cycle catalytique d’une enzyme. Une
enzyme peut convertir une ou plusieurs molécules de réactifs en une ou plusieurs
molécules de produits. L'enzyme illustrée ici transforme deux molécules de
substrat en deux molécules de produits.
4.2 Du gène à l'enzyme
Il existe deux types de protéine : structurale et fonctionnelle : les enzymes sont
des protéines fonctionnelles.
Les protéines sont fabriquées par les ribosomes selon les informations contenues
dans les gènes (contenus dans l’ADN), par l’intermédiaire de l’ARN messager. On
dit que les gènes « codent pour » des protéines.
Les figures ci-dessous illustrent l’expression génétique dans une cellule eucaryote.
École de culture générale, 2023 9
Domaine professionnel santé Le métabolisme 1ère année
L’expression génétique :
ADN -> ARN -> protéine
Dans une cellule eucaryote,
l'ADN nucléaire programme la
production de protéines en
dictant la synthèse de l'ARN
messager (ARNm).
L’expression génétique :
Les cellules utilisent l'information codée
dans un gène pour synthétiser une
protéine fonctionnelle.
École de culture générale, 2023 10
Domaine professionnel santé Le métabolisme 1ère année
4.3 Les voies métaboliques
Nous pouvons imaginer le métabolisme d’une cellule comme une carte routière
complexe montrant les voies suivies par des milliers de réactions qui se produisent
dans la cellule, formant un vaste réseau de voies métaboliques.
Une voie métabolique est une séquence d’étapes au cours desquelles une même
molécule subit des modifications jusqu’à l’obtention d’un produit donné.
Chaque étape de la voie spécifique est catalysée par une enzyme spécifique :
Gène 1 Gène 2 Gène 3
code pour…
La figure ci-dessous illustre les premières étapes de la glycolyse (les enzymes sont
indiqués en bleu) :
Lors de gène défectueux (voire absent) l’enzyme correspondante manque ou
dysfonctionne, ce qui provoque l’absence du produit final et l’accumulation d’un
sous-produit. Cette accumulation peut être toxique pour la cellule et péjorer le bon
fonctionnement de la cellule (ex : phénylcétonurie).
Gène :
Phenylanaline hydrolase
Enzyme :
Phenylanaline hydrolase
phenylalanine tyrosine dégradation…
École de culture générale, 2023 11
Domaine professionnel santé Le métabolisme 1ère année
5 L’énergie
Objectifs d’apprentissage :
- Citer et expliquer les deux mécanismes par lesquels les organismes vivants
obtiennent leurs composés organiques.
- Donner des exemples de composés organiques (nutriments issus des
glucides, lipides et protéines) ;
- Citer les règnes qui utilisent ces deux mécanismes.
L’énergie est la capacité de causer un changement. Elle existe
sous différentes formes et la vie dépend de la capacité des
cellules à la transformer d’un type en un autre.
L’énergie n’a pas de masse. Elle n'est pas faite de matière.
L’énergie existe sous différentes formes. Ses manifestations
les plus évidentes sont : la chaleur, la lumière, l'électricité,
l'énergie cinétique (liée au mouvement) ou encore l’énergie
potentielle. L'énergie potentielle est une forme d'énergie que
la matière possède en raison de sa position ou de sa structure.
Les biologistes appellent énergie chimique l'énergie
potentielle qui peut être libérée au cours d'une réaction
chimique.
" Selon le premier principe de la thermodynamique : « L’énergie ne peut être ni
créée, ni détruite, mais elle peut être transférée d’un objet à un autre ou être
transformée d’une forme en une autre forme. » (Loi de conservation de
l’énergie).
L’énergie n’est donc pas recyclable. La même quantité d’énergie a toujours
existé et existera toujours dans notre Univers de sa création à sa disparition.
" Selon le deuxième principe de la thermodynamique : « On ne peut pas
complètement transformer une forme d’énergie en une autre. ». En effet, lors
d’une transformation, une partie de l’énergie se dissipe en général sous forme
de chaleur et n’est pas utilisée.
Les cellules dépensent continuellement de l’énergie sous les formes les plus
variées : chaleur, mouvement, transport, croissance, reproduction, ….
École de culture générale, 2023 12
Domaine professionnel santé Le métabolisme 1ère année
Pour assurer leur métabolisme, les organismes vivants doivent donc trouver une
source d’énergie dans leur milieu ambiant. La nourriture (contenant de l’énergie
chimique), plus particulièrement les composés organiques, constitue cette
source.
Il existe deux mécanismes par lesquels les organismes vivants obtiennent ces
composés organiques :
1) L’autotrophie : les organismes autotrophes fabriquent eux-mêmes leurs
propres composés organiques grâce à une réaction chimique appelée
photosynthèse. Ce sont les Végétaux, les Algues et certains autres
Protistes, ainsi que certaines Bactéries. On les appelle les producteurs.
Grâce à l’énergie fournie par le soleil, ces organismes sont capables de
synthétiser des composés organiques (glucose) à partir de réactifs
inorganiques (gaz carbonique et eau).
2) L’hétérotrophie : les organismes hétérotrophes doivent trouver des
composés organiques déjà existants. Ces sont les Animaux, les Mycètes,
certains Protistes et la plupart des Bactéries. On les appelle les
consommateurs.
6 Métabolisme des nutriments contenant de l’énergie
Objectifs d’apprentissage :
- Définir en quelques mots la respiration cellulaire ;
- Écrire l’équation chimique de la respiration cellulaire ;
- Expliquer le lien entre respiration cellulaire et synthèse d’ATP ;
- Décrire la structure de l’ATP et expliquer ce qui se passe lorsqu’une cellule
exige de l’énergie ;
- Expliquer la production, l’utilisation et la régénération de l’ATP
Les nutriments contenant de l’énergie sont représentés par 3 catégories : les
glucides, les lipides et les protéines.
La transformation dans l'organisme de ces nutriments passe par 3 étapes
principales comme l'illustre la figure 24.3 (les flèches en bleu représentent des
réactions cataboliques et les flèches en violet représentent des réactions
anaboliques).
École de culture générale, 2023 13
Domaine professionnel santé Le métabolisme 1ère année
L'étape 1 est la digestion qui a lieu dans le type digestif. Le sang apporte les
nutriments absorbés aux cellules des tissus.
L'étape 2 a lieu dans les cellules des tissus. Les nutriments récemment absorbés
sont soit utilisés pour synthétiser des lipides, des protéines ou du glycogène par
des voies anaboliques, soit dégradés par des voies cataboliques dans le cytoplasme
des cellules. L'une des principales voies cataboliques de l'étape 2 est la glycolyse.
L'étape 3, qui se déroule dans les mitochondries, est presque entièrement
catabolique. Elle nécessite de l'oxygène et correspond à la fin de la dégradation
des nutriments ; elle produit de grandes quantités d'ATP mais aussi du dioxyde de
carbone et de l'eau. Le cycle de Krebs est une des voies principales de l'étape 3,
tout comme la phosphorylation oxydative.
Trois étapes du métabolisme des nutriments contenant de l'énergie :
La respiration cellulaire comprend la glycolyse de l'étape 2 et toutes les phases
de l'étape 3 (cycle de Krebs et phosphorylation oxydative) : sa principale fonction
est de produire de l'ATP (molécule dont les liaisons sont riches en énergie).
École de culture générale, 2023 14
Domaine professionnel santé Le métabolisme 1ère année
6.1 La respiration cellulaire
6.1.1 Définition et équation bilan
La respiration cellulaire est le processus lors duquel des composés
organiques (riches en énergie) sont oxydés par le dioxygène libérant
l’énergie nécessaire à la synthèse de l’adénosine triphosphate (ATP).
L’ATP représente le pilier de l’énergie cellulaire. Cette molécule contient deux
liaisons phosphate à haute teneur en énergie (énergie potentielle chimique).
Les mitochondries sont le site principal de la respiration cellulaire.
Équation chimique de la respiration cellulaire :
C6H12O6 + 6 O2 6 CO2 + 6 H2O
Energie
ADP + P ATP
Cette équation signifie que 1 molécule de glucose réagit avec 6 molécules de
dioxygène en formant 6 molécules de dioxyde de carbone et 6 molécules d’eau.
Cette réaction chimique libère l’énergie nécessaire pour faire réagir plusieurs
molécules d’ADP avec plusieurs molécules de phosphate inorganique (P) pour
former des molécules d’ATP.
L’oxydation du glucose est une réaction qui libère de l’énergie (réaction
exothermique) alors que la synthèse d’ATP est une réaction qui nécessite de
l’énergie (réaction endothermique).
Il est important de noter que cette équation est une version simplifiée de la réalité.
En effet, diverses étapes ont lieu entre l’oxydation du glucose et la synthèse d’ATP.
La respiration cellulaire est divisée en 3 grandes étapes :
1. La glycolyse
2. Le cycle de Krebs (ou cycle de l’acide citrique)
3. La phosphorylation oxydative
Chacune de ces étapes permet la formation d’ATP mais le meilleur rendement en
ATP et obtenu lorsque toutes les réactions ont eu lieu.
École de culture générale, 2023 15
Domaine professionnel santé Le métabolisme 1ère année
Aperçu de la respiration cellulaire et rendement en ATP de chaque molécule de
glucose oxydée :
2 ATP 2 ATP 26 à 28 ATP
6.2 L’ATP (adénosine triphosphate)
6.2.1 Structure et hydrolyse de l’ATP
L’ATP, adénosine triphosphate, est
composée d’une molécule organique
appelée adénosine attachée à une
chaîne de trois groupements
phosphate.
C’est une molécule qui contient deux liaisons phosphate à haute teneur en énergie
(énergie potentielle chimique). Les liaisons entre les groupements phosphate de
l’ATP peuvent être rompus par hydrolyse (réaction chimique dans laquelle une
liaison est rompue par action d'une molécule d'eau).
Lorsque la cellule exige de l’énergie, une molécule d’eau brise la liaison du
phosphate terminal libérant ainsi l’énergie contenue dans cette liaison. Les
produits de cette hydrolyse sont une molécule de phosphate inorganique (Pi) et de
l’ADP. L’image ci-dessous illustre la réaction.
École de culture générale, 2023 16
Domaine professionnel santé Le métabolisme 1ère année
Hydrolyse de l’ATP :
L’hydrolyse de l’ATP produit de l’ADP, un phosphate inorganique et de l’énergie.
Structure de l’ATP :
L’adénosine est formée d’une molécule d’adénine (molécule organique) ainsi que
d’une molécule de ribose (glucide).
École de culture générale, 2023 17
Domaine professionnel santé Le métabolisme 1ère année
6.2.2 Utilisation de l’énergie libérée par l’hydrolyse de l’ATP
Les protéines de la cellule utilisent l'énergie dégagée durant l'hydrolyse de l'ATP
de plusieurs manières pour accomplir trois types de travail cellulaire : le travail
chimique, le travail de transport et le travail mécanique.
Exemple de travail chimique le couplage de l'énergie au moyen de l'hydrolyse de
l'ATP :
Exemple de travail de transport (a) et de travail mécanique (b) : l'hydrolyse
de l'ATP modifie la forme et les affinités de liaison des protéines :
École de culture générale, 2023 18
Domaine professionnel santé Le métabolisme 1ère année
6.2.3 Régénération de l’ATP
Dans les cellules, l'énergie dégagée par les réactions de dégradation
(catabolisme) sert à la régénération de l'ATP.
L'énergie chimique emmagasinée dans l'ATP assure la majeure partie du travail
cellulaire.
Énergie
Énergie destinée au
provenant du travail
catabolisme cellulaire
École de culture générale, 2023 19
Domaine professionnel santé Le métabolisme 1ère année
7 Travail pratique sur les réactions enzymatiques
Objectifs d’apprentissage :
- Interpréter les résultats du TP sur les réactions enzymatiques
- Définir un inhibiteur enzymatique ;
- Citer les quatre sortes d’inhibiteurs enzymatiques vus dans le cours et
expliquer leurs effets.
Les enzymes sont des molécules, plus précisément des protéines particulières, qui
jouent le rôle de catalyseurs des réactions biochimiques. Les enzymes ne sont donc
pas vivantes. Une seule molécule d’enzyme peut catalyser des milliards de
milliards de fois la même réaction. Les organismes n’ont donc besoin d’enzymes
qu’à des concentrations très faibles. Ils les synthétisent eux-mêmes.
Les enzymes permettent de réaliser les réactions du métabolisme :
• À la température des êtres vivants
En synthèse organique et sans catalyseurs, les mêmes réactions
nécessiteraient des températures nettement plus élevées que certaines
molécules ne pourraient pas supporter.
• Plus rapidement
A titre d’exemple, in vitro, sans enzyme, l’hydrolyse du saccharose (sucre)
dans l’eau nécessite une année, alors qu’in vivo avec enzyme, la même
réaction ne dure que quelques secondes.
• De manière sélective
Une enzyme sélective permet d’effectuer une réaction particulière avec une
substance particulière. Ainsi, la maltase scinde une molécule de maltose en
produisant deux molécules de glucose, mais elle est incapable de scinder une
molécule de lactose, alors que la lactase peut le faire.
Exemples d’enzymes
" Chez les bactéries : enzymes de nombreuses bactéries qui permettent la
décomposition et le recyclage de la matière organique, p. ex. dans le cycle du
carbone ou celui de l’azote.
École de culture générale, 2023 20
Domaine professionnel santé Le métabolisme 1ère année
" Chez les végétaux : l’amidon-synthétase catalyse la synthèse de l’amidon par
condensation de molécules de glucose.
" Chez les animaux (humain inclus) : l’amylase, contenue dans la salive et le
pancréas, catalyse sélectivement la fragmentation de l’amidon en molécules
de glucose. Les protéases sont des enzymes qui, comme la pepsine, catalysent
la fragmentation des protéines en acides aminés lors de la digestion.
7.1 Réaction et principes de l’expérience
L’urée (formule chimique ci-dessous) est un déchet de dégradation des protéines.
L’urine contient environ 2 % d’urée. L’urée peut réagir avec l’eau en se
transformant en NH3 et CO2, selon l’équation chimique ci-dessous (à équilibrer) :
… CH4N2O + … H2 O → … NH3 + … CO2
Un indicateur est un réactif qui indique la présence d’une substance en changeant
de couleur. L’indicateur que nous utiliserons dans cette expérience est incolore,
mais s’il est mis en présence de NH3, il réagit avec ce dernier en formant une
substance rouge. Si on veut savoir s’il y a NH3, il suffit donc d’y ajouter cet
indicateur. Si la solution reste incolore, il n’y a pas de NH3. Si elle vire au rouge, il
y a du NH3.
1. Introduire env. 2 ml de solution d’urée
dans un tube à essai. Ajouter 1 goutte
d’indicateur.
" Observations et conclusions :
École de culture générale, 2023 21
Domaine professionnel santé Le métabolisme 1ère année
2. Ajouter env. 2 ml de suspension d’uréase
(enzyme) à la solution de l’essai
précédent. Constatation ?
" Observations et conclusions :
3. Introduire env. 2 ml de suspension
d’uréase dans un tube à essai, chauffer à
ébullition sur un bec Bunsen, puis
refroidir à température ambiante.
Ajouter env. 2 ml de solution d’urée et 1
goutte d’indicateur. Observer.
" Observations et conclusions :
4. Introduire env. 2 ml de suspension
d’uréase dans un tube à essai, ajouter 5
gouttes de solution de plomb, puis env. 2
ml de solution d’urée et 1 goutte
d’indicateur. Observer.
" Observations et conclusions :
École de culture générale, 2023 22
Domaine professionnel santé Le métabolisme 1ère année
7.2 Inhibiteurs enzymatiques
Un inhibiteur enzymatique est une substance qui, en se liant à une enzyme, en
diminue ou en annule l'activité.
7.2.1 Pesticides
De nombreux pesticides provoquent la mort des organismes (plantes,
insectes, etc.) en inhibant les enzymes indispensables à des réactions
vitales de leur métabolisme. C’est ainsi qu’agit le glyphosate
(herbicide Roundup ®), l’un des herbicides les plus controversés que
l’Union Européenne était sur le point d’interdire en 2018 parce qu’il est
vraisemblablement cancérigène. Les pesticides sont en grande partie responsables
de la forte régression de la biodiversité. Plus de ¾ des insectes et 40 % des oiseaux
ont disparu de Suisse au cours des 30 dernières années.
7.2.2 Métaux toxiques
Un grand nombre de composés de métaux lourds (avec un
numéro atomique élevé, p. ex. plomb et mercure), sont
toxiques. Même en concentrations très faibles, ils inhibent les
enzymes du métabolisme des êtres vivants. Parmi les sources
de ces métaux, on peut citer les piles et batteries, les
peintures murales (sels de Pb), les plombs de chasse, l’émail
de certaines poteries, etc.
Radiographie d’un genou
ayant accumulé du plomb
Le saturnisme désigne une intoxication par le plomb. caractéristique du saturnisme
7.2.3 Médicaments inhibiteurs :
Des inhibiteurs peuvent être utilisés à des fins
thérapeutiques pour empêcher les réactions chimiques
catalysées par des enzymes qui permettent aux bactéries
ou aux virus de se multiplier. En voici deux exemples :
Les antibiotiques de la famille des pénicillines (comme
l’amoxicilline) agissent en inhibant les enzymes de
bactéries pathogènes. Ils perturbent ainsi le
Le champignon Penicilium excrète de
métabolisme des bactéries et les empêchent de se la péniciline et crée ainsi une zone qui
inhibe la croissance bactérienne.
multiplier.
École de culture générale, 2023 23
Domaine professionnel santé Le métabolisme 1ère année
L’AZT est un médicament de synthèse utilisée dans les trithérapies contre le SIDA.
C’est un inhibiteur d’une enzyme utilisée par le virus du SIDA.
7.2.4 Inhibiteurs de la dégradation de principes actifs
Le pamplemousse contient des substances qui
inhibent une enzyme qui joue un rôle important
dans la transformation de principes actifs de
médicaments en vue faciliter leur élimination par
l’urine. Si l’enzyme est inhibée, les principes actifs
ne sont plus dégradés et peuvent s’accumuler dans
l’organisme, ce qui peut provoquer des troubles graves. Il faut donc éviter de
consommer des médicaments et du pamplemousse ou au moins se renseigner sur
leur compatibilité.
8 Sources
- Marieb E & Hoehn K. (2019). Anatomie et physiologie humaines. Pearson.
- Campbell N. A. (2012). Biologie. Pearson.
École de culture générale, 2023 24
Vous aimerez peut-être aussi
- TD 3 EnzymesDocument5 pagesTD 3 EnzymesLucinéPas encore d'évaluation
- Metabolismes Des Glucides PDFDocument151 pagesMetabolismes Des Glucides PDFMa RyPas encore d'évaluation
- METABOLISME LIPIDIQUE DFGSP-2 ERdeMDocument10 pagesMETABOLISME LIPIDIQUE DFGSP-2 ERdeMsikaokoumassouPas encore d'évaluation
- Métabolisme Des Glucides DR - Khebbat Zerargui F.Document68 pagesMétabolisme Des Glucides DR - Khebbat Zerargui F.oumnia mairechePas encore d'évaluation
- Le Cycle de KrebsDocument19 pagesLe Cycle de KrebsLandry RimbaybarPas encore d'évaluation
- Glucides, métabolisme أيض السكريات QCM.pdf1Document6 pagesGlucides, métabolisme أيض السكريات QCM.pdf1Santos AmedjokpoPas encore d'évaluation
- Cours Bioch Métab Version CP 2 Agro IAV Partie 2Document135 pagesCours Bioch Métab Version CP 2 Agro IAV Partie 2Your fav Aya100% (1)
- Métabolisme Des GlucidesDocument58 pagesMétabolisme Des GlucidesHäsnã HäsnãPas encore d'évaluation
- Métabolisme Des GlucidesDocument63 pagesMétabolisme Des GlucidesKdimosaure KdimoPas encore d'évaluation
- C. Biochimie III. Lipides (III.1. Métabolisme Des Acides Gras)Document41 pagesC. Biochimie III. Lipides (III.1. Métabolisme Des Acides Gras)Rania HamdiPas encore d'évaluation
- Synthèse Des Acides Gras Et TriglycéridesDocument6 pagesSynthèse Des Acides Gras Et TriglycéridesJohns AtsacwounPas encore d'évaluation
- Metabolisme Energetique Et Regulationm1baDocument65 pagesMetabolisme Energetique Et Regulationm1baŽdn ÂśšiaPas encore d'évaluation
- CrebDocument19 pagesCrebevenPas encore d'évaluation
- Correction ED Métabolisme Des Lipides 2020 2021 1Document32 pagesCorrection ED Métabolisme Des Lipides 2020 2021 1Belkis SioudPas encore d'évaluation
- Cycle de Krebs Ou de L Acide CitriqueDocument13 pagesCycle de Krebs Ou de L Acide CitriqueJean-Loïc BauchetPas encore d'évaluation
- Vue Générale Du Métabolisme Des GlucidesDocument18 pagesVue Générale Du Métabolisme Des GlucidesKargamel PeyoPas encore d'évaluation
- Métabolisme Des LipidesDocument17 pagesMétabolisme Des LipidesMei Wan100% (1)
- Cours3-Métabolisme Des Glucides PDFDocument112 pagesCours3-Métabolisme Des Glucides PDFELALLAM YOUSSEF100% (1)
- 1 - Catabolisme Lipides Et AG - PolyDocument12 pages1 - Catabolisme Lipides Et AG - PolyRuth BUKAKAPas encore d'évaluation
- Cours - 5 Regulation - Du - Metabolisme - Des - LipidesDocument8 pagesCours - 5 Regulation - Du - Metabolisme - Des - Lipidesmiss anthropocenePas encore d'évaluation
- Planches 4 - Cours Microbio Industr S6 2022Document10 pagesPlanches 4 - Cours Microbio Industr S6 2022bahaaelbrouzy200100% (1)
- Cours 5Document14 pagesCours 5Saida AdjemiPas encore d'évaluation
- Synth&Degrad AcidesGrasDocument19 pagesSynth&Degrad AcidesGrashanaabekkalbrikciPas encore d'évaluation
- Biochimie-Metabolisme Acides GrasDocument47 pagesBiochimie-Metabolisme Acides GrasPaul FatheadPas encore d'évaluation
- Metabolisme Des LipidesDocument97 pagesMetabolisme Des LipidesFikra PapPas encore d'évaluation
- PR El Maataoui Synthese AgDocument47 pagesPR El Maataoui Synthese AgGhaid MahmoudiPas encore d'évaluation
- Automatisation en BiochimieDocument6 pagesAutomatisation en BiochimiePaul fatheadPas encore d'évaluation
- Metabolisme LipidesDocument49 pagesMetabolisme LipidespartiraretirapasPas encore d'évaluation
- 1 4 Metabolisme Des Lipides PDFDocument22 pages1 4 Metabolisme Des Lipides PDFAya Bouchareb100% (1)
- Biochimie Microbienne 1Document45 pagesBiochimie Microbienne 1페 리알Pas encore d'évaluation
- CoursBiopchimie PDFDocument14 pagesCoursBiopchimie PDFLILIA HAMROUNIPas encore d'évaluation
- Cours Biotech TAACQ2021-1Document95 pagesCours Biotech TAACQ2021-1SiremPas encore d'évaluation
- Lecon 8 Renouvellement PermanentDocument7 pagesLecon 8 Renouvellement PermanentAmveladylanPas encore d'évaluation
- Biochimie Métabolique IIDocument50 pagesBiochimie Métabolique IIKhatar MedPas encore d'évaluation
- DM N°3 SujetDocument10 pagesDM N°3 SujetnaimPas encore d'évaluation
- 21.bioch2an27 Cycle KrebsDocument11 pages21.bioch2an27 Cycle KrebsYousra INDIAPas encore d'évaluation
- 001 - Cours NéoglucogenèseDocument13 pages001 - Cours NéoglucogenèseBlueskyindanPas encore d'évaluation
- Ag Meta .Document47 pagesAg Meta .Nouhaila darkPas encore d'évaluation
- UE7 Annales LipidesDocument3 pagesUE7 Annales LipidesElmaPas encore d'évaluation
- Cahier Galien Clermont BiochimieDocument17 pagesCahier Galien Clermont Biochimieun.profil.test.du.07Pas encore d'évaluation
- 5 Metabolisme 2011-12 PDFDocument19 pages5 Metabolisme 2011-12 PDFsadqiPas encore d'évaluation
- Le Métabolisme Anaérobie LactiqueDocument11 pagesLe Métabolisme Anaérobie LactiquedesshydroPas encore d'évaluation
- CHAP7 MET DES LIPIDES 1 Métabolisme Des Acides Gras 2022 2023 PLUSDocument9 pagesCHAP7 MET DES LIPIDES 1 Métabolisme Des Acides Gras 2022 2023 PLUSdianaPas encore d'évaluation
- Microbioligie S6Document159 pagesMicrobioligie S6abdelmajid.moumouhPas encore d'évaluation
- Cycle de Krebs 2020 2021.BENSAADDocument8 pagesCycle de Krebs 2020 2021.BENSAADdelphinemeviPas encore d'évaluation
- Cycle de CORI - 2022Document17 pagesCycle de CORI - 2022Feryal BhPas encore d'évaluation
- 10 - PR Bouhsain Synthese AGDocument28 pages10 - PR Bouhsain Synthese AGcopie masterPas encore d'évaluation
- La LactatemieDocument20 pagesLa LactatemieDø LLÿPas encore d'évaluation
- 3.métabolisme Des Acides GrasDocument11 pages3.métabolisme Des Acides Graschams.stars666Pas encore d'évaluation
- CH3.Lipogénèse PFDocument25 pagesCH3.Lipogénèse PFkhammar hichemPas encore d'évaluation
- Métabolisme Des GlucidesDocument28 pagesMétabolisme Des GlucidesilaPas encore d'évaluation
- 13.mtabolisme Des Acides Gras.Document41 pages13.mtabolisme Des Acides Gras.paul destinPas encore d'évaluation
- Cahier D'exercice5Document22 pagesCahier D'exercice5GHERMI .M100% (5)
- Cycle de Krebs - Biochimie 2023 ?? ?? ?Document10 pagesCycle de Krebs - Biochimie 2023 ?? ?? ?kviykavianePas encore d'évaluation
- Régulation de L'activité de La LipaseDocument19 pagesRégulation de L'activité de La LipaseBarthélemy Bawar Dit WarbiPas encore d'évaluation
- Exercices Lipides Bloc3 - 3Document8 pagesExercices Lipides Bloc3 - 3Ahmed ChaoukiPas encore d'évaluation
- Cahier Dexercices de Biochimie 5 MetabolismeDocument15 pagesCahier Dexercices de Biochimie 5 Metabolismeيحيى بورغدةPas encore d'évaluation
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- Présentation 1Document7 pagesPrésentation 1ፚᎧᏒᎧ GamerPas encore d'évaluation
- Comportement Des Métaux À Grande Vitesse de Déformation - ModélisationDocument10 pagesComportement Des Métaux À Grande Vitesse de Déformation - ModélisationSamagassi SouleymanePas encore d'évaluation
- Chapitre 1Document6 pagesChapitre 1MohamedBenKacemPas encore d'évaluation
- Cours de Thermodynamique Appliquée 1 - 2Document21 pagesCours de Thermodynamique Appliquée 1 - 2Na WelPas encore d'évaluation
- Forum Sur Cialis and Cialis Pour Le Trouble BipolaireDocument3 pagesForum Sur Cialis and Cialis Pour Le Trouble BipolairedraldovanPas encore d'évaluation
- ThèseDocument126 pagesThèseIlam ZazadaPas encore d'évaluation
- Qualité Des Sols PDFDocument28 pagesQualité Des Sols PDFSisPas encore d'évaluation
- CORRECTUM - Exo Chimie Du SolideDocument8 pagesCORRECTUM - Exo Chimie Du SolideLenz Daniel Jean PaulPas encore d'évaluation
- Cours2 - Acides Et Bases 1Document40 pagesCours2 - Acides Et Bases 1BONNEHPas encore d'évaluation
- Brochure Technique - Chaudieres A VapeurDocument28 pagesBrochure Technique - Chaudieres A VapeurNicole LiPas encore d'évaluation
- Naghraoui - MebarkaDocument82 pagesNaghraoui - MebarkaTahani GouaouPas encore d'évaluation
- Poteau D'incendie A120-A125Document4 pagesPoteau D'incendie A120-A125YOUDBIB Youssef100% (1)
- 2 - Corrigé TD Chapitre 3 AllostérieDocument3 pages2 - Corrigé TD Chapitre 3 AllostérieChaka TraorePas encore d'évaluation
- Etude Des Propriétés Physico-Chimiques de La SiliceDocument61 pagesEtude Des Propriétés Physico-Chimiques de La SiliceSamora danelle NdassiPas encore d'évaluation
- PETROCHIMIEDocument32 pagesPETROCHIMIEGhislain BarakaPas encore d'évaluation
- Alimentation Des Porcs PDFDocument40 pagesAlimentation Des Porcs PDFDelma sam100% (1)
- Palmier A Huile en AfriqueDocument70 pagesPalmier A Huile en AfriqueAlpha Dodi Diallo100% (1)
- Cours Biomolecules Biotech 2019Document145 pagesCours Biomolecules Biotech 2019Kouamé Emiliano Emmanuel N'ZOPas encore d'évaluation
- Composes Organiques OxygenesDocument3 pagesComposes Organiques OxygenesHedi Ben MohamedPas encore d'évaluation
- A085f2 PDFDocument2 pagesA085f2 PDFchakrounePas encore d'évaluation
- Haifa Aloui - Rapport ModifiéDocument26 pagesHaifa Aloui - Rapport Modifiématador_seifPas encore d'évaluation
- Mary HHDocument135 pagesMary HHMariam ZouhairPas encore d'évaluation
- ClimatisationDocument88 pagesClimatisationLhou KhalidPas encore d'évaluation
- PCD Chimie DS2Document2 pagesPCD Chimie DS2nerislapaix812Pas encore d'évaluation
- Homologation Des Indices Des Salaires Et Des Matières - 3ème Trimestre 2011 - Secteur BTPHDocument8 pagesHomologation Des Indices Des Salaires Et Des Matières - 3ème Trimestre 2011 - Secteur BTPHertbhmcentralbetonPas encore d'évaluation
- If Eaux en BouteilleDocument3 pagesIf Eaux en Bouteilleboniface69Pas encore d'évaluation
- Ecoulement A Travers Un Oriffice85Document5 pagesEcoulement A Travers Un Oriffice85Maamar Boukhalkhal90% (21)
- Sds n7330 FRANCEDocument11 pagesSds n7330 FRANCEtimbulPas encore d'évaluation
- SructuresDocument2 pagesSructuresfatimazahra kheraziPas encore d'évaluation
- Exercices Sur Les AlcoolsDocument2 pagesExercices Sur Les AlcoolsMohamed BambaPas encore d'évaluation