Académique Documents
Professionnel Documents
Culture Documents
C5Chim - Reactions - Acidobasiques - Exercices - Bronsted-Lowry PDF
Transféré par
Abdeljalil LoudainiTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
C5Chim - Reactions - Acidobasiques - Exercices - Bronsted-Lowry PDF
Transféré par
Abdeljalil LoudainiDroits d'auteur :
Formats disponibles
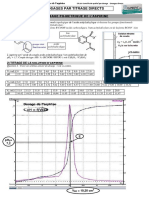
Chimie Chapitre 5 : Ractions acido-basiques en solution aqueuse
Terminale S
P.L. Arsonval Page 1 sur 4
Chap 5 : Transformations associes des ractions
acido-basiques en solution aqueuse Exercices
Exercice n2 p159
chercher sans calculatrice
1. La solution de pHA = 3,0 est la solution contenant la concentration en ion oxonium la plus leve. Cest donc la
solution contenant la concentration en ion hydroxyde la plus faible : [HOaq
]A = 1,0.1011 mol.L1.
La solution de pHC = 3,4 contient quant elle, une concentration lgrement plus leve en ion hydroxyde car son pH
est lgrement plus grand : [HOaq]C = 2,5.1011 mol.L1.
La solution de pHD = 7,6 contient quant elle, une concentration nettement plus leve en ion hydroxyde car son pH
est lgrement nettement grand : [HOaq
]D = 4,0.107 mol.L1.
La solution de pHB = 8,0 contient pour sa part, la plus grande concentration en ion hydroxyde car son pH est le plus
grand : [HOaq]B = 1,0.106 mol.L1.
2. [HOaq]E = 1,0.102 mol.L1, donc pHE = 12,0
[HOaq]F = 5,0.102 mol.L1, donc pHF = 12,7
[HOaq]G = 5,0.103 mol.L1, donc pHG = 11,7
Exercice n5 p159
1. CH3CHOHCO2H(aq) + H2O(l) = CH3CHOHCOaq + H3Oaq
[HOaq]f.V [HOaq]f
xf
2. La valeur de est donne : par dfinition =
=
=
. Ainsi [H3Oaq
]f = .C
xmax
C.V
C
A.N. : [H3Oaq
]f = 0,1475,0.103 = 7,4.104 mol.L1.
Par consquent : Daprs lquation de la raction chimique et la loi conservation de matire :
[CH3CHOHCOaq]f = [H3Oaq]f = 7,4.104 mol.L1.
C = [CH3CHOHCO2H(aq)]f + [CH3CHOHCOaq]f, donc [CH3CHOHCO2H(aq)]f = C [CH3CHOHCOaq]f
A.N. : [CH3CHOHCO2H(aq)]f = 5,0.103 7,4.104 = 4,3.103 mol.L1.
[CHCHOHCOaq
]q.[HOaq]q (7,4.104)2
3. Par dfinition : KA =
=
= 1,3.104.
4,3.103
[CHCHOHCOHaq]q.
De plus, par dfinition, pKA = log KA, ainsi pKA = 3,9 pour le couple acide lactique, ion lactate.
Exercice n8 p159
1. C6H5CO2H(aq) + H2O(l) = C6H5COaq + H3Oaq et pKA1 = 4,2 : valeur intermdiaire : pH = pHC = 3,3
2. HNO2(aq) + H2O(l) = HNOaq
+ H3Oaq et pKA2 = 3,3 : valeur la plus faible : cest le plus acide : pH = pHB = 2,9.
3. NHaq
+ H2O(l) = NH3(aq) + H3Oaq et pKA3 = 9,2 : valeur la plus leve : cest le moins acide : pH = pHA = 5,8.
Exercice n12 p160
1. Ion ammonium : NHaq
; acide actique (acide thanoque) : CH3COOH ; ion fluorure : F et acide nitreux : HNO2(aq).
2. La solution tant aqueuse , le solvant est leau, et en raison de la raction dautoprotolyse, la solution contient
ncessairement des ions oxonium H3Oaq et hydroxyde HOaq.
Les couples mis en jeu sont : H3Oaq / H2O(l) (pKA = 0) et H2O(l) / HOaq (pKA = 14).
3. Faute de place, le schma suivant nest pas lchelle
Augmentation de la force de lacide ( concentration identique)
H3O+
0 H2O
HF
3,17 F
HNO2
CH3COOH
3,30NO2
4,75CH3COO
NH
9,20NH3
H2O
14 HO
pKA
Augmentation de la force de la base ( concentration identique)
4. Entre pH = 3,17 et pH = 3,30, les 4 espces (entoures) sont les espces prdominantes de leur couple
Terminale S
Chimie Chapitre 5 : Ractions acido-basiques en solution aqueuse
P.L. Arsonval Page 2 sur 4
5. pH = 4,2, lespce du couple NHaq
/NH3 qui prdomine est NHaq.
pH = 4,2, lespce du couple CH3COOH/CH3COO qui prdomine est CH3COOH.
pH = 4,2, lespce du couple HF/F qui prdomine est F.
pH = 4,2, lespce du couple HNO2(aq)/NO2 qui prdomine est NO2.
Exercice n14 p160
1. Le graphe correspondant la forme acide est le graphe rouge (pour les faibles pH : 100 % despce).
Le graphe correspondant la forme basique est le graphe vert (pour les forts pH : 100 % despce).
2. Le pKA du bleu de bromophnol est gal 4,1 (valeur du pH lorsque [HInd] = [Ind]).
3. Pour pH = 2, la forme acide prdomine, et la forme basique est ngligeable : lindicateur color est jaune.
Pour pH = 10, la forme basique prdomine, et la forme acide est ngligeable : lindicateur color est bleue violace.
[Ind]
[Ind]
4. Nous savons (ou nous pouvons redmontrer) que pH = pKA + log
. Par consquent : log
= pH pKA.
[HInd]
[HInd]
[Ind]
Et par suite :
= 10pH pKA = 103,5 4,1 = 100,6 = 0,25. Ainsi [Ind]q = 0,25.[HInd]q.
[HInd]
C
Or [HInd]q + [Ind]q = C et par suite [HInd]q + 0,25.[HInd]q = C. Donc 1,25.[HInd]q = C : [HInd]q =
1,25
A.N. : [HInd]q = 15 mmol.L1 et [Ind]q = 5,0 mmol.L1.
Exercice n16 p161
1. Nous savons (ou nous pouvons redmontrer rapidement) que pH = pKA + log
Ainsi log
A.N. :
2.
3.
4.
[HPO2
aq ]
.
[H2POaq]
[H2POaq
]
[H2POaq
]
=
pK
pH
log
=
pK
pH
= 10pKA pH.
A
A
2
2
[H2POaq]
[HPOaq]
[HPOaq]
[HPO2
aq ]
[H2POaq
]
= 106,82 7,4 = 100,6 = 0,25.
2
[HPOaq
]
1
[H2PO aq] = 0,25.[HPO2
aq] = 0,250,257 = 69 mmol.L .
C3H6O3(aq) + HPO2
aq = C3H5O3 (aq) + H2POaq
La raction est totale : [H2POaq] = 0,035 + 0,069 = 0,104 mol.L1. Ainsi [HPO2
aq] =
2
[HPOaq]
,
Ainsi pH = pKA + log
= 6,82 + log
= 7,18 soit de lordre de pH = 7,2
,
[H2POaq]
0,275 0,035 = 0,240 mol.L1.
Exercice n17 p161
1. Zone de virage du bleu de bromothymol : [6,0 7,6]
Zone de virage de la phnolphtaline : [8,2 10]
Le pH de la solution dilue deau de Javel est donc compris entre 7,6 et 8,2 !
[ClOaq
]
[ClOaq
]
2. pH = pKA + log
Ainsi : log
= pH pKA
[HClO(aq)]
[HClO(aq)]
puisque 7,6 < pH < 8,2 alors
7,6 7,5 < pH pKA < 8,2 7,5
[ClOaq
]
100,1 <
< 100,7
[HClO(aq)]
[ClOaq
]
1,3 <
< 5,0
[HClO(aq)]
Exercice n18 p161
1. CH3CO2H(aq) + H2O(l) = CH3COaq + H3Oaq
[HOaq]f.V
xf
2. par dfinition =
, ainsi pour cette raction =
, donc [CH3COaq]f = [H3Oaq]f = .C0
xmax
C0.V
3. Par consquent daprs la conservation de la matire : [CH3COaq
]f + [CH3CO2H(aq)]f = C0.
Ainsi : .C0 + [CH3CO2H(aq)]f = C0 et donc [CH3CO2H(aq)]f = C0(1 )
[CHCOaq
]f.[HOaq]f
.C
.C
4. KA =
=
=
[CHCOHaq]f
C
5.
Terminale S
Chimie Chapitre 5 : Ractions acido-basiques en solution aqueuse
P.L. Arsonval Page 3 sur 4
C0 (mol.L1)
1,0.102
5,0.103
1,0.103
5,0.104
4,0.102
5,6.102
12,5.102
16.102
100
200
1000
2000
C
1,7.103
3,3.103
18.103
30.103
6. Les points sont quasiment aligns : la courbe modlisant ce nuage de points est une droite passant par lorigine.
K
7.
= A. Ainsi KA est la pente de la droite trace prcdemment : KA = 1,5.105 (valeur obtenue par rgression
C
linaire).
Exercice n20 p162
1. La zone de virage de lhlianthine est : (rouge) [3,4 4,4] (jaune)
La zone de virage du vert de bromocrsol est : (jaune) [3,8 5,4] (bleu)
La coloration jaune, en prsence dhlianthine indique que le pH est suprieur 4,4.
La coloration verte, en prsence de vert de bromocrsol indique que le pH est infrieur 5,4 (mais suprieur 3,8).
On peut donc en dduire que le pH de la solution est compris entre 4,4 et 5,4.
2. La zone de virage du rouge de mthyle est : (rouge) [4,2 6,2] (jaune). La coloration, en prsence de rouge de mthyle
de la solution serait donc une superposition de la teinte rouge de la forme acide de lindicateur et de la teinte jaune de
la forme basique : la solution prcdente prendrait alors une teinte orange.
3. a. Par dfinition, [H3Oaq] = 10pH, par consquent : 105,4 mol.L1 < [H3Oaq
] < 104,4 mol.L1
soit 4,0.106 mol.L1 < [H3Oaq] < 4,0.105 mol.L1
Ainsi : soit 4,0.106 mol.L1 < [A] < 4,0.105 mol.L1
et [AH] = C [A] donc :
3
1
8,0.10 mol.L < [AH] < 8,0.103 mol.L1 donc [AH] = 8,0.103 mol.L1
[HOaq].[A] [HOaq
]
b. KA =
=
: 2,0.109 < KA < 2,0.107 et donc 6,7 < pKA < 8,7
[AH]
[AH]
4. Le pKA du couple acide propanoque / ion propanoate est pKA = 4,87 : le flacon ne contient pas dacide propanoque.
Le pKA du couple acide hypochloreux / ion hypochlorite est pKA = 7,30 : le flacon peut contenir de lacide
hypochloreux.
Le pKA du couple phnol / ion phnolate est pKA = 10,0 : le flacon ne contient pas de phnol.
Le flacon contient donc de lacide hypochloreux !
Exercice n21 p162
I. tude thorique
1. a. HA(aq) + H2O(l) = Aaq
+ H3Oaq
b.
quation de la raction
HA(aq)
H2O(l)
Aaq
H3Oaq
tat du systme
avancement
n(HA(aq))
n(H2O(l))
n(Aaq
)
n(H3Oaq)
tat initial
CV
solvant
tat intermdiaire
CV x
solvant
tat final
(quilibre)
xq
CV xq
solvant
xq
xq
xq
= [H3Oaq]q. Daprs lquation de la raction : [Aaq]q = [H3Oaq
]q
V
Daprs la conservation de la matire : [HA(aq)]q = C [H3Oaq]q
c. xq = n(H3Oaq
)q. Par consquent
Ainsi Qr,q =
[HOaq
]q.[Aaq]q
[HAaq]q
[HOaq]q
C [HOaq
]q
2. Par dfinition : = (Aaq).[Aaq
]q + (H3Oaq).[H3Oaq]q = Aaq HOaq .[H3Oaq
]q
car
[Aaq]q
[H3Oaq]q
Terminale S
Chimie Chapitre 5 : Ractions acido-basiques en solution aqueuse
P.L. Arsonval Page 4 sur 4
II. tude exprimentale
1. La solution mre doit tre dilue 10 fois pour obtenir la solution fille. Si lon dispose dune fiole jauge de 100 mL, on
prlvera 10,0 mL de solution avec une pipette jauge de 10,0 mL. On introduit les 10,0 mL dans la fiole jauge, puis
on ajoute de leau distille, jusquau trait de jauge, en deux tapes. Pour finir on homognise la solution en retournant
la fiole jauge 3 ou 4 fois.
,.
3
2. a. Daprs la relation tablie en I.2. : [H3Oaq]q =
=
= 1,86 mol.m =
,. ,.
A HO
1,86.103 mol.L1. Donc Qr,q =
[HOaq
]q
C [HOaq]q
aq
aq
1,1.103, puis log Qr,q = 2,96.
b. concentration gale lacide salicylique est plus dissoci que lacide benzoque
c. Le pKA de lacide salicylique est donc plus faible que celui de lacide benzoque car cest un acide plus fort. En
effet Qr,q tant assimile la constante dacidit log Qr,q est identique pKA. On vrifie bien que la valeur est
plus faible !
Exercice n22 p163
I. Leau de Javel
1. La solution tant 12 chloromtrique, cela signifie quelle est capable de librer 12 L de dichlore gazeux. Sachant
quune mole de gaz occupe, dans les conditions de temprature et de pression considres, 22,4 L, Nous pouvons en
V
dduire que la solution peut librer n =
= 0,54 mol de dichlore gazeux. Or daprs lquation de la raction o le
Vm
dichlore apparat, cela correspond la mme quantit de matire dion hypochlorite. La concentration de la solution en
ion hypochlorite est donc C1 = 0,54 mol.L1.
,
2. On souhaite diluer la solution
= 8,1 fois.
,.
Pour obtenir un litre de solution il faut donc prlever : = 123 mL de solution J1.
,
On vrifie bien que
= 1,5 chloromtrique.
,
3. Lacide conjugu de lion hypochlorite est lacide hypochloreux de formule : HClO.
[HOaq].[ClOaq]
Lexpression de la constante dquilibre KA1 est : KA1 =
.
[HClOaq]
[ClOaq]
[ClOaq
]
4. pH = pKA1 + log
. Ainsi
= 10pHpKA1 = 10pH.10pKA1 = 10pH.KA1 = 1010,93,2.108 = 2,5.103
[HClO(aq)]
[HClO(aq)]
II. Proprit de la liqueur de Dakin
1. La raction acido-basique susceptible de se produire est : HCOaq + HOaq = CO2
aq + H2O(l)
Calculons la constante dquilibre de la raction associe lquation prcdente :
2
[CO2
[COaq
]q.[HOaq]q
KA PKA
aq ]q.
pKA2 ( pKe)
K=
=
=
=
= 10pKe pKA2
pKe = 10
e
[HCOaq]q.[HOaq]q
[HCOaq]
[HOaq]q.[HOaq]
A.N. : K = 1014 10,3 = 103,7 = 5,0.103. La constante dquilibre leve, montre que cette raction peut effectivement
avoir lieu de faon quasi-totale (hors considration cintique).
2. Calcul effectue la question prcdente pour valuer le caractre quantitatif de cette raction.
[ClOaq]
3. Comme montr en 1.4.
= 10pHpKA1 = 10pH.KA1 = 109,43,2.108 = 80 !
[HClO(aq)]
4. Leau de Javel J 2 et leau de Dakin possdent la mme concentration molaire apporte en acide hypochloreux (1,5
chloromtrique). Dans une eau de Dakin, le pH tant plus faible la concentration de lacide hypochloreux est plus
leve que dans une eau de Javel J2. Or lacide est 100 fois plus efficace que sa base conjugue pour son activit
bactricide et virucide. On a donc intrt utiliser leau de Dakin !
Vous aimerez peut-être aussi
- TD Réactions Acido-Basiques: L Mol HCO CDocument3 pagesTD Réactions Acido-Basiques: L Mol HCO ChassouiooPas encore d'évaluation
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - Monobaseel hazbi fadilaPas encore d'évaluation
- NFC15-106 Cabos Terra em PTsDocument17 pagesNFC15-106 Cabos Terra em PTsNuno RodriguesPas encore d'évaluation
- Compte Rendu de BiochimieDocument4 pagesCompte Rendu de Biochimiesafemind75% (16)
- Cours Désignation Des Éléments FiletésDocument17 pagesCours Désignation Des Éléments Filetésntayoub100% (4)
- C5Chim - Reactions - Acidobasiques - Exercices - Bronsted-Lowry PDFDocument4 pagesC5Chim - Reactions - Acidobasiques - Exercices - Bronsted-Lowry PDFAzizElheniPas encore d'évaluation
- Présentation Cours N°6Document13 pagesPrésentation Cours N°6inessPas encore d'évaluation
- Chapitre-5-Les Transformations Liées Par Des Réactions Acido-Basique - DosageDocument13 pagesChapitre-5-Les Transformations Liées Par Des Réactions Acido-Basique - Dosagea houssPas encore d'évaluation
- Transformations Associés A Des Reactions Acido Basiques en Solution AqueusesDocument8 pagesTransformations Associés A Des Reactions Acido Basiques en Solution AqueusesJosé Ahanda NguiniPas encore d'évaluation
- Exo TDDocument8 pagesExo TDBassirou YacoubaPas encore d'évaluation
- Correction TD2 - Calculs de PH (Exos 4,5,6,7,8) V2Document9 pagesCorrection TD2 - Calculs de PH (Exos 4,5,6,7,8) V2Amir NadeauPas encore d'évaluation
- Chapitre 5 PH Des Solutions AqueusesDocument16 pagesChapitre 5 PH Des Solutions AqueusesSyryne DridiPas encore d'évaluation
- C4 Correction Exercices AciditeDocument5 pagesC4 Correction Exercices AciditeAndrés Tobías Mba MICHA ALENEPas encore d'évaluation
- SA-Exos - 1 - 1112 Acido Basique ExocorrigéDocument12 pagesSA-Exos - 1 - 1112 Acido Basique ExocorrigéLarbii BadrourPas encore d'évaluation
- TAT équilibre acido-basiqueDocument17 pagesTAT équilibre acido-basiquedrakox.fortnitePas encore d'évaluation
- Abdelali AhDocument33 pagesAbdelali Ahcerveaumental80Pas encore d'évaluation
- Chap5-Comportement Des Acides Et Des Bases en Solution - CopieDocument3 pagesChap5-Comportement Des Acides Et Des Bases en Solution - CopieMillanTorresPas encore d'évaluation
- C3Chim - Transformations - Limitees - Exercices - Sabatier PDFDocument5 pagesC3Chim - Transformations - Limitees - Exercices - Sabatier PDFAzizElheni0% (1)
- 2004 09 Polynesie Spe Correction TA TACDocument2 pages2004 09 Polynesie Spe Correction TA TACRekkab MohamedPas encore d'évaluation
- Faculté Pluridisciplinaire de Nador SVIDocument4 pagesFaculté Pluridisciplinaire de Nador SVIZakaria AsbaiPas encore d'évaluation
- Série Dexercices Corrigés N°2Document7 pagesSérie Dexercices Corrigés N°2chada100% (1)
- Chapitre 3: Transformations Chimiques S'effectuant Dans LesDocument6 pagesChapitre 3: Transformations Chimiques S'effectuant Dans LesFATIMA fatiiiPas encore d'évaluation
- Les Solutions Aqueuses IoniquesDocument18 pagesLes Solutions Aqueuses IoniquesMétatron GamesPas encore d'évaluation
- Traveaux Dirigés 2Document6 pagesTraveaux Dirigés 2Aymen BaccouchePas encore d'évaluation
- Chim SolDocument4 pagesChim SolÆm Inē100% (2)
- Chimie 2 PDFDocument8 pagesChimie 2 PDFTarik Mlilas50% (2)
- Cours de Chimie: Niveau: Terminale SDocument14 pagesCours de Chimie: Niveau: Terminale SmedPas encore d'évaluation
- Chapitre 3: Transformations Chimiques S'effectuant Dans Les Deux SensDocument6 pagesChapitre 3: Transformations Chimiques S'effectuant Dans Les Deux SensDounia Larhouasli MarrakchiPas encore d'évaluation
- TSP2SP1Ch18T11-TP10 Corrige Destop AspirineDocument5 pagesTSP2SP1Ch18T11-TP10 Corrige Destop AspirineAyoub AinanePas encore d'évaluation
- Correction - TD 6 Acide BaseDocument8 pagesCorrection - TD 6 Acide BaseBILLBOARD TOP AFRICAPas encore d'évaluation
- Exos CH 06Document2 pagesExos CH 06lol testPas encore d'évaluation
- Force Des Acides Et BasesDocument4 pagesForce Des Acides Et Basestjmhfkdkd5Pas encore d'évaluation
- Corrigé de La Série N°2 - Équilibres Acido-BasiquesDocument7 pagesCorrigé de La Série N°2 - Équilibres Acido-Basiqueskim namjoon100% (1)
- Corrigé Série 2Document7 pagesCorrigé Série 2Doudou SamiPas encore d'évaluation
- Bac Blanc (Chimie) GSFADocument3 pagesBac Blanc (Chimie) GSFAahmed amilPas encore d'évaluation
- ILEPHYSIQUE Chimie Terminale Reactions Acido BasiquesDocument4 pagesILEPHYSIQUE Chimie Terminale Reactions Acido BasiquessarahPas encore d'évaluation
- Chimie: - Chimie en Solution AqueuseDocument35 pagesChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- FTSCresume Acide BaseDocument3 pagesFTSCresume Acide BaseWerfelli YassinePas encore d'évaluation
- 2 - Les Acides Et Les BasesDocument21 pages2 - Les Acides Et Les BasesAmine CompanPas encore d'évaluation
- Corrigé Série 1Document5 pagesCorrigé Série 1Mohamed ECHAMAI100% (2)
- Cours Chimie IIDocument37 pagesCours Chimie IINesrine Kaddouri100% (1)
- TD 5Document2 pagesTD 5Serena SouaibyPas encore d'évaluation
- Exercices Et Problèmes de ConcoursDocument12 pagesExercices Et Problèmes de ConcoursSa LimPas encore d'évaluation
- Cg2 Acides Bases AlbourineDocument17 pagesCg2 Acides Bases AlbourineAyoub Elfarwah100% (1)
- Fichier Produit 2232Document48 pagesFichier Produit 2232FlorinaPas encore d'évaluation
- Serie 7 8 Acides Faibles Bases Faibles Solutions TamponsDocument10 pagesSerie 7 8 Acides Faibles Bases Faibles Solutions TamponsBrahim DahaiPas encore d'évaluation
- Chap 5 Equilibres Acidobasiques Et PhmetrieDocument5 pagesChap 5 Equilibres Acidobasiques Et PhmetrieAlidou KOHOUMPas encore d'évaluation
- I. PH D Une Solution AqueuseDocument5 pagesI. PH D Une Solution AqueuseJean-Loïc BauchetPas encore d'évaluation
- E.C4 - Réaction acide base et de précipitationDocument4 pagesE.C4 - Réaction acide base et de précipitationnoamassin78Pas encore d'évaluation
- Correction Des Exercices Du Chapitre 7: Exercice N° 12 P 143Document2 pagesCorrection Des Exercices Du Chapitre 7: Exercice N° 12 P 143aaraychePas encore d'évaluation
- Chemical Engineering LabDocument15 pagesChemical Engineering LabOmairPas encore d'évaluation
- CHP 2 TD - Chimie - SolutionDocument8 pagesCHP 2 TD - Chimie - SolutionSimplice Assemien100% (2)
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseLOUkmen Bel100% (1)
- TP 3 Acide Base PDFDocument8 pagesTP 3 Acide Base PDFadsvgnmPas encore d'évaluation
- Compte Rendu Ph-MètrieDocument8 pagesCompte Rendu Ph-MètrieIKRAM BOULAJOUL50% (2)
- Ch13 Reaction Chimique Echange ProtonDocument5 pagesCh13 Reaction Chimique Echange Protonالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Transformations Acide - Base Eleve NDocument2 pagesTransformations Acide - Base Eleve Nblack HPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- Devoir 1 1bac SC - Exp FRDocument1 pageDevoir 1 1bac SC - Exp FRAbdeljalil LoudainiPas encore d'évaluation
- So CorrigeDocument30 pagesSo CorrigeAbdeljalil LoudainiPas encore d'évaluation
- Memoire - PDF Mecanisme JTDocument103 pagesMemoire - PDF Mecanisme JTAbdeljalil LoudainiPas encore d'évaluation
- Devoir5 CorrectionDocument1 pageDevoir5 CorrectionAbdeljalil LoudainiPas encore d'évaluation
- Formulaire Dérogation PDFDocument2 pagesFormulaire Dérogation PDFAbdeljalil LoudainiPas encore d'évaluation
- Chapitre 9 Réaction DDocument13 pagesChapitre 9 Réaction DAbdeljalil LoudainiPas encore d'évaluation
- Devoir Maths 1bac SX International FR s1 3Document1 pageDevoir Maths 1bac SX International FR s1 3Abdeljalil Loudaini100% (1)
- Devoir 1 1BAC SC - EXP FR PDFDocument1 pageDevoir 1 1BAC SC - EXP FR PDFAbdeljalil LoudainiPas encore d'évaluation
- Chapitre 9 Réaction DDocument13 pagesChapitre 9 Réaction DAbdeljalil LoudainiPas encore d'évaluation
- Devoir 5 Ondes Lulineuses + Suiivi Temporelle PDFDocument8 pagesDevoir 5 Ondes Lulineuses + Suiivi Temporelle PDFAbdeljalil LoudainiPas encore d'évaluation
- 2014 Pondichery Exo2 Correction SyntheseAcetateEthyle 5ptsDocument2 pages2014 Pondichery Exo2 Correction SyntheseAcetateEthyle 5ptsAbdeljalil LoudainiPas encore d'évaluation
- 1er Ds SM 07 08 BDocument3 pages1er Ds SM 07 08 BYassine NoubirPas encore d'évaluation
- PhysiqueChimie Terminal SDocument150 pagesPhysiqueChimie Terminal SAbdeljalil Loudaini100% (11)
- Devoir 21 Ondes Mécan.+lumineuses+ Suivi Temp.Document6 pagesDevoir 21 Ondes Mécan.+lumineuses+ Suivi Temp.Abdeljalil LoudainiPas encore d'évaluation
- Devoir18 Transformations Nucléaires+ R - A.baseDocument3 pagesDevoir18 Transformations Nucléaires+ R - A.baseAbdeljalil LoudainiPas encore d'évaluation
- Concentration Comps É I On I Que Exercice SDocument3 pagesConcentration Comps É I On I Que Exercice SAbdeljalil LoudainiPas encore d'évaluation
- Exos RL CorrigesDocument5 pagesExos RL CorrigesAbdeljalil LoudainiPas encore d'évaluation
- Decoir 1 PhysiqueDocument3 pagesDecoir 1 PhysiqueIhsan MokhlissePas encore d'évaluation
- La Formulation Des BétonsDocument91 pagesLa Formulation Des Bétonssaadomar80Pas encore d'évaluation
- Technique GCDocument8 pagesTechnique GCMalek LakelPas encore d'évaluation
- Notes Cours #1'Document9 pagesNotes Cours #1'paniizakbariiiPas encore d'évaluation
- CMD 2023 Aout AM Jaune BAT All V4Document17 pagesCMD 2023 Aout AM Jaune BAT All V4Sena HimmetogluPas encore d'évaluation
- Analyse TGADocument20 pagesAnalyse TGAzhor El hallaoui100% (1)
- Rapport de Fin de Formation Sous Le Thème CONTRÔLE DE GESTION Encadre ParDocument6 pagesRapport de Fin de Formation Sous Le Thème CONTRÔLE DE GESTION Encadre Parhou- chiPas encore d'évaluation
- T0709 PDFDocument221 pagesT0709 PDFdavinccicodePas encore d'évaluation
- Manuel6 - Technique de Compostage (FR)Document24 pagesManuel6 - Technique de Compostage (FR)Zibbo Housseini AbdoulPas encore d'évaluation
- Devoir Corrigé de Contrôle N°2 - SVT - 1ère AS (2014-2015) MR Mzid MouradDocument2 pagesDevoir Corrigé de Contrôle N°2 - SVT - 1ère AS (2014-2015) MR Mzid Mouradherni100% (2)
- CF Thermochimie PC S1 Janvier 2023Document4 pagesCF Thermochimie PC S1 Janvier 2023elgarouanikaoutarPas encore d'évaluation
- Lutte Integre1Document30 pagesLutte Integre1Amì NèPas encore d'évaluation
- Protection Des BétonsDocument180 pagesProtection Des BétonsClement Dussaussois100% (1)
- Exercice de Spectrometrie de Masse PDFDocument2 pagesExercice de Spectrometrie de Masse PDFMichael50% (2)
- Chap 1Document21 pagesChap 1Radjaa AddPas encore d'évaluation
- Rapport Projet d'Usine-MarcimDocument95 pagesRapport Projet d'Usine-MarcimHasna ZahirPas encore d'évaluation
- Chimie: Autour Du GlycérolDocument11 pagesChimie: Autour Du GlycérolImanePas encore d'évaluation
- Chapitre 1Document9 pagesChapitre 1abderrahmane lalaouiPas encore d'évaluation
- Traitement Des EUDocument13 pagesTraitement Des EUMoez Ben FadhelPas encore d'évaluation
- DTC RenaultDocument3 pagesDTC RenaultAna Belen Ismael AnaeIsmael75% (4)
- SECHIMIEDocument2 pagesSECHIMIEekodolilian36Pas encore d'évaluation
- La Plomberie PDFDocument76 pagesLa Plomberie PDFmrachrane100% (1)
- Serie 3 PDFDocument13 pagesSerie 3 PDFMoha T OmpPas encore d'évaluation
- L'ajout de Boue Rouge A La Farine CrueDocument15 pagesL'ajout de Boue Rouge A La Farine CrueWiam BalloukPas encore d'évaluation
- BATAN - Cours - Chimie Minérale Descriprive - C245 - BCG - S4 - 2019 - 2020Document46 pagesBATAN - Cours - Chimie Minérale Descriprive - C245 - BCG - S4 - 2019 - 2020Yassine MOUHIBPas encore d'évaluation
- NP12-Utilisation SurfactantDocument2 pagesNP12-Utilisation SurfactantnostryPas encore d'évaluation
- Filtration MembranaireDocument15 pagesFiltration Membranairemazell anna100% (1)
- Note Chapitre I RP 2018Document33 pagesNote Chapitre I RP 2018Nêd JmãPas encore d'évaluation