Académique Documents
Professionnel Documents
Culture Documents
Orca Share Media1682275951229 7055976751346358807
Transféré par
Manel 123Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Orca Share Media1682275951229 7055976751346358807
Transféré par
Manel 123Droits d'auteur :
Formats disponibles
SERIE N°2
Exercice N° 1 :
Sur la surface d’un solide à 20 °C, on mesure la quantité ramenée aux conditions standards
TPN de divers gaz. Sachant que la surface du solide est de 1,966 dm 2, et en supposant que
chaque molécule occupe une surface égale au carré de son diamètre.
1.
Molécules Volume (cm3) Diamètre moléculaire (nm) Calculez
H2O 0,354 0,220 dans
CO2 0,064 0,418 chacun
N2 0,049 0,375 des cas
apparaissant dans le tableau qui suit, le nombre de monocouches de molécules.
Exercice N°2 :
L’adsorption de l’oxyde de carbone sur 2,964 g de charbon activé est étudiée à 0 °C. On
mesure la quantité x ramenée aux conditions TPN de gaz adsorbé sous différentes pressions P.
Les résultats apparaissent dans le tableau qui suit :
P (mmHg) 73 180 309 540 882
x (cm )3
7,5 16,5 25,1 38,1 52,3
1. Montrez graphiquement que les résultats se satisfont de l’isotherme de FREUNDLICH.
Calculez les constantes de cette équation.
2. Montrez aussi que ce système suit l'isotherme de LANGMUIR et calculez les coefficients
relatifs à cette isotherme.
3. À partir de ces résultats, calculez le volume d’oxyde de carbone adsorbé par 1 g de
charbon activé en équilibre avec une pression de 400 mmHg de CO.
Exercice N°3:
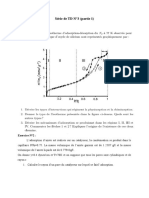
L’adsorption du butane sur un gramme de catalyseur à 0 ºC donne les valeurs suivantes :
P (mmHg) 56,39 89,47 125,22 156,61 179,30 187,46
V (cm3, 28,30
17,09 20,62 23,74 26,09 27,77 La
TPN)
grandeur P
est la pression de vapeur du butane en équilibre avec le catalyseur. La surface
de section d’une molécule de butane est estimée à 0,446 nm 2. À partir de ces données
(P0(butane) = 774,4 mm de mercure):
1. Vérifiez graphiquement que le système obéit à la loi de B.E.T.
2. Evaluez les constantes de B.E.T.
3. Calculez la surface spécifique du catalyseur.
Exercice N°4 :
L’adsorption de l’alcool céthyl benzène sur un échantillon de noir de charbon. L’aire
spécifique déterminée par adsorption d’azote par la méthode BET est de 120 m 2/g. Les
données sont représentées dans le tableau suivant :
1/Q 0.0452 0.0216 0.0158 0.0138 0.0129
1/C 90.9 29.41 14.28 9.8 7.69
1. Montrez qu’il s’agit de l’isotherme de Langmuir.
2. Calculez l’aire occupée par chaque molécule d’alcool céthyl benzène en solution.
Vous aimerez peut-être aussi
- Détermination D'une Formule BruteDocument2 pagesDétermination D'une Formule BruteAhmed Ben Romdhane92% (12)
- Série TD N°2 Chimie Des Surfaces Plus CorrectionDocument10 pagesSérie TD N°2 Chimie Des Surfaces Plus CorrectionKawthar100% (5)
- La Distillation AtmosphériqueDocument62 pagesLa Distillation Atmosphériquerihab tlichPas encore d'évaluation
- Exposé Pétrole & Gaz Naturels IIDocument35 pagesExposé Pétrole & Gaz Naturels IICoulibaly78% (9)
- Cours Des Procedes de RaffinageDocument468 pagesCours Des Procedes de RaffinageBouz Ikram100% (1)
- Exo Cinetique Corrige AmmadoucheDocument82 pagesExo Cinetique Corrige AmmadouchetalebPas encore d'évaluation
- Problème NDocument17 pagesProblème NHaniDjekrif67% (3)
- Correction Des Exercices Du TD1: PV N RT Avec N 1mol, T 273KDocument4 pagesCorrection Des Exercices Du TD1: PV N RT Avec N 1mol, T 273Komar benchiheub0% (1)
- Série + Corrigè de La Série de TD N°1 FinaleDocument8 pagesSérie + Corrigè de La Série de TD N°1 Finaleemiliabelkacemi100% (1)
- Introduction Cryogenie 2016Document18 pagesIntroduction Cryogenie 2016ahmed ahmad100% (1)
- TD2 ThermochimieDocument2 pagesTD2 Thermochimieno one importantPas encore d'évaluation
- Série de TD N1 2020Document2 pagesSérie de TD N1 2020Sara AkliPas encore d'évaluation
- 1 Cours CombustionDocument61 pages1 Cours Combustionbadrezzamane100% (1)
- UE5 MMS M1 Examen 211207 CorrDocument10 pagesUE5 MMS M1 Examen 211207 CorrEslem Islam100% (1)
- TD Procédés Dadsorption Et SéparationDocument3 pagesTD Procédés Dadsorption Et SéparationDZ TECH100% (3)
- La Separation Des Constituants D Un Melange Cours PPT 2Document13 pagesLa Separation Des Constituants D Un Melange Cours PPT 2Chikov ÆminePas encore d'évaluation
- Phénomènes D'adsorptionDocument2 pagesPhénomènes D'adsorptionBouchraPas encore d'évaluation
- UntitledDocument2 pagesUntitledRima mimiPas encore d'évaluation
- TD-Master I.2020Document3 pagesTD-Master I.2020Roselili YasminaPas encore d'évaluation
- Nouvelle Série Dexercices GEDocument3 pagesNouvelle Série Dexercices GETinhinane Cherifi100% (1)
- TD CHimie de SurfaceDocument4 pagesTD CHimie de SurfaceSelma Hassuon100% (3)
- TD 3 Phénomènes de Surface Et Catalyse HétérogèneDocument1 pageTD 3 Phénomènes de Surface Et Catalyse HétérogèneH100% (1)
- Soutien Pcsi 3 Vitesse Et Loi de VitesseDocument5 pagesSoutien Pcsi 3 Vitesse Et Loi de VitesseHarakat ElhoucinePas encore d'évaluation
- 2019-2020 TD Total.Document7 pages2019-2020 TD Total.asics tigerPas encore d'évaluation
- Corrigé de La Première Série de CatalyseDocument10 pagesCorrigé de La Première Série de Catalysesabrina miloudi100% (2)
- Série 2 La Concentration SuperficielleDocument2 pagesSérie 2 La Concentration SuperficielleSalhi Amara75% (4)
- Exercices Corrigé .AdsorptionDocument8 pagesExercices Corrigé .Adsorptionkolta100% (2)
- Série 1Document4 pagesSérie 1Lamia ALACHAHER100% (1)
- Examen smc3 - 2016-17 NormalDocument2 pagesExamen smc3 - 2016-17 NormalDiallo SafaiouPas encore d'évaluation
- 1.4.4 Loi Des Gaz ParfaitsDocument8 pages1.4.4 Loi Des Gaz ParfaitsCHIKHIPas encore d'évaluation
- Devoir FinalDocument5 pagesDevoir FinalKawthar MezennerPas encore d'évaluation
- TD Ads L3Document2 pagesTD Ads L3Souad BouafiaPas encore d'évaluation
- Fiche TD 03docDocument2 pagesFiche TD 03dockadere83Pas encore d'évaluation
- TD CHM 211 - Chapitre 2Document4 pagesTD CHM 211 - Chapitre 2Emmanuel Ket100% (1)
- S14.s1 - Microatelier 08Document4 pagesS14.s1 - Microatelier 08ScribdTranslationsPas encore d'évaluation
- TD 1 Thermochimie L2CDocument2 pagesTD 1 Thermochimie L2Cmeyemarion99Pas encore d'évaluation
- TD2 2018Document6 pagesTD2 2018Hassan ChehouaniPas encore d'évaluation
- TD PSCH - Exo 18-Au 23Document18 pagesTD PSCH - Exo 18-Au 23Inas DrPas encore d'évaluation
- TD PSCH - Exo 35-36 Et 41Document14 pagesTD PSCH - Exo 35-36 Et 41Inas DrPas encore d'évaluation
- Fiche TD 2 Chimie Des Surfaces 2024Document2 pagesFiche TD 2 Chimie Des Surfaces 2024bouchrabell734Pas encore d'évaluation
- TD Thermodynamique Des ÉquilibresDocument19 pagesTD Thermodynamique Des Équilibresbrahimza61Pas encore d'évaluation
- TP ThermoDocument21 pagesTP Thermosamirwane100% (1)
- TD N°1 - 2007/2008 Second Principe de La Thermodynamique ThermochimieDocument2 pagesTD N°1 - 2007/2008 Second Principe de La Thermodynamique ThermochimiemichelPas encore d'évaluation
- Application AdsDocument8 pagesApplication Adsaicha diagnePas encore d'évaluation
- 6 TDPCSIcinetique 2015Document8 pages6 TDPCSIcinetique 2015Nguissaly SonkoPas encore d'évaluation
- Exo ThermoDocument24 pagesExo ThermoSofiene Guedri100% (1)
- Orca Share Media1684691453621 7066108102689054469Document2 pagesOrca Share Media1684691453621 7066108102689054469Manel 1230% (1)
- Cahier de TD (Thermodynamique)Document41 pagesCahier de TD (Thermodynamique)yousraghanem23Pas encore d'évaluation
- TD1 GMP2 2022Document3 pagesTD1 GMP2 2022Hassan ChehouaniPas encore d'évaluation
- CIA Adsorption 2011 PDFDocument29 pagesCIA Adsorption 2011 PDFAbdel Moussa100% (2)
- TD Chimie PhysiqueDocument24 pagesTD Chimie PhysiquemouafoemelinePas encore d'évaluation
- TD Traitement Des Effluents Gazeux À La SourceDocument2 pagesTD Traitement Des Effluents Gazeux À La SourceAyman Ayman100% (2)
- TPCHIM310BDocument8 pagesTPCHIM310BNadège ReyPas encore d'évaluation
- Inbound 5566480752698915028Document11 pagesInbound 5566480752698915028BouchraPas encore d'évaluation
- Cinétique Chimique Exercices 04.TextMarkDocument16 pagesCinétique Chimique Exercices 04.TextMarkAbedPas encore d'évaluation
- Exercice N°1Document5 pagesExercice N°1islam khoPas encore d'évaluation
- TD 1 Phénomènes de Surface Et Catalyse HétérogèneDocument2 pagesTD 1 Phénomènes de Surface Et Catalyse HétérogèneH100% (2)
- Série Corrigé CinétiqueDocument8 pagesSérie Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- Série 1 2017 Smic s1Document6 pagesSérie 1 2017 Smic s1yassineredone4Pas encore d'évaluation
- Capacité Calorifique Des GazDocument4 pagesCapacité Calorifique Des Gazleilalargate_3780929Pas encore d'évaluation
- Résolutions Des TDDocument41 pagesRésolutions Des TDghislain AlowakinnouPas encore d'évaluation
- TD2 Chimie Generale +CORRIGE 2016-2017Document10 pagesTD2 Chimie Generale +CORRIGE 2016-2017Awatif BePas encore d'évaluation
- TD Lois Des Gaz ParfaitsDocument2 pagesTD Lois Des Gaz ParfaitsNguenar SarrPas encore d'évaluation
- Fiche TD 1Document1 pageFiche TD 1hafsaoui younesPas encore d'évaluation
- TD Te l3gpDocument7 pagesTD Te l3gpInas DrPas encore d'évaluation
- Transfert de Chaleur RayonnementDocument6 pagesTransfert de Chaleur RayonnementManel 123Pas encore d'évaluation
- Transfert de Chaleur RayonnementDocument6 pagesTransfert de Chaleur RayonnementManel 123Pas encore d'évaluation
- TP TeneurDocument8 pagesTP TeneurManel 123Pas encore d'évaluation
- TP SéchageDocument4 pagesTP SéchageManel 123Pas encore d'évaluation
- Orca Share Media1679473245335 7044221350803381331Document4 pagesOrca Share Media1679473245335 7044221350803381331Manel 123Pas encore d'évaluation
- Orca Share Media1684105053659 7063648562985318883Document1 pageOrca Share Media1684105053659 7063648562985318883Manel 123Pas encore d'évaluation
- Suport Cours-Réacteurs Homogènes 2022Document30 pagesSuport Cours-Réacteurs Homogènes 2022Manel 123Pas encore d'évaluation
- Orca Share Media1679303447551 7043509167277359930Document3 pagesOrca Share Media1679303447551 7043509167277359930Manel 123Pas encore d'évaluation
- TP-01-adsption-dacide-ac - Tique-Sur-Charbon-Actif - PDF Filename UTF-8''TP-01-adsption-dacide-acétique-sur-charbon-actifDocument3 pagesTP-01-adsption-dacide-ac - Tique-Sur-Charbon-Actif - PDF Filename UTF-8''TP-01-adsption-dacide-acétique-sur-charbon-actifManel 123Pas encore d'évaluation
- Série de TD-GPDocument4 pagesSérie de TD-GPManel 123Pas encore d'évaluation
- Orca Share Media1684691453621 7066108102689054469Document2 pagesOrca Share Media1684691453621 7066108102689054469Manel 1230% (1)
- Page de Garde 3Document1 pagePage de Garde 3Manel 123Pas encore d'évaluation
- Orca Share Media1674410161980 7022985240033758640Document10 pagesOrca Share Media1674410161980 7022985240033758640Manel 123Pas encore d'évaluation
- SERIE DE TD N1 GP 2022 L3 Pheno de Surf Et Catalyse HeterDocument3 pagesSERIE DE TD N1 GP 2022 L3 Pheno de Surf Et Catalyse HeterManel 123100% (2)
- Notions Sur La Simulation Des Procédés ChimiquesDocument7 pagesNotions Sur La Simulation Des Procédés ChimiquesSöû SøùSøú Mîã100% (1)
- Orca Share Media1674385594543 7022882196736552069Document3 pagesOrca Share Media1674385594543 7022882196736552069Manel 123Pas encore d'évaluation
- Procedes Agroalimentaires 2022Document19 pagesProcedes Agroalimentaires 2022Manel 123Pas encore d'évaluation
- Chapitre 1Document4 pagesChapitre 1Amina BadaouiPas encore d'évaluation
- TTP 01Document1 pageTTP 01Manel 123Pas encore d'évaluation
- Procédé CryogeniqueDocument18 pagesProcédé CryogeniqueManel 123Pas encore d'évaluation
- Série de Chimie 1 Exercice À Distance (TD 2) FrancaisDocument3 pagesSérie de Chimie 1 Exercice À Distance (TD 2) FrancaisManel 123Pas encore d'évaluation
- Cours L2 2021 6Document3 pagesCours L2 2021 6Nedjm EddinePas encore d'évaluation
- Na 235Document5 pagesNa 235OUSSAMA taibi100% (1)
- Bac STL 2018 Spécialité SPCL Corrige de CBSV Et SPCLDocument4 pagesBac STL 2018 Spécialité SPCL Corrige de CBSV Et SPCLLETUDIANT100% (1)
- Summary Introduction To Natural Gas-FRDocument13 pagesSummary Introduction To Natural Gas-FRaliPas encore d'évaluation
- M.T 116 01Document71 pagesM.T 116 01Tul IpePas encore d'évaluation
- Serie - Melanges - Separation (WWW - Pc1.ma) PDFDocument2 pagesSerie - Melanges - Separation (WWW - Pc1.ma) PDFNki NonkiPas encore d'évaluation
- Catalyst Technology For Biofuel Production Conversion of Renewable Lipids Into Biojet and Biodiesel-EnglishDocument4 pagesCatalyst Technology For Biofuel Production Conversion of Renewable Lipids Into Biojet and Biodiesel-Englishsaleh4060Pas encore d'évaluation
- Expose de PhysiqueDocument6 pagesExpose de PhysiqueKouame Christian KOUADIO100% (1)
- Cã Digos de Error Caldera Roca 20-20 Laura PDFDocument12 pagesCã Digos de Error Caldera Roca 20-20 Laura PDFemuno008Pas encore d'évaluation
- 8.1 Flodis DN 15 ... 32 MM, Manual Instalare, en PDFDocument4 pages8.1 Flodis DN 15 ... 32 MM, Manual Instalare, en PDFAnonymous HC0tWePas encore d'évaluation
- BFEM Physique Chimie 2017Document3 pagesBFEM Physique Chimie 2017magno MBALLOPas encore d'évaluation
- 4ème 3 TP - COMBUSTIONSDocument6 pages4ème 3 TP - COMBUSTIONSmaouthonjiPas encore d'évaluation
- Chandoul Incendie Chap IDocument15 pagesChandoul Incendie Chap IAbdlmonem ChandoulPas encore d'évaluation
- JANAF Termochemical TablesDocument96 pagesJANAF Termochemical TablesAlan Quintanar HaroPas encore d'évaluation
- Devoir SDocument3 pagesDevoir SMourad MatmourPas encore d'évaluation
- Laouar ImedDocument132 pagesLaouar Imedahmed ahmad0% (1)
- CinétiqueDocument112 pagesCinétiqueRodolphe YoboPas encore d'évaluation
- Gas Catalogue PDFDocument196 pagesGas Catalogue PDFAnonymous 4MLEo9TVQPas encore d'évaluation
- Colmatage Et Nettoyage Des Membranes D'osmose Inverse de DessalementDocument14 pagesColmatage Et Nettoyage Des Membranes D'osmose Inverse de Dessalementyoussef hachimiPas encore d'évaluation
- DufourDocument21 pagesDufourJustin Smart TchikoaPas encore d'évaluation
- Bioreacteur Homogène Fermenteur ConvertiDocument27 pagesBioreacteur Homogène Fermenteur ConvertifatahaymenrowPas encore d'évaluation
- Série Cinétique ChimiqueDocument1 pageSérie Cinétique ChimiqueYoucef KrPas encore d'évaluation
- Corrosion Dans Les Chaudières - LenntechDocument1 pageCorrosion Dans Les Chaudières - LenntechmeratiPas encore d'évaluation