Académique Documents
Professionnel Documents
Culture Documents
MMCh1 Les Changements D'état Cours
Transféré par
egozeelowTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
MMCh1 Les Changements D'état Cours
Transféré par
egozeelowDroits d'auteur :
Formats disponibles
Matière et matériau T STI2D Spé
Ch1 Les changements d’état
Le changement d’état est le
1.Les états de la matière
passage d’un état à l’autre. Les 3 états de l’eau
Un changement d’état se fait
Les différents états d’un
à température constante.
corps pur sont également
appelés phases.
Exemple pour l’eau
2. Changement d’état et liaisons entre molécules
Au niveau microscopique un changement d’état correspond à l’établissement ou la rupture des interactions entre les
molécules (ou atomes).
Dans le cas de l’eau, cette liaison entre l’atome d’hydrogène d’une molécule et l’atome d’oxygène d’une autre molécule
s’appelle la liaison hydrogène.
Liaisons hydrogène
Les changements d’état 1
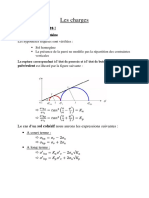
3. Diagramme d’état (P,T)
Le diagramme d’état d’un
corps pur permet de Au point triple, les trois
déterminer la phase dans phases (solide, liquide,
laquelle se trouve ce corps pur gazeux) coexistent.
pour une pression et une
température données.
Au-delà du point critique
C, le fluide possède un
comportement
Les trois courbes (sublimation,
intermédiaire entre celui
fusion et vaporisation) donnent
d’un liquide et d’un gaz.
les coordonnées des points
(T,P), pour lesquelles deux
phases peuvent coexister.
4. Transfert thermique
Un transfert thermique est un transfert d’énergie qui s’effectue toujours du corps le plus chaud vers le corps le plus
froid.
Capacité thermique massique c
Certains corps ont la capacité de stocker de l’énergie lors de l’élévation de sa température. La grandeur qui caractérise
cette capacité est la capacité thermique massique c. Elle permet de calculer l’énergie stockée Q (J).
masse (kg) températures initiale et finale (K)
Q = m.c.(θf – θi)
capacité thermique massique (J.kg-1K-1)
Energie massique de changement d’état L
Lors d’une transfert thermique, on peut observer un changement d’état physique du corps qui se fait à température
constante.
Le corps reçoit de l’énergie si il passe à un état de la matière moins ordonné ; il en cède si il passe à un état plus
ordonné.
L’énergie Q (J) reçue ou cédée pendant le changement d’état est :
masse (kg) énergie massique (J.kg-1)
Q = m.L
Dans un système isolé, la somme des énergies échangées est nulle.
Les changements d’état 2
Les changements d’état 3
Vous aimerez peut-être aussi
- Ch6 (TSTI2D) - Changements Détat Et Transferts Thermique (Prof)Document1 pageCh6 (TSTI2D) - Changements Détat Et Transferts Thermique (Prof)unsheatedsword55Pas encore d'évaluation
- TP N°3Document3 pagesTP N°3Abdelwahab.gfPas encore d'évaluation
- Cours IIA Termo 3Document5 pagesCours IIA Termo 3Nizar BenYahiaPas encore d'évaluation
- Ch21 CP StudentsDocument23 pagesCh21 CP StudentsSoulaima MatmatiPas encore d'évaluation
- Thermochimie: PR: K. Oulad Haj AliDocument97 pagesThermochimie: PR: K. Oulad Haj AliYoussef AkrPas encore d'évaluation
- Chapitre1 Thermodynamique ChimiqueDocument9 pagesChapitre1 Thermodynamique ChimiqueAmira MiraPas encore d'évaluation
- Chapitre 1 RappelDocument14 pagesChapitre 1 RappelHarry PoterPas encore d'évaluation
- TP S2.Chimie2 - 1STH - 2016-2017Document18 pagesTP S2.Chimie2 - 1STH - 2016-2017slimane33% (3)
- Chap I Et II ThermChim SMC - S4 PDFDocument49 pagesChap I Et II ThermChim SMC - S4 PDFAbd BaghadPas encore d'évaluation
- Chapitre 3Document14 pagesChapitre 3Junias PakiPas encore d'évaluation
- CHAP 5 (L'énergie Interne)Document7 pagesCHAP 5 (L'énergie Interne)hepived840Pas encore d'évaluation
- Chapitre 1 de La ThermodynamiqueDocument12 pagesChapitre 1 de La ThermodynamiqueANGE TERENCE NESSY KOUAMEPas encore d'évaluation
- Chapitre IDocument14 pagesChapitre Iهبة الرحمانPas encore d'évaluation
- Cours de Thermodynamique S1Document146 pagesCours de Thermodynamique S1chaimae el aichi100% (3)
- Cours Chapitre-1Document19 pagesCours Chapitre-1amiira bouzouadaPas encore d'évaluation
- 8 - Equilibre Liquide - VapeurDocument52 pages8 - Equilibre Liquide - VapeurEtienne jeoffreyPas encore d'évaluation
- Polycopié Des TP de CHIMIE 2Document10 pagesPolycopié Des TP de CHIMIE 2Walid Ouabas100% (3)
- Cours ThermoDocument62 pagesCours ThermoJaphet DOSSOUPas encore d'évaluation
- Chap 1Document4 pagesChap 1Abdou BoukhalfaPas encore d'évaluation
- Second Principe Du ThermodynamiqueDocument15 pagesSecond Principe Du ThermodynamiqueMario SuperPas encore d'évaluation
- Ther CH1 M1 EltmDocument5 pagesTher CH1 M1 EltmYahya MamloutPas encore d'évaluation
- Thermodynamique Appliquée Pour IngénieurDocument69 pagesThermodynamique Appliquée Pour Ingénieurإبراهيم الزايدي الكيحلPas encore d'évaluation
- Introduction À La ThermodynamiqueDocument3 pagesIntroduction À La ThermodynamiquePierre CARREPas encore d'évaluation
- Cours de Thermodynamyque Sm1-Smp1-Smc1Document146 pagesCours de Thermodynamyque Sm1-Smp1-Smc1Mohamed Ait Kabir100% (1)
- Cours Premier Principe - ChaleurDocument1 pageCours Premier Principe - ChaleurlkmkmlkPas encore d'évaluation
- Chapitre Ii PDFDocument18 pagesChapitre Ii PDFAsmahane FaslaPas encore d'évaluation
- Cours Thermo - Chapitre 3 - Diagramme de Phase Du Corps Pur - 2018Document28 pagesCours Thermo - Chapitre 3 - Diagramme de Phase Du Corps Pur - 2018ait hssain100% (1)
- Les Bases de La Thermodynamique 2 Chapitre II PDFDocument11 pagesLes Bases de La Thermodynamique 2 Chapitre II PDFmahdi amraouiPas encore d'évaluation
- Chap. 11-Transferts ThermiquesDocument3 pagesChap. 11-Transferts ThermiquesBénédicte & Christophe MULLERPas encore d'évaluation
- Chapitre 02Document8 pagesChapitre 02Zach LeitchPas encore d'évaluation
- Cours Thermo3Document49 pagesCours Thermo3Nour El mehdiPas encore d'évaluation
- Cours de Thermodynamique: I-Définitions Fondamentales Et UnitesDocument32 pagesCours de Thermodynamique: I-Définitions Fondamentales Et UnitesNidhal SouifiPas encore d'évaluation
- Cours ThermoDocument4 pagesCours ThermoSall HamidouPas encore d'évaluation
- Cours - Thermodynamique Partie 2-1Document15 pagesCours - Thermodynamique Partie 2-1Fatiha ElmoudenPas encore d'évaluation
- Thermo c8 SiteDocument28 pagesThermo c8 SiteAmin LarouiPas encore d'évaluation
- 6 Cours Energie ThermiqueDocument2 pages6 Cours Energie ThermiqueAbdo BdaPas encore d'évaluation
- Energie Thermique Et Transfert Thermique Resume de Cours 1 2Document2 pagesEnergie Thermique Et Transfert Thermique Resume de Cours 1 2bouby6890100% (1)
- COURS DE FROID ET CLIMATISATION 2nde MHB - CHALEURDocument7 pagesCOURS DE FROID ET CLIMATISATION 2nde MHB - CHALEURThierry roland UmPas encore d'évaluation
- UE1 Chimie 6 ThermodynamiqueDocument15 pagesUE1 Chimie 6 Thermodynamiquesun-nee-chan9Pas encore d'évaluation
- Diagramme de PhasesDocument24 pagesDiagramme de Phaseslaamoh37Pas encore d'évaluation
- Djerrada A. Dgm/Ft/Uamb 1Document7 pagesDjerrada A. Dgm/Ft/Uamb 1Mouhand AoudjitPas encore d'évaluation
- Chapitre 16 - Premier Principe de La ThermodynamiqueDocument4 pagesChapitre 16 - Premier Principe de La ThermodynamiqueZoulikha Iriza100% (1)
- Transfert ThermiqueDocument8 pagesTransfert ThermiqueHamza BPas encore d'évaluation
- CalorimétrieDocument4 pagesCalorimétrieSoh AibPas encore d'évaluation
- CH 3 Transferts Et Isolation ThermiquesDocument8 pagesCH 3 Transferts Et Isolation ThermiquesBader EddPas encore d'évaluation
- Agreg 1993 SujDocument218 pagesAgreg 1993 SujBoussetta ZouhaierPas encore d'évaluation
- Chapitre 5 Diagramme de Phases de Corps Purs-1Document10 pagesChapitre 5 Diagramme de Phases de Corps Purs-1Rayen Jlassi100% (1)
- Chapi IiiDocument69 pagesChapi IiiFaicel MejriPas encore d'évaluation
- SAM 7 Thermodynamique II PDFDocument39 pagesSAM 7 Thermodynamique II PDFKolann Aubert100% (1)
- 2 Substance PureDocument23 pages2 Substance Purebchedhly malakPas encore d'évaluation
- CH I Rappel de Thermodynamique10-11Document15 pagesCH I Rappel de Thermodynamique10-11SirineJamoussiPas encore d'évaluation
- CH I Rappel de Thermodynamique10-11Document15 pagesCH I Rappel de Thermodynamique10-11SirineJamoussiPas encore d'évaluation
- CH8-Etats Matiere PDFDocument35 pagesCH8-Etats Matiere PDFnadia boukherroubPas encore d'évaluation
- Energie ThermiqueDocument3 pagesEnergie ThermiqueJp TauvelPas encore d'évaluation
- Changement D Etat Du Corps Pur CoursDocument4 pagesChangement D Etat Du Corps Pur Courspicasso da vinciPas encore d'évaluation
- Cours - Transferts Thermiques - SMP6 - AU2019-20Document54 pagesCours - Transferts Thermiques - SMP6 - AU2019-20ZahirPas encore d'évaluation
- CH01 Cours ThermodynamiqueDocument13 pagesCH01 Cours ThermodynamiqueFaycal BouhaniaPas encore d'évaluation
- Chapitre VI Thermodynamique Chimique (Ouennoughi)Document24 pagesChapitre VI Thermodynamique Chimique (Ouennoughi)WATAT KAMGA PIERRE LOTIPas encore d'évaluation
- Séance 3Document32 pagesSéance 3AIT KHOUYA YacinPas encore d'évaluation
- Culture Cellulaire COUR 1Document10 pagesCulture Cellulaire COUR 1Hadjer AdaidaPas encore d'évaluation
- Chapitre 11. Nombre D'étages Théoriques Dans Les Systèmes ImmisciblesDocument10 pagesChapitre 11. Nombre D'étages Théoriques Dans Les Systèmes ImmisciblesZizou LeePas encore d'évaluation
- Qualification de Revetements de SurfaceDocument4 pagesQualification de Revetements de SurfaceZANZANPas encore d'évaluation
- ThermodynamiqueDocument65 pagesThermodynamiqueulrich victor kuatePas encore d'évaluation
- Hydrocarbures Aromatiques BisDocument2 pagesHydrocarbures Aromatiques BisNlem NdongoPas encore d'évaluation
- Révisions Physique 3D - Exercices 31-05-20Document30 pagesRévisions Physique 3D - Exercices 31-05-20Mentalité ArchaïquePas encore d'évaluation
- Équipements de Chauffage Et Locaux TechniqueDocument13 pagesÉquipements de Chauffage Et Locaux Techniquebaho btwPas encore d'évaluation
- Cours de Thermodynamique Appliquée - TS STGI 1-1Document74 pagesCours de Thermodynamique Appliquée - TS STGI 1-1francky scottPas encore d'évaluation
- Exercice 1Document4 pagesExercice 1Débonnaire Bandeya100% (1)
- Travail Pratique Sur L'Acidification Et La FermentationDocument8 pagesTravail Pratique Sur L'Acidification Et La FermentationmushiziPas encore d'évaluation
- DS1 Chap1Document1 pageDS1 Chap1valdxPas encore d'évaluation
- E211 - Electrocinéttique 1 DipôlesDocument23 pagesE211 - Electrocinéttique 1 DipôlesM'hammed AbouzianePas encore d'évaluation
- SP00700 DG 1 Water AnalysisDocument4 pagesSP00700 DG 1 Water AnalysisMick VPas encore d'évaluation
- Hydraulique - Dut de Génie CivilDocument96 pagesHydraulique - Dut de Génie CivilJulienne valerie AgodigoPas encore d'évaluation
- Rapport Gec3Document33 pagesRapport Gec3Gharsalli ghofranePas encore d'évaluation
- Referentiels Non Galileens ExercicesDocument6 pagesReferentiels Non Galileens ExercicesRobio GaminGPas encore d'évaluation
- Partie I ElectromagnétiqueDocument31 pagesPartie I Electromagnétiquealeatoire buzzPas encore d'évaluation
- Expose BioinformatiqueDocument10 pagesExpose Bioinformatiquebillel lamairiaPas encore d'évaluation
- 5 Déversement CommentairesDocument105 pages5 Déversement CommentairesRussel Kamwa SohPas encore d'évaluation
- Devoir 2 TS 2015 2016Document4 pagesDevoir 2 TS 2015 2016rranjalalaoPas encore d'évaluation
- TD Magnétostatique-Série 4-2021Document5 pagesTD Magnétostatique-Série 4-2021Zakaria MJPas encore d'évaluation
- CTP Absorbeur Alcoll EthyliqueDocument17 pagesCTP Absorbeur Alcoll EthyliqueRemy Blondel100% (1)
- Bonneau-Jeanmotte-Leon TDC Rapport Edk CompressedDocument59 pagesBonneau-Jeanmotte-Leon TDC Rapport Edk Compressedapi-638155363Pas encore d'évaluation
- Actions Sur ParoiDocument9 pagesActions Sur ParoiMed ElouartiPas encore d'évaluation
- Crushing FinalDocument57 pagesCrushing Finalsheritier80Pas encore d'évaluation
- Conditionnement AirDocument10 pagesConditionnement AirWalid Ch-fPas encore d'évaluation
- Fiche Transport Addition de Poids ExerciceDocument11 pagesFiche Transport Addition de Poids ExercicezfodhilPas encore d'évaluation
- 08 Evolution SpontaneeDocument3 pages08 Evolution SpontaneeChartier JulienPas encore d'évaluation
- Exercices 4 Mouvement de Chute Verticale D'un SolideDocument1 pageExercices 4 Mouvement de Chute Verticale D'un Solideoperarep35Pas encore d'évaluation
- Physique 1ereDTI Eval4 Lycee Classique Dschang 2019 2020Document2 pagesPhysique 1ereDTI Eval4 Lycee Classique Dschang 2019 2020brice mouadjePas encore d'évaluation