Académique Documents
Professionnel Documents
Culture Documents
Exercices Et Corrigés
Transféré par
Abdel Hakim M. NadjibTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Exercices Et Corrigés
Transféré par
Abdel Hakim M. NadjibDroits d'auteur :
Formats disponibles
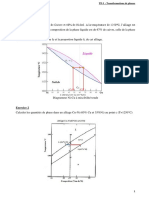
SEANCE DE T.
D N3 Exercice 1 : On donne une reprsentation de la classification priodique 1) Y placer les lments suivants Al, Ar, As(33), Ga(31) , H, He, Kr, Mg, Ne, O , Re(75) , Ce(58) , Tl(81) , W(74) , Te(52) , U(92) , Rn 2) Soit l'lment situ en ligne 5 et colonne 16 a) Quel est son numro atomique b) Quelle est sa configuration lectronique
c) Quel est son schma de Lewis atomique complet (cases quantiques) d) Quel est son schma de Lewis atomique simplifi (tirets et points) Z = 52 ; (Kr) 5s2 4d10 5p4
3) Famille des alcalino-terreux : Be, Mg, Ca, Ba, Ra a) Dans quelle colonne se trouvent les alcalino-terreux ? Colonne 2 b) Quel est leur ion le plus stable ? X2+ c) Quels sont leur numros atomiques respectifs ? 4 ; 12 ; 20 ; 38 ; 56 ; 88 d) Si on dcouvre un jour un nouvel lment de cette famille, quel sera son numro atomique ? Prochain gaz rare + 2 e- : 86 + 2 + 10 + 14 + 6 + 2 = 120
Exercice 2 : Elments Gallium (Z = 31) et Arsenic (Z = 33)
Rgle de Sanderson : un lment est mtallique si le nombre dlectrons sur son niveau de n le plus lev est infrieur ou gal au numro de sa priode.
1) Donner la configuration lectronique de ces deux lments. Ga : Z = 31 = 18 + 13 : (Ar) 3d10 4s2 4p1 As : Z = 33 = 18 + 15 : (Ar) 3d10 4s2 4p3 2) Reprsenter leur schma de Lewis.
3) Pour ces deux lments donner sa position (Ligne et Colonne) dans la classification priodique.
Ga : ligne 4 colonnne 13 As : ligne 4 colonnne 15 Mendeleiev ds 1869 prdit lexistence et dcrivit lavance les proprits dun de ces deux lments quil nomma alors eka-aluminium car il prvoyait des proprits similaires celle de lAluminium.
4) Quel est cet lment Ga ou As ? (justifier simplement votre rponse)
Le Gallium Ga appartient au mme groupe que l'Aluminium Al, sa couche de valence est similaire , il prsente donc des proprits proches de celles de Al.
Mtaux ou non mtaux ? Un de ces lment est un mtal qui possde la proprit dtre liquide temprature ambiante ce qui permet son utilisation dans les thermomtres. Lautre n'est pas un mtal. 5) Rappeler les 2 critres chimiques qui permettent de caractriser les mtaux et les nonmtaux.
Les mtaux donnent des cations et leurs oxydes sont basiques. Les non mtaux donnent des anions et leurs oxydes sont acides.
6) La rgle dite de Sanderson permet, elle aussi, de dterminer si un lment est mtallique ou non. Par utilisation de cette rgle dire entre Ga et As qui est mtallique et qui ne lest pas.
Ga appartient la priode 4 et possde 3 lectrons sur sa couche de valence, d'aprs la rgle de Sanderson, Ga est donc un mtal. As appartient la priode 4 et possde 5 lectrons sur sa couche de valence, d'aprs la rgle de Sanderson, As n'est donc pas un mtal.
Le compos MgGa2O4 peut mettre dans certaines conditions de la lumire verte sil est excit par des U.V. Cette proprit fait quil est utilis dans les photocopieurs "Xerox". 7) En supposant que le compos MgGa2O4 est de nature ionique et que les ions sont les plus stables des lments concerns a) dterminer la charge de lion stable du magnsium Mg
Mg : Colonne 2 s2 : perd facilement 2 lectrons pour donner l'ion Mg2+ dont la configuration
lectronique est identique celle du gaz rare prcdent dans la classification priodique. b) dterminer la charge de lion stable de l'oxygne O O : colonne 16 s2p4 capte facilement 2 lectrons pour donner l'ion O2- dont la configuration lectronique est identique celle du gaz rare suivant dans la classification priodique. c) MgGa2O4 tant lectriquement neutre, en dduire la charge de l'ion du galium Ga prsent dans ce compos Mg2+ : 2 charges positives 4 O2- : 8 charges ngatives Soit 8 2 = 6 charges ngatives pour MgO4 Il faut donc compenser par 6 charges positives pour obtenir l'lectroneutralit de l'difice MgGa2O4 ces 6 charges correspondent deux ion du Galium, soit l'ion Ga3+.
d) Votre rsultat est-il en accord avec vos rponses aux questions 5 et 6 ?
L'ion du Gallium est un cation ce qui montre que Ga est un mtal, la rgle de Sanderson prvoit galement cela, il n'y a donc pas de contradictions.
e) A partir du schma de Lewis du galium justifier la formation de cet ion. Ga perd facilement ses 3 lectrons de valence 4s2 4p1 pour donner Ga3+. f) D'aprs la rgle de l'octet, quel est l'ion le plus stable du Galium ?
Pour ressembler au gaz rare prcdent dans la classification priodique Ga donne Ga3+. Remarque : En fait Ga3+ n'est pas vraiment identique au gaz rare prcdent puisque il possde 10 lectrons de type 3d, mais ce groupe 3d10 tant complet Ga3+ est tout de mme trs stable comme un gaz rare.
g) La rgle de l'octet est-elle suivie dans ce cas particulier ?
C'est bien le cas.
8) Il existe un compos ionique nomm arsniure de gallium de formule GaAs. Ce compos est trs utilis dans la technologie des lasers car il prsente la proprit intressante de pouvoir convertir llectricit en lumire cohrente. GaAs est un compos ionique constitu d'un cation et d'un anion. a) D'aprs vos rponses aux question 5 et 6, dduire qui est l'anion et qui est le cation.
Ga mtal donc cation Ga3+. As non mtal donc anion As3-.
b) D'aprs la rgle de l'octet, quel est l'ion le plus stable de l'arsenic ?
As : colonne 15 s2p3 capte facilement 3lectrons pour donner l'ion As3- dont la configuration lectronique est identique celle du gaz rare suivant dans la classification priodique. c) La rgle de l'octet est-elle suivie dans ce cas particulier ? GaAs neutre, Ga donne Ga3+, donc As donne As3-. La rgle de l'octet esr respecte. d) A partir du schma de Lewis de l'arsenic justifier la formation de cet ion.
10) Il est bien connu que lArsenic est un poison violent. Le compos appel couramment Arsenic nest pas en ralit llment Arsenic lui mme mais un de ces oxydes lanhydride arsnieux de formule As2O3. a) En suivant la mme dmarche qu' la question 7, dterminer la charge de lion de larsenic dans ce compos ? 3 O2- et 2 As3+
b) D'aprs la nature (anionique ou cationique) de l'ion trouv que peut-on conclure de la nature mtallique ou non de l'arsenic ?
As3+ est un cation donc As serait un mtal. c) On observe exprimentalement que cet oxyde se dissous dans l'eau en donnant une solution acide. que peut-on conclure de la nature mtallique ou non de l'arsenic ? L'oxyde est acide, As serait donc un non-mtal. 11) Il existe un autre oxyde de lArsenic nomm anhydride arsnique de formule As2O5. a) En suivant la mme dmarche qu' la question 7, dterminer la charge de lion de larsenic dans ce compos ?
5 O2- et 2 As5+
b) D'aprs la nature (anionique ou cationique) de l'ion trouv que peut-on conclure de la nature mtallique ou non de l'arsenic ?
As5+ est un cation donc As serait un mtal. c) On observe exprimentalement que cet oxyde se dissous dans l'eau en donnant une solution acide. que peut-on conclure de la nature mtallique ou non de l'arsenic ? L'oxyde est acide, As serait donc un non-mtal. 13) Lexistence des composs As2O3 et As2O5 permet-elle de dire si lArsenic est un mtal ou un non-mtal ? As donne des cations mais ces oxydes sont acides, il y a contradiction et on ne peu conclure sur la nature mtallique ou non de As
LArsenic possde donc en ralit, des proprits intermdiaires entre celles des mtaux et des non-mtaux et on le qualifie souvent de semi-mtal. Il donne ainsi trois ions diffrents.
14) Prciser la nature de ces trois ions et justifier simplement leur formation partir du schma de Lewis de lArsenic . As peut capter 3 lectrons pour donner As3- et acqurir la structure du gaz rare suivant Kr. Il peut galement perdre ses 3 lectrons 4p pour donner As3+ dont la configuration sera [Ar] 3d10 4s2 cette configuration ne contient que des couches ou sous-couche totalement remplies et As3+ sera donc trs stable. Il peut de plus perdre ses 2 lectrons 4s pour donner As5+ dont la configuration sera [Ar] 3d10cette configuration ne contient que des couches ou sous-couche totalement remplies et As5+ sera donc trs stable.
Exercice 3 : Un compos ionique a pour formule A2B3 On sait que les lments A et B sont tous deux des lments des deuxime ou troisime priodes de la classification. On sait dautre part que llment A est un METAL alors que B est un NON-METAL (ou METALLODE). Quelles sont les nature possibles pour ce compos ionique ?
A est un mtal et donne donc un cation An+. B est un non-mtal et donne donc un anion Am-. A2B3 est lectriquement neutre. 2n=3m m=2/3n m et n sont des entiers, la solution la plus simple est n = 3 et m = 2. A3+ et B2D'aprs la rgle de l'octet, les lments dont l'ion stable est porteur de 3 charges positives sont ceux de la colonne 13, A est donc soit le bore B, soit l'aluminium Al. D'aprs la rgle de l'octet, les lments dont l'ion stable est porteur de 2 charges ngatives sont ceux de la colonne 16, B est donc soit l'oxygne O soit le soufre S. Il y a donc 4 possibilits : Al2S3 ; Al2O3 ; BO3 ; BS3. Mais le Bore B appartient la deuxime priode et possde 3 lectrons de valence, d'aprs la rgle de Sandersson il n'est donc pas un mtal et on peut donc elliminer BO3 et BS3. L'aluminium avec 3 lectrons de valence et appartenant la priode 3 est bien mtallique d'aprs la rgle de Sanderson. O et S sont bien des non-mtaux d'aprs la rgle de Sanderson. Finalement il reste donc deux possibilits : Al2S3 et Al2O3
Vous aimerez peut-être aussi
- Les Fonctions ThermodynamiquesDocument15 pagesLes Fonctions ThermodynamiquesMariam ZouhairPas encore d'évaluation
- Solution de La Série N°1-1Document4 pagesSolution de La Série N°1-1Fleuretta FleurePas encore d'évaluation
- SMC 3Document113 pagesSMC 3kurts010100% (1)
- Structure Electronique Des MoleculesDocument17 pagesStructure Electronique Des MoleculesFatima EL AROUSSIPas encore d'évaluation
- Assainissemnt Sur Covadis PDFDocument24 pagesAssainissemnt Sur Covadis PDFam_loukili89% (9)
- Calcule Hydrologique Et HydrauliqueDocument22 pagesCalcule Hydrologique Et HydrauliqueAbdel Hakim M. Nadjib100% (3)
- Raport de TP Matériaux de ConstructionDocument57 pagesRaport de TP Matériaux de ConstructionMaroua LahbibPas encore d'évaluation
- Introduction à la physique nucléaire et des particulesD'EverandIntroduction à la physique nucléaire et des particulesPas encore d'évaluation
- Cours2 (190321)Document10 pagesCours2 (190321)elhoussaine saidPas encore d'évaluation
- TD 2 RéseauxDocument9 pagesTD 2 RéseauxSamah SamahPas encore d'évaluation
- Diagramme de FrostDocument19 pagesDiagramme de Frostmehdi100% (1)
- (PDF) Polycopié D'exercices Et Examens Résolus - Mécaniques Des Systèmes de Solides Indéformables - Randriarimanana RICORDEAU MAVANTANA - AcademiaDocument65 pages(PDF) Polycopié D'exercices Et Examens Résolus - Mécaniques Des Systèmes de Solides Indéformables - Randriarimanana RICORDEAU MAVANTANA - AcademiaNambinintsoa Nomenjanahary100% (1)
- 26455560Document4 pages26455560Abderahmene Ghodbane100% (2)
- Examen ChimieDocument9 pagesExamen ChimieRosa Hyo Sonn100% (1)
- Exercices Equilibres de Phases Liquide Solide Des Melanges BinairesDocument7 pagesExercices Equilibres de Phases Liquide Solide Des Melanges BinairesYvan Kayo KamdemPas encore d'évaluation
- TD Potentiomerie - 21Document1 pageTD Potentiomerie - 21Abderrahmane AmzidPas encore d'évaluation
- SMC4 Cristallographie Correction Normale 2016Document4 pagesSMC4 Cristallographie Correction Normale 2016mad100% (2)
- Travaux Diriges Equilibres Chimiques Et Produit de SolubilitéDocument4 pagesTravaux Diriges Equilibres Chimiques Et Produit de Solubiliténoura gnangbePas encore d'évaluation
- BH 3Document6 pagesBH 3pilaf62Pas encore d'évaluation
- Chimie Élément CobaltDocument2 pagesChimie Élément Cobalttcheva jokhanan TiambiPas encore d'évaluation
- CC-Exos1 1011Document11 pagesCC-Exos1 1011Dabo100% (1)
- Chimie - Correction TP 02 - Solutions LectrolytiquesDocument2 pagesChimie - Correction TP 02 - Solutions Lectrolytiquesla physique selon le programme Français100% (3)
- Risa 3Document42 pagesRisa 3Sa Majesté David100% (2)
- Correction TDDocument5 pagesCorrection TDBasmã AlilechePas encore d'évaluation
- TP Potentio Corr PDFDocument4 pagesTP Potentio Corr PDFPS HadjerPas encore d'évaluation
- Expose Usto - Version 1Document8 pagesExpose Usto - Version 1riadPas encore d'évaluation
- TD 4,5 Et 6 PDFDocument5 pagesTD 4,5 Et 6 PDFessadikine anassPas encore d'évaluation
- TD - Chapitre 1Document6 pagesTD - Chapitre 1CharlesPas encore d'évaluation
- SMC4 - M22 - Christallographie - TD-Serie4 Et CorrigéDocument4 pagesSMC4 - M22 - Christallographie - TD-Serie4 Et Corrigéhéma tologiePas encore d'évaluation
- Chapitre III Champ CristallinDocument9 pagesChapitre III Champ Cristallinعبد الصمد بوالعيشPas encore d'évaluation
- TD N°3 Thermo L2-GP Modifiée 2023Document2 pagesTD N°3 Thermo L2-GP Modifiée 2023Clash of Clans Bilal DzPas encore d'évaluation
- Isom Conformation AliphatiqueDocument3 pagesIsom Conformation AliphatiqueSamba BarhamPas encore d'évaluation
- 3 Ato PDFDocument37 pages3 Ato PDFSamah SamahPas encore d'évaluation
- Lecomte Chap 2Document53 pagesLecomte Chap 2Achraf MoutaharPas encore d'évaluation
- Exercices de Chimie OrganométalliqueDocument5 pagesExercices de Chimie OrganométalliqueEddouks FatimazahraePas encore d'évaluation
- COMPOSE CxHyNzDocument2 pagesCOMPOSE CxHyNzmbi informatiquePas encore d'évaluation
- SMP S4 CG TD1 ElomariDocument3 pagesSMP S4 CG TD1 ElomariLamsaaf MohamedPas encore d'évaluation
- Chimie CinetiqueDocument33 pagesChimie CinetiqueomraamPas encore d'évaluation
- Les Diagrammes de Phases BinairesDocument67 pagesLes Diagrammes de Phases BinairesSimon Njoh100% (1)
- tp13 Cinetique Catalyse CorrigeDocument2 pagestp13 Cinetique Catalyse CorrigePR〇FESS〇R・MPas encore d'évaluation
- 2nd C - C9 Tests Didentification de Quelques IonsDocument8 pages2nd C - C9 Tests Didentification de Quelques IonsSoroPas encore d'évaluation
- Electromagnet I Que 6Document3 pagesElectromagnet I Que 6Malick DiopPas encore d'évaluation
- Corrigé TD Oxydoréduction Converti 1Document6 pagesCorrigé TD Oxydoréduction Converti 1kawtarPas encore d'évaluation
- Le Chrome: Manipulation 2Document11 pagesLe Chrome: Manipulation 2meknes aladabPas encore d'évaluation
- Exam Corrige 2016Document3 pagesExam Corrige 2016Gerardo Geusa100% (1)
- Cinetique 03Document3 pagesCinetique 03badrePas encore d'évaluation
- Introduction A La Science PolitiqueDocument8 pagesIntroduction A La Science PolitiqueAs NordinePas encore d'évaluation
- Radiocristallographie TP3Document5 pagesRadiocristallographie TP3يا سينPas encore d'évaluation
- Exemple de Calcul de Variance - ReponseDocument4 pagesExemple de Calcul de Variance - ReponseChikov ÆminePas encore d'évaluation
- Diagramme de FrostDocument19 pagesDiagramme de FrostmehdiPas encore d'évaluation
- Electrochimie ChafouDocument12 pagesElectrochimie ChafouSamah SoltanePas encore d'évaluation
- Ex QCM 2006Document13 pagesEx QCM 2006130660LYC OMAR BENABDELAZIZ NEDROMAPas encore d'évaluation
- TD Chapitre3 Corrige1Document34 pagesTD Chapitre3 Corrige1Niwir NikabouPas encore d'évaluation
- S2 Fi Gmqe Chimiedeselectrolytesp1 CM PDFDocument78 pagesS2 Fi Gmqe Chimiedeselectrolytesp1 CM PDFSaad ElfalahPas encore d'évaluation
- I Am Sharing 'Expose de Chimie 22' With YouDocument23 pagesI Am Sharing 'Expose de Chimie 22' With YouFatima zohra LakhdariPas encore d'évaluation
- TD4 4Document6 pagesTD4 4WIJDANEPas encore d'évaluation
- td1 Diagrammes Binaires mgf2 Caf2 CorrectionDocument2 pagestd1 Diagrammes Binaires mgf2 Caf2 CorrectionŘachida Lk100% (2)
- Ait Hssain TD Thermo Serie2 Cp2Document10 pagesAit Hssain TD Thermo Serie2 Cp2ASsmàâ IDPas encore d'évaluation
- Correction Problème Cristaux Métalliques - PDF Version 1Document3 pagesCorrection Problème Cristaux Métalliques - PDF Version 1SafaGratiPas encore d'évaluation
- Exos CH 05Document2 pagesExos CH 05lol testPas encore d'évaluation
- Binaire PiDocument9 pagesBinaire PiBasmã Alileche100% (1)
- Exercices d'intégrales de lignes, de surfaces et de volumesD'EverandExercices d'intégrales de lignes, de surfaces et de volumesPas encore d'évaluation
- Note de Calcul VRDDocument8 pagesNote de Calcul VRDAbdel Hakim M. NadjibPas encore d'évaluation
- Dimensio Step PtretraittDocument20 pagesDimensio Step PtretraittAbdel Hakim M. NadjibPas encore d'évaluation
- GeneralitesDocument2 pagesGeneralitesGhizlane HajjiPas encore d'évaluation
- PFE ENS Version Final - Impression PDFDocument75 pagesPFE ENS Version Final - Impression PDFAbdel Hakim M. Nadjib100% (1)
- Letravaildequipeefficacejour1Fin PDFDocument27 pagesLetravaildequipeefficacejour1Fin PDFassopapouPas encore d'évaluation
- Déchets Industriels PDFDocument38 pagesDéchets Industriels PDFAbdel Hakim M. Nadjib80% (5)
- Maroc Programme National Assainissement Liquide Epuration Eaux Usees FRDocument51 pagesMaroc Programme National Assainissement Liquide Epuration Eaux Usees FRAbdel Hakim M. Nadjib100% (1)
- Présentation Normes de QualitéDocument19 pagesPrésentation Normes de QualitéAbdel Hakim M. NadjibPas encore d'évaluation
- Etude D'impactDocument13 pagesEtude D'impactAbdel Hakim M. NadjibPas encore d'évaluation
- Partie 1 Complete PDFDocument72 pagesPartie 1 Complete PDFAbdel Hakim M. NadjibPas encore d'évaluation
- Réhabilitation de La Culture de La Betterave Sucrière en Algérie SommaireDocument17 pagesRéhabilitation de La Culture de La Betterave Sucrière en Algérie SommaireAbdel Hakim M. NadjibPas encore d'évaluation
- Chap 3Document12 pagesChap 3Abdel Hakim M. NadjibPas encore d'évaluation
- Partie 1 Complete PDFDocument72 pagesPartie 1 Complete PDFAbdel Hakim M. NadjibPas encore d'évaluation
- Partie 1 Complete PDFDocument72 pagesPartie 1 Complete PDFAbdel Hakim M. NadjibPas encore d'évaluation
- Réhabilitation de La Culture de La Betterave Sucrière en Algérie SommaireDocument17 pagesRéhabilitation de La Culture de La Betterave Sucrière en Algérie SommaireAbdel Hakim M. NadjibPas encore d'évaluation
- Analyses Des SolsDocument200 pagesAnalyses Des SolsAbdel Hakim M. Nadjib100% (1)
- AhbariDocument50 pagesAhbariNomade VoyageurPas encore d'évaluation
- 16 Nov David H - Bases Hydrogeologie PDFDocument25 pages16 Nov David H - Bases Hydrogeologie PDFAbdel Hakim M. NadjibPas encore d'évaluation
- Vocabulaire de L Environnement 2012-1Document21 pagesVocabulaire de L Environnement 2012-1Adil SaddikPas encore d'évaluation
- Chapitre 03. Le Diagnostic FinancierDocument6 pagesChapitre 03. Le Diagnostic FinancierAbdel Hakim M. Nadjib100% (1)
- Conf LambertDocument89 pagesConf LambertAbdel Hakim M. NadjibPas encore d'évaluation
- 07-Bassin Versant Routier 1 (Étude de Cas)Document13 pages07-Bassin Versant Routier 1 (Étude de Cas)Mouhcine MouhcinovichPas encore d'évaluation
- 2mepartiedusupport 150422054904 Conversion Gate01Document12 pages2mepartiedusupport 150422054904 Conversion Gate01Abdel Hakim M. NadjibPas encore d'évaluation
- 19-Bedj 2Document8 pages19-Bedj 2Abdou YahiPas encore d'évaluation
- Analyses Des EauxDocument91 pagesAnalyses Des EauxAbdel Hakim M. NadjibPas encore d'évaluation
- 7038 Didacticiel MensuraDocument11 pages7038 Didacticiel MensuraAbdel Hakim M. NadjibPas encore d'évaluation
- Les Bonn Moments de La VieDocument1 pageLes Bonn Moments de La VieAbdel Hakim M. NadjibPas encore d'évaluation
- Mem PFE PDFDocument95 pagesMem PFE PDFHicham BoutouchePas encore d'évaluation
- ALGODocument42 pagesALGOstrideworldPas encore d'évaluation
- Exam BCG FSTBMDocument2 pagesExam BCG FSTBMSamir Fassi FassiPas encore d'évaluation
- TDIII - 2021 2022 Partie1Document3 pagesTDIII - 2021 2022 Partie1KornichonPas encore d'évaluation
- Fluage Fbaguelin Jubile F. SchlosserDocument29 pagesFluage Fbaguelin Jubile F. SchlosserBenlala Aghiles AzzedinePas encore d'évaluation
- Fiche TD MecasolDocument9 pagesFiche TD MecasolFrank NguediaPas encore d'évaluation
- 3 Phy ELEVE-b Propagation D'une Onde LumineuseDocument6 pages3 Phy ELEVE-b Propagation D'une Onde Lumineuseabel profPas encore d'évaluation
- ! Séries D'exercices ! Sujets Corrigés ! Fiches Mémo: Edition BaldDocument59 pages! Séries D'exercices ! Sujets Corrigés ! Fiches Mémo: Edition BaldAminata PouyePas encore d'évaluation
- TP 1Document4 pagesTP 1Sęl Må75% (4)
- Airpur 81 SawerysynDocument10 pagesAirpur 81 SawerysynrafikrafikyPas encore d'évaluation
- Construction Metallique: Dahmani Lahlou Professeur À L'université Mouloud Mammeri de Tizi-OuzouDocument17 pagesConstruction Metallique: Dahmani Lahlou Professeur À L'université Mouloud Mammeri de Tizi-OuzoulhabsPas encore d'évaluation
- Exerxices CapacitifDocument8 pagesExerxices CapacitifFarah OûPas encore d'évaluation
- BOUYAHIAOUI Oussama KOUROUGHLI Mohamed Amin PDFDocument96 pagesBOUYAHIAOUI Oussama KOUROUGHLI Mohamed Amin PDFHhhh100% (2)
- Cadv - Pa - 2019 2Document31 pagesCadv - Pa - 2019 2Ilias ZeamariPas encore d'évaluation
- Caract Pet PBTDocument67 pagesCaract Pet PBTguetardPas encore d'évaluation
- Règlementation Energétique Au MarocDocument46 pagesRèglementation Energétique Au MarocelkhaldyPas encore d'évaluation
- Utilisation de La Compensation Série Avancée Dans Les Réseaux ÉlectriquesDocument85 pagesUtilisation de La Compensation Série Avancée Dans Les Réseaux Électriquesrahimoetl92% (13)
- Système ThermodynamiqueDocument6 pagesSystème ThermodynamiqueAymene MiringuiPas encore d'évaluation
- 4sc-dc2-1 (3 Files Merged)Document8 pages4sc-dc2-1 (3 Files Merged)Ahmed benabdelkaderPas encore d'évaluation
- Les Ondes Lumineuse: National Polytechnic School of ConstantineDocument12 pagesLes Ondes Lumineuse: National Polytechnic School of ConstantineSamah BoughanemPas encore d'évaluation
- Page Machines E5Document4 pagesPage Machines E5tresorkaomba1Pas encore d'évaluation
- Rapport FM Final PDFDocument32 pagesRapport FM Final PDFAbdo hoda100% (2)
- Projet de Département Géosciences Et Génie CivilDocument14 pagesProjet de Département Géosciences Et Génie CivilOmar Rodriguez del VillarrealPas encore d'évaluation
- Electrocinetique Filtres PDFDocument6 pagesElectrocinetique Filtres PDFSiraj ChahbounPas encore d'évaluation
- Clefs: Les Énergies Les ÉnergiesDocument108 pagesClefs: Les Énergies Les Énergiesguglu doljno bit pohPas encore d'évaluation
- 03 Complexes Complements ExosDocument5 pages03 Complexes Complements ExosBourama DjirePas encore d'évaluation
- PenetronDocument2 pagesPenetronyoussefPas encore d'évaluation
- TC 13 Serie1generalitesfonctionsDocument1 pageTC 13 Serie1generalitesfonctionsMed Amine LagrainePas encore d'évaluation
- °td-Examens Optique-Geo FSM 2020 SMPCDocument36 pages°td-Examens Optique-Geo FSM 2020 SMPCBakary KeitaPas encore d'évaluation