Académique Documents
Professionnel Documents
Culture Documents
Facteurs Influençant Le Stress Oxydatif. Stress Oxydatif
Transféré par
Jean-Loïc BauchetTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Facteurs Influençant Le Stress Oxydatif. Stress Oxydatif
Transféré par
Jean-Loïc BauchetDroits d'auteur :
Formats disponibles
Stress Oxydatif
Le stress oxydant se définit comme l’incapacité de l’organisme de se défendre contre les
espèces réactives de l’oxygène ERO en raison de la perturbation d’équilibre endogène entre
ces derniers et les agents oxydants AO. Ce déséquilibre conduit potentiellement à des
dégâts structuraux et fonctionnels.
Les ERO sont des espèces chimiques oxygénées tels que les radicaux libres ions oxygénés,
peroxydes, rendues chimiquement très réactives par la présence d’électrons de valence non
appariés dans l’orbitale la plus externe. L’équilibre est rétabli soit par oxydation (perte de
cet é libre) ou par réduction (gain d’un autre é). Le caractère radicalaire de la molécule ne
disparait pas, l’électron libre peut passer sur d’autres molécules ; c’est le phénomène
d’oxydation en chaine.
Sommaire
1 Facteurs influençant le stress oxydatif
2 Étude des espèces réactives produites lors du stress oxydatif
2.1 Propriétés
2.2 Mécanisme de génération des ERO
2.3 Formation des radicaux libres
3 Toxicité des ERO
4 Les espèces réactives de l’azote
5 Source des espèces réactives
6 Les moyens de lutte contre le stress oxydatif
7 Quantification des ERO
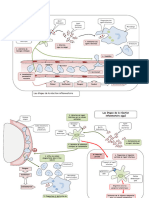
Facteurs influençant le stress oxydatif
Facteurs augmentant la production des ROS : exemple : consommation élevée
d’O2 (activité sportive intense) avec dépenses énergétiques.
Facteurs réduisant les capacités antioxydantes : exemple : déficit enzymatique
congénital (G6PD)
Analytical Toxicology - Stress Oxydatif | 1
Stress Oxydatif
Étude des espèces réactives produites lors du stress
oxydatif
Propriétés
Les ERO sont des espèces électrophiles de courte durée de vie (ns), elles font partie des
systèmes ubiquitaires ayant une réactivité chimique délétère à l’égard des biomolécules,
cette réactivité est inversement proportionnelle au pouvoir oxydant (OH° > RO° > HOO° >
ROO°).
Mécanisme de génération des ERO
Au niveau de la respiration mitochondriale : lors de l’inhibition du transfert d’électron par
découplage de la phosphorylation oxydative.
Modification du potentiel REDOX favorisant l’auto-oxydation des biomolécules.
Exacerbation des phénomènes inflammatoires, et augmentation du taux du Fe libre et
autres métaux de transition.
Bioactivation lors de processus de biotransformation (Formation des RO°), induction des
NOS (Oxyde nitrique synthétase) I, II, III ; Stimulation des oxydases (NOX, MAO, XO)
Formation des radicaux libres
>> Par Scission
Scission homolytique de la liaison covalente
Scission hétérolytique
>> Par dismutation
Réduction monoélectronique :
Analytical Toxicology - Stress Oxydatif | 2
Stress Oxydatif
1.
Oxydation monoélectronique :
1.
Les espèces réactives d’O2 (ROS)
1 *- *
Oxygène singlet O2, anion superoxyde O2 , peroxyde d’hydrogène, radical hydroxyle OH,
l’ozone O3.
Toxicité des ERO
Dommage oxydatifs lipidiques : principalement par peroxydation lipidique : ensemble
des phénomènes oxydatifs non spécifiques des lipides (oxydation non enzymatique). Cibles :
constituants membranaire (acides gras poly insaturés) lipides circulants (lipoprotéines –
Cholestérol libre).
Dommage oxydatifs protéiques : cible : les acides aminés (surtout soufrés (Cystéine)
aromatique (Histidine), les protéines les plus sensibles étant celles qui ont le plus de
groupements sulfhydrile SH.
Deux modes d’action : direct : cible les chaines peptidiques et les chaines latérales. Le
mode indirect essentiellement par glycation (formation de groupement carbonyle) ou par
lipooxydation (formation de bases de Schiff + adduits de Michael).
Dommage oxydatifs de l’ADN : cible : ADN mitochondrial/nucléaire.
Le *OH généré par H2O2 et O2*- est directement responsable de diverses altérations de l’ADN.
Analytical Toxicology - Stress Oxydatif | 3
Stress Oxydatif
Les espèces réactives de l’azote
NO* et ses dérivés : l’anhydride nitreux N2O3, l’ion peroxynitrite (ONOO–).
NO* : la réaction est catalysée par la NOS mitochondriale, implique un atome d’azote de la
L-Arginine et une O2. Ce radical est peu réactif et diffusible dans les milieux biologiques. Il
peut être cependant oxydé en ion nitrosonium NO+ ou réduit en ion nitroxyle NO+.
Rôle : les ERN interviennent essentiellement dans le processus de coagulation sanguine,
ceux sont des vasodilatateurs (cardiovasculaires), responsables d’une relaxation des cellules
musculaires lisses. Sur le plan neurologique, sont impliqués dans la neurotransmission et la
plasticité neuronale ; immunologique, signalisation intra et intercellulaire, dans l’apoptose,
et les mécanismes de défenses, physiologique, maintien de l’intégrité muqueuse gastro-
intestinale.
Toxicité :
NO* > ions nitrites (NO2–) il peut aussi fixer un groupement nitroxyle sur les acides aminés,
comme la tyrosine, pour générer la nitrotyrosine. En présence d’un excès de NO•, on parle
de « stress nitrant ».
La réaction de NO• avec l’•O2 – entraîne la formation de l’ion peroxynitrite (ONOO–) qui est
considéré (espèce réactive de l’azote & de l’oxygène). La protonation en acide peroxynitreux
(ONOOH) donne une espèce très oxydante.
L’autooxydation du NO• par O2 est à l’origine de la formation d’anhydride nitreux, le N2O3.
Ainsi, chaque ERN possède une réactivité qui lui est propre et peut agir sur divers
constituants cellulaires.
Source des espèces réactives
La chaine respiratoire mitochondriale : formation de trois espèces radicalaires O2*-,
OH*, H2O2 : sources majeures : Complexe I (NADH-ubiquinone réductase) & Complexe
III (Ubiquinone-cytochrome C réductase)
Enzymes inflammatoires :
NADPH oxydase (ubiquitaire) au cours de la phagocytose, cette enzyme est
capable de réduire l’O2 en O2*
Analytical Toxicology - Stress Oxydatif | 4
Stress Oxydatif
NO synthétase (I, II, III, m)
MPO (myéloperoxydase) : à l’intérieur de la vacuole phagocytaire, l’anion
superoxyde est dismuté en péroxyde d’hydrogène qui se transforme en acide
hypochloreux sous l’action de la myeloperoxydase.
Systèmes des Cyt P450 : surtout CYP2E1+++ : l’autooxydation du Cyt P450 (FeII)
en Cyt P450 (FeIII) entraine une réduction de l’O2 en O2-*.
Autres sources enzymatiques : MAO (monoamine réductase et H2O2)
Sources non enzymatiques : auto-oxydation de l’adrénaline, dopamine, flavines,
hydroquinone, hémoglobine à O2-*, H2O2, *OH
Les moyens de lutte contre le stress oxydatif
Les antioxydants : toute substance qui, présente à faible concentration par rapport au
substrat oxydable, est capable de ralentir ou inhiber l’oxydation de ce dernier.
Les antioxydants enzymatiques : 1ère ligne de défense principalement représentée par :
Superoxyde dismutase (SOD) métalloenzyme ubiquitaire (élimine l’anion superoxyde
par dismutation)
Catalase: Enzyme héminique ubiquitaire (GR+++) (élimine H2O2 par dismutation)
Système Glutathion peroxydase / Glutathion réductase (GPx/GR) sélénoprotéine
ubiquitaire (7 isoformes) (élimine 70% des proxydes organique et 94% de H2O2 par
réduction)
Thiorédoxines peroxydases (Trx): sélénoenzymes NADPH dépendante (élimine
H2O2, ROOH, ONOO–) par réduction.
Les antioxydants non enzymatiques :
Vitamine E: sous forme α-tocophérol (la plus active et la plus absorbée) antioxydant
majeur des structures lipidiques – autre action ; neutralisation 1O2
Vitamine C : acide ascorbique : agent réducteur et chélateur sous forme d’acide
déhydro-L-ascorbique (DHA) réagit directement sur les radicaux libres et élimine H2O2.
Provitamine A (caroténoïdes) : β-carotène : précurseur de la vitamine A
(interruption du processus de la peroxydation lipidique)
Analytical Toxicology - Stress Oxydatif | 5
Stress Oxydatif
Autres vitamines : Vitamine P (flavonoïdes), Coenzyme Q10
Les oligoéléments : Se, Zn comme cofacteurs GPx, SOD1, SOD3 respectivement
Protéines transporteuses : par séquestration des métaux impliqués dans la
génération des ERO (transferrine Fe).
Glutathion : comme cofacteur d’enzyme (GPx)
Autres mécanismes : réparation de l’ADN
Ceci en cas d’insuffisance ou de défaillance des systèmes antioxydants précédents. La
réparation de l’ADN prévient les risques de mutagenèse (cancers).
Agents toxiques et production endogène des ERO
Chimiques : Métaux (As), Solvant(CCl4), médicament (Paracétamol)
Physiques : radiations ionisantes, rayonnement UV
Dans certaines pathologies le stress oxydatif peut être une cause primordiale (cancers), ou
bien facteur déclenchant (Maladie d’Alzheimer), d’autres peuvent être la cause secondaire
du stress oxydatif (Diabète).
Quantification des ERO
Par mesure directe : (Chimiluminescence, résonance paramagnétique électronique)
Par mesure indirecte : (marqueurs immuno-histochimiques)
Quantification des marqueurs d’oxydation
Marqueurs d’oxydation lipidiques (Ac anti-LDL oxydés)
Marqueurs d’oxydation protéiques : principalement par dosage des protéines
carbonylées
Analytical Toxicology - Stress Oxydatif | 6
Vous aimerez peut-être aussi
- Herboristerie FamilialeDocument103 pagesHerboristerie Familialevilic93100% (1)
- Le Taux Vibratoire PDFDocument15 pagesLe Taux Vibratoire PDFLuca TascaPas encore d'évaluation
- Les Radicaux Libres Et OxygeneDocument10 pagesLes Radicaux Libres Et OxygeneLamia BOUSSADI100% (1)
- Acides AminesDocument11 pagesAcides Aminesislmioun100% (1)
- Les Champs MorphogenetiquesDocument12 pagesLes Champs MorphogenetiquesAnna Hamieux100% (2)
- Perle Martin - Le Lapacho, Arbre de Vie ...Document200 pagesPerle Martin - Le Lapacho, Arbre de Vie ...Nunusse100% (1)
- PURE SANTE-10decouvertesDocument28 pagesPURE SANTE-10decouvertesjean-loïcPas encore d'évaluation
- Le Message Du DR Paul CartonDocument49 pagesLe Message Du DR Paul Cartonalvarez-duran.jesus6752Pas encore d'évaluation
- Naturopathie et nutrition: Comment se nourrir pour une santé optimaleD'EverandNaturopathie et nutrition: Comment se nourrir pour une santé optimalePas encore d'évaluation
- 11-Structure Et Fonction Des ACIDES AMINESDocument55 pages11-Structure Et Fonction Des ACIDES AMINESBook Hunter100% (2)
- Stress Oxydant, RMLG, 2007Document11 pagesStress Oxydant, RMLG, 2007Abdou SAMBAPas encore d'évaluation
- HLA I Et II Cours de Médecine InterneDocument36 pagesHLA I Et II Cours de Médecine InterneAhmed Dbb100% (1)
- Cerveau p17Document15 pagesCerveau p17Betschbel Dorcé100% (1)
- Secretion PancreatiqueDocument15 pagesSecretion PancreatiqueZahia ArichaPas encore d'évaluation
- Physiologie Du ColonDocument33 pagesPhysiologie Du Colonyaya camaraPas encore d'évaluation
- PhytothérapieDocument134 pagesPhytothérapiealexandre FRANKEPas encore d'évaluation
- Le Grand Œuvre AlchimiqueDocument14 pagesLe Grand Œuvre Alchimiqueepoptae100% (1)
- Radicaux Libres PDFDocument21 pagesRadicaux Libres PDFAude Kouakou100% (1)
- Dossier Pour La Science N°3 - 1994-04..06 - La Génétique HumaineDocument128 pagesDossier Pour La Science N°3 - 1994-04..06 - La Génétique HumaineDaniel CaillouxgratosPas encore d'évaluation
- Les Radicaux LibresDocument4 pagesLes Radicaux Libresxol13rdm100% (1)
- DS Cancer Du Sein 978 3 9524915 9 1Document112 pagesDS Cancer Du Sein 978 3 9524915 9 1jm griveauPas encore d'évaluation
- CortisolDocument25 pagesCortisolStefaniaPas encore d'évaluation
- Pharmacognosie Phytochimie Plantes Medicinales 5e Ed - SommaireDocument16 pagesPharmacognosie Phytochimie Plantes Medicinales 5e Ed - SommaireNarcisse-Nathaniel KLOUSSEH50% (2)
- Brochure Pancreas PDFDocument38 pagesBrochure Pancreas PDFAnis S100% (1)
- Bioelectronique - Vincent U. Schreier PDFDocument5 pagesBioelectronique - Vincent U. Schreier PDFjoel_tetard100% (1)
- Médecine 14 Encyclopédie Des Vitamines Et Des Sels Minéraux 2021 07 23Document210 pagesMédecine 14 Encyclopédie Des Vitamines Et Des Sels Minéraux 2021 07 23didier ramatisPas encore d'évaluation
- Chapitre II Expression Des Gènes (Transcription Et Traduction) Leur RégulationDocument9 pagesChapitre II Expression Des Gènes (Transcription Et Traduction) Leur Régulationsolo gamer50% (2)
- Stres Oxydatif Et MNDDocument47 pagesStres Oxydatif Et MNDJoel AmaniPas encore d'évaluation
- Corrigé Du Sujet Bac SVT 2015Document8 pagesCorrigé Du Sujet Bac SVT 2015CourSCiences100% (2)
- Bioresonance EntretienDocument3 pagesBioresonance EntretiengarcialepersPas encore d'évaluation
- Biologie Del ComportementDocument38 pagesBiologie Del ComportementLuis Antonio Buitron RamirezPas encore d'évaluation
- Lithiase VésiculaireDocument35 pagesLithiase Vésiculairehaj khlifa saraPas encore d'évaluation
- 1.la MitochondrieDocument39 pages1.la MitochondrieAB AbPas encore d'évaluation
- Modélisation Moléculaire Cours 2021Document120 pagesModélisation Moléculaire Cours 2021CHEIKH ABDOUL AZIZ H'MEIDYPas encore d'évaluation
- Electro AcupunctureDocument13 pagesElectro AcupunctureCarlos MoreiraPas encore d'évaluation
- Couleurs TaoDocument6 pagesCouleurs TaoGérard EddePas encore d'évaluation
- 1-Ration AlimemtaireDocument24 pages1-Ration AlimemtaireIslęm OuaribPas encore d'évaluation
- Acides AminésDocument8 pagesAcides Aminésami190Pas encore d'évaluation
- TP N° 2 - La Masse Moléculaire - PDFDocument9 pagesTP N° 2 - La Masse Moléculaire - PDFKarim Kisserli100% (1)
- Sante Mag 51Document52 pagesSante Mag 51Cherraben Taha Amine100% (1)
- Bioélectronique Et Quantification de La QualitéDocument17 pagesBioélectronique Et Quantification de La QualitéNapoleon Gonzalez Gil100% (1)
- Chapitre AntioxydantDocument14 pagesChapitre AntioxydantKheira Louiza Bekaddouri100% (1)
- Espèces Réactives de L'oxygène (ROS)Document6 pagesEspèces Réactives de L'oxygène (ROS)Jérèm Bon-BétempsPas encore d'évaluation
- Cours Neurotoxicité HadjerDocument80 pagesCours Neurotoxicité HadjerIkram Hamache100% (1)
- EaupusculeDocument220 pagesEaupusculecourtoiPas encore d'évaluation
- Vitamines Et CoenzymesDocument16 pagesVitamines Et CoenzymesMial Naval RajaofaraPas encore d'évaluation
- Comment Utiliser Oscilloscope PDFDocument2 pagesComment Utiliser Oscilloscope PDFSarah0% (2)
- Aspects Cliniques Et Thérapeutiques de La Maladie de ParkinsonDocument26 pagesAspects Cliniques Et Thérapeutiques de La Maladie de ParkinsonaissaPas encore d'évaluation
- Extrait Genetique Moleculaire Des PlantesDocument5 pagesExtrait Genetique Moleculaire Des Plantesdjaouad bourouaisPas encore d'évaluation
- Photon TechnologiesDocument39 pagesPhoton Technologiesdigital2000100% (1)
- GLUTATHIONDocument11 pagesGLUTATHIONgarcialepersPas encore d'évaluation
- Les MitochondriesDocument40 pagesLes MitochondriesRuth KoudPas encore d'évaluation
- Introduction À La Biologie Cellulaire 1Document6 pagesIntroduction À La Biologie Cellulaire 1fouad abdelhamidPas encore d'évaluation
- Dioxyde de Soufre1Document54 pagesDioxyde de Soufre1Ala Eddine MarzouguiPas encore d'évaluation
- EndocrinotoxicitéDocument82 pagesEndocrinotoxicitéKhaoula Kouloughli100% (1)
- BIOCHIMIEDocument46 pagesBIOCHIMIEdht2ts9zw9Pas encore d'évaluation
- Alimentation Et Carie DentaireDocument45 pagesAlimentation Et Carie Dentaireelloumimalak01Pas encore d'évaluation
- Tissus ConjonctifsDocument33 pagesTissus ConjonctifsAmïn FïlalïPas encore d'évaluation
- Parasites Internes ChiensDocument1 pageParasites Internes Chiensnicolas_salayaPas encore d'évaluation
- Équilibre AlimentaireDocument32 pagesÉquilibre AlimentaireFati2021 FatiPas encore d'évaluation
- Cours - L'eau Entre Abondance Et RareteDocument5 pagesCours - L'eau Entre Abondance Et Rareteapi-3719426100% (3)
- Partie 2 - Alimentation Et Environnement.Document5 pagesPartie 2 - Alimentation Et Environnement.salimo kitaPas encore d'évaluation
- Ecole Hahnemannienne de Fréjus ST RaphaelDocument1 pageEcole Hahnemannienne de Fréjus ST RaphaelJhonSeaPas encore d'évaluation
- ScientologieDocument12 pagesScientologiemichelargouet100% (1)
- Aliments Et Education Alimentaire Cours MaDocument9 pagesAliments Et Education Alimentaire Cours MaImanePas encore d'évaluation
- Métabolisme Et BioénergétiqueDocument21 pagesMétabolisme Et BioénergétiqueRihab MaachouPas encore d'évaluation
- Doctorat BOUSBIA - Nabil PDFDocument176 pagesDoctorat BOUSBIA - Nabil PDFSamir MazafranPas encore d'évaluation
- AlimentationDocument1 pageAlimentationhamada2002Pas encore d'évaluation
- Le Dernier Defi de La Physique Moderne PDocument37 pagesLe Dernier Defi de La Physique Moderne PJean-Loïc BauchetPas encore d'évaluation
- Vortex Instructions 1Document15 pagesVortex Instructions 1Anonymous xFDpeji3HWPas encore d'évaluation
- L Eau Et Le Principe de VieDocument39 pagesL Eau Et Le Principe de VieJean-Loïc BauchetPas encore d'évaluation
- DigestionDocument15 pagesDigestionkenniaevelynsullcabePas encore d'évaluation
- L Ensemble Arc-En-CielDocument35 pagesL Ensemble Arc-En-CielJean-Loïc BauchetPas encore d'évaluation
- Le PH 1. Lautoprotolyse de Leau - 2014Document6 pagesLe PH 1. Lautoprotolyse de Leau - 2014MouadBastaouiPas encore d'évaluation
- La Notion de Terrain BiologiqueDocument2 pagesLa Notion de Terrain BiologiqueJean-Loïc BauchetPas encore d'évaluation
- Les Étapes de La Réaction InflammatoireDocument6 pagesLes Étapes de La Réaction InflammatoireJean-Loïc BauchetPas encore d'évaluation
- Kit de DynamisationDocument2 pagesKit de DynamisationJean-Loïc BauchetPas encore d'évaluation
- La Mort Par La MedecineDocument10 pagesLa Mort Par La MedecineJean-Loïc BauchetPas encore d'évaluation
- Élément OxygeneDocument38 pagesÉlément OxygeneJean-Loïc BauchetPas encore d'évaluation
- Gerson KelleyDocument52 pagesGerson KelleyAssia Oumou MohamedPas encore d'évaluation
- Index Phytotherapie PDFDocument20 pagesIndex Phytotherapie PDFeforgues564100% (1)
- Heureux Chaque JourDocument111 pagesHeureux Chaque JourcenderillastoryPas encore d'évaluation
- Initiation À La Spagyrie Et Aux Médecines AlchimiquesDocument11 pagesInitiation À La Spagyrie Et Aux Médecines Alchimiquesphilosophe662511Pas encore d'évaluation
- EndofDocument7 pagesEndofOusmanePas encore d'évaluation
- HYDROGENE PDF OK Effets Bénéfiques - GEOENERGIES PagesDocument11 pagesHYDROGENE PDF OK Effets Bénéfiques - GEOENERGIES PagesJean-Loïc BauchetPas encore d'évaluation
- Grecs 4 ElementsDocument7 pagesGrecs 4 ElementsJean-Loïc BauchetPas encore d'évaluation
- Equilibre-Acide-Base VIDocument33 pagesEquilibre-Acide-Base VIANDRIANOME tafitaPas encore d'évaluation
- Fleurs de Bach PDFDocument38 pagesFleurs de Bach PDFNulli TasPas encore d'évaluation
- DavenportDocument28 pagesDavenportCheick SANOUPas encore d'évaluation
- Élément OxygeneDocument38 pagesÉlément OxygeneJean-Loïc BauchetPas encore d'évaluation
- EFFETS TAMPONS RÉGULATION DU PHDocument26 pagesEFFETS TAMPONS RÉGULATION DU PHJean-Loïc BauchetPas encore d'évaluation
- Cours D'immunologie Partie 2 Fév23Document16 pagesCours D'immunologie Partie 2 Fév23abdou2004trPas encore d'évaluation
- Cours SVT SpéDocument2 pagesCours SVT SpéMariama SIDIBEPas encore d'évaluation
- 1 - lES ORGANES LYMPHOIDESDocument5 pages1 - lES ORGANES LYMPHOIDESSaibiPas encore d'évaluation
- Biology Part 4Document49 pagesBiology Part 4AMR IzzaPas encore d'évaluation
- Embryo23 03-GametogeneseDocument9 pagesEmbryo23 03-GametogeneseChouaib MeraoumiaPas encore d'évaluation
- CR1122101254Document2 pagesCR1122101254ابراهيم سويسيPas encore d'évaluation
- Comment L'organisation Extracellulaire Assure-T-Elle La Cohésion Tissulaire ?Document2 pagesComment L'organisation Extracellulaire Assure-T-Elle La Cohésion Tissulaire ?Capucine MasiPas encore d'évaluation
- Chez Les Végétaux: Mais Quand Il y A Un Problème Avec La Température Ou Le Soi-Disant Le Stresse ThermiqueDocument11 pagesChez Les Végétaux: Mais Quand Il y A Un Problème Avec La Température Ou Le Soi-Disant Le Stresse ThermiqueNasro NaserddinPas encore d'évaluation
- Fiche de TD1 2016 2017-1Document3 pagesFiche de TD1 2016 2017-1Berthe Aristide Ngue Nkongo100% (3)
- Totipotence Chez Le VegetalDocument22 pagesTotipotence Chez Le Vegetalbasillaiscelestin1Pas encore d'évaluation
- Immunité Anti-Tumorale Et Thérapies Cellulaires Du Cancer: M/S: Médecine SciencesDocument12 pagesImmunité Anti-Tumorale Et Thérapies Cellulaires Du Cancer: M/S: Médecine SciencesFeriel KrelilPas encore d'évaluation
- Corrigé La Maturation Du Systeme Immunitaire en 3 Points.Document4 pagesCorrigé La Maturation Du Systeme Immunitaire en 3 Points.kilm. gujo.Pas encore d'évaluation
- SVT-Bac SVTF-NORMAL 2021Document8 pagesSVT-Bac SVTF-NORMAL 2021Adnane AhadafPas encore d'évaluation
- Examen Blanc 2014 CorrectionDocument9 pagesExamen Blanc 2014 CorrectionLorenz MeurrensPas encore d'évaluation
- 4 - BDR - Physiologie, Régulation Et Signalisation de L'axe Gonadotrope Masculin (Partie 1)Document26 pages4 - BDR - Physiologie, Régulation Et Signalisation de L'axe Gonadotrope Masculin (Partie 1)Hay LinPas encore d'évaluation
- CHAP1 PV Chap5 Nutrition MinéraleDocument4 pagesCHAP1 PV Chap5 Nutrition MinéraleSagacious IvejutenPas encore d'évaluation
- Examen Final de Biologie Moleculaire 2022 - 2023.Document6 pagesExamen Final de Biologie Moleculaire 2022 - 2023.s.lakhloufi5682Pas encore d'évaluation
- PreparationDocument14 pagesPreparationYoucef TelmaniPas encore d'évaluation
- Module CelluleDocument51 pagesModule CelluleAbdellah EL AnsariPas encore d'évaluation
- Tissu NerveuxDocument6 pagesTissu NerveuxOussama FendaliPas encore d'évaluation
- ANA FA FRDocument12 pagesANA FA FRMichel LeundjieuePas encore d'évaluation
- (Bact Viro) (Spé Gen)Document198 pages(Bact Viro) (Spé Gen)Aymane AlaouiPas encore d'évaluation
- L1 BPC Part 1 Cel Excitables VVW v2-8 Light CM1Document29 pagesL1 BPC Part 1 Cel Excitables VVW v2-8 Light CM1remi.giryPas encore d'évaluation
- Corrig Bac 2011 SC Exp ContrleDocument3 pagesCorrig Bac 2011 SC Exp Contrlele sage67% (3)
- Systeme Immunitaire CutaneDocument7 pagesSysteme Immunitaire CutaneSébastien ANTOINEPas encore d'évaluation
- Embryologie S1 2014 2015 1Document27 pagesEmbryologie S1 2014 2015 1L'enfant SucréPas encore d'évaluation
- EndocytoseDocument15 pagesEndocytosek.aitaliPas encore d'évaluation