Académique Documents
Professionnel Documents
Culture Documents
Fiche LT
Transféré par
requiemforathrowawayTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Fiche LT
Transféré par
requiemforathrowawayDroits d'auteur :
Formats disponibles
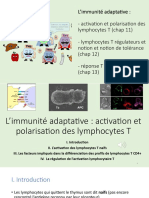
Activation et différenciation fonctionnelle des lymphocytes T
1. TCR alphabeta : structure et diversité des ligands
Il existe deux types de lymphocytes T. On se concentre ici sur les lymphocytes T alphabeta.
Le TCR est constitué de deux chaînes alpha et beta ancrées dans la membrane plasmique.
Chaque chaîne possède deux domaines extracellulaires :
- Un domaine constant C
- Un domaine variable V
Le TCR s’associent à 6 protéines CD3 par des liaisons ioniques et qui sont 6 chaînes de
transduction du signal. Le TCR est spécifique d’un antigène et le CD3 sert à traduire le
signal d’activation. Le domaine V de la chaîne alpha possède trois sous-domaines
hypervariables CDR (complimentary determining regions).
Malgré une grande spécificité, il peut se produire une reconnaissance dégénérée :
- Alloréactivité : reconnaissance des CMH du non-soi avec des peptides du non-soi.
Cela se produit lorsqu’il y a une ressemblance du CMH étranger avec son complexe
nominal.
Environ 10% des lymphocytes T sont capables d’alloréactivité qui est responsable
du rejet de greffe entre individus non apparentés. Seulement 10% en sont capables
car peu de complexe allogéniques ressemblent à des complexe nominaux dans la
nature.
- Réactions croisées : les réactions croisées ont lieu entre un complexe CMH du soi-
peptide viral et un complexe CMH du soi-peptide du soi.
Elles sont à l’origine de maladies auto-immunes.
2. Présentation des Ag aux lymphocytes T alphabeta
Lorsqu’un tissu est infecté, les Ag parviennent aux ganglions lymphatiques par les
vaisseaux lymphatiques. Ils y rencontrent les lymphocytes naïfs qui viennent de la
circulation sanguine qu’ils ont rejoint par le canal thoracique.
Les lymphocytes arrivent dans les ganglions par des veinules postcapillaires au niveau du
paracortex.
Etapes de la migration dans le ganglion :
- Roulement : interactions LT (L-sélectine) - cellules endothéliales (CD34)
réversibles qui entraînent un roulement sur la surface
- Activation : activation de l’intégrine LFA-1 des LT par les chémokines localisées
sur la surface endothéliale
- Arrêt/adhésion : changement de conformation de LFA-1 conduisant à une forte
adhésion avec ICAM-1 et arrêt du LT
- Migration transendothéliale : attirance par les chémokines produites dans l’OL
et passage à travers la paroi du vaisseau
Les cellules dendritiques sont capables d’activer des LT naïfs.
Les DC immatures dans les tissus sont phagocytiques et endocytiques : s’il y a infection
elles vont capturer les antigènes. Les DC immatures reconnaissent les signaux de danger
associés aux pathogènes ingérés (PAMP pour pathogen-associated molecular pattern)
grâce à leurs récepteurs de reconnaissance de motifs moléculaires (PRR pour pattern
recognition receptors).
Après maturation, les DC changent de morphologie (plus de surface d’échange) et migrent
dans les OLS pour présenter les antigènes aux LT.
Caractéristiques des DC matures :
- Nombreuses dendrites
- Migration dans les OLS après capture des Ag
- Expression durable de fortes densités de complexes CMH-peptide
- Expression de fortes densités des molécules de costimulation B7
- Sécrétion de chimiokines
3. Conditions de l’activation des lymphocytes T : costimulation, anergie,
rétrocontrôle
Un lymphocyte T naïf s’active en recevant 2 signaux donnés par une CPA. Il s’agit :
- Du signal antigénique (CD3/CMH, LFA-1/IMCA-1, CD2/LFA-3). Le peptide
antigénique est présenté au TCR des lymphocytes T.
- Du signal de costimulation (aussi appelé signal de danger). Le signal de
costimulation est reçu par la protéine CD28 présente à la surface du lymphocyte T
lorsqu’elle se lie à ses ligands CD80 (B7-1) et CD86 (B7-2), eux-mêmes présents à
la surface des CPA. L’expression de CD80 et CD86 est induite en surface de la CPA
en cas d’inflammation et/ ou en présence de molécules microbiennes, c’est
pourquoi leur expression est synonyme de danger pour l’organisme.
En dehors de ces situations, CTLA-4 a plus d’affinité pour B7 que CD28 et induit
l’inhibition plutôt que la stimulation de la réponse. Les lymphocytes T qui reconnaissent
l’antigène sans recevoir ce signal de costimulation entrent en anergie (mécanisme majeur
du maintien de la tolérance au soi), et sont donc incapables de s’activer et de proliférer. À
la suite de ces signaux, les lymphocytes T s’activent, prolifèrent et se différencient.
4. Conséquences de l’activation
4.1. Prolifération clonale
L’interleukine 2 (IL-2) est une cytokine sécrétée par les LT qui joue un rôle de médiation
du système immunitaire par la promotion des cellules T régulatrices qui limitent l’action
des cellules T effectrices. IL-2 promeut également la différenciation entre LT effecteurs et
LT mémoires, ainsi que la différenciation en LT helper. Elle permet d’éviter certaines
dérives auto-immunitaires. Pour tout cela, IL-2 se lie à IL-2R qui est le récepteur d’IL-2
sur les LT.
4.2. Différenciation fonctionnelle et fonctions majeures des LT CD8+
Dans ce modèle, une augmentation de calcium intracellulaire induit une exocytose au
cours de laquelle les granules fusionnent avec la membrane du CTL (cytotoxic T
lymphocyte) et libèrent de la perforine monomérique dans le petit espace entre les deux
cellules. Les monomères de perforine vont changer de conformation ce qui leur permet
de s’insérer dans la membrane de la cible. Toujours en présence de calcium, les
monomères se polymérisent avec la membrane formant des pores cylindriques. Cela fait
passer les granzymes dans la cible pour aller détruire l’ADN. En même temps, le ligand
FAS se lie à au récepteur de mort FAS qui change de conformation et recrute FADD par
l’intermédiaire de son DD. FADD recrute ensuite des caspases initiatrices qui vont induire
l’apoptose de la cellule.
4.3. Différenciations fonctionnelles et fonctions majeures des LT CD4+
4.3.1. Différenciation des LT CD4 en LT CD4 Th1
Les LT CD4 Th1 expriment des molécules de surface adaptées à la migration de l’OLS dans
le foyer infectieux. Ils sont capables de sécréter des cytokines (TNF-alpha, IL-2, IFN-
gamma, etc.). Les LT CD4 Th1 sécrètent des IL-2 qui leur permettent de proliférer mais
qui vont également se lier aux récepteurs IL-2R des CTL activés pour les aider à proliférer.
Ils vont également activer les macrophages dans le foyer infectieux. Ils reconnaissent leur
Ag sur le macrophage et sécrètent des IFN-gamma ainsi que des TNF-beta qui vont activer
le macrophage.
4.3.2. Différenciation des LT CD4 en LT CD4 Th2
Les LT CD4 Th2 réactivent les LB spécifiques du même Ag dans l’OLS. Ils sont capables de
sécréter des cytokines (IL-4, IL-5, IL-13, …) et expriment des molécules de surface CD40L.
Les LB vont être activés par les Th2 via les interactions CD40/CD40L
4.4. Différenciation des LT mémoires
Les LT mémoires ont une spécialisation similaire à celle des effecteurs (cytotoxiques, Th1,
Th2). Ils expriment des molécules à la surface de leur membrane qui leur permettent de
recirculer dans l’organisme et ont une longue durée de vie.
4.5. Homéostasie des lymphocytes T
Vous aimerez peut-être aussi
- Chapitre III - 1 - Activation Des Lymphocytes TDocument12 pagesChapitre III - 1 - Activation Des Lymphocytes TFatima BENHAFSSAPas encore d'évaluation
- Activation Des Ly PDFDocument39 pagesActivation Des Ly PDFikram BencherifPas encore d'évaluation
- Les Lymphocytes - 2017 - 2018Document58 pagesLes Lymphocytes - 2017 - 2018amina.chafi1-etuPas encore d'évaluation
- 03 - Les Lymphocytes TDocument14 pages03 - Les Lymphocytes TaminedhaPas encore d'évaluation
- Immuno 03. LyT Khadidja FerdjDocument8 pagesImmuno 03. LyT Khadidja Ferdjmaya mhdPas encore d'évaluation
- Cellules SIDocument14 pagesCellules SIimane yakhlefPas encore d'évaluation
- Lymphocytes TDocument12 pagesLymphocytes TmissjellyfishPas encore d'évaluation
- Immunité CellulaireDocument4 pagesImmunité CellulaireAymenPas encore d'évaluation
- Immuno1 Chap11 12et132020Document41 pagesImmuno1 Chap11 12et132020Irvine KwamenPas encore d'évaluation
- 1 - IMMUNGEN - Part1c - PolycopeDocument6 pages1 - IMMUNGEN - Part1c - PolycopehoucineaboutarikPas encore d'évaluation
- Lymphocyte TDocument51 pagesLymphocyte TAmiraBenhammouPas encore d'évaluation
- 2eme Bio Soufane Séries de TD Immunolgie CorrigéeDocument22 pages2eme Bio Soufane Séries de TD Immunolgie CorrigéeOumia HarbitPas encore d'évaluation
- Déroulement de La Réponse Immunitaire Spécifique-ConvertiDocument20 pagesDéroulement de La Réponse Immunitaire Spécifique-ConvertiHk Eh100% (2)
- 7-LT N.MDocument3 pages7-LT N.MwissemPas encore d'évaluation
- Chap 15Document3 pagesChap 15Frédéric JanvierPas encore d'évaluation
- Les CytokinesDocument47 pagesLes CytokinesOusmane SyllaPas encore d'évaluation
- Partager - 1 - Les Interactions Cellulaires Au Cours de La Réponse - PPTX 2020Document45 pagesPartager - 1 - Les Interactions Cellulaires Au Cours de La Réponse - PPTX 2020Sabrina KoufiPas encore d'évaluation
- Cours 5 Ontogénèse de LTDocument4 pagesCours 5 Ontogénèse de LTAmina Feriel KadriPas encore d'évaluation
- Support de Cours R Ponse Immunitaire Humorale Et CellulaireDocument12 pagesSupport de Cours R Ponse Immunitaire Humorale Et CellulaireBOURRAKH HAMZAPas encore d'évaluation
- preparation علم المناعة 2 biofDocument7 pagespreparation علم المناعة 2 biofKotbi MohamedPas encore d'évaluation
- Cours Immunologie - 2ème Sciences Biologiques Section 01 - OUABEDDocument22 pagesCours Immunologie - 2ème Sciences Biologiques Section 01 - OUABEDKakashi HatakéPas encore d'évaluation
- Cours Immunité Adaptative PDFDocument6 pagesCours Immunité Adaptative PDFL kPas encore d'évaluation
- Chapitre 6 - Le CMH - Etudiants PDFDocument3 pagesChapitre 6 - Le CMH - Etudiants PDFLennaPas encore d'évaluation
- Lymphocytes TDocument47 pagesLymphocytes Tdagnogo armelPas encore d'évaluation
- Les Cellules DendritiquesDocument1 pageLes Cellules DendritiquesManel BrahimiPas encore d'évaluation
- Null PDFDocument26 pagesNull PDFAziz OualidPas encore d'évaluation
- Cours Immunologie - 2ème Sciences Biologiques Section 01 - OUABEDDocument19 pagesCours Immunologie - 2ème Sciences Biologiques Section 01 - OUABEDDjihadnoorPas encore d'évaluation
- Déroulement de La Réponse Immunitaire SpécifiqueDocument6 pagesDéroulement de La Réponse Immunitaire SpécifiqueDalili SVTPas encore d'évaluation
- Les Cellules NK Cours 1Document9 pagesLes Cellules NK Cours 1Lili VongPas encore d'évaluation
- Cellules LymphoïdesDocument4 pagesCellules LymphoïdesI.m. DanielPas encore d'évaluation
- Lymphocyte TDocument7 pagesLymphocyte TAnonymous nWdUS7jn8fPas encore d'évaluation
- Cours IV Tolérance Immunitaire Et Auto ImmunitéDocument13 pagesCours IV Tolérance Immunitaire Et Auto ImmunitétinaPas encore d'évaluation
- Resume L2 Cours ImmunologieDocument10 pagesResume L2 Cours Immunologieإلهام فريضيPas encore d'évaluation
- Immuno3an Lymphocytes-TDocument23 pagesImmuno3an Lymphocytes-TSaid AkcentPas encore d'évaluation
- Fiches - Master Immunologie 2ème SemestreDocument26 pagesFiches - Master Immunologie 2ème Semestredric8884Pas encore d'évaluation
- 10 LymphocytesDocument29 pages10 LymphocytesCheikh SalehPas encore d'évaluation
- Bilan Chapitre 3 L ' Immunite AdaptativeDocument6 pagesBilan Chapitre 3 L ' Immunite Adaptativeahmedrayanelali23Pas encore d'évaluation
- NK GradeDocument35 pagesNK GradeLyes DahmaniPas encore d'évaluation
- ImmunologieDocument53 pagesImmunologielot usPas encore d'évaluation
- 97 1BDocument8 pages97 1BTewfik TGrPas encore d'évaluation
- 8 HomingDocument50 pages8 HomingFarah SalhiPas encore d'évaluation
- Cours Chap 5Document7 pagesCours Chap 5Thevoice KidsPas encore d'évaluation
- Système Lymphoïde 2020-2021Document81 pagesSystème Lymphoïde 2020-2021ouni mohamedPas encore d'évaluation
- L'immunité Innée Acteurs Cellulaires Maria HassaniDocument5 pagesL'immunité Innée Acteurs Cellulaires Maria HassaniKader Emmanuel Stéphane SanonPas encore d'évaluation
- ImmunitéDocument31 pagesImmunitélahlou Lh100% (1)
- Ts t3 Cii II Coop III Maturation Corr Doc Ele CoursDocument6 pagesTs t3 Cii II Coop III Maturation Corr Doc Ele CoursOdunayo OnésimePas encore d'évaluation
- B) Amplification ClonaleDocument3 pagesB) Amplification ClonaleOwen DormoisPas encore d'évaluation
- 12-TCR BCR AcmDocument41 pages12-TCR BCR AcmBMA belguedjPas encore d'évaluation
- Cours Chapitre IIDocument7 pagesCours Chapitre IIErwan GuioniePas encore d'évaluation
- Corrigé La Maturation Du Systeme Immunitaire en 3 Points.Document4 pagesCorrigé La Maturation Du Systeme Immunitaire en 3 Points.kilm. gujo.Pas encore d'évaluation
- Cours Immuno 2020-2021Document18 pagesCours Immuno 2020-2021Kourbam AramsPas encore d'évaluation
- Lymphocyte Et Reponse ImmunitaireDocument62 pagesLymphocyte Et Reponse Immunitaireanaischauvin12Pas encore d'évaluation
- Cours 4 Immunité Non Spécifique Et Immunité Spécifique1485400321Document26 pagesCours 4 Immunité Non Spécifique Et Immunité Spécifique1485400321amel bekkayePas encore d'évaluation
- S SVT Obligatoire 2017 Polynesie CorrigeDocument8 pagesS SVT Obligatoire 2017 Polynesie CorrigeWilfriedPas encore d'évaluation
- LT Effecteurs Benihoud 2023-2024Document21 pagesLT Effecteurs Benihoud 2023-2024cattylunaticPas encore d'évaluation
- IMMUNOLOGIE1Document3 pagesIMMUNOLOGIE1Ilyes MraidiaPas encore d'évaluation
- 13 CytokinesDocument60 pages13 CytokinesBMA belguedjPas encore d'évaluation
- Theme 3 Chapitre 16 3 Et 4Document2 pagesTheme 3 Chapitre 16 3 Et 4louislucasbaptistaPas encore d'évaluation
- Système immunitaire: Les Grands Articles d'UniversalisD'EverandSystème immunitaire: Les Grands Articles d'UniversalisPas encore d'évaluation
- 5-Cycle ÇDocument25 pages5-Cycle ÇMohamed OuHouissPas encore d'évaluation
- BIO111 Introduction Et ChapitreIDocument8 pagesBIO111 Introduction Et ChapitreIBerthe Aristide Ngue NkongoPas encore d'évaluation
- Arguments Pour La GenetiqueDocument3 pagesArguments Pour La Genetiquemennarais55Pas encore d'évaluation
- SVT 6eme 5eme 3emeDocument4 pagesSVT 6eme 5eme 3emeMamadou Ndiaye100% (1)
- Biologie Cellulaire: Enseignements DirigesDocument30 pagesBiologie Cellulaire: Enseignements DirigesKourdePas encore d'évaluation
- Hématologie Le Sang 2014Document124 pagesHématologie Le Sang 2014Vino DongaPas encore d'évaluation
- Chapitre 5 - Tissu OsseuxDocument12 pagesChapitre 5 - Tissu OsseuxFernando KollaPas encore d'évaluation
- EpithéliumDocument9 pagesEpithéliumdcdPas encore d'évaluation
- Biologie Moléculaire - RévisionDocument5 pagesBiologie Moléculaire - RévisionKhadija ChouaibiPas encore d'évaluation
- Cour 3 UnlockedDocument43 pagesCour 3 UnlockedarminPas encore d'évaluation
- Sujet SVT Serie C 1999 2022Document83 pagesSujet SVT Serie C 1999 2022Nemir MimirPas encore d'évaluation
- Introduction À La Parasitologie - Mycologie 2024Document36 pagesIntroduction À La Parasitologie - Mycologie 2024drsoniaoualiPas encore d'évaluation
- Cours Propriétés Colligatives Des Solutions 2.0Document12 pagesCours Propriétés Colligatives Des Solutions 2.0Modo HecatePas encore d'évaluation
- Anatomie FonctionnelleDocument86 pagesAnatomie FonctionnelleLara BebenPas encore d'évaluation
- CHAPITRE 2 - Thème - 1A - ELEVEDocument5 pagesCHAPITRE 2 - Thème - 1A - ELEVEMykolaZPas encore d'évaluation
- Chapitre Syntha Se ProtaiqueDocument29 pagesChapitre Syntha Se ProtaiqueNouha HadjPas encore d'évaluation
- Tailles Méthodes AlternativesDocument35 pagesTailles Méthodes AlternativesJérôme GuilleminPas encore d'évaluation
- QCM TD 3Document3 pagesQCM TD 3michelbakimbi9Pas encore d'évaluation
- Monocyte Et Macrophage.Document7 pagesMonocyte Et Macrophage.Rofaida FidaPas encore d'évaluation
- Psychologie de L'adolescentDocument22 pagesPsychologie de L'adolescentYoussef LasPas encore d'évaluation
- LX Broth - 2078540 - 1.0 - 42626Document2 pagesLX Broth - 2078540 - 1.0 - 42626MostafaMahmoudAliPas encore d'évaluation
- Techniques Biologie Cellulaire 2016-2017Document8 pagesTechniques Biologie Cellulaire 2016-2017Meryem EramiPas encore d'évaluation
- Isolement Des Microorganismes Du SolDocument2 pagesIsolement Des Microorganismes Du SolcosmixvjPas encore d'évaluation
- Chapitre 04Document23 pagesChapitre 04Jalil YCPas encore d'évaluation
- BO2018 - LGAJLJ Tome 1 - Cahier-de-collectes-Cm1Document19 pagesBO2018 - LGAJLJ Tome 1 - Cahier-de-collectes-Cm1Yassine JazairiPas encore d'évaluation
- PlasmideDocument35 pagesPlasmidea.itatahinePas encore d'évaluation
- Correction - Examen - BI - 125 - Structure - Fonction - de La - CelluleDocument2 pagesCorrection - Examen - BI - 125 - Structure - Fonction - de La - CelluleBerthe Aristide Ngue NkongoPas encore d'évaluation
- Cours9 HLBI409Document31 pagesCours9 HLBI409FFFFFFFFFFPas encore d'évaluation
- Fiche Pedagogique SVT 3 1Document10 pagesFiche Pedagogique SVT 3 1abdelatif svtPas encore d'évaluation
- Cours 2 Biologie VégétaleDocument58 pagesCours 2 Biologie VégétaleIliass NaouadirPas encore d'évaluation