Académique Documents
Professionnel Documents
Culture Documents
Chimie C Chap11 Application Electrolyse PDF
Transféré par
Yassir Rochd0 évaluation0% ont trouvé ce document utile (0 vote)
69 vues1 pageTitre original
Chimie-C-chap11-application-electrolyse.pdf
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
69 vues1 pageChimie C Chap11 Application Electrolyse PDF
Transféré par
Yassir RochdDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 1
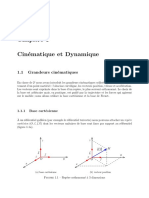
Cours de TS Applications de l’électrolyse
Chimie
LES APPLICATIONS DE L’ELECTROLYSE
1) Les accumulateurs :
Certaines piles utilisées couramment sont nommées improprement piles rechargeables. Celles-ci sont
en fait des accumulateurs.
L’accumulateur le plus usuel est celui que l’on rencontre dans nos véhicules : l’accumulateur au plomb.
On ne peut pas recharger toutes les piles car l’électrolyse de certaines d’entre elles conduirait à la
production de gaz ce qui constitue un danger. De plus, les aspects cinétiques de certaines transformations
ne peuvent permettre à la pile d’être rechargée.
Equation des réactions aux électrodes lors de la décharge :
A la cathode : PbO2 (s) + SO42-(aq) + 4 H+(aq) + 2 e- = PbSO4 (s) + 2 H2O(l)
A l'anode : Pb(s) + SO42-(aq) = PbSO4 (s) + 2 e-
D’où : réaction de décharge : PbO2 (s) + Pb(s) + 2 SO42-(aq) + 4 H+(aq) = 2 PbSO4 (s) + 2 H2O(l)
Equation de charge : 2 PbSO4 (s) + 2 H2O(l) = PbO2 (s) + Pb(s) + 2 SO42-(aq) + 4 H+(aq)
2) Applications industrielles :
L’électrolyse d’une solution de chlorure de sodium permet d’obtenir du dichlore, du dihydrogène,
de la soude et de l’eau de javel (cela dépend des conditions d’électrolyse).
A l’aide d’un procédé qui se nomme “électrolyse à anode soluble”, on peut purifier des métaux
comme le plomb, le fer, le zinc ou le cuivre :
Pour ce dernier, on effectue une électrolyse avec deux électrodes en cuivre, l’anode est
composé de cuivre impur, la cathode de cuivre pur. Ces deux électrodes plongent dans
une solution de sulfate de cuivre.
Pendant l’électrolyse, l’anode va se solubiliser : il y a formation d’ions cuivre et les
d’impuretés, non oxydables, se déposent. L’anode s’est donc solubilisée mais aussi
purifiée.
A la cathode, les ions cuivre sont réduits et donne du cuivre métal.
3) Deux autres applications intéressantes :
La galvanostégie consiste à déposer une couche de métal sur un objet rendu conducteur :
La cathode sera constituée par l’objet à recouvrir.
L’anode peut être constituée du métal que l’on veut déposer.
Ces deux électrodes plongent dans un bain contenant le cation à déposer.
La galvanoplastie suit le même procédé, dans le but de reproduire des objets :
La cathode est cette fois-ci le moule de l’objet à reproduire qui a été rendu conducteur.
L’anode est par exemple du cuivre et le bain une solution d’ions cuivre II.
On obtient alors une reproduction de l’objet en cuivre.
4) Une transformation forcée dans un autre domaine :
Voici un document qui montre les processus de respiration et de photosynthèse qui s’effectuent au sein
des végétaux : Rappelez quelles sont ces deux réactions en sachant que
les espèces mises en jeu sont :
CO2 (g) ; H2O(l) ; CnH2nOn (s) et O2 (g) (n nombre entier)
Respiration :
CnH2nOn (s) + n O2 (g) n CO2 (g) + n H2O (l)
Photosynthèse :
n CO2 (g) + n H2O (l) CnH2nOn (s) + n O2 (g)
De ces deux transformations, laquelle est spontanée ?
Laquelle est forcée ? Quelle énergie permet de la
forcer ?
La transformation forcée est la photosynthèse, c’est
l’énergie lumineuse qui la permet.
Vous aimerez peut-être aussi
- Introduction à la physique de la matièreD'EverandIntroduction à la physique de la matièreÉvaluation : 3 sur 5 étoiles3/5 (1)
- Chapitre-8-Transformation Forcée L'électrolyseDocument5 pagesChapitre-8-Transformation Forcée L'électrolysea houssPas encore d'évaluation
- Cours Electrolyse ElouardeDocument6 pagesCours Electrolyse Elouarderihab100% (1)
- ElectrochimieDocument92 pagesElectrochimieThelegenge Isborn100% (3)
- Oxydoreduction Cours 01Document19 pagesOxydoreduction Cours 01Sa LimPas encore d'évaluation
- Chimie Des SolutionsDocument17 pagesChimie Des SolutionsamaghchichePas encore d'évaluation
- Correction Exercices Chapitre N°8 - Oxydo-Réduction Dans Les Piles Et AccumulateursDocument3 pagesCorrection Exercices Chapitre N°8 - Oxydo-Réduction Dans Les Piles Et Accumulateursunsheatedsword55Pas encore d'évaluation
- 15 C3a9lectrolyseDocument10 pages15 C3a9lectrolyseazerfazPas encore d'évaluation
- Cours OxydoreductionDocument35 pagesCours OxydoreductionSoleil Algeria100% (2)
- COURS Equilibre OxredDocument19 pagesCOURS Equilibre Oxredsembei1Pas encore d'évaluation
- Chimie 9éme-1Document29 pagesChimie 9éme-1Hama Coulibaly88% (8)
- Oxydo ReductionDocument55 pagesOxydo ReductionMeryem MaatallahPas encore d'évaluation
- 7 - Transformations Forcées - ÉlectrolyseDocument3 pages7 - Transformations Forcées - ÉlectrolysesdoulajPas encore d'évaluation
- Série Transformation Forcée CorrectionDocument8 pagesSérie Transformation Forcée CorrectionAmine AlaoUii AlaouiPas encore d'évaluation
- Cours OxydoreductionDocument4 pagesCours Oxydoreductionblackcat.fantomasPas encore d'évaluation
- Electrolyse NaClDocument9 pagesElectrolyse NaClImane ARPas encore d'évaluation
- Chapitre VDocument10 pagesChapitre VSERGIOPas encore d'évaluation
- 1 - Transformations Rapides Et Transfomations RapidesDocument5 pages1 - Transformations Rapides Et Transfomations Rapidesyoussefoutter22Pas encore d'évaluation
- Cours Chimie Des Eaux Et Cinétique 2019-2020 - PR TOUILDocument105 pagesCours Chimie Des Eaux Et Cinétique 2019-2020 - PR TOUILFatima Ezzahra LaftouhiPas encore d'évaluation
- Science 2Document8 pagesScience 2whs8s977ntPas encore d'évaluation
- Leçon 22Document12 pagesLeçon 22wafaPas encore d'évaluation
- Ch.3-Theorie Notebook - STE-2020 - ProfDocument21 pagesCh.3-Theorie Notebook - STE-2020 - ProfgabrielaPas encore d'évaluation
- CoursDocument19 pagesCourskapalab108Pas encore d'évaluation
- OS Corrige RedoxDocument31 pagesOS Corrige RedoxMahdiNaani100% (2)
- Nombre D'oxydation Cours N°2Document4 pagesNombre D'oxydation Cours N°2Amine NouarPas encore d'évaluation
- Les Reactions D Oxydo Reduction Cours 4Document3 pagesLes Reactions D Oxydo Reduction Cours 4mohmedPas encore d'évaluation
- CorrosionDocument9 pagesCorrosionHalima ZaghbibPas encore d'évaluation
- LC05 OxydantsEtReducteursDocument9 pagesLC05 OxydantsEtReducteursgü zelPas encore d'évaluation
- Elaboration Industrielle Du Zinc: Les Différentes Parties de Cet Exercice Sont Indépendantes. DonnéesDocument2 pagesElaboration Industrielle Du Zinc: Les Différentes Parties de Cet Exercice Sont Indépendantes. Donnéesrufin rufin rufinPas encore d'évaluation
- Chimie Générale5Document50 pagesChimie Générale5Talouth TourePas encore d'évaluation
- Chapitre 8, Transformations Forcées, Cours, Activités, Exercices D'applicationDocument6 pagesChapitre 8, Transformations Forcées, Cours, Activités, Exercices D'applicationasma oumo douaPas encore d'évaluation
- Cours - Chimie Electrolyse - Bac Technique (2011-2012) MR Ouerghemmi PDFDocument5 pagesCours - Chimie Electrolyse - Bac Technique (2011-2012) MR Ouerghemmi PDFLotfi Bouchareb100% (3)
- Les Phenomenes Doxydoreduction - Theorie - 2020Document18 pagesLes Phenomenes Doxydoreduction - Theorie - 2020Lawrence Mundene-timotheePas encore d'évaluation
- Sa1 (1) 2021Document8 pagesSa1 (1) 2021Clement HergéPas encore d'évaluation
- l2 - Cours1 Oxydoreduction Fevrier 2019Document23 pagesl2 - Cours1 Oxydoreduction Fevrier 2019Alexandre Kpangny BéniPas encore d'évaluation
- Correction D'exercices Sur La Conversion de L'énergie Lumineuse en Énergie ChimiqueDocument5 pagesCorrection D'exercices Sur La Conversion de L'énergie Lumineuse en Énergie ChimiqueConstantin Nilda NgueyaPas encore d'évaluation
- Notion de Couple OxydantDocument4 pagesNotion de Couple OxydantRoosvelt feujioPas encore d'évaluation
- Roman Arthur RimbaudDocument3 pagesRoman Arthur Rimbaudjasmine.rkm13Pas encore d'évaluation
- S6 Chapitre 6 Cinetique Chimique PDFDocument12 pagesS6 Chapitre 6 Cinetique Chimique PDFAzizElheni100% (1)
- Chimie 2007Document17 pagesChimie 2007pmarcautPas encore d'évaluation
- 03 OxydoréductionDocument11 pages03 OxydoréductionIbrahim Labhar100% (1)
- Hydrometallurgie Du ZincDocument8 pagesHydrometallurgie Du Zincimane bakassi100% (1)
- Électrolyse: 8.1. Principes de Base - DéfinitionsDocument5 pagesÉlectrolyse: 8.1. Principes de Base - DéfinitionsabdelbarrPas encore d'évaluation
- Chapitre IDocument9 pagesChapitre IInes BoudjahemPas encore d'évaluation
- Chimie Minérale 2Document27 pagesChimie Minérale 2amineahlam311Pas encore d'évaluation
- Chapitre 2 CorrosionDocument16 pagesChapitre 2 CorrosionhajjiPas encore d'évaluation
- Chimie Des Solutions Mpsi-1Document9 pagesChimie Des Solutions Mpsi-1mounirPas encore d'évaluation
- PC 1ère CD-C14 ElectrolyseDocument7 pagesPC 1ère CD-C14 ElectrolyseAssi MardochéePas encore d'évaluation
- Chapitre 5cDocument14 pagesChapitre 5cAbderrafie BCPas encore d'évaluation
- ChimieMinSyst IRDDocument36 pagesChimieMinSyst IRDKalosoiretrotchgmail.com KalosoPas encore d'évaluation
- TD Eq5Document10 pagesTD Eq5hala shooowPas encore d'évaluation
- Transformations ForcéesDocument4 pagesTransformations ForcéesaffanefatimaezzahraaPas encore d'évaluation
- Chapitre III Ox RedDocument76 pagesChapitre III Ox RedAbdelhakim Bailal100% (4)
- Chapitre 1 Oxydoreduction (Nouveau) - ConvertiDocument17 pagesChapitre 1 Oxydoreduction (Nouveau) - ConvertiMiss KPas encore d'évaluation
- Compte Rendu Chimie Des SolutionDocument12 pagesCompte Rendu Chimie Des Solutionmeriem.bouaouda7102100% (1)
- Partie Ii Reaction Oxydo-ReductionDocument31 pagesPartie Ii Reaction Oxydo-ReductionAmr BahriPas encore d'évaluation
- 1année S2 Chimie II OxydoréductionDocument9 pages1année S2 Chimie II OxydoréductionDenis KaldjobPas encore d'évaluation
- Chimie Biologie Yaounde 2004Document9 pagesChimie Biologie Yaounde 2004Tagne yvanPas encore d'évaluation
- CoursDocument5 pagesCoursYassir RochdPas encore d'évaluation
- Exo Gravitation 3 4 5 6 CorrDocument2 pagesExo Gravitation 3 4 5 6 CorrYassir RochdPas encore d'évaluation
- Fiche Technique 2-Phmetrie PDFDocument1 pageFiche Technique 2-Phmetrie PDFYassir RochdPas encore d'évaluation
- 3 Ex Travail Puiss Energ 13 ComprDocument7 pages3 Ex Travail Puiss Energ 13 ComprYassir RochdPas encore d'évaluation
- Fiche Technique 7-ConductimetrieDocument2 pagesFiche Technique 7-ConductimetrieYassir RochdPas encore d'évaluation
- TD Oscillation Mecanique 2014 Lolb-Wahab DiopDocument5 pagesTD Oscillation Mecanique 2014 Lolb-Wahab DiopYassir Rochd100% (2)
- (Torrent9.red) Larousse - Orthographe - Les Indispensables PDFDocument122 pages(Torrent9.red) Larousse - Orthographe - Les Indispensables PDFgranmystePas encore d'évaluation
- Série Ec PDFDocument2 pagesSérie Ec PDFYassir RochdPas encore d'évaluation
- Phy 3Document13 pagesPhy 3Yassir Rochd100% (1)
- Cinema TiqueDocument32 pagesCinema TiqueAhmed HaniPas encore d'évaluation
- Exercice Bac Blanc Physique Ondes Sonores PDFDocument3 pagesExercice Bac Blanc Physique Ondes Sonores PDFYassir Rochd50% (2)
- Oscillateur À Résistance Négative Cours Morchid PDFDocument8 pagesOscillateur À Résistance Négative Cours Morchid PDFYassir RochdPas encore d'évaluation
- TermS PH Chap11Document17 pagesTermS PH Chap11Yassir RochdPas encore d'évaluation
- Exercices de DYNAMIQUE de RotationDocument13 pagesExercices de DYNAMIQUE de RotationYassir RochdPas encore d'évaluation
- Ex Dipole RLCDocument4 pagesEx Dipole RLClamilouch6498100% (1)
- Chimie C Chap11 Application Electrolyse PDFDocument1 pageChimie C Chap11 Application Electrolyse PDFYassir RochdPas encore d'évaluation
- Tp03complet PDFDocument12 pagesTp03complet PDFYassir RochdPas encore d'évaluation
- Fiche-La Radioactivite PDFDocument5 pagesFiche-La Radioactivite PDFYassir RochdPas encore d'évaluation
- Exercice Corrige Bac Blanc Physique Ondes Sonores PDFDocument2 pagesExercice Corrige Bac Blanc Physique Ondes Sonores PDFYassir Rochd0% (1)
- 151 1s Ii.0 Formulaire PDFDocument2 pages151 1s Ii.0 Formulaire PDFYassir RochdPas encore d'évaluation
- Energie Interne Et Calorimètre Exercices FR 16Document2 pagesEnergie Interne Et Calorimètre Exercices FR 16Yassir Rochd100% (1)
- Physique-Chapitre7-Transfert Thermique Et Energie InterneDocument3 pagesPhysique-Chapitre7-Transfert Thermique Et Energie InterneYassir RochdPas encore d'évaluation
- Physique 1bac Cours - 05 Travail Et Energie Interne PDFDocument3 pagesPhysique 1bac Cours - 05 Travail Et Energie Interne PDFYassir RochdPas encore d'évaluation
- TPE (FR)Document1 pageTPE (FR)Mouhamed NdaoPas encore d'évaluation
- Fascicule 2007-2008-2eme Partie Chi PhysikDocument96 pagesFascicule 2007-2008-2eme Partie Chi PhysikHenri Elias HabibPas encore d'évaluation
- Geochimie IsotopiqueDocument25 pagesGeochimie IsotopiqueWillPas encore d'évaluation
- Titrage CompléxométriqueDocument1 pageTitrage Compléxométriqueimad.elrhair7Pas encore d'évaluation
- Les MatériauxDocument4 pagesLes MatériauxCHERIFPas encore d'évaluation
- DS N3-Physique PDFDocument2 pagesDS N3-Physique PDFndiouma dioufPas encore d'évaluation
- Cours Designation Des Materiaux Fiche 1 eDocument1 pageCours Designation Des Materiaux Fiche 1 ehanane hamidi100% (1)
- 16 - Determination-Des-Metaux-Lourds-Par-VoieDocument7 pages16 - Determination-Des-Metaux-Lourds-Par-VoieMaria MirceaPas encore d'évaluation
- Matériaux Utilisés Dans La Vie QuotiienneDocument3 pagesMatériaux Utilisés Dans La Vie QuotiienneYassinePas encore d'évaluation
- NuancierDocument26 pagesNuancierViteVitePas encore d'évaluation
- Alcalinité (TA Et TAC) PDFDocument2 pagesAlcalinité (TA Et TAC) PDFSoumaya SILINIPas encore d'évaluation
- 4 Élaboration de L'acier+ DésignationDocument69 pages4 Élaboration de L'acier+ DésignationGames PlayerPas encore d'évaluation
- Cours Atomistique - Licence 1 - Sciences PhysiquesDocument63 pagesCours Atomistique - Licence 1 - Sciences PhysiquesMichael JamesPas encore d'évaluation
- 2004 03 NelleCaledonie Sujet Exo3 TempsDemiVie DemiReaction 4ptsDocument3 pages2004 03 NelleCaledonie Sujet Exo3 TempsDemiVie DemiReaction 4ptsAlain StantéPas encore d'évaluation
- Chemistry Paper 1 HL SpanishDocument20 pagesChemistry Paper 1 HL SpanishRenzo Karol Marcelo De la cruz astetePas encore d'évaluation
- Arcelor Catalogue Web 2020 Avec Liens Bouton LightDocument261 pagesArcelor Catalogue Web 2020 Avec Liens Bouton LightJose RegueiroPas encore d'évaluation
- Solution de Lexercice 1 Série 1Document9 pagesSolution de Lexercice 1 Série 1Otman RamliPas encore d'évaluation
- Exercices 29 Decroissance Radioactive (Mahdade Allal)Document7 pagesExercices 29 Decroissance Radioactive (Mahdade Allal)yassin2009xxxxPas encore d'évaluation
- TD Radioactivite Et Reaction Nucleaire CCRDocument5 pagesTD Radioactivite Et Reaction Nucleaire CCROumar TraorePas encore d'évaluation
- MANGANIMÉTRIEDocument2 pagesMANGANIMÉTRIEDiallo100% (1)
- 02 CHM144 - FSS - Atomes - Atomistique - S2-1Document32 pages02 CHM144 - FSS - Atomes - Atomistique - S2-1Eric OuakaraPas encore d'évaluation
- Catalogue-2012 VictoriaDocument38 pagesCatalogue-2012 Victoriakristel davyPas encore d'évaluation
- 01 - 1ère-Activité1 - 2-Juste Les Questions-Correction'Document2 pages01 - 1ère-Activité1 - 2-Juste Les Questions-Correction'Youldes GhoumaPas encore d'évaluation
- SMPC s2 CHP 2Document31 pagesSMPC s2 CHP 2Abdelhakim BailalPas encore d'évaluation
- Eurl Afroquartz Ten 0.95Document5 pagesEurl Afroquartz Ten 0.95chouaibPas encore d'évaluation
- NucleaireDocument36 pagesNucleaireLati FaePas encore d'évaluation
- Uranium Au SénégalDocument8 pagesUranium Au SénégalhajlaouiPas encore d'évaluation
- Propriétés Physiques Des Semi ConducteursDocument11 pagesPropriétés Physiques Des Semi ConducteursWiàm ZanobàPas encore d'évaluation
- Cours3equadiff1 11Document31 pagesCours3equadiff1 11Abdias PierrePas encore d'évaluation
- 2° Contrôle SMPC S2 2012 2013 PDFDocument2 pages2° Contrôle SMPC S2 2012 2013 PDFAbdelah El Arabi100% (2)