Académique Documents
Professionnel Documents
Culture Documents
Devoir 6
Transféré par
valdxCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Devoir 6
Transféré par
valdxDroits d'auteur :
Formats disponibles
Santé Devoir 6 Santé Devoir 6
Chapitres 2 - 3
Médicaments / Molécules et synthèse 1/2 Chapitres 2 - 3
Médicaments / Molécules et synthèse 2/2
A. Etude de deux molécules :
1. Donner les formules brutes et semi-développées des molécules et .
Document : Le propan-1-ol et l’isopropanol
Le propan-1-ol est souvent employé comme solvant organique en pharmacologie. L’isopropanol est employé comme 2. Entourer, sur les formules semi-développées précédentes, les groupes caractéristiques présents et
désinfectant et antiseptique. en déduire à quelle(s) famille(s) chimique(s) appartiennent les molécules et .
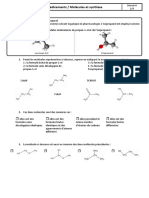
Voici, représentés ci-dessous, les modèles moléculaires du propan-1-ol et de l’isopropanol :
3. Ces deux molécules sont-elles des isomères ? Justifier.
Document 3 : Réaction chimique de synthèse de l’acide acétylsalicylique.
Pour produire de l’acide acétylsalicylique, on fait réagir l’acide salicylique avec de l’anhydride éthanoïque. Il se forme
alors l’acide acétylsalicylique recherché et de l’acide éthanoïque.
Le propan-1-ol L’isopropanol
Acide salicylique + Anhydride éthanoïque Acide acétylsalicylique + Acide éthanoïque
1. Ecrire les formules brutes et semi-développées des deux molécules.
2. Montrer que ses deux molécules sont des isomères. Document 4 : Protocole expérimental.
On introduit dans un ballon 10,0 g d’acide salicylique, 21,6 g d’anhydride éthanoïque et quelques gouttes d’acide
3. Ecrire la formule semi-développée d’un autre isomère à ces deux molécules. sulfurique qui sert à accélérer la réaction. On réalise ensuite un chauffage à reflux du mélange à une température de
60 °C pendant 20 minutes.
B. Préparation d’une solution :
4. Le montage de chauffage à reflux utilisé est schématisé
Document : La solution de glucose. ci-contre. Compléter la légende manquante. Sortie d’eau
Une solution de glucose est un liquide qui peut être administré par voie intraveineuse à des personnes qui viennent
de subir une opération chirurgicale, qui sont en hypoglycémie ou encore qui sont déshydratées. 5. On possède au laboratoire, une bouteille d’anhydride
éthanoïque liquide. Quel volume de ce produit doit-on
On souhaite préparer 100 mL d’une solution de glucose de concentration massique Cm = 20 g.L-1. prélever pour respecter le protocole expérimental
1. Proposer un protocole expérimental précis (nom du matériel, étapes, …) permettant de préparer proposé dans le document 4 ? Bien justifier. Entrée d’eau
cette solution.
6. De quelle famille fait partie l’acide éthanoïque ?
Cette solution est en réalité trop concentrée et on souhaite réaliser une dilution d’un facteur x = 10.
2. Proposer un protocole expérimental précis (nom du matériel, étapes, …) permettant de préparer 7. En déduire, parmi les formules semi-développées ci-
à partir de la solution précédente 200 mL de cette solution diluée. dessous, celle de l’acide éthanoïque. Justifier.
3. Quelle sera alors la concentration massique en glucose de cette nouvelle solution ? O O
a) CH3 C b) CH3 C
C. L’acide acétylsalicylique :
CH3 NH2
Document 1 : L’aspirine.
L’acide acétylsalicylique, plus connu sous le nom d’aspirine, est le principe actif de nombreux médicaments aux CH3 O
propriétés antalgiques, antipyrétiques et anti-inflammatoires. C’est un des médicaments les plus consommés au
monde. La synthèse de l’aspirine est assez simple et peut être réalisée à partir de l’acide salicylique que l’on trouve c) CH3 C d) CH3 C
naturellement dans certains végétaux comme le saule ou la reine-des prés. OH OH
Document 2 : Acide salicylique et acide acétylsalicylique.
Voici représentés ci-dessous, les modèles moléculaires de l’acide salicylique et de l’acide acétylsalicylique. Pour plus
de facilité, on appellera l’acide salicylique molécule et l’acide acétylsalicylique molécule .
Molécule : acide salicylique Molécule : acide acétylsalicylique Données : Densité de l’anhydride éthanoïque : d = 1,08 Masse volumique de l’eau : ρeau = 1 000 g.L-1
Vous aimerez peut-être aussi
- Devoir 6 QCMDocument4 pagesDevoir 6 QCMvaldxPas encore d'évaluation
- Devoir ExtractionDocument5 pagesDevoir ExtractionMalika BENHAMADAPas encore d'évaluation
- Chapitre 7 - Separation Et Purification - ExercicesDocument5 pagesChapitre 7 - Separation Et Purification - Exerciceselzineb066Pas encore d'évaluation
- Epreuve Bac 2022 Chimie Série C D e Cameroun PDFDocument2 pagesEpreuve Bac 2022 Chimie Série C D e Cameroun PDFAmza Farel100% (2)
- Sujet Bac S - Hysique ChimieDocument10 pagesSujet Bac S - Hysique ChimieLetudiant.fr100% (12)
- TD4 - Les BiomoléculesDocument10 pagesTD4 - Les Biomoléculesmelo.lasserrePas encore d'évaluation
- Sujet Bac Physique S 2009 ObligatoireDocument10 pagesSujet Bac Physique S 2009 ObligatoireMariem BissanePas encore d'évaluation
- Exercice 1 (7 Points) L'acide LactiqueDocument7 pagesExercice 1 (7 Points) L'acide LactiqueAli Rammal100% (1)
- TD MD ChimieDocument2 pagesTD MD ChimieMatthias KingPas encore d'évaluation
- Analyse de La VéganineDocument15 pagesAnalyse de La VéganineFatima BenPas encore d'évaluation
- m Moundounga Pour MehDocument3 pagesm Moundounga Pour Mehjuvelyescobar0Pas encore d'évaluation
- tp19_hemisynthse_aspirineDocument4 pagestp19_hemisynthse_aspirineAccorPas encore d'évaluation
- BAC Physique-Chimie-Specialite 2009 SDocument11 pagesBAC Physique-Chimie-Specialite 2009 SLetudiant.fr100% (7)
- Exercices PC 2bac Science International FR 22 2Document5 pagesExercices PC 2bac Science International FR 22 2HAMADA1972Pas encore d'évaluation
- Travaux Diriges 2021Document11 pagesTravaux Diriges 2021alex talakaPas encore d'évaluation
- CEEMS Chimie 2008Document5 pagesCEEMS Chimie 2008Madi Diop0% (1)
- BAC Sciences Physiques Et Chimiques 2010 ST2SDocument9 pagesBAC Sciences Physiques Et Chimiques 2010 ST2SLetudiant.frPas encore d'évaluation
- TP AspirineDocument8 pagesTP AspirineTaim Khouri100% (3)
- S Physique Chimie Obligatoire 2020 Polynesie Remplacement Sujet OfficielDocument15 pagesS Physique Chimie Obligatoire 2020 Polynesie Remplacement Sujet OfficielShahnas HAMITHPas encore d'évaluation
- Sujet 10.Document19 pagesSujet 10.ShadowZ Serveur 1Pas encore d'évaluation
- EsterficationsDocument9 pagesEsterficationssaid khachouPas encore d'évaluation
- Synthese Des Especes Chimiques Exerc2Document4 pagesSynthese Des Especes Chimiques Exerc2said khachouPas encore d'évaluation
- Coeff de PartageDocument6 pagesCoeff de Partagenadpharm13Pas encore d'évaluation
- série-1-Espèces-chimiques-Extraction-séparation-et-identification-despèces-chimiques-TC-BIOF-réalisée-par-Pr-JENKAL-RACHIDDocument3 pagessérie-1-Espèces-chimiques-Extraction-séparation-et-identification-despèces-chimiques-TC-BIOF-réalisée-par-Pr-JENKAL-RACHIDzzomaridoPas encore d'évaluation
- TP SaponificationDocument30 pagesTP SaponificationYoussef Che0% (1)
- Série D'exercices N°7-2BAC PC-CHIMIEDocument2 pagesSérie D'exercices N°7-2BAC PC-CHIMIEAymanePas encore d'évaluation
- TD Physio VegDocument10 pagesTD Physio Vegultima1606100% (1)
- TD Sur Les Alcools Terminale CD 2023Document3 pagesTD Sur Les Alcools Terminale CD 2023Admi BraccPas encore d'évaluation
- Controle de L Evolution D Un Systeme Chimique Exercices Non Corriges 2Document8 pagesControle de L Evolution D Un Systeme Chimique Exercices Non Corriges 2stefan0% (1)
- 2020 Polynesie Exo1 Sujet Boisson 9pts - 0Document6 pages2020 Polynesie Exo1 Sujet Boisson 9pts - 0Jœël Crèspœ KhæmænœPas encore d'évaluation
- Ch4 Les EstersDocument6 pagesCh4 Les EstersrdprofpcPas encore d'évaluation
- Chimie Exemple 3Document9 pagesChimie Exemple 3Serge DemirdjianPas encore d'évaluation
- TP N 2 - Titrages PH-M Triques (Titrage de L'aspirine)Document12 pagesTP N 2 - Titrages PH-M Triques (Titrage de L'aspirine)Safae Rezzouk100% (1)
- TP25 - 26 - Synthese Acétate de BenzyleDocument2 pagesTP25 - 26 - Synthese Acétate de Benzylechristophe38gauthierPas encore d'évaluation
- Serie D'extraction Et Synthese FrancaieDocument2 pagesSerie D'extraction Et Synthese FrancaieJamal ChahiriPas encore d'évaluation
- 2-Tp Chimie LaitDocument4 pages2-Tp Chimie LaitmeriemPas encore d'évaluation
- UntitledDocument1 pageUntitledBenji JeanPas encore d'évaluation
- ch13 Separation Extraction BenzocaineDocument3 pagesch13 Separation Extraction Benzocaineالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Chimie PD 3Document2 pagesChimie PD 3joseph leringPas encore d'évaluation
- Synthèse de L'arôme de JASMIN CORRECTIONDocument5 pagesSynthèse de L'arôme de JASMIN CORRECTIONMOHAMMEDI AYMANPas encore d'évaluation
- CEEMS 2013 Chimie-1Document5 pagesCEEMS 2013 Chimie-1Aida MbodjiPas encore d'évaluation
- Synthèse de L'arôme de JASMINDocument4 pagesSynthèse de L'arôme de JASMINchaou chaimaPas encore d'évaluation
- Chimie TleDocument2 pagesChimie TleHaman Bello OumarouPas encore d'évaluation
- Exercices Chimi IndustrielleDocument7 pagesExercices Chimi IndustrielleMohamed khalido KHNPas encore d'évaluation
- ds1 Chap1 CorrigeDocument3 pagesds1 Chap1 CorrigeMagatte DiopPas encore d'évaluation
- Série 1 Espèces Chimiques Réalisé Par Prof JENKALRACHIDDocument2 pagesSérie 1 Espèces Chimiques Réalisé Par Prof JENKALRACHIDEsma EbounaimPas encore d'évaluation
- Sujet 1Document5 pagesSujet 1Lilia AlouiPas encore d'évaluation
- TP Lampe A LaveDocument2 pagesTP Lampe A LaveRAZA LUCPas encore d'évaluation
- SVT 1ere D - L11 - LA DIGESTION DES ALIMENTSDocument13 pagesSVT 1ere D - L11 - LA DIGESTION DES ALIMENTSAdopoPas encore d'évaluation
- Bac-Blanc 2022-2023 - MaisonDocument9 pagesBac-Blanc 2022-2023 - MaisonnjnPas encore d'évaluation
- 2 2 B Digestion MacromoleculesDocument4 pages2 2 B Digestion MacromoleculesTasnim Tas NimPas encore d'évaluation
- Epreuve de Chimie: Exercice 2: Application Des Savoirs 8 PointsDocument2 pagesEpreuve de Chimie: Exercice 2: Application Des Savoirs 8 Pointsmichelakon1Pas encore d'évaluation
- 9-Série de TD N°9 Physique Pharmaceutique 2021-2022Document2 pages9-Série de TD N°9 Physique Pharmaceutique 2021-2022fadia sellami100% (1)
- Chimie D Chap12 Esterification Et HydrolyseDocument7 pagesChimie D Chap12 Esterification Et HydrolyseDinica DanielaPas encore d'évaluation
- 201704071220521Document6 pages201704071220521paixdedieu90Pas encore d'évaluation
- Solution Tp OrganiqueDocument5 pagesSolution Tp OrganiqueIkram KhedimPas encore d'évaluation
- TP1 CorrectionDocument6 pagesTP1 CorrectionTaim KhouriPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Études et recherches sur l'alimentation et le travail du cheval de troupeD'EverandÉtudes et recherches sur l'alimentation et le travail du cheval de troupePas encore d'évaluation
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- Devoir 6bisDocument2 pagesDevoir 6bisvaldxPas encore d'évaluation
- Devoir 5Document2 pagesDevoir 5valdxPas encore d'évaluation
- Devoir 5 CorrectionDocument4 pagesDevoir 5 CorrectionvaldxPas encore d'évaluation
- Devoir 5Document2 pagesDevoir 5valdxPas encore d'évaluation
- Devoir 7Document3 pagesDevoir 7valdxPas encore d'évaluation
- Devoir 4Document2 pagesDevoir 4valdxPas encore d'évaluation
- Devoir 4 CorrectionDocument3 pagesDevoir 4 CorrectionvaldxPas encore d'évaluation
- Devoir 3Document1 pageDevoir 3valdxPas encore d'évaluation
- Devoir 6 CorrectionDocument4 pagesDevoir 6 CorrectionvaldxPas encore d'évaluation
- TP1 Pointage Variation Vecteur VitesseDocument3 pagesTP1 Pointage Variation Vecteur VitessevaldxPas encore d'évaluation
- Devoir 4Document2 pagesDevoir 4valdxPas encore d'évaluation
- Devoir 1Document2 pagesDevoir 1valdxPas encore d'évaluation
- Devoir 2Document2 pagesDevoir 2valdxPas encore d'évaluation
- Activite1 Analyses Sanguines Chap1Document1 pageActivite1 Analyses Sanguines Chap1valdx100% (1)
- DS1 Chap1Document1 pageDS1 Chap1valdxPas encore d'évaluation
- Activité Exp 2 Composition Piece Dosage EtalonnageDocument2 pagesActivité Exp 2 Composition Piece Dosage Etalonnagevaldx0% (1)
- II.3.8 Activité Bonus Brouillon CorrectionDocument1 pageII.3.8 Activité Bonus Brouillon CorrectionvaldxPas encore d'évaluation
- DS2 Chap2 3Document3 pagesDS2 Chap2 3valdxPas encore d'évaluation
- Activite2 Volume Molaire Chap1Document1 pageActivite2 Volume Molaire Chap1valdxPas encore d'évaluation
- TP2 CORRECTION Titrage Chap8Document1 pageTP2 CORRECTION Titrage Chap8valdxPas encore d'évaluation
- Fiche Méthode spidHRDocument2 pagesFiche Méthode spidHRvaldxPas encore d'évaluation
- II.3.7 TP Echelle de TeinteDocument2 pagesII.3.7 TP Echelle de TeintevaldxPas encore d'évaluation
- II.3.4 Groupe CaractéristiqueDocument4 pagesII.3.4 Groupe CaractéristiquevaldxPas encore d'évaluation
- II.3.6 TP Noté Préparation de SolutionsDocument3 pagesII.3.6 TP Noté Préparation de SolutionsvaldxPas encore d'évaluation
- DS 1Document2 pagesDS 1valdx100% (1)
- DS 2Document1 pageDS 2valdxPas encore d'évaluation
- II.3.5 La Concentration MassiqueDocument2 pagesII.3.5 La Concentration MassiquevaldxPas encore d'évaluation
- Avoir Une Sexualite EpanouieDocument195 pagesAvoir Une Sexualite EpanouieA100% (2)
- Qualité de L'eau: Norme Française HomologuéeDocument5 pagesQualité de L'eau: Norme Française HomologuéeOuraghni AnassPas encore d'évaluation
- Interview DGDocument1 pageInterview DGMustapha FilaliPas encore d'évaluation
- Exercices - Epargne Et Consommation 6Document5 pagesExercices - Epargne Et Consommation 6berardgrungePas encore d'évaluation
- L Echantillonnage Des Sols en Agriculture PDFDocument6 pagesL Echantillonnage Des Sols en Agriculture PDFMouhammad NabiiPas encore d'évaluation
- Fiche S4 - 2 Prise en Charge Infirmiere Du Pied Diabetique PDFDocument3 pagesFiche S4 - 2 Prise en Charge Infirmiere Du Pied Diabetique PDFCheka22 gmail.comPas encore d'évaluation
- 2003 09 Antilles Exo2 Sujet Acides 6 5ptsDocument2 pages2003 09 Antilles Exo2 Sujet Acides 6 5ptsMed BriniPas encore d'évaluation
- Generalite Sur L'oncologieDocument36 pagesGeneralite Sur L'oncologieMassire CamaraPas encore d'évaluation
- Mémoire ANATO Willibrod Modeste_compressedDocument85 pagesMémoire ANATO Willibrod Modeste_compressedFréjusPas encore d'évaluation
- Examen Catalyse Enzymatique 2020-2021Document3 pagesExamen Catalyse Enzymatique 2020-2021PaulPas encore d'évaluation
- Série Ias 20 +Document5 pagesSérie Ias 20 +Master semaistre1Pas encore d'évaluation
- Exemple de Rapport Du Test Psychometrique AtmanCoDocument20 pagesExemple de Rapport Du Test Psychometrique AtmanCoismail100% (1)
- Boudechiche LamiaDocument218 pagesBoudechiche LamiaAbdelmoumen EllilePas encore d'évaluation
- (Des) Raisons Résonnent Par Henri SaveyDocument5 pages(Des) Raisons Résonnent Par Henri SaveyHenri SaveyPas encore d'évaluation
- Cod Caen 2010Document45 pagesCod Caen 2010Gabriel GirbovanPas encore d'évaluation
- Exos GDocument1 pageExos GTiohounPas encore d'évaluation
- Annie AnzieuDocument2 pagesAnnie AnzieumaomaccPas encore d'évaluation
- IsoDocument7 pagesIsoMohamadou NdjiddaPas encore d'évaluation
- Calcul Des PalierDocument2 pagesCalcul Des Paliermadjid tighiltPas encore d'évaluation
- B2 - 3 - Cahier - Module - 13-14-1-7 NeurostiinteDocument19 pagesB2 - 3 - Cahier - Module - 13-14-1-7 NeurostiinteAlina Topor Psi-MedicalPas encore d'évaluation
- Notice Diaglinide 2mg Comp B 30Document1 pageNotice Diaglinide 2mg Comp B 30Manel MaroufPas encore d'évaluation
- Fiche Mémo Chap.4 COMPLETEDocument5 pagesFiche Mémo Chap.4 COMPLETElouloubutez0Pas encore d'évaluation
- L'agroécologie Expliquée en 10 Points Par Pierre RabhiDocument2 pagesL'agroécologie Expliquée en 10 Points Par Pierre RabhiLysergik100% (2)
- 1 Résumé FROID Cours Fluide Frigorifique 1.2.et3Document29 pages1 Résumé FROID Cours Fluide Frigorifique 1.2.et3nejmeddine bouamPas encore d'évaluation
- Guide Generique de La Securite Pour Org HumanitaireDocument135 pagesGuide Generique de La Securite Pour Org Humanitaireaklimohand0% (1)
- AntalgiceDocument2 pagesAntalgiceAlina IsacPas encore d'évaluation
- Accumulateur Nickel CadmiumDocument3 pagesAccumulateur Nickel CadmiumMohamed SoussiPas encore d'évaluation
- Facteurs Favorisant La Malnutrition Chez Les Enfants de 0-59 Mois Dans La Ville de KinduDocument7 pagesFacteurs Favorisant La Malnutrition Chez Les Enfants de 0-59 Mois Dans La Ville de Kinducongo research papersPas encore d'évaluation
- Paie 100Document2 pagesPaie 100Gédéon AkradjiPas encore d'évaluation
- Protocole 1 Banane PlantainDocument7 pagesProtocole 1 Banane Plantainalexandrio gyrardPas encore d'évaluation