Académique Documents
Professionnel Documents
Culture Documents
Cours M2 PINGPONG
Transféré par
Allah Beurem BonheurTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cours M2 PINGPONG
Transféré par
Allah Beurem BonheurDroits d'auteur :
Formats disponibles
Cinétique enzymatique à deux substrats.
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer
l'ordre de fixation des substrats, les constantes cinétiques caractérisant la fixation de chacun
d'eux en présence et en absence de l'autre ainsi que la vitesse maximale de la réaction qui
est mesurée quand les deux substrats sont à concentration saturante.
I - Etude des vitesses initiales de la réaction :
-les mécanismes séquentiels (ou à simple déplacement) qui se subdivisent en mécanisme
séquentiel ordonné ou mécanisme séquentiel au hasard
- Séquentiel : la réaction enzymatique n'intervient qu'après formation d'un complexe entre
l'enzyme et les deux substrats (complexe ternaire ).
-Non séquentiel : système où un produit est relargué entre les additions successives des
substrats exemple : système à double déplacement dit "ping-pong"
1- Nomenclature des systèmes :
Les réactions sont classées : Uni, Bi, Ter ou Quad en fonction du nombre de substrats ou de
produits.
Bi Bi : système impliquant 2 substrats et 2 produits..
Bi Uni (ou Uni Bi) : système impliquant 2 substrats et 1 produit (ou l'inverse). Exemple : Bi Bi
ordonné.
Iso : système impliquant une isomérisation de l'enzyme (changement de conformation E <=>
E'). Exemple : Iso ping-pong.
2-Mécanismes séquentiels :
On parle de mécanisme séquentiel lorsque la réaction enzymatique n'intervient qu'après
formation d'un complexe entre l'enzyme et les deux substrats. La fixation des substrats peut
elle même être ordonnée (l'un des substrats se fixant nécessairement en premier lieu) ou se
produire au hasard (l'un ou l'autre des substrats se fixant en premier, sa présence pouvant
soit ne pas modifier, soit défavoriser la fixation de l'autre)
* Fixation au hasard : Deux substrats, A et B, se fixent de manière aléatoire sur l'enzyme
libre E (c'est-à-dire qu'il n'y a pas de fixation privilégiée de l'un ou l'autre des deux substrats)
avec une constante de dissociation KA et KB, respectivement.
Représentation de Cleland :
Le schéma et les constantes qui permettent de rendre compte des cinétiques s'écrivent
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
E-A et E-B sont appelés les complexes binaires et E-A-B le complexe ternaire. On peut définir
les deux constantes d'équilibre caractérisant les complexes binaires :
On dénomme ces constantes d'équilibre Ki, car chacun des substrats, présent en l'absence
de l'autre, se comporte comme un inhibiteur compétitif (avec Ki comme constante
d'inhibition), si l'enzyme peut catalyser une réaction entre deux autres substrats.
KiA et KiB étant les constante d'équilibres définies précédemment entre l'enzyme libre et les
substrats. KiA = ([E][A])/[E-A] et KiB = ([E][B])/[E-B]
-Ka et Kb sont les constantes de Mickaelis des substrats A et B, c'est à dire les [substrat] pour
lesquelles la vitesse (mesurée à concentration saturante de l'autre substrat) est égale à la
moitié de la vitesse maximale. Si l'on peut faire l'hypothèse du quasi-équilibre pour la
fixation des substrats et s'il n'existe qu'une seule étape cinétique pour la transformation de
E-A-B en E + P + Q; Ka est égale à la constante de dissociation de l'équilibre
E-A-B :::::::::::::: E-B + A et Kb à celle de l'équilibre E-A-B ::::::::::: E-A + B.
KA = ([A][EB])/[EAB] KB = ([B][EA])/[EAB] K iAK B = KiB KA
L'équation de vitesse est de la forme : V = Kcat [Et]/1+(KA/[A]+KB/[B]+KiA.KiB/[A][B])
Les représentations des 1/V en fonction de l'inverse de l'un des substrats (ex: 1/[A]), la
concentration de l'autre étant maintenue constante, sont linéaires lorsque l'enzyme est
Mickaeilien. On les appelle les représentations primaires. Les droites obtenues dans une
représentation primaire sont concourantes pour les mécanismes séquentiels.
L'abscisse du point d'intersection de concours des droites de la représentation primaire en
fonction de 1/[A] est égale à - 1/Kia.
L'ordonnée du point d'intersection est égale à : 1/(Kcat [Et])x1-(Ka/Kia).
E-A-B ::::::::::: E-B + A. On parle alors de fixation indépendante si KA=KiA et de fixation
dépendante dans le cas contraire (KA≠KIA). Les droites se coupent sur l'axe des abscisses
dans le cas d'une fixation indépendante, au dessus de cette axe si la fixation du second
substrat est facilitée par la présence du premier, au dessous dans le cas contraire.
L'intersection avec l'axe des ordonnées des droites obtenues dans les représentations
primaires varie avec la concentration de l'autre substrat.
Ainsi, l'ordonnée à l'origine des droites :
1/V = f(1/[A]), correspond à 1/Va = Kcat.[Et]/1+(Kb/[B]).
Elle représente l'inverse de la vitesse mesurée à concentration saturante de A et à la
concentration utilisée de B.
La représentation de 1/Va = f(1/[B]) (appelée représentation secondaire) est une droite; elle
s'extrapole sur l'axe des abscisses à - 1/Kb, Kb étant la constante de Mickaelis de B.
L'intersection avec l'axe des ordonnées de la représentation secondaire correspond à :
1/Kcat.[Et] = 1/Vm, Vm étant la vitesse mesurée lorsque les deux substrats sont
saturants.
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
-1/KiA
-1/KIA
-1/KIA
Représentation Primaire ( indépendante et dépendante ) 1/V = f( 1/A)
Représentation Secondaire
Exemple de bibi aléatoire : la créatine Phosphokinase
La créatine phosphokinase (CPK) ,catalyse le transfert d’un radical phosphoryl du substrat, le
phosphate de créatine, vers un coenzyme transporteur, l’ADP.
• L’affinité de l’enzyme pour ces deux corps chimiques étant voisine, la liaison de l’enzyme
avec chacun d’entre eux se fait dans un ordre qui dépend uniquement des concentrations
3
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
** Fixation ordonnée : Dans un tel système, l'ordre de fixation est obligatoire : le substrat A
doit se fixer à l'enzyme libre E avant le substrat B. En d'autres termes, le substrat B ne peut se fixer
qu'au complexe EA. Représentation de Cleland
KiA = (E)(A)/(EA) K B = (EA)(B)/(EAB)
Si A est le substrat qui se fixe le premier, la constante KiB est infinie (B n'a aucune affinité
pour l'enzyme libre) et KA = 0 (A ne pouvant se dissocier du complexe E-A-B, la constante
d'équilibre de dissociation est nulle).
kiB= 0 et KA = 0 cela signifie que B ne peut se fixer sur son site enzymatique que si A se trouve déjà
fixé
L'équation de vitesse se simplifie: V = Kcat.[Et]/1+(KB/[B])+(KiA.KB/[A][B]) (Ka=0)
Les faisceaux de droites concourantes des représentations primaires se coupent au-dessus
de l'axe des abscisses, en un point d'ordonnée 1/Vm. Dans le cas de la représentation en
fonction de 1/[A]; l'abscisse du point d'intersection est - 1/KiA.
Les droites de la représentation primaire de 1/V = f(1/[B]) se coupent sur l'axe des
ordonnées (puisque 1/KiA= 0): aux concentrations saturantes de B, la vitesse mesurée est
égale à Vm, même aux faibles valeurs de A.
Etant donnée que B ne se fixe que sur le complexe E-A, sa présence en excès déplace
l'équilibre entre E et A vers les formes complexées et tout l'enzyme est alors sous la forme E-
A-B; on mesure ainsi la vitesse maximale.
-1/KIA
Représentation Primaire : 1/V = f ( 1/A)
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
Représentation Secondaire
Exemple de bibi ordonné : l’alcool Déshydrogénase :
L’alcool déshydrogénase est une enzyme, catalyse l’oxydation de l’éthanol en acétaldéhyde
en réduisant simultanément un coenzyme NAD+ en NADH.
• Cette réaction se déroule selon un mécanisme de type bibi ordonné : l’enzyme n’a pas
d’affinité pour l’alcool si elle n’est pas préalablement associée au coenzyme NAD + en un
premier complexe ; puis le complexe ternaire Enzyme-NAD+-Ethanol se transforme en un
complexe Enzyme-NADH-Acétaldéhyde ; ce dernier complexe se dissocie en libérant
l’acétaldéhyde puis le NAD réduit.
Exemple de bibi ordonné : la malate Déshydrogénase
La malate déshydrogénase est une enzyme ,catalyse l’oxydation du malate en oxaloacétate en
réduisant simultanément un coenzyme NAD+ en NADH.
• Cette réaction se déroule selon un mécanisme de type bibi ordonné : l’enzyme n’a pas
d’affinité pour le malate si elle n’est pas préalablement associée au coenzyme NAD+ en un
premier complexe ; puis le complexe ternaire Enzyme-NAD+-Malate se transforme en un
complexe Enzyme-NADH-Oxaloacétate ; ce dernier complexe se dissocie en libérant
l’oxaloacétate puis le NAD réduit.
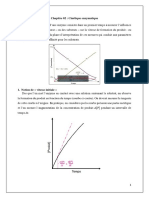
Mécanisme ping-pong :
Si la réaction enzymatique ne nécessite pas la formation d'un complexe ternaire, l'enzyme,
après avoir fixé un des substrats, le transforme et libère le produit correspondant.
L'enzyme ensuite fixe l'autre substrat, le transforme et libère le second produit. C'est le
mécanisme ping-pong qui se distingue des précédents par le fait qu'il intervient, entre les
5
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
étapes de fixation des deux substrats, une étape irréversible en absence des produits de la
réaction.
L'équation de la vitesse in fonction de la concentration des substrats fait apparaître un
comportement Mickaelien, en utilisant l'approximation de l'état stationnaire ou celle du
quasi-équilibre.
Elle est de la forme : V = Kcat [Et]/1+(KA/[A]+KB/[B])
Les représentations primaires de 1/V = f(1/[A]) ou f(1/[B]) sont des droites parallèles.
Comme précédemment, les intersections avec l'axe des ordonnées correspond à 1/Va ou
1/Vb; l'inverse de la vitesse mesurée à concentration saturante du substrat considéré.
L'étude des variations de Va en fonction de [B] permet de déterminer la constante de
Mickaelis de B et la vitesse maximale de la réaction, celle mesurée lorsque les deux substrats
sont saturants.
Représentation secondaire : 1/Vi = f( 1/B) , intersection avec axe des y : 1/Vmax = 1/Kcat, et
avec l’axe des x : -1/KB (KMB pour le substrat B)
Pour le substrat A : tgα(pente) = (1 /Vmax).KMA = KMA /Vmax
Exemple de ping-pong : l’alanine aminotransférase = ALAT
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
L’ALAT catalyse le transfert de la fonction amine de l’alanine vers l’α-cétoglutarate qu’elle
transforme en glutamate.
• Dans un premier temps, l’ALAT se lie à l’alanine puis transfère la fonction amine sur un
coenzyme lié : le phosphate de pyridoxal qui devient phosphate de pyridoxamine sans cesser
d’êtrelié à l’enzyme. L’enzyme se dissocie alors du pyruvate.
• Dans le second temps, l’enzyme liée au phosphate de pyridoxamine, forme un complexe
avec l’α-cétoglutarate, puis transfère la fonction amine du coenzyme qui redevient phosphate
de pyridoxal, vers le second substrat qui est transformé en glutamate. Enfin, le complexe
ALAT glutamate se dissocie : l’enzyme et son coenzyme lié ont recouvré leurs structures
initiales.
- l’aspartate aminotransférase = ASAT
L’ASAT catalyse le transfert de la fonction amine de l’aspartate vers l’α-cétoglutarate qu’elle
transforme en glutamate.
• Dans un premier temps, l’ASAT se lie à l’aspartate puis transfère la fonction amine sur un
coenzyme lié : le phosphate de pyridoxal qui devient phosphate de pyridoxamine sans cesser
d’être lié à l’enzyme. L’enzyme se dissocie alors de l’oxaloacétate.
• Dans le second temps, l’enzyme liée au phosphate de pyridoxamine, forme un complexe
avec l’α-cétoglutarate, puis transfère la fonction amine du coenzyme qui redevient phosphate
de pyridoxal, vers le second substrat qui est transformé en glutamate. Enfin, le complexe
ASAT glutamate se dissocie : l’enzyme et son coenzyme lié ont recouvré leurs structures
initiales.
II - Etude des inhibiteurs :
L'existence de schémas différents, donnant des équations de vitesse à dépendance similaire
vis-à-vis des concentrations des substrats, oblige à compléter l'étude pour analyser le
mécanisme cinétique des réactions.
L'une des méthodes cinétiques souvent utilisée est l'étude des effets des inhibiteurs sur la
vitesse de la réaction soit d'analogues des substrats, soit des produits de la réaction.
1) Etude des analogues de substrat :
L'étude de ces inhibiteurs obéit aux mêmes règles que celles des réactions à un seul
substrat.
-On observe un effet inhibiteur à forte [S] lorsque le substrat et l'inhibiteur sont présents
ensemble sur au moins une forme d'enzyme. On l'observe aussi même lorsque l'inhibiteur et
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
le substrat ne sont jamais présents ensemble, chaque fois que l'excès de substrat ne peut
empêcher la fixation de l'inhibiteur.
-On observe un effet inhibiteur à faible [S] si l'inhibiteur se fixe sur au moins une forme
d'enzyme présente lorsque la [S] tend vers 0.
L'inhibiteur est de type compétitif lorsque l'effet inhibiteur disparaît à forte [S], de type un-
compétitif lorsqu'il n'y a pas d'effet inhibiteur à faible [S], et de type non compétitif lorsque
l'effet inhibiteur existe aussi bien à forte qu'à faible [S].
L'application de ces règles simples au cas des mécanismes à deux substrats permet de définir
le type d'inhibiteur observé pour les analogues, dans les différents schémas, lors des
mesures de vitesses initiales:
a) Fixation séquentielle au hasard, avec approximation du quasi-équilibre :
Un analogue de A est compétitif vis-à-vis de A (sa fixation est exclusive de celle de A);
non compétitif vis-à-vis de B (il peut s'associer à l'enzyme, que B soit fixé ou non).
Un analogue de B est non compétitif vis-à-vis de A, compétitif vis-à-vis de B.
b) Fixation séquentielle ordonnée, avec approximation du quasi-équilibre, A étant le premier
substrat :
Un analogue de A est compétitif vis-à-vis de A et vis-à-vis de B (un excès de B
empêche la fixation de l'inhibiteur par déplacement d'équilibre).
Un analogue de B est un-compétitif vis-à-vis de A (la forme d'enzyme sur laquelle il se
fixe devient très minoritaire lorsque la [A] tend vers 0) et compétitif vis-à-vis de B.
c) Fixation séquentielle ordonnée, avec approximation de l'état stationnaire, A étant le
premier substrat :
Un analogue de A est compétitif vis-à-vis de A, non compétitif vis-à-vis de B (l'excès de
B n'empêche la fixation de l'analogue).
Un analogue de B est un-compétitif vis-à-vis de A, compétitif vis-à-vis de B.
d) Mécanisme ping-pong :
Un analogue de A est compétitif vis-à-vis de A, un-compétitif vis-à-vis de B (la forme
d'enzyme sur laquelle il se fixe devient très minoritaire lorsque la [B] tend vers 0).
Un analogue de B est un-compétitif vis-à-vis de A, compétitif vis-à-vis de B.
Pr.Miloud SLIMANI , Département de Biologie –Université Dr TaharMoulay de Saida
Vous aimerez peut-être aussi
- Resumé ENZYMOLOGIEDocument13 pagesResumé ENZYMOLOGIEislamouahabiPas encore d'évaluation
- Correction TD Enzymologie 5 PDFDocument29 pagesCorrection TD Enzymologie 5 PDFSalah Eddine Msiky90% (10)
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- TD Enzymologie + SolutionDocument5 pagesTD Enzymologie + SolutionAbdel SePas encore d'évaluation
- Mecanismes PDFDocument11 pagesMecanismes PDFAbdoulaye Diallo0% (1)
- TD Enzymo Biochimie Met 1Document31 pagesTD Enzymo Biochimie Met 1Saminat RidjaliPas encore d'évaluation
- Cinétique Enzymatique À 2 SubstratsDocument7 pagesCinétique Enzymatique À 2 Substratsamina44Pas encore d'évaluation
- Cinetique Enz.a 2 Sub1Document14 pagesCinetique Enz.a 2 Sub1Mira45Pas encore d'évaluation
- Cours de Cinetique A Deux SubstratsDocument8 pagesCours de Cinetique A Deux Substratsmistic JayPas encore d'évaluation
- Cours de Cinetique A Deux Substrats PDFDocument7 pagesCours de Cinetique A Deux Substrats PDFJalelo AbdelPas encore d'évaluation
- 06-Cinétique Enzymatique à Deux SubstratsDocument8 pages06-Cinétique Enzymatique à Deux SubstratsSlimkhane DzPas encore d'évaluation
- ENZYMOLOGIE II.2021pptDocument59 pagesENZYMOLOGIE II.2021pptKaren DominiquePas encore d'évaluation
- Kira ADocument5 pagesKira AManon righiniPas encore d'évaluation
- Séance VI - COURS. Enzymologie UE-SF 2Document51 pagesSéance VI - COURS. Enzymologie UE-SF 2Lamisse AbedPas encore d'évaluation
- 2 - Introduction A L - Enzymologie PDFDocument9 pages2 - Introduction A L - Enzymologie PDFGabrielle NnomoPas encore d'évaluation
- 4 - Catalyse Enzymatique PDFDocument14 pages4 - Catalyse Enzymatique PDFPrince Abdoo100% (1)
- 10.03.2016 Les EnzymesDocument14 pages10.03.2016 Les EnzymesEaPas encore d'évaluation
- EnzymologieDocument12 pagesEnzymologieBasmã AlilechePas encore d'évaluation
- Chapitre 6Document7 pagesChapitre 6maryam.dellalPas encore d'évaluation
- Introduction EnzymatologieDocument9 pagesIntroduction Enzymatologiefiras7Pas encore d'évaluation
- 3 Chapitre II EnzymesDocument62 pages3 Chapitre II EnzymesNour El HoudaPas encore d'évaluation
- La Cinétique EnzymatiqueDocument6 pagesLa Cinétique EnzymatiqueTCHEMMIK NazihaPas encore d'évaluation
- Chap 2-La Structure Des ProteinesDocument10 pagesChap 2-La Structure Des ProteinesClément LabitriePas encore d'évaluation
- Cours Enzymologie 2022Document86 pagesCours Enzymologie 2022Adja Aïta BaPas encore d'évaluation
- 2 лекция ферментыDocument10 pages2 лекция ферментыE BPas encore d'évaluation
- Kira DriveDocument7 pagesKira DriveManon righiniPas encore d'évaluation
- Enzymologie TP Invertase PolycopieDocument14 pagesEnzymologie TP Invertase Polycopieiliass lahmassPas encore d'évaluation
- 7 - Mécanisme de La CatalyseDocument34 pages7 - Mécanisme de La Catalyseangelo.terrisse1Pas encore d'évaluation
- 4e DS1 2010 2011Document4 pages4e DS1 2010 2011fethi10% (1)
- Biochimie1an-Cinetique Enzymatique2020feraga PDFDocument4 pagesBiochimie1an-Cinetique Enzymatique2020feraga PDFAsmaPas encore d'évaluation
- Génie Enzymologique - Asmaa BenjrinijaDocument19 pagesGénie Enzymologique - Asmaa BenjrinijaLEMRAHRI kaheliPas encore d'évaluation
- CM CHI 201 - 2022 Royal Partie 1Document53 pagesCM CHI 201 - 2022 Royal Partie 1Vera Legba-MonyPas encore d'évaluation
- 3a - Cinetique EnzymatiqueDocument8 pages3a - Cinetique EnzymatiqueSameh Khemir100% (2)
- Chapitre1 Chimie Organique 2Document8 pagesChapitre1 Chimie Organique 2jean luc abdias konanPas encore d'évaluation
- Chapitre 4 Cinétique Et InhibitionDocument14 pagesChapitre 4 Cinétique Et Inhibitionkgu yryrtyPas encore d'évaluation
- Chapitre 02 Cinétique EnzymatiqueDocument5 pagesChapitre 02 Cinétique Enzymatiqueamina44Pas encore d'évaluation
- Enymo1 PDFDocument51 pagesEnymo1 PDFELALLAM YOUSSEFPas encore d'évaluation
- Cinétique EnzymatiqueDocument14 pagesCinétique Enzymatiqueرزقي إبن فلسطينPas encore d'évaluation
- Chapitre 1 Définition, Classification Et StructureDocument10 pagesChapitre 1 Définition, Classification Et Structureryadh2203Pas encore d'évaluation
- Fiche D'exercicesDocument3 pagesFiche D'exercicesNjounhassi PatricePas encore d'évaluation
- Je partage « 4_5969563937924977041 » avec vousDocument6 pagesJe partage « 4_5969563937924977041 » avec vouskerdartsPas encore d'évaluation
- Cinétique À Deux Substrat.mDocument9 pagesCinétique À Deux Substrat.mKEBIR ZAHRAPas encore d'évaluation
- Examen Enzymologie Et Métabolisme 2021 - Session Normale CorrigéDocument5 pagesExamen Enzymologie Et Métabolisme 2021 - Session Normale Corrigéa.elabbassiPas encore d'évaluation
- Cours Cinetique Et Catalyse Homogene La CatalyseDocument23 pagesCours Cinetique Et Catalyse Homogene La Catalysemohamed.mohamed-aminePas encore d'évaluation
- DM N°1 de Biochimie:: Tutorat 2012 - 2013Document6 pagesDM N°1 de Biochimie:: Tutorat 2012 - 2013kamiliaPas encore d'évaluation
- Compilés EnzymologieDocument5 pagesCompilés EnzymologieHadrien De GreefPas encore d'évaluation
- Chap 11 CDocument4 pagesChap 11 CStachis Madiamba100% (1)
- Exam L2 Biochimie Session 1 2019 + Corrigã©Document5 pagesExam L2 Biochimie Session 1 2019 + Corrigã©ssicuriniPas encore d'évaluation
- Polycopié Catalyse 21 22Document18 pagesPolycopié Catalyse 21 22mehdi manaaPas encore d'évaluation
- Cin Tique Et Catalyse HomogŠnePDocument20 pagesCin Tique Et Catalyse HomogŠnePKhaled BouchaourPas encore d'évaluation
- Cours Cinétique SabeurDocument4 pagesCours Cinétique SabeurSabeur Khemakhem100% (1)
- Réactivité en Chimie Organique PDFDocument9 pagesRéactivité en Chimie Organique PDFAchwak BelfadelPas encore d'évaluation
- Cinetique Enzy 2Document44 pagesCinetique Enzy 2DidaLalouPas encore d'évaluation
- Chap 4Document13 pagesChap 4Chihab GhlalaPas encore d'évaluation
- Cinetique Enzymatique-1 PDFDocument15 pagesCinetique Enzymatique-1 PDFTCHEMMIK NazihaPas encore d'évaluation
- 6 Mecani 2015Document19 pages6 Mecani 2015Zizou LeePas encore d'évaluation
- UE1-chimie - 5 - Mécanismes RéactionnelsDocument16 pagesUE1-chimie - 5 - Mécanismes Réactionnelssun-nee-chan9Pas encore d'évaluation
- ENS-CACHAN Chimie-Moleculaire 2013 PDFDocument15 pagesENS-CACHAN Chimie-Moleculaire 2013 PDFHamza TadlawiPas encore d'évaluation
- TD 01 EnzymologieDocument2 pagesTD 01 EnzymologieBENYAHIA NESRINEPas encore d'évaluation
- Vocabulaire - Biochimie IIDocument3 pagesVocabulaire - Biochimie IIRafaPas encore d'évaluation
- Le Metier de Scripte Face A La Diversité Des Langages CinematographiquesDocument60 pagesLe Metier de Scripte Face A La Diversité Des Langages CinematographiquesArturo Avendaño MorineauPas encore d'évaluation
- Financial & Lifestyle Magazine 03 - FR - of Puilaetco Dewaay Private BankersDocument86 pagesFinancial & Lifestyle Magazine 03 - FR - of Puilaetco Dewaay Private BankersDominiek VanwynsberghePas encore d'évaluation
- Capsule 2&3 Du 19-12-2023 & 26-12-2023Document43 pagesCapsule 2&3 Du 19-12-2023 & 26-12-2023oussou othmanePas encore d'évaluation
- CocaDocument5 pagesCocatheobromine100% (4)
- Year 7 French TestDocument6 pagesYear 7 French TestSama HelmyPas encore d'évaluation
- Le BachelierDocument642 pagesLe BachelierMr. AndroidPas encore d'évaluation
- Exercices Pages 119,121,173Document2 pagesExercices Pages 119,121,173JudaPas encore d'évaluation
- Manuel Du Voyageur en Italie (... ) Giegler Jean-Pierre Bpt6k56988717Document712 pagesManuel Du Voyageur en Italie (... ) Giegler Jean-Pierre Bpt6k56988717mediacalabriaPas encore d'évaluation
- Entretien Rampe de FiltrationDocument28 pagesEntretien Rampe de FiltrationFATMA YOUCEFIPas encore d'évaluation
- Memoire de Sortie 3Document123 pagesMemoire de Sortie 3Willy JasminPas encore d'évaluation
- M&ADocument12 pagesM&AManuel YounesPas encore d'évaluation
- Ebook - Les 7 Conseils Pour Réussir Son TOEICDocument10 pagesEbook - Les 7 Conseils Pour Réussir Son TOEICaigle d'orPas encore d'évaluation
- CHARLES HENRY Cercle ChromatiqueDocument170 pagesCHARLES HENRY Cercle ChromatiqueCarlos López CharlesPas encore d'évaluation
- 100 Mots Espagnol Pas À PasDocument2 pages100 Mots Espagnol Pas À PasDebPas encore d'évaluation
- La Situation ComplexeDocument25 pagesLa Situation ComplexeArouna KonePas encore d'évaluation
- Les Gisements Et Les Problèmes D'eauDocument9 pagesLes Gisements Et Les Problèmes D'eauGhislain Atche100% (4)
- Le ClassicismeDocument2 pagesLe Classicismejismail100% (1)
- Traités Et Accords Concernant Le (... ) Rouard de bpt6k141228r PDFDocument145 pagesTraités Et Accords Concernant Le (... ) Rouard de bpt6k141228r PDFElamrani KarimPas encore d'évaluation
- Le Petit Forestier 1 2Document20 pagesLe Petit Forestier 1 2Anonymous 476I0KkRPas encore d'évaluation
- TETES OUVRAGES HYDRAULIQUE TYPE BUSES AUTOCAD - Recherche GoogleDocument2 pagesTETES OUVRAGES HYDRAULIQUE TYPE BUSES AUTOCAD - Recherche GoogleBraised.Mountains-Association AssociationPas encore d'évaluation
- Pec Concomitante EsmsDocument1 pagePec Concomitante EsmsLaëtitia FraissePas encore d'évaluation
- Programme Festival Rendez-Vous Contes !Document24 pagesProgramme Festival Rendez-Vous Contes !magali schaalPas encore d'évaluation
- RESEAUX CELLULAIRES 5G LFI3 Chaabane Ali Ben Maouia Takoua Heni KoussayDocument15 pagesRESEAUX CELLULAIRES 5G LFI3 Chaabane Ali Ben Maouia Takoua Heni KoussayPFE100% (1)
- Convenances Spirituelles de La Voie Adab Et Tariq PDFDocument42 pagesConvenances Spirituelles de La Voie Adab Et Tariq PDFludovic1970Pas encore d'évaluation
- VesteDocument5 pagesVesteMaxPas encore d'évaluation
- Tawhid1 PDFDocument19 pagesTawhid1 PDFAndré SovaĝaPas encore d'évaluation
- TD4 Régulation Zigler Broida TAP74 Rev3 18012021Document3 pagesTD4 Régulation Zigler Broida TAP74 Rev3 18012021Abderraouf HARCHEPas encore d'évaluation
- 13 Exos Geometrie EspaceDocument17 pages13 Exos Geometrie Espacemogala2392Pas encore d'évaluation
- Boostrap ElazzabyDocument59 pagesBoostrap ElazzabyhassaniPas encore d'évaluation
- L'Aventure Chevaleresque - Eric KohlerDocument2 pagesL'Aventure Chevaleresque - Eric KohlerSombre Arcane ZinePas encore d'évaluation