Académique Documents
Professionnel Documents
Culture Documents
2020 Rat CRC
Transféré par
douchnaima09Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2020 Rat CRC
Transféré par
douchnaima09Droits d'auteur :
Formats disponibles
Nom : |_|_|_|_|_|_|_|_|_|_|_|_| N° Examen : |_|_|_|_|
Prénom : |_|_|_|_|_|_|_|_|_|_|_|_| CNE : |_|_|-|_|_|_|_|_|_|_|_|
Filière : SMC6 – EXAMEN DU Module : C H . D E S CR I P T I V E II & C H . DE C O O RD I N AT I ON
Session : R A T T R A P A G E – Date : 19 OCT OB R E 2020 – Durée : 1 H 30
I. Soient les complexes et les ions complexes
Isomérie optique pour Cis
suivants :
(a) [CoNO2(NH3)5]Cl ; (µexp = 1,72 MB) ;
(b) [CoCl2(en)2]+ ; (µexp = 4,90 MB) ;
(c) Chlorure de -hydroxobis(pentaammine chrome
(III)) ; (c) Isomérie d’ionisation: [(NH3)5Co-OH-
(d) [Cu(NH3)2]+ ; (µexp = 0 MB) ; Co(NH3)5]Cl5 et [(NH3)5Co-Cl-Co(NH3)5]Cl4,OH
(e) [Ni(CO)4] ; (µexp = 0 MB) ; 2 4. Donner, en justifiant votre réponse, le type
d’hybridation du métal en appliquant la théorie de
(f) Ion de dichlorotétraammine cobalt (III).
la liaison de valence pour les composés (a), (b),
½ 1. Donner les formules correspondant aux (d) et (e).
espèces suivantes : (a) Co2+ : …3d7
(c) [(NH3)5Cr-OH-Cr(NH3)5]Cl5 Puisque exp(a) = 1,72 MB, on doit avoir 1 électron
(f) [CoCl2(NH3)4]+ célibataire, donc 3 orbit. 3d seront pleines et un
électron passe sur l’orb. 4d d’où hybridation d2sp3 .
1 2. Donner les noms des espèces ci-dessous :
↑↓ ↑↓ ↑↓
(a) Chlorure de nitropentaammine cobalt (II)
(b) Ion dichlorobis(éthylènediamine) cobalt (III) (b) Co3+ : …3d6 ; puisque exp(b) = 4,9 MB, on doit
avoir 4 électrons célibataires, donc toutes les
(d) Ion diammine cuivre (I)
orbitales seront pleines d’où hybridation sp3d2 .
(e) Tétracarbonyl nickel (0)
↑↓ ↑ ↑ ↑ ↑
2 3. Donner et représenter les différents isomères
(d) Cu+ : …4s13d9 ; puisque exp(d) = 0, on aura un
pour les composés (a), (b) et (c).
arrangement des électrons qui va conduire à une
(a) Isomérie de liaison et d’ionisation : orbitale 4s vide et 3d saturée, donc
hybridation sp puisque le composé est linéaire.
[CoNO2(NH3)5]Cl et [CoCl(NH3)5]NO2
[CoNO2(NH3)5]Cl et [CoONO(NH3)5]Cl ↑↓ ↑↓ ↑↓ ↑↓ ↑↓
(e) Ni : …4s23d8 ; puisque exp(e) = 0, on aura un
(b) Isomérie géométrique : cis – trans
arrangement des électrons qui va conduire à une
orbitale 4s vide et 3d saturée, donc hybridation
sp3 puisque le composé est tétracoordonné.
↑↓ ↑↓ ↑↓ ↑↓ ↑↓
trans cis Données : Z(Co) = 27 ; Z(Ni) = 28 ; Z(Cu) = 29
II. Soit l’ion complexe [Fe(C2O4)2(en)] m avec m la III. En appliquant la théorie du champ cristallin :
charge de l’ion complexe. Son moment magnétique
expérimental est µexp = 1,75 MB. ½ 1. Comparer l’énergie de dédoublement
½ 1. Déduire le nombre d’électrons célibataires. t2g - eg () entre les complexes [Co(C2O4)(en)2] et
[Rh(C2O4)(en)2].
µexp = √n(n + 2) = 1,75 MB
→ n = 1 électron célibataire Co2+ : …3d7 et Rh2+ : …4d7 (même groupe)
1½ 2. Sachant que le numéro atomique du fer est Co2+ → 1re série des métaux de transition,
Z = 26, déterminer la valeur de la charge m de l’ion Rh2+ → 2e série → o(Rh2+) > o(Co2+)
complexe en utilisant la théorie de Pauling et en
supposant la présence du Fe2+ ou la présence du 1 2. Comment se situe par rapport à l’énergie
Fe3+. d’appariement pour les deux composés ?
- Présence du Fe : Fe : …3d
2+ 2+ 6
* [Co(C2O4)(en)2] :
Si Chp. faible → 4 élec célib. ↑↓ ↑ ↑ ↑ ↑
< (Champ faible : HS)
Si Chp. fort → 0 élec célib. ↑↓ ↑↓ ↑↓ * [Rh(C2O4)(en)2] :
[Fe(C2O4)2(en)] m possède 1 e- célib. donc pas de > (Champ faible : BS)
Fe2+
1 3. Calculer leur moment magnétique.
- Présence du Fe3+ : Fe3+ : …3d5
* [Co(C2O4)(en)2] ↑ ↑ eg
Si Chp. faible → 5 élec célib. ↑ ↑ ↑ ↑ ↑
↑↓ ↑↓ ↑ t2g
Si Chp. fort → 1 élec célib. ↑↓ ↑↓ ↑ µ = 3,87 MB
Avec Fe3+ on a bien 1 élec célib., on peut donc * [Rh(C2O4)(en)2] ↑ eg
calculer la charge : m = +3(Fe) -4(C2O4) → m = -1
↑↓ ↑↓ ↑↓ t2g
1½ 3. On substitue le ligand éthylènediamine (en) par µ = 1,73 MB
-
les ligands CN . Donner pour le nouveau composé :
1½ 4. Les 2 complexes ont un entourage octaédrique,
a. La formule avec la nouvelle charge.
expliquer, en justifiant votre réponse, pourquoi les
-3
[Fe(CN)2(C2O4)2] deux polyèdres (géométries) sont différents ?
([Fe(C2O4)2(CN)2]-3 est comptée aussi juste)
* [Co(C2O4)(en)2]
b. Le moment magnétique.
Co2+ : ...3d7 ; conf. HS → on aura une répartition
Les ligands CN- créent un champ fort
égale des électrons sur les orbitales t2g et eg.
→ donc on aura toujours un seul élec. célibataire.
→ µ = 1,73 MB. → Octaèdre régulier
c. Le changement de couleur par rapport au * [Rh(C2O4)(en)2]
composé de départ (donner le sens).
Rh2+ : ...4d7 ; conf. BS → répartition inégale des
-
CN crée un champ plus fort que (en) élect. sur les orbit. eg → déformation (allongement
→ Δo(CN-) > Δo(en) d’où (CN-) < (en) ou aplatissement) de l’octaèdre (effet J.T).
→ Déplacement vers l’UV. Données : Z(Co) = 27 ; Z(Rh) = 45
IV. Le monoxyde de titane TiO possède la même V. En utilisant la théorie du champ cristallin :
structure que l’oxyde CrO. 2½ 1. Montrer, en supposant que l’oxygène crée un
½ 1. Ecrire la formule de la solution solide de champ faible, que ZnMn2O4 est un spinelle direct.
substitution de titane par le chrome qui peut
exister entre ces deux composés ? - Energie de stabilisation de Zn :
Zn2+ ...3d10
(1-x) TiO + x CrO → Ti1-x Crx O
avec 0 ≤ x ≤ 1 Es[6] = 6 2/5 o – 4 3/5 o = 0
Es[4] = 4 3/5 t – 6 2/5 t = 0
……………………………………………………..
2 ½ 2. Tracer la courbe représentative de - Energie de stabilisation de Mn :
l’évolution de la constante de Curie C de cette Mn3+ : ...3d4
solution solide en fonction de x (C = f(x)).
Es[6] = 3 2/5 o – 1 3/5 o = 3/5 o
2+ 2+
Ct = (1-x) C(Ti ) + x C(Cr ) Es[4] = 2 3/5 t – 2 2/5 t = 2/5 t = 1/5 o
Ti2+ : ...3d2 → (Ti2+) = 2,83 MB
- Energie de stabilisation du spinelle directe SD :
(Ti2+) = √8C(Ti ) → C(Ti2+) = 8/8 = 1
2+
* SD → Zn2+[ Mn3+2]O4
Cr2+ : ...3d4 → (Cr2+) = 4,9 MB Es = 0 + 2 3/5 o = 6/5 o
(Cr2+) = √8C(Cr2+) → C(Cr2+) = 24/8 = 3
- Energie de stabilisation du spinelle indirecte SI :
→ Ct = (1-x) CTi2+ + x CCr2+ = (1-x) 1 + x 3 * SI → Mn3+[Zn2+ Mn3+]O4
d’où Ct = 1 + 2x
E’s = 1/5 o + 0 + 3/5 o = 4/5 o
Courbe C=f(x)
Conclusion : On a Es(SD) > E’s(SI)
→ la configuration stable est le spinelle SD
1 2. Expliquer pourquoi la structure de ce spinelle
présente une symétrie quadratique (justifier votre
réponse).
Spinelle directe → Mn3+ en site octa.
Mn3+ : ...3d4 ; configuration HS car l’oxygène crée
un champ faible :
↑ eg
↑ ↑ ↑ t2g
½ 3. Quel est l’intérêt d’une telle courbe ? On a une répartition inégale des élec. sur les
orbitales eg → déformation (effet J.T).
Elle permet de déterminer la formule d’une
Puisqu’on a une symétrie quadratique, donc on
solution solide connaissant son moment
aura un allongement de l’octaèdre selon l’axe z, car
magnétique ou sa constante de Curie et
l’électron se place sur l’orbitale dz2.
inversement
Données :
Données : Z(Ti) = 22 ; Z(Cr) = 24 Z(Mn) = 25 ; Z(Zn) = 30
Vous aimerez peut-être aussi
- 2020 NR CRCDocument3 pages2020 NR CRCdouchnaima09Pas encore d'évaluation
- Chi CoordDocument11 pagesChi CoordAbderrahim BelmJouJPas encore d'évaluation
- SMC6 TD Série 3 Chimie de CoordinationDocument3 pagesSMC6 TD Série 3 Chimie de CoordinationKarin Wambu73% (11)
- Annales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésD'EverandAnnales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésÉvaluation : 4.5 sur 5 étoiles4.5/5 (4)
- TD N°1-Corrigé Ex 9 À 21Document5 pagesTD N°1-Corrigé Ex 9 À 21lucas lucasPas encore d'évaluation
- Exercices Chimie Des MatériauxDocument14 pagesExercices Chimie Des Matériaux7box.bePas encore d'évaluation
- TD Chimie de CoordinationDocument13 pagesTD Chimie de Coordinationayyoub dhb29% (7)
- Cor Seance 2Document6 pagesCor Seance 2Paul Mbede SedenaPas encore d'évaluation
- EXO4Document6 pagesEXO4Arthur Franck Patrick BledouPas encore d'évaluation
- Corrigé CNC Chimie 2012 MPDocument6 pagesCorrigé CNC Chimie 2012 MPzazazaz2000100% (1)
- Oxydo - Réduction Sujet Et CorrigéDocument6 pagesOxydo - Réduction Sujet Et Corrigémehdi benmassoudPas encore d'évaluation
- Devoir de Synthèse N°3 2012 2013 (Ramzi Rebai)Document4 pagesDevoir de Synthèse N°3 2012 2013 (Ramzi Rebai)Abderahmen Haj DahmenPas encore d'évaluation
- 2016 NRDocument4 pages2016 NRdouchnaima09Pas encore d'évaluation
- TD - Electrochimie - IUT Bobo Mai 2022Document5 pagesTD - Electrochimie - IUT Bobo Mai 2022Abdoul Kader OUATTARAPas encore d'évaluation
- TD PH SymetrieM Serie3 19Document2 pagesTD PH SymetrieM Serie3 19jalilpadawou55Pas encore d'évaluation
- 2008 Examen Chimie Mai SolveDocument3 pages2008 Examen Chimie Mai SolvekarimovPas encore d'évaluation
- TD 3 Avec Corrigé de Chimie en SolutionDocument7 pagesTD 3 Avec Corrigé de Chimie en SolutionETUSUPPas encore d'évaluation
- TD Chimie Inorganique 1: A. Termes de L'ion LibreDocument4 pagesTD Chimie Inorganique 1: A. Termes de L'ion LibreYoussef ChePas encore d'évaluation
- Corrigà SÃrie NÂ4Document13 pagesCorrigà SÃrie NÂ4Raouia MakhloufPas encore d'évaluation
- 1 Polycopié TP S6 CHMDocument12 pages1 Polycopié TP S6 CHMChoaib NouhyPas encore d'évaluation
- E3a 2007 PDFDocument4 pagesE3a 2007 PDFJean Donald BonyPas encore d'évaluation
- Introduction A La Science PolitiqueDocument8 pagesIntroduction A La Science PolitiqueAs NordinePas encore d'évaluation
- 2017-2018 IE2 CorrigeDocument4 pages2017-2018 IE2 CorrigeEugene FoucherPas encore d'évaluation
- Redox ExoDocument10 pagesRedox ExoAbdo AiaichePas encore d'évaluation
- TD 5 Structure de La Matière + CorrectionDocument6 pagesTD 5 Structure de La Matière + CorrectionKhawla ChoukriPas encore d'évaluation
- PolyChimie PDFDocument39 pagesPolyChimie PDFLarbi BadrourPas encore d'évaluation
- CPI101 DS2 Decembre2010 CORRDocument4 pagesCPI101 DS2 Decembre2010 CORRSamah SamahPas encore d'évaluation
- Examens de Chimie de Coordination PDFDocument17 pagesExamens de Chimie de Coordination PDFPower Smox70% (10)
- 2011 Examen Mai Solve PDFDocument7 pages2011 Examen Mai Solve PDFkarimovPas encore d'évaluation
- TD BCG C244 Chimie Minerale 1 2021Document8 pagesTD BCG C244 Chimie Minerale 1 2021imad sahliPas encore d'évaluation
- Cnc-Chimie-Mp-19999a CorrigéDocument7 pagesCnc-Chimie-Mp-19999a CorrigéAz-eddine KaibaPas encore d'évaluation
- Devoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaDocument7 pagesDevoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaTawfiq Weld EL ArbiPas encore d'évaluation
- Chapitre II Liaisons Chimiques 19-20Document24 pagesChapitre II Liaisons Chimiques 19-20bouikheffatimaezzahraPas encore d'évaluation
- TD 04 Corrige-Liaisons ChimiquesDocument14 pagesTD 04 Corrige-Liaisons ChimiquesAlbert SamaPas encore d'évaluation
- Serie 2-1 PDFDocument15 pagesSerie 2-1 PDFMoha T OmpPas encore d'évaluation
- Devoir de Synthèse N°3 Avec Correction - Sciences Physiques - Bac Sciences Exp (2015-2016) MR BARHOUMI EZZEDINEDocument10 pagesDevoir de Synthèse N°3 Avec Correction - Sciences Physiques - Bac Sciences Exp (2015-2016) MR BARHOUMI EZZEDINEMohamed SaidiPas encore d'évaluation
- TD 4 Avec Corrigé de Chimie Des SolutionsDocument7 pagesTD 4 Avec Corrigé de Chimie Des SolutionsETUSUP100% (1)
- Ellingham ExercicesDocument6 pagesEllingham ExercicesBerenger MabéléPas encore d'évaluation
- 8.les Reactions D' Oxydo ReductionDocument12 pages8.les Reactions D' Oxydo ReductionMétatron GamesPas encore d'évaluation
- Chimie Descriptive-El3d PDFDocument12 pagesChimie Descriptive-El3d PDFayoub dahbiPas encore d'évaluation
- Bac Blanc 2009Document7 pagesBac Blanc 2009Seif Souid67% (3)
- Exercices TD Introduction État Solide 2017-2018Document12 pagesExercices TD Introduction État Solide 2017-2018héma tologie100% (1)
- TD Chimie Minerale Descriptive L2 PC 2019-2020 PDFDocument4 pagesTD Chimie Minerale Descriptive L2 PC 2019-2020 PDFMaxwell Boussin83% (6)
- EF Chimie 1 14 01 2018Document2 pagesEF Chimie 1 14 01 2018Nadia Ait AhmedPas encore d'évaluation
- Exercices Atomes PolyDocument2 pagesExercices Atomes Polyعادل الحمديPas encore d'évaluation
- Examen Finaux Et Corrigé - 230516 - 232706Document37 pagesExamen Finaux Et Corrigé - 230516 - 232706bensalimyoussef94Pas encore d'évaluation
- ChemDocument5 pagesChemAnonymous svBEhGhEIPas encore d'évaluation
- AoutDocument2 pagesAoutBaroka julien YANEPas encore d'évaluation
- Diapo Coord 2016 2017 Belghiti - pdf418411674Document98 pagesDiapo Coord 2016 2017 Belghiti - pdf418411674CHEIKH ABDOUL AZIZ H'MEIDYPas encore d'évaluation
- Tp1 de CristallographieDocument14 pagesTp1 de CristallographieHAMZA AZZAARIPas encore d'évaluation
- Cristallochimie S5 Ayoub PDFDocument49 pagesCristallochimie S5 Ayoub PDFkoko kimaPas encore d'évaluation
- Épreuve Sciences Physiques Classe 4ème Sciences 1 Prof: Chebbi RachidDocument4 pagesÉpreuve Sciences Physiques Classe 4ème Sciences 1 Prof: Chebbi RachidMohamed SaidiPas encore d'évaluation
- TD Rev Cristallo 2018Document4 pagesTD Rev Cristallo 2018اجي تقرىPas encore d'évaluation
- DS 2 Orga PCSI + Binaires LV + Solutions + OA OM - CompressedDocument9 pagesDS 2 Orga PCSI + Binaires LV + Solutions + OA OM - CompressedAbdelbassit FadilPas encore d'évaluation
- 205 Chapitre 2Document44 pages205 Chapitre 2Imed SeghierPas encore d'évaluation
- TD-Série #4Document2 pagesTD-Série #4Snaptube 2022Pas encore d'évaluation
- Fiche TD-5 Avec CorrigéDocument6 pagesFiche TD-5 Avec CorrigéFarouk AliPas encore d'évaluation
- 2019 NRDocument4 pages2019 NRdouchnaima09Pas encore d'évaluation
- 2016 RatDocument3 pages2016 Ratdouchnaima09Pas encore d'évaluation
- 2017 NR ExamDocument3 pages2017 NR Examdouchnaima09Pas encore d'évaluation
- 2016 NRDocument4 pages2016 NRdouchnaima09Pas encore d'évaluation
- 2016 Rat CRTDocument3 pages2016 Rat CRTdouchnaima09Pas encore d'évaluation
- 2015 Rat ExamDocument3 pages2015 Rat Examdouchnaima09Pas encore d'évaluation
- 2015 NRDocument4 pages2015 NRdouchnaima09Pas encore d'évaluation
- 2021 NRDocument4 pages2021 NRdouchnaima09Pas encore d'évaluation
- 2015 Rat CRTDocument3 pages2015 Rat CRTdouchnaima09Pas encore d'évaluation
- Trans 2 Sens Cours FilaliDocument5 pagesTrans 2 Sens Cours FilaliMohammed HassaniPas encore d'évaluation
- F - Plastic Cement - Fiche TechniqueDocument2 pagesF - Plastic Cement - Fiche TechniqueAlexandre RogerPas encore d'évaluation
- Controle 1 - 5 S1 PC 1bac FRDocument3 pagesControle 1 - 5 S1 PC 1bac FRbrinimed06gmail.comPas encore d'évaluation
- Chimie 1Document4 pagesChimie 1tcheva jokhanan TiambiPas encore d'évaluation
- Chimie 2nd C Evaluation 3Document2 pagesChimie 2nd C Evaluation 3FREDERIC NOUGEPas encore d'évaluation
- Boite Pharmacie (BPH) Chek-List ModuleDocument3 pagesBoite Pharmacie (BPH) Chek-List Modulekassou hse100% (2)
- CCT 46Document27 pagesCCT 46Lharrak SimoPas encore d'évaluation
- Dermatites de Contact Professionnelles Chez Les Personnels de SantéDocument19 pagesDermatites de Contact Professionnelles Chez Les Personnels de Santéfayssal bouakazPas encore d'évaluation
- Ece 23 PC 48Document5 pagesEce 23 PC 48AlbacaPas encore d'évaluation
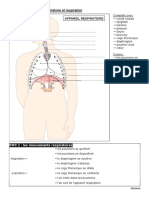
- Appareil Respiratoire Et RespirationDocument4 pagesAppareil Respiratoire Et Respirationwaly sowPas encore d'évaluation
- c03 Lubrification A05Document26 pagesc03 Lubrification A05haoues23Pas encore d'évaluation
- Chap 02Document55 pagesChap 02sarraboulanouar79Pas encore d'évaluation
- TP 2 Godet FernandezDocument5 pagesTP 2 Godet Fernandezsos cissonPas encore d'évaluation
- Etude de La Qualite Des Huiles - Mohammed FEDOUL - 4025Document43 pagesEtude de La Qualite Des Huiles - Mohammed FEDOUL - 4025TAMKOUKT MohamedPas encore d'évaluation
- Article IDDocument4 pagesArticle IDImoona iiPas encore d'évaluation
- Tehnologie Farmaceutica Vol 4Document340 pagesTehnologie Farmaceutica Vol 4Funebre NimoPas encore d'évaluation
- Cours Respiratoire1Document117 pagesCours Respiratoire1Rachida FAOUZI100% (1)
- Memoire de Fin D'Etude: Etude de L'effet Des Cycles Thermiques Sur Le Superalliage À Base Nickel INC 738 LCDocument128 pagesMemoire de Fin D'Etude: Etude de L'effet Des Cycles Thermiques Sur Le Superalliage À Base Nickel INC 738 LCMEHDA AMARAPas encore d'évaluation
- 3iem Seq PCTDocument4 pages3iem Seq PCTBelmond NONOPas encore d'évaluation
- Récap TP 2018 2019 FR PDFDocument49 pagesRécap TP 2018 2019 FR PDFGhina El EssPas encore d'évaluation
- 15 C3a9lectrolyseDocument10 pages15 C3a9lectrolyseazerfazPas encore d'évaluation
- ATOMISTIQUEDocument7 pagesATOMISTIQUEImmeed DaahmaniiPas encore d'évaluation
- Quantité de HHO Idéale - Générateur HHODocument5 pagesQuantité de HHO Idéale - Générateur HHOFlorine RazaiarimalalaPas encore d'évaluation
- TD TC-D Chimie Septembre N°1Document4 pagesTD TC-D Chimie Septembre N°1Jacqueline AlliancePas encore d'évaluation
- J1302 - Transfert de Matières Et de Chaleur Au Sein Des AdsorbantsDocument8 pagesJ1302 - Transfert de Matières Et de Chaleur Au Sein Des AdsorbantsfahimPas encore d'évaluation
- AcétonitrileDocument11 pagesAcétonitrileyodhurPas encore d'évaluation
- Cours 3 - 04112020 GandonDocument59 pagesCours 3 - 04112020 GandonzddzPas encore d'évaluation
- Serie I - Les GlucidesDocument6 pagesSerie I - Les GlucidesIman BelhadiaPas encore d'évaluation
- Ain El Atti TafilaletDocument7 pagesAin El Atti TafilaletIMMELOUI MohamedPas encore d'évaluation
- Chap 4 Chimie OrganiqueDocument10 pagesChap 4 Chimie Organiquedonfack paulPas encore d'évaluation
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Harmonisation Energétique des Personnes: Manuel de Curothérapie 2020D'EverandHarmonisation Energétique des Personnes: Manuel de Curothérapie 2020Évaluation : 4 sur 5 étoiles4/5 (8)
- Revue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteD'EverandRevue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteÉvaluation : 3 sur 5 étoiles3/5 (3)
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Production et propagation des sons: Les Grands Articles d'UniversalisD'EverandProduction et propagation des sons: Les Grands Articles d'UniversalisPas encore d'évaluation
- Affirmations positives : Perte de poids pour les femmesD'EverandAffirmations positives : Perte de poids pour les femmesPas encore d'évaluation
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Conception & Modélisation CAO: Le guide ultime du débutantD'EverandConception & Modélisation CAO: Le guide ultime du débutantPas encore d'évaluation
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Semer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumeD'EverandSemer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumePas encore d'évaluation
- Mes inventions (Traduit): Autobiographie de Nikola TeslaD'EverandMes inventions (Traduit): Autobiographie de Nikola TeslaÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Physique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresD'EverandPhysique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresÉvaluation : 5 sur 5 étoiles5/5 (2)