Académique Documents
Professionnel Documents
Culture Documents
Deficit Immunitaire
Transféré par
Christian MartensTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Deficit Immunitaire
Transféré par
Christian MartensDroits d'auteur :
Formats disponibles
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 551
I - 8 Q 115bis
RR
DÉFICIT IMMUNITAIRE
Dr Felipe Suarez
Service d’hématologie adulte, hôpital Necker-Enfants malades, 75743 Paris Cedex 15, France
felipe.suarez@nck.aphp.fr
OBJECTIFS
ARGUMENTER les principales
situations cliniques et/ou biologiques
Système
faisant suspecter un déficit immunitaire immunitaire
chez l’adulte et chez l’enfant.
Défense contre Mécanismes
les infections homéostatiques
es déficits immunitaires regroupent plusieurs affections
L touchant le système immunitaire qui entraînent des infec-
tions inhabituelles par leur répétition, leur sévérité, ou par
l’agent infectieux impliqué (infections opportunistes). Le système
Immunosurveillance
antitumorale
immunitaire participant aussi à l’homéostasie générale de l’orga-
nisme (cicatrisation ou développement de tumeurs malignes, Infections Auto-immunité
tolérance du soi), des manifestations allant de l’auto-immunité au
développement de tumeurs malignes peuvent également être
observées au cours des déficits immunitaires (fig. 1).
Agents infectieux Prolifération
oncogéniques lymphocytaire inadaptée
Différentes fonctions du système immunitaire :
rappels de physiologie (tableau 1)
Système immunitaire inné Tumeurs
Il permet une réponse rapide aux infections. Il se compose du malignes
complément, des cellules phagocytaires (polynucléaires neutro-
philes et macrophages) et des lymphocytes NK (natural killer). Le
complément facilite l’élimination de certains pathogènes (opsoni- FIGURE 1 Diversité des complications survenant au cours d’un déficit
sation, lyse par le complexe d’attaque des membranes). Les immunitaire.
polynucléaires neutrophiles et les macrophages phagocytent les
agents pathogènes et les détruisent dans des vacuoles (phago-
lysosomes). Les lymphocytes NK lysent directement les cellules antigènes sont générés par la recombinaison somatique de plusieurs
infectées ou transformées par la sécrétion d’enzymes comme la dizaines de segments géniques codés dans le génome (V, D, J),
perforine. permettant une diversité de reconnaissance quasiment infinie.
Cette recombinaison V(D)J fait intervenir des molécules comme
Système immunitaire adaptatif les recombinases (RAG1/2). Le système immunitaire adaptatif
Il est constitué des lymphocytes B et T (CD4 et CD8) qui expriment est doté d’une mémoire immunitaire qui permet une réponse
à leur surface des récepteurs spécifiques aux antigènes (immuno- secondaire plus rapide et plus affine, lors d’un contact ultérieur
globulines, récepteurs des lymphocytes T). Ces récepteurs aux avec l’antigène.
LA REVUE DU PRATICIEN VOL. 60
20 avril 2010 551
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 552
RR Q 115 bis I-8 DÉFICIT IMMUNITAIRE
Quelques exemples de déficits immunitaires
Classification des déficits immunitaires
primitifs ou secondaires
Les déficits immunitaires primitifs (fig. 2 et tableau 2A) sont
d’origine génétique, et les secondaires (tableau 2B) sont acquis. Les formes secondaires sont les plus fréquentes et représentent,
Les mécanismes physiopathologiques qui sous-tendent les au moins chez l’adulte, le principal diagnostic différentiel à éliminer
DIP résultent soit de mutations interférant avec le développe- avant de porter un diagnostic de déficit immunitaire primitif.
ment (absence de développement d’une ou plusieurs cellules du Les formes rencontrées chez l’enfant sont le plus souvent pri-
système immunitaire) ou la fonction des différentes cellules du mitives, à l’exception de l’infection par le VIH ou des déficits
système immunitaire (défaut d’activation ou de migration) (fig. 2). secondaires aux traitements immunosuppresseurs. Certains
TABLEAU 1
Les différents acteurs de la réponse anti-infectieuse, mécanismes d’action et tests diagnostiques
Type Éléments du système
de réponse immunitaire Rôle Tests diagnostiques
Phase humorale
Innée ❚ Peptides antimicrobiens ❚ Activité microbicide directe ❚ Pas en routine
❚ Complément ❚ Opsonisation (récepteurs du C3) ❚ C3, C4, CH50, AP50
❚ Lyse (complexe d’attaque membranaire C5-C9)
Adaptative ❚ Anticorps ❚ Opsonisation (récepteurs FcR) ❚ Dosage pondéral IgG, A, M,
❚ Fixation du complément (lyse, phagocytose) sous-classes IgG (IgG1 à 4)
❚ Sérologies (antigènes vaccinaux)
Phase cellulaire
Innée ❚ Polynucléaires ❚ Phagocytose (bactéries extracellulaires, ❚ Hémogramme, études des fonctions oxydatives
neutrophiles champignons) (réduction du NBT et chémoluminescence),
❚ Macrophages ❚ Phagocytose (bactéries extracellulaires, de la phagocytose, du chimiotactisme
champignons)
❚ Présentation d’antigènes
Intersection ❚ Cellules dendritiques ❚ Présentation d’antigènes ❚ Pas en routine
inné/adaptatif
❚ Lymphocytes NK ❚ Reconnaissance de cellules infectées ❚ Immunophénotypage (CD3-CD16+CD56+)
ou transformées (indépendante de l’antigène) ❚ Production de cytokines
❚ Production de cytokines (IFNγ) ou immunomarquage intracytoplasmique (IFNγ)
Adaptative ❚ Lymphocytes B ❚ Production d’anticorps ❚ Immunophénotypage (CD19, sIgD/M, CD27)
(différenciation en plasmocytes)
❚ Présentation d’antigènes
❚ Lymphocytes T CD4 ❚ Activation et maturation (cellules dendritiques, ❚ Immunophénotypage
lymphocytes B, lymphocytes T CD8) (CD3+CD4+, CD3+CD8+)
❚ Production de cytokines (IL4, IFNγ) ❚ Prolifération aux mitogènes
et antigènes vaccinaux
❚ Lymphocytes T CD8 ❚ Reconnaissance et lyse spécifique
❚ Production de cytokines
(dépendante de l’antigène) des cellules infectées
ou immuno-marquage intracytoplasmique (IFNγ)
ou transformées (perforine, granzyme B)
❚ Tétramère marqué
❚ Production de cytokines (IFNγ)
NBT : nitrobleu de tétrazolium ; IFN : interféron ; IL : interleukine
552 LA REVUE DU PRATICIEN VOL. 60
20 avril 2010
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 553
Q RR 115 bis
Progéniteur myéloïde commun NEUTROPÉNIE CONGÉNITALE SÉVÈRE
x{ Polynucléaire neutrophile
x{ GRANULOMATOSE SEPTIQUE CHRONIQUE
Monocytes/macrophages
Cellule souche hématopoïétique
AGAMMAGLOBULINÉMIE
DÉFICIT IMMUNITAIRE
x{ Lymphocyte B
COMBINÉ SÉVÈRE
DÉFICIT IMMUNITAIRE COMMUN VARIABLE
x{
x{
Progéniteur lymphoïde commun x{ DÉFICITS IMMUNITAIRES COMBINÉS
Lymphocyte T
x{ SYNDROME DE WISKOTT-ALDRICH
FIGURE 2 Mécanismes physiopathologiques des déficits immunitaires primitifs ( x : mutations bloquant le développement d’une lignée ; x : mutations interférant
avec la fonction des cellules).
{ {
déficits immunitaires primitifs se révèlent ou ne sont diagnostiqués des granuleux (G-CSF) par voie sous-cutanée. Tous les épisodes
qu’à l’âge adulte. Le bilan doit s’efforcer d’exclure une origine infectieux doivent être traités efficacement (antibiothérapie paren-
secondaire à tout déficit immunitaire évoqué chez l’adulte, térale, antifongiques). Le risque de transformation en myélodys-
notamment une hémopathie lymphoïde B sous-jacente (leucé- plasie ou en leucémie aiguë myéloblastique nécessite la surveil-
mie lymphoïde chronique, myélome). lance régulière du myélogramme et du caryotype médullaire.
Déficits immunitaires primitifs : syndromes
et âge de révélation variables
TABLEAU 2A
Il existe plus de 200 déficits immunitaires génétiques différents.
Différents types de déficits immunitaires
Plus de 150 gènes ont été identifiés, mais pour certains déficits
primitifs en fonction du mécanisme
primitifs le mécanisme génétique n’est pas encore élucidé. L’hé- Atteinte Exemples
rédité est surtout mendélienne (autosomique dominante ou
récessive, récessive liée à l’X). Le caractère héréditaire peut ne Déficit immunitaire primitif inné
pas être apparent (formes sporadiques, pénétrance ou expres- Complément ❚ Déficit en C2, C4, C3, complexe
sion variable, hérédité multigénique). d’attaque membranaire (C5-9)
Les formes primitives peuvent se révéler dans l’enfance (parfois Phagocytes ❚ Granulomatose septique chronique
dès la naissance pour les plus sévères) ou à l’âge adulte (expres- ❚ Neutropénie congénitale sévère
sion à l’âge adulte du phénotype, formes modérées et rencontre
tardive avec le pathogène ou encore retard diagnostique d’une Déficit immunitaire primitif adaptatif
affection se manifestant depuis l’enfance). B (déficits humoraux) ❚ Agammaglobulinémies
1. Déficits touchant le système immunitaire inné ❚ Hypogammaglobulinémies
Neutropénies congénitales sévères : liées à un blocage de maturation T (déficits combinés) ❚ Déficits immunitaires combinés sévères
des progéniteurs granuleux entraînant une agranulocytose pro- ❚ Syndrome de Wiskott-Aldrich
fonde (PNN < 0,2 G/L). Les infections sont précoces et sévères. Le ❚ Ataxie-Télangiectasie
traitement repose sur l’administration à vie de facteurs de croissance
LA REVUE DU PRATICIEN VOL. 60
20 avril 2010 553
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 554
RR Q 115
TABLEAU 2B
bis I-8 DÉFICIT IMMUNITAIRE
Exemples de déficits immunitaires secondaires (DIS)
Étiologie Exemples Mécanismes Complications
Infections rétrovirales ❚ VIH/sida ❚ Lymphopénie T CD4 ❚ Infections opportunistes
❚ HTLV1 ❚ Tumeurs malignes
Hémopathies malignes ❚ Hémopathies lymphoïdes (leucémie ❚ Hypogammaglobulinémie ❚ Infections bactériennes (germes
lymphoïde chronique, myélome) encapsulés), auto-immunité (LLC)
❚ Lymphocytes T (déficit fonctionnel) ❚ Infections opportunistes
(zona, pneumocystose)
❚ Leucémies aiguës ❚ Neutropénie (insuffisance médullaire) ❚ Infections bactériennes et fongiques
Médicamenteux ❚ Corticoïdes ❚ Diminution de la phagocytose ❚ Infections bactériennes et fongiques
❚ Hypogammaglobulinémie ❚ Infections bactériennes
❚ Lymphocytes T (déficit fonctionnel) ❚ Infections opportunistes
❚ Immunosuppresseurs (ciclosporine, ❚ Lymphocytes T (déficit fonctionnel) ❚ Infections opportunistes
azathioprine, cyclophosphamide)
TABLEAU 3
Acteurs de la réponse anti-infectieuse, susceptibilité aux infections et exemples de déficits associés
Atteinte du système Susceptibilité Tableau clinique Principaux Principaux déficits
immunitaire à déficits primitifs secondaires
Phagocytes ❚ Bactéries extracellulaires ❚ Gingivostomatites ❚ Granulomatose septique ❚ Corticoïdes
❚ Champignons ❚ Angines nécrotiques chronique ❚ Diabète
❚ Cellulites ❚ Neutropénie congénitale ❚ Chimiothérapie
❚ Septicémies sévère
❚ Pneumopathies
❚ Abcès profonds
(hépatiques)
Lymphocytes T ❚ Bactéries intracellulaires ❚ Mycobactériose ❚ Déficit immunitaire ❚ Corticoïdes
❚ Virus disséminée combiné sévère ❚ Immunosuppresseurs
❚ Parasites ❚ Pneumocystose ❚ Syndrome ❚ Chimiothérapies
❚ Champignons ❚ Cytomégalovirus de Wiskott-Aldrich (analogues des purines)
(pneumocystis, ❚ Adénovirus disséminé ❚ Ataxie-Télangiectasie ❚ Sida
cryptococcus) ❚ Transplantation
Lymphocytes B ❚ Bactéries extracellulaires ❚ Infections ORL ❚ XLA (Bruton) ❚ Leucémie lymphoïde
(anticorps) (encapsulées) et bronchopulmonaires ❚ Déficit immunitaire chronique, myélome
❚ Giardia intestinalis ❚ Diarrhées chroniques commun variable ❚ Rituximab
❚ Entérovirus ❚ Méningo-encéphalites ❚ Chimiothérapies
❚ Corticoïdes
❚ Allogreffes de moelle
Complément ❚ Neisseria meningitidis ❚ Méningites ❚ Déficit en C3
❚ Méningococcémies ❚ Déficit en C5-9
❚ Déficit en MBL
554 LA REVUE DU PRATICIEN VOL. 60
20 avril 2010
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 555
Granulomatose septique chronique : elle est liée à un défaut de micro-
Q RR 115 bis
Exemples de tableaux cliniques associés
TABLEAU 4
bicidie des macrophages et des polynucléaires neutrophiles
secondaire à un déficit de la NAPDH oxydase (voie oxydative) à diverses atteintes du système immunitaire
mais ces cellules sont présentes à un taux normal. Il existe une et déficits associés
susceptibilité aux infections bactériennes catalase + (S. aureus,
Complication Déficit immunitaire
Salmonella sp., Burkholderia sp.) et fongiques (surtout champi-
gnons filamenteux comme Aspergillus sp.). Des granulomes Dilatation des bronches ❚ Agamma-
inflammatoires se développent dans différents organes (tube et hypogammaglobulinémie
digestif notamment) et peuvent nécessiter une corticothérapie
(augmentation du risque infectieux). Le traitement repose sur la Granulomes ❚ Granulomatose
prophylaxie à vie des infections bactériennes (cotrimoxazole) et des septique chronique
et hypogammaglobulinémie
infections fongiques (itraconazole). Comme dans les neutropénies
congénitales sévères, l’allogreffe de moelle peut être indiquée. Cancers secondaires ❚ Ataxie-Télangiectasie
2. Déficits touchant le système immunitaire adaptatif ❚ Déficit immunitaire commun
Déficit immunitaire combiné sévère (DICS) : ils sont liés à un défaut de variable
développement complet des lymphocytes secondaires (mutations
❚ VIH/sida
de gènes RAG1/2 ou pour des récepteurs à certaines cytokines).
La lymphopénie est apparente dès la naissance, et il existe une Auto-immunité ❚ Déficit immunitaire commun
atrophie précoce du thymus (organe de développement des lym- variable
phocytes T) visible sur un simple cliché du thorax. Le début des ❚ Syndrome de Wiskott-Aldrich
manifestations est très précoce, vers le 3e mois, par des infections
opportunistes (pneumocystose, candidose) ou une diarrhée
importante avec retard de croissance staturo-pondéral. Les défi-
cits sont constamment létaux en l’absence d’allogreffe. Des pro- transmis passivement pendant la grossesse). Les infections tou-
tocoles de thérapie génique sont en cours de développement. chent la sphère ORL et bronchopulmonaire. Les patients déve-
Le syndrome de Wiskott-Aldrich : il est caractérisé par la triade loppement aussi des infections intestinales (Giardia intestinalis)
eczéma, déficit immunitaire et thrombopénie avec micropla- ou à entérovirus (encéphalites). Le traitement repose sur la subs-
quettes et lié à la mutation du gène WAS qui entraîne une ano- titution à vie par immunoglobulines polyvalentes. Le pronostic est
malie de migration et d’activation des lymphocytes T. L’auto- excellent chez les patients correctement substitués.
immunité est fréquente (anémie hémolytique auto-immune). Les 4. Déficit immunitaire primitif de révélation adulte
formes peu sévères sont compatibles avec une survie prolongée. Il s’agit le plus souvent de déficits de l’immunité humorale.
Le traitement repose sur la prophylaxie des infections opportu- Déficit en IgA : Il s’agit du plus fréquent des déficits primitifs, tou-
nistes (cotrimoxazole, valaciclovir) et sur la substitution par chant environ 1 individu sur 600, mais il est rarement symptoma-
immunoglobulines polyvalentes. Une corticothérapie prolongée tique (infections surtout ORL). Il est parfois associé à un déficit en
ou la splénectomie sont parfois nécessaires pour traiter les compli- sous-classes d’IgG (déficit en IgG1, déficit en IgG2 ± IgG4).
cations auto-immunes (majoration du risque infectieux). L’allo- Déficit immunitaire commun variable (DICV) : c’est le plus fréquent des
greffe est indiquée dans les formes sévères. déficits immunitaires primitifs symptomatiques de l’adulte (1 individu
Ataxie-télangiectasie : les mutations du gène ATM entraînent un sur 25 000). Les mécanismes génétiques sont le plus souvent
défaut de réparation de l’ADN. Les signes associent des télan- non identifiés et probablement multigéniques. L’hypogammaglo-
giectasies oculocutanées, une ataxie débutant généralement à bulinémie est constante mais variable (touchant 1 ou plusieurs
l’âge de la marche qui s’aggrave progressivement et une grande isotypes d’immunoglobulines). Certains patients présentent un
susceptibilité aux tumeurs malignes. Un déficit immunitaire d’inten- déficit T variable associé (infections opportunistes).
sité variable (cellulaire ou seulement humoral) est présent dans Les infections sont liées au premier plan à l’hypogammaglobu-
environ la moitié des cas. linémie. Les patients présentent souvent des complications auto-
3. Déficits B ou humoraux immunes, une hyperplasie lymphoïde, des granulomes ou des
Agammaglobulinémies : la plus fréquente est la maladie de Bruton lymphomes.
(agammaglobulinémie liée à l’X) liée à une mutation du gène Btk Les symptômes débutent entre 15 et 25 ans, mais le diagnostic
qui entraîne une absence complète de développement des lympho- est souvent plus tardif, entre 30 et 40 ans.
cytes B. Les autres cellules du système immunitaire se développent Le traitement repose sur la substitution à vie en immunoglobu-
et fonctionnent normalement. Le déficit est exclusivement lié à lines polyvalentes, le traitement par antibiotiques de toute infec-
l’absence d’immunoglobulines. Les symptômes débutent entre le tion et la kinésithérapie respiratoire pour prévenir les séquelles,
6e et le 9e mois de vie (après élimination des anticorps maternels notamment la dilatation des bronches.
LA REVUE DU PRATICIEN VOL. 60
20 avril 2010 555
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 556
RR Q 115 bis I-8 DÉFICIT IMMUNITAIRE
Déficits immunitaires secondaires Examen clinique devant une suspicion de déficit
En dehors de l’infection par le VIH, les formes secondaires sont immunitaire
iatrogènes (corticoïdes, traitement immunosuppresseur, trans- Il doit être complet et rigoureux.
plantation) ou secondaires à une hémopathie lymphoïde B Anamnèse : il faut rechercher :
mature (leucémie lymphoïde chronique et myélome). – facteurs de risque VIH ;
Hémopathies lymphoïdes B : la leucémie lymphoïde chronique et le – histoire vaccinale : réactions aux vaccins vivants (tels que le
myélome s’accompagnent souvent d’une hypogammaglobulinémie BCG), infections en dépit de la vaccination ;
parfois responsable d’infections qui peuvent survenir même chez – antécédents infectieux : âge de début, type d’infection, répéti-
les patients non traités. L’infection révèle parfois l’hémopathie sous- tion, durée, antibiothérapie prolongée ;
jacente (25 % des cas). La chimiothérapie ou la corticothérapie par- – manifestations associées : auto-immunité, allergies, tumeurs ;
fois utilisée majorent le risque infectieux. Il existe aussi une atteinte – antécédents familiaux et arbre généalogique complet (consan-
de l’immunité cellulaire au cours de la leucémie lymphoïde chronique guinité, décès en bas âge).
qui peut être démasquée par le traitement avec un risque d’infections Examen physique : doivent être envisagés :
opportunistes (prévention prophylaxie par cotrimoxazole et vala- – retard de croissance ;
ciclovir). La substitution par immunoglobulines poylvalentes est – anomalie de la peau et des muqueuses : éruption, verrues,
indiquée quand l’hypogammaglobulinémie est symptomatique. candidose chronique, état buccodentaire, télangiectactasies,
Syndrome de Good : il s’agit d’un déficit immunitaire avec hypo- aspect des cheveux (albinisme) et des phanères (dystrophie) ;
gammaglobulinémie et lymphopénie B profonde et atteinte de – anomalies des organes lymphoïdes : adénopathies, splénomé-
l’immunité cellulaire secondaire à un thymome. L’âge de début galie, hépatomégalie, hypoplasie des organes lymphoïdes
est plus tardif, autour de 50 ans. Il doit être systématiquement secondaires (ganglions, amydgales) observée dans l’agamma-
recherché par un scanner thoracique. globulinémie congénitale ;
Infection par le virus de l’immunodéficience humaine (VIH) : l’infection – pathologie ORL : otites, sinusites ;
par le VIH ne sera pas développée ici, sinon pour rappeler qu’elle – pathologie ophtalmologique : conjonctivites chroniques,
entraîne un déficit immunitaire cellulaire par diminution progres- uvéites, télangiectasies conjonctivales ;
sive des lymphocytes T CD4. Les infections opportunistes (cyto- – complications pulmonaires : toux chronique, bronchites ou pneumo-
mégalovirus, pneumocystose, toxoplasmose, cryptococcose, pathies récurrentes, dilatation des bronches, hippocratisme digital ;
cryptosporidiose, microsporidiose, tuberculose et mycobacté- – troubles digestifs : appétit, transit, perte de poids, douleurs
rioses atypiques) ou des complications tumorales (lymphomes, abdominales récurrentes ;
sarcome de Kaposi) sont fonction de la profondeur du déficit de – atteinte neurologique : ataxie, retard mental, microcéphalie.
l’immunité cellulaire (corrélé au taux de lymphocytes CD4).
Il existe aussi un déficit de l’immunité humorale malgré l’hyper- Bilan de suspicion ou d’exploration de déficit
gammaglobulinémie (augmentation des infections pneumococ- immunitaire
ciques).
Les traitements antirétroviraux permettent le plus souvent de L’ensemble du bilan suivant doit être envisagé.
restituer un taux de CD4 suffisant et de faire régresser le déficit Hémogramme : neutropénie, lymphopénie (surtout chez l’enfant
immunitaire. chez qui elle revêt une importance particulière puisqu’il existe
Une prophylaxie des infections opportunistes, essentiellement une lymphocytose physiologique de l’enfant). Chez l’adulte, un
la pneumocystose et la toxoplasmose, est indiquée quand les résultat est significatif s’il est inférieur à 1 G/L. Une lymphocytose
CD4 sont inférieurs à 200/µL. peut traduire une leucémie lymphoïde chronique. L’anémie ou
la thrombopénie sont habituellement des stigmates d’auto-
Manifestations cliniques des déficits immunitaires immunité, parfois associée au déficit immunitaire.
Immunophénotypage des lymphocytes B, T, NK : il permet le diagnostic
Infections d’une leucémie lymphoïde chronique chez l’adulte. Le déficit
Plusieurs types de manifestations infectieuses s’observent en peut être quantitatif avec la mise en évidence d’une lymphopénie
fonction de l’atteinte du système immunitaire (tableau 3). (B dans l’agammaglobulinémie, T dans les déficits immunitaires
combinés [± sévères] sous-populations CD4/CD8 pour le VIH).
Manifestations non infectieuses observées au cours Test fonctionnels : dosage des anticorps naturels (allohémaggluti-
des déficits immunitaires nines de groupe ABO) et des antigènes vaccinaux (diphtérie,
Elles peuvent résulter de la dérégulation du système immunitaire tétanos, polio, pneumocoque) ; prolifération lymphocytaires in
(rupture d’homéostasie, anomalies de la réparation de l’ADN) ou vitro aux mitogènes et antigènes vaccinaux ; tests fonctionnels des
des complications des infections récurrentes (dilatations des polynucléaires neutrophiles : explosion oxydative, chimiotactisme,
bronches, sinusite chronique) (tableau 4). phagocytose.
556 LA REVUE DU PRATICIEN VOL. 60
20 avril 2010
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 557
Q RR 115
– la vaccination qui doit être proposée autant que possible. Les
bis
Déficit immunitaire vaccins vivants atténués sont contre-indiqués en cas de déficit
POINTS FORTS À RETENIR de l’immunité cellulaire. Les déficits immunitaires cellulaires ou
humoraux profonds rendent cependant l’efficacité des vaccins
Les déficits immunitaires primitifs peuvent se révéler très aléatoire ;
à l’âge adulte (début de l’expression ou retard diagnostique). – la substitution en immunoglobulines (IV ou sous-cutanée) en
Les déficits immunitaires primitifs et secondaires cas d’hypogammaglobulinémie symptomatique.
peuvent se compliquer de manifestations non infectieuses Antibiothérapie curative
(auto-immunité, granulomes tissulaires, tumeurs malignes)
qui peuvent précéder les complications infectieuses et doivent Il faut s’acharner à documenter tout épisode infectieux pour
faire évoquer un déficit immunitaire en fonction du contexte. permettre un traitement adapté (prélèvements ciblés). Les exa-
cerbations d’infection bronchopulmonaires ou ORL chez les
Les déficits immunitaires secondaires doivent être recherchés
patients avec hypogammaglobulinémie doivent être traitées par
systématiquement, notamment chez l’adulte, avant de conclure
antibiotiques pour réduire le risque de séquelles (dilatation des
à un déficit immunitaire primitif (notamment recherche de
bronches).
leucémie lymphoïde chronique et de gammapathie monoclonale
devant toute hypogammaglobulinémie). Substitution en immunoglobulines polyvalentes
Toute surinfection (bronchique, ORL) doit être Elles sont préparées à partir de plasma de donneurs volon-
systématiquement traité par antibiotiques afin d’éviter taires (en France) ou rémunérés (ailleurs dans le monde). Elles
le développement de complications (notamment dilatation s’administrent par voie intraveineuse (toutes les 3 à 4 semaines
des bronches). en hôpital de jour ou à domicile) ou sous-cutanée (une fois par
semaine, géré par le patient, à domicile). La surveillance de l’effi-
cacité se fait sur la clinique (réduction des épisodes infectieux) et
Dosage des immunoglobulines : électrophorèse des protéines sur le dosage pondéral d’IgG (cible entre 5 et 8 g/L).
sériques ± immunofixation (indispensable chez l’adulte pour La substitution en Ig est définitive, sauf dans les cas de déficits
écarter une gammapathie monoclonale) ; dosage pondéral des secondaires où elle peut n’être que transitoire, le temps de la
IgG, A, M (mise en évidence d’une hypogammaglobulinémie glo- récupération (plusieurs mois). Dans les hypogammaglobuliné-
bale ou sélective) ; dosage des sous-classes d’IgG (IgG1 à 4). mies modérées, la substitution en immunoglobulines polyva-
Imagerie : radiographie du thorax chez l’enfant (ombre thymique), lentes peut être limitée à la période la plus à risque d’infections
scanner thoracique (thymome, dilatation des bronches, nodules (automne et hiver).
pulmonaires, adénopathies médiastinales), échographie ou
scanner abdominal (adénopathies profondes, splénomégalie). Allogreffe de cellules souches hématopoïétiques
Recherche de mutation en fonction de l’orientation : la recherche des et thérapie génique
mutations de plus de 150 gènes identifiés dans des déficits immu- Elles ne sont justifiées que pour des déficits sévères et compli-
nitaires primitifs est possible dans des laboratoires spécialisés. Elle qués, le plus souvent chez l’enfant. Les déficits immunitaires pri-
permet un conseil génétique et un diagnostic anténatal. mitifs avec hypogammaglobulinémie au premier plan ne sont pas
des indications de greffe du fait du bon pronostic moyennant une
Traitements prise en charge adaptée.
Prophylaxie Kinésithérapie respiratoire
Peuvent être envisagés selon les cas : La kinésithérapie respiratoire est indispensable à la prise en
– le cotrimoxazole (prévention de la pneumocystose et de la charge des patients atteints de déficit primitif avec hypogamma-
toxoplasmose dans les déficits cellulaires) ; globulinémie profonde pour prévenir l’apparition ou l’aggravation
– l’acyclovir ou valaciclovir (prévention des infections à Herpes de la dilatation des bronches et des surinfections.
simplex et zona) ;
– l’oracilline en cas d’asplénie ou d’antécédent d’infection inva- Mesures psychosociales
sive à pneumocoque (myélome ou leucémie lymphoïde chro- Les déficits immunitaires primitifs peuvent entraîner ou s’asso-
nique). Une substitution en immunoglobulines est en règle cier à un handicap physique (insuffisance respiratoire chronique,
générale associée ; déficit neurologique syndromique), psychologique (retard mental
– l’antibiothérapie prophylactique alternée (cotrimoxazole, syndromique ou syndrome dépressif réactionnel) ou social
amoxicilline, céphalosporine orale de 3e génération), surtout (absentéisme scolaire ou au travail) qui doit être pris en charge
chez l’enfant avec hypogammaglobulinémie ; (prestations adultes handicapés, soutien psychologique).
LA REVUE DU PRATICIEN VOL. 60
20 avril 2010 557
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
551_RDP4_ref_suarez:Mise en page 1 9/04/10 14:00 Page 558
RR Q 115 bis I-8 DÉFICIT IMMUNITAIRE
Conclusion le Centre de référence des déficits immunitaires héréditaires
(CEREDIH) permet de structurer l’approche diagnostique et théra-
Le développement des thérapeutiques immunosuppressives peutique touchant aux déficits immunitaires primitifs et propose
pour les pathologies auto-immunes et les transplantations s’ac- plusieurs documents d’information destinés aux médecins et
compagne d’une augmentation des patients présentant un défi- aux patients impliqués.•
cit immunitaire secondaire parfois sévère et pouvant être respon-
L’auteur déclare n’avoir aucun conflit d’intérêts concernant les données publiées
sable d’une morbidité et d’une mortalité importante. dans cet article.
Les déficits immunitaires primitifs représentent un ensemble
très hétérogène de pathologies rares et mal connues mais dont
les manifestations diverses peuvent toucher toutes les spécialités POUR LA REVUE DU
EN SAVOIR PRATICIEN
médicales. Ils peuvent se révéler à l’âge adulte, souvent après de 1 5 O C T O B R E 2 0 0 7 / T O M E 5 7 N º 1 5
Monographie
nombreuses années d’évolution, entraînant des séquelles, notam- Déficits
ment pulmonaires, parfois invalidantes. Une meilleure connaissance immunitaires
IMONOGRAPHIEI
des déficits immunitaires primitifs doit permettre un diagnostic Déficits immunitaires
OPTIMISER LEUR APPROCHE
Rev Prat 2007;
plus précoce et une prise en charge adaptée (antibioprophylaxie, OUVERTURES
B Ostéoporose : ce qui est
nouveau B Lymphome du MALT
RÉFÉRENCES UNIVERSITAIRES
Le temps de lire et la règle d’Ingelfinger B Qu’est-ce qui peut tomber à
l’examen ? B Phénomène de Raynaud B Incontinence urinaire de l’adulte B
57:(15):1637-702
pulmonaire B Presse : Sonde Diarrhée aiguë du nourrisson B Bases de la psychologie médicale
urinaire • Artériopathie•
Exposition au gazole DE MÉMOIRE DE MÉDECIN L’aventure du « Médicophone »
antibiothérapie curative, substitution en immunoglobuline, www.larevuedupraticien.fr publicat ion bimensuelle de format ion médicale con t inue
conseil génétique). Faisant suite au Plan national maladies rares,
Qu’est-ce qui peut tomber à l’examen ?
Un patient de 35 ans est adressé en consultation pour suspicion de déficit immunitaire QUESTION N° 6
après la découverte d’une hypogammaglobulinémie. À la suite d’une pneumopathie Vous revoyez le patient après 3 mois.
franche lobaire aiguë à S. pneumoniæ, une électrophorèse des protéines sériques Il présente une bronchite traînante depuis
a montré une hypogammaglobulinémie globale à 1,5 g/L (normale entre 6,5 et 12 g/L). 15 jours, avec des expectorations sales,
Le dosage pondéral des immunoglobulines confirme l’hypogammaglobulinémie globale : mais il est apyrétique, et l’état général est
IgG 2 g/L (6-13), IgA < 0,06 g/L (0,6-2,5), IgM 0,2 g/L (0,4-1,5). excellent. Son médecin traitant lui a dit
L’évolution a été favorable après un traitement antibiotique. Dans ses antécédents, on qu’il ne fallait pas prendre d’antibiotiques,
note quelques otites (1 ou 2 épisodes par an) jusqu’à l’âge de 8 ans et des bronchites car « les antibiotiques c’est pas
tous les ans (2 à 4 épisodes par an) à partir de l’âge de 13 ans. Il rapporte par ailleurs automatique ». Êtes-vous d’accord avec
cette affirmation dans son cas et pourquoi ?
une sinusite chronique depuis une dizaine d’années, qualifiée d’« allergique ».
Il a fait une pleurésie purulente il y a 10 ans, traitée par drainage et antibiothérapie. QUESTION N° 7
L’hémogramme montre un taux de lymphocytes normal. L’immunophénotypage montre
Quelle mesure non médicamenteuse est
un taux normal de lymphocytes B (CD19+) et des différentes sous-populations nécessaire pour la prise en charge ?
de lymphocytes T (CD3+CD4+ et CD3+CD8+).
QUESTION N° 8
QUESTION N° 1 80 et 100 G/L. Existe-t-il un lien entre Vous le revoyez après plusieurs années
Le diagnostic de déficit immunitaire cet antécédent et le diagnostic envisagé ? durant lesquelles les complications
primitif vous paraît-il compatible avec les infectieuses ont été bien contrôlées par
données de l’anamnèse et du bilan fourni ? QUESTION N° 4 les mesures prescrites. Il a une altération
Sur quels arguments ? Après s’être renseigné sur Internet, le de l’état général avec un amaigrissement,
patient vous demande à quels agents une fièvre sans point d’appel et des
QUESTION N° 2 pathogènes il est exposé et quelles sont polyadénopathies. Quelle complication
Quels diagnostics différentiels devez-vous les principales infections qu’il risque. Que non infectieuse suspectez-vous ?
éliminer ? lui répondez-vous ? Existe-t-il un lien avec ses antécédents ?
QUESTION N° 3 QUESTION N° 5
Il vous apprend qu’il a eu un diagnostic de Vous posez l’indication d’une substitution Retrouvez toutes les réponses
purpura thrombocytopénique « idiopathique » par immunoglobulines. Quelles en sont les et les commentaires sur
à l’âge de 15 ans. Il garde depuis voies d’administration ? La fréquence ? www.larevuedupraticien.fr
une thrombocytopénie modérée entre La durée d’administration ? onglet Références Universitaires
OK
558 LA REVUE DU PRATICIEN VOL. 60
20 avril 2010
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN
Vous aimerez peut-être aussi
- Akos (Traite de Medecine) Mise A Jour Ii 2020 PDFDocument87 pagesAkos (Traite de Medecine) Mise A Jour Ii 2020 PDFMoncef PechaPas encore d'évaluation
- Cours D'immunologie Médicale PDFDocument17 pagesCours D'immunologie Médicale PDFMafankoloPas encore d'évaluation
- L'Immunologie - SVT 1èrea Tome2Document7 pagesL'Immunologie - SVT 1èrea Tome2Guy TangaPas encore d'évaluation
- Une Immunité Remarquable par des Aliments Remarquables: The BlokeheadD'EverandUne Immunité Remarquable par des Aliments Remarquables: The BlokeheadPas encore d'évaluation
- Livre Amine Laboudi PDFDocument167 pagesLivre Amine Laboudi PDFRadia RadiaPas encore d'évaluation
- Allergie et hypersensibilité: Les Grands Articles d'UniversalisD'EverandAllergie et hypersensibilité: Les Grands Articles d'UniversalisPas encore d'évaluation
- Physiopathologie de L'inflammationDocument30 pagesPhysiopathologie de L'inflammationtom624100% (4)
- I. Organes Et Cellules Du SI Oct 16Document22 pagesI. Organes Et Cellules Du SI Oct 16pppPas encore d'évaluation
- ImmunoDocument29 pagesImmunoIkram DahmaniPas encore d'évaluation
- 1 Er Cours Immuno Appl BS 202 PDFDocument10 pages1 Er Cours Immuno Appl BS 202 PDFHasna BentPas encore d'évaluation
- Ref185 SuarezDocument9 pagesRef185 SuarezitsaidaPas encore d'évaluation
- 115b - Déficit ImmunitaireDocument8 pages115b - Déficit ImmunitaireNebel GesangPas encore d'évaluation
- Thomas 2019Document11 pagesThomas 2019Doha assadPas encore d'évaluation
- FORMATION ACCR DITEE - 2022-Complete-Finale.Document124 pagesFORMATION ACCR DITEE - 2022-Complete-Finale.ΆθικτοςPas encore d'évaluation
- RappelDocument11 pagesRappelNadjib A. NedjarPas encore d'évaluation
- cours immunologie S5 (2)Document113 pagescours immunologie S5 (2)hamzaabzou154Pas encore d'évaluation
- Résumé6 ImmunologieDocument19 pagesRésumé6 Immunologieg69wwpfw5kPas encore d'évaluation
- Fonctionnement Du Système Immunitaire - Immunologie de La Vaccination - Professionnels de La Santé - MSSSDocument6 pagesFonctionnement Du Système Immunitaire - Immunologie de La Vaccination - Professionnels de La Santé - MSSSMaï SsaPas encore d'évaluation
- Livre Amine Laboudi-128-139Document12 pagesLivre Amine Laboudi-128-139Muddymae SugginsPas encore d'évaluation
- Fievre Chez L'id PDFDocument7 pagesFievre Chez L'id PDFHanaa ZianiPas encore d'évaluation
- Cous Immuno MMBDocument470 pagesCous Immuno MMBNabil holmesPas encore d'évaluation
- 13 VaccinationsDocument28 pages13 VaccinationsZakarya BelguebliPas encore d'évaluation
- Introduction 2021-2022 PDFDocument75 pagesIntroduction 2021-2022 PDFStephanePas encore d'évaluation
- 01 - Introduction Du Système ImmunitareDocument15 pages01 - Introduction Du Système ImmunitareAnas El MalhiPas encore d'évaluation
- 01 Introd Si PDFDocument15 pages01 Introd Si PDFAnas El MalhiPas encore d'évaluation
- IMMUNOTOX110204Document12 pagesIMMUNOTOX110204Mariam ZougouriPas encore d'évaluation
- Physiopathologie Mai Final 2Document5 pagesPhysiopathologie Mai Final 2EbePas encore d'évaluation
- NourDocument30 pagesNourManel GharbiPas encore d'évaluation
- Cours Immunologie 2022-2023Document34 pagesCours Immunologie 2022-2023massinizouhairPas encore d'évaluation
- VaccinationsDocument10 pagesVaccinationsiri NaPas encore d'évaluation
- Immunite Deuxieme Partie Dysfonctionnemen Du SiDocument3 pagesImmunite Deuxieme Partie Dysfonctionnemen Du SiGabin KenfackPas encore d'évaluation
- ImmunologieDocument24 pagesImmunologieayoub berrePas encore d'évaluation
- DI PrimitifDocument9 pagesDI Primitifhiba brinsiPas encore d'évaluation
- Immunite Specifique Anti-InfectieuseDocument15 pagesImmunite Specifique Anti-InfectieuseKhaled NabiPas encore d'évaluation
- #Cours Fonctionnement SIDocument8 pages#Cours Fonctionnement SIbeom13moaPas encore d'évaluation
- Chap_01_-_02___version_2015_2016Document170 pagesChap_01_-_02___version_2015_2016Jérémy FranchePas encore d'évaluation
- MAI DermatoDocument6 pagesMAI DermatoJustine GrdsrtPas encore d'évaluation
- 3-L'immunité InnéeDocument5 pages3-L'immunité InnéeOsama O-bPas encore d'évaluation
- 32 Chap 26Document13 pages32 Chap 26Fadila MararPas encore d'évaluation
- 2019 - Miot C - RFLEq7Document11 pages2019 - Miot C - RFLEq7Joseph NewmanPas encore d'évaluation
- Mécanisme Échappment FlivurusDocument7 pagesMécanisme Échappment FlivurusYousra NanoPas encore d'évaluation
- l'Immunité Anti InfectueuselDocument80 pagesl'Immunité Anti InfectueuselPekoJhames08gmail.comPas encore d'évaluation
- Cours ImmunologieDocument285 pagesCours ImmunologiedouinienPas encore d'évaluation
- Terminale S Fiche Revision ImmunologieDocument4 pagesTerminale S Fiche Revision ImmunologieMiantsa Ramahaliarivo100% (1)
- Immunologie Generale P 1)Document53 pagesImmunologie Generale P 1)Mehdi MaàroufPas encore d'évaluation
- Chap 1 PDFDocument35 pagesChap 1 PDFJouda BivaPas encore d'évaluation
- SVTEEHB Tle D Se10 PDFDocument3 pagesSVTEEHB Tle D Se10 PDFRomario nzouPas encore d'évaluation
- Introduction ImmunologieDocument29 pagesIntroduction Immunologieagag.salahPas encore d'évaluation
- VaccinationDocument58 pagesVaccinationFabienne GEDEONPas encore d'évaluation
- Et Programmes: Principales Vaccinations Des VolaillesDocument3 pagesEt Programmes: Principales Vaccinations Des VolaillesDhaif dhaifPas encore d'évaluation
- FR - Semaine 1 - FinalDocument43 pagesFR - Semaine 1 - FinalRima OswaldPas encore d'évaluation
- Partie 1Document7 pagesPartie 1Lilà ØūkhPas encore d'évaluation
- ImmunitéDocument2 pagesImmunitéAni TrghwiPas encore d'évaluation
- Cours D'immunothérapie BDocument33 pagesCours D'immunothérapie BLessini Franciane100% (1)
- Le Pourquoi Et Le Commentde L'auto-ImmunitéDocument12 pagesLe Pourquoi Et Le Commentde L'auto-ImmunitéCDM achiffaPas encore d'évaluation
- Physiopathologie Du Lupus SystémiqueDocument4 pagesPhysiopathologie Du Lupus SystémiqueHenry TraoréPas encore d'évaluation
- Fiche N°16 Dysfonctionnement Et Déficiences Du Système ImmunitaireDocument10 pagesFiche N°16 Dysfonctionnement Et Déficiences Du Système Immunitairesabou.denonPas encore d'évaluation
- Exposé ImmunoDocument3 pagesExposé ImmunoFréjusPas encore d'évaluation
- CHAPITRE 4 Immunité InnéeDocument13 pagesCHAPITRE 4 Immunité InnéeJuan Sebastian MoraPas encore d'évaluation
- Chapitre 1. Introduction Au Système ImmunitaireDocument69 pagesChapitre 1. Introduction Au Système Immunitairefallone zannouPas encore d'évaluation
- Protozoaires Et Protozooses AnimalesDocument5 pagesProtozoaires Et Protozooses AnimalesHoucïne KerkoubPas encore d'évaluation
- 4 5938093668870129517 PDFDocument8 pages4 5938093668870129517 PDFMal RaiserPas encore d'évaluation
- Microbio QuizzDocument8 pagesMicrobio QuizzYas ChdidPas encore d'évaluation
- CoprocultureDocument23 pagesCoprocultureFodié Aly CamaraPas encore d'évaluation
- Brochure 1er Traitement 11 07 2017 PDFDocument28 pagesBrochure 1er Traitement 11 07 2017 PDFSid AhmedPas encore d'évaluation
- Recepteurs Associes A Une Tyrosine KinaseDocument13 pagesRecepteurs Associes A Une Tyrosine KinaseFatima ZahraPas encore d'évaluation
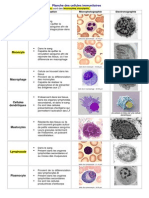
- Planche Cellules ImmunitairesDocument1 pagePlanche Cellules ImmunitairesInfamara ManéPas encore d'évaluation
- Hygien MicrobienneDocument6 pagesHygien MicrobienneFatïma ZohraPas encore d'évaluation
- Rapport de Synthese Mensuelle LaboratoireDocument2 pagesRapport de Synthese Mensuelle LaboratoireOumar BaPas encore d'évaluation
- Combinepdf-2 CompressedDocument190 pagesCombinepdf-2 Compressedapi-365867316Pas encore d'évaluation
- 1.prescription Des ATB-1Document4 pages1.prescription Des ATB-1ikhlasPas encore d'évaluation
- IFI Lyon09 BIENVENUDocument12 pagesIFI Lyon09 BIENVENUFathi CherifPas encore d'évaluation
- Aspects Biologiques Fertilite Masculine IDocument41 pagesAspects Biologiques Fertilite Masculine Ibouendeu pagnolPas encore d'évaluation
- L'expression de L'information GénétiqueDocument15 pagesL'expression de L'information GénétiqueAMINE 16Pas encore d'évaluation
- AntibiotiqueDocument24 pagesAntibiotiqueamel amoulPas encore d'évaluation
- Guide D Intervention Rage Juin 2007Document203 pagesGuide D Intervention Rage Juin 2007Julie SavoiePas encore d'évaluation
- Serie Exercices Heredité Humaine TS2 A Tirer 2Document3 pagesSerie Exercices Heredité Humaine TS2 A Tirer 2Marc SagnaPas encore d'évaluation
- Chap 2Document28 pagesChap 2Zineb ZinebPas encore d'évaluation
- Antibiogramme Staph2008 PDFDocument10 pagesAntibiogramme Staph2008 PDFDjouri KhouildiPas encore d'évaluation
- 2352509Document18 pages2352509AbdelOuahidSenhadjiPas encore d'évaluation
- ImmunitéDocument31 pagesImmunitélahlou Lh100% (1)
- Sol TD DihybridismeDocument6 pagesSol TD DihybridismenaomieeffoliPas encore d'évaluation
- 10 1 2 PhysiopathologieDocument5 pages10 1 2 PhysiopathologieRabah BouthibaPas encore d'évaluation
- Cours sv1 Biocell PDFDocument52 pagesCours sv1 Biocell PDFADILPas encore d'évaluation
- La Revue La Garance Voyageuse Numero Virtuel 2019Document34 pagesLa Revue La Garance Voyageuse Numero Virtuel 2019HighHiggsPas encore d'évaluation
- Sciences de La Vie Et de La Terre: Durée: 4H Coefficient: 4 Baccalaureat Blanc SESSION 2023 Série DDocument4 pagesSciences de La Vie Et de La Terre: Durée: 4H Coefficient: 4 Baccalaureat Blanc SESSION 2023 Série DdodoPas encore d'évaluation
- Therapie GéniqueDocument9 pagesTherapie GéniqueAsma MhPas encore d'évaluation
- D2F 3 hDocument31 pagesD2F 3 hErdem pelicat GowanitPas encore d'évaluation
- Les Antibiotiques USJDocument49 pagesLes Antibiotiques USJfouadzzzPas encore d'évaluation