Académique Documents
Professionnel Documents
Culture Documents
Résumé Cénitique L2 GP Et Exo Avec Sol
Transféré par
luckfi binadsTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Résumé Cénitique L2 GP Et Exo Avec Sol
Transféré par
luckfi binadsDroits d'auteur :
Formats disponibles
Solution exo1 chimie cinétique L2 GP
[A] mol/L 0,1 0,093 0,087 0,073 0,060 0,046
t(s) 0 30 63 132 219 330
Ln[A] -2,302 -2,375 -2,441 -2,617 -2,813 -3,079
y = -2,35E-03x - 2,30
Ln[A]=f(t) R² = 1,00
0
0 50 100 150 200 250 300 350
-0.5
-1
-1.5
-2
-2.5
-3
-3.5
1) La loi de Vitesse dans l’ordre 1 C’est :
𝑳𝒏[𝑨] = −𝒌𝒕 + 𝑳𝒏[𝑨]𝟎
𝑳𝒏[𝑨] − 𝑳𝒏[𝑨]𝟎 = −𝒌𝒕
𝑳𝒏[𝑨]
= −𝒌𝒕
𝑳𝒏[𝑨]𝟎
𝒃 = 𝑳𝒏[𝑨]𝟎 = −𝟐, 𝟑𝟎 𝒎𝒐𝒍 /𝑳 ⇨ [𝑨]𝟎 = 𝒆−𝟐,𝟑𝟎 = 𝟓, 𝟎𝟏 ∗ 𝟏𝟎−𝟑 𝒎𝒐/𝑳
L’unité de constante de vitesse C’est 𝐬−𝟏 donc l’ordre de réaction et 1.
2) La constante de vitesse k et temps demi de réaction :
La constante de vitesse 𝒌 :
(−𝟑, 𝟎𝟕𝟗 − (−𝟐, 𝟑𝟎𝟐)
𝒂 = 𝒕𝒂𝒏𝜶 = −𝒌 = = −𝟐, 𝟑𝟓 ∗ 𝟏𝟎−𝟑 𝒔−𝟏
(𝟑𝟑𝟎 − 𝟎)
−𝟑 −𝟏
𝒌 = 𝟐, 𝟑𝟓 ∗ 𝟏𝟎 𝒔
temps demi de réaction 𝒕𝟏⁄ :
𝟐
𝒍𝒏𝟐 𝟎, 𝟎𝟔𝟗
𝒕𝟏⁄ = = = 𝟐𝟗𝟒, 𝟗𝟓 𝐬
𝟐 𝒌 𝟐, 𝟑𝟓 ∗ 𝟏𝟎−𝟑
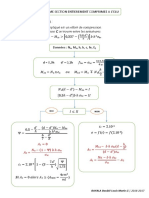
Sol Exo2 examen cinétique :
𝜶 𝜷
𝟎] 𝓿 = 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎 ∗ [𝑶𝑯−
𝜶 𝜷
𝟏𝟎] 𝓿𝟏 = 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟏 ∗ [𝑶𝑯−
𝜶 𝜷
𝟐𝟎] 𝓿𝟐 = 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟐 ∗ [𝑶𝑯−
𝜶 𝜷
𝟑𝟎] 𝓿𝟑 = 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟑 ∗ [𝑶𝑯−
نحدد 𝛂 بقسمة 𝟑𝓿 على 𝟏𝓿 كالتالي:
𝜶 𝜷
𝟑𝟎] 𝓿𝟑 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟑 ∗ [𝑶𝑯−
=
𝜷 𝟏𝟎] 𝓿𝟏 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟏 𝜶 ∗ [𝑶𝑯−
𝜷 𝟑𝟎] [𝑶𝑯− ]𝟎𝟏 𝜷 = [𝑶𝑯−
𝜶 𝛂
𝟑𝟎] 𝟐𝑶𝒍𝑪[ 𝟑𝓿 𝟑𝟎] 𝟐𝑶𝒍𝑪[
= (= )
𝜶 𝟏𝟎] 𝟐𝑶𝒍𝑪[ 𝟏𝓿 𝟏𝟎] 𝟐𝑶𝒍𝑪[
𝛂
𝟑𝓿 𝟑𝟎] 𝟐𝑶𝒍𝑪[
(= )
𝟏𝓿 𝟏𝟎] 𝟐𝑶𝒍𝑪[
بإدخال اللوغارثم النيبيري نجد:
𝛂
𝟑𝓿 𝟑𝟎] 𝟐𝑶𝒍𝑪[
( 𝐧𝐥 ( 𝐧𝐥 = ) )
𝟏𝓿 𝟏𝟎] 𝟐𝑶𝒍𝑪[
𝟑𝓿 𝟑𝟎] 𝟐𝑶𝒍𝑪[
( 𝐧𝐥 ∗ 𝛂 = ) ( 𝐧𝐥 )
𝟏𝓿 𝟏𝟎] 𝟐𝑶𝒍𝑪[
𝟑𝓿 𝟐𝟏, 𝟏𝟔 ∗ 𝟏𝟎−
) ( 𝐧𝐥 ( 𝐧𝐥 𝟖𝟏 ) 𝟐,
𝟏𝓿 𝟑𝟏, 𝟏𝟔 ∗ 𝟏𝟎−
=𝛂 = = 𝟐=
𝟑𝟎] 𝟐𝑶𝒍𝑪[ 𝟓𝟒𝟎 𝟎, 𝟏, 𝟗𝟎
( 𝐧𝐥 ) ( 𝐧𝐥 )
𝟏𝟎] 𝟐𝑶𝒍𝑪[ 𝟓𝟏𝟎 𝟎,
𝟐=𝛂
نحدد 𝛃 بقسمة 𝟐𝓿 على 𝟏𝓿 كالتالي:
𝜶 𝜷
𝟐𝟎] 𝓿𝟐 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟐 ∗ [𝑶𝑯−
=
𝜷 𝟏𝟎] 𝓿𝟏 𝒌 ∗ [𝑪𝒍𝑶𝟐 ]𝟎𝟏 𝜶 ∗ [𝑶𝑯−
𝜶 𝟏𝟎] 𝟐𝑶𝒍𝑪[ = 𝜶 𝟐𝟎] 𝟐𝑶𝒍𝑪[
𝛃
𝟐𝓿 𝜷 𝟐𝟎] [𝑶𝑯− 𝟐𝟎] [𝑶𝑯−
(= (=) )
𝟏𝓿 𝜷 𝟏𝟎] [𝑶𝑯− 𝟏𝟎] [𝑶𝑯−
𝛃
𝟐𝓿 𝟐𝟎] [𝑶𝑯−
(= )
𝟏𝓿 𝟏𝟎] [𝑶𝑯−
بإدخال اللوغارثم النيبيري نجد:
𝛃
𝟐𝓿 𝟐𝟎] [𝑶𝑯−
( 𝐧𝐥 = ) ( 𝐧𝐥 )
𝟏𝓿 𝟏𝟎] [𝑶𝑯−
𝟐𝓿 𝟐𝟎] [𝑶𝑯−
( 𝐧𝐥 ∗ 𝛃 = ) ( 𝐧𝐥 )
𝟏𝓿 𝟏𝟎] [𝑶𝑯−
𝓿 𝟐𝟐, 𝟔 ∗ 𝟏𝟎−
) 𝟐 ( 𝐧𝐥 ( 𝐧𝐥 )𝟐(𝐧𝐥 )
𝟏𝓿 𝟑𝟏, 𝟑 ∗ 𝟏𝟎−
=𝛃 = = 𝟏=
𝟐𝟎] [𝑶𝑯− 𝟓𝟎 𝟎, 𝐧𝐥 )𝟐(
( 𝐧𝐥 ) ( 𝐧𝐥 )
𝟏𝟎] [𝑶𝑯− 𝟓𝟐𝟎 𝟎,
𝟏=𝛃
𝟑 =𝟏𝒏= 𝜶+𝜷 = 𝟐+
𝟑 = 𝒏 Donc l’ordre globale C’est
Vous aimerez peut-être aussi
- Examen Corrigé Thermodynamique USTHB 2012Document4 pagesExamen Corrigé Thermodynamique USTHB 2012mono legasPas encore d'évaluation
- Examen Ratt 2019 - Corrigé TypeDocument5 pagesExamen Ratt 2019 - Corrigé TypeTOGBE Mismadji sosthènePas encore d'évaluation
- Résumé Cour Complexe-2bac - SMDocument2 pagesRésumé Cour Complexe-2bac - SMSven Way83% (6)
- TD Stereochimie 5Document5 pagesTD Stereochimie 5Jean TellPas encore d'évaluation
- Correction TD 1 Robotique 2021-2022Document4 pagesCorrection TD 1 Robotique 2021-2022mina boucPas encore d'évaluation
- Rappel MathematiqueDocument2 pagesRappel Mathematiquemina boucPas encore d'évaluation
- Examen Blanc Maths 2bac Eco SGC Juin 2020 Sujet FRDocument3 pagesExamen Blanc Maths 2bac Eco SGC Juin 2020 Sujet FRAbdellah DaoudiPas encore d'évaluation
- Manipilation 1 Cinétique Hamza BahDocument4 pagesManipilation 1 Cinétique Hamza Bahlailaelkharraz08Pas encore d'évaluation
- MNA2Document5 pagesMNA218188yem3761Pas encore d'évaluation
- Résumé Cours Nombres ComplexesDocument2 pagesRésumé Cours Nombres Complexeshiba06hiba1234Pas encore d'évaluation
- Examen Ratt 2018 Corrigé TypeDocument5 pagesExamen Ratt 2018 Corrigé TypeNadia Berakna100% (1)
- Serie 01-Elts Ressorts-CorrigéDocument4 pagesSerie 01-Elts Ressorts-CorrigéAymen MizouniPas encore d'évaluation
- PST - L3 - Fiche TD 3 + CorrigéDocument8 pagesPST - L3 - Fiche TD 3 + Corrigémayar mimiPas encore d'évaluation
- Cours 3 Pr. HICHAM MAHAJAR Pr. YOUSSEF TABIT PDFDocument4 pagesCours 3 Pr. HICHAM MAHAJAR Pr. YOUSSEF TABIT PDFMatadour SalmanPas encore d'évaluation
- Faz 1 Exercice 3 DS 2 Karim Zrafi 22 23 CorrDocument4 pagesFaz 1 Exercice 3 DS 2 Karim Zrafi 22 23 CorrmouynmehdyPas encore d'évaluation
- Chap3+td3 TitoumDocument7 pagesChap3+td3 Titoumyazid belazzouguiPas encore d'évaluation
- Logique Mathematique Serie Dexercices 1Document2 pagesLogique Mathematique Serie Dexercices 1saidighir94Pas encore d'évaluation
- Correction LOGARITHME 2bac BiofDocument18 pagesCorrection LOGARITHME 2bac BiofAbde Aitoutbib100% (2)
- CorrectionTD2 2017-2018 Traitement Du Signal LicenceDocument11 pagesCorrectionTD2 2017-2018 Traitement Du Signal LicenceMartine KenfackPas encore d'évaluation
- La ContiniutéDocument2 pagesLa ContiniutéJalil ElmouPas encore d'évaluation
- Interrogation de Module Propagation Et AntenneDocument8 pagesInterrogation de Module Propagation Et AntenneBrahim LeguebedjPas encore d'évaluation
- TSE Comp 2et 10-11Document6 pagesTSE Comp 2et 10-11Camara MahamadouPas encore d'évaluation
- Calcul IntegralDocument1 pageCalcul IntegralAbdelKarim dergoulPas encore d'évaluation
- Solution-Examen1 Mécanique Des Fluides ApprofondieDocument2 pagesSolution-Examen1 Mécanique Des Fluides ApprofondieBrice GamintePas encore d'évaluation
- Ensembles Et Applications Corrige Serie D Exercices 2 PDFDocument17 pagesEnsembles Et Applications Corrige Serie D Exercices 2 PDFIlyass AtidePas encore d'évaluation
- 1) Equation D'état de Peng - Robinson (PR) (1976) :: Où: V Volume de Gaz (FT Par 1 Mole de Gaz, FT /mol)Document10 pages1) Equation D'état de Peng - Robinson (PR) (1976) :: Où: V Volume de Gaz (FT Par 1 Mole de Gaz, FT /mol)aoua1997Pas encore d'évaluation
- Correction Mécadessyst PC 2021 Session1Document2 pagesCorrection Mécadessyst PC 2021 Session1glokpaijeanjaures3Pas encore d'évaluation
- Corrigé de La Première Série T.D MEFDocument6 pagesCorrigé de La Première Série T.D MEFali BourenanePas encore d'évaluation
- Concours DDocument4 pagesConcours DmouradPas encore d'évaluation
- Traqueur Du Soleil (Corrigé)Document5 pagesTraqueur Du Soleil (Corrigé)bhasalma220Pas encore d'évaluation
- Modèle Geometrique InverseDocument6 pagesModèle Geometrique InverseMed MaxPas encore d'évaluation
- Chap - I - Moment Cinètique (Enregistrement Automatique)Document16 pagesChap - I - Moment Cinètique (Enregistrement Automatique)Wissal RoumayssaePas encore d'évaluation
- Cours 3Document38 pagesCours 3othnieledi02Pas encore d'évaluation
- Interro 2017 Corrigé PDFDocument3 pagesInterro 2017 Corrigé PDFElîñe ŘošPas encore d'évaluation
- Solution-TD4 Mathématique StatistiqueDocument3 pagesSolution-TD4 Mathématique Statistiquedjennad.kh99Pas encore d'évaluation
- TDN 5 Exercice 1: On Désire Concevoir Une Commande Prédictive Généralisée (GPC) Pour UnDocument9 pagesTDN 5 Exercice 1: On Désire Concevoir Une Commande Prédictive Généralisée (GPC) Pour Unkhmarwan1998Pas encore d'évaluation
- Bac 2022-2Document2 pagesBac 2022-2Chéikhńe O BéíđāhPas encore d'évaluation
- Corrige Serie 3 SuiteDocument4 pagesCorrige Serie 3 Suitesisi serinePas encore d'évaluation
- Exercices Dapplication Acide BaseDocument4 pagesExercices Dapplication Acide BaseMaryem OurriPas encore d'évaluation
- Serie 2 Rotation 2024 Avec CorrectionDocument3 pagesSerie 2 Rotation 2024 Avec Correctionasmamajoul8Pas encore d'évaluation
- TPMCC Auriol Idriss ElliottDocument13 pagesTPMCC Auriol Idriss Elliottoteme Mbella King DuclairPas encore d'évaluation
- Contrôle Continu N2S2 2022-2023 TCDocument2 pagesContrôle Continu N2S2 2022-2023 TCnadaelhaousPas encore d'évaluation
- Correction de L - Exercice N°7 de La Série N°4Document6 pagesCorrection de L - Exercice N°7 de La Série N°4Karim KisserliPas encore d'évaluation
- Organigramme Section Entierement ComprimeeDocument1 pageOrganigramme Section Entierement ComprimeeangePas encore d'évaluation
- Corrigé Du Control Continu 01 en Mécanique Analytique2019-2020Document9 pagesCorrigé Du Control Continu 01 en Mécanique Analytique2019-2020Moulay ZoubirPas encore d'évaluation
- Corrigé Ex de Rattrapage de Physique 1Document2 pagesCorrigé Ex de Rattrapage de Physique 1rayad mahrezPas encore d'évaluation
- 6 - Cours Statistique - 4 SC 2018Document6 pages6 - Cours Statistique - 4 SC 2018alexgeorge1122Pas encore d'évaluation
- Trigonometrique Fin Résume 1bacDocument3 pagesTrigonometrique Fin Résume 1bacDMAR JUSTPas encore d'évaluation
- Loi Normale BivariéeDocument4 pagesLoi Normale BivariéeRayhane OUANANIPas encore d'évaluation
- Correction Série 5 Suite 1bac SCDocument10 pagesCorrection Série 5 Suite 1bac SCchaimaeelkhamar2Pas encore d'évaluation
- Correction de L'examen Des Enseignants Cadres Des Académies 2023 Matière: Physique Et ChimieDocument32 pagesCorrection de L'examen Des Enseignants Cadres Des Académies 2023 Matière: Physique Et ChimieMohamed AIT KASSIPas encore d'évaluation
- Modelisation de Systéme A Deux Bacs CHABANE Fatah (Théodore)Document13 pagesModelisation de Systéme A Deux Bacs CHABANE Fatah (Théodore)hoho100% (1)
- Solution Serie 03Document5 pagesSolution Serie 03Nardjes AbPas encore d'évaluation
- Corrigé td2Document3 pagesCorrigé td2Adem RessaissiPas encore d'évaluation
- Exo Dapp C6Document1 pageExo Dapp C6Alhousseynou DialloPas encore d'évaluation
- Cours Math 3 en ProgressionDocument19 pagesCours Math 3 en Progressionfazfrito lacaviataPas encore d'évaluation
- Etude de Fonctions - Golden Bac - 94193616Document11 pagesEtude de Fonctions - Golden Bac - 94193616Mohamed aziz ben sassiPas encore d'évaluation
- Tableau DeriveesDocument4 pagesTableau DeriveesDr VerdasPas encore d'évaluation
- Chapitre 2-Phénomènes de Surfaces-SolutionsDocument8 pagesChapitre 2-Phénomènes de Surfaces-Solutionsluckfi binadsPas encore d'évaluation
- Cinetique Chimique Carte 2223Document1 pageCinetique Chimique Carte 2223luckfi binadsPas encore d'évaluation
- Exercices TD-N01 - TC - 2023-2024Document1 pageExercices TD-N01 - TC - 2023-2024luckfi binadsPas encore d'évaluation
- Cours Transfert Thermique TC01Document27 pagesCours Transfert Thermique TC01jado thirlwallPas encore d'évaluation
- GénéralitésDocument5 pagesGénéralitésluckfi binadsPas encore d'évaluation
- Chapitre 1 TMDocument17 pagesChapitre 1 TMluckfi binadsPas encore d'évaluation
- Cours D ElectrochimieDocument35 pagesCours D ElectrochimieAdel LaimechePas encore d'évaluation
- Chapitre 2 StéréochimieDocument31 pagesChapitre 2 StéréochimieBirane BaPas encore d'évaluation
- StereoisomerieDocument6 pagesStereoisomerieSorel SikapPas encore d'évaluation
- TP ChimieDocument3 pagesTP Chimienougningguichel100% (1)
- Courschim 3Document42 pagesCourschim 3Firaş BenzaidPas encore d'évaluation
- Série TD N3-S3-20-21Document2 pagesSérie TD N3-S3-20-21فيصل البلخلفيPas encore d'évaluation
- td02 Chimie4Document3 pagestd02 Chimie4Samba BarhamPas encore d'évaluation
- Chapitre 5 Chimie OrganiqueDocument58 pagesChapitre 5 Chimie OrganiqueleloPas encore d'évaluation
- Rattrapage I 6Document3 pagesRattrapage I 6majdaPas encore d'évaluation
- Chimie 4 - StéréochimieDocument12 pagesChimie 4 - StéréochimieNathan CohenPas encore d'évaluation
- Corrigé de L'exercice 47Document4 pagesCorrigé de L'exercice 47mariem OuriPas encore d'évaluation
- UntitledDocument3 pagesUntitledAbdeldjalil MayachePas encore d'évaluation
- CHM144 Chimie Organique FSS P5Document76 pagesCHM144 Chimie Organique FSS P5Pascal GadedjissoPas encore d'évaluation
- TD N°2 - Stéréochimie-ÉnoncéDocument3 pagesTD N°2 - Stéréochimie-Énoncélucas lucasPas encore d'évaluation
- Exercices CHM144 FSS TD5Document9 pagesExercices CHM144 FSS TD5Omega SigmaPas encore d'évaluation
- H2022 - Misession 1 - CorrigéDocument8 pagesH2022 - Misession 1 - CorrigéCassandra MaaloufPas encore d'évaluation
- TD MGS Et StaffDocument11 pagesTD MGS Et StaffdiayeloupPas encore d'évaluation
- StereochimieDocument4 pagesStereochimieninaPas encore d'évaluation
- Fascicule CM UE1-Ch Org 2011-2012Document75 pagesFascicule CM UE1-Ch Org 2011-2012Djonmo ringtoingPas encore d'évaluation
- StereochimieDocument2 pagesStereochimiecamelaPas encore d'évaluation
- TD N 1 de Chimie II Les Composes OrganiqDocument5 pagesTD N 1 de Chimie II Les Composes Organiqmohamed2023ftPas encore d'évaluation
- Chim303atd00 02Document2 pagesChim303atd00 02Kader MilanoPas encore d'évaluation
- Série2 Corrigée SVI S2Document9 pagesSérie2 Corrigée SVI S2Zineb DahmaniPas encore d'évaluation
- TD Stéréochimie 16goodprepaDocument4 pagesTD Stéréochimie 16goodprepaYoussef LaaoujePas encore d'évaluation
- TD5 Stereochimie ConfigurationDocument4 pagesTD5 Stereochimie ConfigurationkushanjidPas encore d'évaluation
- Aermos PharmaDocument2 pagesAermos PharmaIssouf BerthePas encore d'évaluation
- Cours IsomerieDocument11 pagesCours IsomerieJean-François Abena100% (1)
- TD2 (2021)Document2 pagesTD2 (2021)SoufianePas encore d'évaluation
- Descripteurs StéréochimiquesDocument7 pagesDescripteurs StéréochimiquesAbdessamed GherbaouiPas encore d'évaluation
- Isomérie Stéreochimie (Résumé)Document29 pagesIsomérie Stéreochimie (Résumé)Kamal DehbiPas encore d'évaluation