Académique Documents
Professionnel Documents
Culture Documents
Biotransformation Khaoula
Transféré par
Khaoula Kouloughli0 évaluation0% ont trouvé ce document utile (0 vote)
649 vues166 pagesTitre original
5. Biotransformation khaoula
Copyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
649 vues166 pagesBiotransformation Khaoula
Transféré par
Khaoula KouloughliDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 166
Facult de medecine de Constantine
Laboratoire de toxicologie CHUC
Cours de 1
e
anne rsidanat anne 2013/2014
Khaoula KOULOUGHLI
Le 16 Dcembre 2013
1
Plan :
I. Introduction ;
II. Gnralit ;
III. Phase I ;
IV. Phase II ;
V. Pase III ;
V. Facteurs variabilit de la biotransformation;
VI. Rsultats de la biotransformation et bioactivation ;
VII. Interet de la connaissance de la biotransformation
VIII. Exploration de la biotransformation
IX. Conclusion.
bibliographie
2
Le mtabolisme des xnobiotiques est invitable.
L'accumulation sans fin xnobiotiques mme non
toxiques est incompatible avec la survie des
organismes vivants.
Des stratgies de protection sont mis en eouvre,
dont le mtabolisme des xnobiotiques (6).
3
Le mtabolisme des xnobiotiques comme un
domaine de recherche est n au cours de la
premire moiti du 19
e
sicle:
Dcouverte de l'acide hippurique (le conjugu de la
glycine de l'acide benzoque) dans l'urine de cheval.
Dans les annes 1950 ltude du mtabolisme a
vraiment dcoll en raison de la prise de conscience
progressive des scientifiques sur la varit et
l'importance des ractions mtaboliques.
4
5
La biotransformation est un ensemble de
processus biochimiques mis en oeuvre pour
former des composs :
plus polaires, hydrophiles, moins toxiques
facilement excrtables par le rein ou la bile
(dtoxification : dans la majorit des cas).
Parfois la biotransformation peut conduire des
produits plus toxiques (toxification).
6
Le lieu principal de la biotransformation est le
foie.
En raison de son flux sanguin
lev 1.5L/min + sa richesse
en enzymes de mtabolisation.
Peut se produire dans dautres organes :
Poumon, estomac, placenta, intestin, peau, et
rein.
7
Les ractions de biotransformation se divisent en deux types :
Raction de phase I / Dgradation/ Fonctionnalisation:
Ractions de phase II/synthse
/ Conjugaison :
La molcule-mre ou les mtabolites (produit de phase I) se conjuguent
avec une substance endogne.
Phase III la phase dans laquelle les mtabolites quittent la cellule grce a
des protines, pour tre limins (Glycoprotine P par exemple) (2).
8
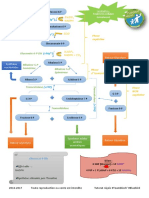
Figure 1. Biotransformation
9
10
Cest la raction de biotransformation la plus
importante (2).
Les mtabolites qui en rsultent sont nombreux.
Loxydation est catalyse par des systmes
enzymatiques :
=> Monooxygnase cyt P450.
flavine.
=> Amine oxydase.
=> dhydrognase
Microsomale
Non Microsomale
11
12
Les monooxygnases sont des oxydorductases
catalysant le transfert dlectrons.
Monooxygnation :
Lincorporation dun groupement hydroxyl sur le
substrat.
Au cours de cette raction :
=> Deux atomes doxygnes sont rduits en un
groupement hydroxyl;
=> Une molcule deau sera libre par oxydation
concomitante du NADPH.
13
Cyt P450 :
Les CYP constituent une famille dhmoprotines
initialement identifies comme
des pigments dans
des microsomes de foie de rat.
Ils sont caractriss par
une bande d'absorption intense
450 nm en prsence de monoxyde de carbone.
Impliqus dans le mtabolisme de substances endognes
(tel que les stroides) et exognes.
14
CYP450 sont composs de :
hme (Fe3+) (groupement
prosthtique) + apoprotine
+ cystinate+Site actif de CYP450.
Localisation:
Prsents en grande quantit dans les hpatocytes, dans les
entrocytes de lintestin grle.
En plus faible quantit dans dautres tissus comme le rein, le
poumon,le cerveau, la peau (5).
Se trouve dans la partie externe du REL. Et au niveau des
mitochondries (9).
15
Le systme P450 des microsomes eucaryotes
contient deux composantes: NADPH CYP450
rductase, une flavoprotine contenant la
fois FAD et FMN, et P450.
FMN et cytochrome b5, assure les transport
des lectrons depuis FAD au CYP450.
16
Les CYP450 ont besoin de deux lments :
>> Une source dlectrons : la NADP
cytochrome P450 rductase (flavoprotine
donneuse dlctrons)(3).
>> Phospholipide (PL) CYP450 (de la mbr du
RE) : assure la cohsion monooxygnase-
rductase.
17
Structure du CYP450 :
18
Des familles de gnes de CYP450 ont t identifies chez
lHomme.
Trois familles sont impliques dans la plupart des
biotransformations de drogues sont CYP1, CYP2 et CYP3.
Ils sont diviss sur la base de similarits de squences
d'acides amins, et chaque famille peut tre divise en
sous-familles, qui sont dsigns par des lettres majuscules
aprs la dsignation de la famille (par exemple, CYP3A).
Enzymes individuels sont ensuite indiqus par des chiffres
arabes (par exemple, CYP3A4).
19
20
21
Un seul hpatocytes peut contenir une varit de CYP450.
Sa spcificit peut tre :
Relative :un isoforme va mtaboliser des substrats diffrents.
Chevauchante :un mme substrat est mtabolis par plusieurs
isoformes.
Homologie de la
squence
dacide amin
Mme famille 40%
Mme sous-
famille
59%
Mme iso-
fomre
97%
22
Tableau montrant les substrats des CYP450 (11) :
23
24
Raction gnrale :
Oxydation par CYP450 est une source physiologique de
stress oxydant (libration dun o au cours du cycle
catalytique).
25
Cycle catalytique du CYP450 (5) :
26
Monooxygnase flavine oxydase :
Un groupe d'enzymes qui catalysent des ractions
chimiques par l'intermdiaire du cofacteur li la
flavine.
Ces protines microsomales catalysent l'oxygnation
de l'azote , de soufre , de phosphore et slnium
atomes nuclophiles dans une gamme de composs de
structures diverses .
L'utilisation d'un cofacteur NADPH et groupement
prosthtique FAD.
27
FMOs ont t impliqus dans le mtabolisme
d'un certain nombre de produits
pharmaceutiques, de pesticides et de
substances toxiques .
Cinq formes de la FMO sont maintenant
connus et ont t dsigns de FMO1 - FMO5
28
Une certaine comptition peut exister entre
les CYP et les FMO vis--vis de certains
substrats.
dans le foie on observe 85 % de CYP pour
seulement 15 % de FMO.
dans la peau seulement 33 % de CYP pour 66
% de FMO.
29
30
Les amine oxydases sont des enzymes largement
distribues dans lorganisme.
Catalysent la dsamination oxydative.
Classes en deux groupes :
FAD amine oxydase : Monoamine oxydase,
polyamine oxydase.
Amine oxydases carbonyles dpendentes :
diamine oxydase... (8).
31
Les MAO sont localisation mitochondriale,
DAO : enzyme soluble (8).
Isoformes :
Les monoamine oxydases (MAO-A et MAO-B)
sont diffrencies selon leur spcificit vis vis
des substrats et selon leur sensiblit aux
inhibiteurs .
Elles diffrent aussi par leur poids molculaire
(MAO A=60kDa, MAO B= 58kDa)(8).
32
Fonction des MAO :
Elles vitent la pntration de ces
amines vasoconstrictives ou toxiques
dans lorganisme comme la tyramine
(3).
33
Les monoamine oxydases sont prsentes dans le
systme nerveux central, qui participent au
catabolisme des amines endognes.
Leau oxygne produite au cours de cette
raction est dtruite par la catalase ou une
peroxydase (3).
34
Enzyme qui oxyde un substrat par le transfert
d'un ou plusieurs ions (H+) un accepteur,
gnralement un coenzyme type
NAD+/NADP+ ou flavine comme le FAD ou
le FMN.
Laldhyde dhydrognase ;
Lalcool dhydrognase.
35
1. Aldhyde dhydrognase (ALDH) :
Enzyme polymorphe responsable de l'oxydation des aldhydes en
acides carboxyliques.
Localises dans de nombreux tissus, principalement au niveau du
foie.
Il existe trois types diffrentes de ces enzymes chez les
mammifres :
ALDH 1 : cytosolyque,
ALDH 2 : mithochondrial,
ALDH 3 : tumeurs, l'estomac et la corne.
ALDH1 et ALDH2 (ttramriques) sont les plus importantes.
36
Il existe des formes
constitutives et
inductibles
2. Alcool dhydrognase ADH :
Lalcool dshydrognase (ADH) est une enzyme
dimrique, hpatique et cytoplasmique.
Lenzyme est aussi prsente dans le rein et le
tube digestif.
LADH catalyse loxydation dun alcool en
aldhyde en transportant les hydrognes sur le
coenzyme NAD
+
.
37
2. Alcool dhydrognase ADH :
Spcificit :
Spcifique des alcools primaires, particulirement
lalcool ethylique.
NB :
Le foie peut aussi oxyder partiellement lalcool par des
hydroxylases cyt p450 (CYP 2E1) inductibles (MEOS
= Microsomal Ethanol Oxidizing System).
Il existe aussi une trs faible oxydation par des
catalases.
38
Classification de lADH (13):
39
40
41
1. Oxydation aliphatique ;
2. Oxydation aromatique ;
3. Epoxydation ;
4. O. Dsalkylation ;
5. N. Dsalkylation ;
6. S. Dsalkylation ;
7. Dsamination oxydative ;
8. N. Oxygnation ;
9. Sulfoxydation;
10. N. Hydroxylation;
11. Dsulfuration oxydative ;
12. Dshalognation.
42
1. Oxydation aliphatique :
La plus frquente ;
Donne des alcools primaires et secondaires qui vont eux mme
subir dautre oxydation.
43
2. Oxydation aromatique :
Deux mcanismes : hydroxylation/par
intermdiare epoxyde :
44
3. Epoxydation :
Ex : Epoxydation des alcnes: formation
despces ractives potentiellement toxiques.
45
4. O-dsalkylation :
46
5. N. Dsalkylation :
47
6. S-Dsalkylation :
48
7. Dsamination oxydative :
49
8. N. Oxygnation :
Peut tre une tape prliminaire de la N.
Dsalkylation.
Les flavine oxydase interviendraient aussi dans ce
mcanisme.
50
9. Sulfoxydation :
Processus mtabolique gnral des
phnothiazines.
Aboutit la formation du sulfoxide
correspondant puis de la sulfone.
Les flavines oxydases prendraient par aussi ce
mcanisme(2).
51
10. N. Hydroxylation :
52
11. Dsulfuration oxydative :
53
12. Dshalognation oxydative :
54
12. Dshalognation oxydative :
Le chloroforme peut former loxychlorure
doxygne (phosgne) toxique (2).
55
56
Oxydation des amines :
Les amines oxydases les transforment en
aldhydes.
Dhydrognation des alcools :
Par ALDH et ADH.
57
58
Les ractions de rduction sont peu courantes.
peuvent impliquer des enzymes microsomales
CYP450.
Ces ractions sont beaucoup plus intenses chez
les bactries intestinales que dans les tissus des
mammifres.
La rduction du prontosil en sulfanilamide en est
un exemple remarquable.
59
1. Rduction des drivs nitrs en une amine :
Assure par la nitrorductase.
60
2. Rduction des drivs azoiques en amines:
Assure par lazorductase.
Azobenzne => aniline.
R-N=N-R => R-NH2 + R-NH2.
61
Cest la raction reverse des
dshydrognase.
62
63
De nombreux xnobiotiques peuvent
subir des hydrolyses sous leffet
destrases et damidases.
Ces enzymes se trouvent dans les
tissus, et le plasma des mammifres.
64
A. Estrases (2):
Regroupes en 4 catgories:
1. Aryl estrases: hydrolysant les esters
aromatiques.
2. Carboxyl estrases: les esters aliphatiques.
4. Actyl estrase : hydrolyse les esters dont la
moiti acide est lacide actique.
5. Choline estrases: les esters dont le rsidu est
un alcool.
65
B. Amidases (2):
Contrairement aux estrases, les amidases ne
peuvent tre classes en fonction de leur
spcificit pour leur substrat.
De plus, l'hydrolyse enzymatique des amides se
produit beaucoup plus lentement que celle des
esters, probablement par manque de spcificit.
66
Exemples dhydrolyse (2) :
67
Linhibition ou lactivation de ces
enzymes peut entrainer une toxicit :
Ex :
Les OP agissent par inhibition de lAch
Esterase.
68
69
Dfinies par la liaison covalente dune molcule
endogne (polaire) un groupement fonctionnel
dune molcule substrat (hydrophobe).
Certains substrat contenant un groupement
fonctionnel appropri puisse directement subir la
phase II du mtabolisme.
Mais la conjugaison se produit souvent
conscutivement une raction de phase I.
70
C'est la forme de conjugaison la plus courante et la plus
importante.
Molcule endogne Acide glucuronique.
Forme active : l'UDPGA (acide uridine-5'-
diphospho-a-D-glucuronique).
Enzyme et
localisation
UDP-glucuronyltransfrase (UGT): localise
dans le rticulum endoplasmique. Foie,
rein , intestin.
Deux familles: UGT1,2.
Les UGT sont impliques dans la dtoxification
des endobiotiques (ex. bilirubine, thyroxine,
strodes) et des xnobiotiques .
Substrat Alcools aliphatiques ou aromatiques,
Acides carboxyliques,
Composs soufrs ,
Amines.
71
La raction aboutira la formation de S, O, N
glucuronides polaires, limins dans la bile et les urines.
Lhydrolyse du conjugu cause du PH urinaire ou
cause des Bta-glucoronidases des bactries intestinales
gnrent des molcules toxiques. Ex : 2-naphtyl amine ;
libration dion nitrnium lectrophile cancrogne (2-
naphtyl hydroxyl amine).
72
Devenir des glucuronides :
PM < 250 : limination urinaire.
PM > 250 : excrtion biliaire, limination fcale
ou hydrolyse par les -Glucoronidases
intestinales.
73
Molcule endogne Sulfate.
Forme active: PAPS (3-
phosphoadnosine-5'-
phosphosulfate).
Enzyme et
localisation
Sulfotransfrase : localises dans le
cytosol du foie, rein, intestin.
03 familles (SULT 1,2,3) : 16 isoformes/
Substrats les phnols, les alcools aliphatiques
et les amines aromatiques.
74
Molcule endogne CH3
Forme active s adnosyl
mthionine.
Enzyme et
localisation
N. Mthyltransfrases.
S. Met transfrase
O. Met transfrase.
06 isoformes.
Substrat Phnol, amine, thiol, As.
75
Les produits mthyls ne sont pas
ncessairement plus hydrosolubles.
76
Molcule endogne Actyl : CO-CH3
Forme active Actyl CoA.
Enzyme et
localisation
N-actyltransfrases : cytosolique
foie ,intestin ,rein ,poumon.
2 isoformes :NAT1 et NAT2
Substrat Des amines aromatiques
primaires,
Des hydrazides,
Des sulfonamides,
Certaines amines aliphatiques
primaires.
77
A cause du polymorphisme gnrique, certains
individus sont des actyleurs rapides, dautres
des actyleurs lents.
Les actyleurs lents seraient plus sensibles
lapparition de cancer dus aux amines
aromatiques.
Les mtabolites actyls sont limins de
lorganisme par excression rnale.
78
Mais pour lisoniaside lactylation produit des
composs moins hydrosolubles, qui se cristalisent
au niveau rnal : nphrotoxicit (!).
Les effets secondaires neurologiques seraient
plus importants chez les actyleurs lents (12).
79
Molcule endogne Glutathion tripeptide : ac
glutamique cystine-glycine
Enzyme et
localisation
glutathion S-transfrases . Au moins
5 sous-familles, 20 isoformes :A1
,A2 M1 ,M2.
cytosol (A,M P T )+ RE (Z) + noyau
surtout foie ,reins ,poumon ,intestin
Substrat grande varit de composs
environnementaux (carcinognes
(ex :benzo[a]pyrne)
mdicaments :Paractamol
,anticancreux (alkylants).
= les lectrophiles
80
De nombreux mtabolites lectrophiles se
forment au cours de la biotransformation des
toxiques:
Certains de ces mtabolites peuvent ragir avec
des constituants cellulaires et causer la mort de
la cellule ou induire la formation de tumeurs.
La fonction du glutathion (nuclophile) est de
ragir avec ces mtabolites lectrophiles et de
prvenir ainsi leurs effets nocifs sur les cellules.
81
L'exposition de grandes quantits de ces
mtabolites ractifs peut diminuer la quantit de
glutathion disponible et provoquer des effets
toxiques marqus.
Ex : Le 3-mthylindole est bioactiv
principalement dans les poumons, et aprs avoir
abaiss la teneur en glutathion, produit des
lsions pulmonaires (1).
82
Certains conjugus du glutathion
peuvent tre toxiques (1).
83
Conjugaison des acides amins.
Cette conjugaison est catalyse par des acides
amins dj conjugus et le coenzyme A.
Les acides carboxyliques aromatiques,
Les acides arylactiques,
Les arylacides aryl-substitus,
Peuvent former des conjugus avec
des a-aminoacides, principalement la glycine,
mais aussi avec la glutamine(1).
84
Molcule endogne Thiosulfate Na
2
S
2
O
3.
Enzyme et localisation Rhodanse = transulfurase.
Mitochondrie.
Substrat Cyanure : assure leur
dtoxification en thiosulfate.
Raction
Na
2
S
2
O
3
+ CN
-
SCN
-
+ Na
2
SO
3
85
Les transporteurs membranaires facilitent la
capture ou lefflux des composs endognes,
dions et de xnobiotiques travers la membrane
cellulaire.
Ils influencent par consquent la biodisponibilit
des xnobiotiques dans lorganisme en
participant leur absorption, leur distribution et
leur limination (10).
86
Les transporteurs sont diviss en deux catgories:
La superfamille des transporteurs ABC (ATP-binding
cassette) :
Des pompes defflux qui dpendent de lhydrolyse de
lATP afin dactiver le passage des substrats au travers
des membranes biologiques.
Limitent laccumulation de composs cytotoxiques.
Les transporteurs ABC incluent larchtype P-
glycoprotine (P-gp ou Multidrug resistance protein
1 [MDR1] (10).
87
La superfamille des transporteurs de soluts (solute
carriers [SLC]):
Assurent gnralement la capture cellulaire des
nutriments comme le glucose ou les acides amins,
soit par mcanisme de transport passif ou actif.
Jouent un rle prononc dans la pharmacocintique
(absorption, distribution et limination) dun large
panel de mdicaments, toxines, composs
endognes et de leurs mtabolites (10).
88
Les transporteurs defflux rduisent la charge
locale cellulaire de composs toxiques,
renforant ainsi la protection de la cellule contre
les effets toxiques.
Ces transporteurs sont essentiellement exprims
dans la membrane apicale des cellules
pithliales (comme les entrocytes) qui sont
exposes aux xnobiotiques.
=> phase III : transport de lefflux, ou extrusion
(10).
89
Causes de variation du mtabolisme (5):
1. Polymorphisme:
Le niveau dactivit enzyamtique est soumis
une rgulation gntique.
Les mutations des gnes codant pour une
enzyme peuvent donner lieu des variations :
lactivit de lenzyme peut tre plus leve,
plus basse ou nulle.
90
Le polymorphisme divise la population en
deux catgories de mtaboliseurs :
Les mtaboliseurs lents;
Les mtaboliseurs rapides ou extensifs.
91
Mtaboliseurs lents :
En cas de dtoxification :
Il se produit une accumulation de la molcule.
Pour les mdicaments a entrainera
lapparition deffets indsirables, voir de
surdosage.
En cas de toxification : Absence deffets.
92
Mtaboliseurs rapides :
En cas de dtoxification : pas de rponse.
En cas de toxification :
Accumulation du mtabolite toxique dans
lorganisme.
93
2.ge :
A. Nouveau n :
A la naissance, la concentration totale des
cytochromes P450 hpatiques reprsente 30% du
niveau adulte.
Le CYP 3A7 chez le feotus, joue le role du CYP 3A4
chez ladulte.
B. Personne age :
Linfluence de lge sur les cytochromes reste
controverse.
De plus, elle est difficile tudier en raison des
variations interindividuelles non dpendantes de
lge.
94
3. Sexe :
La diffrence dactivit enzymatique entre les
hommes et les femmes peut sexpliquer par la
prsence dhormones strodes, comme les
oestrognes et la progestrone en plus grande
quantit chez la femme.
Les hormones strodes semblent activer les
CYP 3A4 (substrat endogne).
De plus, il a t prouv que les contraceptifs oraux
peuvent influencer le mtabolisme de certains
mdicaments en inhibant par un mcanisme suicide
les cytochromes P450, et en particulier le CYP 3A4.
95
4. Obsit :
Les tudes ont montr que leffet de lobsit sur les
cytochromes P450 tait fonction des isoenzymes.
Les rsultats les plus concluants ont t rapports pour le
CYP 3A4 et pour le CYP 2E1 :
Pour le CYP 3A4, lactivit est diminue.
A linverse, lactivit du CYP 2E1 est augmente.
96
5. Pathologies hpatiques :
Les effets sont plus marqus avec la cirrhose quavec
une hpatite chronique et une cholestase.
Les maladies hpatiques rduisent lactivit des
cytochromes de faon spcifique.
Ex : en cas de cirrhose quelque soit sa gravit 1A
diminue.
Le cyp 2C semble tre moins affect par les
pathologies hpatiques.
97
6. CYP450 et interactions :
1. Inhibition du CYP450 :
Certaines substances ont la capacit dinhiber le
CYP450.
Linhibition est gnralement spcifiques dune
isoenzyme .
Phnomne plus dangereux que linduction.
98
6. CYP450 et interactions :
Essentiellement 3 tapes au niveau du cycle du
cytochrome sont particulirement vulnrables
linhibition :
Ltape 1 quand le substrat se fixe sur lenzyme.
Ltape 3 quand loxygne molculaire se fixe sur
le fer ferreux.
Ltape 6 quand la molcule doxygne est
transfre sur le substrat.
99
6. CYP450 et interactions :
Mcanismes de linhibition :
Rduction de synthse ou augmentation du
catabolisme;
Lintroduction dans la membrane du REL de
substances dsorganisant les structures de la mbr.
De la fixation sur le groupement hme du CYP450
de molcules bloquant le cycle catalytique.
100
6. CYP450 et interactions :
Types dinhibitions :
Rversible
Irreversible.
101
6. CYP450 et interactions :
1. A. Inhibition rversible :
Les plus puissants inhibiteurs rversibles ont
dans leur structure chimique des groupements :
imidazoles, pyridines ou quinoliques.
La fonction du cytochrome est restaure aprs
limination par lorganisme de linhibiteur (il t
li par une liaison faible).
102
6. CYP450 et interactions :
1. A. Inhibition rversible :
Comptitive :
La liaison de linhibiteur empche la fixation du
substrat sur le site actif de lenzyme car linhibiteur a
une plus forte concentration au niveau du site actif.
Une substance inhibitrice dune enzyme nest pas
ncessairement le substrat de cette enzyme.
Se produit et sestompe rapidement car aucune
synthse enzymatique nest requise.
103
6. CYP450 et interactions :
1. A. Inhibition rversible :
Non comptitive :
La liaison se fait sur un site diffrent du site actif
et ne bloque pas la fixation du substrat.
Entrane une modification de la conformation
tridimensionnelle de lenzyme la rendant ainsi
non fonctionnelle.
104
6. CYP450 et interactions :
1. A. Inhibition rversible :
Exemples dinhibition rversible :
Cimtidine.
Antifongiques azols (CYP3A).
Jus de pamplemousse (CYP3A intestinale).
105
6. CYP450 et interactions :
1. B. Inhibition irreversible :
Certains agents peuvent tre oxyds par le cytochrome en
intermdiaire ractif qui va provoquer une inactivation
irrversible (destruction).
Substrat suicide: intermdiaires ractifs se lient de faon
covalente lhme, la protine ou aux deux.
Un phnomne rapide, dose et temps dpedant.
La synths de nouvelle enzymes est ncessaire pour
restaurer lactivit.
106
6. CYP450 et interactions :
1. B. Inhibition irreversible :
Exemples dinhibition irreversible :
Ethymyloestradiol : (3A4).
Chloramphnicol : (2B, 2C).
107
6. CYP450 et interactions :
2. Induction enzymatique/Mcanisme :
108
6. CYP450 et interactions :
2. Induction enzymatique :
En cas de dtoxification :
La concentration plasmatique du substrat est
notablement rduites ( de la tox).
En cas de toxification :
Le mtabolite actif saccumule dans lorganisme
( de la tox).
109
6. CYP450 et interactions :
1. Induction enzymatique :
Linduction enzymatique est un phnomne:
Non spcifique (activent de trs nombreux
systmes enzymatiques);
Progressif (dans son apparition et sa disparition),
Non immdiat ;
Rversible.
110
6. CYP450 et interactions :
1. Induction enzymatique :
Ex :
Millepertuis: lhyperforine: acclre la synthse
CYP3A4.
Phnobarbital : (2C ,2D6 ,3A).
Ethanol : (2 E1).
Fume de cigarette : (1A).
111
Figure. Exemples dinducteur et dinhibiteur des isoforme CYP450 (11)
112
2. variabilit alcool dhydrognase ADH :
ADH2 :3 variants :
=> 1 forme sauvage ADH2*1.
=> 2 formes atypiques ADH2*2 ,ADH2*3 :
activit.
113
114
115
Si les deux allles sont muts, une
accumulation dactaldhyde va se produire;
Apparition du syndrome de Flushing :
raction dintolrance = effet antabuse
(vasodilatation, tachycardie, sueur, nause,
vomissement, intolrance alcool, protection
contre alcoolisme )
1. glucuroconjugaison :
Espces : les chats nont pas dUGT.
Age : elle est faible la naissance (ictre du n.n)
Environnement:
Induction par HAP ,phnobarbital ,thanol
Polymorphisme gntique
NB : bilirubine UGT1
homme :mutation sur UGT1A1 :
hyperbilirubinmie
syndrome de Gilbert et syndrome de crigler Najar
(mortel la naissance)
116
V.2. Facteurs modifiant les ractions de phase II
2. Glutathion :
Induction :HAP ,phnobarbital...
Polymorphisme gntique :M1 ,P1 ,T1 ,M3
117
V.2. Facteurs modifiant les ractions de phase II
3. Actylation :
Espces : chien :pas pour amines I.
souris :3 isoformes.
Polymorphisme gntique :
NAT2 :9 mutation dtectes dont 4 ont une
activit trs faible :phnotype actyleur lent
118
V.2. Facteurs modifiant les ractions de phase II
4. Sulfoconjugaison :
porc : pas de sulfconjugaison.
Polymorphisme gntique.
119
V.2. Facteurs modifiant les ractions de phase II
5. Mthylation :
polymorphisme sur TMPT.
caucasiens : 11% mthyleurs lents.
1 personne/300 :activit nulle.
120
V.2. Facteurs modifiant les ractions de phase II
121
122
Dans la majorit des cas le mtabolisame aboutit
une dtoxification, et une limination.
Les produits forms sont pharmacologiquement
moins efficaces et de toxicit diminue.
123
Pour les mdicaments, il est possible que le
mtabolite form soit plus actif que la molcule
mre.
Ex : Dsipramine (forme par N-dmthylation
de limipramine) de plus forte proprit
antidpressive (2).
124
Mais, certains composs chimiquement stables
peuvent tre convertis en mtabolites ractifs.
Ces ractions sont gnralement catalyses par
des monooxygnases cytochrome P-450, mais
d'autres enzymes, y compris ceux de la flore
intestinale, interviennent dans certains cas (1).
125
Les ractions de bioactivations :
Epoxydation
126
Les CYP 450 peuvent produire la conversion de
nombreux composs aromatiques en epoxydes.
Ex :
Aflatoxine B1 ;
Benzne ;
Benzo [a] pyrne ;
Furosmide ;
Polychlorobiphnyl ;
Trichlorthylne ;
Chlorures de vinyl.
127
Lepoxydation se produit principalement au
niveau hpatique.
Les mtabolites forms contractent des
liaisons covalentes avec les macromolcules
cellulaires : provoquent des ncroses et des
cancers (2).
128
Certains mtabolites hydroxyls forment aussi
des liasons covalentes peuvent tre lorigine de
cancers et de ncrose tissulaires.
Les mtabolites N.Hydroxyls des amines
aromatiques peuvent induire une hmolyse ou
une mthmoglobinmie (2).
129
Au cours du mtaboisme rductif de certains
xnobiotiques (nitrobenzne, aniline, anticancreux
de de la classe des anthraquinone), se forment des
structures intermdiaires radicalaires.
Anions superoxydes, peroxyde dhydrogne, radical
hydroxyl.
Les radicaux se lient de faon covalente avec les
protines et les lipides insaturs=> peroxydation des
lipides et une srie de phnomnes toxiques (2).
130
Dsulfuration : Parathion => paraoxon : OP
inhibiteurs plus puissant de la choline estrase.
La dhydrognation de lthanol entraine la
formation de lactaldhyde impliqu dans
certaines manifestations toxiques de lthanol.
131
Certains composs peuvent subir une activation
dans le tube digestif:
Ex: les nitrites et certaines amines peuvent
former des nitrosamines.
les nitrates, qui peuvent tre convertis en nitrites
et induire de la mthmoglobinmie.
132
La glucuroconjugaison est une raction de dtoxification,
Les substances glucuroconjugues sont facilement
xcrts, et ont moins dactivit biologique ou chimique
par rapport la molcule mre.
Cependant certains glucuronides ayant une ctivit
chimique lectrophile peuvent tre impliqus dans des
ractions pharmacologiques ou toxicologiques (14).
Ex : N-O glucuronide de lacide hydroxamique (N-hydroxy-
N-acetyl-arylamines) et les acyl glucuronides de lacide
carboxylique (14).
Figure : (6) Rpartition des ractions formant des mtabolites ractifs et/ou toxiques pour les mdicaments.
Bernard Testa & al. Foundation review: Reactions and enzymes in the metabolism of drugs and other
xenobiotics. Drug Discovery Today Volume 17, Numbers 11/12 June 2012.
133
134
135
136
1. Thrapeutique :
Permet dviter les interactions
mdicamenteuses (inhibition/induction
enzymatique).
=> Minimiser les risques de toxicit et
dechec thrapeutique.
137
1. Thrapeutique :
mdicament Mtabolite
actif inactif
prodrogue actif
actif actif
actif toxique
138
1. Thrapeutique :
Elle permet aussi de choisir les traitements efficaces
en cas dintoxication :
Ex : thanol en cas dintoxication par mthanol.
ADH plus affine pour lethanol que le mthanol, en
plus les mtabolites issus de son action sur
lthanol(acide actique) sont moins toxique que
ceux du mthanol (acide formique).
Phnobabital : ictre du n n, maladie de Gilbert.
139
1. Thrapeutique :
Les tudes biochimiques pour la conception de
nouvelles molcules mdicamenteuses doivent tre plus
attentives quant la formation de mtabolites
chimiquement ractifs (dsipramine ) ou toxiques
(paractamol en PAQI) au cours de essais cliniques et
mme en post-commercialisation (6).
140
2. Analytique :
Quantification des mtabolites :
La mtabolisation de la molcule mre va rendre
difficile sa dtection dans les liquides
biologiques.
La recherche des mtabolites trouve alors tout
son intret.
141
2. Analytique :
En analyse chromatographique :
Ex : limipramine donne plusieurs mtabolites.
Sa chromatographie est complexe.
En cas dabsorption massive lors dune intoxication aigue,
on trouve :
un spot produit absorb.
une srie de taches dintensit variable divers
mtabolites.
142
2. Analytique :
Les liquides daspiration ou de lavage
gastrique offre un avantage car ils
renfrment les molcules non
mtabolises.
143
3. toxicologique :
Permet de dterminer les ractions de
toxification et de dtoxification des substances
toxiques.
144
3. toxicologique :
Bioactivation :
Paractamol en NAPQI (oxydation).
2-naphtylamine en 2 naphtylhydroxylamine
responsable de cancer vsical (oxydation).
Dtoxification (la plus frquente) :
Paraoxon en paranitrophnol (hydrolyse).
Phnol en phnol glucuronide (glucuroconjugaison).
Cyanure en thiocyanate.
145
146
147
Ligne directrice de lOCDE N417
toxicocintique-mtabolisme (7) :
Permet didentifier les mtabolites
produits aprs ladministration du
substrat.
148
Protocole :
Espce : les meme espces utilises dans les
autre essai de toxicit : rat ;
ge et souche: jeune adulte sain 6 a 12 semaines
au moment de ladministration de la dose.
Nombre et sexe des animaux : au minimum 4
animaux du mme sexe. (il convient de justifier le
sexe des animaux employs).
149
Hbergement: Placs dans des cages individuelles pendant la
priode dessai*.
Substance dessai : radiomarque au 14C**.
Choix des doses :
Etude pilote : dose orale unique, non toxique, sufisamment
leve pour permettre lidentification des mtabolites dans les
excrta.
Etude principale : au minimum deux doses de prfrence***.
Lorsque deux doses sont administres, elles sont toutes deux
suffisamment leves pour permettre lidentification des
mtabolites dans les excrta.
150
On recueille les excrta (et, le cas chant, le
plasma) afin didentifier et de quantifier la
substance dessai et ses mtabolites.
Identifier tous les mtabolites prsents hauteur
de 5 % ou plus de la dose administre et pour
fournir un schma mtabolique de la substance
dessai.
151
Identification des mtabolites :
Chromatographie gazeuse/spectromtrie de
masse (CG-SM),
Chromatographie liquide/spectromtrie de
masse (CL-SM),
Chromatographie liquide/spectromtrie de
masse en tandem (CL-SM/SM),
Spectromtrie par RMN,
Peuvent fournir une identification non ambigu.
152
La ligne directrice OCDE estime que ltude
de linduction et de linhibition
enzymatique est ncessaire dans certaines
situations particulires.
153
Permettent de dterminer la voie
mtabolique implique dans la
biotransformation dune substance.
154
1. Les enzymes recombinates :
Obtenue partir de lADNc, exprimes sur diffrents types
cellulaires.
Offre un systme enzymatique individuel permettant
dtudier le mtabolisme de la substance et les
interactions.
Toutefois, en raison de l'absence de voies mtaboliques
comptitives dans ces systmes, il est impossible
d'obtenir des donnes sur la contribution relative de
l'isoforme en question sur le mtabolisme global in vivo.
155
On trouve maintenant sur le march des prparations
recombinantes purifies pour la plupart des enzymes du
mtabolisme :
CYP co-exprims avec cytochrome P450 rductase et
optionnellement cytochrome b5, UGT, mono-
oxygnases flavine, poxyde hydrolase et glutathion S-
transfrases.
156
2. Fraction cellulaire :
Englobe les microsomes, dautres organelles
cellulaires.
Comporte : les microsomes, fraction S9 (contient
des enzymes microsomiales et des enzymes
cytosliques), la fraction cytosolique S100
(comporte 3 enzymes solubles de la phaseII).
3. Culture cellulaire et organes perfuss, etc.
157
158
Identification des enzymes responsables des
ractions de biotransformation (10) :
Plusieurs approches existent pour tudier le
mtabolisme in vitro (phnotypage), et une
combinaison de mthodes est souvent
ncessaire.
159
1. test de comptence (enzyme recombinantes):
Determiner lisoforme responsable du
mtabolisme de la molcule.
Par incubation de la substance avec des
isoformes diffrents et une seule
concentration.
160
2. Test dinhibition :
Une seconde approche implique des incubations
menes dans des fractions subcellulaires ou
ventuellement en culture cellulaire, et lutilisation
dinhibiteurs chimiques et/ou des dimmuno-
inhibiteurs slectifs de voies enzymatiques
spcifiques.
Incubations avec diffrents inhibiteurs en comparant
les taux relatifs de mtabolisme, permet didentifier
quel inhibiteur rduit significativement le mtabolisme
global et ainsi dcouvrir la voie mtabolique.
161
3. Test de correlation :
En utilisant la mme banque de microsomes, le test de
corrlation se fait entre des activits spcifiques
dtermines pour chaque enzyme et les activits
obtenues pour la sustance tester.
Une corrlation significative dmontre limplication de
lisoforme.
162
Extrapolation in vivo in vitro :
Extrapolations restent semi-quantitatives compte tenu
des difficults de la prise en considration des facteurs
de variabilits physiologiques (flux sanguin hpatique,
fixation aux protines plasmatiques, mtabolisme
extrahpatique )(10).
163
Anticiper la biotransformation de tout compos
donn (6).
Expertise humaine reste certainement
irremplaable, mais son efficacit peut tre
grandement amliore par des mthodes in silico
visant fournir des prvisions fiables mais ne
sont pas ncessairement infaillibles (6).
La biotransformation des xnobiotiques est un
phnomne majeur de dtoxification, mais
qui peut aussi entrainer la formation dentit
plus ractive.
Sa connaissance est primordial pour tout
xnobiotique.
164
165
1. Franc Lu, toxicologie gnrale 1991.
2. Alain Viala, Alain Botta, toxicologie, 2
e
dition.
3. Facult de mdecine Pierre & Marie Curie www.chups.jussieux.fr.
5. Amlie Mathie, thse de doctorat universit de Lorraine, Rle des cytochromes P450 dans les
interactions mdicamenteuses et environnementales rencontres lofficine.
6. Bernard Testa & al. Foundation review: Reactions and enzymes in the metabolism of drugs and
other xenobiotics. Drug Discovery Today Volume 17, Numbers 11/12 June 2012.
7. Ligne directrice OCDE 417, juillet 2010.
8. Rana Youssef CHAAYA, Thse de doctorat de luniversit de Toulouse. RLE DU STRESS OXYDANT
INDUIT PAR LES MONOAMINE OXYDASES DANS LA FIBROSE RNALE.
9. Les cytochromes P450 : mtabolisme des xnobiotiques, rgulation et rle en clinique(Ann Biol
Clin 2006).
10. Koukeb ROUGUIEG-MALKI, thse de doctorat de luniversit de Limoge, Etudes des relations
gnotype-phnotype des enzymes du mtabolisme et des transporteurs defflux des xnobiotiques.
11. Xavier Decleves, Universit paris Descartes, Mtabolisme et Excrtion : Aspects Physiologiques
et Mthodes dExploration.
12. http://www.lab-cerba.com. (isoniazide)
13. http://www.ipubli.inserm.fr analyse/ mtabolisme de lthanol.
14. Joseph K. Ritter , Roles of glucuronidation and UDP-glucuronosyltransferases in xenobiotic
bioactivation reactions Chemico-Biological Interactions 129 (2000) 171193.
15. www.pharmacorama.com.
166
Vous aimerez peut-être aussi
- Pranayama La Dynamique Du SouffleDocument151 pagesPranayama La Dynamique Du Soufflealexandre_brillantPas encore d'évaluation
- ReprotoxicitéDocument83 pagesReprotoxicitéKhaoula Kouloughli100% (3)
- Les OpéronsDocument13 pagesLes OpéronsSOO BABA100% (1)
- Electrophorèse 2014.2015Document29 pagesElectrophorèse 2014.2015Khaoula Kouloughli100% (1)
- Statique Du SolideDocument4 pagesStatique Du SolideHal Sof100% (1)
- Cours - Introduction À L'enzymologieDocument27 pagesCours - Introduction À L'enzymologieElbouk Valia100% (2)
- Enzymologie CoursDocument49 pagesEnzymologie CoursSoufiane KarchaliPas encore d'évaluation
- Toxicocinétique Des Xénobiotiques: I - Généralités - DéfinitionsDocument14 pagesToxicocinétique Des Xénobiotiques: I - Généralités - DéfinitionsHabibi BarryPas encore d'évaluation
- Dosage RedoxDocument13 pagesDosage RedoxLina BahazPas encore d'évaluation
- Chapitre 2 Moteurs À Combustion InterneDocument34 pagesChapitre 2 Moteurs À Combustion InterneDile Stephen SAMBA SAMBAPas encore d'évaluation
- Biochimie Microbienne 1 1Document25 pagesBiochimie Microbienne 1 1khalilsassi90Pas encore d'évaluation
- BioénergétiqueDocument16 pagesBioénergétiqueomarou18100% (6)
- Cours Acides Aminés PDFDocument9 pagesCours Acides Aminés PDFTCHEMMIK Naziha0% (1)
- Pfe PhosphateDocument12 pagesPfe PhosphateAnouarJebraoui100% (4)
- Facteurs Influençant La Toxicité KhaoulaDocument62 pagesFacteurs Influençant La Toxicité KhaoulaKhaoula Kouloughli100% (7)
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Biotransformation PDFDocument22 pagesBiotransformation PDFLinaMimosaPas encore d'évaluation
- Les Sels Nutritif Dans L'oceanDocument32 pagesLes Sels Nutritif Dans L'oceansamir hamadPas encore d'évaluation
- Isolement Et Purification Des EnzymesDocument17 pagesIsolement Et Purification Des Enzymesikramguellal3Pas encore d'évaluation
- ANTOCYANDocument5 pagesANTOCYANfarracygmailcomPas encore d'évaluation
- COURS BCF EtudiantsDocument22 pagesCOURS BCF Etudiantsamine bedjaPas encore d'évaluation
- Fiche (5) DigestionDocument2 pagesFiche (5) DigestionzebbPas encore d'évaluation
- Cours 9 Formes Galeniques Et Voies D'administrationDocument35 pagesCours 9 Formes Galeniques Et Voies D'administrationGhazoua MerchaouiPas encore d'évaluation
- Cours de Phytochimie 1 MASTERDocument22 pagesCours de Phytochimie 1 MASTERFANKELE ALASSANE KONE100% (1)
- Phenicoles 2010 Hux1Document4 pagesPhenicoles 2010 Hux1Ouedraogo SoumailaPas encore d'évaluation
- Sfa+ Chimie Seche 2017Document2 pagesSfa+ Chimie Seche 2017kimoPas encore d'évaluation
- Ue Bio 233 Etudes Des Mouvements RespiraDocument10 pagesUe Bio 233 Etudes Des Mouvements Respirajacques yiborPas encore d'évaluation
- CM - Pharmacie GaléniqueDocument10 pagesCM - Pharmacie GaléniqueLeya MarechalPas encore d'évaluation
- Biochimie TPDocument11 pagesBiochimie TPdjeldjelli nawelPas encore d'évaluation
- Mémoire: Option: Biochimie Moléculaire Et SantéDocument97 pagesMémoire: Option: Biochimie Moléculaire Et Santétahaniu gouaouPas encore d'évaluation
- Cours Phytochimie Boumerfeg S.Document24 pagesCours Phytochimie Boumerfeg S.Clementine Eyezo'oPas encore d'évaluation
- Enzymologie Théorique Bio 2 M1Document34 pagesEnzymologie Théorique Bio 2 M1mouassimPas encore d'évaluation
- Structure Des GlucidesDocument28 pagesStructure Des GlucidesWissal ElbarPas encore d'évaluation
- FermentariDocument53 pagesFermentariBulat AlexandrinaPas encore d'évaluation
- 1 Conception Et Processus de Développement Des Medicaments FINALDocument14 pages1 Conception Et Processus de Développement Des Medicaments FINALtebbakh tebbakhPas encore d'évaluation
- Etude de L'Effet De, Le Sélénium Et Le Senps Sur Des Troubles Physiologiques Et Métaboliques Induits Par Le Plomb Chez Des Rattes GestantesDocument106 pagesEtude de L'Effet De, Le Sélénium Et Le Senps Sur Des Troubles Physiologiques Et Métaboliques Induits Par Le Plomb Chez Des Rattes Gestantesmaroua henka100% (1)
- TSTL - Bioch.Cours .Chap.1.Les Glucides.I.Les - OsesDocument15 pagesTSTL - Bioch.Cours .Chap.1.Les Glucides.I.Les - OsesBiochemistry Hunter100% (1)
- BiocatalyseDocument23 pagesBiocatalysemohamed benlaraguePas encore d'évaluation
- Syntheses de SaponificationDocument10 pagesSyntheses de SaponificationMoed MoedPas encore d'évaluation
- TP N2. Évaluation de Lactivité Antioxydante de Lacide Ascorbique636Document4 pagesTP N2. Évaluation de Lactivité Antioxydante de Lacide Ascorbique636rayane youcef100% (1)
- Techniques D'analyses Des Proteines-1Document37 pagesTechniques D'analyses Des Proteines-1immPas encore d'évaluation
- C. Biochimie III. Lipides (III.1. Métabolisme Des Acides Gras)Document41 pagesC. Biochimie III. Lipides (III.1. Métabolisme Des Acides Gras)Rania HamdiPas encore d'évaluation
- Cours - Biochimie Structurale - Lipides - CAG - UNA - 2019 - CopieDocument83 pagesCours - Biochimie Structurale - Lipides - CAG - UNA - 2019 - CopieStellaPas encore d'évaluation
- 3les ProteinesDocument55 pages3les ProteinesHaddy MarouanePas encore d'évaluation
- Correction TD Metabolisme Glucidique 2Document31 pagesCorrection TD Metabolisme Glucidique 2acheparfaite958Pas encore d'évaluation
- Compte Rendu BV tp9Document8 pagesCompte Rendu BV tp9Jean gabriel MouchePas encore d'évaluation
- 1 Materiel GenetiqueDocument50 pages1 Materiel Genetiqueoussama bousseloubPas encore d'évaluation
- Voir Le Cours Sur Les Cinétiques À 2 Substrats.: Enzymologie: Réactions Enzymatiques À Deux SubstratsDocument5 pagesVoir Le Cours Sur Les Cinétiques À 2 Substrats.: Enzymologie: Réactions Enzymatiques À Deux SubstratsLAMINE DEGUISTARPas encore d'évaluation
- Tableau Comparatif Des Techniques ChromatographiquesDocument1 pageTableau Comparatif Des Techniques Chromatographiqueskhouloud gazzehPas encore d'évaluation
- 2 - Corrigé TD Chapitre 3 AllostérieDocument3 pages2 - Corrigé TD Chapitre 3 AllostérieChaka TraorePas encore d'évaluation
- Enzymologie TP Invertase PolycopieDocument14 pagesEnzymologie TP Invertase Polycopieiliass lahmassPas encore d'évaluation
- Voie Des Pentoses Phosphates (MaJ) - 2Document1 pageVoie Des Pentoses Phosphates (MaJ) - 2Hadrien De Greef100% (2)
- Série N°1-TP BromatologieDocument6 pagesSérie N°1-TP Bromatologieparapharmacie oumaymaPas encore d'évaluation
- COMPTE RENDU DE CHIMIE MINERALE 2 2023 FinalDocument5 pagesCOMPTE RENDU DE CHIMIE MINERALE 2 2023 FinalMeryem Bouh0% (1)
- Enzymologie 1Document59 pagesEnzymologie 1Dr.Zakaria MFTPas encore d'évaluation
- L - Histoire de La Pharmacie Et Du Medicament - PPT (Mode de Compatibilité)Document175 pagesL - Histoire de La Pharmacie Et Du Medicament - PPT (Mode de Compatibilité)ilyass.charfadiPas encore d'évaluation
- Activite Synthese de La Lidocaine-2Document8 pagesActivite Synthese de La Lidocaine-2Malika AkesbiPas encore d'évaluation
- Bio224 TDDocument2 pagesBio224 TDTagne yvanPas encore d'évaluation
- Travail Pratique Chimie Des PolymèresDocument13 pagesTravail Pratique Chimie Des PolymèresEddouks Fatimazahrae100% (1)
- S1 TD2 Protides PDFDocument8 pagesS1 TD2 Protides PDFmartinmune67% (3)
- Enzymes Allostã - RiquesDocument29 pagesEnzymes Allostã - RiquesAmine DidoPas encore d'évaluation
- BiochimieDocument59 pagesBiochimieChristian Ngala100% (1)
- Compte Rendu Des Travaux Pratiques de BiochimieDocument4 pagesCompte Rendu Des Travaux Pratiques de BiochimieStefan Madalina100% (1)
- Acides AminésDocument14 pagesAcides AminésA100% (1)
- 03-Glycolyse 2021Document7 pages03-Glycolyse 2021Mery Sage100% (1)
- Manuel de TP Biochimie Structurale 2020 TP1Document8 pagesManuel de TP Biochimie Structurale 2020 TP1ZAKARIA HADDANEPas encore d'évaluation
- Expose Sur LDocument3 pagesExpose Sur LIwan WazniPas encore d'évaluation
- CytosqueletteDocument24 pagesCytosquelettefellah aminaPas encore d'évaluation
- Icp 2014.2015Document43 pagesIcp 2014.2015Khaoula Kouloughli100% (1)
- EndocrinotoxicitéDocument82 pagesEndocrinotoxicitéKhaoula Kouloughli100% (1)
- CancerogenèseDocument90 pagesCancerogenèseKhaoula Kouloughli80% (5)
- Traitement Des Intoxications KhaoulaDocument103 pagesTraitement Des Intoxications KhaoulaKhaoula Kouloughli100% (3)
- PneumotoxicitéDocument70 pagesPneumotoxicitéKhaoula Kouloughli88% (8)
- NeurotoxicitéDocument77 pagesNeurotoxicitéKhaoula Kouloughli100% (1)
- Toxicité Aigue KhaoulaDocument85 pagesToxicité Aigue KhaoulaKhaoula Kouloughli100% (10)
- Vibrations Série TD N°01 CorrigéDocument76 pagesVibrations Série TD N°01 CorrigétmyyounesPas encore d'évaluation
- Résistivité Des MétauxDocument7 pagesRésistivité Des MétauxAnes ArcPas encore d'évaluation
- Datations Chronologie Introduction Générale: Diop-MaesDocument26 pagesDatations Chronologie Introduction Générale: Diop-MaesJean RobertPas encore d'évaluation
- Cours Analyse Dim M1Document16 pagesCours Analyse Dim M1Bouzid BlhPas encore d'évaluation
- Rapport AZIZ FILALI Stage Ouvrier STEG 1Document24 pagesRapport AZIZ FILALI Stage Ouvrier STEG 1oussamakorbosliPas encore d'évaluation
- CHIMIEcoursn°2 ENT 15 15Document3 pagesCHIMIEcoursn°2 ENT 15 15Anonymous XoqNgbPas encore d'évaluation
- Mecanique Des Fluides-Ch1Document7 pagesMecanique Des Fluides-Ch1PFEPas encore d'évaluation
- Downloadfile 119Document2 pagesDownloadfile 119rayhanadouaab1Pas encore d'évaluation
- 2 MercureDocument4 pages2 MercureRayane NouiPas encore d'évaluation
- Chapitre IIIDocument5 pagesChapitre IIIMy SpacePas encore d'évaluation
- PosterJB TRAMECH-VII20132Document2 pagesPosterJB TRAMECH-VII20132fadma aboudraPas encore d'évaluation
- Under Balance DrillingDocument27 pagesUnder Balance DrillingMohamed Bourenane50% (2)
- Induction Electromagnetique-Chapitre 4-Circuit Fixe Dans Un Champ Magnetique VariableDocument29 pagesInduction Electromagnetique-Chapitre 4-Circuit Fixe Dans Un Champ Magnetique VariableKkoPas encore d'évaluation
- Devoir N°4 - Physique Chimie - 2nd L - SunudaaraDocument6 pagesDevoir N°4 - Physique Chimie - 2nd L - SunudaaraAhmadou Gueule SallPas encore d'évaluation
- Dosage GlucoseDocument2 pagesDosage GlucosesambaPas encore d'évaluation
- Web Etablissmt PsychroDocument6 pagesWeb Etablissmt PsychroAbde TamPas encore d'évaluation
- Les Atomes Et Les Ions Exercices Non Corriges 1Document2 pagesLes Atomes Et Les Ions Exercices Non Corriges 1Aymane ElPas encore d'évaluation
- Contributio A L'amelioration - AFOUKAL Fatima - 849Document28 pagesContributio A L'amelioration - AFOUKAL Fatima - 849Elkhalil OunarhiPas encore d'évaluation
- Chapitre 2: Mécanique de ContactDocument37 pagesChapitre 2: Mécanique de ContactmohammedPas encore d'évaluation
- Exposé de Caractérisation Des MatériauxDocument12 pagesExposé de Caractérisation Des Matériauxأحمد حمان100% (1)
- Homo 20T 5200Document301 pagesHomo 20T 5200Mohamed GhaziPas encore d'évaluation
- TD1 - Classification de Section Et Dimensionnement Des PoutresDocument4 pagesTD1 - Classification de Section Et Dimensionnement Des PoutresAmy FallPas encore d'évaluation
- Republique TunisienneDocument22 pagesRepublique Tunisiennebe betterPas encore d'évaluation
- Partie03 Quiz1055 Matériaux Q103Document21 pagesPartie03 Quiz1055 Matériaux Q103Brek SPas encore d'évaluation
- Chapitre 2 Les CristauxDocument3 pagesChapitre 2 Les CristauxNora LagouPas encore d'évaluation