Académique Documents
Professionnel Documents
Culture Documents
Equilibres Chimiques
Transféré par
Mounib BnCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Equilibres Chimiques
Transféré par
Mounib BnDroits d'auteur :
Formats disponibles
8) Les équilibres chimiques
I) Introduction
Lors d'une transformation chimique les réactifs réagissent pour donner des produits.
Certaines réactions sont totales et s'arrêtent à la disparition d'un des réactifs, d'autres sont
dites équilibrées.
Pour ces dernières une partie des produits réagissent entre eux pour redonner des réactifs.
Dans tous les cas la transformation chimique est modélisée par une équation de réaction,
dans laquelle les coefficients stoechiométriques donnent les proportions des différentes
espèces mises en jeu.
II) Activité et quotient de réaction
Soit l'équation suivante correspondant à une transformation équilibrée :
b B + c C d D+eE
Avec B et C les réactifs, D et E les produits (b, c, d, et e étant les coefficients
stœchiométriques).
Le quotient de réaction vaut alors :
Où a(B) représente l'activité chimique de l'espèce B.
Les activités prenant les valeurs qui suivent :
Soluté dans une Solide pur ou liquide Liquide dans un
Constituant Z Gaz parfait
solution diluée seul dans sa phase mélange homogène
Pression
Concentration
partielle Fraction molaire
Activité a(Z) effective 1
[ ]
Remarques :
L'activité est sans unité, tout comme le quotient de réaction.
L'activité du solvant est égale à 1.
III) Constante d'équilibre
La constante d'équilibre K est la valeur du quotient de réaction à l'équilibre. Cette valeur
ne dépend que de la température.
Si K > 104 la réaction est dite totale (très déplacée dans le sens direct)
Si 0 < K < 10-4 la réaction est quasi nulle.
Dans les autres cas elle est équilibrée.
Cours Chimie Analytique I
L2 Chimie Fondamentale
S. MANSOURI Université de BOUIRA
IV) Déplacement d'un équilibre : Principe de Le-Chatelier
La loi de modération nous explique que si on modifie un des facteurs d'équilibre,
l'équilibre se déplace de façon à modérer la modification.
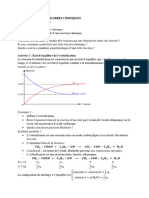
IV.1) Influence de la température
Si on élève la température, l'équilibre se déplacera de dans le sens qui consomme de
l'énergie thermique : le sens endothermique.
Si on diminue la température, l'équilibre se déplacera de dans le sens qui consomme de
l'énergie thermique : le sens exothermique.
IV.2) Influence de la concentration molaire
Si on ajoute du réactif, ou qu'on enlève du produit, la transformation évolue vers la droite.
On peut donc rendre la réaction totale en supprimant un des produits…
IV.3) Influence de la pression
Une augmentation de pression déplace l'équilibre dans le sens de diminution de la quantité
de matière de gaz.
Exemples :
2 C(s) + O2 (g) 2 CO (g)
Dans cette transformation la quantité de matière de gaz augmente. Si on augmente la
pression on déplace l'équilibre vers la gauche.
FeO (s) + CO (g) Fe (S) + CO2(g)
Dans ce cas il y a autant de gaz parmi les réactifs et parmi les produits, la pression n'est
pas un facteur d'équilibre.
Cours Chimie Analytique I
L2 Chimie Fondamentale
S. MANSOURI Université de BOUIRA
Vous aimerez peut-être aussi
- CHAPITRE 1 Partie 2Document14 pagesCHAPITRE 1 Partie 2hamid ibbakhPas encore d'évaluation
- Equilibres ChimiquesDocument14 pagesEquilibres ChimiquesCRYPTEXPas encore d'évaluation
- Les Equilibres ChimiquesDocument7 pagesLes Equilibres Chimiquesdembamamadou274Pas encore d'évaluation
- TP EquilibrechimiqueDocument8 pagesTP Equilibrechimiquecherazer67% (3)
- Chapitre 2Document4 pagesChapitre 2Moustapha Bassirou NianePas encore d'évaluation
- Document Sans TitreDocument6 pagesDocument Sans TitreMohamed MahdiPas encore d'évaluation
- 1 Cours DescriptionDunSystemeFermeEnTransformationChimiqueCours VFDocument2 pages1 Cours DescriptionDunSystemeFermeEnTransformationChimiqueCours VFMed RhaiouzPas encore d'évaluation
- Chapitre3 PDFDocument18 pagesChapitre3 PDFhakdzPas encore d'évaluation
- Chapitre 3 Equilibres Chimiques 3ème Génie Des ProcédésDocument23 pagesChapitre 3 Equilibres Chimiques 3ème Génie Des ProcédésCherif LaifaPas encore d'évaluation
- Anal 2Document13 pagesAnal 2Mrd ArlPas encore d'évaluation
- Chap It Re 3Document18 pagesChap It Re 3sidiahmedJSPas encore d'évaluation
- 06 Evolution Spontanee D Un Systeme ChimiqueDocument7 pages06 Evolution Spontanee D Un Systeme ChimiqueElec FoPas encore d'évaluation
- Chapitre 5A Complété Quotient de Réaction Et Constante d' ÉquilibreDocument3 pagesChapitre 5A Complété Quotient de Réaction Et Constante d' Équilibreairfann67Pas encore d'évaluation
- CR Equilibre ChimiqueDocument3 pagesCR Equilibre Chimiquemohamed mohPas encore d'évaluation
- Rappels Cinetique ChimiqueDocument22 pagesRappels Cinetique ChimiqueSaid Soilihi ZayadPas encore d'évaluation
- L'équilibre Chimique 2Document16 pagesL'équilibre Chimique 2medPas encore d'évaluation
- Evolution SpontaneeDocument4 pagesEvolution SpontaneeloujeynPas encore d'évaluation
- Solutions Et Expression de ConcentrationDocument11 pagesSolutions Et Expression de ConcentrationNicoleta ChivuPas encore d'évaluation
- ch2 - Transformation Chimique Dun Systã Me - complétéDocument24 pagesch2 - Transformation Chimique Dun Systã Me - complétéd.xw.wx3Pas encore d'évaluation
- 1 Equilibres ChimiquesDocument6 pages1 Equilibres ChimiquesMira MslPas encore d'évaluation
- I-1 Réactions Chimiques - Rappels - Hafid2021Document27 pagesI-1 Réactions Chimiques - Rappels - Hafid2021Raih NabilPas encore d'évaluation
- CH03 EquilibreChimique EleveDocument10 pagesCH03 EquilibreChimique EleveVictor B.Pas encore d'évaluation
- Cours Chim 06Document28 pagesCours Chim 06fsqiypiyiherafzferkPas encore d'évaluation
- Partie II Transformation de La Matière - MPSIDocument13 pagesPartie II Transformation de La Matière - MPSIGhreg BISSIEMOPas encore d'évaluation
- Reactivité Chimique - Chapitre 1Document44 pagesReactivité Chimique - Chapitre 1abraham LincolnPas encore d'évaluation
- Analyse 3Document19 pagesAnalyse 3ibrahimPas encore d'évaluation
- Réactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Document63 pagesRéactivité Chimique: S3 Mip, FST - Fès Année Universitaire 2020/2021Oumayma IkhlefPas encore d'évaluation
- Transformation ReactionDocument6 pagesTransformation ReactionhossamkamalPas encore d'évaluation
- BioE LST PlanchesDocument4 pagesBioE LST PlanchesSOUKAINA FEZZARIPas encore d'évaluation
- Résumé Équilibre ChimiqueDocument4 pagesRésumé Équilibre ChimiqueMehdi BnmssdPas encore d'évaluation
- Cours Chim 5Document2 pagesCours Chim 5abderrahimnPas encore d'évaluation
- Activité D'apprentissage Du Principe de Le Chatelier - Document D'étudeDocument5 pagesActivité D'apprentissage Du Principe de Le Chatelier - Document D'étudeRayan AllachePas encore d'évaluation
- Cours 13 Équilibres ChimiquesDocument4 pagesCours 13 Équilibres ChimiquesArti80% (5)
- CM CHI 201 - 2022 Royal Partie 1Document53 pagesCM CHI 201 - 2022 Royal Partie 1Vera Legba-MonyPas encore d'évaluation
- Cours Thermochimie 2021Document109 pagesCours Thermochimie 2021Hiba AmalouPas encore d'évaluation
- Equilibre Chimique, Word 1Document2 pagesEquilibre Chimique, Word 1Lourdes Gerges0% (1)
- 6.equilibre ChimiqueDocument3 pages6.equilibre ChimiqueDan GrigorePas encore d'évaluation
- Résolution Examen Blanc 2019-2020 - Question 1Document1 pageRésolution Examen Blanc 2019-2020 - Question 1arthursimon374Pas encore d'évaluation
- Equilibre ChimiqueDocument7 pagesEquilibre ChimiquecherazerPas encore d'évaluation
- Les Équilibres ChimiquesDocument3 pagesLes Équilibres ChimiquesabdderahmaneameurPas encore d'évaluation
- SN2-Chapitre 04 H2024Document40 pagesSN2-Chapitre 04 H2024alyssiamorrissette7Pas encore d'évaluation
- Chp. Transformation ChimiqueDocument5 pagesChp. Transformation ChimiqueyvancharlesmendoumeessengPas encore d'évaluation
- Chapitre 1 INTRO - 1Document12 pagesChapitre 1 INTRO - 1chaimaagherbi5Pas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Document2 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Resume de Cours 1Fatima Zahrae El BouhmidiPas encore d'évaluation
- CoursDocument7 pagesCoursMohammed TahriPas encore d'évaluation
- Chapitre1 Transformation ChimiqueDocument5 pagesChapitre1 Transformation ChimiqueElaattachi MohamedPas encore d'évaluation
- Extrait PDFDocument8 pagesExtrait PDFjelloPas encore d'évaluation
- CHM224 2022 2023Document102 pagesCHM224 2022 2023Franel YolandaPas encore d'évaluation
- Notions Fondamentales de La ThermodynamiqueDocument3 pagesNotions Fondamentales de La ThermodynamiqueWalid AzzamPas encore d'évaluation
- Cours - Physique Loi de Moderation Et Loi Daction de Masse - Bac Math (2013-2014) MR Afdal AliDocument3 pagesCours - Physique Loi de Moderation Et Loi Daction de Masse - Bac Math (2013-2014) MR Afdal AliceddmefPas encore d'évaluation
- Bilan Titrage Colorimetrique Et OxydoreductionDocument2 pagesBilan Titrage Colorimetrique Et Oxydoreductionbazoly.rambeloPas encore d'évaluation
- Fiche Sur Notion Déquilibre ChimiqueDocument3 pagesFiche Sur Notion Déquilibre ChimiquechadaPas encore d'évaluation
- Pvogel Fonctions React Org-1 Chapitre-1Document66 pagesPvogel Fonctions React Org-1 Chapitre-1Cisse MoustaphaPas encore d'évaluation
- GFTHKFDocument101 pagesGFTHKFFedoua BenamerPas encore d'évaluation
- Exercices L2 SPS 2023-2024 EquilibresDocument3 pagesExercices L2 SPS 2023-2024 Equilibresj29024688Pas encore d'évaluation
- TD1 Me ÜmoiresDocument3 pagesTD1 Me ÜmoiresalaeelhassanyPas encore d'évaluation
- Notice de Sécurité IncendieDocument114 pagesNotice de Sécurité IncendieYasser MeftouhPas encore d'évaluation
- Parkside PKS2000-4 (Tronçonneuse)Document20 pagesParkside PKS2000-4 (Tronçonneuse)Georges KouroussisPas encore d'évaluation
- La très petite entreprise (TPE) en AfriqueDocument8 pagesLa très petite entreprise (TPE) en Afriquetheodoreahoton1Pas encore d'évaluation
- 201 Coute - NR 4 2023Document68 pages201 Coute - NR 4 2023luPas encore d'évaluation
- 5analyse TypomorphologiqueDocument10 pages5analyse Typomorphologiqueyasmine bouheloufPas encore d'évaluation
- Techniques D Obfuscation de Code Chiffrer Du Clair Avec Du ClairDocument20 pagesTechniques D Obfuscation de Code Chiffrer Du Clair Avec Du ClairMouhamed Rassoul GueyePas encore d'évaluation
- Techniques D'elevage Intensif Et D'alimentation de Poissons Et de CrustacesDocument19 pagesTechniques D'elevage Intensif Et D'alimentation de Poissons Et de CrustacesDao SouleymanePas encore d'évaluation
- Expose Equipements de Production Tarek SenigraDocument5 pagesExpose Equipements de Production Tarek Senigratarek senigraPas encore d'évaluation
- Projet 02. Séq 02. BOUSEKKINE Anfel 2Document25 pagesProjet 02. Séq 02. BOUSEKKINE Anfel 2Renda ReziguiPas encore d'évaluation
- Sicareme Assurances: Certificat D'Assurances Etudes + Stages POLICE #470.2020.00000049Document1 pageSicareme Assurances: Certificat D'Assurances Etudes + Stages POLICE #470.2020.00000049Aladine MardyPas encore d'évaluation
- MR 258 Super5 4 5 9Document259 pagesMR 258 Super5 4 5 9Van Aster EricPas encore d'évaluation
- 0709 ArduinoDocument6 pages0709 Arduinohamza ayechePas encore d'évaluation
- La Grammaire Des Premiers Temps V1 Reponses Corriges PDFDocument32 pagesLa Grammaire Des Premiers Temps V1 Reponses Corriges PDFadastraperalasporci100% (2)
- Facture Freemobile 20231230Document2 pagesFacture Freemobile 20231230ashwineuPas encore d'évaluation
- Rituel CBCS Pour Chevaliers Et EcuyersDocument94 pagesRituel CBCS Pour Chevaliers Et EcuyerskimonthPas encore d'évaluation
- Corrigé UE11 - DCG 2011Document17 pagesCorrigé UE11 - DCG 2011Med Reda BouasriaPas encore d'évaluation
- 7.3.3 - Herminette - Rapport FinalDocument44 pages7.3.3 - Herminette - Rapport FinalMajdouline SeddikiPas encore d'évaluation
- Liste Des Variétés de PoiresDocument3 pagesListe Des Variétés de Poiresmohamedadjeb2001Pas encore d'évaluation
- Cours n2Document4 pagesCours n2Sophie BarrierePas encore d'évaluation
- Exposé SVT Les Minerais A MadagascarDocument7 pagesExposé SVT Les Minerais A MadagascarJohan RaharisonPas encore d'évaluation
- Economie IndustrielleDocument4 pagesEconomie IndustrielleLatifa HadekPas encore d'évaluation
- Microscope Électronique À BalayageDocument29 pagesMicroscope Électronique À BalayageS0UM0HPas encore d'évaluation
- Inf302 TDDocument34 pagesInf302 TDRio LoboPas encore d'évaluation
- Les 7 Étapes À Franchir Afin D'être Utile Et Profitable Pour Dieu - Le Blog ParolevivanteDocument12 pagesLes 7 Étapes À Franchir Afin D'être Utile Et Profitable Pour Dieu - Le Blog ParolevivanteEmmanu’EL “1CORTH2:5” MikamonaPas encore d'évaluation
- Matrice Multi CritèresDocument57 pagesMatrice Multi CritèresOthmane AouinatouPas encore d'évaluation
- Justificatif LienDocument1 pageJustificatif Lienimmavillena0Pas encore d'évaluation
- Voie LactéeDocument34 pagesVoie Lactéejulian perezPas encore d'évaluation
- Heyman - Measurement of The Influence of Lateral Earth PressureDocument5 pagesHeyman - Measurement of The Influence of Lateral Earth PressureMarcelaMarquesPas encore d'évaluation
- Blondel - La Religion. Le Problème de La MystiqueDocument40 pagesBlondel - La Religion. Le Problème de La MystiquemolinerPas encore d'évaluation
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Revue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteD'EverandRevue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteÉvaluation : 3 sur 5 étoiles3/5 (3)
- Harmonisation Energétique des Personnes: Manuel de Curothérapie 2020D'EverandHarmonisation Energétique des Personnes: Manuel de Curothérapie 2020Évaluation : 4 sur 5 étoiles4/5 (8)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Guide De Démarrage De L'Apiculture: Le Guide Complet Pour Élever Des AbeillesD'EverandGuide De Démarrage De L'Apiculture: Le Guide Complet Pour Élever Des AbeillesPas encore d'évaluation
- Affirmations positives : Perte de poids pour les femmesD'EverandAffirmations positives : Perte de poids pour les femmesPas encore d'évaluation
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Vous saurez tout sur le permis: Un livre rassurant pour les maudits du volantD'EverandVous saurez tout sur le permis: Un livre rassurant pour les maudits du volantPas encore d'évaluation
- Production et propagation des sons: Les Grands Articles d'UniversalisD'EverandProduction et propagation des sons: Les Grands Articles d'UniversalisPas encore d'évaluation
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- L'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaD'EverandL'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaÉvaluation : 3 sur 5 étoiles3/5 (1)
- Anatomie & 100 étirements essentiels pour le running: Principes de base, Techniques, Tableaux de séries, Précautions à prendre, Conseils, Programmes d'étirementsD'EverandAnatomie & 100 étirements essentiels pour le running: Principes de base, Techniques, Tableaux de séries, Précautions à prendre, Conseils, Programmes d'étirementsPas encore d'évaluation
- Cosmologie Égyptienne, L’Univers Animé, Troisième ÉditionD'EverandCosmologie Égyptienne, L’Univers Animé, Troisième ÉditionPas encore d'évaluation
- Physique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresD'EverandPhysique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresÉvaluation : 5 sur 5 étoiles5/5 (2)
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Mes inventions (Traduit): Autobiographie de Nikola TeslaD'EverandMes inventions (Traduit): Autobiographie de Nikola TeslaÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Bioénergie et Sciences Occultes: Pour un corps sain et un esprit sain dans un lieu sainD'EverandBioénergie et Sciences Occultes: Pour un corps sain et un esprit sain dans un lieu sainÉvaluation : 4 sur 5 étoiles4/5 (2)
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)