Académique Documents
Professionnel Documents
Culture Documents
Physio Endocrino
Transféré par
Eric Charles HadjiTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Physio Endocrino
Transféré par
Eric Charles HadjiDroits d'auteur :
Formats disponibles
Physiologie de l’appareil urinaire LS3 – LS4
PHYSIOLOGIE DU SYSTEME ENDOCRINIEN
I- INTRODUCTION
Dans l’organisme, il existe 2 systèmes qui assurent la coordination et l’harmonisation des
fonctions de tous les organes qui sont ainsi subordonnés aux besoins de l’individu ou de l’espèce
animale. Il s’agit :
- du système nerveux qui est adapté aux régulations immédiates et dont les commandes
sont rapides et proviennent des influx qui cheminent dans les nerfs.
- du système endocrinien ou hormonal qui est adapté aux régulations lentes et durables.
Ce système nécessite la synthèse d’hormones qui constituent les médiateurs chimiques
de l’influx. Les hormones sont secrétées par des glandes endocrines.
Une glande endocrine est un organe interne qui sécrète des hormones dans la circulation
sanguine qui les mène vers des organes ou des cellules cibles distants, où elles exercent des
fonctions spécifiques.
Les glandes endocrines sont réparties dans l'organisme, au sein duquel elles forment un réseau
appelé système endocrinien.
Les épithéliums glandulaires endocrines peuvent être sous forme:
de glandes endocrines bien individualisées (ex: thyroïde, hypophyse; testicules, ovaires.)
d'amas de cellules endocrines (ex: îlots de Langherans du pancréas, cellules de Leydig au
sein des testicules)
dispersée, diffuse, au sein d'autres organes (ex: cellules endocrines du tube digestif).
Les glandes endocrines pures sont la thyroïde, les parathyroïdes, les surrénales, l'hypophyse, le
corps pinéal, et beaucoup d'autres.
Certaines sont mixtes, associant une partie exocrine, comme le pancréas ou les gonades
(testicules et ovaires).
Enfin, la plupart des organes (cœur, graisse, rein, etc.) ont une fonction endocrine.
Pendant la grossesse, le placenta joue également le rôle d'une glande endocrine ; il devient le
principal producteur d'hormones stéroïdes.
L’hormone synthétisée agit à faible dose et à distance sur un organe cible qui est l’effecteur soit
de façon spécifique sur un type d’effecteurs, soit de façon non spécifique sur plusieurs types
d’effecteurs. L’organe qui sécrète l’hormone est dit hormonogène.
Docteur Simon-Pierre ASSANE FSS 1
Physiologie de l’appareil urinaire LS3 – LS4
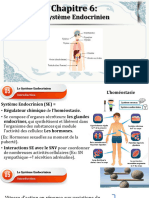
1- Glande pinéale (épiphyse)
2- Glande pituitaire (hypophyse)
3- Glande thyroïde
4- Thymus
5- Glande surrénale
6- Pancréas
7- Ovaire
8- Testicule
Le système endocrinien
II- GENERALITES SUR LES HORMONES
On appelle hormone, toute substance chimique biologiquement active, sécrétée par une
glande endocrine et qui, déversée dans le sang, agit à distance en exerçant une action
physiologique au niveau de divers organes sur des récepteurs spécifiques.
Les hormones agissent en tant que messagers chimiques, régulant de nombreuses
fonctions de l'organisme telles que la croissance, le développement, la reproduction, le
métabolisme, la pression artérielle, la glycémie et l'équilibre des fluides.
Le terme « hormone » (du grec ὁρμάω, mettre en mouvement) a été adopté par Starling en 1905
pour désigner les substances qui assurent la liaison entre les divers organes.
Docteur Simon-Pierre ASSANE FSS 2
Physiologie de l’appareil urinaire LS3 – LS4
A- BIOSYNTHESE ET SECRETION
Les organes hormonogènes contiennent un matériel appelé préhormonal à partir duquel
des hormones sont synthétisées et déversées dans le sang.
La sécrétion hormonale comporte donc 2 phases :
- une phase de biosynthèse où l’hormone est élaborée. C’est un phénomène continu.
- une phase de libération, phase sécrétoire proprement dite qui est une phase discontinue et
qui est contrôlée par les besoins.
Matériel pré hormonal
Enzymes PHASE DE BIOSYNTHESE
HORMONE
(Stock)
PHASE DE LIBERATION
SANG
BIOSYNTHESE ET SECRETION DES HORMONES
La sécrétion endocrine présente 3 critères qui sont:
- Histologiques : les différentes sécrétions sont orientées par rapport aux vaisseaux et non par
rapport aux canaux excréteurs.
- Physiologiques : l’ablation de la glande provoque des troubles qui sont corrigés par apport
d’extraits ou greffe de la glande ; le sang efférent glandulaire possède des propriétés spécifiques
dont on juge par son influence quand il est transfusé chez un animal témoin ou « essayé » sur des
organes isolés.
Docteur Simon-Pierre ASSANE FSS 3
Physiologie de l’appareil urinaire LS3 – LS4
- Chimiques : parmi des produits isolés dans la glande, on découvre ceux possédant le pouvoir de
suppléer aux effets de l’ablation de la glande.
La connaissance de la biogenèse des différentes hormones, permet de préciser leur origine et les
étapes successives de leur formation.
B – TRANSPORT HORMONAL
Ce transport se fait par l’intermédiaire de protéines plasmatiques appelées protéines
vectrices. Celles-ci présentent 3 caractéristiques :
- Affinité : force avec laquelle l’hormone se lie à la protéine
- Spécificité : aptitude particulière qu’a une protéine de se lier à une hormone donnée.
La spécificité est liée à l’affinité.
- Capacité : nombre d’hormones que peut transporter une protéine vectrice.
Par conséquent, un transporteur qui a une grande capacité possède une faible spécificité et une
faible affinité.
L’hormone liée à la protéine est inactive et représente la forme de stockage et de transport. Il
existe un équilibre entre la forme liée et la forme libre de l’hormone.
C- SPECIFICITE ET CLASSIFICATION DES HORMONES
1) Spécificité
On distingue 3 spécificités pour une hormone :
- Spécificité d’origine qui indique l’origine de l’hormone.
Ex : hormone thyroïdienne.
- spécificité de transport qui détermine la nature de l’hormone transportée.
Ex: SBG (Sex Binding globulin)
- spécificité d’action qui détermine le type d’effecteur Ex : FSH- ovaire
2) Classification
Les hormones sont classées soit selon leur origine, soit selon leur structure chimique :
Docteur Simon-Pierre ASSANE FSS 4
Physiologie de l’appareil urinaire LS3 – LS4
Selon l’origine, on a :
- les hormones hypothalamiques (RF / R H)
- les hormones antéhypophysaires. (les stimulines)
- les hormones post-hypophysaires (les neurohormones)
- les hormones surrénaliennes (Corticosurrénale : corticoïdes ; Médullosurrénale :
catécholamines)
- les hormones thyroïdiennes (T3 / T4)
- les hormones parathyroïdiennes (métabolisme phosphocalcique)
- les hormones pancréatiques (contrôle de la glycémie)
- les hormones gastro- intestinales
- les hormones gonadiques
Selon la structure chimique
On distingue 4 grands groupes :
- les hormones polypeptidiques
Leur taille dépend du nombre d’acides aminés qui les constitue. On cite parmi ces hormones : La
parathormone, les kinines, l’insuline, les hormones gastro-intestinales, STH (hormone de
croissance), la thyréostimuline, le thyroglobuline.
- Les hormones stéroïdes : Ces hormones dérivent du cholestérol ou de ses précurseurs (les
acétates). Elles comprennent les glucocorticoïdes (cortisol) ; les minéralocorticoïdes
(aldostérone) et les hormones gonadiques (œstrogènes, testostérone).
- les hormones dérivées d’amines : elles proviennent de la transformation chimique d’acides
aminés. Il s’agit de l’hormone thyroïdienne et des catécholamines qui dérivent de la tyrosine
(Exemple : catécholamines, thyroxine).
- Les hormones à base de lipides et de phospholipides sont dérivées de lipides comme l'acide
linoléique et de phospholipides comme l'acide arachidonique. Les eïcosanoïdes sont la classe
principale, parmi lesquels les plus étudiés sont les prostaglandines.
Docteur Simon-Pierre ASSANE FSS 5
Physiologie de l’appareil urinaire LS3 – LS4
D- MECANISME D’ACTION DES HORMONES
Les hormones, une fois, libérées circulent dans le sang en partie dissoute dans le plasma,
en partie, fixées aux protéines porteuses (vectrices ou binding protein). Au niveau des organes
cibles, les hormones agissent selon 2 mécanismes.
1- Action membranaire
Dans ce mécanisme, l’hormone ne pénètre pas l’intérieur de la cellule.
Les hormones polypeptidiques agissent par ce mécanisme. Les récepteurs de ces hormones
peptidiques mais aussi ceux des facteurs de croissance, des cytokines, et des neurotransmetteurs
sont membranaires et la stimulation initiale des cellules cibles s'effectue donc à ce niveau. . Elles
activent des enzymes au niveau de la membrane, l’Adenyl cyclase et la phospholipase C :
- L’Adénylcyclase catalyse la biosynthèse d’AMP cyclique dont la dégradation est assurée
par des nucléotides phosphodiestérases. L’AMPc intervient ensuite comme 2e messager.
- La phospholipase C catalyse la biosynthèse de deux seconds messagers, le diacylglycérol
et l’inositol triphosphate qui à son tour provoque la sortie d’ions calcium vers le
cytoplasme à partir du réticulum endoplasmique.
Les seconds messagers stimulent ensuite des protéine-kinases spécifiques: la PKA pour
l’AMPc et la PKC pour le diacylglycérol en collaboration avec le calcium cytosolique libéré par
l’inositol triphosphate. Les protéines kinases phosphorylent ensuite divers substrats spécifiques
(enzymes, facteurs de transcription, protéines du cytosquelette etc.) ; ce qui entraîne une
modification de leurs activités et/ou de leurs structures et, en conséquence, produit des réponses
cellulaires à l’hormone considérée.
2- Action intracellulaire
C’est le mode d’action des hormones stéroïdes. Ici il y a pénétration intracytoplasmique
de l’hormone, contact avec l’ADN et élaboration d’ARNm et d’une autre enzyme.
Que ce soit par le mécanisme membranaire ou intracellulaire, l’action de l’hormone s’effectue
selon une chronologie.
Docteur Simon-Pierre ASSANE FSS 6
Physiologie de l’appareil urinaire LS3 – LS4
E- CONTROLE DE LA SECRETION HORMONALE
La mise en jeu des mécanismes régulateurs est réglée par le trouble même à compenser et
freinée par l’excès d’hormone en circulation. C’est donc un système à autorégulation par
rétrocontrôle (feedback).
Il y a 2 types de glandes endocrines selon le mécanisme de contrôle de la régulation :
- les glandes non hypophyso-dépendantes dont la sécrétion ne dépend pas des stimulations
hypophysaires mais de leur propre métabolisme. On décrit essentiellement 2 glandes :
- la glande parathyroïde qui sécrète la parathormone.
- le pancréas endocrine qui sécrète l’insuline et le glucagon.
- les glandes hypophyso-dépendantes dont la sécrétion est sous le contrôle de l’axe hypothalamo-
hypophysaire.
La régulation de la sécrétion de ces glandes hypophyso-dépendantes est assurée par le
mécanisme de rétrocontrôle ou feed-back qui est commandé par le complexe hypothalamo-
hypophysaire.
Dans ce mécanisme, c’est le taux d’hormone dans le sang qui règle sa propre sécrétion.
Il y a un détecteur de toute diminution du taux de l’hormone et un réacteur ramène le taux de
l’hormone à la valeur normale.
Le rétrocontrôle est dit « positif » si il induit une augmentation de sécrétion de l'hormone, et
« négatif » s'il induit une diminution de la sécrétion hormonale.
Exemple : la GnRH contrôle la libération de FSH et LH. (Elle agit donc sur leurs propres cycles
de rétrocontrôle pour influer sur leurs concentrations). FSH et LH jouent un rôle majeur dans la
libération d'hormones sexuelles dans le sang. C'est en fonction de cette concentration en
hormones sexuelles qu'est libérée la GnRH.
Docteur Simon-Pierre ASSANE FSS 7
Physiologie de l’appareil urinaire LS3 – LS4
Glande endocrine
Précurseur hormonal
HORMONE (stock)
SANG
Forme liée Forme libre
Forme libre
ORGANE CIBLE (effet hormonal)
Dégradation
METABOLITES
ELIMINATION / EXCRETION (selles ; urines)
Docteur Simon-Pierre ASSANE FSS 8
Physiologie de l’appareil urinaire LS3 – LS4
CHRONOLOGIE DE L’ACTION DES HORMONES
HYPOTHALAMUS
RH / RF RC COURT
+/-
HYPOPHYSE
STIMULINES
RC LONG
+/-
GLANDES ENDOCRINES
HORMONES
(Sang)
ORGANE CIBLE
SCHEMA DE LA REGULATION DE LA SECRETION DES GLANDES
HYPOPHYSO-DEPENDANTES
RC = Retrocontrôle RH = Realising Hormons RF = Realising Factors
Docteur Simon-Pierre ASSANE FSS 9
Physiologie de l’appareil urinaire LS3 – LS4
APERCU SUR LES DIFFERENTES GLANDES
I - LE COMPLEXE HYPOTALAMO – HYPOPHYSAIRE
L'hypophyse ou glande pituitaire (hypophysis, glandula pituitaria) est une glande
endocrine qui se trouve dans une petite cavité osseuse à la base du cerveau, la selle turcique
(sella turcica). Elle est reliée à une autre partie du cerveau appelée l'hypothalamus.
L'hypophyse se divise en deux lobes : l'antéhypophyse (adénohypophyse) en avant et la post-
hypophyse (neurohypophyse) en arrière. L'adénohypophyse dérive du plafond de la cavité
buccale primitive (stomodeum) tandis que la post-hypophyse est une extension de l'hypothalamus
et contient les axones de neurones dont les corps cellulaires se trouvent dans l'hypothalamus.
L'hypothalamus est relié à l'hypophyse par la tige pituitaire. La jonction hypothalamus/anté-
hypohyse est réalisée par voie sanguine tandis que la post-hypophyse est réellement reliée par la
tige pituitaire constituée par les axones des neurones hypothalamiques.
L’hypophyse produit des hormones qui gèrent une large gamme de fonctions corporelles, dont
les hormones trophiques qui stimulent les autres glandes endocrines.
1 - L’appareil hypothalamo-post hypophysaire
La post-hypophyse ou neurohypophyse est en fait une projection de l'hypothalamus. Elle
ne produit pas ses propres hormones ; elle ne fait qu'entreposer et distribuer les hormones
ocytocine et vasopressine sous forme de neurosécrétions (neurohormones).
La post hypophyse joue donc un rôle de stockage et de sécrétion.
Les 2 hormones post hypophysaires ont une parenté biochimique, d’où découle une parenté
d’action. En effet, l’ocytocine possède 2% d’effet ADH-like et l’ADH possède 10 % d’effet
ocytocique.
- L’ocytocine est sécrétée en grande partie par les noyaux paraventriculaires de l’hypothalamus et
en petite quantité par les noyaux supra optiques. Cette hormone a des effets excitants sur la
Docteur Simon-Pierre ASSANE FSS 10
Physiologie de l’appareil urinaire LS3 – LS4
contraction utérine et intervient dans l’expulsion du foetus lors de l’accouchement. Elle a
également un effet lactogène sur la glande mammaire pendant l’allaitement.
- La vasopressine est secrétée en grande partie par les noyaux supra optiques et en petite quantité
par les noyaux paraventriculaires. Elle intervient au niveau du rein ou elle règle en partie la
réabsorption tubulaire de l’eau, participant ainsi au maintien de l’équilibre hydro-minéral et de la
pression osmotique.
2 – L’appareil hypothalamo-anté hypophysaire
L'antéhypophyse contient de nombreux types cellulaires différents qui sécrètent chacun
une ou plusieurs des hormones suivantes :
l'hormone de croissance (GH) (stimulant spécifique de la croissance viscérale et
squelettique),
la prolactine (stimule la sécrétion du lait),
l'hormone folliculo-stimulante (FSH)
l'hormone lutéinisante (LH),
la thyréostimuline (TSH),
l'hormone adrénocorticotrope (ACTH),
la mélanostimuline (MSH),
les endorphines,
et d'autres hormones.
Ce sont des stimulines. Celles-ci constituent les agents de commande et d’entretien des
activités thyroïdiennes, cortico-surrénaliennes, ovariennes et testiculaires ; et enfin la glande
mammaire (qui est une glande exocrine). Par ces stimulines, l’activité hypophysaire peut
retentir sur presque toutes les glandes endocrines.
En cas de défaut de production on parle d'hypopituitarisme (insuffisance
antéhypophysaire). Il peut s'agir d'un déficit d'une ou plusieurs hormones (insuffisance
somatotrope isolée chez l'enfant par exemple, se traduisant par un retard de croissance).
Docteur Simon-Pierre ASSANE FSS 11
Physiologie de l’appareil urinaire LS3 – LS4
L'hypersécrétion est due le plus souvent à un adénome. Les adénomes sont par ordre de
fréquence :
- adénome lactotrope (sécrétion de prolactine d'où hyperprolactinémie)
- adénome somatotrope (sécrétion de GH d'où acromégalie)
- adénome gonadotrope ou non secrétant (synthèse de LH et FSH, pas toujours libérée dans
le sang)
- adénome corticotrope (sécrétion d'ACTH d'où syndrome de Cushing)
- adénome thyréotrope (très rare, hyperthyroïdie par excès de TSH).
Il existe des adénomes mixtes : somatotrope et lactotrope surtout, mais d'autres
associations sont possibles.
Docteur Simon-Pierre ASSANE FSS 12
Physiologie de l’appareil urinaire LS3 – LS4
II – LA GLANDE THYROIDE
La thyroïde ou glande thyroïde est la plus volumineuse des glandes endocrines (sécrétant
des hormones). Elle sécrète en effet :
la T3 ou triiodothyronine
la T4 ou thyroxine
la thyrocalcitonine intervenant dans le métabolisme du calcium.
La production de ces hormones thyroïdiennes est régie par la thyréostimuline (TSH, thyroid-
stimulating hormon), produite par l'antéhypophyse.
II-1 MORPHOLOGIE
Située à la face antérieure du cou, elle est superficielle : ses déformations sont visibles
sous la peau (on parle de goitre quand le volume de la thyroïde est augmenté). La thyroïde se
compose de deux lobes droit et gauche reliés à leur partie inférieure par l'isthme thyroïdien,
lequel se projette au niveau des 2ème, 3ème et 4ème anneaux trachéaux . Elle présente deux types de
rapports :
Les nerfs laryngés récurrents qui passent en arrière et se terminent dans le larynx.
Les quatre glandes parathyroïdes : petites glandes situées à la face postérieure de la
thyroïde et jouant un rôle dans le métabolisme phosphocalcique.
Les deux lobes ont un sommet supérieur ainsi qu'une grande base inférieure. On leur décrit 3
faces : médiale, postérieure et antéro-latérale. Sa hauteur est d'environ 6 cm pour une longueur de
6 à 8 cm. On trouve souvent entre les deux lobes, donc au niveau de l'isthme, le lobe pyramidal
de Lalouette, souvent déporté vers la gauche : c'est un reliquat du canal thyréoglosse.
La thyroïde, moulée sur l'axe trachéo-laryngé, est de consistance ferme, de couleur rosée, et pèse
30 grammes (légèrement plus chez les femmes) mais en cas de goitre son poids peut augmenter
jusqu'à 100 -150 grammes. Elle est entourée d'une capsule qui lui est propre et qui est différente
de la loge thyroïdienne.
Docteur Simon-Pierre ASSANE FSS 13
Physiologie de l’appareil urinaire LS3 – LS4
Il existe des variations morphologiques, s'expliquant par l'embryologie : en effet les deux lobes
sont parfois éloignés l'un de l'autre sans qu'il n'y ait d'isthme, ou au contraire peuvent être soudés
donnant une thyroïde en forme de V.
II-2 VASCULARISATION
La thyroïde est un organe richement vascularisé. En effet on retrouve :
Deux artères principales :
artère thyroïdienne supérieure (ATS), première branche de l'artère carotide externe ;
elle se divise en 3 branches une fois la glande atteinte.
artère thyroïdienne inférieure (ATI), naissant du tronc thyro-cervical, branche
collatérale de l'artère subclavière. Elle se divise également en trois branches dans la
thyroïde.
Il existe néanmoins d'autres artères, moins volumineuses, inconstantes, naissant directement de
l'arc aortique. Par exemple l'artère thyroïda ima vascularisant la partie isthmique.
Trois veines principales :
veine thyroïdienne supérieure (VTS), résultant de la confluence de 3 veines dans la
glande, et formant avec les veines linguale et faciale, le tronc thyro-lingo-facial qui se
jette dans la veine jugulaire interne.
veine thyroïdienne moyenne (VTM), réunion de plusieurs branches pas très
volumineuses se jetant dans la veine jugulaire interne.
veine thyroïdienne inférieure (VTI), formée par la confluence de 3 veines dans la
glande et se jetant dans le tronc veineux brachio-céphalique.
De même que pour les artères, certaines veines plus accessoires vascularisant préférentiellement
l'isthme, vont rejoindre les troncs veineux brachio-céphaliques droit et gauche.
II-3 LES HORMONES THYROIDIENNES
Les hormones thyroïdiennes, la thyroxine (T4) et la triiodothyronine (T3), sont des
hormones à base de tyrosine, produites par la glande thyroïde. Elles agissent sur le corps pour
Docteur Simon-Pierre ASSANE FSS 14
Physiologie de l’appareil urinaire LS3 – LS4
augmenter le métabolisme basal, agir sur la synthèse des protéines et rendre le corps plus sensible
aux catécholamines comme l'adrénaline.
L'iode est un important composant dans leur synthèse et la fonction endocrine de la thyroïde
dépend de l’apport exogène d’iode ; celle-ci peut être perturbée en cas de carence d’apport ou en
cas d’apport excessif.
Dans le sang, la principale représentante des hormones thyroïdiennes est la thyroxine (T4). Celle-
ci est convertie en T3 active dans les cellules par des déiodinases.
La plupart des hormones thyroïdiennes circulant dans le sang sont liées à des protéines de
transport :
la TBG (thyroid binding globulin)
la TBPA (Thyroid binding prealbumin) (cette protéine est également responsable du
transport du rétinol, et on préfère maintenant l'appeler transthyrétine (TTR))
l'albumine
Seule une très petite fraction de l'hormone circulante est libre (non liée) - T4 (0,03 %) et T3
(0,3%). Cette fraction libre est biologiquement active, et dès lors mesurer les concentrations
d'hormones thyroïdiennes libres a une grande importance diagnostique. Ces valeurs sont référées
en tant que fT4 et fT3. Un autre outil de diagnostic critique est le taux de TSH (thyroid-
stimulating hormone).
Les hormones thyroïdiennes liées sont inactives ; ce qui compte, c'est le taux de T3/T4 libre.
C'est pourquoi la mesure de la thyroxine totale du sang peut amener à des conclusions erronées.
La thyroïde présente des particularités par rapport aux autres glandes endocrines :
- Chez l’enfant : elle est indispensable au développement du fœtus dans la vie intra-utérine,
au développement du nouveau-né et de l’enfant. Elle assure surtout le développement du
cerveau et la croissance osseuse.
- Chez l’adulte, la principale activité des hormones thyroïdiennes s’exerce sur les
métabolismes intermédiaires et la thermogenèse dans tous les tissus.
- C’est la seule glande qui stocke en quantités considérables les hormones sous formes liées
aux grosses protéines.
- La synthèse d’hormones thyroïdiennes dépend de l’apport d’iode alimentaire.
Docteur Simon-Pierre ASSANE FSS 15
Physiologie de l’appareil urinaire LS3 – LS4
II-4 STRUCTURE ET PRODUCTION DES HORMONES THYROÏDIENNES
La thyroïde est très vascularisée. Les cellules de la thyroïde sont organisées en follicules
autour d'une vésicule appelée colloïde. Ces cellules sont orientées, c'est à dire qu'elles possèdent
un pôle apical du côté de la colloïde et un pôle basal du côté des vaisseaux sanguins. La
membrane apicale est séparée de la membrane baso-latérale par des jonctions serrées. Le noyau
des cellules folliculaires est relativement actif, la présence de Réticulum Endoplasmique
Granuleux démontre une forte activité protéique et l'appareil de golgi est lui-même très actif car
on peut observer de nombreuses vésicules au pôle apical.
Ces cellules permettent l'échange de molécules du sang vers la colloïde et inversement.
- Le sang fournit les acides aminés nécessaires à la synthèse d'une protéine appelée
thyroglobuline (dans le REG des cellules folliculaires). Celle-ci passe ensuite dans l'appareil de
golgi et est internalisée dans les vésicules. Ces vésicules fusionnent avec la membrane apicale
des cellules folliculaires et la thyroglobuline est sécrétée dans la colloïde.
- La thyroglobuline subit une iodation dans la colloïde. L'iode est apporté par une source
alimentaire, transporté dans le sang et capté par les cellules folliculaires (le transport actif contre
le gradient de concentration explique la présence de nombreuses mitochondries au pôle basal des
cellules de la thyroïde). Le gradient chimique permet le passage passif de l'iode dans la colloïde
où des peroxydases transforment l'ion iodure (I -) en diiode (I2).
- Les acides aminés tyrosines de la thyroglobuline subissent ensuite une iodation. On peut
obtenir une monoiodothyroglobuline (une seule tyrosine iodée) ou une diiodothyroglobuline
(deux tyrosines iodées).
- Les groupements phénols de ces molécules peuvent ensuite se condenser. Si deux
diiodothyroglobulines s'associent, on a formation de T4 ou thyroxine. Si il y a condensation entre
une monoiodothyroglobuline et une diiodothyroglobuline, on obtient de la T3. La T4 est
synthétisée en plus grande quantité que la T3. Ces deux hormones sont stockées dans la colloïde
jusqu'à ce qu'il y ait stimulation de la thyroïde par une hormone hypophysaire appelée TSH (ou
thyréostimuline).
La membrane apicale des cellules folliculaires s'invagine et endocyte des fragments de colloïde.
Les hormones T3 et T4 sont alors sécrétées dans le sang. Les autres constituants de la colloïde
Docteur Simon-Pierre ASSANE FSS 16
Physiologie de l’appareil urinaire LS3 – LS4
(ions iodures, thyroglobuline...) sont recyclés ou dégradés dans les lysosomes des cellules de la
thyroïde.
La calcitonine est une hormone hypocalcémiante qui participe au métabolisme du calcium et du
phosphore . Spécifiquement, elle réduit la calcémie de trois manières :
Principalement, elle active les ostéoblastes, ce qui augmente le stockage du calcium dans
les os
Elle diminue l'absorption du calcium par le duodénum en diminuant l'activité de la
vitamine D
Elle augmente l'excrétion du calcium par les reins.
La majeure partie de la calcitonine du corps humain est produite dans les Cellules C (cellules
parafolliculaires) de la glande thyroïde.
La calcitonine est utilisée dans le traitement de l'ostéoporose postménopausale.
II-5 EFFETS PHYSIOLOGIQUES DES HORMONES THYROIDIENNES
1- Sur la consommation d’oxygène : les hormones thyroïdiennes augmentent la
consommation de l’oxygène et la calorigénèse, assurant ainsi la thermorégulation.
2- Sur les différents métabolismes :
- Elles élèvent le métabolisme basal
- Protides : - favorisent la synthèse des acides nucléiques
- à dose physiologique, elles sont anabolisantes
- à dose supra physiologique, elles entraînent un catabolisme exagéré avec bilan
azoté négatif. C’est ce qui explique l’amaigrissement dans les hyperthyroïdies
et l’élévation des protéines plasmatiques dans les hypothyroïdies.
- Lipides : accélération du catabolisme des graisses (lipolyse)
- Glucides : action hyperglycémiante
- Hydro électrolytique : effet diurétique ; calciurie.
3 – Sur les différentes fonctions de l’organisme
- Sur l’appareil cardio-vasculaire : le cœur est énormément sensible à l’action des
hormones thyroïdiennes. L’hyperthyroïdie entraîne une tachycardie sinusale ; à l’inverse,
l’hypothyroïdie provoque une bradycardie.
- Sur le système nerveux central : elles ont une action excitatrice sur le psychisme.
Docteur Simon-Pierre ASSANE FSS 17
Physiologie de l’appareil urinaire LS3 – LS4
- Sur le tube digestif : elles stimulent la motricité intestinale.
Les troubles de fonctionnement sont de 2 ordres :
- hyperfonctionnement : maladie de BASEDOW, adénome toxique, goitre
multinodulaire
- hypofonctionnement : hypothyroïdies (myxoedème).
III – LES SURRENALES
Les glandes surrénales ou plus simplement les surrénales sont deux glandes endocrines
triangulaires situées au-dessus des reins. Elles sont principalement responsables de la gestion des
situations de stress via la synthèse de corticostéroïdes (cortisol) et de catécholamines
(adrénaline).
La glande est divisée en deux structures distinctes :
la moelle ou médullo-surrénale
le cortex ou cortico-surrénale
Ces structures sont toutes deux connectées en permanence au système nerveux. Comme le nom
l'indique, la médullo-surrénale est située à l'intérieur de la surrénale, alors que la cortico-
surrénale en recouvre la surface.
Le cortex est issu de tissu mésodermique (épithélium cœlomique), alors que la médulla vient de
cellules de la crête neurale. Les deux parties se rencontrent après 7 semaines. La médulla
s’invagine progressivement dans le cortex. La zone fasciculée est formée après 20 semaines. La
zone glomérulée est formée à la naissance. La zone réticulée n’apparaît vraiment que chez
l’adulte.
Docteur Simon-Pierre ASSANE FSS 18
Physiologie de l’appareil urinaire LS3 – LS4
1 – Les corticosurrénales
Elles constituent la partie externe, corticale, et résistante de chacune des 2 glandes. Elles
sont indispensables pour le maintien de la vie. La corticosurrénale présente à décrire 3 zones
histologiques :
La zone glomérulaire ou glomérulée
C’est la partie la plus externe située la capsule externe. Cette zone glomérulée synthétise
principalement des minéralocorticoïdes, à savoir l'aldostérone qui intervient dans le métabolisme
hydro-minéral (réabsorption du Na+ au niveau des tubules rénaux). Elle représente 15% de la
corticosurrénale. Ces cordons s'organisent en réseaux arrondis, en glomérules.
Les manifestations de l’excès d’aldostérone constituent le syndrome de CONN
(hyperaldostéronisme primaire).
La zone fasciculaire ou fasciculée
Elle représente la partie moyenne, la plus volumineuse (65 % de la corticosurrénale). La
zone fasciculée synthétise des glucocorticoïdes, à savoir Cortisol et Corticostérone.
Le cortisol contrôle la production du glucose par le foie et réduit l’utilisation périphérique du
glucose. C'est une hormone lipophile.
Elle agit en se liant au complexe récepteur-protéine HSP. Cette protéine chaperonne est détruite
par la liaison, et le complexe peut migrer vers une séquence particulière de l'ADN appelée HRE
(Élément de Réponse à l'Hormone), ce qui va permettre au cortisol d'exercer son action de
transcription des gènes cibles.
Le cortisol active dans le foie les enzymes de la néoglucogénèse et facilite le stockage du
glycogène.
Au niveau du tissu adipeux, il va inhiber l'entrée de glucose et activer la lipolyse.
Il favorise la production de glucose à partir de substrats non glucidiques, des acides aminés et de
l'oxydation des acides gras via la formation de corps cétoniques, pour maintenir une glycémie
constante.
Docteur Simon-Pierre ASSANE FSS 19
Physiologie de l’appareil urinaire LS3 – LS4
Il diminue la synthèse des protéines et augmente la protéolyse au niveau musculaire. Le cortisol
augmente les dépôts graisseux.
Les glucocorticoïdes présentent 3 types d’effets par leur rôle physiologique :
- Effets sur le métabolisme général
- Effets anti-inflammatoires et immunosuppressifs
- Effets spécifiques sur les différents tissus.
Les perturbations du fonctionnement de la fasciculée entraînent des manifestations pathologiques
liées :
- soit à l’excès : syndrome de CUSHING
- soit à la carence : maladie d’ADDISON
Docteur Simon-Pierre ASSANE FSS 20
Physiologie de l’appareil urinaire LS3 – LS4
La zone réticulaire ou réticulée
C’est la zone la plus interne, au contact de la médullosurrénale. Elle représente 10% de la
corticosurrénale. Ses cordons s'organisent en réseaux anastomosés (branchés). Elle synthétise les
stéroïdes sexuels dont le précurseur commun est le Cholestérol. Du cholestérol aux hormones
actives, la biosynthèse passe par l’intermédiaire de plusieurs réactions enzymatiques et au cours
desquelles l’ACTH est indispensable.
La 1ère étape transforme le cholestérol en D-5-Pregnenolone qui est le principal précurseur de
toutes les hormones stéroïdes. A partir du Pregnenolone sont synthétisées les 3 catégories de
stéroïdes :
- Les stéroïdes à 21 atomes de carbone dérivant du noyau Pregnane. Ils sont appelés
corticostéroïdes car, ils ne sont synthétisés que par la corticosurrénale. Il s’agit de :
Progestérone, Aldostérone, et Cortisol.
Docteur Simon-Pierre ASSANE FSS 21
Physiologie de l’appareil urinaire LS3 – LS4
- Les stéroïdes à 19 atomes de carbone dérivant du noyau Androstane : ce sont les
Androgènes (Testostérone, androgènes surrénaliens).
- Les stéroïdes à 18 atomes de carbone qui dérivent du noyau Oestrane ; Ce sont les
Oestrogènes (Oestradiol).
Les stéroïdes à 19 C et à 18 C sont aussi synthétisés par les gonades (C19 : testicules ; C18 :
ovaires).
2 – Les médullo-surrénales
La médullo-surrénale est la principale source corporelle d'hormones du groupe des
catécholamines. Il s’agit de l’Adrénaline (ou Epinéphrine) et de la Noradrénaline (ou
Norépinéphrine). A côté de ces 2 hormones, il y a un dérivé synthétique qui est la Dopamine.
L’Adrénaline est toujours une hormone sécrétée par la médullo-surrénale ; la Noradrénaline et la
Dopamine sont soit hormones soit médiateurs chimiques libérés par les terminaisons nerveuses
du système nerveux sympathique. La matière première des catécholamines est la tyrosine qui
elle-même provient de l’oxydation de la phénylalanine au niveau du foie selon la réaction
suivante :
Docteur Simon-Pierre ASSANE FSS 22
Physiologie de l’appareil urinaire LS3 – LS4
Tyrosine hydroxylase
Dopadécarboxylase
(Acide ascorbique)
DA Hydroxylase
Tyrosine oxydase
Transméthylase
Phe Tyr DOPA Dopamine NorAdr ADR
(DihydroxyPhe ) CO2
Sur le plan physiologique, l’action des catécholamines est identique à celle du système nerveux
sympathique par l’intermédiaire des récepteurs α et β.
La médullo-surrénale a pour rôle d’adapter l’organisme aux agressions. Elle provoque une
distribution de la masse sanguine et globulaire qu’elle dévie vers les muscles, le cerveau et les
artères coronaires en cas de nécessité. Elle corrige le débit cardiaque et la ventilation, réajuste le
taux de glucose circulant et met l’organisme dans les conditions favorables pour faire face à un
événement dangereux ou inhabituel qui exige de l’organisme une véritable mobilisation.
Docteur Simon-Pierre ASSANE FSS 23
Physiologie de l’appareil urinaire LS3 – LS4
IV – LE PANCREAS
Le pancréas est un organe abdominal péritonéal (mais considéré comme rétro péritonéal
en chirurgie) situé derrière l'estomac, devant et au-dessus des reins. Il a des fonctions endocrines
et exocrines et il est relié au duodénum par le canal de Wirsung.
Le pancréas, étymologiquement "tout en viande" (pan : tout ; kréas : viande), fut décrit pour la
première fois par Herophilus, un anatomiste et chirurgien grec. Il fut nommé quelques centaines
d'années plus tard par un autre anatomiste grec, Ruphos.
Le pancréas est la deuxième glande la plus grosse en volume après le foie. Le pancréas a deux
fonctions, exocrine et endocrine. C’est une glande mixte ou amphicrine.
La fonction exocrine du pancréas est la sécrétion des enzymes pancréatiques dans le
duodénum, par le canal de Wirsung. Le suc pancréatique contient des proenzymes
biosynthétisées par les cellules acineuses. Ces proenzymes sont inactives: elles seront activées
dans l'estomac pour détruire des plus ou moins grosses molécules, elles seront alors appelées
hydrolases. Les sécrétions pancréatiques ont un pH compris entre 7,5 et 8,2. Le suc pancréatique
est donc alcalin ce qui permet de tamponner le chyme stomacal.
Sa fonction endocrine est de produire le glucagon et l'insuline, deux hormones nécessaires à
la régulation du glucose. Le glucagon et l'insuline sont produits par les îlots de Langerhans ; le
glucagon est produit par les cellules α et l'insuline par les cellules β des îlots de Langerhans. Les
Docteur Simon-Pierre ASSANE FSS 24
Physiologie de l’appareil urinaire LS3 – LS4
cellules δ secrètent la somatostatine qui a un effet inhibiteur sur la sécrétion d'insuline et de
glucagon.
En termes simples, le glucagon accélère la glycogénolyse . L'insuline, elle, fait l'effet contraire,
car elle favorise la glycogénogenèse.
1- Régulation de la sécrétion et effets des hormones pancréatiques
1-1 Insuline
a- Régulation
Le glucose est le principal facteur de régulation de la sécrétion d’insuline. En effet, à dose
physiologique, le glucose est capable de stimuler la biosynthèse et la sécrétion de l’insuline.
L’insuline est sécrétée selon 2 modes :
- en continu: maintien d’un niveau constant tout au long de la journée, environ 1 UI/h (soit 20%
de la sécrétion quotidienne). C’est la sécrétion basale.
- en mode réponse à un stimulus glycémique.
La réponse sécrétoire de l’insuline à la stimulation par le glucose est caractéristique :
A partir d’une sécrétion de base, le taux d’insuline s’élève au bout de 30 secondes à 1 minute
lorsque la glycémie monte au-dessus de 800 mg/l. Ce taux atteint un 1er pic au bout de 5 à 10
minutes, décroche puis remonte ensuite pour culminer au bout de 30 minutes.
La phase aiguë ou précoce correspond à la libération de l’insuline stockée prête à être libérée
(pool d’insuline immédiatement mobilisable (granules au contact de la membrane)) ; la phase
prolongée ou tardive correspond à la libération des autres granules stockées mais aussi de
l’insuline nouvellement synthétisée.
L’insuline secrétée est transportée dans le sang par le Peptide C. elle est captée et détruite par le
foie.
Au niveau de la membrane cellulaire, l’insuline se fixe sur un récepteur glycoprotéique fait de :
- 2 sous-unités α "extra membranaire, site spécifique de reconnaissance
- et de 2 sous unités β transmembranaires douées d’une activité tyrosine kinase pour la
transmission du message. L’activation enzymatique par la tyrosine kinase détermine
l’action spécifique de l’hormone dans la cellule.
Docteur Simon-Pierre ASSANE FSS 25
Physiologie de l’appareil urinaire LS3 – LS4
Réponse sécrétoire de l’insuline à la stimulation par le glucose
Phase aiguë Phase prolongée
Docteur Simon-Pierre ASSANE FSS 26
Physiologie de l’appareil urinaire LS3 – LS4
b- Effets physiologiques
L’insuline produit les effets physiologiques suivant :
- sur le foie :
- Stimule la glycogénogénèse (stockage en glycogène), foie étant un organe de
réserve du glucose. Après un repas, l’excédent de glucose est mis en réserve dans
les cellules hépatiques. La capacité de stockage du foie est limitée à 100 g.
- Inhibe la néoglucogenèse: inhibe les enzymes et diminue les substrats
- stimule la lipogenèse hépatique
- action anabolique sur les protéines
- Sur le muscle :
- l’insuline augmente l’utilisation du glucose.
- stimule la glycogénèse et la glycolyse.
- inhibe la protéolyse et la lipolyse.
- vue l’absence du G6P au niveau musculaire, la glycogénolyse aboutit non pas au
glucose mais à l’acide pyruvique en aérobiose et à l’acide lactique en anaérobiose.
- Le stockage du glucose musculaire est limité à 400 g
- Sur le tissu adipeux :
- éponge l’excès de glucose (l’excès de glucose est convertie en graisses ; ceci
explique que les régimes hyperglycémiques induisent une prise depoids pouvant
mener à l’obésité)
- stimule la lipogenèse (c’est la seule hormone anti-lipolytique de l’organisme)
- diminue la glycogénolyse et la protéolyse.
- favorise la mise en réserve des substrats énergétiques
- Autres effets :
- Augmentation de la perméabilité membranaire aux K+, Mg2+
- Activation de la pompe Na/K avec entrée massive de K+ à l’intérieur des cellules
(risque d’hypokaliémie sous insuline, traitement des hyperkaliémies)
- stimule la réabsorption tubulaire de Na+ (risque d’hypernatrémie)
- contrôle les gènes codant pour les facteurs de croissance
Docteur Simon-Pierre ASSANE FSS 27
Physiologie de l’appareil urinaire LS3 – LS4
c- Facteurs de sécrétion
- Facteurs métaboliques : glucides (glucose), acides aminés (arginine, leucine, lysine),
corps cétoniques, acides gras
- Facteurs pharmacologiques : Sulfamides hypoglycémiants
- Facteurs hormonaux :
- Hormones pancréatiques: le glucagon stimule la sécrétion d’insuline par effets
directs sur les cellules β, la somatostatine inhibe la sécrétion d’insuline
- l’élévation de l’ACTH, corticostéroïdes, œstrogène, progestérone et parathormone
(effet anti-insuline)
- la GH stimule aussi la sécrétion basale d’insuline
- facteurs nerveux :
- SN sympathique: effet α adrénergique: inhibe la sécrétion, effet β adrénergique:
stimule la sécrétion de l’insuline
- SN parasympathique : Acétylcholine stimule la sécrétion d’insuline
- L’activité physique est un puissant facteur hypoglycémiant, elle améliore la sensibilité
tissulaire à l’insuline d’où son indication dans le traitement du diabète.
1-2 Glucagon
Le glucagon est une hormone hyperglycémiante. En synergie avec les catécholamines, elle
permet de mobiliser le glucose dans un temps très court.
L’hypoglycémie est plus grave que l’hyperglycémie parce qu’elle provoque des effets surtout
neurologiques avec des séquelles parfois irréversibles.
Une molécule de glucagon peut forcer la libération 10 millions de glucose. Le cortisol, les
hormones thyroïdiennes et l’hormone de croissance sont des hormones hyperglycémiantes mais à
action progressive.
C’est un polypeptide secrété par les cellules α pancréatiques. Il est synthétisé sous forme d’un
préproglucagon (180 AA) qui est clivé en proglucagon (37 AA), puis en glucagon (29 AA) qui
est stocké dans l'appareil de Golgi avec formation de granules de stockage. La sécrétion se fait
par exocytose.
Le glucagon se fixe sur son récepteur qui change alors de conformation pour interagir avec une
protéine Gs. La sous-unité αs de cette protéine se détache pour aller activer une adénylate
cyclase. Celle-ci hydrolyse alors l'ATP en AMP cyclique. L’AMPc constitue le messager
Docteur Simon-Pierre ASSANE FSS 28
Physiologie de l’appareil urinaire LS3 – LS4
secondaire, il se fixe sur la Protéine Kinase A. La PKA peut alors initier une réponse rapide ou
une réponse lente :
- Réponse rapide :
- hydrolyse le glycogène en glucose utilisable par l’organisme (glycogénolyse).
- Inactive et empêche de polymériser le glucose en glycogène (inhibition de la
glycogénèse).
- Réponse lente : stimulation de la néoglucogenèse qui permettra à l’organisme de produire du
glucose à partir de composés non glucidiques.
Il est dégradé dans le foie surtout mais également dans le rein et le plasma. Il n'est pas retrouvé
dans les urines.
a- Régulation de la sécrétion
- Effets des substrats :
- Le glucose : la diminution (glycémie< 0.5 g/l) stimule la sécrétion de glucagon, alors
que l'élévation de la glycémie (> 1.6 g/l) l’inhibe.
- les acides aminés stimulent la sécrétion de glucagon.
- les acides gras libres : l'ingestion des lipides augmente la sécrétion de glucagon.
- Effets du système nerveux
- le système parasympathique : l'acétylcholine et la stimulation du nerf vague augmentent
la sécrétion de glucagon
- la noradrénaline par son effet α inhibe le glucagon, alors qu’elle la stimule par l’effet β.
- Effets des hormones:
- l'insuline et la somatostatine inhibent la libération de glucagon.
- le cortisol, la cholécystokinine et la sécrétine stimulent la libération de glucagon.
b- Effets physiologiques
- Sur le foie : la cible principale du glucagon est le foie. C’est le seul organe qui peut libérer
le glucose en cas d’hypoglycémie. La libération du glucose hépatique permet le maintien
de la glycémie entre les repas (glycogénolyse et néoglucogenèse), permettant de maintenir
la glycémie en cas de jeûne prolongé ou en situation d’exercice musculaire intense.
Docteur Simon-Pierre ASSANE FSS 29
Physiologie de l’appareil urinaire LS3 – LS4
- Sur le métabolisme lipidique : il stimule la lipase hormono-sensible, responsable d'une
hydrolyse des triglycérides en glycérol et en acides gras (effet lipolytique) ; les acides gras
permettront de fournir du glucose par néoglucogénèse aux cellules souffrant
d’hypoglycémie. Le glucagon induit aussi la cétogenèse.
2 – Régulation de la glycémie
Une glycémie stable est l’une des constantes du milieu intérieur. La constance de la glycémie est
assurée par un équilibre entre les apports des glucides et leur utilisation par les tissus. Elle résulte
de l’équilibre entre la formation du glucose et sa disparition par son utilisation ou son
élimination.
La régulation de la glycémie met en jeu le système hormonal, ainsi que plusieurs organes (foie et
pancréas principalement). Cette régulation fait partie des processus de maintien de l'homéostasie
au sein de l'organisme.
La glycémie normale est comprise entre 3,9 et 5,8 mmol/L (soit 0,7 et 1,10 g/l).
Le glucose joue un rôle capital dans l'organisme: il est la source d'énergie principale servant au
fonctionnement des muscles et organes du corps humain, notamment du cerveau. La régulation
de la glycémie est donc extrêmement contrôlée.
En temps normal, elle fait intervenir l'insuline, le glucagon, et l'adrénaline en période de stress.
Ces hormones sont des messagers primaires qui se fixent sur leurs récepteurs membranaires et
activent, par l'intermédiaire de l'AMP cyclique, le messager secondaire (sauf pour l'insuline) des
enzymes.
1-1 Rôle du pancréas
En plus du suc pancréatique servant à la digestion, le pancréas produit une hormone
hyperglycémiante (glucagon) et une hormone hypoglycémiante (insuline) dont les actions et
effets seront détaillés ci-après.
Le pancréas est composé de 4 types de cellules :
- Cellules alpha (α): «15 à 20 %» des cellules d’un îlot ; elles secrètent le glucagon qui est
une hormone hyperglycémiante.
Docteur Simon-Pierre ASSANE FSS 30
Physiologie de l’appareil urinaire LS3 – LS4
- Cellules Beta (β): majorité des cellules d’un ilot (70%) ; responsables de la synthèse et de
la sécrétion de l’insuline qui est une hormone hypoglycémiante. La cellule β fonctionne
comme un véritable détecteur métabolique des variations de la glycémie.
- Cellules Delta (δ): représentent seulement 5 %. elles produisent la somatostatine. Cette
hormone est inhibitrice des secrétions endocrines (glucagon, insuline et l’hormone de
croissance) et exocrines (sécrétine, la cholécystokinine, du suc pancréatique).
- Cellules PP: 1 % des cellules de l’ilot. Elles sont stimulées par les repas, l’exercice
physique et le nerf vague. Elles secrètent le polypeptide pancréatique qui a des
effets inhibiteurs de la sécrétion exocrine pancréatique, de la contraction vésiculaire et de
la motilité gastro-intestinale.
Une ablation partielle du pancréas (pancréatectomie partielle) n'a aucun effet sur le taux de
glucose sanguin. Toutefois, deux de ses systèmes sont vitaux: les individus qui en sont
dépourvus ne sont pas viables.
L’un de ces systèmes est constitué par l’ensemble : cellules β (bêta) des îlots de
Langerhans du pancréas, insuline, système de transport du glucose dans les cellules cibles.
L’autre est un système qui détecte la baisse des réserves de nutriments et/ou de leur
concentration sanguine. Il déclenche la sensation de faim et le comportement de recherche
puis de prise d’aliments. Le système responsable de la sensation de satiété et de l’arrêt de
la prise d’aliments est également un système de régulation de la glycémie.
D’autres systèmes sont en cours d’étude : les capteurs digestifs ou peut-être portaux (dans la
veine porte) et les incrétines qui potentialisent la sécrétion d’insuline.
Docteur Simon-Pierre ASSANE FSS 31
Physiologie de l’appareil urinaire LS3 – LS4
L'insuline et le glucagon sont clairement antagonistes quant à leur fonction hypo et
hyperglycémiante. Les cellules α et ß sont des capteurs sensibles à la glycémie du sang qui
perfuse le foie. On notera aussi que, même si elle n'est pas représentée, la commande nerveuse
existe aussi bien pour les cellules α que ß. Globalement la stimulation du système
parasympathique active la libération de glucagon et inhibe la sécrétion d'insuline alors que celle
du sympathique a un effet antagoniste.
Docteur Simon-Pierre ASSANE FSS 32
Physiologie de l’appareil urinaire LS3 – LS4
1-2 Rôle des autres organes
Rôle du foie
Le rôle du foie dans la régulation de la glycémie a été mis en évidence par l'expérience
dite "du foie lavé" par Claude Bernard en 1855.
Par le biais de la circulation sanguine, et plus précisément de la veine porte hépatique, le foie
reçoit le glucose issu de l'alimentation. Son rôle est de retenir le glucose excédentaire après un
apport important (repas copieux), et de le libérer lors des périodes de jeûne afin que la glycémie
reste constante et égale à sa valeur normale (environ 0,9 g/L).
Pour ce faire, le foie régule la production et le stockage du glucose grâce à 3 voies métaboliques:
La glycogénogenèse, qui correspond au stockage du glucose dans le foie sous forme de
glycogène.
La glycogénolyse, qui est la libération du glucose, sous forme de glucose-1-phosphate, par
phosphorolyse du glycogène.
La néoglucogenèse, c'est-à-dire la production de glucose par le foie, à partir d'acide
lactique ou d'acides aminés, déclenchée par une baisse de la glycémie en dessous de sa
valeur normale.
Le foie est un organe vital, car sans celui-ci une hypoglycémie est rapidement mortelle.
Rôle du rein
Le glucose étant un élément important, il n'est, en temps normal, pas présent dans les
urines. On dit que la glycosurie est nulle. Il est réabsorbé dans la circulation sanguine lors de la
filtration du sang par le rein, au niveau du tubule proximal. Pourtant, si la teneur en glucose du
sang arrivant dans le rein dépasse les capacités de réabsorption (9 mmol/l environ), il y aura
glycosurie. Cet état pathologique révèle un problème de régulation en amont, et peut être le signe
d'un diabète.
Le rein contribue donc, dans une moindre mesure, au maintien de la glycémie.
Docteur Simon-Pierre ASSANE FSS 33
Physiologie de l’appareil urinaire LS3 – LS4
Rôle du système nerveux
La régulation par le foie et le pancréas ne nécessite pas une intervention du système
nerveux. Mais, du fait de son action sur la sécrétion de l’insuline, le SNA agit sur la régulation de
la glycémie :
- SN sympathique: effet α adrénergique: inhibe la sécrétion, effet β adrénergique:
stimule la sécrétion de l’insuline
- SN parasympathique : Acétylcholine stimule la sécrétion d’insuline
1–3 Action d’autres hormones
Selon qu'elles soient hyperglycémiantes ou hypoglycémiantes, les hormones mises en jeu
n'agissent pas de la même manière.
Action de l'adrénaline
Issue de la médullo-surrénale, la production d’adrénaline augmente lors d'un stress, ou d'un
effort.
En agissant sur la glycogénolyse, elle provoque une hausse de la glycémie et permet un apport
rapide en glucose aux muscles lors d'un effort.
Les cellules cibles de l'adrénaline sont les hépatocytes et les cellules musculaires.
Les cellules cibles du glucagon sont les hépatocytes et les adipocytes.
Le glucagon et l'adrénaline, en se fixant sur leurs récepteurs, activent l'adényl cyclase qui
catalyse la synthèse d'AMP cyclique, le messager secondaire.
Celui-ci active une protéine kinase qui catalyse la phosphorylation de :
La phosphorylase kinase (active quand elle est phosphorylée), responsable de la
phosphorylation de la phosphorylase. Cette dernière, active quand elle est phosphorylée,
catalyse l'hydrolyse du glycogène en glucose.
La glycogène synthétase, inactive quand elle est phosphorylée, incapable de catalyser la
polymérisation du glucose en glycogène.
Docteur Simon-Pierre ASSANE FSS 34
Physiologie de l’appareil urinaire LS3 – LS4
Ces deux phénomènes entraînent une consommation du glycogène (en favorisant la
glycogénolyse et en inhibant la glycogénogenèse) au niveau du foie.
Il se produit donc une libération de glucose dans le sang: le glucagon et l'adrénaline sont donc
des hormones hyperglycémiantes.
Action du cortisol
Le cortisol est une hormone stéroïde hyperglycémiante, qui agit en cas de jeûne prolongé
(lors de la néoglucogenèse).
C'est une hormone lipophile, synthétisée dans la couche fasciculée de la cortico-surrénale.
Elle agit en se liant au complexe récepteur-protéine HSP. Cette protéine chaperonne est détruite
par la liaison, et le complexe peut migrer vers une séquence particulière de l'ADN appelée HRE
(Élément de Réponse à l'Hormone), ce qui va permettre au cortisol d'exercer son action de
transcription des gènes cibles.
Le cortisol active dans le foie les enzymes de la néoglucogénèse et facilite le stockage du
glycogène. Au niveau du tissu adipeux, il va inhiber l'entrée de glucose et activer la lipolyse.
Il favorise la production de glucose à partir de substrats non glucidiques, des acides aminés et de
l'oxydation des acides gras via la formation de corps cétoniques, pour maintenir une glycémie
constante.
3 – Explorations de la fonction endocrine du pancréas
a- Explorations fonctionnelles statiques
- La glycémie à jeûn : normale (0.8 – 1.10 g/l) (gycémie veineuse ou capillaire)
- Index glycémique : C’est le pouvoir hyperglycémiant des aliments glucidiques
dans les 2 heures suivant la prise d’aliments ; par rapport à un sucre de référence
(glucose), il est calculé pour 50 de glucides apportés par l’aliment. L’index
glycémique est variable selon la nature chimique des glucides de l’aliment, la
texture de l’aliment, la présence de fibres, et le degré de cuisson de l’aliment.
- Dans les urines : glycosurie (apparaît si glycémie ≥ 1.80 g/l)
Docteur Simon-Pierre ASSANE FSS 35
Physiologie de l’appareil urinaire LS3 – LS4
b- Explorations fonctionnelles dynamiques
- Glycémie post prandiale : une glycémie à jeun et une glycémie 2 h après l’ingestion d’un
repas riche en glucide. Cet examen renseigne sur l’adaptation de l’organisme à l’apport
glucidique dans les conditions physiologiques. Chez le sujet normal, la glycémie post
prandiale ne doit pas dépasser 1.40g/l.
- Hyperglycémie provoquée par voie orale : HGPO
- indication: si la glycémie à jeun comprise entre 1.10 et 1.26 g/l ou si la glycémie
post prandiale est entre 1.40 - 2 g/l.
- Condition: Un premier prélèvement de sang à t0 ; le sujet doit ingérer dans 5 mn ;
75 g de glucose dissout dans 250 ml d’eau (chez l’enfant la dose recommandée est
de 1.75g/kg -Chez la femme enceinte elle est de 100 g). Les glycémies sont dosées
toutes les 30 minutes, et la glycosurie est recherchée après 1 H et 2 H
- Résultats : Normalement la glycémie augmente et atteint son maximum entre 30 et
60 mn, cette variation doit être inférieure à 0.5 g/l ; le retour à la normale
s’effectue à t 2 H puis survient une hypoglycémie liée à l’insuline.
- Si glycémie ≤ 1.40g/l : sujet normal
- Si glycémie ≥ 2 g/l : sujet diabétique
- Si glycémie située entre 1.40 et 1.99g : intolérance aux hydrates de carbone
- Hyperglycémie provoquée par voie veineuse : HGPV
- On donne 0.33 g/kg du glucose par voie IV (0.66 ml de SGI 5%) puis on fait des
prélèvements toutes les 10 minutes pendant 1 heure chez l’adulte (enfant toutes les
4 mn pendant 30 minutes)
- Résultats : la glycémie augmente jusqu’à 2.50 g/l puis diminue. Cette épreuve
permet de déterminer un coefficient K qui traduit la captation cellulaire du glucose.
- Si K bas, sujet diabétique ; si K élevé, hyperinsulinisme.
- Tests de surveillance de l’équilibre glycémique : Hb1c =hémoglobine glyquée
- Bon marqueur de l’équilibre glycémique à moyen terme (6 à 8 semaines) ; donc il vérifie
l’équilibre glycémique et l’efficacité thérapeutique.
- Valeur normale : 4 à 6% ; si ≤ 7% = diabète équilibré, mais si ≥ 10 %, diabète mal
équilibré
Docteur Simon-Pierre ASSANE FSS 36
Vous aimerez peut-être aussi
- La Rédaction Du Certificat Médical de Décès-2023Document66 pagesLa Rédaction Du Certificat Médical de Décès-2023Ali AIT-MOHANDPas encore d'évaluation
- Protocole Hopital Universitaire Justinien 1Document63 pagesProtocole Hopital Universitaire Justinien 1Peguy GeffrardPas encore d'évaluation
- Le Système EndocrinienDocument23 pagesLe Système Endocrinienchadi ouechtatiPas encore d'évaluation
- 1-Generalites en Endocrinologie PDFDocument21 pages1-Generalites en Endocrinologie PDFthierno amadou bahPas encore d'évaluation
- 1-Physiologie Endocrinienne Generalites en EndocrinologieDocument102 pages1-Physiologie Endocrinienne Generalites en EndocrinologieAfdal BiosicaPas encore d'évaluation
- 1-Generalites en EndocrinoDocument21 pages1-Generalites en EndocrinobasassynenedianePas encore d'évaluation
- EndocrinologieDocument43 pagesEndocrinologiePierre MonharoulPas encore d'évaluation
- Chapitre1 Physiologie AnimaleDocument8 pagesChapitre1 Physiologie AnimaleMounir MarhlifiPas encore d'évaluation
- Physio Endocrino23-01glandes EndocrinesDocument4 pagesPhysio Endocrino23-01glandes EndocrinesVictorin FANDREBOPas encore d'évaluation
- Chap Iv Systeme EndocrinienDocument56 pagesChap Iv Systeme Endocrinienbaazizitopo mohamedPas encore d'évaluation
- 01-Principes Des Systemes de Controle HormonalDocument2 pages01-Principes Des Systemes de Controle HormonalLem AhPas encore d'évaluation
- Physiologie Endocrinienne Et Métabolique.G2UEA2020Document187 pagesPhysiologie Endocrinienne Et Métabolique.G2UEA2020Mercy MwemeraPas encore d'évaluation
- Anatomie Du Système EndocrinienDocument44 pagesAnatomie Du Système EndocrinienvinickPas encore d'évaluation
- Système EndocrinienDocument22 pagesSystème EndocrinienngoufacktsougmoPas encore d'évaluation
- Cours N°1d'endocrinologie S4 2020Document32 pagesCours N°1d'endocrinologie S4 2020Younes Masoud100% (1)
- Principes Des Systemes de Controle HormonalDocument2 pagesPrincipes Des Systemes de Controle Hormonalfafoufa133Pas encore d'évaluation
- UE8 TC Physio Cours 2 - Régulation Endocrinienne Tutorat 2013-2014Document10 pagesUE8 TC Physio Cours 2 - Régulation Endocrinienne Tutorat 2013-2014Ali EL Kihel100% (1)
- MNE CM3bis Physiologie Axe Hypothalamo HypophysaireDocument13 pagesMNE CM3bis Physiologie Axe Hypothalamo HypophysaireSoheib RahrahPas encore d'évaluation
- Cours - 3 Les Régulation Hormonale de La MétabolismeDocument9 pagesCours - 3 Les Régulation Hormonale de La Métabolismemiss anthropocenePas encore d'évaluation
- Notions D'endocrinoDocument119 pagesNotions D'endocrinoyaya camaraPas encore d'évaluation
- Les Neurohormones Chez HommeDocument17 pagesLes Neurohormones Chez HommeNisrine 2112Pas encore d'évaluation
- P Fonctions Du Système Endocrinien - (L. Bayer) - 23.04.21Document8 pagesP Fonctions Du Système Endocrinien - (L. Bayer) - 23.04.21nasten16fhPas encore d'évaluation
- Endocrinologie 23 1 2022Document53 pagesEndocrinologie 23 1 2022DA4OUR ytPas encore d'évaluation
- 1.système EndocrinienDocument31 pages1.système EndocrinienSid ahmed Zerrouki sbaPas encore d'évaluation
- BIO5067 GuideDocument119 pagesBIO5067 GuideHikari KazuePas encore d'évaluation
- Endocrinologie s6 Dahbi.-1Document9 pagesEndocrinologie s6 Dahbi.-1Zineb DahmaniPas encore d'évaluation
- 2014 7 Le Systeme EndocrinienDocument15 pages2014 7 Le Systeme EndocrinienSamira MBasskarPas encore d'évaluation
- Poly S1 PCEM2 2020Document113 pagesPoly S1 PCEM2 2020pvfbszf9mtPas encore d'évaluation
- Système Endocrinien DR BouraimaDocument34 pagesSystème Endocrinien DR Bouraimaaba djibaPas encore d'évaluation
- Cours IFCS 1° Année 2011Document39 pagesCours IFCS 1° Année 2011Fatim-Zahra DrissiPas encore d'évaluation
- Exposé EndocrinoDocument7 pagesExposé EndocrinociliaPas encore d'évaluation
- Fichier Produit 2218Document5 pagesFichier Produit 2218Alycia SafaPas encore d'évaluation
- 4 Système HormonalDocument18 pages4 Système HormonalbilynadoPas encore d'évaluation
- WP6 Del28.31-SS La-Communication-Hormonale ItalyDocument18 pagesWP6 Del28.31-SS La-Communication-Hormonale Italyone asslanPas encore d'évaluation
- Cours Endocrinologie de La ReproductionDocument49 pagesCours Endocrinologie de La ReproductionLukusa MauricePas encore d'évaluation
- Cours Dendocrinologie 2021-2022 - Partie 1Document32 pagesCours Dendocrinologie 2021-2022 - Partie 1carineyenkeyPas encore d'évaluation
- Le Système Endocrinien-1Document2 pagesLe Système Endocrinien-1Saîda SalahPas encore d'évaluation
- Universite Saad Dahleb Faculte de Medecine 2 Annee Medecine Cours de BiochimieDocument9 pagesUniversite Saad Dahleb Faculte de Medecine 2 Annee Medecine Cours de BiochimieDîãmønd QùeenPas encore d'évaluation
- 7 Le Systeme EndocrineDocument9 pages7 Le Systeme EndocrineRym YakhlifiPas encore d'évaluation
- SE Cours 3OSDocument22 pagesSE Cours 3OSLara FarquharsonPas encore d'évaluation
- Principes Des Systèmes de Contrôle HormonalDocument34 pagesPrincipes Des Systèmes de Contrôle HormonalSouha MessaoudiPas encore d'évaluation
- Cours EM Fusionné 2020Document99 pagesCours EM Fusionné 2020Serge Mbainoudji TendoPas encore d'évaluation
- Version ImprimableDocument22 pagesVersion ImprimableSylvain GravelaisPas encore d'évaluation
- Hormones GénéralitésDocument65 pagesHormones GénéralitésHadil TahraouiPas encore d'évaluation
- Physio Endocrine Revise 2019Document78 pagesPhysio Endocrine Revise 2019mbusaPas encore d'évaluation
- TD1 Regulation SABRINA.2019Document5 pagesTD1 Regulation SABRINA.2019axelPas encore d'évaluation
- Les HormonesDocument15 pagesLes Hormonessrhiri.lina2006Pas encore d'évaluation
- Physiologie Endocrinienne USTA 2023Document213 pagesPhysiologie Endocrinienne USTA 2023hamasakina19Pas encore d'évaluation
- Le Systeme EndocrinienDocument13 pagesLe Systeme EndocrinienAlexiPas encore d'évaluation
- 1 Introduction A La Physiologie Des Glandes EndocrinesDocument16 pages1 Introduction A La Physiologie Des Glandes EndocrinesAlina Topor Psi-MedicalPas encore d'évaluation
- QE de Physiologie EndocrinoDocument12 pagesQE de Physiologie EndocrinoN.Pas encore d'évaluation
- 01 - Principes - Generaux - de - La - Physiologie - Des - Glandes - Endocrines - DR - SILINIDocument29 pages01 - Principes - Generaux - de - La - Physiologie - Des - Glandes - Endocrines - DR - SILINIkilo Romeo23Pas encore d'évaluation
- Le Système EndocrinienDocument39 pagesLe Système EndocrinienRivaldo Nvo Nguema AvomoPas encore d'évaluation
- Chapitre V MineDocument19 pagesChapitre V MineMer IemPas encore d'évaluation
- Cours Physiologie S4 2017Document62 pagesCours Physiologie S4 2017Narciso RodriguezPas encore d'évaluation
- Hormone Et Régulation MasterDocument85 pagesHormone Et Régulation Mastermebarekwahida4Pas encore d'évaluation
- Cours 6Document27 pagesCours 6BouabidiPas encore d'évaluation
- CM 7 PhysioDocument31 pagesCM 7 PhysioMehdiPas encore d'évaluation
- Le Systeme Endocrinien WDocument9 pagesLe Systeme Endocrinien WsafemindPas encore d'évaluation
- Cours Histologie Glandes Endocrines 1Document3 pagesCours Histologie Glandes Endocrines 1Dany MelPas encore d'évaluation
- Endocrinologie IDocument88 pagesEndocrinologie Iritajbeily1611Pas encore d'évaluation
- Hormones: Les Grands Articles d'UniversalisD'EverandHormones: Les Grands Articles d'UniversalisPas encore d'évaluation
- Physio RespirationDocument40 pagesPhysio RespirationEric Charles HadjiPas encore d'évaluation
- Chap 8 PHYSIOLOGIE DU TRONC CEREBRALDocument10 pagesChap 8 PHYSIOLOGIE DU TRONC CEREBRALEric Charles HadjiPas encore d'évaluation
- Physio ReproductionDocument16 pagesPhysio ReproductionEric Charles HadjiPas encore d'évaluation
- Physio. DigDocument34 pagesPhysio. DigEric Charles HadjiPas encore d'évaluation
- FécondationDocument47 pagesFécondationEric Charles HadjiPas encore d'évaluation
- Estomac Et Ses VaisseauxDocument6 pagesEstomac Et Ses VaisseauxEric Charles HadjiPas encore d'évaluation
- Colon Et Ses Vaisseaux InternatDocument7 pagesColon Et Ses Vaisseaux InternatEric Charles HadjiPas encore d'évaluation
- 01 - Examen Clinique en PneumoDocument4 pages01 - Examen Clinique en PneumomouloudPas encore d'évaluation
- Physiopathologie: Facteurs de RisqueDocument1 pagePhysiopathologie: Facteurs de Risquegobeaux2959Pas encore d'évaluation
- ETT VM+VAoDocument7 pagesETT VM+VAoCLINIQUE INTERNATIONALE MARRAKECHPas encore d'évaluation
- Physiologie RespiratoireDocument6 pagesPhysiologie RespiratoireiduPas encore d'évaluation
- CoeurDocument6 pagesCoeurToth CsongorPas encore d'évaluation
- Traumatisme RateDocument61 pagesTraumatisme RatelordroentgenPas encore d'évaluation
- Algantil Enfant 080517Document4 pagesAlgantil Enfant 080517ismail jnainiPas encore d'évaluation
- Le Diabète - Chapitre Nutrition - BTS 2 Epms-1Document83 pagesLe Diabète - Chapitre Nutrition - BTS 2 Epms-1Clément AdamPas encore d'évaluation
- AbtoutNacera AghaRDocument99 pagesAbtoutNacera AghaRIssam KenouniPas encore d'évaluation
- Topo Embolie Pulmonaire Rea 2Document40 pagesTopo Embolie Pulmonaire Rea 2Zineb El BachraouiPas encore d'évaluation
- Veto Anapath Cours 4anDocument69 pagesVeto Anapath Cours 4andzsergioPas encore d'évaluation
- Pancréatite AigueDocument29 pagesPancréatite AiguedsjdhPas encore d'évaluation
- Artères Rénales Echo-Doppler - DR M DADONDocument75 pagesArtères Rénales Echo-Doppler - DR M DADONARMVOP100% (1)
- 0-Médecine Légale 2020-2021 - Qrocs - Cas CliniquesDocument76 pages0-Médecine Légale 2020-2021 - Qrocs - Cas Cliniquesresidanatblida2023Pas encore d'évaluation
- Path de L'estomacDocument22 pagesPath de L'estomacKatshuva Guy HeritierPas encore d'évaluation
- 6.système NerveuxDocument6 pages6.système NerveuxRahal karimPas encore d'évaluation
- L'ElectrocardiographeDocument61 pagesL'Electrocardiographebwassim403Pas encore d'évaluation
- 03 28 A3 Vertical Auriculothérapie Gauche DroiteDocument4 pages03 28 A3 Vertical Auriculothérapie Gauche DroiteKungfudjusuModerneWushuPas encore d'évaluation
- Bank D'anatomie 2019 PDFDocument16 pagesBank D'anatomie 2019 PDFKHALIFPas encore d'évaluation
- 11 - Cat Hémorragie Digestive BasseDocument36 pages11 - Cat Hémorragie Digestive Basseh4pd57452sPas encore d'évaluation
- Fonctionnement Du Coeur (Cycle Cardiaque), L2Document21 pagesFonctionnement Du Coeur (Cycle Cardiaque), L2safemindPas encore d'évaluation
- La Cirrhose Et Ses Complications M2Document65 pagesLa Cirrhose Et Ses Complications M2andrePas encore d'évaluation
- Cardio D1 OkDocument94 pagesCardio D1 OkBernard SendulaPas encore d'évaluation
- 39 - Choc CourDocument10 pages39 - Choc CourAbderrahmenPas encore d'évaluation
- Désir de Grossesse Chez Une Femme Hypertendue: Revues GénéralesDocument6 pagesDésir de Grossesse Chez Une Femme Hypertendue: Revues GénéralesSarah HouasniaPas encore d'évaluation
- Dyspneee 2018Document3 pagesDyspneee 2018OUMAIMA EL CHAALPas encore d'évaluation
- Introduction À La Pathologie Respiratoire CarineDocument261 pagesIntroduction À La Pathologie Respiratoire CarineTef YouPas encore d'évaluation
- Anevrysme AortDocument8 pagesAnevrysme AortElbordji100% (1)