Académique Documents
Professionnel Documents
Culture Documents
Les Ne Ovaisseaux Du Sujet Jeune - Original
Transféré par
abaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Les Ne Ovaisseaux Du Sujet Jeune - Original
Transféré par
abaDroits d'auteur :
Formats disponibles
Rétine médicale
Les néovaisseaux du sujet jeune
William Beaumont et Oudy Semoun - Créteil
L
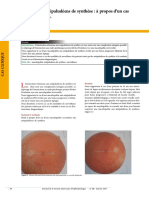
a survenue d’un néovaisseau myopie forte (-14,5 dioptries) et qui L’angiographie à la fluorescéine nous
choroïdien (NVC) est un évé- consulte en urgence pour une baisse montre au temps tardif une diffusion
nement potentiellement grave, d’acuité de l’œil gauche à 20/32. À du colorant en regard d’une rupture
aux séquelles parfois cécitantes, et l’examen du fond d’œil, nous retrou- de la membrane de Bruch (Figure 1b),
pouvant induire des implications vons un staphylome de type V associé avec une augmentation progressive de
majeures dans la vie des patients. à une dysversion papillaire (Figure 1a). l’intensité et de la taille de l’hyper-
Cela est d’autant plus vrai lorsque les Sur le bord de ce staphylome, nous fluorescence au cours de la séquence
néovaisseaux se développent chez notons de nombreuses ruptures de la angiographique. Une coupe SD-OCT
des sujets jeunes, en pleine activité membrane de Bruch qui témoignent passant par la lésion hyper-fluores-
professionnelle. de contraintes mécaniques au niveau cente (Figure 1d) retrouve du gris
de la jonction du staphylome et de la pré-épithélial à bords flous, avec un
La fréquence globale de la survenue rétine normale. épaississement rétinien en regard,
d’un NVC du sujet jeune n’est pas bien sans logettes intrarétiniennes.
établie. De nombreux facteurs étiolo-
giques ont été décrits. Ces néovais-
seaux apparaissent le plus souvent à
la suite d’une atteinte de l’épithélium
pigmentaire, qui entraîne la sécrétion
de facteurs pro-angiogéniques. La
plupart des NVC du sujet jeune sont
secondaires à une pathologie préexis-
tante, et sont pour la grande majorité
pré-épithéliaux (1). Cohen et al. ont
montré que 62 % des NVC du sujet
jeune sont associés à une myopie forte,
17 % sont idiopathiques, 12 % secon-
daires à une choroïdite multifocale et
5 % à des stries angioïdes, les 4 %
restants résultant de pathologies
variées (2).
Nous décrivons ici 4 cas de NVC du
sujet jeune, illustrant ces étiologies
variées.
•
●●●●●●●● La myopie forte
Figure 1 : a. Cliché infrarouge montrant les ruptures de membrane de Bruch (flèche noire) ;
Nous présentons ici le cas d’une jeune b. Angiographie à la fluorescéine montrant une diffusion localisée du colorant (flèche blanche) ;
patiente de 35 ans qui est atteinte de d : Coupe OCT passant par la lésion montrant du gris pré-épithélial (flèche).
N°236 - Tome 25 - juin 2020 - RéfleXions Ophtalmologiques 35
Les néovaisseaux du sujet jeune
Ces examens permettent de diagnos- •
●●●●●●●● Les néovaisseaux
idiopathiques du sujet
toire étant sans particularité, le dia-
tiquer un NVC de type 2, compliquant gnostic de néovaisseau idiopathique
une myopie forte. Ces NVC se situent jeune du sujet jeune a été retenu.
le plus souvent en regard d’une rupture Voici le cas d’une jeune femme de
de la membrane de Bruch (3,4). Dans le 23 ans qui s’est présentée en urgence Elle a bénéficié d’une injection d’anti-
cas spécifique du staphylome de pour baisse d’acuité visuelle brutale VEGF, avec une bonne réponse anato-
type 5, la complication néovasculaire (20/60) de l’œil droit associée à des mique et fonctionnelle à 1 mois
se situe le plus souvent au niveau de métamorphopsies. L’examen du fond (acuité visuelle à 20/25). Elle a cepen-
la jonction entre la rétine normale et d’œil droit retrouve une hémorragie dant présenté une récidive à 6 mois,
le staphylome inférieur (5,6). fovéolaire. L’angiographie à la fluores- nécessitant une nouvelle injection.
céine retrouve une diffusion tardive
Concernant le traitement, les recom- bien localisée, juxtafovéolaire Les néovaisseaux idiopathiques du
mandations actuelles sont de prévoir (Figure 2b), tandis que l’angiographie sujet jeune sont la deuxième cause de
une injection d’anti-VEGF, puis de au vert d’indocyanine montre un lacis NVC chez le sujet jeune, mais restent
suivre les patients selon un schéma néovasculaire dans la zone correspon- un diagnostic d’exclusion. Certains
pro re nata (PRN)(7). Les NVC du myope dante (Figure 2a). Ces éléments sont patients peuvent développer par la
fort sont en effet sensibles aux anti- en faveur de NVC de type 2, ce que suite une pathologie inflammatoire
VEGF et nécessitent, dans la plupart confirme l’OCT-angiographie, qui met chorio-rétinienne (choroïdite multifo-
des cas, moins d’injections intravi- en évidence ce néovaisseau au-dessus cale, par exemple) (8). Pour certains
tréennes que d’autres étiologies néo- du plan de l’épithélium pigmentaire auteurs, ces néovaisseaux idiopa-
vasculaires telles que la DMLA. Une (Figure 2d), avec du flux visible sur le thiques sont à considérer comme
absence de traitement est toujours B-scan correspondant (Figure 2c). secondaires à une maladie inflamma-
défavorable avec l’apparition d’une toire. D’autres pensent plutôt que c’est
tache de Fuchs, secondaire à la fibrose. La patiente ne présentant pas d’anté- le NVC qui pourrait déclencher une
cédents particuliers et le reste de maladie inflammatoire (9).
Cette patiente a pu bénéficier d’un l’examen ainsi que le bilan inflamma-
traitement par injection d’anti-VEGF
(2 injections), ce qui lui a permis de
récupérer une bonne acuité visuelle à
20/25 et une cicatrisation du néovais-
seau sans récidive à 1 an.
• La prévalence de NVC chez les
myopes forts varie entre 4 et 11 %,
selon les études, avec un risque de
bilatéralisation de 30 % à 8 ans.
• Il s’agit de la première cause de NVC
chez les sujets de moins de 50 ans.
• Première cause de cécité chez les
myopes forts avant l’arrivée des trai-
tements anti-VEGF.
• Bonne réponse thérapeutique, la
plupart du temps.
Figure 2 : a. ICGA temps précoce ; b. Angiofluo temps intermédiaire ;
c : B-scan montrant le flux intralésionnel ; d : OCT-A vue de face.
36 N°236 - Tome 25 - juin 2020 - RéfleXions Ophtalmologiques
Les néovaisseaux du sujet jeune
Le NVC idiopathique est en général
unilatéral et se déclare dans la 2e ou
3e décade. Il s’agit toujours d’un type 2.
Le pronostic est plutôt bon lorsque le
traitement par injection d’anti-VEGF
est instauré rapidement. Il est conseillé
de programmer une seule injection et
de suivre le patient selon un schéma
PRN, car ces NVC se stabilisent après
1,7 injections en moyenne (10).
• Il s’agit de la deuxième cause de
NVC chez le sujet jeune.
• Bon pronostic en cas de prise en
charge très précoce.
• Très bonne réponse thérapeutique.
• Il s’agit d’un diagnostic d’élimina-
tion, afin de ne pas méconnaître une Figure 3 : a. Angiofluo au temps tardif ; b. ICGA temps tardif ; c. Autofluorescence ; d. B-scan OCT-A ;
maladie inflammatoire rétino-choroï- e et f. OCT-A en face.
dienne.
choroïdite multifocale (12 % des NVC •
●●
●
●●
●●
● La choriorétinite
séreuse centrale
•
●●●●●●●● Les maladies
du sujet jeune) (2). Il existe un débat
pour savoir quel est l’élément causal (CRSC)
inflammatoires et quelle est la complication (9), la
chronologie n’étant pas toujours facile Un autre cas moins fréquent, mais tout
Une jeune patiente de 18 ans se pré- à mettre en évidence. Par exemple, aussi intéressant, est la complication
sente en urgence pour une baisse dans notre cas, il est impossible de néovasculaire d’une CRSC chronique.
d’acuité de l’œil droit (20/32) depuis savoir si le NVC est apparu avant le Elle est rare (2 % des cas de CRSC
quelques jours. Les examens per- MEWDS ou si le MEWDS a entraîné chronique (12)), mais il est important
mettent de diagnostiquer un syndrome l’apparition du NVC. Ce sujet reste de la détecter, car un traitement
des taches blanches évanescentes débattu, mais le traitement demeure adapté est primordial.
(MEWDS) caractérisé par de nom- consensuel, à savoir des injections
breuses taches hyper-autofluores- d’anti-VEGF afin de stabiliser le NVC Prenons le cas suivant d’un patient de
centes (Figure 3c). Ces taches (11)
. Un traitement systémique anti- 45 ans, suivi depuis des années pour
apparaissent hyper-fluorescentes aux inflammatoire est parfois indiqué dans une CRSC chronique. Nous pouvons
temps précoces de l’angiographie à la certaines choroïdites multifocales. constater au niveau de l’œil gauche un
fluorescéine, avec augmentation de la décollement sous-rétinien (DSR)
fluorescence aux temps tardifs associé à un « flat irregular pigment
(Figure 3a), associées à des taches • Une part non négligeable des NVC epithelium detachment » (FIPED
hypofluorescentes à l’ICG tardif est d’origine inflammatoire. (Figure 4b). L’OCT-angiographie per-
(Figure 3b). Une complication néovas- • La choroïdite multifocale est le plus met de mettre en évidence un NVC de
culaire de type 2, para-fovéolaire, est souvent en cause. type 1 au sein de ce FIPED (Figure 4c
mise en évidence par les angiogra- • La part néovasculaire doit être et d).
phies, ainsi que par l’OCT. traitée par injection d’anti-VEGF.
• Traiter, lorsque cela est nécessaire, La plupart des FIPED sont avasculaires,
Les choriocapillarites sont une des la maladie inflammatoire sous-jacente. et une néovascularisation de type 1 est
causes de néovascularisation secon- mise en évidence dans seulement
daire, dont la plus pourvoyeuse est la 18,9 % des cas (13) en angiographie. Une
N°236 - Tome 25 - juin 2020 - RéfleXions Ophtalmologiques 37
Les néovaisseaux du sujet jeune
• La CRSC chronique est une cause de
de NVC.
• Diagnostic difficile, même avec
l’imagerie multimodale.
• Meilleure sensibilité de l’OCT-A dans
la détection de ces NVC.
• Les NVC sont sous-épithéliaux.
• La présence d’un FIPED est associée
dans plus d’un tiers des cas à un NVC.
•
●●●●●●●● Conclusion
Les néovaisseaux du sujet jeune sont
Figure 4 : a. Cliché infrarouge ; b. Coupe SD-OCT montrant le FIPED ; d’origines diverses, la myopie forte
c. B-scan montrant le flux dans le FIPED ; d. OCT-A vue de face.
étant la pathologie la plus fréquem-
ment en cause. Il est important de faire
étude plus récente a montré la place cas à une complication néovasculaire, un bilan initial complet avec une ima-
intéressante de l’OCT-angiographie ouvrant la possibilité d’un traitement gerie multimodale afin de déterminer
pour détecter ces néovaisseaux, l’in- par injections d’anti-VEGF. Les carac- le contexte dans lequel est apparu ce
terprétation de l’angiographie clas- téristiques morphologiques du FIPED NVC. Le traitement de première inten-
sique étant plus délicate dans un sont importantes et peuvent nous tion repose sur les injections intra-
contexte d’hyperperméabilité choroï- orienter vers la présence d’une com- vitréennes d’anti-VEGF, avec une
dienne associée à l’atrophie de l’épi- plication néovasculaire. Ainsi, les injection initiale, puis un schéma
thélium pigmentaire. Dans cette étude, FIPED hyporéflectifs sont générale- thérapeutique en PRN afin d’injecter
la sensibilité de l’OCT-angiographie a ment avasculaires, alors que les FIPED « à la demande » et de pouvoir suivre
permis de mettre en évidence un lacis hyper-réflectifs sont avasculaires dans dans le temps le patient, initialement
néovasculaire dans 35,6 % des FIPED 44 % des cas (14). À noter que le traite- de façon mensuelle. Généralement, le
(contre 25 % pour l’imagerie multimo- ment d’un FIPED néovascularisé peut nombre d’injections est moins impor-
dale classique) (14). La présence d’un aider à la diminution du DSR, mais tant que pour les NVC de la DMLA.
FIPED est donc un signe d’alerte, n’intervient pas dans le traitement de
Liens d’intérêts : Les auteurs ne présentent pas
puisqu’il est associé dans un tiers des la CRSC à l’origine du NVC. de conflits d’intérêts en lien avec cet article.
RÉFÉRENCES
1. Liu B, Zhang X, Peng Y, Mi L, Wen F. Etiologies and Characteristics of Choroidal Neovascularization in Young Chinese Patients. Ophthalmologica. 2019;241:73-80.
2. Cohen SY, Laroche A, Leguen Y, Soubrane G, Coscas GJ. Etiology of choroidal neovascularization in young patients. Ophthalmology 1996;103:1241-4.
3. Ikuno Y, Sayanagi K, Soga K, Sawa M, Gomi F, Tsujikawa M, Tano Y. Lacquer crack formation and choroidal neovascularization in pathologic myopia. Retina 2008;28:1124-31.
4. Ohno-Matsui K, Yoshida T, Futagami S, Yasuzumi K, Shimada N, Kojima A, Tokoro T, Mochizuki M. Patchy atrophy and lacquer cracks predispose to the development of
choroidal neovascularisation in pathological myopia. Br J Ophthalmol 2003;87:570-3.
5. Stur M. Congenital tilted disk syndrome associated with parafoveal subretinal neovascularization. Am J Ophthalmol 1988;105:98-9.
6. Prost M, De Laey JJ. Choroidal neovascularization in tilted disc syndrome. Int Ophthalmol 1988;12:131-5.
7. Wolf S, Balciuniene VJ, Laganovska G, Menchini U, Ohno-Matsui K, Sharma T, Wong TY, Silva R, Pilz S, Gekkieva M; RADIANCE Study Group. RADIANCE: a randomized
controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology 2014.
8. Machida S, Fujiwara T, Murai K, Kubo M, Kurosaka D. Idiopathic choroidal neovascularization as an early manifestation of inflammatory chorioretinal diseases. Retina
2008;28:703-10.
9. Mathis T, Delaunay B, Cahuzac A, Vasseur V, Mauget-Faÿsse M, Kodjikian L. Choroidal neovascularisation triggered multiple evanescent white dot syndrome (MEWDS) in
predisposed eyes. Br J Ophthalmol 2018;102:971-6.
10. Mandal S, Garg S, Venkatesh P, Mithal C, Vohra R, Mehrotra A. Intravitreal bevacizumab for subfoveal idiopathic choroidal neovascularization. Arch Ophthalmol 2007;125:1487-92.
11. Battaglia Parodi M, Iacono P, Zucchiatti I, Bandello F. Choroidal Neovascularization Associated with Multiple Evanescent White Dot Syndrome Treated with Intravitreal
Ranibizumab. Ocul Immunol Inflamm 2018;26:608-11.
12. Daruich A, Matet A, Dirani A, Bousquet E, Zhao M, Farman N, Jaisser F, Behar-Cohen F. Central serous chorioretinopathy: Recent findings and new physiopathology hypothesis.
Prog Retin Eye Res 2015;48:82-118.
13. Hage R, Mrejen S, Krivosic V, Quentel G, Tadayoni R, Gaudric A. Flat irregular retinal pigment epithelium detachments in chronic central serous chorioretinopathy and
choroidal neovascularization. Am J Ophthalmol 2015;159:890-903.
14. Bousquet E, Bonnin S, Mrejen S, Krivosic V, Tadayoni R, Gaudric A. Optical coherence tomography angiography of flat irregular pigment epithelium detachment in chronic
central serous chorioretinopathy. Retina 2018;38:629-38.
38 N°236 - Tome 25 - juin 2020 - RéfleXions Ophtalmologiques
Vous aimerez peut-être aussi
- Glaucomes SecondairesDocument21 pagesGlaucomes SecondairesMajda BoukessessaPas encore d'évaluation
- Le Glaucome Néovasculaire Au Cours de La Rétinopathie DiabétiqueDocument3 pagesLe Glaucome Néovasculaire Au Cours de La Rétinopathie DiabétiqueKouamé MasseniPas encore d'évaluation
- Maculopathie TraumatiqueDocument3 pagesMaculopathie TraumatiqueBayoudh KarimPas encore d'évaluation
- NF tp1 PDFDocument4 pagesNF tp1 PDFAnonymous Z1tUl3n8aPas encore d'évaluation
- Chap09 - RETINOPATHIE - DIABETIQUE PDFDocument13 pagesChap09 - RETINOPATHIE - DIABETIQUE PDFabdo chaibiPas encore d'évaluation
- Cryptococcose Cérébro-Méningée À Présentation Pseudo-VasculaireDocument3 pagesCryptococcose Cérébro-Méningée À Présentation Pseudo-VasculaireDoloko BowayPas encore d'évaluation
- Stries AngioïdesDocument25 pagesStries AngioïdesPhilip McNelsonPas encore d'évaluation
- 8906 21333 1 SMDocument4 pages8906 21333 1 SMsoukaina soukainaPas encore d'évaluation
- 111-116 DOCDrLangis1006Document6 pages111-116 DOCDrLangis1006Viergelene PercinePas encore d'évaluation
- RO188 HubertDocument6 pagesRO188 HubertDęr NøtPas encore d'évaluation
- Cataracte Intumescente Compliquee D'Hypertonie Oculaire: RésuméDocument6 pagesCataracte Intumescente Compliquee D'Hypertonie Oculaire: RésuméSarkov HichemPas encore d'évaluation
- Les GlaucomesDocument6 pagesLes Glaucomesmila mimaPas encore d'évaluation
- Cdo243 Hemorragies Vitre Oretiniennes G NguyenDocument3 pagesCdo243 Hemorragies Vitre Oretiniennes G Nguyenmidou113Pas encore d'évaluation
- Maladie de BeçhetDocument5 pagesMaladie de BeçhetSerigne Sohibou GayePas encore d'évaluation
- Cour 03 Les Glaucomes ConvertiDocument9 pagesCour 03 Les Glaucomes ConvertiRania FzPas encore d'évaluation
- d0ae0319d103d9a7aa2c59dad68b5cc6Document3 pagesd0ae0319d103d9a7aa2c59dad68b5cc6sr89d9sb92Pas encore d'évaluation
- Cdo244 Clinique e Bousquet Syndrome Taches BlanchesDocument5 pagesCdo244 Clinique e Bousquet Syndrome Taches Blancheslaetitia.flowerainbowPas encore d'évaluation
- Séance 9 - QCM Et CAT GlaucomeDocument7 pagesSéance 9 - QCM Et CAT GlaucomeCheese CakePas encore d'évaluation
- Œil RougeDocument10 pagesŒil RougeAb ZakyPas encore d'évaluation
- Epreuves Classantes Nationales Oeil Rouge Ou DouloureuxDocument13 pagesEpreuves Classantes Nationales Oeil Rouge Ou DouloureuxPhilip McNelsonPas encore d'évaluation
- Urgences en OphtalmologieDocument15 pagesUrgences en OphtalmologieJulio FaculdadePas encore d'évaluation
- Imagerie Des Urgences en Neuro-Ophtalmologie 2014Document23 pagesImagerie Des Urgences en Neuro-Ophtalmologie 2014abdoulePas encore d'évaluation
- GlaucomeDocument4 pagesGlaucomemedPas encore d'évaluation
- AbcesDocument6 pagesAbcesloredanachiritescuPas encore d'évaluation
- LES URGENCES NON TRAUMATIQUES DU POLE POSTERIEURDocument37 pagesLES URGENCES NON TRAUMATIQUES DU POLE POSTERIEURDidier chanelPas encore d'évaluation
- Neuromyélite OptiqueDocument5 pagesNeuromyélite OptiquelunaPas encore d'évaluation
- DMLA CoursDocument9 pagesDMLA CourskamkermaPas encore d'évaluation
- La Conjonctivite Ligneuse Du Diagnostic Au Traitement - OriginalDocument2 pagesLa Conjonctivite Ligneuse Du Diagnostic Au Traitement - OriginalabaPas encore d'évaluation
- 4- Urgences ophtalmologiquesDocument117 pages4- Urgences ophtalmologiquesHiba TerrafiPas encore d'évaluation
- Bensalem 2018Document1 pageBensalem 2018HakimoPas encore d'évaluation
- La Revue de Médecine Interne Volume 29 Issue Supp-S1 2008 (Doi 10.1016/j.revmed.2008.03.320) N. Schleinitz E. Jean N. Bouhlila L. Benarous V. Veit E. Be - Administration Des Immunoglobulines P PDFDocument2 pagesLa Revue de Médecine Interne Volume 29 Issue Supp-S1 2008 (Doi 10.1016/j.revmed.2008.03.320) N. Schleinitz E. Jean N. Bouhlila L. Benarous V. Veit E. Be - Administration Des Immunoglobulines P PDFSuesy HopePas encore d'évaluation
- Les UvéitesDocument4 pagesLes UvéitesIlhammoukhlissePas encore d'évaluation
- CAT Devant Une Névrite OptiqueDocument5 pagesCAT Devant Une Névrite OptiqueSebti Benhadda100% (1)
- Poster Sfo NOTDocument23 pagesPoster Sfo NOTamina111amouriPas encore d'évaluation
- Pediatre Face À Oeil RougeDocument3 pagesPediatre Face À Oeil Rougehichem RAJAPas encore d'évaluation
- Le GlaucomeDocument1 pageLe GlaucomeflavientmdhPas encore d'évaluation
- Atteinte Neurologique Au Cours de La Maladie de Behc EtDocument1 pageAtteinte Neurologique Au Cours de La Maladie de Behc EtHakimoPas encore d'évaluation
- Occlusions Veineuses Rétiniennes: Retinal Vein OcclusionDocument18 pagesOcclusions Veineuses Rétiniennes: Retinal Vein Occlusionmouad hajjoujPas encore d'évaluation
- Maculopathie en TorpilleDocument3 pagesMaculopathie en TorpilleIlies IliesPas encore d'évaluation
- 8927 21371 1 SMDocument2 pages8927 21371 1 SMSouleymane DiabatePas encore d'évaluation
- Baisse D'acuite Visuelle BrutaleDocument5 pagesBaisse D'acuite Visuelle BrutaleJosué NguimatioPas encore d'évaluation
- Ophtalmo GrimmingerDocument48 pagesOphtalmo GrimmingerZOUHAIR KADDIOUIPas encore d'évaluation
- 8938 21394 1 SMDocument5 pages8938 21394 1 SMTesnime BouchelouhPas encore d'évaluation
- Glauco MeDocument31 pagesGlauco MeouaskokmohamedPas encore d'évaluation
- Manifestaciones Oculares de Wegener A Proposito de Una Obervacion (Francia 2009)Document11 pagesManifestaciones Oculares de Wegener A Proposito de Una Obervacion (Francia 2009)Denisse LizarragaPas encore d'évaluation
- Cours PDFDocument10 pagesCours PDFrgconxolPas encore d'évaluation
- Agboranderson2000,+014+Ao+Abba+Cataracte+2851 7642 1 SMDocument3 pagesAgboranderson2000,+014+Ao+Abba+Cataracte+2851 7642 1 SMHyacinthe Ehoussou BrouPas encore d'évaluation
- Traumatismes 2021Document8 pagesTraumatismes 2021Dol BergPas encore d'évaluation
- Nodules Thyroidiens TramalloniDocument36 pagesNodules Thyroidiens TramalloniAhmed SenhajiPas encore d'évaluation
- Tuberculose Vertébrale de L'adulteDocument15 pagesTuberculose Vertébrale de L'adulteespritdeboisPas encore d'évaluation
- RMS 22 1517Document5 pagesRMS 22 1517belanny97Pas encore d'évaluation
- 5 - Œil Et Maladies GénéralesDocument13 pages5 - Œil Et Maladies Généralesferhat.rahmaPas encore d'évaluation
- Le Manuel Du Généraliste - OphtalmologieDocument90 pagesLe Manuel Du Généraliste - OphtalmologieMf Pil100% (1)
- Complicatii Craniene Si Endocraniene Ale Sinuzitelor AcuteDocument8 pagesComplicatii Craniene Si Endocraniene Ale Sinuzitelor AcuteMihaela BorzaPas encore d'évaluation
- RAPDDocument2 pagesRAPDburnandPas encore d'évaluation
- Oeil RougeDocument16 pagesOeil RougeDolande BOUKAPas encore d'évaluation
- Le Manuel Du Généraliste - OphtalmologieDocument90 pagesLe Manuel Du Généraliste - OphtalmologiealdoPas encore d'évaluation
- 00 1035Document7 pages00 1035hizballah27Pas encore d'évaluation
- Maladie de CoatsDocument9 pagesMaladie de CoatsSerigne Sohibou GayePas encore d'évaluation
- Serie ImmunologieDocument4 pagesSerie ImmunologieWiem BenchahbounPas encore d'évaluation
- KololololozzzoeldoflfDocument307 pagesKololololozzzoeldoflfحامدي يعقوبPas encore d'évaluation
- 3-ToxocaroseDocument19 pages3-ToxocaroseSreypich VanPas encore d'évaluation
- WCRF 3Document45 pagesWCRF 3bib Abd-elkaderPas encore d'évaluation
- TSV 2019Document202 pagesTSV 2019Feth-allah SebbaghPas encore d'évaluation
- Les Dix Raisons de Consommer Le TamarinDocument5 pagesLes Dix Raisons de Consommer Le TamarinBALOGOUN BobiPas encore d'évaluation
- Préparation Rapide Document Facile À LireDocument522 pagesPréparation Rapide Document Facile À LireScribdTranslationsPas encore d'évaluation
- Dissection Escargot Petit Gris 1Document18 pagesDissection Escargot Petit Gris 1Djaser GOUASMIAPas encore d'évaluation
- CAS Clinique Paludisme GraveDocument30 pagesCAS Clinique Paludisme Graveamédée junior wawaPas encore d'évaluation
- Dyscalcemies 2Document38 pagesDyscalcemies 2Sophia BPas encore d'évaluation
- Psychologie MedicaleDocument18 pagesPsychologie MedicaleEdliePas encore d'évaluation
- Syndrome de Decompression Pericardique: Lorsque Le Drainage Pericardique Tourne Au Desastre :a Propos Dun CasDocument4 pagesSyndrome de Decompression Pericardique: Lorsque Le Drainage Pericardique Tourne Au Desastre :a Propos Dun CasIJAR JOURNALPas encore d'évaluation
- Cours 2 270Document23 pagesCours 2 270Hadilhz HadilhzPas encore d'évaluation
- Staloral France Not 025-21-Clean Validee 24-05-2022 ArDocument11 pagesStaloral France Not 025-21-Clean Validee 24-05-2022 ArMohammed SohaibmaherPas encore d'évaluation
- 149 - Angines Et Rhinopharyngites.Document8 pages149 - Angines Et Rhinopharyngites.TinaPas encore d'évaluation
- Y5 - Path-Chir - Pr. Mam Vithyarith Q25Document5 pagesY5 - Path-Chir - Pr. Mam Vithyarith Q25Sela KHPas encore d'évaluation
- PosterDocument4 pagesPosterlarbisalaheddine2002Pas encore d'évaluation
- Les Diarrhées Aiguës BactériennesDocument10 pagesLes Diarrhées Aiguës BactériennesSarah TitoPas encore d'évaluation
- Anévrisme de L'aorte AbdominaleDocument1 pageAnévrisme de L'aorte AbdominaleDoc OdocPas encore d'évaluation
- Les Antiparasitaires 2018Document35 pagesLes Antiparasitaires 2018Mary Louli100% (1)
- Tubage GastriqueDocument16 pagesTubage GastriqueOUSSAMA100% (1)
- Anatomie Du Rachis Et Du DosDocument78 pagesAnatomie Du Rachis Et Du Doszelfria.girlPas encore d'évaluation
- Traitement Au Dioxyde de Chlore CDSDocument2 pagesTraitement Au Dioxyde de Chlore CDSbalypatricia33Pas encore d'évaluation
- Occlusion Néonatal 1Document11 pagesOcclusion Néonatal 1Amina AminaPas encore d'évaluation
- 1 Appendicites AiguesDocument27 pages1 Appendicites AiguesClinique AMEPSGUI PITAPas encore d'évaluation
- Les Dangers de Tabac Sur La SantéDocument10 pagesLes Dangers de Tabac Sur La SantéᾄṩмᾄPas encore d'évaluation
- Péricardites Mai 2023 Final-1Document20 pagesPéricardites Mai 2023 Final-1Lamine SavadogoPas encore d'évaluation
- Sport Et Cardiologie RevisionpaecardioDocument3 pagesSport Et Cardiologie RevisionpaecardiofichesevcPas encore d'évaluation
- Renvoise 2593035580K TH PDFDocument109 pagesRenvoise 2593035580K TH PDFChiraz ChirazPas encore d'évaluation
- Acrosyndromes VasculairesDocument5 pagesAcrosyndromes VasculairesLydia BenazzouzPas encore d'évaluation