Académique Documents
Professionnel Documents
Culture Documents
TD CHORG SVTTU S2 2018 2019 Version Site Web Université
Transféré par
samsam100098Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
TD CHORG SVTTU S2 2018 2019 Version Site Web Université
Transféré par
samsam100098Droits d'auteur :
Formats disponibles
DEPARTEMENT DE CHIMIE
FILIERE SVTU/S2
TRAVAUX DIRIGES RESOLUS
CHIMIE ORGANIQUE
Préparés par : Pr. A. Tikad
Pr. A. Amechrouq
ANNEE UNIVERSITAIRE : 2018-2019
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 1
Exercice 1 :
Encerclez et nommez les groupements fonctionnels qui contiennent des atomes d’oxygène
et/ou d’azote dans les molécules suivantes :
NH 2
OH
HN H N OH
H
O
H N O
H O N
O
H
O O
(A) (B)
Exercice 2 :
Déterminez l’hybridation des carbones et des hétéroatomes dans la molécule suivante :
N OH
H2 N
O
H
(C)
CO2 Me
N
Exercice 3 :
Donnez les formules topologiques des molécules suivantes :
1) 2-Hydroxyhex-1-én-4-yn-3-one
2) N-méthyl-N-propyl-2-formyl-5-iodooctanamide
3) 4-Ethyl-2,2,7-triméthylnon-3-én-5-ol
4) 2,2-Dibromo-6-fluoro-4-isopropylhept-4-énal
TD Chimie Organique SVTU-S2 2
Département de Chimie Année Universitaire : 2018-2019
5) 6-Amino-3-chloro-5-hydroxyheptan-2-one
6) Acide 2-cyano-4-oxopent-2-énoïque
7) 2-Chloro-3-isopropylcyclobutanone
Exercice 4 :
Donnez le nom systématique de chacune des molécules suivantes selon les règles de
nomenclature de l’IUPAC :
Cl Ph
N O
Br
O
(a) (b) (c)
OH
F F O
N
H
(f) F Br
(d) Cl (e)
Ph
NH2 O
O HO
H CHO
O O O
(g) (h) (i)
OH O
OH
(j) CN (k) F (l)
Br O
O
OH
N (o)
(m) I (n)
TD Chimie Organique SVTU-S2 3
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 2
Exercice 1 :
Représentez tous les isomères de constitution de formule moléculaire suivante (calculez le
nombre d’insaturation de chaque molécule) :
a) C4H10O b) C2H5N c) C4H6
Exercice 2 :
1) Dessinez les deux conformations chaise de chacune des molécules suivantes :
a) Cis-1,4-dibromocyclohexane
b) Trans-1,4-dibromocyclohexane
2) Parmi les quatre conformations laquelle est la plus stable ? justifiez votre réponse.
3) Donnez la représentation de Newman de la conformation la plus stable (on regardera le
long des liaisons C1-C6 et C3-C4).
Exercice 3 :
Présentez par un astérisque (*) les carbones asymétriques et précisez la configuration (Z) ou
(E) des doubles liaisons appartenant au composé naturel suivant :
OMe
O
OH
O OH O
HO
OH
OMe
Bafilomycin
Exercice 4 :
Selon la règle séquentielle de Cahn-Ingold-Prelog (CIP), classez par ordre de priorité les
substituants suivants :
a) -CH2F -Cl -CH2Br -I
b) -COOCH3 -OCH3 -CH2OCH3 -COCH3
c) -CH=CH2 -CH(CH3)2 -C(CH3)3 -CH2CH3
d) -CN -CH2NH2 -NH2 -CH2NHCH3
e) -Ph -CH2SCH3 -SCH3 -CH3
TD Chimie Organique SVTU-S2 4
Département de Chimie Année Universitaire : 2018-2019
Exercice 5 :
Déterminez la configuration absolue (R, S) des carbones asymétriques dans les molécules
suivantes :
C2H 5 H3C H H 2C CH
HO H
H3C C CH
Cl H O
HO
a b c d
H OH H 2N H Ph CN H3C H
OH Br
C2H5 CH3 H3C H Cl H
HO H H CO2 H Cl H Cl CH3
e f g h
COCH3 CH3 CHO CO 2H
H Cl HS H F H HO H
I H H NH2 H F H 3C Br
C 2H 5 C2 H5 CH2 OH CH 3
i j k l
Exercice 6 :
Dessinez les structures de chacune des molécules suivantes en montrant clairement la
configuration absolue de chaque carbone asymétrique :
a) (R)-3-Bromo-3-méthylhexane d) (5S,3Z)-4-chloro-5-Fluorohex-3-én-2-one
b) Acide (2S,4R)-4-amino-2-cyanopentan- e) (3R,5S)-3-Hydroxy-5-méthylheptanal
oïque
c) (R)-2-Chloro-3-méthylbutane f) (1R,3S)-1-Iodo-3-méthylcyclopentane
Exercice 7 :
On considère le composé A dont la représentation en perspective de Cram est la suivante :
F COCH3
A:
H F
C2 H 5 C 6 H5
a) Déterminez la configuration absolue (R, S) des carbones asymétriques du composé A.
b) Représentez en projection de Newman toutes les conformations décalées et éclipsées du
composé A selon l’axe C3-C4.
c) Représentez en projection de Fischer le composé A.
d) Représentez en projections de Cram et Fischer l’inverse optique de A en indiquant la
configuration absolue de ses carbones asymétriques.
TD Chimie Organique SVTU-S2 5
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 3
Exercice 1 :
On considère les représentations de Fischer des molécules suivantes :
CH 3 CH3 CH 3 CH3
F H F H H F H F
H F F H F H H F
CH 3 CH3 CH 3 CH3
A B C D
a) Déterminez la configuration absolue des carbones asymétriques pour chaque
représentation.
b) Quelle est la relation stéréochimique ‘’énantiomères, diastéréoisomères ou méso’’ entre
les différents isomères ?
c) Déterminez les molécules chirales et achirales.
d) Représentez la molécule A en projection de Newman avec les deux groupements CH3 en
Syn et Anti, et la molécule B en projection de Cram.
Exercice 2 :
On considère le composé A : H3C―CHF―CH═CH―CHBr―CH3
1) Combien y a-t-il de stéréoisomères possibles de A ? indiquez-les par leurs configurations.
2) Donnez la représentation en perspective de Cram des isomères (2R,3E,5S) et (2S,3E,5R).
Exercice 3 :
1) Donnez toutes les formes limites et l’hybride de résonance des molécules suivantes :
O HO H O CN
Br CH3
OH
CH 3 Cl
a b c
2) Classez ces acides carboxyliques par ordre décroissant de pKa. Justifiez votre réponse.
Cl CO2H Cl CO2 H Br CO2H H 3C CO2 H
1 2 3 4
F H 3C Cl
H C CO2 H H3 C C CO2 H Cl H C CO2 H
CO2 H
F H 3C Cl
5 6 7 8
TD Chimie Organique SVTU-S2 6
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 4
Exercice 1 :
Le traitement du composé A avec de la soude à chaud conduit à la formation des deux
produits B (majoritaire) et C (minoritaire) :
H 3C H
H NaOH
B (maj) + C (min)
CH3
Br A C2 H5
1) Sachant que la vitesse est V = [A] [OH-], de quelle réaction s’agit-t-il ?
2) Donnez le mécanisme expliquant la formation des composés B et C ainsi que leurs
configurations.
3) Justifiez la formation majoritaire de B.
Exercice 2 :
Donnez la structure des produits A, B, C et D des réactions suivantes :
Br EtOH O Ether
1) + A C
NaI
25°C
3) Br + CH2MgBr
anhydre
Cl Cl
EtOH EtOH
2) + EtONa B 4) + NaOH D
∆ ∆
Exercice 3 :
On considère la réaction suivante :
CH3
H Cl
H B + B'
C6H5 C 2 H5
A
1) De quelle réaction s’agit-il ?
2) Donnez le mécanisme de la réaction, en précisant la configuration absolue des produits
obtenus.
3) Quelle relation stéréochimique existe-t-il entre B et B’ ?
TD Chimie Organique SVTU-S2 7
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 5
Exercice 1 :
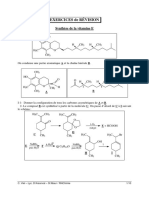
L’alcène A de configuration (E) a subi plusieurs réactions d’oxydation ci-dessous, soit par
ozonolyse soit en présence de KMnO4 :
O3 KMnO 4
? ?
H 2O concentré
Ph H
à chaud
H 3C C 2H 5
O3 A KMnO 4
? ?
H2 O/Zn dilué
à froid
1) Trouvez le(s) produit(s) de chaque réaction en indiquant la configuration absolue des
carbones asymétriques s’il y en a.
2) L’hydratation de l’alcène A avec de l’eau en présence d’une quantité catalytique de H2SO4
conduit à un mélange racémique.
a) Détaillez le mécanisme de la réaction, en précisant la configuration absolue des deux
produits obtenus.
b) Donnez la nomenclature systématique complète des produits obtenus.
Exercice 2 :
Complétez chacune des réactions suivantes :
a)
H3COC CN AlCl3
+ Cl2 ?
? O
b) + ?
c) Cl AlCl3
CF3 + ?
TD Chimie Organique SVTU-S2 8
Département de Chimie Année Universitaire : 2018-2019
d) ?
+ ?
e) H2SO4
+ HNO3 ?
FeBr3
f) H3C + Br2 ?
H2SO4
g) + SO3 ?
CO2H
h) ? + KMnO4 OH
à chaud CO2H
Exercice 3 :
Identifiez les composés A, B, C, D, E, F, G, H, I, J, K et L :
NaNH2 C 2H 5Br
Ph A B
H /H2O
H 3C C
Hg 2+
H /H 2O H2
A + C D E F
Pd/C
H G (Majoritaire) + H (Minoritaire)
F
HBr
G I
KMnO4
G J + C
cc à chaud
KMnO4
G K + L
dilué à froid
TD Chimie Organique SVTU-S2 9
Département de Chimie Année Universitaire : 2018-2019
Corrections
TD Chimie Organique SVTU-S2 10
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 1
Corrigé exercice 1 :
amine
alcool primaire amine
imine NH2 tertiaire
OH
HN H N OH
H
O
H N O
H O N acide
O nitrile
H ester carboxylique
cétone O O
(A) aldéhyde (B) amide
tertiaire
Corrigé exercice 2 :
sp3 sp2 sp3
sp sp3 O
sp N
sp 2 sp3 H
H 2N
C O C sp2
C
C C H
H
(C) O
sp2 C C
sp C sp2
C
sp3
H sp2
O
sp N sp3 CH3
3
sp
Corrigé exercice 3 :
1) 2-Hydroxyhex-1-én-4-yn-3-one 2) N-méthyl-N-propyl-2-formyl-5-iodooctanamide
6
5 OH CHO
4
2 8 6 4 2
3 5 1 N
1
7 3
O I O
TD Chimie Organique SVTU-S2 11
Département de Chimie Année Universitaire : 2018-2019
3) 4-Ethyl-2,2,7-triméthylnon-3-én-5-ol 4) 2,2-Dibromo-6-fluoro-4-isopropylhept-4-énal
O
7 5 3
8 6 4 2 6 2
7 5 1
9 1 4 H
3
F Br Br
OH
5) 6-Amino-3-chloro-5-hydroxyheptan-2-one 6) Acide 2-cyano-4-oxopent-2-énoïque
NH2 O O
4 5 3
6 5 3 4 2
2 1
7 1 OH
OH Cl O CN
7) 2-Chloro-3-isopropylcyclobutanone
O 1 2
Cl
4 3
Corrigé exercice 4 :
1 3
2 4 1
Cl Ph N O
5
5 2
8 6 5 3 3 1
10 9 7 7 6 4
Br O
(c)
(a) (b)
(a) : 8-Ethyl-3-méthyl-5-propyl-4-tert-butyldécane
(b) : 2-Bromo-6-chloro-4-phénylheptane
(c) : 3-N,N-diméthylaminohex-5-énoate de méthyle
1
2 OH F F O
1 7 3
4 5 4 3 2
4 5 6 1 N
6
2 H
(f) F Br
5
Cl (d) (e)
6
(d) : 4-Chloro-5-cyclobutyl-6-méthylnon-2-én-7-yne
(e) : 4-Ethyl-5-méthyl-3-propylhexan-2-ol
(f) : N-méthyl-2-bromo-3,4,5-trifluorohexanamide
TD Chimie Organique SVTU-S2 12
Département de Chimie Année Universitaire : 2018-2019
Ph NH 2 O
6
5 6
O 1 3 HO
2 4 1
5 3 1
H 2 4 7
CHO
3
O 4 (g) (h)
5
O O 8
(i)
(g) : 3-Pentyl-2-phénylpent-4-énoate d'isopropyle
(h) : 3-Amino-4-oxohex-5-ynal
(i) : Acide 7-formyl-4,5-diméthylocta-4,6-dièn-2-ynoïque
6 6 9
2 6 OH O 7 8
3 4 5
1 7 5 4 1
3 1 4
OH 3 5
(j) 2
CN (k) F (l)
(j) 3-Cyclopropyl-2,4,5-triméthylhepta-1,6-diène
(k) Acide 4-cyano-3-hydroxyhex-5-énoïque
(l) 5-Butyl-6-éthyl-4-fluoronon-1-ène
5 Br O
4
4 6
6 5
2
O 1 7 3 1
3
3
2 OH
5 4 2
1 (o)
6 N
(n)
(m) I
(m) : N-Ethyl-N-méthyl-2-iodo-5-phénylhex-2-énamide
(n) : 2-Isopropyl-5-méthylcyclohexanol
(o) : 6-Bromo-5-cyclohexylhept-3-én-2-one
TD Chimie Organique SVTU-S2 13
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 2
Corrigé exercice 1 :
a) Pour la formule brute CxHyOzNt, le nombre d’insaturation Ni = (2x+2-y+t)/2.
Pour C4H10O, Ni = (8+2-10+0)/2 = 0. Les isomères de constitution possibles sont :
OH OH
OH
OH
O
O O
b) C2H5N, le nombre d’insaturation Ni = (4+2-5+1)/2 = 1 (c’est-à-dire : une double liaison ou
un cycle)
Donc les isomères de constitution possibles sont :
H
NH 2 NH N N
c) C4H6, le nombre d’insaturation Ni = (8+2-6+0)/2 = 2 (c’est-à-dire : 1 triple liaison, 2
doubles liaisons, 2 cycles ou une double liaison et un cycle).
Donc les isomères de constitution possibles sont :
CH 3 CH 3 CH 2
1 triple 2 doubles
liaison liaisons 1 double liaison + 1 cyle 2 cycle
Corrigé exercice 2 :
1) Les deux conformations chaise du 1,4-dibromocyclohexane :
a) Cis-1,4-dibromocyclohexane
Br Br
1 4
Br Br
4 1
(1ax, 4éq) (1éq, 4ax)
TD Chimie Organique SVTU-S2 14
Département de Chimie Année Universitaire : 2018-2019
b) Trans-1,4-dibromocyclohexane
Br
6 4
1 5
Br Br
4 2
1 3
Br
(1ax, 4ax) (1éq, 4éq)
2) Le conformère le plus stable est (1éq,4éq) car c’est celui où les interactions 1,3-diaxials
sont minimales.
3) La représentation de Newman de la conformation la plus stable (1éq,4éq) (on regardera le
long des liaisons C1-C6 et C3-C4).
H H
6 2 4
Br H
6 4
5 1 3
Br 1 Br
2 3
H Br
5
H H
(1éq, 4éq)
(1éq, 4éq) selon Newman
Corrigé exercice 3 :
Les carbones asymétriques sont présentés par un astérisque (*) :
OMe
Z E
O
* OH
*
* O OH O
* *
E E
* * * * * * *
HO
OH
OMe
Bafilomycin
Corrigé exercice 4 :
Selon la règle séquentielle de Cahn-Ingold-Prelog (CIP), le classement par ordre de priorité
des substituants est le suivant :
a) -I > -Cl > -CH2Br > -CH2F
b) -OCH3 > -COOCH3 > -COCH3 > -CH2OCH3
Justification:
TD Chimie Organique SVTU-S2 15
Département de Chimie Année Universitaire : 2018-2019
O O
OCH 3 C OCH3 C CH3 CH2OCH3
O C O C H
H C O C O C H
O C H H H H
H O C H C H O C H
H H H
c) -C(CH3)3 > -CH=CH2 > -CH(CH3)2 > -CH2CH3
Justification:
C(CH3)3 C CH2 CH(CH3)2 CH2CH3
H
H
H H H
C H H H H
H C C H H
C C H C C C C H C H H
C H C H C H
H H H
H H
H
d) -NH2 > -CN > -CH2NHCH3 > -CH2NH2
Justification:
NH2 N CH2NHCH3 CH2NH2
C H H
H N
N C C C H H C H
N
H N C H
H N H
N H H
e) -SCH3 > - CH2SCH3 > -Ph > -CH3
Justification:
SCH3 CH2SCH3 C CH3
H H
H H H
C C H
S C H C S C H C C H
H H H H
C C
C C
C
Corrigé exercice 5 :
Détermination de la configuration absolue (R,S) des carbones asymétriques :
H3C H H2 C CH
HO H C2H5
H 3C C CH
Cl H O
HO
a (S) b (ni R ni S) c (R) d (S)
TD Chimie Organique SVTU-S2 16
Département de Chimie Année Universitaire : 2018-2019
H OH H2N H Ph CN H3C H
3 3 2 OH Br
CH3 2
C2H5 2 H3C H 3 Cl H 3 2
HO H H CO2H Cl H Cl CH3
e (2R,3R) f (2S,3S) g (2S,3S) h (2R,3S)
COCH 3 CH 3 CHO CO2H
3 2 2 2
H Cl HS H F H HO H
3
I 4 H H 3 NH 2 H 3 F H3C Br
C 2H 5 C 2H 5 CH 2OH CH3
i (3S,4S) j (2R,3R) k (2R,3R) l (2R)
Corrigé exercice 6 :
Les structures de chacune des molécules avec la configuration absolue des carbones
asymétriques :
a) (R)-3-Bromo-3-méthylhexane : d) (5S,3Z)-4-Chloro-5-fluorohex-3-én-2-
one :
Br CH3
O Cl
2 4 6 6
1 3 5 1 5
2 4
3
b) Acide (2S,4R)-4-amino-2-cyanopentan-
H F
oïque :
H CN H NH2 e) (3R,5S)-3-Hydroxy-5-méthylheptanal :
HO 1 H 1 3 5
2 4 2 4 6
5 7
3
O O HO H H CH 3
c) (R)-2-Chloro-3-méthylbutane : f) (1R,3S)-1-Iodo-3-méthylcyclopentane :
Cl H 2
I CH3
1 3 1 3
2 4
H H
5 4
Corrigé exercice 7 :
a) Détermination de la configuration absolue (R, S) :
Selon la règle de Cahn-Ingold et Prelog l’ordre de priorité est :
- Pour C3* : F > C4* > COCH3 > C6H5 avec le 4ème élément en avant).
- Pour C4* : F > C3* > C2H5 > H
TD Chimie Organique SVTU-S2 17
Département de Chimie Année Universitaire : 2018-2019
Pour le carbone asymétrique 3, le 4ème élément (C6H5) est en avant donc la configuration
absolue de ce dernier est l’inverse de ce qu’on trouve après rotation.
O
1
F CH3
2
4
A (3S,4R) : 3
H F
C2 H 5 C 6H 5
b) Projections de Newman du composé A :
Pour décrire les différentes conformations du composé A, on représente la molécule en
Newman suivant l’axe de la liaison C3-C4. La rotation d’un angle de 60° permet d’avoir au
total six conformations (A1-A6), trois éclipsées et trois décalées :
COCH 3 COCH 3 COCH 3
F 4 Et
4 Et F 4
60° 3 60°
3 3
Ph F
H F
Ph Et F H Ph H F
F A 1 éclipsée A 2 décalée A 3 éclipsée
COCH3
4 3
60° 60°
H F
C2H 5 C6H 5 COCH3 COCH3 COCH 3
A 4 H 4
F H 4 H Et
3 60° 60° 3
3
Ph F Ph F
Et
Et Ph F F F
A6 décalée A5 éclipsée A4 décalée
c) Représentation de Fischer du composé A :
Pour la représentation de Fischer du composé A on doit d’abord effectuer une rotation de
120° du centre C4* autour de l’axe C3-C4 pour transcrire la chaine carbonée dans le plan.
Ensuite, l’observateur doit regarder dans le sens opposé de la chaine carbonée de telle sorte
que les substituants horizontaux soient vers l’avant et les substituants verticaux de la chaine
carbonée (COCH3 et C2H5) soient vers l’arrière. Noter bien que la tête de l’observateur doit
être placée vers le carbone le plus oxydé (dans notre cas c’est le groupement COCH3).
TD Chimie Organique SVTU-S2 20
Département de Chimie Année Universitaire : 2018-2019
COCH3 COCH3
F COCH 3 C 2H 5 COCH 3 3 3
4 3
120° 4 3 Ph F Ph F
H F F F 4 4
C 6 H5 H F H F
C2 H 5 H C 6H5
A (3S,4R) C2 H5 C2H 5
Fischer
de A (3S,4R)
d) Représentation en projections de Cram et Fischer de l’inverse optique de (A) :
L’inverse optique du composé A c’est son énantiomère, c’est-à-dire son image dans un
miroir :
miroir miroir
COCH 3 COCH 3
F COCH3 H3COC F 3 3
3 4
Ph F F Ph
4 3
H F F H 4 4
H F F H
C 2H 5 C6 H5 C 6H 5 C2 H5
C 2H 5 C 2 H5
A (3S,4R) B (3R,4S)
A (3S,4R) B (3R,4S)
représentation de Cram
représentation de Fischer
TD Chimie Organique SVTU-S2 21
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 3
Corrigé exercice 1 :
a) Détermination de la configuration absolue :
CH 3 CH3 CH 3 CH3
2 2 2 2
F H F H H F H F
H 3 F F 3
H F 3 H H 3 F
CH 3 CH3 CH 3 CH3
A (2R,3R) B (2R,3S) C (2S,3S) D (2S,3R)
b) Relation stéréochimique entre les différents isomères :
Diastéréoisomères : A et B; A et D; B et C; C et D.
Enantiomères : A et C.
Méso : B et D.
Les deux molécules B (2R,3S) et D (2S,3R) sont identiques puisqu’elles possèdent un plan de
symétrie. Si on fait une rotation de 180° de la molécule B dans le plan de la feuille on tombe
sur la molécule D. Dans ce cas, on dit que les deux molécules B et D sont Méso.
CH3 CH3
2 rotation de 180° 2
F H dans le plan H F plan de
F H H F symétrie
3 3
CH3 CH3
B (2R,3S) D (2S,3R)
Méso Méso
c) Détermination des molécules chirales et achirales :
Les molécules chirales sont : A et C car elles ont 2 carbones asymétriques et ne possèdent ni
plan ni centre de symétrie.
Les molécules achirales sont : B et D car elles possèdent un plan de symétrie.
TD Chimie Organique SVTU-S2 22
Département de Chimie Année Universitaire : 2018-2019
d) Représentation de Newman de la molécule A avec les deux groupements CH3 en Syn et
Anti :
CH3 CH 3 CH 3 CH3
2 2
H3C rotation 3
F H F H 3 F H
180° 2
2
H 3
F H 3
F
F F H
CH3 CH 3 FH H CH3
Conformation Conformation
A (2R,3R) Syn Anti
Newman
La représentation de Cram de la molécule B :
CH 3 CH 3
2 2 H3 C CH3
F H F H 3 2
F 3
H F 3
H H H
CH 3 CH 3 F F
B (2R,3S)
B (2R,3S)
Cram
Corrigé exercice 2 :
H H
6 4 3 1
(A) : H3C C C C C 2 CH3
5
F H H Br
1) Le composé (A) possède deux carbones asymétriques et une double liaison, donc il a 23 = 8
stéréoisomères : (2R,3E,5R), (2S,3E,5S), (2R,3E,5S), (2S,3E,5R), (2R,3Z,5R), (2S,3Z,5S),
(2R,3Z,5S), (2S,3Z,5R).
2) La représentation en perspective de Cram des isomères (2R,3E,5S) et (2S,3E,5R) :
H F F H
5 2 CH 3 5 2 CH3
H 3C H3C
Br H H Br
(2R,3E,5S) (2S,3E,5R)
TD Chimie Organique SVTU-S2 23
Département de Chimie Année Universitaire : 2018-2019
Corrigé exercice 3 :
1) Les formes limites et les hybrides de résonance des différentes molécules :
O
O δ−
O O
δ+
OH OH OH OH
Br CH3 Br CH3 Br CH3 Br CH3
a
hybride de résonance
HO H O O O
HO H HO H
CH3 CH3 CH 3
Cl Cl Cl
b
−
HO H Oδ HO H O HO H O
CH3 CH3 CH 3
+
Clδ Cl Cl
hybride de
résonance
δ−
N N N N N N
C C C C C C
δ+ δ+
c δ+
hybride de
résonance
2) Classement des acides carboxyliques par ordre décroissant de pKa :
Cl CO2H Cl CO2 H Br CO2H H 3C CO2 H
1 2 3 4
EI (-I) EI (-I) EI (-I) EI (+I)
Cl Cl Br CH 3
F H 3C Cl
H C CO2 H H 3 C C CO2 H Cl H C CO2 H
CO2H
F H 3C Cl
5 6 7 8
EI (-I) EI (+I) EI (-I) EI (-I)
2F 3CH3 Cl 2Cl
TD Chimie Organique SVTU-S2 24
Département de Chimie Année Universitaire : 2018-2019
- L'influence du fluor, du brome et du chlore se caractérise par un effet inductif attracteur (-I).
Cet effet fragilise la liaison O-H (en augmentant la polarité de la liaison) donc elle devient
plus acide.
- X(F) > X(Cl) > X(Br) et pKa= -logKa donc pKa(5) < pKa(8) et pKa(2) < pKa(3).
- Lorsque le nombre de groupements attracteurs augmente, l'effet inductif électroattracteur
augmente, donc l’acidité augmente : 8 est plus acide que 2 donc pKa(8) < pKa(2).
- L’effet inductif diminue avec la distance donc pKa(2) < pKa(7) < pKa(1).
- La molécule 6 porte 3 groupements donneurs CH3 (+I), c’est la moins acide, son pKa est la
plus grande. pKa(4) < pKa(6).
pKa décroissant
6 4 1 7 3 2 8 5
TD Chimie Organique SVTU-S2 25
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 4
Corrigé exercice 1 :
1) Le composé A est traité avec de la soude à chaud donc il s’agit d’une réaction
d’élimination, de type E2 car la vitesse de la réaction V = K [A] [OH-], dépend à la fois de la
concentration du substrat et de la base (une seule étape).
2) Le mécanisme réactionnel et la configuration des composés B et C :
La réaction se fait en une seule étape : l'arrachage du proton par la base, la formation de la
double liaison, et le départ du bromure (nucléofuge).
A rappeler que la réaction E2 ne se fait que lorsque le proton et le groupe partant sont en
position antipériplanaire. Obtention d’un seul alcène de configuration Z ou E.
voie 2
H
voie 1 H
H2C H H CH3 H H
H
Na,OH
CH3 + - NaBr +
3R CH3
Br A C2 H 5 - H 2O H 3C C 2 H5 H
C 2H5
B (maj) C (min)
conf: Z conf: ni Z ni E
3) La formation majoritaire de B est justifiée par la règle de Zaitsev : lors d'une réaction
d'élimination, le proton part préférentiellement du carbone le moins hydrogéné pour donner
l'alcène le plus substitué (B).
Corrigé exercice 2 :
La structure des produits A, B, C et D des réactions suivantes :
Br EtOH I substitution
1) + NaI nucléophile
25°C
A
Cl
EtOH Elimination
2) + EtONa ∆
B
TD Chimie Organique SVTU-S2 26
Département de Chimie Année Universitaire : 2018-2019
O Ether O
+ substitution
3) Br CH 2MgBr anhydre nucléophile
C
Cl EtOH
4) + NaOH Elimination
∆
D
Corrigé exercice 3 :
1) C’est une réaction d’addition électrophile de H-Cl sur un alcène.
2) Le mécanisme réactionnel ainsi que la configuration absolue des produits obtenus :
1ère étape : l'électrophile H+ réagit sur les électrons π de la double liaison de manière à former
le carbocation (intermédiaire) le plus stable suivant la règle de Markovnikov.
Règle de Markovnikov : lors de l'addition électrophile ionique d'un composé Aδ+―Bδ- sur un
alcène dissymétrique, B se fixe sur le carbone le plus substitué (le moins hydrogéné).
2ème étape : l'ion halogénure vient alors attaquer le carbocation soit par le haut (voie 1), soit
par le bas (voie 2) pour finalement former les deux molécules chlorées B et B’:
voie 1
CH3 H 3C CH3 2ème Cl CH 3 Ph CH3
H Cl Cl étape 2 3 H3 C 2 3
+
H 1ère H H3 C H H
Ph Et étape Ph Et Ph Et Cl Et
A voie 2
carbocation B (2S,3S) B' (2R,3S)
(mélange racémique)
3) B et B’ sont des diastéréoisomères.
TD Chimie Organique SVTU-S2 27
Département de Chimie Année Universitaire : 2018-2019
Travaux dirigés de chimie organique
Filière SVTU-S2
Série N° 5
Corrigé exercice 1 :
1) La réaction de A avec KMnO4 dilué à froid est une réaction de dihydroxylation (syn
addition) qui donne accès à un mélange racémique de deux énantiomères D et D’. Le zinc
joue le rôle d’un réducteur qui permet l’arrêt de l’oxydation au niveau de l’aldéhyde.
Ph OH O3 KMnO 4 Ph OH
O+O O + O
H2 O concentré
Me A B Et Ph H Me A B Et
à chaud
Me Et HO OH Me Et
Ph H O3 A KMnO 4 2 3
O+ O Ph 2 3 H
H 2O/Zn dilué Ph H +
Me A C Et à froid Me Et HO OH
D (2S,3S) D' (2R,3R)
2) L’hydratation de l’alcène A avec de l’eau en présence d’une quantité catalytique de H2SO4
conduit à un mélange racémique.
a) Le mécanisme de l’hydratation :
1ère étape : l’électrophile H+ se fixe sur le carbone le moins substitué, formant ainsi un
carbocation sur le carbone le plus substitué, suivant la règle de Markovnikov.
2ème étape : une molécule d'eau se lie au carbocation soit par le haut (voie 1), soit par le bas
(voie 2) pour conduire finalement au mélange racémique de deux alcools E et E’ après
déprotonation.
H
voie 1
Ph H Ph H 2ème H O Me
H O étape Ph
H H H Pr + Pr
1ère Ph
Me Et Me Et Me H O
A étape voie 2
H
-H
HO Me
2R Ph 2S
Pr + Pr
Ph
Me HO
E E'
TD Chimie Organique SVTU-S2 28
Département de Chimie Année Universitaire : 2018-2019
b) La nomenclature systématique complète des produits obtenus :
HO Me
2R Ph 2S
Pr Pr
Ph
Me HO
E (R)-2-phé nylpentan-2-ol E' (S)-2-phé nylpentan-2-ol.
Corrigé exercice 2 :
H3COC CN
H3COC CN AlCl3
a) + Cl2
Cl
AlCl3
b) + Cl
O O
iPr
Cl AlCl3
c) CF3 + CF3
d) Cl AlCl3
+
H2SO4
e) + HNO3 NO2
FeBr3 H3C
f) H3C + Br2 + H3C Br
Br
H2SO4
g) + SO3 SO3H
CH3 CO2H
h) OH
+ KMnO4
CH3 à chaud CO2H
TD Chimie Organique SVTU-S2 29
Département de Chimie Année Universitaire : 2018-2019
Corrigé exercice 3 :
L’identification des composés A, B, C, D, E, F, G, H, I, J, K et L :
NaNH 2 C 2H 5 Br
Ph Ph Na Ph C 2 H5
A B
O
H /H2 O
H 3C
Hg2+ H 3C CH3
C
O Na H /H O OH H2 OH
2
A + C Ph Ph
Pd/C Ph
D E F
H
F +
∆ Ph Ph
(règle de Zaitsev)
G (Majoritaire) H (Minoritaire)
HBr
(règle de Markovnikov)
Ph Ph Br
I
G
O
KMnO 4
Ph CO2 H +
Ph cc à chaud J C
G
HO OH PhH 2C Me
KMnO 4 2 3
Me
H 2 3
H Me +
Ph dilué à froid
G PhH 2 C Me HO OH
K L
TD Chimie Organique SVTU-S2 30
Vous aimerez peut-être aussi
- Serie 1,2 Et 3 SVTU (S2)Document23 pagesSerie 1,2 Et 3 SVTU (S2)Coulibaly HammaPas encore d'évaluation
- CH Org Tdcorr 1Document22 pagesCH Org Tdcorr 1Hugues Roodly JeannitePas encore d'évaluation
- Edoc - Pub - Examen Correction l1 Chimie Organique 2006 2Document7 pagesEdoc - Pub - Examen Correction l1 Chimie Organique 2006 2Mohamed DahmanePas encore d'évaluation
- Série TD N3-S3-20-21Document2 pagesSérie TD N3-S3-20-21فيصل البلخلفيPas encore d'évaluation
- Exercices Corrigés NomenclatureDocument4 pagesExercices Corrigés NomenclatureMalek abidi100% (5)
- Examen Correction L1 Chimie Organique 2006 2Document7 pagesExamen Correction L1 Chimie Organique 2006 2med madPas encore d'évaluation
- Examen de Chimie Organique 2014Document4 pagesExamen de Chimie Organique 2014RedOne DerrouazinPas encore d'évaluation
- Exercices Corrigés NomenclatureDocument4 pagesExercices Corrigés Nomenclaturemedimegh.insaf2020Pas encore d'évaluation
- TD MGS Et StaffDocument11 pagesTD MGS Et StaffdiayeloupPas encore d'évaluation
- Session 1 2016Document7 pagesSession 1 2016Yc YacinePas encore d'évaluation
- Série 1Document2 pagesSérie 1samiraPas encore d'évaluation
- TD L2 Suite New 2015 2016Document18 pagesTD L2 Suite New 2015 2016Najimou Alade TidjaniPas encore d'évaluation
- Epreuve Juin smc6 14 15Document2 pagesEpreuve Juin smc6 14 15cvbn100% (1)
- Epreuve Juin smc6 14 15Document2 pagesEpreuve Juin smc6 14 15santaPas encore d'évaluation
- Série No 6 L2PCSM 2022Document2 pagesSérie No 6 L2PCSM 2022NgagneseckPas encore d'évaluation
- TD CHM13220 Physicien PDFDocument6 pagesTD CHM13220 Physicien PDFArsène KekpenaPas encore d'évaluation
- Corrigé Contro Continu Chimie 4 2019Document2 pagesCorrigé Contro Continu Chimie 4 2019evilievPas encore d'évaluation
- TD de Chimie Organique (Aldéhydes-Cétones-Acides) .2023Document4 pagesTD de Chimie Organique (Aldéhydes-Cétones-Acides) .2023assekoted99Pas encore d'évaluation
- Hétérocycles Saturés ExercicesDocument3 pagesHétérocycles Saturés ExercicesMohamed BirouPas encore d'évaluation
- Klubprepa 3899Document2 pagesKlubprepa 3899berkatimanel22Pas encore d'évaluation
- 1 Éxamen de Chimie Organique-SMP-s3.Ratt-2017Document6 pages1 Éxamen de Chimie Organique-SMP-s3.Ratt-2017Ghizlane KarimPas encore d'évaluation
- DS2 de Chimie Organique 2022Document2 pagesDS2 de Chimie Organique 2022romain.albierPas encore d'évaluation
- Exercices CHM144 FSS TD4Document3 pagesExercices CHM144 FSS TD4Omega SigmaPas encore d'évaluation
- TD1 S3 SMP 2020Document4 pagesTD1 S3 SMP 2020Al Hiani AnasPas encore d'évaluation
- TD Éffets Électroniques 2020Document3 pagesTD Éffets Électroniques 2020Berthe AmiPas encore d'évaluation
- Exercices Reaction ChimiqueDocument8 pagesExercices Reaction ChimiqueJean-François Abena100% (1)
- Exercice 1: Trouver Une Formule Semi-Développée Pour Chacun Des Composés SuivantsDocument2 pagesExercice 1: Trouver Une Formule Semi-Développée Pour Chacun Des Composés Suivantssteve dademPas encore d'évaluation
- Heterocycles SaturesDocument3 pagesHeterocycles SaturesJean-François Abena100% (2)
- exo-ISI-effet Électronique-Réaction Et MécanismeDocument5 pagesexo-ISI-effet Électronique-Réaction Et MécanismeJoseph 27Pas encore d'évaluation
- Exercices-Chapitre-2 #BiolDocument5 pagesExercices-Chapitre-2 #BiolZinou Bourbia100% (1)
- Serie de TD ChimieDocument5 pagesSerie de TD Chimieraouf teach 04Pas encore d'évaluation
- smc5 Session 1 2020Document7 pagessmc5 Session 1 2020adnanPas encore d'évaluation
- Corrige PC s2 2013 2Document6 pagesCorrige PC s2 2013 2Essohanam AwatePas encore d'évaluation
- Exercices Reaction ChimiqueDocument9 pagesExercices Reaction ChimiquePride Algerian ツPas encore d'évaluation
- EXAMEN 1 CORRIGéDocument3 pagesEXAMEN 1 CORRIGéSOUFYANE MUSTAPA100% (1)
- Car Bony Les Alpha-Beta InsaturesDocument7 pagesCar Bony Les Alpha-Beta InsaturesJean-François Abena100% (2)
- Corrigé de Examen Final OrganiqueDocument2 pagesCorrigé de Examen Final OrganiqueRedOne DerrouazinPas encore d'évaluation
- 1 Nomenclatureexercices2Document4 pages1 Nomenclatureexercices2Evilasio CostaPas encore d'évaluation
- A V FDLL V 11 (T, PB) - Il (T, PA) V VDocument5 pagesA V FDLL V 11 (T, PB) - Il (T, PA) V VAhlem KabadouPas encore d'évaluation
- S6 Hoc TD4 2020Document2 pagesS6 Hoc TD4 2020donaldPas encore d'évaluation
- EPSS2017 VersionaDocument2 pagesEPSS2017 VersionaaxelPas encore d'évaluation
- RevisionDocument10 pagesRevisionChimiste ChimistePas encore d'évaluation
- TD Heteroéléments en Chimie OrganiqueDocument3 pagesTD Heteroéléments en Chimie OrganiqueazizPas encore d'évaluation
- Série 2 Isomérie 2020-2021Document3 pagesSérie 2 Isomérie 2020-2021Ayoub HmPas encore d'évaluation
- Corrige Examen Session 1 2010Document5 pagesCorrige Examen Session 1 2010adnanPas encore d'évaluation
- Acide CarboxderivesDocument40 pagesAcide CarboxderivesLevier PoidsPas encore d'évaluation
- DS 7 Orga + Binaires SL + ComplexesDocument10 pagesDS 7 Orga + Binaires SL + ComplexesAbdelbassit FadilPas encore d'évaluation
- Série-1 Corrigée Chimie4Document4 pagesSérie-1 Corrigée Chimie4poly educationPas encore d'évaluation
- Planche TD 2009Document8 pagesPlanche TD 2009Natacha N'GUESSANPas encore d'évaluation
- Organique 13-14 SolutionDocument2 pagesOrganique 13-14 Solutiondrisszekraoui14Pas encore d'évaluation
- Heterocycles AromatiquesDocument5 pagesHeterocycles AromatiquesJean-François Abena88% (8)
- Fiche Ex 04Document2 pagesFiche Ex 04Dony KravitzPas encore d'évaluation
- Exercices NomenclatureDocument5 pagesExercices NomenclatureJean-François Abena71% (7)
- CH Org TD 10 PDFDocument11 pagesCH Org TD 10 PDFMohammed MaalalPas encore d'évaluation
- Mécanique Du Point TDDocument2 pagesMécanique Du Point TDsamsam100098Pas encore d'évaluation
- Exmecanique 2008-2009 2Document15 pagesExmecanique 2008-2009 2Alae LazààrPas encore d'évaluation
- FASCICULE EznDocument98 pagesFASCICULE EznRomaric VossanouPas encore d'évaluation
- Algorithmique... B K 7Document14 pagesAlgorithmique... B K 7samsam100098Pas encore d'évaluation
- Corrigés Mecanique Du Point 1Document2 pagesCorrigés Mecanique Du Point 1samsam100098Pas encore d'évaluation
- Magnéto ÉpreuvesDocument9 pagesMagnéto Épreuvessamsam100098Pas encore d'évaluation
- Exo Pile Saline CorrigeDocument11 pagesExo Pile Saline CorrigetalebPas encore d'évaluation
- 2019 TD - Chapitre - 16 - Redox-1 PDFDocument4 pages2019 TD - Chapitre - 16 - Redox-1 PDFDavid KonanPas encore d'évaluation
- Sujet 03Document2 pagesSujet 03samsam100098Pas encore d'évaluation
- PDFDocument22 pagesPDFSaikou Oumar BarryPas encore d'évaluation
- sérieTD ATODocument6 pagessérieTD ATOsamsam100098Pas encore d'évaluation
- Cours - Ait Ahmed Nadia - Cours Et Exercices de Chimie Organique 1Document97 pagesCours - Ait Ahmed Nadia - Cours Et Exercices de Chimie Organique 1Emilienne Monkon100% (1)
- BF492 mgt16041Document139 pagesBF492 mgt16041Michel BMPas encore d'évaluation
- Rapport de StageDocument15 pagesRapport de StageAgossa BénédictePas encore d'évaluation
- 15 May 2013Document343 pages15 May 2013Download_Scribd_stufPas encore d'évaluation
- Philosophie Subtile ParacelseDocument16 pagesPhilosophie Subtile Paracelseredvelvetmask2343Pas encore d'évaluation
- Examen Pruebas de Acceso A La Universidad FRANCES 2021 2022Document13 pagesExamen Pruebas de Acceso A La Universidad FRANCES 2021 2022Andres HerreraPas encore d'évaluation
- 1901 Vierendeel. Stabilite Des Constructions. Tome III PDFDocument137 pages1901 Vierendeel. Stabilite Des Constructions. Tome III PDFmouradPas encore d'évaluation
- Club944 - Net - Injection Bosch L-JetronicDocument8 pagesClub944 - Net - Injection Bosch L-JetronicYann DaynatPas encore d'évaluation
- Corbin 1458816683Document1 pageCorbin 1458816683rodrigomichellPas encore d'évaluation
- Cahier de Poutres Bloc Administration 1Document8 pagesCahier de Poutres Bloc Administration 1Ourajim issamPas encore d'évaluation
- Avp Loi 67.15 FRDocument9 pagesAvp Loi 67.15 FRSerge KohemunPas encore d'évaluation
- Revenu 1357Document28 pagesRevenu 1357concombre2607Pas encore d'évaluation
- Protocole KINE PREOP Etude Pilote Sur La Préhabilitation Pulmonaire en Libéral Dans Le Cadre de La Chirurgie Thoracique Pulmonaire OncologiqueDocument103 pagesProtocole KINE PREOP Etude Pilote Sur La Préhabilitation Pulmonaire en Libéral Dans Le Cadre de La Chirurgie Thoracique Pulmonaire OncologiqueSelmaPas encore d'évaluation
- Nouveau Microsoft Word DocumentDocument3 pagesNouveau Microsoft Word DocumentIlyas BoutouahanPas encore d'évaluation
- Brand PriceDocument6 pagesBrand PriceBonnesAffairesConstantine100% (1)
- Chapitre 3 IRMPartie 3Document42 pagesChapitre 3 IRMPartie 3Khadhra LassouedPas encore d'évaluation
- Mouvements Plans Cours 1 2Document8 pagesMouvements Plans Cours 1 2kenza.elkansouriPas encore d'évaluation
- 1Document8 pages1Ladys Ruth Caballero PeluffoPas encore d'évaluation
- Bulletin Service Manilles 2013.02 (FR)Document3 pagesBulletin Service Manilles 2013.02 (FR)bestoff82100% (1)
- Rapport RFIDDocument29 pagesRapport RFIDed-fer666Pas encore d'évaluation
- Exo 18 Partitifs en LigneDocument1 pageExo 18 Partitifs en LigneMaria SousaPas encore d'évaluation
- Centre Universitaire Nour Bachir, El-Bayadh Institut Des Sciences 2ème Année Licence Génie Civil Exposé Écrit Pour Évaluation SemestrielleDocument8 pagesCentre Universitaire Nour Bachir, El-Bayadh Institut Des Sciences 2ème Année Licence Génie Civil Exposé Écrit Pour Évaluation SemestrielleMelek LakelPas encore d'évaluation
- Med 5an Cas Clinique1 GynecoDocument7 pagesMed 5an Cas Clinique1 GynecoIbtissem TissamPas encore d'évaluation
- 179 PDFDocument104 pages179 PDFaghilif100% (1)
- Coefficient K, Devis Estimatif, Quantitatif Et PlanificationDocument21 pagesCoefficient K, Devis Estimatif, Quantitatif Et PlanificationMarco JoyPas encore d'évaluation
- Notice de La Commande Numerique DSP BRAXESDocument11 pagesNotice de La Commande Numerique DSP BRAXESHassan HassanPas encore d'évaluation
- OEIL ROUGE ConstantineDocument45 pagesOEIL ROUGE Constantinemidou113Pas encore d'évaluation
- Wcms 183740Document4 pagesWcms 183740Bakaye DembelePas encore d'évaluation
- BrainstormingDocument4 pagesBrainstormingndeyadiop1203Pas encore d'évaluation
- Attachement Du ChantierDocument10 pagesAttachement Du ChantierOussamaBahloul100% (1)
- Video RO1Document39 pagesVideo RO1lovebooksPas encore d'évaluation