Académique Documents
Professionnel Documents
Culture Documents
Chap 5
Transféré par
ali akredTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Chap 5
Transféré par
ali akredDroits d'auteur :
Formats disponibles
Centre Universitaire de Ghardaïa 1ére S.N.
V: 2010-2011
CHAP. 5 : LA LIAISON CHIMIQUE
I/ Introduction
Les atomes n’existent que très rarement à l’état isolé (gaz rares, hydrogène), Ils s’associent pour
former des édifices plus stables que les atomes isolés, pouvant être soit des molécules, soit des
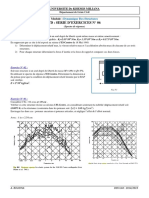
ions dans les cristaux. La fig.1 montre la variation de l’énergie totale qui intervient lorsque deux
atomes d’hydrogène se rapprochent, les orbitales1s de H
se rapprochent et se couvrent pour former un espace où
les électrons des deux atomes vont pouvoir se mouvoir.
L’apparition du recouvrement va provoquer la baisse
d’énergie du système jusqu’à une distance qu’on appelle 0,74 longueur de liaison
distance d’équilibre et ensuite la répulsion nucléaire va
prendre le dessus et l’énergie remonte pour devenir
répulsive. Le point correspondant à l’énergie la plus
basse est l’énergie de liaison de la molécule H2 : -436
436KJ/mol , la distance d’équilibre étant de 0.74 Å.
Diagramme d’énergie de H2
On distingue deux grandes catégories de liaisons chimiques :
- Des liaisons qu’on peut décrire par une mise en commun d’électrons (liaisons
covalentes et liaisons datives).
- Des liaisons qu’on peut décrire par le biais d’interactions électrostatiques entre charges
de signes opposés, telles que les liaisons ioniques et les liaisons intermoléculaires.
II / modèle de Lewis et la liaison covalente :
1) liaison covalente : la description la plus simple de la liaison covalente a été proposé par
LEWIS en 1915, la liaison entre deux atomes provient du partage (ou de la mise en commun de
deux électrons de valence)
a) covalence propre : chacun des deux atomes fournit un électron de sa couche externe occupant
seul une case quantique.
A• + •B A••B ou A-B
Exp1 : formation de la molécule Cl2:
17Cl : 1s2 2s2 2p6 3s2 3p5 couche externe
(diagramme de Lewis de Cl2) chaque atome de chlore est entouré par 8 électrons (la règle de
l’octet est respectée).
Exp2 : Formation de la molécule d’ammoniac NH3 :
7N : 1s2 2s2 2p3
1H: 1s1
b) Coordinance : Dans la liaison de coordination ou dative, l’un des atomes (le donneur) fournit
un doublet d’électrons de sa couche externe , l’autre (l’accepteur) reçoit le doublet dans une case
vide de sa couche externe.
A + ••B A••B ou A-B
Module: Chimie1 1 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
Exp : formation de l’ion ammonium à partir de l’ammoniac NH3
2) Electrons liants et non liants : Dans la molécule d’eau , l’oxygène possède deux doublets
liants et deux non liants : H••O••H ou H-O-H
3) Liaison multiples : Deux atomes peuvent mettre en commun plus d’un doublet électronique, ils
s’unissent par une liaison double (2 doublets) ou triple (3 doublets).
Exp : Molecule d’oxygène O2 : 8O : 1s2 2s2 2p4
monoxyde de carbone CO: 8O : 1s2 2s2 2p4
6C : 1s2 2s2 2p2 on a 2 liaisons et 1
Les deux ou trois liaisons n’ont pas des caractéristiques identiques, en particulier, il y correspond
des énergies de liaisons différentes. Les électrons qui assurent la liaison sont appelés électrons
, ceux de la liaison sont dits électrons .
Mode de formation de la liaison
Mode de formation de la liaison
Module: Chimie1 2 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
Exp ! Le diazote N2 (1 liaison + 2 liaisons )
Z Y
x: —
z: —
y: —
Recouvrement entre les orbitales 2p de deux atomes d’azote : N
4) Les états de valence :
6C: 1s2 2s2 2p2 possède deux électrons de valence impairs, donc devrait former deux liaisons
covalentes. Or le composé le plus simple formé à partir de C et H c’est le méthane CH4. Pour
pouvoir contracter les 4 liaisons, le carbone doit disposer de 4 électrons impairs, ce qui est obtenu
par l’état de valence (état excité de C)
6C : 1s2 2s2 2p2 6C* : 1s2 2s1 2p3
D’ou la structure du méthane:
Exp. Molécule de trichlorure de phosphore :PCl3
15P : [Ne] 3s2 3p3
Exp. Molécule de pentachlorure de phosphore :PCl5
15P* : [Ne] 3s1 3p3 3d1
Module: Chimie1 3 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
III ) Liaison ionique et liaison polarisée
1) Moment dipolaire, liaison polarisée
Lorsque deux atomes liés par covalence sont identiques tel que H2, Cl2… le doublet d’électrons
qu’ils ont en commun est partagé entre eux, l’ensemble du nuage électronique est symétrique et
équidistant des noyaux. Mais si les deux atomes ne sont pas les mêmes comme pour HCl, CO …,
l’un est plus électronégatif que l’autre, et il attire fortement le doublet électronique. Le nuage
électronique n’est plus symétrique, il est déplacé vers l’atome le plus électronégatif.
H-Cl
=q.d : moment dipolaire. (en Debye D) avec 1D=3,33 10-30 C.m
d : distance entre les deux noyaux (longueur de liaison en m)
Q : charge en coulomb C
Remarque : Si la liaison était 100 % ionique la charge q serait égale à la charge élémentaire e
on a ( =e.d ). Si la liaison était purement covalente 0 % ionique on a =0
On définit la caractère ionique tel que ; =(q/e).100
Composé Valeurs (XB-XA ) Caractère ionique
NaCl 3-0.9=2.1 67 %
KCl 3-0.8=2.2 92 %
NaF 4-0.9=3.1 70 %
Tableau renfermant les % ioniques de quelques sels
Le moment dipolaire d’une molécule polyatomique est la résultante des moments dipolaires des
liaisons polarisées entre atomes d’électronégativités différentes.
Exp : molécule d’eau H2O
H2o=2. OH .cos( /2) H OH
H2o=1.85D H2o O
/2=52.5° OH
H
donc OH =1.51 D (pour chaque liaison)
2) la liaison ionique
la liaison ionique s’établit entre deux éléments d’électronégativités différentes, telle que :
XB-XA>2, ce qui représente la force d’attraction qui lie l’ion A à l’ion B. Il y’a transfert d’électrons
de l’élément le moins électronégatif ver l’élément le plus électropositif et formation de deux ions :
A(cation) et B (anion) A• + •B A+ B-
Exp. Na. + Cl. Na+Cl-
Module: Chimie1 4 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
Comparaison des liaisons covalente et ionique
IV/ Niveaux énergétiques des O.M. : Méthode L.C.A.O
Dans le modèle ondulatoire de la liaison covalente, l’idée de mise en commun d’un doublet
électronique introduite par Lewis, se complète de celle du recouvrement de deux orbitales
atomiques qui se fusionnent pour donner une orbitale moléculaire. Ces O.M. sont solution de
l’équation de Schrödinger qui ne peut être résolue que dans des cas simples avec une méthode
d’approximation : L.C.A.O (combinaison linéaire des orbitales atomiques).
Dans le cas de H2, la résolution conduit à deux solutions possibles qui correspondent à deux
orbitales, l’une liante de basse énergie et l’autre anti liante de plus haute énergie.
1s
Diagramme énergétique de la molécule H2
* Pour établir la structure électronique des molécules à l’état fondamental, on place les électrons
dans les O.M. par ordre d’énergie croissante et à raison de deux électrons par OM au maximum,
(principe de Pauli).
* En soustrayant du nombre d’électrons liants le nombre d’électrons non liants, on obtient le
nombre d’électrons qui assurent effectivement la stabilité de la molécule.
* En divisant ce nombre par deux, on obtient l’ordre de liaison : O.L.=(nl-n*)/2
* Un O.L. élevé implique une forte liaison, un O.L nul implique la molécule ne se forme pas.
Exp : Formation de la molécule He2? E
OL=1/2(2-2)=0 donc He2 n’existe pas
Diagramme énergétique de la molécule He2
Module: Chimie1 5 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
Exp : l’oxygène O2
Structure électronique :
O2 : (1s )2 (1s *)2 (2s )2 (2s *)2(2p )2(2p )4(2p *)2
Ou encore :
O2 : ( 1s)2 ( *1s)2 2s)2 *2s)2 2pz)2( 2px)2( 2py)2
( *2x)1( *2y)1
Nombre d’e- liants=10
Nombre d’é- non liants=6
O.L.= (10-6) /2=2
Diagramme énergétique de la molécule O2
Remarque :
• une molécule est dite paramagnétique si elle possède au moins un électron célibataire
dans sa dernière O.M. Dans l’exemple ci-dessus : O2 possède deux électrons célibataires
donc elle est paramagnétique.
• Si l’atome B est plus électronégatif que A, l’énergie est plus basse au voisinage de B,
l’énergie des OM 2p devient supérieure à celle des OM 2p ,le diagramme énergétique
devient comme suit :
Diagramme énergétique en cas où les 2
atomes ont des électronégativités différentes
V/ Liaisons intermoléculaires
Entre les molécules existent des liaisons qui assurent la cohésion de la matière. Ces liaisons sont
de nature électrostatiques comme les liaisons interatomiques, mais d’énergie beaucoup plus
faibles. On distingue : les liaisons de Van Der Waals et les liaisons hydrogène.
Module: Chimie1 6 Prof: HADJ SEYD AEK
Centre Universitaire de Ghardaïa 1ére S.N.V: 2010-2011
1) Liaisons de Van Der Waals :
Elles résultent de l’interaction des électrons d’une molécule par les noyaux des molécules
voisines. Elles sont faibles (El<10 KJ/mol et de longueur de liaison variant entre 0,3 et 0,5 nm).
2) Liaison Hydrogène :
L’Hydrogène lié à un atome ayant une électronégativité très élevée est capable de former une
deuxième liaison avec un autre atome fortement électronégatif d’une autre molécule. Cette liaison
dipôle-dipôle entre molécules par pont hydrogène est appelé liaison hydrogène. C’est une
liaison de type Van Der Waals, mais beaucoup plus énergétique.
- + -
X H Y
La liaison hydrogène permet d’expliquer certaines propriétés physiques tel que la température
d’ébullition, température de fusion, chaleur de changement d’état …
Par exemple l’eau a une température d’ébullition plus élevée compte tenu de sa faible masse
moléculaire, le passage de l’eau à l’état de vapeur nécessite la rupture des liaisons H. Ce qui
impose un apport d’énergie important donc une Teb élevée.
Remarque : La liaison H peut se former entre deux groupements fonctionnels d’une même
molécule : C’est la liaison hydrogène intramoléculaire.
Module: Chimie1 7 Prof: HADJ SEYD AEK
Vous aimerez peut-être aussi
- Fermions: Les Grands Articles d'UniversalisD'EverandFermions: Les Grands Articles d'UniversalisPas encore d'évaluation
- La Liaison Chimique 2020 2021Document16 pagesLa Liaison Chimique 2020 2021ayachelayanePas encore d'évaluation
- 06-La Liaison Chimique 2020-2021Document13 pages06-La Liaison Chimique 2020-2021Walid AzzamPas encore d'évaluation
- Chapitre 05 Liaisons ChimiquesDocument17 pagesChapitre 05 Liaisons Chimiquesامين لتصميم الديكوراتPas encore d'évaluation
- Chap 1 Liaison Covalente - Théorie de LewisDocument68 pagesChap 1 Liaison Covalente - Théorie de Lewisyassineredone4Pas encore d'évaluation
- Université Des Sciences Et Département de Chimie Techniques de Masuku Faculté Des SciencesDocument19 pagesUniversité Des Sciences Et Département de Chimie Techniques de Masuku Faculté Des SciencesRene VoumaPas encore d'évaluation
- Cours de Liaison Chimique EtudiantsDocument50 pagesCours de Liaison Chimique EtudiantsAnge PastoréPas encore d'évaluation
- Chapitre 5Document12 pagesChapitre 5Imane EmyPas encore d'évaluation
- Cours - Liaison - Chim ChapI - II - ElalemDocument18 pagesCours - Liaison - Chim ChapI - II - ElalemFatima EL AROUSSIPas encore d'évaluation
- 2 - Liaisons ChimiquesDocument58 pages2 - Liaisons ChimiquesIvan LikkasPas encore d'évaluation
- Cours de Liaison Chimique NewDocument47 pagesCours de Liaison Chimique Newwww.doukoureabdoulaye1Pas encore d'évaluation
- Cours de Liaison Chimique NewDocument45 pagesCours de Liaison Chimique NewJean Emmanuel BlehouePas encore d'évaluation
- Cours Chimie Organique SMC-S3-2020-2021 (Partie1)Document44 pagesCours Chimie Organique SMC-S3-2020-2021 (Partie1)MOHAMED MAZOUARIPas encore d'évaluation
- Cours Chimie Organique SMC S3 2020 2021Document98 pagesCours Chimie Organique SMC S3 2020 2021MOHAMED MAZOUARIPas encore d'évaluation
- Chimie - Chapitre VDocument15 pagesChimie - Chapitre Vmahjoub lachgarPas encore d'évaluation
- La Liaison Chimique2021Document26 pagesLa Liaison Chimique2021Fai RouzPas encore d'évaluation
- Chapitre VIDocument79 pagesChapitre VIYouCeF MouiSsiPas encore d'évaluation
- ChapV AtomistiqueDocument13 pagesChapV AtomistiqueAbdessamad ErraouiPas encore d'évaluation
- Chap IIDocument9 pagesChap IILengani Kader EvaricePas encore d'évaluation
- La Liaison Chimique 01Document26 pagesLa Liaison Chimique 01Nouh FouhalPas encore d'évaluation
- Chapitre 5 Ing Les Liaisons ChimiquesDocument17 pagesChapitre 5 Ing Les Liaisons ChimiquesIslem BensalemPas encore d'évaluation
- El-Handout 2 CHM212 PDFDocument28 pagesEl-Handout 2 CHM212 PDFWajih AbboudPas encore d'évaluation
- Chm161 Chapitre 1 KodomDocument14 pagesChm161 Chapitre 1 KodomstanPas encore d'évaluation
- Cours IntroductionCHODocument15 pagesCours IntroductionCHOrima.lettreuchPas encore d'évaluation
- Fichier Produit 2114Document52 pagesFichier Produit 2114FlorinaPas encore d'évaluation
- Cours Chimie Quantique - Chapitre 6 PDFDocument7 pagesCours Chimie Quantique - Chapitre 6 PDFEfreme pepin BilePas encore d'évaluation
- Cours introductionCHODocument15 pagesCours introductionCHOrima.lettreuchPas encore d'évaluation
- UE CHM 131 Liaisons Chimiques - Pdfue CHM 131 Liaisons ChimiquesDocument20 pagesUE CHM 131 Liaisons Chimiques - Pdfue CHM 131 Liaisons ChimiquesWildPas encore d'évaluation
- Chapitre 8Document15 pagesChapitre 8khalilkbdzPas encore d'évaluation
- 5 Chapitre V Les Liaisons Chimiques CompressedDocument17 pages5 Chapitre V Les Liaisons Chimiques CompressedAnas KhaldiPas encore d'évaluation
- Chapitre 1 Introduction Et Modèle de LEWISDocument58 pagesChapitre 1 Introduction Et Modèle de LEWISYassine AarabPas encore d'évaluation
- 2 SC C2Document2 pages2 SC C2Hanine HmidaPas encore d'évaluation
- Laisson Chimiques SMPC S2Document37 pagesLaisson Chimiques SMPC S2Saidi AbdelghaniPas encore d'évaluation
- 2 - Liaisons Orbitales Et MoléculaireDocument12 pages2 - Liaisons Orbitales Et MoléculaireDeadshot xx (ReyoxDZ)Pas encore d'évaluation
- TD 4Document4 pagesTD 4Peter Banks100% (1)
- Cours Chimie OrganiqueDocument60 pagesCours Chimie OrganiqueFarah BahriPas encore d'évaluation
- Structure Électronique #1Document7 pagesStructure Électronique #1Nursalwani SABDANIPas encore d'évaluation
- ch12 Transform Chim Orga MicroDocument4 pagesch12 Transform Chim Orga Microtaoufik akabliPas encore d'évaluation
- Cours Réactions ChimiquesDocument19 pagesCours Réactions ChimiquesSamuel BaneckPas encore d'évaluation
- CHIMIE Seconde SDocument8 pagesCHIMIE Seconde Stoto TOTOROTOPas encore d'évaluation
- BTS CPI 1 CH 2 Edifices Moléculaires Et IoniquesDocument5 pagesBTS CPI 1 CH 2 Edifices Moléculaires Et IoniquesLucas Filipuzzi100% (4)
- Cours de Liaisons Chimiques Complet BG L1-S1Document110 pagesCours de Liaisons Chimiques Complet BG L1-S1honorehien04Pas encore d'évaluation
- REVISION Chimie Orga Ecole (Enregistrement Automatique)Document28 pagesREVISION Chimie Orga Ecole (Enregistrement Automatique)Charaf SekhsoukhPas encore d'évaluation
- Trouver Le Schema de Lewis MoleculesDocument8 pagesTrouver Le Schema de Lewis MoleculesRita AkoumePas encore d'évaluation
- SArie Liaison 20202 2023Document2 pagesSArie Liaison 20202 2023Serine LaraPas encore d'évaluation
- Chapitre I - Modèle de LewisDocument6 pagesChapitre I - Modèle de Lewisadnanwww16Pas encore d'évaluation
- UE1 Chimie 2 NomenclatureDocument19 pagesUE1 Chimie 2 Nomenclaturesun-nee-chan9Pas encore d'évaluation
- Chap2 - EC1 - CHM131 - Liaisons Chimiques - 2022 - ONDocument85 pagesChap2 - EC1 - CHM131 - Liaisons Chimiques - 2022 - ONDylanPas encore d'évaluation
- Partie 3Document27 pagesPartie 3ngm4tg2hgcPas encore d'évaluation
- Cours Chimie oDocument26 pagesCours Chimie oAy Ou ChaPas encore d'évaluation
- Réactions Électrochimiques Et Courbes Intensité - Potentiel: I) Definitions Generales I-1 ElectrodeDocument47 pagesRéactions Électrochimiques Et Courbes Intensité - Potentiel: I) Definitions Generales I-1 ElectrodemugiPas encore d'évaluation
- Chimie Organique - Cours EpoDocument236 pagesChimie Organique - Cours EpoMohamed Salim CompaorePas encore d'évaluation
- Liaisons ChimiquesDocument28 pagesLiaisons ChimiquesMamineTecDelmaPas encore d'évaluation
- Effets Electroniques PDFDocument14 pagesEffets Electroniques PDFmohsatPas encore d'évaluation
- 3-Les MoléculesDocument47 pages3-Les MoléculeslilybarachantPas encore d'évaluation
- Atomistique Exercices Corriges 06 - CompressedDocument4 pagesAtomistique Exercices Corriges 06 - CompressedJean SoroPas encore d'évaluation
- C5 Structures et polarités eleveDocument6 pagesC5 Structures et polarités elevefabiosaturnePas encore d'évaluation
- Représentation D'une MoléculeDocument7 pagesReprésentation D'une MoléculeGericault IfoaratianaPas encore d'évaluation
- Liaison Chimique Partie I V 14 Déc 2020.ppDocument47 pagesLiaison Chimique Partie I V 14 Déc 2020.ppmamecheikhgaye5Pas encore d'évaluation
- TD DDS S04-2014 - 2015 PDFDocument1 pageTD DDS S04-2014 - 2015 PDFali akredPas encore d'évaluation
- Compte Rendu TP: Département de Génie Mécanique Master 1: Construction MécaniqueDocument1 pageCompte Rendu TP: Département de Génie Mécanique Master 1: Construction Mécaniqueali akredPas encore d'évaluation
- Compte Rendu TP: TPN° 02:l'essai de Torsion Module: TP RDMDocument7 pagesCompte Rendu TP: TPN° 02:l'essai de Torsion Module: TP RDMali akredPas encore d'évaluation
- TP - rdm-1 FlexDocument6 pagesTP - rdm-1 Flexali akredPas encore d'évaluation
- TD DDS 01 - 2018 PDFDocument1 pageTD DDS 01 - 2018 PDFali akredPas encore d'évaluation
- TD DDS S01-2014 - 2015 PDFDocument1 pageTD DDS S01-2014 - 2015 PDFali akredPas encore d'évaluation
- TD DDS S05-2014 - 2015Document1 pageTD DDS S05-2014 - 2015ali akredPas encore d'évaluation
- TD DDS S06-2014 - 2015Document3 pagesTD DDS S06-2014 - 2015ali akredPas encore d'évaluation
- TD DDS S03-2014 - 2015Document1 pageTD DDS S03-2014 - 2015ali akredPas encore d'évaluation
- Chap 3Document7 pagesChap 3ali akredPas encore d'évaluation
- TD DDS S02-2014 - 2015Document1 pageTD DDS S02-2014 - 2015ali akredPas encore d'évaluation
- Examen Corrigé Dynamique Des Structures M1 PDFDocument8 pagesExamen Corrigé Dynamique Des Structures M1 PDFSergio Rodríguez50% (4)
- Dyn Struct - C01 - Vibration Libre PDFDocument28 pagesDyn Struct - C01 - Vibration Libre PDFali akredPas encore d'évaluation
- GC 2017 Mvoa M1 S1 GV712Document5 pagesGC 2017 Mvoa M1 S1 GV712Talbi Mohammed Abdallah0% (1)
- Chap 4Document6 pagesChap 4ali akredPas encore d'évaluation
- DDS L3 Révision SEP2020Document24 pagesDDS L3 Révision SEP2020ali akredPas encore d'évaluation
- Chap 6Document5 pagesChap 6ali akredPas encore d'évaluation
- Amélioration de L'efficacité de Turbines À Gaz Dans L'industrieDocument6 pagesAmélioration de L'efficacité de Turbines À Gaz Dans L'industriebananosnetPas encore d'évaluation
- Chap 1Document3 pagesChap 1عبد الحميدPas encore d'évaluation
- Caract Mouvmt EXO Ennonc SDocument2 pagesCaract Mouvmt EXO Ennonc SzakiPas encore d'évaluation
- Cours CinematiqueDocument19 pagesCours Cinematiqueoussama22Pas encore d'évaluation
- Chap 2Document4 pagesChap 2ali akredPas encore d'évaluation
- La Viscosité PDFDocument15 pagesLa Viscosité PDFDi SecrètePas encore d'évaluation
- 3-Dynamique Du Point PDFDocument6 pages3-Dynamique Du Point PDFali akredPas encore d'évaluation
- Chapitre2 2Document18 pagesChapitre2 2Ibrahim AmichlaPas encore d'évaluation
- Tude de La Pollution de L'eau Souterraine de La Ville de Niamey, NigerDocument5 pagesTude de La Pollution de L'eau Souterraine de La Ville de Niamey, Nigerali akredPas encore d'évaluation
- I-2. Ressources en Eau Souterraine Et Relations Avec Le Lac: D. D, G. FDocument22 pagesI-2. Ressources en Eau Souterraine Et Relations Avec Le Lac: D. D, G. Fali akredPas encore d'évaluation
- Carte Des Ressources en Eau Souterraine de La Tunisie: Feuille De. Ïhala N 10Document24 pagesCarte Des Ressources en Eau Souterraine de La Tunisie: Feuille De. Ïhala N 10ali akredPas encore d'évaluation
- Gisements Petroles PDFDocument11 pagesGisements Petroles PDFali akredPas encore d'évaluation
- Edgalilee TH 2016 Ben AliDocument223 pagesEdgalilee TH 2016 Ben Alimahjouba amgounePas encore d'évaluation
- 1.B.Liaisons AtomiquesDocument16 pages1.B.Liaisons AtomiquesOmar GhPas encore d'évaluation
- Phenomènes Météorologiques SignificatifsDocument48 pagesPhenomènes Météorologiques SignificatifsMouhamadouPas encore d'évaluation
- Azolla FiliculoidesDocument6 pagesAzolla FiliculoidesSylva MalindaPas encore d'évaluation
- D'où Viennent Les NuagesDocument5 pagesD'où Viennent Les NuagesKhoa NguyenPas encore d'évaluation
- Correction Tp2iemlnewtonDocument4 pagesCorrection Tp2iemlnewtonMaryam YammPas encore d'évaluation
- Les Grandeurs Liées À La Quantité de MatièreDocument2 pagesLes Grandeurs Liées À La Quantité de MatièreHoda hodatiPas encore d'évaluation
- 2008C CorrigeDocument16 pages2008C CorrigeZakaria AIT EL CAIDPas encore d'évaluation
- Bilan 2 Les Atouts de L'electricitéDocument3 pagesBilan 2 Les Atouts de L'electricitéfeliponsio48Pas encore d'évaluation
- Présentation Au CCPS Du 14102022Document40 pagesPrésentation Au CCPS Du 14102022jeanostwindPas encore d'évaluation
- MEMOIRE Samer MoussaDocument94 pagesMEMOIRE Samer Moussatoni JabbourPas encore d'évaluation
- Tahar Neffati-Introduction À L'électronique Analogique - Cours Et Exercices CorrigésDocument258 pagesTahar Neffati-Introduction À L'électronique Analogique - Cours Et Exercices CorrigésRiadh Bachrouch67% (3)
- Section 1-Module4 (Roches)Document24 pagesSection 1-Module4 (Roches)PAPas encore d'évaluation
- Cours Chaine TrophiqueDocument83 pagesCours Chaine TrophiqueKodji n'cho Guy StephanePas encore d'évaluation
- Rapport Four Solaire PDFDocument37 pagesRapport Four Solaire PDFmâ wàf100% (1)
- Ernst Schmidt VDI (Auth.) - VDI-Wasserdampftafeln - VDI-Steam Tables - Tables VDI Des Constantes de La Vapeur D'eau - Mit Einem Mollier (I, S)Document119 pagesErnst Schmidt VDI (Auth.) - VDI-Wasserdampftafeln - VDI-Steam Tables - Tables VDI Des Constantes de La Vapeur D'eau - Mit Einem Mollier (I, S)anass anasPas encore d'évaluation
- Rapport P6 2017 17Document46 pagesRapport P6 2017 17Afkir HamzaPas encore d'évaluation
- Chimie Électrochimie Résumés de Cours Et Exercices Corrigés Niveau A Télécharger, Lire PDFDocument7 pagesChimie Électrochimie Résumés de Cours Et Exercices Corrigés Niveau A Télécharger, Lire PDFjello100% (9)
- FeuilletageDocument30 pagesFeuilletageErrahaPas encore d'évaluation
- Exercices Supplémentaires Sur Le Chapitre 1Document2 pagesExercices Supplémentaires Sur Le Chapitre 1ben binah100% (3)
- La Biomasse Memoire 1 PDFDocument16 pagesLa Biomasse Memoire 1 PDFEn Zo80% (5)
- BG Epreuve Anticipee Francais ES S 2018Document7 pagesBG Epreuve Anticipee Francais ES S 2018LETUDIANT100% (1)
- Recherche & Développement Sujet 3 Etude Sur Les Séchoirs SolairesDocument17 pagesRecherche & Développement Sujet 3 Etude Sur Les Séchoirs SolairesSalim DoumbiaPas encore d'évaluation
- Microsonde ÉlectroniqueDocument12 pagesMicrosonde ÉlectroniqueKacem Hanoun100% (1)
- 13167710A03-024-ARF SANOFI v8.0Document85 pages13167710A03-024-ARF SANOFI v8.0Serge RINAUDOPas encore d'évaluation
- Cahier D'activité 3APIC 2022 - 2023Document94 pagesCahier D'activité 3APIC 2022 - 2023ASMA AHARTAFPas encore d'évaluation
- Transfo PsimDocument13 pagesTransfo PsimParfumerie Actu'EllePas encore d'évaluation
- Les Facteurs ClimatiquesDocument5 pagesLes Facteurs ClimatiquesSere100% (2)
- TD AcvDocument3 pagesTD AcverikwedPas encore d'évaluation
- Transition ÉnergétiqueDocument3 pagesTransition ÉnergétiqueIkram MouhibPas encore d'évaluation