Académique Documents
Professionnel Documents
Culture Documents
Carbonyl Es 2
Transféré par
جعدبندرهمCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Carbonyl Es 2
Transféré par
جعدبندرهمDroits d'auteur :
Formats disponibles
© Thierry Ollevier Chimie organique II CHM-2000
RÉACTIVITÉ DU GROUPEMENT CARBONYLE
6. Acétals
RO OR RO OR
R1 H R1 R2
Acétal dérivé d'un aldéhyde Acétal dérivé d'une cétone
O
RO OR
+ 2 ROH + H 2O
R1 H R1 H
!
Aldéhyde Acétal
O
RO OR
+ 2 ROH + H 2O
R1 R2 R1 R2
!
Cétone Acétal
Caractéristiques
- Les acétals sont formés en milieu acide.
- Les acétals sont stables en milieu basique.
- Les acétals, contrairement aux hémiacétals, sont des composés
isolables (stables).
carbonyles-21 2016-01-12 15:45
© Thierry Ollevier Chimie organique II CHM-2000
Mécanisme de formation de l'acétal (en milieu acide !)
O
H+ RO OR
+ 2 ROH + H 2O
R1 H R1 H
H
O
R1 H
H H H
O O O
H+ R H
O O
R
R1 H R1 H R1 H
R H
O + H+
O O O O
H R H R
- H 2O
R1 H R1 H R1 H
R H H
O O
O O O O
R R R R R
R1 H R1 H R1 H
carbonyles-22 2016-01-12 15:45
© Thierry Ollevier Chimie organique II CHM-2000
Commentaires
– La formation de l'acétal s'effectue via la formation d'un hémiacétal.
– Un hémiacétal peut être formé en conditions basiques ou acides
mais pour passer de l'hémiacétal à l'acétal il faut se trouver en milieu
acide (car l'acétal ne peut se former qu'en conditions acides).
Illustration
Le groupe hydroxyle doit pouvoir être protoné pour pouvoir passer
de l'hémiacétal à l'acétal.
H R
O O O
H R + H+ O O
H R
R1 H
- H 2O R1 H
R1 H
ROH
O O
R R
R1 H
carbonyles-23 2016-01-12 15:47
© Thierry Ollevier Chimie organique II CHM-2000
Commentaires (suite)
– La formation de l'acétal s'effectue en présence de quantités
catalytiques d'acide.
– La réaction est globalement équilibrée (toutes les étapes sont
réversibles) mais l'équilibre pourra être déplacé du côté droit en
ajoutant un excès d'alcool et/ou en enlevant l'eau.
Illustration
O
H+ RO OR
+ 2 ROH + H 2O
R1 H R1 H
- quantité catalytique d'acide
- excès de ROH
- H 2O enlevée du milieu réactionnel (par distillation)
O
H+ RO OR
+ 2 ROH + H 2O
R1 H R1 H
- quantité catalytique d'acide
- excès de H 2O
- H 2O laissée dans le milieu réactionnel
carbonyles-24 2016-01-12 15:48
© Thierry Ollevier Chimie organique II CHM-2000
Exemples
O
H+ EtO OEt
+ 2 EtOH + H 2O
H 3C CH3 H 3C CH3
O
MeO OMe
H+
+ 2 MeOH + H 2O
H+ = HCl gazeux (anhydre)
ou
H 2SO 4 concentré (anhydre)
carbonyles-25 2016-01-12 15:49
© Thierry Ollevier Chimie organique II CHM-2000
Acétals cycliques
O HO O
H+
+ + H 2O
H O
HO H
HO O
O H+
+ + H 2O
O
HO
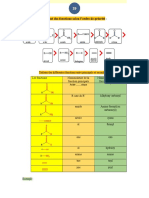
Acétals cycliques
La formation des acétals cycliques (réaction du dérivé carbonylé avec
1 molécule de diol) est favorisée par rapport à la formation des acétals
non cycliques (réaction du dérivé carbonylé avec 2 molécules d'alcool).
Cl Cl
N
N O O
N
propiconazole
fongicide
carbonyles-26 2016-01-12 15:49
© Thierry Ollevier Chimie organique II CHM-2000
Réaction inverse d'hydrolyse des acétals
Etant donné :
O
H+ RO OR
+ 2 ROH + H 2O
R1 H R1 H
- quantité catalytique d'acide
- excès de H 2O
- H 2O laissée dans le milieu réactionnel
Cela indique donc qu'un acétal est hydrolysé en dérivé carbonylé en
présence d'acide aqueux.
O
RO OR H+
+ 2 ROH
H 2O
R1 H R1 H
Cela implique qu'un dérivé carbonylé peut être masqué
temporairement en acétal puis être reconverti par la suite en dérivé
carbonylé.
O ROH H 2O O
RO OR
H+ H+
- H 2O
R1 H R1 H R1 H
excès d'alcool excès d'eau
acide anhydre en quantité catalytique acide aqueux en quantité catalytique
carbonyles-27 2016-01-12 15:50
© Thierry Ollevier Chimie organique II CHM-2000
☞ Problèmes : 16.9, 16.10 (dans Solomons)
☞ Problèmes complémentaires :
1) O
CH3OH en excès
?
KOH aqueux
Me
2) O
CH3OH en excès
?
H 2SO 4 concentré
Me
3) O
+ HO H+ ?
HO
4) OH O
réactif ?
H+
O
OH
carbonyles-28 2016-01-12 15:52
© Thierry Ollevier Chimie organique II CHM-2000
Solutions aux problèmes :
1) O
HO OCH3
CH3OH en excès
KOH aqueux
Me Me
L'équilibre est complètement déplacé vers la gauche. Globalement,
il n'y a pas de réaction : l'hémiacétal ne peut pas être isolé.
2) O
H 3CO OCH3
CH3OH en excès
H 2SO 4 concentré
Voir mécanisme détaillé dans les notes de cours.
Me Me
3) O
+ HO H+
O O
HO
via :
H
HO O HO O
HO HO
carbonyles-29 2017-01-27 08:15
© Thierry Ollevier Chimie organique II CHM-2000
+ H+
H
O
A
H O O
HO
HO
HO O
O O O
H
H H
- H+
HO O
O O
Ne se fait pas car très peu tendance à faire un
cation secondaire de ce type ! :
La formation du cation A est bien plus favorisée !
4) OH O
O
H+
O
OH
carbonyles-30 2016-01-12 15:56
© Thierry Ollevier Chimie organique II CHM-2000
Transacétalisation
O RO OR O
RO OR H+
+ +
R1 R2 R3 R4 R1 R2 R3 R4
"Transfert" de la fonction acétal d'un composé carbonylé à un autre
(synthèse d'un acétal, donc conditions anhydres obligatoires)
O MeO OMe
O
MeO OMe
+ +
HCl anhydre
H Me H H H
O O O
MeO OMe H+ MeO OMe MeO OH MeO OH
+ + +
MeOH MeOH H+
H 2O
+
H H Me H
H
O O HO OMe HO OMe O MeO OMe MeO OMe
H+
+
H+
Exercices types
O EtO OEt
O
1) EtO OEt HCl(g)
+ +
O HCl(g) O
O O O
2) O
H H
3) HCl (g)
O HO O
O
OH
carbonyles-31.cdx 2016-01-12 16:31
© Thierry Ollevier Chimie organique II CHM-2000
✎ Rappel mécanistique : activation par un acide de Lewis
De même que l'activation d'un carbonyle par un acide protique se passe
par le mécanisme suivant :
H H
O O O
H
R1 H R1 H R1 H
l'activation d'un carbonyle par un acide de Lewis se passe par le mécanisme similaire
AL AL
O O O
AL
R1 H R1 H R1 H
AL = acide de Lewis
AL AL
O O O
AL
R1 H R1 H R1 H
carbonyles-32 2016-01-12 17:52
© Thierry Ollevier Chimie organique II CHM-2000
✎ Rappel mécanistique : activation par un acide de Lewis
Dans le cas de la formation d'un acétal catalysée par un acide de Lewis :
O
AL RO OR
+ 2 ROH + H 2O
R1 H R1 H
BF 3
si AL = BF 3, le mécanisme O
pourrait être :
R1 H
BF 3 H H
O O O
BF 3 O O
R F 3B R
R1 H R1 H R1 H
-H
R H
O + H+
O O O O
F 3B R F 3B R
R1 H R1 H R1 H
R H H
O O
O O O O
R R R R R
R1 H R1 H R1 H
carbonyles-33 2016-01-12 17:53
© Thierry Ollevier Chimie organique II CHM-2000
RÉACTIVITÉ DU GROUPEMENT CARBONYLE
7. Thioacétals
RS SR
R1 R2
(R1 et/ou R 2 peuvent être un/des H)
O
Acide H 3CS SCH 3
+ 2 CH3SH + H 2O
R1 R2 R1 R2
Thioacétal
O
Acide S S
+ 1 + H 2O
R1 R2 HS SH R1 R2
Thioacétal
cyclique
Caractéristiques
- Les thioacétals sont les analogues soufrés des acétals. Ils sont
formés par un mécanisme similaire (carbonyle activé préalablement
par un acide).
- La formation des thioacétals est catalysée par un acide (acide
protique ou acide de Lewis comme ZnCl2 ou BF 3).
- Les thioacétals, tout comme les acétals, constituent souvent des
groupements protecteurs du dérivé carbonylé de départ.
carbonyles-34 2016-01-12 17:53
© Thierry Ollevier Chimie organique II CHM-2000
S S
H 3C CH3
responsable de l'odeur des truffes noires
Exemple
O HS SH
HO
BF 3•Et 2O
OH OH
S
HO
OH OH S
intermédiaire important
dans la synthèse de l'Aplasmomycine
carbonyles-35 2016-01-12 17:53
© Thierry Ollevier Chimie organique II CHM-2000
REACTIVITE DU GROUPEMENT CARBONYLE
8. Dérivés d'amines
Addition des nucléophiles de type R-NH 2
O R
H
N
+ N + H 2O
R1 R2 H R
R1 R2
Mécanisme
! étape d'addition
! étape d'élimination
carbonyles-36 2016-01-12 17:53
© Thierry Ollevier Chimie organique II CHM-2000
RÉACTIVITÉ DU GROUPEMENT CARBONYLE
Différents nucléophiles de type amine, hydroxylamine, hydrazines,... :
H H H
N N N
H R H H OH
amine phénylamine hydroxylamine
H H H
N N N
H NH 2 H NH H NH
NO 2
NO 2
hydrazine phénylhydrazine 2,4-dinitrophénylhydrazine
A noter au niveau de l'électrophile :
les aldéhydes réagissent beaucoup plus vite que les cétones.
carbonyles-37 2016-01-12 17:54
© Thierry Ollevier Chimie organique II CHM-2000
Réaction avec les amines primaires
R
O H N
+ N + H 2O
R1 R2 H R R1 R2
amine imine ("base de Schiff")
Ph Ph
N N
H 3C H H 3C H
imine E imine Z
Réaction avec l'hydroxylamine
OH
O H N
+ N + H 2O
R1 R2 H OH R1 R2
hydroxylamine oxime
OH HO
N N
H 3C H H 3C H
oxime E oxime Z
carbonyles-38 2016-01-12 17:54
© Thierry Ollevier Chimie organique II CHM-2000
Réaction avec les hydrazines
NH 2
O H N
+ N + H 2O
R1 R2 H NH 2 R1 R2
hydrazine hydrazone
Ph
N
O H N H
+ N Ph + H 2O
R1 R2 H N R1 R2
H
phénylhydrazine phénylhydrazone
NO 2
NO 2
NO 2 N
O H N H
+ N + H 2O
R1 R2 H N R1 R2
H NO 2
dinitrophénylhydrazine dinitrophénylhydrazone
carbonyles-39 2016-01-12 17:54
© Thierry Ollevier Chimie organique II CHM-2000
Réaction avec la semicarbazide
H
H N NH 2
O H N NH 2 N
N
+ + H 2O
O
R1 R2 H O R1 R2
semicarbazide semicarbazone
Remarques
- Les oximes, hydrazones, semicarbazones, ... sont souvent des
produits solides dont le point de fusion permet souvent
l'identification des aldéhydes ou cétones de départ.
- Rappel : les aldéhydes et les cétones sont condensés avec les
amines primaires (RNH 2) et fournissent des imines.
Condensation avec une amine secondaire (R 2NH)
R1
amine
N secondaire
H R2
O N
+
N
H
énamine
carbonyles-40 2016-01-12 17:54
Vous aimerez peut-être aussi
- Signet Fonctions OrganiquesDocument1 pageSignet Fonctions OrganiquesSab 433Pas encore d'évaluation
- Orga 15Document3 pagesOrga 15Ishak NkttPas encore d'évaluation
- Orga 6Document11 pagesOrga 6Romain Laher100% (1)
- Doc1 CarboxylesDocument4 pagesDoc1 CarboxylesDominique LoeuilletPas encore d'évaluation
- Chimie OrganiqueDocument117 pagesChimie OrganiqueIbrahimaPas encore d'évaluation
- Orga 9Document14 pagesOrga 9SalahPas encore d'évaluation
- CombinepdfDocument6 pagesCombinepdfINFINITY & BEYONDPas encore d'évaluation
- Chap 2, AlcènesDocument8 pagesChap 2, AlcènesChTri LyricsPas encore d'évaluation
- U7orgaanacs2 02Document3 pagesU7orgaanacs2 02Daniel NdPas encore d'évaluation
- Reaction D'oxydationDocument53 pagesReaction D'oxydationFa TehPas encore d'évaluation
- Ester If Ication 2020Document4 pagesEster If Ication 2020anwarPas encore d'évaluation
- Complement de Cours Chap2. Isomerie Et Stereoisomerie PDFDocument30 pagesComplement de Cours Chap2. Isomerie Et Stereoisomerie PDFMorel TegangPas encore d'évaluation
- Chap2 Aldéhydes Et CétonesDocument34 pagesChap2 Aldéhydes Et CétonesEssemlali Abde SamadPas encore d'évaluation
- U4orgaanas1 00cDocument2 pagesU4orgaanas1 00cEssamiPas encore d'évaluation
- IChO1-Structure de La Matière - CorrigéDocument2 pagesIChO1-Structure de La Matière - CorrigéDominique LoeuilletPas encore d'évaluation
- Chap9coursaldéhyde PDFDocument14 pagesChap9coursaldéhyde PDFChedly TrimechPas encore d'évaluation
- Chimie Oraganique 2 SMC4Document126 pagesChimie Oraganique 2 SMC4Yc YacinePas encore d'évaluation
- Wa0006Document135 pagesWa0006Yc Yacine100% (1)
- 2021 03 Metro Sujet1 ExoA ChouRouge 5ptsDocument2 pages2021 03 Metro Sujet1 ExoA ChouRouge 5ptsClémentine TakumiPas encore d'évaluation
- TD Polymère 3Document4 pagesTD Polymère 3mostafa bounabPas encore d'évaluation
- Cours Chapitre 1 - BiomoléculesDocument13 pagesCours Chapitre 1 - BiomoléculesGrace MM.Pas encore d'évaluation
- Barbi Turi QuesDocument9 pagesBarbi Turi QuesmatPas encore d'évaluation
- Cour Sur Les EnolsDocument13 pagesCour Sur Les EnolsZino ZindinPas encore d'évaluation
- Aromatique S 2Document20 pagesAromatique S 2HâmŽą LãyaÇhïPas encore d'évaluation
- 2021 03 Metro Sujet1 ExoA ChouRouge 5pts CorrectionDocument3 pages2021 03 Metro Sujet1 ExoA ChouRouge 5pts CorrectionClémentine TakumiPas encore d'évaluation
- Examen 20141 SDocument7 pagesExamen 20141 SElbachaPas encore d'évaluation
- ANTIÉPILEPTIQUESDocument35 pagesANTIÉPILEPTIQUESTidjouguena Mawena CasimirPas encore d'évaluation
- GCRO Condensation (Suite) Réaction de WittigCatalyseur de Transfert de PhaseDocument45 pagesGCRO Condensation (Suite) Réaction de WittigCatalyseur de Transfert de PhaseOussama BajaddaPas encore d'évaluation
- Cours CoumarineDocument12 pagesCours CoumarineM.B. IsmailPas encore d'évaluation
- Chapitre 5 - PhénolsDocument8 pagesChapitre 5 - PhénolsBeatrice Florin100% (1)
- Condensation AldoliqueDocument20 pagesCondensation AldoliqueZorgani TarekPas encore d'évaluation
- Chimie-Organique Cor CH4 PDFDocument9 pagesChimie-Organique Cor CH4 PDFCatherine DebeiPas encore d'évaluation
- TD Biochimie FEVDocument52 pagesTD Biochimie FEVAbdou SaiPas encore d'évaluation
- Chap4 OrganiqueDocument19 pagesChap4 OrganiqueMostafa McafsPas encore d'évaluation
- Tanins 2020 PDFDocument93 pagesTanins 2020 PDFKhaled Rahmani100% (1)
- Aldéhydes Et CétonesDocument34 pagesAldéhydes Et Cétonesatika benslimanePas encore d'évaluation
- Activité 4 IbuprofèneDocument4 pagesActivité 4 IbuprofèneDiego Alves SilvaPas encore d'évaluation
- Chapitre 5 Les AlcoolsDocument7 pagesChapitre 5 Les AlcoolsBeatrice Florin100% (6)
- Ch7 Composes Halogenes&OrganometalliquesDocument65 pagesCh7 Composes Halogenes&OrganometalliquesGaetan CasanovaPas encore d'évaluation
- Chimie Orga 1Document61 pagesChimie Orga 1Badr ZemmouriPas encore d'évaluation
- Les Aldéhydes Et Les Cétones - Activation Et Protection Du Groupe CarbonyleDocument14 pagesLes Aldéhydes Et Les Cétones - Activation Et Protection Du Groupe CarbonylejenndPas encore d'évaluation
- S6 HOC CH Chapitre 4Document21 pagesS6 HOC CH Chapitre 4Eddouks Fatimazahrae100% (2)
- PR Belhachemi Corrigé Du DM-5 GRTD MIPCDocument2 pagesPR Belhachemi Corrigé Du DM-5 GRTD MIPCYasser ElamraniPas encore d'évaluation
- Partiel 2022 Avec CorrectionDocument6 pagesPartiel 2022 Avec CorrectionHafsa SlamiPas encore d'évaluation
- Chapitre 7 TaninsDocument89 pagesChapitre 7 TaninsAlexandre Kpangny BéniPas encore d'évaluation
- Chimie Organique Fonctionelle S5Document120 pagesChimie Organique Fonctionelle S5أمين حسونيPas encore d'évaluation
- Chimie Organique Fonctionelle S5Document120 pagesChimie Organique Fonctionelle S5fskPas encore d'évaluation
- Bioelectronique - Vincent U. Schreier PDFDocument5 pagesBioelectronique - Vincent U. Schreier PDFjoel_tetard100% (1)
- P39oxbenzoine PersaDocument8 pagesP39oxbenzoine Persaayoub dahbi0% (1)
- Glucide 1Document1 pageGlucide 1imane AGOURRAMPas encore d'évaluation
- Chapitre II - Réactions de CondensationDocument25 pagesChapitre II - Réactions de CondensationHiba MnsPas encore d'évaluation
- H PDFDocument1 pageH PDFHenAbdoPas encore d'évaluation
- GlucidesDocument13 pagesGlucidesTimi BelaidiPas encore d'évaluation
- Examen 20093 SDocument6 pagesExamen 20093 Sfrancis luther kayoulouPas encore d'évaluation
- Stereochimie Chim 201-05-06cDocument13 pagesStereochimie Chim 201-05-06cToumany FofanaPas encore d'évaluation
- Chimie de Coordination 2008 Chapitre 1 C PDFDocument32 pagesChimie de Coordination 2008 Chapitre 1 C PDFKhaled DrissiPas encore d'évaluation
- Ent Et TerDocument38 pagesEnt Et TerJoel PERRETPas encore d'évaluation
- A/ Différentes Formules Pour Représenter Une MoléculeDocument4 pagesA/ Différentes Formules Pour Représenter Une MoléculeJeremy ForoiPas encore d'évaluation
- Sujet 4 Coag Floc MS 8hDocument4 pagesSujet 4 Coag Floc MS 8hجعدبندرهمPas encore d'évaluation
- TD05Document8 pagesTD05جعدبندرهمPas encore d'évaluation
- Exo T6liqvapDocument8 pagesExo T6liqvapجعدبندرهمPas encore d'évaluation
- Exercices IsomerieDocument1 pageExercices IsomerieجعدبندرهمPas encore d'évaluation
- Rev Ac Bas ConvertiDocument10 pagesRev Ac Bas ConvertiجعدبندرهمPas encore d'évaluation
- ch2 TP Dosage PH Vinaigre Guide enDocument3 pagesch2 TP Dosage PH Vinaigre Guide enجعدبندرهمPas encore d'évaluation
- TPCH1 TSdosageDocument2 pagesTPCH1 TSdosageجعدبندرهمPas encore d'évaluation
- Exam EmballageDocument4 pagesExam Emballageجعدبندرهم100% (1)
- Vinaigre CondDocument2 pagesVinaigre CondجعدبندرهمPas encore d'évaluation
- Grille EvalfstDocument13 pagesGrille EvalfstجعدبندرهمPas encore d'évaluation
- Travaux Dirigés DboDocument2 pagesTravaux Dirigés DboجعدبندرهمPas encore d'évaluation
- Btsa Sta Ress RMT Pres OutilsDocument10 pagesBtsa Sta Ress RMT Pres OutilsجعدبندرهمPas encore d'évaluation
- Calcul Des Reacteurs Chimiques HomogeneDocument16 pagesCalcul Des Reacteurs Chimiques HomogeneجعدبندرهمPas encore d'évaluation
- S Net EliminationDocument137 pagesS Net EliminationجعدبندرهمPas encore d'évaluation
- TP 7 Extraction Acide Benzoi QueDocument4 pagesTP 7 Extraction Acide Benzoi QueجعدبندرهمPas encore d'évaluation
- 1.3 Construction Binaire Liquide VapeurDocument7 pages1.3 Construction Binaire Liquide VapeurجعدبندرهمPas encore d'évaluation
- Calcul de Réacteurs ChimiquesDocument39 pagesCalcul de Réacteurs ChimiquesجعدبندرهمPas encore d'évaluation
- Caractérisation de Variétés de DattesDocument11 pagesCaractérisation de Variétés de DattesجعدبندرهمPas encore d'évaluation
- Cours FragmentationDocument9 pagesCours FragmentationجعدبندرهمPas encore d'évaluation
- Diagramme Binaire 1Document30 pagesDiagramme Binaire 1جعدبندرهمPas encore d'évaluation
- Diagramme BinaireDocument20 pagesDiagramme BinaireجعدبندرهمPas encore d'évaluation
- Ex2-STAV-Concentration - DilutionDocument2 pagesEx2-STAV-Concentration - DilutionجعدبندرهمPas encore d'évaluation
- Reforme STL2011 2012 Distillations Simple Et Fractionnée Gpe3Document6 pagesReforme STL2011 2012 Distillations Simple Et Fractionnée Gpe3جعدبندرهم100% (1)
- Chapitre 2 Bilans Matiere Regime PermanentDocument10 pagesChapitre 2 Bilans Matiere Regime Permanentجعدبندرهم75% (4)
- Chapitre 1 GeneralitesDocument9 pagesChapitre 1 GeneralitesجعدبندرهمPas encore d'évaluation
- Mineure Santé S2 Dérivés CarbonylésDocument31 pagesMineure Santé S2 Dérivés CarbonylésParis DE CHERBOURGPas encore d'évaluation
- Aldehydes CetonesDocument29 pagesAldehydes Cetonesvaslek terriyo100% (1)
- De Aldéhyde:: (R Représente Une Chaîne Carbonée.)Document8 pagesDe Aldéhyde:: (R Représente Une Chaîne Carbonée.)Rima RabiaPas encore d'évaluation
- Rétrosynthèse, Corrigés Des ExercicesDocument19 pagesRétrosynthèse, Corrigés Des Exercicesfantamat974Pas encore d'évaluation
- L2 Cours de Chimie OrganiqueDocument8 pagesL2 Cours de Chimie OrganiqueBeny MaboundaPas encore d'évaluation
- Ch10 Aldehydes Et CetonesDocument54 pagesCh10 Aldehydes Et CetonesSalah Láálám100% (1)
- Wa0006Document135 pagesWa0006Yc Yacine100% (1)
- Chapitre II-Les Carbonylés (Les Aldéhydes Et Les Cétones)Document48 pagesChapitre II-Les Carbonylés (Les Aldéhydes Et Les Cétones)Park-j TailPas encore d'évaluation
- Cours Licence - FONCTION CARBONYLEDocument82 pagesCours Licence - FONCTION CARBONYLEFatima Ben100% (1)
- Chapitre 6 Aldéhydes Et CétonesDocument7 pagesChapitre 6 Aldéhydes Et CétonesBeatrice Florin100% (8)
- Aldehydes CetonesDocument29 pagesAldehydes CetonesAhmad Elhamri100% (1)
- TD N°14 Carbonyle CorrigéDocument2 pagesTD N°14 Carbonyle CorrigéRobertoPas encore d'évaluation
- Chimie Organique Fonctionelle S5Document120 pagesChimie Organique Fonctionelle S5أمين حسونيPas encore d'évaluation
- Carbonyl Es 2Document20 pagesCarbonyl Es 2جعدبندرهمPas encore d'évaluation
- AlcoolDocument9 pagesAlcoolAmine FelloussiaPas encore d'évaluation
- Chimie Organique PDFDocument62 pagesChimie Organique PDFSarra BessadokPas encore d'évaluation
- Aldéhydes CétonesDocument56 pagesAldéhydes CétonesRoi AroufPas encore d'évaluation
- Chapitre 2 - Aldehydes& Cetones ModDocument104 pagesChapitre 2 - Aldehydes& Cetones ModYoussef Aouin100% (1)
- Grandes Fonctions en Chimie Organique ÉtudiantsDocument140 pagesGrandes Fonctions en Chimie Organique ÉtudiantsKossivi issa SALOUFOUPas encore d'évaluation
- Acétal Et CétalDocument9 pagesAcétal Et CétalFrederic WustPas encore d'évaluation
- Derives CarbonylesDocument31 pagesDerives CarbonylesDarel Nadjiera100% (1)
- Examen 20141 SDocument7 pagesExamen 20141 SElbachaPas encore d'évaluation
- Chimie Oraganique 2 SMC4Document126 pagesChimie Oraganique 2 SMC4Yc YacinePas encore d'évaluation
- Aldehydes Et CetonesDocument24 pagesAldehydes Et CetonesAhmed Ben AmmarPas encore d'évaluation
- Acides Carboxyliques, Corrigés Des ExercicesDocument54 pagesAcides Carboxyliques, Corrigés Des ExercicesDado DjiguibaPas encore d'évaluation
- Chap 6c ALCOOLS Et AminesDocument8 pagesChap 6c ALCOOLS Et AminesAugues NZOULOU MABIALAPas encore d'évaluation
- UE1-Chimie-9-fonctions DivalentesDocument21 pagesUE1-Chimie-9-fonctions Divalentessun-nee-chan9Pas encore d'évaluation
- Le PolyoxydeDocument8 pagesLe PolyoxyderadjaamenasriPas encore d'évaluation
- TD N°14 CarbonyleDocument2 pagesTD N°14 CarbonyleRobertoPas encore d'évaluation
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Revue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteD'EverandRevue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteÉvaluation : 3 sur 5 étoiles3/5 (3)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- Mes inventions (Traduit): Autobiographie de Nikola TeslaD'EverandMes inventions (Traduit): Autobiographie de Nikola TeslaÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Production et propagation des sons: Les Grands Articles d'UniversalisD'EverandProduction et propagation des sons: Les Grands Articles d'UniversalisPas encore d'évaluation
- Affirmations positives : Perte de poids pour les femmesD'EverandAffirmations positives : Perte de poids pour les femmesPas encore d'évaluation
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Conception & Modélisation CAO: Le guide ultime du débutantD'EverandConception & Modélisation CAO: Le guide ultime du débutantPas encore d'évaluation
- Physique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresD'EverandPhysique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresÉvaluation : 5 sur 5 étoiles5/5 (2)
- Transformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitD'EverandTransformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitÉvaluation : 4 sur 5 étoiles4/5 (14)
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)